黑素细胞调节肽的制作方法
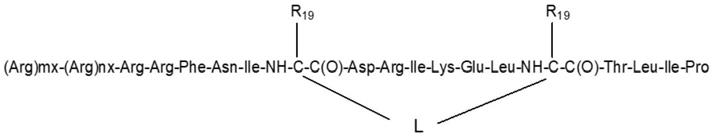
黑素细胞调节肽
1.本技术要求于2019年8月2日提交的欧洲专利申请ep19382674.0的权益。
技术领域
2.本发明整体上涉及黑素细胞相关病症的领域。具体地,本发明涉及具有调节黑素生成能力的肽,其促进或减少黑色素的产生,以及抑制恶性黑素细胞的增殖;涉及含有其作为活性成分的药物和化妆品组合物,以及它们在治疗和化妆品中的用途。
背景技术:
3.通过称为黑素生成的过程,黑素细胞产生黑色素,这是一种在皮肤、眼睛、头发、鼻腔和内耳中发现的色素。这种黑素生成导致了持久的色素沉着,其与源于已经存在的黑色素的氧化的色素沉着形成对比。
4.黑素生成有基础和激活两种水平;一般来说,肤色较浅的人具有低基础水平的黑素生成。暴露于uv-b辐射导致黑素生成增加。黑素生成的目的是保护皮下组织(皮肤下的一层)免受uv-b辐射的伤害。黑色素的颜色是黑色的,从而允许它吸收大部分uv-b光,并阻止它穿过表皮。
5.众所周知,在一个人的一生中,他/她的皮肤颜色会发生明显的变化,因此,例如,老年人面部、胸部和手部皮肤上出现的痕迹是衰老的明显迹象。此外,持续过度暴露于uv辐射不仅会导致皮肤的加速老化,称为光老化,其特征在于在更早的年龄出现皮肤老化迹象,其中包括过度暴露于uv辐射的皮肤区域中出现痕迹;而且还会导致色素沉着过度的癌性病变或黑色素瘤的形成。
6.经常发生的情况是,在一个人的皮肤区域中,黑素细胞内的黑色素密度大于周围区域,因此该人受影响区域的颜色比其他区域的颜色更深。这些区域被称为色素沉着过度区域。色素沉着过度的原因包括激素变化、黄褐斑、雀斑样痣、斑驳病、爱迪生氏病、由于有利于辐射作用(光毒性)的试剂引起的对紫外线辐射的超敏反应,或炎性病变导致的色素沉着过度。与痤疮、湿疹、疤痕或脱毛相关的痕迹属于最后一种色素沉着过度,并且是甚至可以持续几年的痕迹。
7.一个人的皮肤区域也有可能比周围区域黑色素密度低。白癜风、白糠疹、花斑癣和炎症后效应是色素损失的常见原因。色素沉着的不规则性的减弱是由于衰老和/或光老化、激素紊乱或炎症后过程引起的,并且特别地,因此通过局部应用在受白癜风影响的区域中重建色素沉着引起化妆品和制药业的关注。
8.色素性病症是一个全球性的问题。尽管色素性病症很常见,但仍然很难治疗。
9.治疗色素沉着过度病症的主要方法主要基于防止过度活跃的黑素细胞产生黑色素或者通过增加表皮细胞更新来促进黑色素从表皮中去除。目前,许多抑制酪氨酸酶(参与黑色素合成的限速酶)的药剂被用于治疗色素沉着过度的病症,并取得了一定的成功。这些药剂包括氢醌、曲酸(也称为“ka”)、熊果苷、对甲氧酚和壬二酸。接触性皮炎是一种常见的副作用,发生在高达15%使用这些药剂的患者中,从而限制了它们的使用。这些药剂的功效
在患者之间差异很大。局部类视黄醇经由酪氨酸酶的抑制来减少表皮黑色素,还增加表皮更新,从而促进黑色素的分散和去除。然而,刺激性皮炎可能是一种常见的不良反应,并且在深色皮肤类型中使用较高浓度的局部类视黄醇时应谨慎使用,因为由此产生的刺激可能导致红斑、脱屑和进一步的炎症后色素沉着过度。激光疗法有时可能对色素沉着过度是有效的。然而,这给深色皮肤的患者带来了一个严重的问题,他们的基线表皮黑色素增加,这也是针对这些波长的。
10.色素脱失病症还涉及炎症和自身免疫发病机制,因此局部皮质类固醇和免疫调节剂可能在治疗方案中有用。因为在炎症过程结束后,炎症后色素沉着不足通常在临床上是明显的,所以这些相同的局部药剂在这个晚期阶段可能没有益处。光疗法,包括但不限于补骨脂素加uva(口服或局部)、补骨脂素和自然阳光、uvb、窄带uvb和308nm准分子激光,已被用于治疗色素沉着不足和色素脱失两者。色素脱失病症(例如白癜风)可能特别难以治疗,因为滤泡间表皮中完全没有黑素细胞。因此,疗法的目的是向这些部位补充或移植黑素细胞。
11.因此,尽管做出了努力,但仍然需要开发可以有效调节黑素细胞活性并因此可以有效治疗色素性病症的其他分子(肽)。
技术实现要素:
12.本发明人已经发现序列seq id no:1和2的肽有效调节黑素细胞活性。
13.一方面,本发明人已惊奇地发现,本发明的肽参与黑素生成途径。因此,所述肽中的一些刺激黑色素的产生,这可能是黑素细胞活化的标志,而其他肽(诸如f22和f29)则大大减少了黑色素的量。更值得注意的是,当与现有技术中已知的其他化合物相比时,本发明的肽在调节黑色素生成方面更有效。在这点上,发现当通常用于色素沉着过度的ka以1μm的浓度使用时,减少量显著低于用相同浓度下的本发明的肽所实现的减少量。因此,这些数据不仅支持本发明的肽对黑色素生成的作用,而且说明它们甚至比现有技术中用于相同目的的其他化合物更有效。
14.另一方面,本发明人还已发现,这些肽不仅在黑色素形成方面,而且在细胞增殖方面调节黑素细胞活性。如表2所示,本发明的肽在抑制癌细胞增殖,特别是黑色素瘤细胞系,包括转移性黑色素瘤细胞系方面是活性的。
15.因此,在第一方面,本发明提供了一种肽或其药物或化妆品可接受的盐,所述肽具有相对于序列seq id no:1或2具有至少85%同一性的氨基酸序列:
16.(trp)
m-(asn)
n-lys-gly-thr-ile-leu-lys-ala-ser-val-asp-tyr-ile-arg-lys-(leu)
p-(gln)qꢀꢀ
(seq id no:1)
17.(arg)
mx-(arg)
nx-arg-arg-phe-asn-ile-asn-asp-arg-ile-lys-glu-leu-gly-thr-leu-(ile)
px-(pro)
qx
ꢀꢀ
(seq id no:2)
18.其中
[0019]“m”、“n”、“p”和“q”代表整数,并且选自0和1;
[0020]“m
x”、“n
x”、“p
x”和“q
x”代表整数,并且选自0和1;
[0021]
c末端对应于-c(o)r4;
[0022]
n末端对应于-nhr5;
[0023]
r4是选自由-oh和-nr
17r18
组成的组的基团;
[0024]
r5是选自由以下组成的组的基团:-h、(c
1-c
20
)烷基和被选自由卤素、(c
1-c
10
)烷基、-or6、-nr7r8、-sr9、-sor
10
、-so2r
11
和-co2r
12
组成的组的一个或多个基团取代的和(c
1-c
10
)烷基;并且
[0025]r17
和r
18
是独立地选自由以下组成的组的基团:-h和(c
1-c
10
)烷基和被选自由卤素、(c
1-c
10
)烷基、-or6、-nr7r8、-sr9、-sor
10
、-so2r
11
和-co2r
12
组成的组的一个或多个基团取代的(c
1-c
10
)烷基;所述肽任选地包括式(i)的接头双自由基“l”[0026]-[(r1)
a-(r2)-(r3)b]c‑ꢀꢀ(i)[0027]
其连接位于肽序列中位置“i”处的氨基酸的α碳原子和位于位置“i+4”或“i+7”处的氨基酸的α碳原子,
[0028]
其中
[0029]“a”和“b”相同或不同,并且是0或1;
[0030]“c”由1至10组成;
[0031]
r1和r3是独立地选自由以下组成的组的双自由基:(c
1-c
10
)烷基;被选自由以下组成的组的一个或多个基团取代的(c
1-c
10
)烷基:卤素、(c
1-c
10
)烷基、-or6、-nr7r8、-sr9、-sor
10
、-so2r
11
和-co2r
12
;(c
2-c
10
)烯基;被选自由以下组成的组的一个或多个基团取代的(c
2-c
10
)烯基:卤素、(c
1-c
10
)烷基、-or6、-nr7r8、-sr9、-sor
10
、-so2r
11
和-co2r
12
;(c
2-c
10
)炔基;和被选自由以下组成的组的一个或多个基团取代的(c
2-c
10
)炔基:卤素、(c
1-c
10
)烷基、-or6、-nr7r8、-sr9、-sor
10
、-so2r
11
和-co2r
12
;
[0032]
r2是选自由以下组成的组的双自由基:-o-、c(=o)、c(=o)nr
13
、c(=o)o、s(=o)、s(=o)2、nr
14
、(c
1-c
10
)烷基、(c
2-c
10
)烯基、(c
2-c
10
)炔基、-nr
15-nr
16-、-n=n-、-s-s-,以及包含3至14个成员的已知环体系,所述体系包含1至3个环,其中:
[0033]
所述环中的每一个均是饱和的、部分不饱和的或芳族的;
[0034]
所述环是孤立的、部分或全部稠合的,
[0035]
形成已知环体系的成员中的每一个选自由以下组成的组:-ch-、-ch
2-、-nh-、-n-、-sh-、-s-和-o-;并且
[0036]
所述环体系任选地被独立地选自由以下组成的组的一个或多个基团取代:卤素、-oh、-no2、(c
1-c
10
)烷基、(c
1-c
10
)卤代烷基和(c
1-c
10
)烷基-o-;并且
[0037]
r6、r7、r8、r9、r
10
、r
11
、r
12
、r
13
、r
14
、r
15
和r
16
是独立地选自由以下组成的组的基团:-h和(c
1-c
10
)烷基;并且
[0038]
通过接头连接的氨基酸具有式(ii)
[0039][0040]
其中
[0041]r19
是选自由以下组成的组的单自由基:(c
1-c
10
)烷基、(c
2-c
10
)烯基、(c
2-c
10
)炔基,以及包含3至14个成员的已知环体系,所述体系包含1至3个环,其中:
[0042]
所述环中的每一个均是饱和的、部分不饱和的或芳族的;
[0043]
所述环是孤立的、部分或全部稠合的,
[0044]
形成已知环体系的成员中的每一个选自由以下组成的组:-ch-、-ch
2-、-nh-、-n-、-sh-、-s-和-o-。
[0045]
在第二方面,本发明提供了一种化妆品或药物组合物,其包含化妆品或治疗有效量的如本发明的第一方面所定义的肽以及可接受的化妆品或药物赋形剂和/或载体。
[0046]
在第三方面,本发明提供了如本发明的第一方面所定义的肽或其药物盐或本发明的第二方面的药物组合物,用作药物。这一方面可以替代性地表述成如本发明的第一方面所定义的肽或其药物盐或本发明的第二方面的药物组合物在制造用于治疗疾病的药物中的用途。这一方面也可以替代性地表述成一种治疗疾病的方法,所述方法包括向有需要的受试者施用有效治疗量的如本发明的第一方面所定义的肽或其药物盐或本发明的第二方面的药物组合物。
[0047]
在第四方面,本发明提供了如本发明的第一方面所定义的肽或其药物盐或如本发明的第二方面所定义的药物组合物,用于治疗癌症。这一方面可以替代性地表述成如本发明的第一方面所定义的肽或其药物盐或如本发明的第二方面所定义的药物组合物在制造用于治疗癌症的药物中的用途。这一方面也可以替代性地表述成一种治疗癌症的方法,所述方法包括向有需要的受试者施用有效治疗量的如本发明的第一方面所定义的肽或其药物盐或如本发明的第二方面所定义的药物组合物。
[0048]
在第五方面,本发明还提供了如本发明的第一方面所定义的肽或其化妆品盐或如本发明的第二方面所定义的化妆品组合物用于调节黑素生成,特别是用于减少或增加黑色素产生的非治疗用途。
[0049]
在最后一个方面,本发明提供了一种在有需要的受试者中处理色素沉着过度或色素沉着不足的美容方法,所述方法包括将如本发明的第一方面所定义的肽或其化妆品盐或如本发明的第二方面所定义的化妆品组合物应用于患有色素沉着过度或色素沉着不足的受影响区域。
[0050]
在另外的方面,本发明提供:(a)包含如本发明的第一或第二方面所定义的肽或其药物盐及治疗剂、特别是抗癌剂的组合;(b)包含如本发明的第一或第二方面所定义的肽或其药物盐及治疗剂、特别是抗癌剂的组合,用作药物,更具体地用于治疗癌症;(c)如本发明的第一或第二方面所定义的肽或其药物盐,用于预防或治疗癌症的组合疗法,其中所述疗法包括将其与抗癌剂同时、依次或分别施用至受试者;和(d)用于与如本发明的第一或第二方面所定义的肽或其药物盐的组合疗法用途中的抗癌剂,其中所述用途包括预防或治疗癌症。
附图说明
[0051]
图1示出了经治疗的黑色素瘤细胞中黑色素相对于未治疗的黑色素瘤细胞的百分比。作为阳性对照,使用不同浓度(0.1、1和10μm)的曲酸(ka)。
具体实施方式
[0052]
除非另有说明,否则本技术中如本文所用的所有术语应以本领域已知的普通含义来理解。如在本技术中使用的某些术语的其他更具体的定义如下所述,并且旨在整个说明
书和权利要求书中统一地应用,除非另外明确表示的定义提供了更宽泛的定义。
[0053]
出于本发明的目的,给出的任何范围包括该范围的下端点和上端点两者。
[0054]
如上所述,本发明提供了包含与seq id no:1或2具有至少85%程度同一性的序列的肽。
[0055]
在本发明中,术语“同一性”是指当序列最佳比对时,两个序列中相同残基的百分比。如果在最佳比对中,第一序列中的一个位置被与第二序列中相应位置相同的氨基酸残基占据,则所述序列相对于该位置表现出同一性。两个序列之间的同一性水平(或“序列同一性百分比”)被测量为序列共享的相同位置的数量相对于序列大小的比率(即序列同一性百分比=(相同位置的数量/位置的总数)
×
100)。
[0056]
用于快速获得最佳比对和计算两个或更多个序列之间同一性的许多数学算法是已知的,并被结合到许多可用的软件程序中。此类程序的实例包括用于氨基酸序列分析的match-box、multain、gcg、fasta和robust程序等。优选的软件分析程序包括align、clustal w和blast程序(例如,blast 2.1、bl2seq及其更高版本)。
[0057]
对于氨基酸序列分析,权重矩阵,诸如blosum矩阵(例如,blosum45、blosum50、blosum62和blosum80矩阵)、gonnet矩阵或pam矩阵(例如,pam30、pam70、pam120、pam160、pam250和pam350矩阵)用于确定同一性。
[0058]
blast程序提供至少两个氨基酸序列的分析,通过将选择的序列与数据库(例如genseq)中的多个序列进行比对,或者使用bl2seq在两个选择的序列之间进行比对。blast程序优选地由低复杂度的过滤程序修改,诸如dust或seg程序,它们优选地集成到blast程序操作中。如果使用空位存在罚分(gap existence cost)(或空位分数),则空位存在罚分优选地设置在约-5和-15之间。类似的空位参数可以酌情用于其他程序。blast程序及其基本原理在例如altschul等人,“basic local alignment search tool”,1990,j.mol.biol,v.215,第403-410页中有进一步描述。
[0059]
对于多序列分析,可以使用clustal w程序。clustal w程序最好使用“dynamic”(相对于“fast”)设置运行。根据序列之间的同一性水平,使用一组可变的blosum矩阵来评估氨基酸序列。clustal w程序和基本操作原理在例如higgins等人,“clustal v:improved software for multiple sequence alignment”,1992,cabios,8(2),第189-191页中有进一步描述。
[0060]
如本文所用,术语“药物或化妆品可接受的盐”是指在合理的医学判断的范围内适合用于与人和低等动物的组织接触,而没有不适当的毒性、刺激、过敏应答等,并且与合理的益处/风险比相称的那些盐。药物和化妆品可接受的盐在本领域中是熟知的。药物和化妆品可接受的无毒酸加成盐的实例是与无机酸(诸如盐酸、氢溴酸、磷酸、硫酸和高氯酸)形成,或与有机酸(诸如乙酸、三氟乙酸、草酸、马来酸、酒石酸、柠檬酸、琥珀酸或丙二酸)形成,或通过使用本领域中使用的其他方法(诸如离子交换)形成的氨基盐。其他药物和化妆品可接受的盐包括己二酸盐、藻酸盐、抗坏血酸盐、天冬氨酸盐、苯磺酸盐、苯酸盐、硫酸氢盐、硼酸盐、丁酸盐、樟脑酸盐、樟脑磺酸盐、柠檬酸盐、环戊烷丙酸盐、二葡糖酸盐、十二烷基硫酸盐、乙磺酸盐、甲酸盐、富马酸盐、葡庚糖酸盐、甘油磷酸盐、葡糖酸盐、半硫酸盐、庚酸盐、己酸盐、氢碘酸盐、2-羟基-乙磺酸盐、乳糖醛酸盐、乳酸盐、月桂酸盐、十二烷基硫酸盐、苹果酸盐、马来酸盐、丙二酸盐、甲磺酸盐、2-萘磺酸盐、烟酸盐、硝酸盐、油酸盐、草酸
盐、棕榈酸盐、双羟萘酸盐、果胶酸盐、过硫酸盐、3-苯基丙酸盐、磷酸盐、苦味酸盐、新戊酸盐、丙酸盐、硬脂酸盐、琥珀酸盐、硫酸盐、酒石酸盐、硫氰酸盐、对-甲苯磺酸盐、十一酸盐、戊酸盐等。衍生自适当碱的盐包括碱金属、碱土金属和铵。代表性的碱金属或碱土金属盐包括钠、锂、钾、钙、镁等。另外的药物和化妆品可接受的盐包括(当适当时)无毒的铵、季铵和胺阳离子,其使用抗衡离子诸如卤化物、氢氧化物、羧酸盐、硫酸盐、磷酸盐、硝酸盐、低级烷基磺酸盐和芳基磺酸盐形成。
[0061]
术语(c1至c
10
)烷基是指具有1至10个碳原子的饱和直链或支链烷基链。例示性非限制性实例是:甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、n-戊基、新戊基和正己基。
[0062]
术语(c1至c
20
)烷基是指具有1至20个碳原子的饱和直链或支链烷基链。
[0063]
术语(c2至c
10
)烯基是指含有2至10个碳原子并且还含有一个或多个双键的饱和直链或支链烷基链。例示性非限制性实例是:乙烯基、丙烯基、丁烯基、1-甲基-2-丁烯-1基等。
[0064]
术语(c
2-c
10
)炔基是指含有2至20个碳原子并且还含有一个或多个三键的饱和直链或支链烷基链。实例包括乙炔基、1-丙炔基、2-丁炔基、1,3-丁二炔基、4-戊炔基和1-己炔基等。
[0065]
术语“卤素”是指周期表中由五种化学相关元素组成的族:氟(f)、氯(cl)、溴(br)、碘(i)和砹(at)。
[0066]
术语(c
1-c
10
)卤代烷基是指由(c
1-c
10
)烷基的一个或多个氢原子被一个或多个,优选1至6个可以是相同或不同的卤素原子替代而得到的基团。实例包括三氟甲基、氟甲基、1-氯乙基、2-氯乙基、1-氟乙基、2-氟乙基、2-溴乙基、2-碘乙基、2,2,2-三氟乙基、五氟乙基、3-氟丙基、3-氯丙基、2,2,3,3-四氟丙基、2,2,3,3,3-五氟丙基、七氟丙基、4-氟丁基和九氟丁基。
[0067]
如本文所用的术语“已知”环体系是指化学上可行并且在本领域中已知的环体系,因此旨在排除化学上不可能的那些环体系。
[0068]
根据本发明,当环体系由“孤立的”环形成时,意味着环体系由两个、三个或四个环形成,并且所述环经由键从一个环的原子结合到另一个环的原子。术语“孤立的”也包括其中环体系仅具有一个环的实施方案。由一个环组成的已知环体系的例示性非限制性实例是衍生自以下的那些:环丙基、环丁基、环戊基、环己基、环庚基、环丙烯基、环丁烯基、环戊烯基、苯基和环庚基。
[0069]
根据本发明,当环体系具有“完全稠合”的环时,意味着环体系由两个、三个或四个环形成,其中两个或更多个原子为两个相邻环所共有。例示性非限制性实例是1,2,3,4-四氢萘基、1-萘基、2-萘基、蒽基或菲基。
[0070]
根据本发明,当环体系是“部分稠合的”时,这意味着环体系由三个或四个环形成,所述环中的至少两个是完全稠合的(即两个或更多个原子为两个相邻环所共有),并且剩余的一个或多个环经由键从一个环的原子结合到一个稠合环的原子。
[0071]
除非另有说明,否则形成本发明的肽的氨基酸可以具有l-构型或d-构型。
[0072]
用于构建本发明的肽的氨基酸可以通过有机合成制备,或者通过其他途径获得,例如像天然来源的降解或分离。
[0073]
在本发明的第一方面的一个实施方案中,所述肽不同于序列seq id no:24、25或
26中的一种。
[0074]
在本发明的第一方面的一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽是其中m和n相同的肽。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽是其中p和q相同的肽。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,m和n代表1,并且p和q代表0。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,m和n代表0,并且p和q代表1。
[0075]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽是线性肽。
[0076]
在本发明中,术语“线性肽”意指它不包括“l”双自由基。
[0077]
在本发明的第一方面的一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽是由seq id no:1组成的线性肽,其中:
[0078]-当“m”和“n”相同时,则“p”与“q”不同;并且
[0079]-当m是0且n=p=1时,则q是1。
[0080]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽是由seq id no:1组成的线性肽,并且选自以下肽,其中:
[0081]-m、n、p和q中的至少三个相同;或者,可替代地,
[0082]-当“m”是0且“n”是1时,则“p”是0且“q”是0或1;或者,可替代地
[0083]-当“m”是0且“n”是1时,则“p”是0或1且“q”是1。
[0084]
在本发明的第一方面的一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽是其中m
x
和n
x
相同的肽。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽是其中p
x
和q
x
相同的肽。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,m
x
和n
x
代表1,并且p
x
和q
x
代表0。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,m
x
和n
x
代表0,并且p
x
和q
x
代表1。
[0085]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是包含“l”接头的肽或其盐,其中a=1。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是包含“l”接头的肽或其盐,其中b=1。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是包含“l”接头的肽或其盐,其中c=1。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是包含“l”接头的肽或其盐,其中a=b=c=1。
[0086]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是包含“l”接头的肽或其盐,其中r1和r3是独立地选自由以下组成的组的双自由基:(c
1-c
10
)烷基;(c
2-c
10
)烯基;和(c
2-c
10
)炔基。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是包含“l”接头的肽或其盐,其中r1和r3相同或不同,并且代表(c
1-c
10
)烷基。
[0087]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是包含“l”接头的肽或其盐,其中r2是选自由以下组成的组的
双自由基:-o-、c(=o)、c(=o)nr
13
、c(=o)o、s(=o)、s(=o)2、nr
14
、(c
1-c
10
)烷基、(c
2-c
10
)烯基、(c
2-c
10
)炔基、-nr
15-nr
16-、-n=n-、-s-s-,以及由一个3至6个成员的环组成的已知环体系,所述环:
[0088]
是饱和的、部分不饱和的或芳香的;
[0089]
形成已知环体系的成员中的每一个选自由以下组成的组:-ch-、-ch
2-、-nh-、-n-、-sh-、-s-和-o-;并且
[0090]
环体系任选地被独立地选自由以下组成的组的一个或多个基团取代:卤素、-oh、-no2、(c
1-c
10
)烷基、(c
1-c
10
)卤代烷基和(c
1-c
10
)烷基-o-。
[0091]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是包含“l”接头的肽或其盐,其中r2是选自由以下组成的组的双自由基:(c
1-c
10
)烷基、(c
2-c
10
)烯基和(c
2-c
10
)炔基。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是包含“l”接头的肽或其盐,其中r2是(c
2-c
10
)烯基。
[0092]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是包含“l”接头的肽或其盐,其中r1和r3相同或不同,并且代表(c
1-c
10
)烷基;并且r2是(c
2-c
10
)烯基。
[0093]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是包含“l”接头的肽或其盐,其中r1和r3相同或不同,并且代表(c
1-c
10
)烷基;r2是(c
2-c
10
)烯基;并且a=b=c=1。
[0094]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是其中r
19
选自由以下组成的组的肽或其盐:(c
1-c
10
)烷基、(c
2-c
10
)烯基和(c
2-c
10
)炔基。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是其中r
19
是(c
1-c
10
)烷基单自由基的肽或其盐。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是包含“l”接头的肽或其盐,其中r1、r3和r
19
是相同或不同的,并且代表(c
1-c
10
)烷基;并且r2是(c
2-c
10
)烯基。
[0095]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是其中r4是-oh(即,c末端是-c(o)oh)的肽或其盐。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是其中r4是-nr
17r18
,r
17
和r
18
含义相同的肽或其盐。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述n末端对应于-nh2。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,本发明的肽的c末端和n末端分别是-c(o)oh和-nh2。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,本发明的肽的c末端和n末端分别是-c(o)nh2和-nh2。
[0096]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,本发明的肽的c末端和n末端分别是-c(o)oh和-nhr5,其中r5选自(c
1-c
20
)烷基和被选自由卤素、(c
1-c
10
)烷基、-or6、-nr7r8、-sr9、-sor
10
、-so2r
11
和-co2r
12
组成的组的一个或多个基团取代的(c
1-c
10
)烷基。
[0097]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,本发明的肽的c末端和n末端分别是-c(o)r4和-nh2,其中r4意指-nhr
18
,并且r
18
是选自由以下组成的组的基团:(c
1-c
10
)烷基和被选自由卤素、(c
1-c
10
)烷基、-or6、-nr7r8、-sr9、-sor
10
、-so2r
11
和-co2r
12
组成的组的一个或多个基团取代的(c
1-c
10
)烷基。
[0098]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,本发明的肽的c末端和n末端分别是-c(o)r4和-nh2,其中r4意指-nr
17r18
,并且r
17
和r
18
是独立地选自由以下组成的组的基团:(c
1-c
10
)烷基和被选自由卤素、(c
1-c
10
)烷基、-or6、-nr7r8、-sr9、-sor
10
、-so2r
11
和-co2r
12
组成的组的一个或多个基团取代的(c
1-c
10
)烷基。
[0099]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,式(i)的接头双自由基在位于序列seq id no:1的肽序列的位置
“ⅰ”
处的氨基酸的α碳原子和位于肽序列seq id no:1的位置
“ⅰ
+7”处的氨基酸的α碳原子之间。
[0100]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐选自由氨基酸序列seq id no:3至8组成的组:
[0101]
seq id no:3
[0102][0103]
seq id no:4
[0104][0105]
seq id no:5
[0106][0107]
seq id no:6
[0108][0109]
seq id no:7
[0110]
和
[0111]
seq id no:8
[0112]
[0113]
其中“m”、“n”、“p”、“q”、“l”和“r
19”如前述实施方案中任一项所定义。
[0114]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,式(i)的接头双自由基在位于seq id no:2的肽序列的位置
“ⅰ”
处的氨基酸的α碳原子和位于seq id no:2的肽序列的位置
“ⅰ
+7”处的氨基酸的α碳原子之间。
[0115]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐选自由氨基酸序列seq id no:9至16组成的组:
[0116]
seq id no:9
[0117][0118]
seq id no:10
[0119][0120]
seq id no:11
[0121][0122]
seq id no:12
[0123][0124]
seq id no:13
[0125][0126]
seq id no:14
[0127][0128]
seq id no:15
[0129]
以及
[0130]
seq id no:16
[0131][0132]
其中“m
x”、“n
x”、“p
x”、“q
x”、“l”和“r
19”如前述实施方案中任一项所定义。
[0133]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是与序列seq id no:3至8具有至少85%同一性的肽或其盐,其中r1、r3和r
19
相同或不同,并且代表(c
1-c
10
)烷基;并且r2是(c
2-c
10
)烯基。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是与序列seq id no:3至8具有至少85%同一性的肽或其盐,其中r1、r3和r
19
相同或不同,并且代表(c
1-c
10
)烷基;r2是(c
2-c
10
)烯基;c末端选自-c(o)oh;和-conh2,并且n末端是-nh2。
[0134]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是与序列seq id no:9至16具有至少85%同一性的肽或其盐,其中r1、r3和r
19
相同或不同,并且代表(c
1-c
10
)烷基;并且r2是(c
2-c
10
)烯基。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是与序列seq id no:9至16具有至少85%同一性的肽或其盐,其中r1、r3和r
19
相同或不同,并且代表(c
1-c
10
)烷基;r2是(c
2-c
10
)烯基;并且c末端选自-c(o)oh和-conh2,并且n末端是-nh2。
[0135]
在本发明的第一方面的另一个实施方案中,所述肽是与选自由序列seq id no:17至23组成的组的氨基酸序列具有至少85%同一性的肽,或其药物或化妆品盐:
[0136]
seq id no:17(以下也称为“f22”)
[0137][0138]
seq id no:18(以下也称为“f29”)
[0139][0140]
seq id no:19(以下也称为“f31”)
[0141][0142]
seq id no:20(以下也称为“f05”)
[0143][0144]
seq id no:21(以下也称为“f13”)
[0145][0146]
seq id no:22(以下也称为“f16”)
[0147][0148]
seq id no:23(以下也称为“f18”)
[0149][0150]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是相对于序列seq id no:1至23中的任一者具有85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的肽,并且“m”、“n”、“p”、“q”、“m
x”、“n
x”、“p
x”、“q
x”、l和r
19
如以上实施方案中的任一个所定义。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽或其盐是相对于序列seq id no:1至23中的任一者具有100%同一性的肽,并且“m”、“n”、“p”、“q”、“m
x”、“n
x”、“p
x”、“q
x”、l和r
19
如以上实施方案中的任一个所定义。在一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,当进行比对以确定用于确认同一性程度的相同位置时,不考虑由接头连接的两个氨基酸残基。
[0151]
在本发明的第一方面的一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,第一方面的肽缀合至一部分,诸如标记、药物或细胞穿透肽。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽缀合至标记。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述标记缀合至所述肽的n或c末端。
[0152]
如本文所用的“标记”是可以通过多种方法检测的分子或化合物,包括荧光、电导率、放射性、大小等。所述标记可以固有地能够发射信号,例如像荧光标记,其在被另一个较低的特征波长的光激发后发射特定波长的光。可替代地,所述标记可能不能够固有地发射信号,但它可能能够被发射信号的另一种化合物结合。后一种情况的一个实例是标记,诸如生物素,其本身不发射信号,但当它与经标记的抗生物素蛋白或链霉亲和素分子结合时可以被检测到。后一种标记的其他实例是特异性结合特定受体的配体。允许可检测标记的受体与配体标记的单位特异性标记物结合,以便使此类标记物可视化。
[0153]
根据本发明可以使用的标记包括但不限于电子自旋共振分子、荧光分子、化学发光分子、放射性同位素、酶底物、酶、生物素分子、抗生物素蛋白分子、电荷转移分子、半导体纳米晶体、半导体纳米颗粒、胶体金纳米晶体、配体、微珠、磁珠、顺磁性分子、量子点、生色底物、亲和分子、蛋白质、肽、核酸、碳水化合物、半抗原、抗原、抗体、抗体片段和脂质。
[0154]
放射性同位素可以用膜或电荷耦合器件(ccd)来检测,配体可以通过结合具有荧
光、化学发光或酶标签的受体来检测,并且微珠可以使用电子或原子力显微镜来检测。
[0155]
标记与肽的缀合可以按照本领域技术人员熟知的常规方案来进行。
[0156]
在另一个实施方案中,本发明的第一方面的肽,任选地结合以上或以下提供的实施方案中的任一个,缀合至药物。在一个实施方案中,所述药物缀合至所述肽的n末端。
[0157]
在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述肽缀合至细胞穿透肽。
[0158]
在本发明中,术语“细胞穿透肽”(“cpp”)是指促进细胞摄取各种分子货物(从纳米尺寸的颗粒至小的化学分子和大的dna片段)的短肽。“货物(cargo)”经由c(t)端或n(t)端,或者通过经由共价键的化学键,或者通过非共价相互作用与肽结合。cpp的功能是将货物递送到细胞中,这一过程通常通过内吞作用发生。目前的使用受到cpp介导的货物递送中缺乏细胞特异性和对其摄取方式理解不足的限制。cpp通常具有含有高相对丰度的带正电荷的氨基酸(诸如赖氨酸或精氨酸)的氨基酸组成,或者具有含有极性/带电荷氨基酸和非极性疏水氨基酸交替模式的序列。这两种类型的结构分别称为聚阳离子或两亲性。第三类cpp是疏水肽,仅含有非极性残基,净电荷低或具有对细胞摄取至关重要的疏水氨基酸基团。cpp与本发明提供的肽的缀合可以按照熟知的常规方案进行,诸如固相合成或溶液选择性封端。(参见copolovici d.m.等人,“cell-penetrating peptides:design,synthesis,and applications”,2014,acs nano,2014,8(3),第1972-1994页)。在本发明的第一方面的另一个实施方案中,任选地结合以上或以下提供的实施方案中的任一个,所述细胞穿透肽是聚阳离子cpp、聚arg,或者可替代地,穿透肽。
[0159]
根据本发明的第一方面的肽的制备方法包括:
[0160]
(1.a)通过缩合将肽的相应氨基酸与式(iii)的化合物和式(iv)的化合物偶联,式(iii)的化合物和式(iv)的化合物对应于称为“i”和“i+4”或“i+7”的氨基酸。化合物(iii)和(iv)将经历随后的环化步骤以生成“l”双自由基:
[0161][0162]
其中r
19
如以上所定义,z1和z2相同或不同,并且代表(c
2-c
10
)烯基;以及(1.b)环化步骤,包括在溶液中用格拉布斯(i或ii生成)催化剂进行z1和z2的闭环复分解(参见kim young-woo等人,“synthesis of all-hydrocarbon stapled a-helical peptides by ring-closing olefin metathesis”,nature protocols,2011,6(6),第761-771页;scott j.m.等人,“application of ring-closing metathesis to the synthesis of rigidified amino acids and peptides”,j.am.chem.soc.,1996,v.118(40),第9606-9614页);或者,可替代地,
[0163]
(2a)通过缩合偶联所需的氨基酸,包括式(v)的化合物和式(vi)的化合物,它们对应于称为“i”和“i+4”或“i+7”的氨基酸。化合物(v)和(vi)将经历随后的环化步骤以生成“l”双自由基:
[0164]
[0165]
其中r
19
如以上所定义,z3和z4相同或不同,选自由以下组成的组:卤素-sh、-nhr
20
、-oh、(c
2-c
10
)烷基-sh、(c
1-c
10
)烷基-oh、(c
1-c
10
)烷基-nhr
21
、c(=o)oh、(c
1-c
10
)c(=o)oh、c(=o)nhr
22
、(c
1-c
10
)烷基c(=o)nhr
23
、or
24
、c(=o)-卤素、c(=o)-or
25
、s(=o)-卤素、s(=o)-or
26
、s(=o)2r
27
,其中r
20
、r
21
、r
22
、r
23
、r
24
、r
25
、r
26
和r
27
是选自由氢、(c
1-c
10
)烷基、(c
2-c
10
)烯基和(c
2-c
10
)炔基组成的组的单自由基;包含3至14个碳原子的已知环体系,所述体系包含1至3个环,其中:
[0166]
所述环中的每一个均是饱和的、部分不饱和的或芳族的;
[0167]
所述环是孤立的、部分或全部稠合的,
[0168]
形成已知环体系的成员中的每一个选自由以下组成的组:-ch-、-ch
2-、-nh-、-n-、-sh-、-s-和-o-;并且
[0169]
所述环体系任选地被独立地选自由以下组成的组的一个或多个基团取代:卤素、-oh、-nh2、-sh、c(=o)-卤素、(c
1-c
10
)卤代烷基和(c
1-c
10
)烷基-o-;以及
[0170]
(2b)环化步骤,包括z3和z4基团之间的偶联反应;或者,可替代地,
[0171]
(3a)通过缩合将肽的相应氨基酸与式(vii)的化合物和式(viii)的化合物偶联,式(vii)的化合物和式(viii)的化合物对应于称为“i”和“i+4”或“i+7”的氨基酸。化合物(vii)和(viii)将经历随后的环化步骤以生成“l”双自由基:
[0172][0173]
其中r
19
如以上所定义,z5和z6中的一个是(c
2-c
10
)炔基,并且另一个是(c
2-c
10
)烷基n3,以及
[0174]
(3.b)环化步骤,包括通过熟知的方案诸如cu(i)介导的huisgen 1,3-偶极环加成反应(也称为“点击”反应)使z5和z6基团缩合以生成1,4-取代的1,2,3-三唑桥(参见kolb h.c.等人,“the growing impact of click chemistry on drug discovery”,2003,drug discov today,8(24):1128-1137)。
[0175]
根据本发明的第二方面的肽的制备方法包括通过缩合将一个氨基酸的羧基或c末端与另一个氨基酸的氨基或n末端偶联,该偶联反应重复所需的次数,直到获得所需的肽。
[0176]
式(iii)、(iv)、(v)、(vi)、(vii)和(viii)的化合物可商购获得,并通过缩合与肽序列的已形成部分偶联。这些化合物可以携带用于肽的适当固相合成的珠,以及羧基、氨基或侧链的保护基。化合物的例示性非限制性实例是:2-(2'-丙烯基)丙氨酸、2-(3'-丁烯基)甘氨酸、2-(4'-戊烯基)丙氨酸、2-(6'-庚烯基)丙氨酸、2-(7'-辛烯基)丙氨酸、烯丙基-甘氨酸、5-叠氮基-正缬氨酸和α-炔丙基-丙氨酸等。
[0177]“偶联”步骤可以使用如以上所定义的氨基酸以及式(ii)至(vii)的α-α二取代氨基酸,通过一个氨基酸的羧基与另一个氨基酸残基的氨基缩合,按照方案“去保护-洗涤-偶联-洗涤”在固相中进行。
[0178]
固相肽合成的一般原理是重复去保护-洗涤-偶联-洗涤的循环。固相连接肽的游离n末端胺与单个n保护氨基酸单元偶联。然后将该单元去保护,得到一个新的n末端胺,其上可以连接另一个氨基酸。氨基酸在n和c末端处具有反应性部分,这有利于合成过程中的氨基酸偶联。许多氨基酸还具有反应性侧链官能团,其在合成和肽延伸过程中可以与自由
末端或其他侧链基团相互作用,并对产率和纯度产生负面影响。为了以最小的侧链反应性促进适当的氨基酸合成,已经开发了化学基团来结合特定的氨基酸官能团,并阻断或保护官能团免受非特异性反应。这些保护基虽然性质广泛,但可以分为以下三类:n末端保护基、c末端保护基(多用于液相合成)和侧链保护基。
[0179]
为了偶联所述肽,羧基通常被活化。这对加快反应很重要。存在两种主要类型的活化基团:碳二亚胺和三唑醇。然而,使用五氟苯基酯(fdpp,pfpoh])和bop-cl可用于肽的环化。
[0180]
纯化的单个氨基酸在合成前与这些保护基反应,然后在肽合成的特定步骤中被选择性除去。
[0181]
本发明可以使用的示例性树脂包括但不限于:(1)烯基树脂(例如,rem树脂、乙烯砜聚合物结合树脂、乙烯基-聚苯乙烯树脂);(2)胺官能化树脂(例如,脒树脂、n-(4-苄氧基苄基)羟胺聚合物结合的、(氨基甲基)聚苯乙烯、聚合物结合的(r)-(+)-a-甲基苄胺、2-氯三苯甲基knorr树脂、2-n-fmoc-氨基-二苯并环庚-1,4-二烯、聚合物结合的树脂、4-[4-(1-fmoc-氨基乙基)-2-甲氧基-5-硝基苯氧基]丁酰胺甲基-聚苯乙烯树脂、4-苄氧基苄胺聚合物结合的、聚合物结合的4-羧基苯磺酰胺、聚合物结合的双(叔丁氧基羰基)硫代假脲、二甲氨基甲基聚苯乙烯、fmoc-3-氨基-3-(2-硝基苯基)丙酸聚合物结合的、n-甲基氨基甲基化聚苯乙烯、pal树脂、sieber酰胺树脂、n-(2-巯基乙基)氨基甲酸叔丁基酯聚合物结合的、三苯基氯甲烷-4-甲酰胺聚合物结合的);(3)二苯甲基胺(bha)树脂(例如,2-氯二苯甲基氯聚合物结合的、的hmpb-二苯甲基胺聚合物结合、4-甲基二苯甲醇聚合物结合的、二苯甲基氯聚合物结合的、二苯甲基胺聚合物结合的);(4)br-官能化树脂(例如,4-(苄氧基)苄基溴聚合物结合的、4-溴代聚苯乙烯、溴化ppoa树脂、溴化wang树脂、溴缩醛聚合物结合的、溴代聚苯乙烯、200br、用于肽合成的聚苯乙烯a-br、溴化硒聚合物结合的、tentagel hl-br、tentagelmb-br、tentagel s-br);(5)氯甲基树脂(例如,聚合物结合的5-[4-(氯甲基)苯基]戊基]苯乙烯、聚合物结合的4-(苄氧基)苄基氯、聚合物结合的4-甲氧基二苯甲基氯);(6)cho官能化树脂(例如,(4-甲酰基-3-甲氧基苯氧基甲基)聚苯乙烯、(4-甲酰基-3-甲氧基苯氧基甲基)聚苯乙烯,3-苄氧基苯甲醛聚合物结合的、4-苄氧基-2,6-二甲氧基苯甲醛聚合物结合的、甲酰基聚苯乙烯、200cho、吲哚树脂、聚苯乙烯a—ch(oet)2、tentagel hl—ch(oet)2);(7)cl官能化树脂(例如,苯甲酰氯聚合物结合的、(氯甲基)聚苯乙烯、梅里菲尔德树脂);(8)co2h官能化树脂(例如,羧乙基聚苯乙烯、200cooh、聚苯乙烯am—cooh、tentagel hl—cooh、tentagel mb—cooh、tentagel s-cooh);(9)hypo-gel树脂(例如,200fmp、200phb、200trt-oh、200hmb);(10)i-官能化树脂(例如,4-碘苯酚聚合物结合的、碘聚苯乙烯);janda-jels
tm
(酰胺、jandajel-nh2、jandajel—cl、jandajel-4-羟基苯硫酚、jandajel-oh、jandajel-1-(3-二甲基氨基丙基)-3-乙基碳二亚胺、jandajel-1,3,4,6,7,8-六氢-2h-嘧啶并-[1,2-a]嘧啶、jandajel-吗啉、jandajel-聚吡啶、jandajel-三苯基膦、jandajel-wang);(11)mbha树脂(3[4
′‑
((羟甲基)苯氧基]丙酸-4-甲基二苯甲胺树脂、与mbha树脂聚合物结合的4-(羟甲基)苯氧基乙酸、hmba-4-甲基二苯甲胺聚合物结合的、4-甲基二苯甲胺盐酸盐聚合物结合的capacity(胺));(12)nh2官能化
树脂((氨甲基)聚苯乙烯、(氨甲基)聚苯乙烯、200nh2、聚苯乙烯am-nh2、2-氨基乙基化聚苯乙烯微球、2-溴乙基化聚苯乙烯微球、2-羟基乙基化聚苯乙烯微球、tentagelhl-nh2、tentagel m br、tentagel m nh2、tentagel m oh、tentagel mb-nh2、tentagel s-nh2、tentagel s-nh2);(13)oh官能化树脂(例如,4-羟甲基苯甲酸聚合物结合的、羟甲基树脂(hydroxymethyl resins)、oh官能化的wang树脂);(14)肟树脂(例如,4-氯二苯甲酮肟聚合物结合的、二苯甲酮肟聚合物结合的、4-甲氧基二苯甲酮肟聚合物结合的);(15)peg树脂(例如,乙二醇聚合物结合的);(16)boc-/blz肽合成树脂(例如,boc-lys(boc)-lys[boc-lys(boc)]-cys(acm)-b-ala-o-pam树脂、boc-lys(fmoc)-lys[boc-lys(fmoc)]-b-ala-o-pam树脂、boc-lys(boc)-lys[boc-lys(boc)]-lys{boc-lys(boc)-lys[boc-lys(boc)]}-b-ala-o-pam树脂、boc-lys(fmoc)-lys[boc-lys(fmoc)]-lys[boc-lys(fmoc)-lys{boc-lys(fmoc)]}-b-ala-o-pam树脂、boc-lys(boc)-lys[boc-lys(boc)]-lys{boc-lys(boc)-lys[boc-lys(boc)]}—cys(acm)-b-ala-o-pam树脂、预载pam树脂);(17)fmoc-/t-bu肽合成树脂(例如,fmoc-lys(fmoc)-lys[fmoc-lys(fmoc)]-b-ala-o-wang树脂、fmoc-lys(fmoc)-lys[fmoc-lys(fmoc)]-lys{fmoc-lys(fmoc)-lys[fmoc-lys(fmoc)]}-b-ala-o-wang树脂、预载s三苯甲基树脂、预载树脂、预载三苯甲基树脂、预载wang树脂、预载氨基醇的三苯甲基树脂);(19)硫醇官能化树脂(例如,200s-trt、聚苯乙烯am-s-三苯甲基、tentagelhl-s-三苯甲基、tentagel mb-s-三苯甲基、tentagel s-s-三苯甲基);和(20)wang树脂(例如,fmoc-ala-wang树脂、fmoc-arg(pbf)-wang树脂、fmoc-arg(pmc)-wang树脂、fmoc-asn(trt)-wang树脂、fmoc-asp(otbu)-wang树脂、fmoc-cys(acm)-wang树脂、fmoc-cys(stbu)-wang树脂、fmoc-cys(trt)wang树脂、fmoc-gln(trt)-wang树脂、fmoc-glu(otbu)-wang树脂、fmoc-gly-wang树脂、fmoc-his(trt)-wang树脂、fmoc-ile-wang树脂、fmoc-leu-wang树脂、fmoc-lys(boc)-wang树脂、fmoc-met-wang树脂、fmoc-d-met-wang树脂、fmoc-phe-wang树脂、fmoc-pro-wang树脂、fmoc-ser(tbu)-wang树脂、fmoc-ser(trt)-wang树脂、fmoc-thr(tbu)-wang树脂、fmoc-trp(boc)wang树脂、fmoc-trp-wang树脂、fmoc-tyr(tbu)-wang树脂、fmoc-val-wang树脂)。
[0182]“保护基”(pg)是指当与分子中的反应性基团连接时,掩蔽、降低或阻止该基团反应性的一组原子。
[0183]
合适的氨基保护基包括氨基甲酸甲酯、氨基甲酸乙酯、9-芴基氨基甲酸甲酯(fmoc)、9-(2-磺基)芴基氨基甲酸甲酯、9-(2,7-二溴)芴基氨基甲酸甲酯、2,7-二叔丁基-[9-(10,10-二氧代-10,10,10,10-四氢噻吨基)]氨基甲酸甲酯(dbd-tmoc)、4-甲氧基苯甲酰甲基氨基甲酸酯(phenoc)、2,2,2-三氯乙基氨基甲酸酯(troc)、2-三甲基甲硅烷基氨基甲酸乙酯(teoc)、2-苯乙基氨基甲酸酯(hz)、1-(1-金刚烷基)-1-甲基乙基氨基甲酸酯(adpoc)、1,1-二甲基-2-卤代乙基氨基甲酸酯、1,1-二甲基-2,2-二溴乙基氨基甲酸酯(db-t-boc)、1,1-二甲基-2,2,2-三氯乙基氨基甲酸酯(tcboc)、1-甲基-1-(4-联苯基)乙基氨基甲酸酯(bpoc)、1-(3,5-二叔丁基苯基)-1-甲基氨基甲酸乙酯(t-bumeoc)、2-(2'-和4'-吡啶基)氨基甲酸乙酯(pyoc)、2-(n,n-二环己基甲酰胺基)氨基甲酸乙酯、叔丁基氨基甲酸酯(boc)、1-金刚烷基氨基甲酸酯(adoc)、氨基甲酸乙烯酯(voc)、烯丙基氨基甲酸酯(alloc)、1-异丙基烯丙基氨基甲酸酯(ipaoc)、肉桂基氨基甲酸酯(coc)、4-硝基肉桂基氨基甲酸酯
(noc)、8-喹啉基氨基甲酸酯、n-羟基哌啶基氨基甲酸酯、烷基二硫代氨基甲酸酯、氨基甲酸苄酯(cbz)、对甲氧基氨基甲酸苄酯(moz)、对-硝基苄基氨基甲酸酯、对-溴苄基氨基甲酸酯、对-氯苄基氨基甲酸酯、2,4-二氯苄基氨基甲酸酯、4-甲基亚磺酰基苄基氨基甲酸酯(msz)、9-蒽基甲基氨基甲酸酯、二苯基甲基氨基甲酸酯、2-甲硫基乙基氨基甲酸酯、2-甲磺酰基乙基氨基甲酸酯、2-(对甲苯磺酰基)乙基氨基甲酸酯、[2-(1,3-二噻烷基)]氨基甲酸甲酯([2-(1,3-dithianyl)]methylcarbamate,dmoc)、4-甲基噻吩基氨基甲酸酯(mtpc)、2,4-二甲基噻吩基氨基甲酸酯(bmpc)、2-磷酰氨基甲酸乙酯(peoc)、2-三苯基磷酰异丙基氨基甲酸酯(ppoc)、1,1-二甲基-2-氰基乙基氨基甲酸酯、间-氯-对-酰氧基苄基氨基甲酸酯、对-(二羟基硼基)苄基氨基甲酸酯、5-苯并异噁唑基甲基氨基甲酸酯、2-(三氟甲基)-6-色酮基甲基氨基甲酸酯(tcroc)、间-硝基苯基氨基甲酸酯、3,5-二甲氧基苄基氨基甲酸酯、邻-硝基苄基氨基甲酸酯、3,4-二甲氧基-6-硝基苄基氨基甲酸酯、苯基(邻-硝基苯基)氨基甲酸甲酯、吩噻嗪基-(10)-羰基衍生物、n'-对-甲苯磺酰氨基羰基衍生物、n'-苯基氨基硫代羰基衍生物、氨基甲酸叔戊酯、s-苄基硫代氨基甲酸酯、对-氰基苄基氨基甲酸酯、环丁基氨基甲酸酯、环己基氨基甲酸酯、环戊基氨基甲酸酯、环丙基甲基氨基甲酸酯、对-癸氧基苄基氨基甲酸酯、2,2-二甲氧基羰基乙烯基氨基甲酸酯、邻-(n,n-二甲基甲酰胺基)苄基氨基甲酸酯、1,1-二甲基-3-(n,n-二甲基甲酰胺基)丙基氨基甲酸酯、1,1-二甲基丙炔基氨基甲酸酯、二(2-吡啶基)甲基氨基甲酸酯、2-呋喃基甲基氨基甲酸酯、2-碘乙基氨基甲酸酯、异冰片基氨基甲酸酯、氨基甲酸异丁酯、异烟酰基氨基甲酸酯、对-(对'-甲氧基苯基偶氮)苄基氨基甲酸酯、1-甲基环丁基氨基甲酸酯、1-甲基环己基氨基甲酸酯、1-甲基-1-环丙基甲基氨基甲酸酯、1-甲基-1-(3,5-二甲氧基苯基)乙基氨基甲酸酯、1-甲基-1-(对-苯基偶氮苯基)氨基甲酸乙酯、1-甲基-1-苯基乙基氨基甲酸酯、1-甲基-1-(4-吡啶基)氨基甲酸乙酯、苯基氨基甲酸酯、对-(苯基偶氮)苄基氨基甲酸酯、2,4,6-三叔丁基苯基氨基甲酸酯、4-(三甲基铵)苄基氨基甲酸酯、2,4,6-三甲基苄基氨基甲酸酯、甲酰胺、乙酰胺、氯乙酰胺、三氯乙酰胺、三氟乙酰胺、苯乙酰胺、3-苯基丙酰胺、吡啶甲酰胺、3-吡啶甲酰胺、n-苯甲酰基苯丙氨酰衍生物、苯甲酰胺、对-苯基苯甲酰胺、邻-硝基苯基乙酰胺、邻-硝基苯氧乙酰胺、乙酰乙酰胺、(n'-二硫代苄氧羰基氨基)乙酰胺、3-(对-羟基苯基)丙酰胺、3-(邻-硝基苯基)丙酰胺、2-甲基-2-(邻-硝基苯氧基)丙酰胺、2-甲基-2-(邻-苯偶氮苯氧基)丙酰胺、4-氯丁酰胺、3-甲基-3-硝基丁酰胺、邻-硝基肉桂酰胺、n-乙酰甲硫氨酸衍生物、邻-硝基苯甲酰胺、邻-(苯甲酰氧基甲基)苯甲酰胺、4,5-二苯基-3-噁唑啉-2-酮、n-邻苯二甲酰亚胺、n-二硫代琥珀酰亚胺(dts)、n-2,3-二苯基马来酰亚胺、n-2,5-二甲基吡咯、n-1,1,4,4-四甲基二甲硅烷基氮杂环戊烷加合物(stabase)、5-取代的1,3-二甲基-1,3,5-三氮杂环己烷-2-酮、5-取代的1,3-二苄基-1,3,5-三氮杂环己烷-2-酮、1-取代的3,5-二硝基-4-吡啶酮、n-甲胺、n-烯丙胺、n-[2-三甲基甲硅烷基)乙氧基]甲胺(sem)、n-3-乙酰氧基丙胺、n-(1-异丙基-4-硝基-2-氧代-3-吡喃并-3-基)胺、季铵盐、n-苄胺、n-二(4-甲氧基苯基)甲胺、n-5-二苯并环庚胺、n三苯基甲胺(tr)、n-[(4-甲氧基苯基)二苯基甲基]胺(mmtr)、n-9-苯基芴基胺(phf)、n-2,7-二氯-9-芴基亚甲基胺、n-二茂铁基甲胺(fcm)、n-2-吡啶甲基氨基n'-氧化物、n-1,1-二甲基硫代亚甲基胺、n-亚苄基胺、n-对-甲氧基亚苄基胺、n-二苯基亚甲基胺、n-[(2-吡啶基)均三甲苯基]亚甲基胺、n-(n',n'-二甲基氨基亚乙基)胺、n,n'-异亚丙基二胺、n-对-硝基亚苄基胺、n-亚水杨基胺、n-5-氯亚水杨基胺、n-(5-氯-2-羟基苯基)苯
基亚甲基胺、n-亚环己基胺、n-(5,5-二甲基-3-氧代-1-环己烯基)胺、n-硼烷衍生物、n-二苯基硼酸衍生物、n-[苯基(五羰基铬或钨)羰基]胺、n-铜螯合物、n-锌螯合物、n-硝基胺、n-亚硝基胺、胺n-氧化物、二苯基膦酰胺(dpp)、二甲基硫代膦酰胺(mpt)、二苯基硫代膦酰胺(ppt)、二烷基氨基磷酸酯、二苄基氨基磷酸酯、二苯基氨基磷酸酯、苯亚磺酰胺、邻-硝基苯亚磺酰胺(nps)、2,4-二硝基苯亚磺酰胺、五氯苯亚磺酰胺、2-硝基-4-甲氧基苯亚磺酰胺、三苯基甲基亚磺酰胺、3-硝基吡啶亚磺酰胺(npys)、对-甲苯磺酰胺(ts)、苯磺酰胺、2,3,6,-三甲基-4-甲氧基苯磺酰胺(mtr)、2,4,6-三甲氧基苯磺酰胺(mtb)、2,6-二甲基-4-甲氧基苯磺酰胺(pme)、2,3,5,6-四甲基-4-甲氧基苯磺酰胺(mte)、4-甲氧基苯磺酰胺(mbs)、2,4,6-三甲基苯磺酰胺(mts)、2,6-二甲氧基-4-甲基苯磺酰胺(imds)、2,2,5,7,8-五甲基苯并二氢吡喃-6-磺酰胺(pmc)、甲磺酰胺(ms)、β-三甲基甲硅烷基乙磺酰胺(ses)、9-蒽磺酰胺、4-(4',8'-二甲氧基萘甲基)苯磺酰胺(dnmbs)、苯甲基磺酰胺、三氟甲基磺酰胺和苯甲酰甲基磺酰胺。
[0184]
适当保护的羧酸的实例还包括但不限于甲硅烷基、烷基、烯基、芳基和芳基烷基保护的羧酸。合适的甲硅烷基的实例包括三甲基甲硅烷基、三乙基甲硅烷基、叔丁基二甲基甲硅烷基、叔丁基二苯基甲硅烷基、三异丙基甲硅烷基等。合适的烷基的实例包括甲基、苄基、对甲氧基苄基、3,4-二甲氧基苄基、三苯甲基、叔丁基、四氢吡喃-2-基。合适的烯基的实例包括烯丙基。合适的芳基的实例包括任选取代的苯基、联苯基或萘基。合适的芳基烷基的实例包括任选取代的苄基(例如,对甲氧基苄基(mpm)、3,4-二甲氧基苄基、邻硝基苄基、对硝基苄基、对卤代苄基、2,6-二氯苄基、对氰基苄基)和2-和4-甲基吡啶基。
[0185]
在第二方面,本发明提供了一种药物或化妆品组合物。
[0186]
如本文所用的表述“治疗有效量”是指当施用时传递到血流并且足以预防待解决疾病的发展或在一定程度上减轻其一种或多种症状的化合物的量。根据本发明施用的肽的具体剂量当然将通过围绕病例的特定情况确定,所述特定情况包括施用的化合物、施用的途径、所治疗的具体病症以及类似的考虑因素。在本发明的第二方面的一个实施方案中,药物组合物是肠胃外组合物。在另一个实施方案中,药物组合物用于口服施用。
[0187]
在本发明的上下文中,表述“化妆品有效量”是指当应用(例如局部)时保留在皮肤组织内(诸如在皮下水平)而没有显著到达或没有到达血流,从而在皮肤结构内发挥局部作用的化合物的量。根据本发明施用的肽的具体剂量当然将围绕病例的具体情况决定。在本发明的一个实施方案中,本发明的肽的“化妆品有效量”高于、等于或低于在通过肠胃外途径、特别是静脉途径施用时达到治疗效果所需的量。
[0188]
术语“药学上可接受的”是指适用于在制药技术中用于制备具有医疗用途的组合物的赋形剂或载体。
[0189]
本文中可互换使用的术语“化妆品可接受的”是指适于与人皮肤接触使用而没有不当毒性、不相容性、不稳定性、过敏反应等的赋形剂或载体。
[0190]
表述“赋形剂和/或载体”是指可接受的材料、组合物或媒介物。每种组分在可与组合物的其他成分相容的意义上必须是药学上或化妆品可接受的。它们还必须适用于与人和非人动物的组织或器官接触而不产生过度毒性、刺激、过敏反应或其他问题或并发症且与合理的益处/风险比相称。合适的可接受赋形剂的实例是溶剂、分散介质、稀释剂或其他液体媒介物、分散或悬浮助剂、表面活性剂、等渗剂、增稠剂或乳化剂、防腐剂、固体粘合剂、润
滑剂等。除非在任何常规的赋形剂介质与物质或其衍生物不相容,诸如通过产生任何不希望的生物作用或以有毒方式与药物或化妆品组合物的任何其他组分相互作用的情况下,否则其用途被考虑在本发明的范围内。
[0191]
本文所述的药物和化妆品组合物的配制品可以通过药理学和化妆品领域已知的或今后开发的任何方法来制备。通常,此类制备方法包括以下步骤:使活性成分(所述肽)与赋形剂和/或一种或多种其他辅助成分联合,并且然后如果必要和/或希望,将产物成形和/或包装成所希望的单剂量或多剂量单位。
[0192]
本发明的药物组合物可以作为单一单位剂量和/或作为多个单一单位剂量进行制备、包装和/或批量出售。如本文所用,“单位剂量”是包含预定量的活性成分的药物组合物的个别量。
[0193]
本发明的组合物中活性成分(即如前述方面和实施方案中任一项所定义的肽)、可接受的赋形剂和/或任何另外的成分的相对量将根据所治疗受试者的身份、体型和/或病症并且进一步根据所述组合物的施用途径而变化。
[0194]
用于制造这些组合物的可接受的赋形剂包括但不限于惰性稀释剂、分散剂和/或制粒剂、表面活性剂和/或乳化剂、崩解剂、粘合剂、防腐剂、缓冲剂、润滑剂和/或油。此类赋形剂可以任选地包含在本发明的配制品中。根据配方师的判断,诸如可可脂和栓剂蜡、着色剂、包衣剂、甜味剂、调味剂和香化剂的赋形剂可以存在于组合物中。
[0195]
示例性稀释剂包括但不限于碳酸钙、碳酸钠、磷酸钙、磷酸二钙、硫酸钙、磷酸氢钙、磷酸钠乳糖、蔗糖、纤维素、微晶纤维素、高岭土、甘露醇、山梨醇、肌醇、氯化钠、干淀粉、玉米淀粉、糖粉及其组合。
[0196]
示例性制粒剂和/或分散剂包括但不限于马铃薯淀粉、玉米淀粉、木薯淀粉、羧甲淀粉钠、粘土、海藻酸、瓜尔胶、柑橘果肉、琼脂、膨润土、纤维素和木制品、天然海绵、阳离子交换树脂、碳酸钙、硅酸盐、碳酸钠、交联聚乙烯吡咯烷酮(交聚维酮)、羧甲基淀粉钠(羧甲淀粉钠)、羧甲基纤维素、交联羧甲基纤维素钠(交联甲羧纤维素)、甲基纤维素、预胶化淀粉(淀粉1500)、微晶淀粉、水不溶性淀粉、羧甲基纤维素钙、硅酸铝镁(veegum)、月桂基硫酸钠、季铵化合物及其组合。
[0197]
示例性表面活性剂和/或乳化剂包括但不限于天然乳化剂(例如,阿拉伯胶、琼脂、海藻酸、海藻酸钠、黄蓍胶、角叉菜(chondrux)、胆固醇、黄原胶、果胶、明胶、蛋黄、酪蛋白、羊毛脂、胆固醇、蜡和卵磷脂)、胶质粘土(例如膨润土[硅酸铝]和veegum[硅酸镁铝])、长链氨基酸衍生物、高分子量醇(例如硬脂醇、十六醇、油醇、单硬脂酸三乙酯、乙二醇二硬脂酸酯、单硬脂酸甘油酯以及丙二醇单硬脂酸酯、聚乙烯醇)、卡波姆(例如,羧基聚亚甲基、聚丙烯酸、丙烯酸聚合物和羧基乙烯基聚合物)、角叉菜胶、纤维素衍生物(例如,羧甲基纤维素钠、粉状纤维素、羟甲基纤维素、羟丙基纤维素、羟丙基甲基纤维素、甲基纤维素)、山梨醇酐脂肪酸酯{例如,聚氧乙烯脱水山梨醇酐单月桂酸酯[tween 20]、聚氧乙烯脱水山梨醇酐[tween 60]、聚氧乙烯脱水山梨醇酐单油酸酯[tween 80]、脱水山梨醇酐单棕榈酸酯[span 40]、脱水山梨醇酐单硬脂酸酯[span 60]、脱水山梨醇酐三硬脂酸酯[span 65]、甘油单油酸酯、脱水山梨醇酐单油酸酯[span 80])、聚氧乙烯酯(例如,聚氧乙烯单硬脂酸酯[myrj 45]、聚氧乙烯氢化蓖麻油、聚乙氧基蓖麻油、聚甲醛硬脂酸酯和solutol)、蔗糖脂肪酸酯、聚乙二醇脂肪酸酯(例如,cremophor)、聚氧乙烯醚(例如,聚氧乙烯月桂基醚[brij 30])、
聚(乙烯基-吡咯烷酮)、二甘醇单月桂酸酯、三乙醇胺油酸酯、油酸钠、油酸钾、油酸乙酯、油酸、月桂酸乙酯、月桂基硫酸钠、pluronic f 68、poloxamer 188、西曲溴铵、氯化十六烷基吡啶、苯扎氯铵、多库酯钠等和/或其组合。
[0198]
示例性粘合剂包括但不限于淀粉(例如,玉米淀粉和淀粉糊);明胶;糖(例如,蔗糖、葡萄糖、右旋糖、糊精、糖蜜、乳糖、乳糖醇、甘露醇);天然和合成树胶(例如,阿拉伯树胶、海藻酸钠、爱尔兰苔藓提取物、panwar树胶、印度树胶、等足类动物(isapol)外皮的粘液、羧甲基纤维素、甲基纤维素、乙基纤维素、羟乙基纤维素、羟丙基纤维素、羟丙基甲基纤维素、微晶纤维素、醋酸纤维素、聚乙烯吡咯烷酮)、硅酸铝镁(veegum)和落叶松阿拉伯半乳聚糖);藻酸盐;聚环氧乙烷;聚乙二醇;无机钙盐;硅酸;聚甲基丙烯酸酯;蜡;水;酒精;及其组合。
[0199]
示例性防腐剂可以包括抗氧化剂、螯合剂、抗微生物防腐剂、抗真菌防腐剂、酒精防腐剂、酸性防腐剂和其他防腐剂。示例性抗氧化剂包括但不限于α生育酚、抗坏血酸、抗坏血酸棕榈酸酯、丁基化羟基茴香醚、丁基化羟基甲苯、单硫代甘油、焦亚硫酸钾、丙酸、没食子酸丙酯、抗坏血酸钠、亚硫酸氢钠、焦亚硫酸钠和亚硫酸钠。示例性螯合剂包括乙二胺四乙酸(edta)、柠檬酸一水合物、乙二胺四乙酸二钠、乙二胺四乙酸二钾、乙二胺四乙酸、富马酸、苹果酸、磷酸、乙二胺四乙酸钠、酒石酸和乙二胺四乙酸三钠。示例性抗微生物防腐剂包括但不限于苯扎氯铵、苄索氯铵、苯甲醇、溴硝醇、西曲溴铵、氯化十六烷基吡啶、氯己定、氯丁醇、氯甲酚、氯二甲苯酚、甲酚、乙醇、甘油、海克替啶、咪脲、苯酚、苯氧乙醇、苯乙醇、硝酸苯汞、丙二醇和硫柳汞。示例性抗真菌防腐剂包括但不限于对羟基苯甲酸丁酯、对羟基苯甲酸甲酯、对羟基苯甲酸乙酯、对羟基苯甲酸丙酯、苯甲酸、羟基苯甲酸、苯甲酸钾、山梨酸钾、苯甲酸钠、丙酸钠和山梨酸。示例性醇防腐剂包括但不限于乙醇、聚乙二醇、苯酚、酚类化合物、双酚、氯代丁醇、羟基苯甲酸酯和苯乙醇。示例性酸性防腐剂包括但不限于维生素a、维生素c、维生素e、β-胡萝卜素、柠檬酸、乙酸、脱氢乙酸、抗坏血酸、山梨酸和植酸。其他防腐剂包括但不限于生育酚、生育酚醋酸酯、甲磺酸迪特奥希姆(deteroxime mesylate)、西曲溴铵、丁基化羟基茴香醚(bha)、丁基化羟基甲苯(bht)、乙二胺、十二烷基硫酸钠(sls)、十二烷基醚硫酸钠(sles)、亚硫酸氢钠、焦亚硫酸钠、亚硫酸钾、焦亚硫酸钾、glydant plus、phenonip、对羟基苯甲酸甲酯、germall 115、germaben ii、尼奥龙(neolone)、凯松(kathon)和euxyl。在某些实施方案中,所述防腐剂是抗氧化剂。在其他实施方案中,所述防腐剂是螯合剂。
[0200]
示例性缓冲剂包括但不限于柠檬酸盐缓冲溶液、乙酸盐缓冲溶液、磷酸盐缓冲溶液、氯化铵、碳酸钙、氯化钙、柠檬酸钙、葡乳醛酸钙、葡庚糖酸钙、葡萄糖酸钙、d-葡萄糖酸、甘油磷酸钙、乳酸钙、丙酸、乙酰丙酸钙、戊酸、磷酸氢钙、磷酸、磷酸三钙、氢氧化钙磷酸盐、乙酸钾、氯化钾、葡萄糖酸钾、钾混合物、磷酸氢二钾、磷酸二氢钾、磷酸钾混合物、乙酸钠、碳酸氢钠、氯化钠、柠檬酸钠、乳酸钠、磷酸氢二钠、磷酸二氢钠、磷酸钠混合物、氨丁三醇、氢氧化镁、氢氧化铝、海藻酸、无热原水、等渗盐水、林格氏溶液、乙醇及其组合。
[0201]
示例性润滑剂包括但不限于硬脂酸镁、硬脂酸钙、硬脂酸、二氧化硅、滑石、麦芽、甘油二十二烷酸酯(glyceryl behanate)、氢化植物油、聚乙二醇、苯甲酸钠、乙酸钠、氯化钠、亮氨酸、十二烷基硫酸镁、十二烷基硫酸钠及其组合。
[0202]
示例性油包括但不限于杏仁、杏核油、鳄梨、巴巴苏、佛手柑、黑醋栗种子、琉璃苣、
杜松、甘菊、卡诺拉、香菜、巴西棕榈、蓖麻、肉桂、可可脂、椰子、鱼肝、咖啡、玉米、棉籽、鸸鹋、桉树、月见草、鱼、亚麻籽、香叶醇、葫芦、葡萄籽、榛子、牛膝草、肉豆蔻酸异丙酯、荷荷巴、石栗(kukui)果、杂薰衣草、薰衣草、柠檬、山苍子、夏威夷坚果、锦葵、芒果种子、白芒花籽、貂、肉豆蔻、橄榄、橙子、橙连鳍鲑、棕榈树、棕榈仁、桃仁、花生仁、罂粟籽、南瓜子、油菜籽、米糠、迷迭香、红花、檀香、山茶花(sasquana)、香薄荷、沙棘、芝麻、乳木果、硅树脂、大豆、向日葵、茶树、蓟、椿、香根草、核桃和小麦胚芽油。示例性油包括但不限于硬脂酸丁酯、辛酸甘油三酯、癸酸甘油三酯、环聚二甲基硅氧烷、癸二酸二乙酯、二甲聚硅氧烷360、肉豆蔻酸异丙酯、矿物油、辛基十二烷醇、油醇、硅油及其组合。
[0203]
用于肠胃外施用的液体剂型包括但不限于药学上可接受的脂质体乳液、微乳液、溶液、悬浮液、糖浆剂和酏剂。除了活性成分之外,所述液体剂型可以包含本领域常用的惰性稀释剂,例如像,水或其他溶剂、增溶剂以及乳化剂,诸如乙醇、异丙醇、碳酸乙酯、乙酸乙酯、苯甲醇、苯甲酸苄酯、丙二醇、1,3-丁二醇、二甲基甲酰胺、油(具体地说,棉籽油、花生油、玉米油、胚芽油、橄榄油、蓖麻油以及芝麻油)、甘油、四氢糠醇、聚乙二醇以及脱水山梨醇的脂肪酸酯及其混合物。在肠胃外施用的某些实施方案中,本发明的缀合物与增溶剂(诸如聚乙氧基蓖麻油(例如cremophor
tm
)、醇、油、改性油、二醇、聚山梨醇酯、环糊精、聚合物及其组合)混合。
[0204]
可注射制剂,例如无菌可注射水性或油性悬浮液,可以根据已知技术使用合适的分散剂或湿润剂和悬浮剂来配制。无菌可注射制剂可以是在非毒性的、肠胃外可接受的稀释剂或溶剂中的无菌可注射的溶液、悬浮液或乳液,例如作为在1.3-丁二醇中的溶液。可以采用的可接受的媒介物和溶剂是水、林格氏溶液、u.s.p.以及等渗氯化钠溶液。此外,常规地采用无菌的固定油作为溶剂或悬浮介质。为此目的,可以采用任何温和的固定油,包括合成的甘油单酯或甘油二酯。此外,将脂肪酸(诸如油酸)用于制备注射剂。可替代地,所述制剂可以是脂质体的形式。
[0205]
可以将可注射配制品灭菌,例如,通过细菌保留过滤器过滤,或通过掺入无菌固体组合物形式的灭菌剂,所述灭菌剂在使用前可以溶解或分散在无菌水或其他无菌可注射介质中。
[0206]
为了延长药物的作用,经常希望减缓皮下注射或肌肉内注射的药物的吸收。这可以通过使用水溶性差的结晶或无定形材料的液体悬浮液来实现。药物的吸收速率则取决于其溶解速率,而溶解速率又可以取决于晶体大小和晶形。可替代地,通过将药物溶解或悬浮于油媒介物中来完成肠胃外施用的药物形式的延迟吸收。
[0207]
如上所述,本发明的肽可以是具有一种或多种赋形剂的微囊密封形式。在一个实施方案中,本发明的肽配制在脂质体中。
[0208]
应理解,本发明的肽和药物组合物可以用于组合疗法。在组合方案中使用的特定疗法组合(治疗或程序)将考虑所需治疗和/或程序的兼容性以及要实现的所需治疗效果。应理解,所采用的治疗可以实现对相同目的的所需效果(例如,可用于检测肿瘤的本发明缀合物可以与可用于检测肿瘤的另一种药剂同时施用),或者它们可以实现不同的效果(例如,控制任何副作用)。
[0209]
本发明的药物组合物可以单独施用或者与一种或多种其他治疗剂组合施用。“与
……
组合”并不旨在暗示所述药剂必须同时施用和/或一起配制用于递送,但是这些递
送方法在本发明的范围内。所述组合物可以与一种或多种其他所需的治疗或医疗程序同时、在其之前或之后施用。通常,每种药剂将以针对所述药剂确定的剂量和/或时间表来施用。另外,本发明包括肽或药物组合物与可以提高其生物利用度、减少和/或改变其代谢、抑制其排泄和/或改变其在体内分布的药剂组合的递送。
[0210]
在组合方案中采用的疗法特定组合将考虑所需治疗和/或程序的兼容性以及要实现的所需治疗效果。应理解,所采用的疗法可以实现对相同病症的所需效果(例如,本发明的肽可以与用于治疗相同病症的另一种生物活性剂同时施用),和/或它们可以实现不同的效果(例如,控制任何副作用)。将进一步理解的是,用于这种组合的生物活性剂可以在单一组合物中一起施用,或者在不同组合物中分别施用。
[0211]
表述“与
……
组合”还包括(通过化学-物理相互作用)将本发明的肽与以上和以下提到的任何其他药剂缀合的可能性,所述药剂可以是治疗剂或用于改善肽特性(诸如生物利用度)的药剂等。
[0212]
在一个实施方案中,本发明的肽与一种或多种抗癌剂组合施用。抗癌剂可以是例如甲氨蝶呤、长春新碱、阿霉素、顺铂、不含糖的氯乙基亚硝脲、5-氟尿嘧啶、丝裂霉素c、博莱霉素、多柔比星、达卡巴嗪、紫杉醇、fragyline、meglamine gla、戊柔比星、卡莫司汀(carmustaine)和聚苯丙生(poliferposan)、mmi270、bay 12-9566、ras法尼基转移酶抑制剂、法尼基转移酶抑制剂、mmp、mta/ly231514、ly264618/lometexol、glamolec、ci-994、tnp-470、hycamtin/拓扑替康、pkc412、伐司朴达(valspodar)/psc833、米托蒽醌(novantrone)/mitroxantrone、metaret/苏拉明(suramin)、巴马司他、e7070、bch-4556、cs-682、9-ac、ag3340、ag3433、incel/vx-710、vx-853、zd0101、isi641、odn 698、ta 2516/marmistat、bb2516/marmistat、cdp 845、d2163、pd183805、dx895 if、lemonal dp 2202、fk 317、沙培林(picibanil)/ok-432、ad 32/戊柔比星、metastron/锶衍生物、temodal/替莫唑胺、evacet/脂质体多柔比星、yewtaxan/紫杉醇(paclitaxel)、紫杉酚/紫杉醇、xeload/卡培他滨、氟铁龙(furtulon)/去氧氟尿苷、cyclopax/口服紫杉醇、口服紫杉烷、spu-077/顺铂、hmr 1275/夫拉平度(flavopiridol)、cp-358(774)/egfr、cp-609(754)/ras癌基因抑制剂、bms-182751/口服铂类、uft(替加氟/尿嘧啶)、ergamisol/左旋咪唑、恩尿嘧啶(eniluracil)/776c85/5fu增强剂、开普拓(campto)/左旋咪唑、camptosar/伊立替康、tumodex/ralitrexed、leustatin/克拉屈滨、paxex/紫杉醇、doxil/脂质体多柔比星、caelyx/脂质体多柔比星、fludara/氟达拉滨、pharmarubicin/表柔比星、depocyt、zd1839、lu 79553/双-萘酰亚胺、lu 103793/dolastain、caetyx/脂质体多柔比星、gemzar/吉西他滨、zd 0473/anormed、ym 116、碘种子、cdk4和cdk2抑制剂、parp抑制剂、d4809/dexifosamide、ifes/mesnex/ifosamide、vumon/替尼泊苷、paraplatin/卡铂、plantinol/顺铂、vepeside/依托泊苷、zd 9331、泰素帝(taxotere)/多西他赛、鸟嘌呤阿拉伯糖苷的前药、紫杉烷类似物、亚硝基脲、烷基化剂(诸如melphelan和环磷酰胺)、氨鲁米特(aminoglutethimide)、天冬酰胺酶、白消安、卡铂、苯丁酸氮芥、阿糖孢苷hcl、放线菌素d、柔红霉素hcl、雌莫司汀磷酸钠、依托泊苷(vp16-213)、氟尿苷、氟尿嘧啶(5-fu)、氟他胺、羟基脲(羟基尿素)、异环磷酰胺、干扰素α-2a、α-2b、醋酸亮丙瑞林(lhrh释放因子类似物)、环己亚硝脲(ccnu)、二氯甲二乙胺hcl(氮芥)、巯嘌呤、美司钠、米托坦(o.p-ddd)、米托蒽醌hcl、奥曲肽、普卡霉素、甲基苄肼hcl、链脲佐菌素、枸橼酸他莫昔芬、硫鸟嘌呤、噻替派、硫
chemical);茚三酮(国药集团化学试剂有限公司);哌啶(vertellus);二甲基甲酰胺、dmf(浙江江山化工有限公司);三氟乙酸,tfa(三氟乙酸,solvay),tis(茴香硫醚,solvay)。
[0224]
简而言之,线性多肽是以rink酰胺mbha树脂为载体,使用基于fmoc的spps(固相多肽合成法)人工合成的。
[0225]
使用了以下方案:
[0226]
1.用dmf中的20%哌啶去除fmoc保护基。
[0227]
2.用dmf洗涤树脂五次。
[0228]
3.随后使用fmoc-aa(3当量)、hbtu(3当量)和n-甲基吗啉(6当量)将fmoc保护的氨基酸偶联45min。
[0229]
4.用dmf洗涤树脂五次。通过茚三酮测试检查偶联。
[0230]
5.从步骤1开始重复。
[0231]
6.通过与琥珀酸酐(10当量)和n-甲基吗啉(10当量)反应将n-末端封端。
[0232]
通过暴露于溶液f(95%tfa,2.5%水,2.5%tis)将肽从树脂上切割下来并去保护,并且冻干。
[0233]
使用c18柱通过反相hplc纯化冻干肽(详情参见化合物表征)。通过lc-ms-esi对肽进行了鉴定。所有化合物的所有质谱数据在下表1中示出。
[0234]
如下购买材料:fmoc保护的α-氨基酸(包括烯属氨基酸fmoc-[(s)-2-(4戊烯基)丙氨酸]oh、fmoc-[(r)-2-(4戊烯基)丙氨酸]oh、fmoc-[(s)-2-(7辛烯基)丙氨酸]oh、fmoc-[(r)-2-(4戊烯基)丙氨酸]oh、2-(6-氯-1-h-苯并三唑-1-基)-1,1,3,3-四甲基氨基六氟磷酸盐(tbtu)、树脂、二甲基甲酰胺(dmf)、n,n-二异丙基乙胺(diea)、三氟乙酸(tfa)、1,2-二氯乙烷(dce)、grubbs ru(iv)催化剂和哌啶购自不同供应商。
[0235]
简而言之,线性多肽是使用fmoc固相肽化学用自动合成器合成的。仅在从反应器容器中取出树脂后人工进行与烯属氨基酸的偶联,如前一节所公开。
[0236]
在从树脂上切割线性肽后,在含有第一代grubbs催化剂的溶液中进行闭环复分解反应,如scott j.m.及其同事所公开(scott j.m.等人,“application of ring-closing metathesis to the synthesis of rigidified amino acids and peptides”,1996,j.am.chem.soc.,1996,118(40),第9606-9614页)。
[0237]
将去保护的肽用甲基叔丁基醚在4℃下沉淀并冻干。
[0238]
使用c18柱通过反相hplc纯化冻干肽(详情参见化合物表征)。通过lc-ms-esi对肽进行了鉴定。所有化合物的所有质谱数据在下表1中示出。
[0239]
hplc条件:
[0240]
idp-f05。使用30%-40%b的线性梯度,通过hplc-rp(c-18柱;泵a:含0,1%tfa的h2o;泵b:含0,1%tfa的乙腈)在20分钟内纯化所述化合物(r.t.=10,2)。通过hplc测定纯度级别为95,06%;
[0241]
idp-f13。使用32%-42%b的线性梯度,通过hplc-rp(c-18柱;泵a:含0,1%tfa的h2o;泵b:含0,1%tfa的乙腈)在20分钟内纯化所述化合物(r.t.=14,26)。通过hplc测定纯度级别为97,5%;
[0242]
idp-f16。使用35%-45%b的线性梯度,通过hplc-rp(c-18柱;泵a:含0,1%tfa的h2o;泵b:含0,1%tfa的乙腈)在20分钟内纯化所述化合物(r.t.=7,30)。通过hplc测定纯
度级别为95,7%;
[0243]
idp-f18。使用51%-61%b的线性梯度,通过hplc-rp(c-18柱;泵a:含0,1%tfa的h2o;泵b:含0,1%tfa的乙腈)在20分钟内纯化所述化合物(r.t.=10.97-11.97)。通过hplc测定纯度级别为95,6%;
[0244]
idp-f22。使用53%-63%b的线性梯度,通过hplc-rp(c-18柱;泵a:含0,1%tfa的h2o;泵b:含0,1%tfa的乙腈)在20分钟内纯化所述化合物(r.t.=10.1-11.36)。通过hplc测定纯度级别为97,06%;
[0245]
idp-f29。使用30%-40%b的线性梯度,通过hplc-rp(c-18柱;泵a:含0,1%tfa的h2o;泵b:含0,1%tfa的乙腈)在20分钟内纯化所述化合物(r.t.=8,91)。通过hplc测定纯度级别≤为50%;
[0246]
idp-f31。使用38%-48%b的线性梯度,通过hplc-rp(c-18柱;泵a:含0,1%tfa的h2o;泵b:含0,1%tfa的乙腈)在20分钟内纯化所述化合物(r.t.=10,65)。通过hplc测定纯度级别为95,49%。
[0247]
表1:质量表征
[0248]
[0249]
x双自由基代表下式的化合物:
[0250][0251]
并且对应于-(ch2)
3-ch=ch-(ch2)
3-或-(ch2)
6-ch=ch-(ch2)
3-的l双自由基连接每个序列中的两个xs基团。
[0252]
细胞系:
[0253]
sk-mel-28,皮肤,人恶性黑色素瘤,atcc-htb-72
tm
。
[0254]
igr-37,皮肤,人黑色素瘤来源于转移部位:腹股沟淋巴结。
[0255]
igr-39,皮肤,人黑色素瘤来源于转移部位:腹股沟淋巴结。
[0256]
b16-f10,皮肤,小鼠黑色素瘤,atcc-crl-6475
tm
。
[0257]
501-mel,皮肤,人恶性黑色素瘤。
[0258]
细胞培养
[0259]
将细胞系sk-mel-28、igr-37、igr-39、b16-f10、501-mel和a-375在培养箱中于37℃下在杜尔贝科改良的eagle培养基(invitrogen life technologies,加利福尼亚州福斯特市)中培养,所述培养基含有10%灭活胎牛血清(fbs,法国dutscher)、青霉素(50u/ml)和硫酸链霉素(50mg/ml)(gibco brl,德国)。在扩增步骤和测定过程中,用dpbs(杜尔贝科磷酸盐缓冲盐水,sigma d1283)冲洗贴壁细胞三次,然后用胰蛋白酶([0,5g/ml]/edta[0.2g/ml])(gibco-brl,15400054)在37℃的dpbs溶液中处理5分钟,并且一旦分离,就转移到培养基中。在用台盼蓝(tripan-blue)标记后,在neubauer室中对细胞进行计数。每次测定仅在存活率高于90%时进行。
[0260]
存活率测定
[0261]
将细胞系sk-mel-28、igr-37、b16-f10、501-mel和a-375以1,000个细胞/孔的密度接种在96孔板中。在24小时后,加入待测试的化合物,以用系列稀释法计算浓度为10μm时的功效。对照是未处理的细胞。一式三份地进行了每个实验。
[0262]
将细胞在培养箱中在37℃的co2气氛下孵育72小时。通过比色mtt(3-(4,5-二甲基噻唑-2-基)-2,5-二苯基溴化四唑)测定测量细胞存活率。将mtt再孵育4小时,然后丢弃培养基。加入dmso以溶解甲瓒产物,并且用酶标仪(multiskan,labsystems)测量570nm处的吸光度。通过用给定化合物处理的细胞的吸光度值除以未处理细胞的吸光度来计算细胞存活率百分比。
[0263]
统计学
[0264]
进行数据分析,计算归一化的细胞存活率相比于阴性对照值(其被认为等于100%)的百分比。剂量/反应曲线通过sigmoidal方程剂量-反应(可变斜率)拟合,并且如下计算ec
50
值:
[0265]
y=底部+(顶部-底部)/(1+10^{[(logec50-x)*hillslope]},
[0266]
其中:x是化合物浓度(对数标度)并且y是反应。
[0267]
计算和图表是使用graphpad棱镜(用于窗口的棱镜6)进行的。
[0268]
2.结果
[0269]
2.1功效结果
[0270]
表2a、2b和2c提供了在10um下几种黑色素瘤细胞系的抗增殖活性。
[0271]
表2a
[0272][0273][0274]
表2b
[0275]
化合物igr-37f1340f1650f1860f2280f3130
[0276]
表2c
[0277]
化合物b16-f10f0560f1840f2240f3150
[0278]
本发明的所有肽对测试的黑色素瘤细胞系(即便是侵袭性表型)均显示出显著的抗癌活性。
[0279]
2.2 b16-f10黑色素瘤细胞中黑色素含量的测量
[0280]
将b16-f10黑色素瘤细胞接种到25cm2细胞培养瓶中并孵育24小时。然后,加入0.1μmα-msh,并且用上述肽以低于其各自ic50的剂量处理细胞,总共孵育48小时。在用磷酸盐缓冲盐水洗涤两次后,将细胞溶解在1ml的1n naoh中。为了测量黑色素含量,然后将100μl等分溶液置于96孔板中,并使用酶标仪在450nm处测量吸光度。用黑色素占未治疗黑色素瘤细胞的百分比来表示抗黑色素活性。作为阳性对照,使用不同浓度(0.1、1和10μm)的曲酸(ka)。
[0281]
结果汇总于图1中。可以看出,本发明的肽参与黑素生成途径。因此,所述肽中的一些刺激黑色素的产生,这可能是黑素细胞活化的标志,而其他肽(诸如f22和f29)则大大减少了黑色素的量。更值得注意的是,当与其他化合物相比时,本发明的肽在调节黑素细胞方面更有效。在这点上,发现当ka以1um的浓度使用时,减少量显著低于当本发明的肽f22以相同浓度使用时所实现的减少量。
[0282]
因此,该数据不仅支持本发明的肽对黑素细胞活性的作用,而且说明它们甚至比现有技术中用于相同目的的其他化合物更有效。
[0283]
2.3斑马鱼胚胎中脱色素活性的测定。
[0284]
在斑马鱼的发育过程中,色素形成由视网膜色素上皮(rpe)在约24hpf下开始,然后向背外侧皮肤发展,黑素细胞分布在背外侧皮肤。在未处理的胚胎中进行生化黑色素定量,以与用化合物f22处理的胚胎进行比较。将f22溶解在1x pbs中,以形成储备溶液。为了进行斑马鱼胚胎药物孵育,在e3培养基中连续稀释f22以获得:最终体积为1ml的2.5μm。
[0285]
黑色素定量测定
[0286]
每一式三份收集50个胚胎,并在95℃的裂解缓冲液中溶解30分钟。将200μl溶液置于96孔板中,并且使用光谱仪在490nm处定量总的黑色素含量。将结果与合成黑色素进行比较。通过绘制每个黑色素标准品的平均空白校正的490nm测量值相比于其浓度(μg/ml)的标准曲线。将标准曲线用于测定每个未知样品的黑色素蛋白浓度。
[0287]
图像分析:
[0288]
将胚胎置于机器人微流体系统vast(union biometrica)中,所述系统允许在显微镜(leica,dm6-b)下自动抽吸、放置和旋转幼体。一旦胚胎被放置在直角下(背面视图),则通过vast机载相机获取图像。每个幼体获取一张背部图像。将fiji程序用于定量。将rgb图像转换为8位,并确定幼体的方向。应用固定阈值从图像生成二进制掩码。根据幼体的方向选择特定感兴趣区域roi。生成roi,使得眼睛被排除在定量之外。然后使用分析像素命令测量roi内的分割区域。色素沉着水平被提供为这些区域中所有像素的总和。
[0289]
结果:黑色素定量
[0290]
表1.通过生化分析进行黑色素定量。该表以百分比示出了孵育72小时时与阴性对照(e3培养基)相比的黑色素定量。星号表示单向anova后的统计显著性:*p《0.05;**p《0.01;***p《0.001。
[0291][0292]
表2.通过图像分析进行黑色素定量。黑色素含量计算为在96hpf下与每个斑马鱼幼体(e3培养基)的身体相关的像素的总和的平均值。星号表示单向anova后的统计显著性:*p《0.05;**p《0.01;***p《0.001。
[0293][0294]
从所使用的两个定量,可以得出结论,当分析生物化学黑色素量并与成像研究的分析相比较时,有证据表明2.5μm下的化合物f22具有脱色素效果。
[0295]
引用列表
[0296]
altschul等人,“basic local alignment search tool”,1990,j.mol.biol,v.215,pp 403-410;
[0297]
copolovici d.m.等人,“cell-penetrating peptides:design,synthesis,and applications”,2014,acs nano,2014,8(3),pp 1972-1994;
[0298]
higgins等人,“clustal v:improved software for multiple sequence alignment”,1992,cabios,8(2),pp 189-191;
[0299]
kim young-woo等人,“synthesis of all-hydrocarbon stapled a-helical peptides by ring-closing olefin metathesis”,nature protocols,2011,6(6),p.761-771;
[0300]
kolb h.c.等人,“the growing impact of click chemistry on drug discovery”,2003,drug discov today,8(24):1128-1137);以及
[0301]
scott j.m.等人,“application of ring-closing metathesis to the synthesis of rigidified amino acids and peptides”,1996,j.am.chem.soc.,1996,118(40),pp9606-9614。
[0302]
出于完整性的原因,本发明的各个方面在以下编号的条款中列出:
[0303]
条款
[0304]
1.一种肽或其药物或化妆品可接受的盐,所述肽具有相对于序列seq id no:1或2具有至少85%同一性的氨基酸序列:
[0305]
(trp)
m-(asn)
n-lys-gly-thr-ile-leu-lys-ala-ser-val-asp-tyr-ile-arg-lys-(leu)
p-(gln)qꢀꢀ
(seq id no:1)
[0306]
(arg)
mx-(arg)
nx-arg-arg-phe-asn-ile-asn-asp-arg-ile-lys-glu-leu-gly-thr-leu-(ile)
px-(pro)
qx
ꢀꢀ
(seq id no:2)
[0307]
其中
[0308]“m”、“n”、“p”和“q”代表整数,并且选自0和1;
[0309]“m
x”、“n
x”、“p
x”和“q
x”代表整数,并且选自0和1;
[0310]
c末端对应于-c(o)r4;
[0311]
n末端对应于-nhr5;
[0312]
r4是选自由-oh和-nr
17r18
组成的组的基团;
[0313]
r5是选自由以下组成的组的基团:-h、(c
1-c
20
)烷基和被选自由卤素、(c
1-c
10
)烷
n-、-sh-、-s-和-o-。
[0334]
2.根据条款1所述的肽,其相对于序列seq id no:1或2具有100%的同一性。
[0335]
3.根据前述条款中任一项所述的肽,其中式(i)的接头双自由基在位于序列seq id no:1的肽序列的位置
“ⅰ”
处的氨基酸的α碳原子和位于肽序列seq id no:1的位置
“ⅰ
+7”处的氨基酸的α碳原子之间;或者,可替代地,在位于序列seq id no:2的肽序列的位置
“ⅰ”
处的氨基酸的α碳原子和位于肽序列seq id no:2的位置
“ⅰ
+7”处的氨基酸的α碳原子之间。
[0336]
4.根据前述条款中任一项所述的肽,其中a=b=c=1。
[0337]
5.根据前述条款中任一项所述的肽,其中
[0338]
r1和r3是独立地选自由以下组成的组的双自由基:(c
1-c
10
)烷基;(c
2-c
10
)烯基;和(c
2-c
10
)炔基;
[0339]
r2是选自由以下组成的组的双自由基:(c
1-c
10
)烷基、(c
2-c
10
)烯基和(c
2-c
10
)炔基;并且
[0340]r19
是选自由以下组成的组的单自由基:(c
1-c
10
)烷基、(c
2-c
10
)烯基和(c
2-c
10
)炔基。
[0341]
6.根据前述条款中任一项所述的肽,其中r1、r3和r
19
是(c
1-c
10
)烷基;并且r2是(c
2-c
10
)烯基。
[0342]
7.根据前述条款中任一项所述的肽,其中所述c末端对应于-c(o)oh或-c(o)nh2,并且所述n末端对应于-nh2。
[0343]
8.根据前述条款中任一项所述的肽,其与肽序列seq id no:3至16至少85%、至少90%、至少95%或100%相同,其中“l”、“r19”、“m”、“n”、“p”、“q”、“mx”、“nx”、“px”和“qx”如前述条款中任一项所定义。
[0344]
9.根据前述条款中任一项所述的肽,其是具有与选自由seq id no:17至23组成的组的氨基酸序列至少85%、至少90%、至少95%或100%相同的氨基酸的肽。
[0345]
10.一种药物或化妆品组合物,其包含治疗或化妆品有效量的如条款1-9中任一项所定义的肽,以及可接受的药物或化妆品赋形剂和/或载体。
[0346]
11.如条款1-9中任一项所定义的肽或其化妆品盐或如条款10中所定义的化妆品组合物用于调节黑素生成,特别是用于减少或增加黑色素产生的非治疗用途。
[0347]
12.根据条款11所述的肽用于治疗色素沉着过度或色素沉着不足的非治疗性用途。
[0348]
13.如条款1-9中任一项所定义的肽或其药物盐,或如条款10所定义的药物组合物,用作药物。
[0349]
14.如条款1-9中任一项所定义的肽或其药物盐,或如条款10所定义的药物组合物,用于治疗和/或预防癌症,特别是黑色素瘤癌症,诸如转移性黑色素瘤癌症。
[0350]
15.如条款1-9中任一项所定义的肽或其药物盐,或如条款10所定义的药物组合物,用于治疗和/或预防与黑素生成失调相关的疾病,特别是通过抑制癌症黑素细胞增殖治疗和/或预防与黑素生成失调相关的疾病。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1