脐带血血浆制品、组织和细胞外泌体的分离方法,其组合物及使用方法
脐带血血浆制品、组织和细胞外泌体的分离方法,其组合物及使用方法
1.相关申请的交叉引用
2.本技术要求于2019年11月29日提交的美国临时专利申请号62/942,063的优先权,其全部内容通过引用并入本文。
发明领域
3.本发明整体上涉及从脐带血、外周血以及其他生物液体和组织中分离血小板、外泌体、纤维蛋白原、白蛋白、球蛋白、外泌体的方法,及其组合物和使用方法,包括用于培养哺乳动物细胞和治疗疾病和病症的药剂和方法。
4.发明背景
5.脐带血(ucb)是出生后留在胎盘中的婴儿血液。ucb在胎盘中产生,是除胎盘外最丰富的干细胞来源,比包括骨髓在内的任何成人组织都丰富。ucb血浆是ucb、胎盘和胎儿的细胞外液体,含有蛋白、脂质因子和携带胎盘、子宫、母体和婴儿之间的信号的外泌体。约5%的ucb采集自全世界每年超过3000万的新生儿。大多数ucb存有包括干细胞在内的单核细胞。
6.ucb血浆含有血小板、生长因子(vegf、g-csf、egf和fgf)、促炎细胞因子(il-2、il-6、ifn-γ、tnf-α)和其他促进人细胞存活和生长的因子(ehrhart,et al.,2018)。ev是细胞释放到细胞外环境中的细胞质囊泡。血小板是没有细胞核的小细胞(2-3μm)。由称为巨核细胞的细胞产生的血小板含有被包装成颗粒的生长因子和细胞因子。当被激活时,血小板会释放这些细胞因子和生长因子。人血小板长期以来一直用在培养人细胞的生长培养基中,以及用在治疗骨科和牙科问题和干眼综合征中。
7.细胞培养基需要生长因子和细胞因子来支持和刺激细胞生长和分化。传统上,细胞在获自妊娠奶牛的胎牛的胎牛血清(fbs)中生长。在fbs中生长的人细胞会摄取牛血清蛋白,而牛血清蛋白在细胞被移植到人体中时会引发免疫应答。由于广泛食用牛奶,许多人都具有对牛蛋白的抗体。在fbs中生长的细胞可能表达在被移植时激活免疫排斥的牛血清蛋白。出于这个原因,美国食品和药物管理局(fda)要求使用“无异源(xeno-free)”培养基来培养用于移植到人体中的细胞。
8.血小板是血液中的“第一反应者”。血小板可由骨髓干细胞产生。人生长培养基的最常用来源是人血小板裂解物。血小板裂解物还用于促进关节和牙齿的愈合,以及用于治疗疾病,例如影响全世界超过2亿人的干眼综合征。许多公司都出售用于细胞培养的人血小板裂解物(klatte-schulz et.al.,int jmol sci,2018.19(1))。大多数人血小板裂解物由成人血浆制备,所述成人血浆通过离心成人外周血以获得富血小板血浆(prp)、单核细胞(mnc)和红细胞部分(rcf)而收集。许多制造prp的团体和公司都将mnc和prp合并。大多数血小板最终在血浆层中,但具有粘性并可能被困在mnc层或rcf中。通常大多数从成人血液中采集血小板的设备都将mnc和prp合并,从而造成mnc浪费。冷冻的血小板显示出活化反应降低和信号传导受损(waters et.al.,transfusion,2017.57(12):p.2845-2857)。血小板裂
解物的标准尚未确定(astori,g.,et al.,stem cell res ther,2016.7(1):p.93)。
9.外泌体是直径为50-150nm的小的ev。外泌体产生自多囊泡体(multivesicular body,mvb)向内芽生形成的内体,并且具有靶向特定细胞的表面蛋白。mvb与细胞的外质膜融合,以将外泌体释放到细胞外空间。细胞通过外泌体相互发送信息。
10.ucb外泌体发挥对细胞显著的有益治疗和生长作用,以及对脑、心脏以及其他器官和组织的抗免疫、再生和其他作用。ucb外泌体是胎盘与发育中的胎儿交流的主要方式,并且可能含有刺激细胞生长和分化的转录因子、mrna和μrna。胎盘外泌体具有抗免疫作用,使细胞能够分泌和表达关闭免疫细胞的分子。
11.血浆还含有纤维蛋白原、凝血因子以及白蛋白和球蛋白(分别占血浆蛋白的50%和40%以上)。血浆纤维蛋白原和凝血因子可用于治疗患有纤维蛋白原血症和凝血功能障碍的患者,其与凝血酶组合时还可用作手术胶。白蛋白是细胞悬浮液的重要赋形剂。白蛋白是许多激素、细胞因子和药物的运载分子。球蛋白包括所有类型的免疫球蛋白(iga、igg、igm等)以及其他可作为信号传导分子的球蛋白。纤维蛋白原通常通过冷沉淀(cryoprecipitation)来分离,而白蛋白通常通过化学方法提取。
12.分离外泌体的传统方法效率低且劳动强度大,需要在蔗糖梯度中长时间(大于18小时)超速离心(大于100,000g)。与超速离心相关的离心力和蔗糖梯度的渗透力可能会破坏外泌体并将其内容物释放到细胞外液体中。其他分离外泌体的方法包括抗体包被的磁性微珠和用疏水成分提取。
13.因此,仍然需要更有效且高效的方法来从组织、血液、尿液、唾液、眼液和其他体液中分离血小板、外泌体、纤维蛋白原、白蛋白、球蛋白和ev,以使用这些组分提高培养基支持人和其他细胞生长和分化的能力以及用于治疗各种疾病。
技术实现要素:
14.本文描述了用于分级(fractionating)和分离(isolating)血小板、血小板和细胞外囊泡衍生(platelet-and extracellular vesicle-derived)的生长因子、外泌体、球蛋白、纤维蛋白原和白蛋白的新方法,以及使用分离的血小板、血小板和细胞外囊泡衍生的生长因子、外泌体、球蛋白、纤维蛋白原和白蛋白在受试者中再生组织,治疗受试者的纤维蛋白原血症或凝血缺陷,以及治疗受试者的干眼综合征、骨科疾病或牙科疾病的方法。本文所述的一些方法包括从富血小板血浆(platelet-rich-plasma,prp)分离和冷冻干燥血小板以获得去血小板血浆(platelet-depleted plasma,pdp),所述pdp是用于细胞培养的生长因子和外泌体的极好来源。这些方法包括从pdp中提取大于90%的外泌体,并从剩余的血浆分离和冷冻干燥白蛋白、球蛋白和凝血蛋白。本文还描述了激活pdp的方法。在下文所述的实验中,如本文所述的激活pdp的方法产生了含有1%pdp的细胞培养基,其刺激hela细胞生长的效果与10%胎牛血清(fbs)相当或优于10%胎牛血清(fbs)。本文还描述了用于培养哺乳动物(例如人)细胞的生长培养基。
15.本文还描述了从ucb制备pdp和使用浓缩的cacl2溶液激活ucb pdp以刺激细胞培养中细胞生长的方法。从ucb pdp提取外泌体的方法包括使用超声处理的聚乙二醇(peg)和外泌体的冷(例如4℃)提取。这些提取外泌体的方法是迄今为止从生物体液中提取外泌体的最有效的方法,可从小(1ml)至大体积(数升)的液体中回收超过90%的外泌体。本文描述
了ucb pdp和外泌体的新的临床和实验室用途,包括改善受精卵的植入以用于体外受精、治疗新生儿贫血、治疗脑缺氧-缺血、治疗干眼综合征以及许多其他用途。
16.因此,本文描述了一种从组织来源分离血小板和细胞外囊泡(extracellular vesicle,ev)的方法。所述方法包括:(i)提供血小板和ev的组织来源;(ii)以第一速度对组织来源进行离心,然后以高于第一速度的第二速度离心,以分离包含血浆、血小板和ev的富血小板血浆(prp)层;(iii)用包含直径为0.22μm的孔的微孔过滤器过滤prp层,以从prp层中分离血小板和直径大于220nm的颗粒,产生附着在微孔过滤器上的分离的血小板和基本上由直径小于约220nm的颗粒组成的血浆滤出物;(iv)在使生长因子从所述分离的血小板中释放出来的条件下,在容器中冷冻干燥所述微孔过滤器;和(v)处理血浆滤出物以分离直径小于约220nm的ev。在所述方法的多个实施方案中,步骤(v)中直径小于220μ的ev包括直径为50-150μ的外泌体。在所述方法的多个实施方案中,容器在步骤(iv)之后储存在-20℃或更低的温度下。所述方法可以进一步包括:(vi)将培养基添加到容器中以解冻和溶解生长因子,从而产生包含生长因子的生长溶液;和(vii)从容器中取出生长溶液。在所述方法的多个实施方案中,组织来源可以是例如ucb、脐带、脐带内衬层(umbilical cord lining)、脐带基质细胞(华通氏胶(wharton’s jelly))、羊水、羊膜、胎盘和外周血。在所述方法的实施方案中,微孔过滤器去除了直径大于220nm的颗粒。在所述方法的多个实施方案中,容器可以包括封闭系统。
17.本文还描述了培养哺乳动物细胞的方法。所述方法包括在包含本文所述方法制备的生长溶液的培养基中培养哺乳动物细胞群体。在多个实施方案中,哺乳动物细胞群体是人细胞。在多个实施方案中,组织来源是ucb。
18.本文进一步描述了包含本文所述方法制备的生长溶液的细胞培养基。
19.本文还进一步描述了一种生产去血小板血浆(pdp)的方法。所述方法包括:(i)获取和解冻ucb;(ii)离心ucb,产生富血小板血浆(prp)部分;(iii)将prp部分分离;和(iv)通过离心贫血小板血浆(platelet-poor-plasma,ppp)或过滤pdp和细胞碎片以及大于220nm的细胞外囊泡来去除血小板,产生含有柠檬酸磷酸右旋葡萄糖(citrate phosphate dextrose,cdp)、外泌体和血浆蛋白的pdp部分。在一些实施方案中,所述方法进一步包括通过将cacl2添加到pdp部分中以沉淀cpd来激活pdp部分。在一些实施方案中,添加6mcacl2。在一些实施方案中,添加5m cacl2以达到100mm的浓度以沉淀cpd。在一些实施方案中,添加不同量的cacl2以沉淀cpd。本文还描述了获得pdp部分和通过添加cacl2(例如,约5m或约6m cacl2以达到100mm浓度)以沉淀cpd来激活所述pdp部分的方法。
20.本文还描述了一种从组织来源分离外泌体、球蛋白、纤维蛋白原和白蛋白中的一种或多种的方法。所述方法包括:(i)提供外泌体、球蛋白、纤维蛋白原和白蛋白的组织来源;(ii)用包含直径为0.22μm的孔的微孔过滤器过滤组织来源,从而产生包含外泌体、球蛋白、纤维蛋白原、白蛋白和cpd的血浆滤出物;(iii)将血浆滤出物添加到第一离心管中的包含聚乙二醇(peg)的溶液中,使得外泌体分配到peg泡中;(iv)将第一离心管冷却至2℃至8℃;(v)将第一离心管离心,使得外泌体和peg形成第一沉淀物,并形成第一上清液,第一上清液包含白蛋白、球蛋白、cpd和纤维蛋白原;(vi)将第一上清液转移到第二离心管中,并冷冻包含外泌体和peg的第一沉淀物以进行储存,(vii)将沉淀剂与第一上清液混合以沉淀cpd;(viii)过滤沉淀剂和第一上清液的混合物以去除cpd,产生没有cpd的第二上清液;
(ix)将第二上清液冷却至2℃至8℃,以形成包含纤维蛋白原的冷沉淀物(cryoprecipitate);(x)在第三离心管中离心冷沉淀物,以形成第二沉淀物和第三上清液,(xii)去除包含白蛋白的第三上清液,并将包含纤维蛋白原的冷沉淀物冷冻干燥;和(xii)将含有白蛋白的第三上清液冷冻干燥。在所述方法的多个实施方案中,分离出组织来源的约80%至约95%的外泌体。在所述方法的多个实施方案中,分离出组织来源的约90%的外泌体。在所述方法的多个实施方案中,分离出外泌体、纤维蛋白原和白蛋白。在所述方法的多个实施方案中,在步骤(iv)中,在使血浆滤出物中的球蛋白交联纤维蛋白原、外泌体分配到peg中以及沉淀试剂沉淀cpd的条件下,将第一离心管冷却。在所述方法的多个实施方案中,在步骤(v)中,将第一离心管以每分钟约1000至约5000转(rpm)的速度离心约5分钟至约30分钟的时间。在所述方法的多个实施方案中,沉淀剂是cacl2。在所述方法的多个实施方案中,组织来源可以是例如ucb、脐带、脐带内衬层、脐带基质细胞(华通氏胶)、羊水、羊膜、胎盘和外周血。
21.本文进一步描述了一种产生富外泌体血浆(exosome-rich plasma,erp)的方法。所述方法包括将血浆或盐溶液(例如,pbs)添加到如本文所述的分离外泌体的方法获得的外泌体沉淀物中。
22.本文还进一步描述了一种培养哺乳动物细胞的方法。所述方法包括在包含通过本文所述的方法分离的外泌体和/或白蛋白的培养基中培养哺乳动物细胞群体。在多个实施方案中,哺乳动物细胞群体是人细胞。在多个实施方案中,组织来源是ucb。
23.本文还描述了一种细胞培养基,其包含通过本文所述的方法分离的外泌体和/或纤维蛋白原和/或白蛋白。本文描述了包含含有根据本文所述方法分离的外泌体或通过本文所述方法产生的激活的pdp的生长溶液的细胞培养基。
24.本文还描述了一种药物组合物,其包含通过本文所述的方法分离的血小板和ev,或通过本文所述的方法分离的外泌体、纤维蛋白原和/或白蛋白,通过本文所述的方法产生的pdp,或通过本文所述的方法产生的erp。
25.本文进一步描述了一种用于在受试者(例如,人受试者)中再生组织(例如,心血管组织、中枢神经系统组织、眼组织等)的方法。所述方法包括向受试者施用有效量的通过本文所述的方法分离的外泌体。在多个实施方案中,受试者是患有至少一种疾病例如组织损伤、脑退化、中枢神经系统退化和心血管退化的人。
26.本文还进一步描述了一种治疗受试者中的纤维蛋白原血症或凝血缺陷的方法。所述方法包括向患有纤维蛋白原血症或凝血缺陷的受试者施用有效量的通过本文所述的方法分离的纤维蛋白原。
27.本文还进一步描述了一种治疗受试者的干眼综合征、骨科疾病或牙科疾病的方法。所述方法包括向患有干眼综合征、骨科疾病或牙科疾病的受试者施用有效量的通过本文所述的方法分离的血小板,或通过本文所述的方法产生的pdp或erp。
28.本文还描述了一种培养哺乳动物细胞的方法。所述方法包括在包含含有根据本文所述的方法分离的外泌体或通过本文所述的方法产生的激活的pdp的生长溶液的培养基中培养哺乳动物细胞群体。
29.本文还描述了一种治疗受试者中的缺氧(hypoxia)、缺血(ischemia)或卒中(stroke)的方法。所述方法包括向患有缺氧、缺血或卒中的受试者施用根据本文所述的方
法分离的外泌体或通过本文所述的方法产生的pdp。
30.本文进一步描述了一种刺激有此需要的受试者(例如,女人)中的子宫血管形成的方法。所述方法包括向受试者的子宫腔施用通过本文所述的方法产生的pdp或通过本文所述的方法产生的erp。在多个实施方案中,可以向受试者施用包含pdp或erp的组合物。
31.为了帮助理解本公开的组合物和方法的详述,提供了一些明确的定义以促进本公开的多个方面的明确公开。除非另有定义,否则本文使用的所有技术和科学术语具有与本公开所属领域的普通技术人员通常理解的相同含义。
32.如在本说明书和所附权利要求中使用的,单数形式“a”、“an”和“the”包括复数,除非上下文另有明确规定。除非另有说明,否则术语“包括”、“包含”、“含有”或“具有”及其变体意在涵盖其后列出的项及其等同物以及另外的主题。
33.短语“在一个实施方案中”、“在各个实施方案中”、“在一些实施方案中”等重复使用。此类短语不一定是指相同的实施方案,但除非上下文另有说明,否则它们可以指相同的实施方案。
34.术语“和/或”或“/”意指与该术语相关联的项中的任一项、项的任何组合或所有项。
35.术语“约”可以指具体值的
±
5%、
±
10%、
±
20%或
±
25%的变化。例如,在一些实施方案中,“约50”%可以涵盖45%到55%的变化。对于整数范围,术语“约”可包括比所述整数大和/或小一个或两个整数。除非本文另有说明,否则术语“约”旨在包括接近所述范围的值(例如重量百分比),该值在单个成分、组合物或实施方案的功能方面是等效的。
36.如本文所用,当用于指代项的集合时,术语“每个”旨在说明集合中的单独项,但不一定是指集合中的每一项。如果明确公开或上下文另有明确规定,则可能会出现例外情况。
37.术语“去血小板血浆”和“pdp”意指已部分去除或完全去除血小板的血浆。术语“激活的pdp”和“apdp”意指已用钙离子处理以沉淀柠檬酸-磷酸-右旋葡萄糖(cpd)和其他化学物质(这些化学物质结合并降低钙离子浓度至足以阻止血液凝固的水平),从而使钙离子活性恢复至足以支持细胞生长的水平的去血小板血浆。
38.如本文所用,术语“红细胞部分”和“rcf”意指含有红细胞的离心外周血或脐带血的部分。
39.术语“富血小板血浆”和“prp”意指含有血小板的血浆。血浆应含有与正常血液或脐带血(ucb)一样多或比正常血液或脐带血(ucb)更多的血小板。
40.如本文所用,术语“erp”和“富外泌体血浆”意指含有浓度高于正常血液的外泌体的血浆。erp与prp的不同之处在于erp含有外泌体和很少或没有血小板,而prp含有血小板和外泌体两者。
41.如本文所用,术语“纯化的”是指从其他化合物或实体分开的化合物或实体(例如细胞)。所述化合物或实体(例如蛋白、肽、细胞)可以是部分纯化的、基本上纯化的或纯的。
42.当化合物或实体从基本上所有其他化合物或实体(即,优选至少约90%)中移出时,认为所述化合物或实体是纯的。
43.术语“分离的”和短语“生物上纯的”是指基本上或大体上不含在其天然状态下发现通常与之伴随的组分的物质。
44.术语“患者”、“受试者”和“个体”在本文中可互换使用,并且意指待治疗、诊断和/
或从中获得生物样品的哺乳动物(例如人)受试者。受试者可受累于例如贫血、缺氧-缺血、卒中、子宫内膜低下(hypo-endometria)、自身免疫病况(例如多发性硬化、系统性红斑狼疮、风湿性关节炎、银屑病关节炎)等。
45.如本文所用,术语“治疗剂”意在涵盖能够治愈、愈合、减轻、缓解、改变、补救、改善、改进或影响疾病、疾病的症状或对疾病的易感性的任何分子、细胞、化学实体、组合物、药物或生物剂。术语“治疗剂”包括多肽、肽、细胞、有机或无机分子、天然或合成化合物等。
46.如本文所用,术语“治疗”和“疗法”意指将治疗剂应用或施用至患者,或将治疗剂应用或施用至来自患者的分离的组织,所述患者具有疾病或病况、疾病或病况的症状或对疾病或病况的易感性,其目的在于治愈、愈合、减轻、缓解、改变、补救、改善、改进、消除或以其他方式影响疾病或病况、疾病或病况的症状或对疾病或病况的易感性。治疗包括药物组合物,其可以抑制、减少、降低或消除不良(例如身体)症状、病症、病、疾病或由疾病导致或与疾病相关的并发症,例如贫血、缺氧-缺血、卒中、干眼综合征、纤维蛋白原血症或凝血缺乏症、骨科疾病、牙科疾病、子宫内膜低下、多发性硬化、系统性红斑狼疮、风湿性关节炎、银屑病关节炎等。
47.短语“治疗有效量”和“有效剂量”意指足以产生治疗上(例如临床上)希望的结果的量;例如,所述结果可以是刺激血管形成和血流(例如,刺激子宫内膜生长),改善受试者(例如哺乳动物,包括人)从缺氧和/或缺血(例如,缺氧-缺血性脑病)中的神经恢复,抑制患有自身免疫病况的受试者的免疫系统,治疗受试者的纤维蛋白原血症或凝血缺陷,治疗受试者中的干眼综合征,治疗受试者中的骨科疾病,治疗受试者中的牙科疾病等。
48.如本文所用,“脊髓损伤”和“sci”是指由创伤(trauma,包括长时间压迫(大于20分钟)、挫伤(大于0.5m/秒)和局部切断或横断)以及非创伤性原因(如炎症、感染、水肿(肿胀)、毒素、由心脏骤停或主动脉动脉瘤导致的缺氧-缺血、椎管狭窄(变窄)、脱髓鞘和肿瘤浸润)引起的对脊髓的损害。脊髓压迫产生于椎间盘突出、骨移位、肿瘤生长和粘连导致的脊髓压陷。挫伤是以接近或超过0.5m/sec的速度对脊髓的快速压陷,导致组织快速移位以拉伸并破坏包括树突和轴突在内的细胞过程。局部切断或横断则是由于侵入脊髓的穿透性伤口。炎症可来自自身免疫炎性疾病,例如红斑狼疮、炎性细胞(白细胞)或感染性细胞(细菌、真菌、寄生虫、病毒)的侵入、脑膜感染(脑膜炎)、由于粘连或泄漏导致的脑脊液(csf)流动丧失。来自许多来源(包括细菌和真菌)的毒素均可损害脊髓。感染包括肺结核、狂犬病、病毒和真菌。脱髓鞘可能是由于毒素和自身免疫对少突神经胶质细胞的攻击。肿瘤浸润可发生于中枢神经系统的转移性肿瘤或内在肿瘤。当应用于脊髓损伤时,术语“急性”意指发生损伤或其他事件的早期阶段,而术语“慢性”意指损伤后持续的稳定状态。
49.如本文所用,脑和脊髓的“缺氧性缺血”意指脑的氧合作用和流向脑的血流减少。脑或脊髓缺氧和缺血的最常见原因是由夹层动脉瘤或创伤引起的颈动脉闭塞、心脏骤停、主动脉闭塞。在新生儿中,脐带在分娩过程中勒缢颈部以及在产道中长时间通过会导致缺氧性缺血。
50.如本文所用,“卒中”是指由脑内或通向脑的血管的闭塞、这些血管的出血或血管栓塞而导致的脑损害。例如,心脏骤停不会被认为“卒中”,而是心脏不再泵血导致的缺氧性缺血。卒中的发病率并不相同,在35-44岁的人群中为每年每100,000人中有30至120人,在65-70岁的人群中为每100,000人中有670至970人。在美国,每年有约800,000人患有首次卒
中或复发性卒中,并且有约3%(约700万)的成年人已经患过卒中(https://www.ncbi.nlm.nih.gov/pmc/articles/pmc3250269/)。全世界有超过8000万人患有与卒中相关的长期神经性障碍。
51.如本文所用,“黄斑变性”意指称为神经节细胞(ganglionic cell)的视网膜神经元的退行。最常见的类别是年龄相关性黄斑变性(amd),它是全世界范围内失明的主要原因,影响全世界超过2亿人。在美国,约有1100万人患有黄斑变性。黄斑变性的其他原因包括黄斑缺血,其包括与糖尿病相关的眼部病况和神经节细胞损失的其他原因。黄斑缺血的治疗包括预防黄斑变性、再生视神经或更换已经退行的视网膜神经节神经元。需要注意的是,其他治疗包括更换滋养视网膜视觉细胞的色素性视网膜上皮细胞。脐带血血浆和外泌体可刺激视网膜神经节生长。
52.如本文所用,术语“干眼综合征”和“des”意指眼液不能为眼睛提供足够或合适质量的润滑的病况。des与许多炎性病况有关,例如sjogren氏综合征、类风湿性关节炎和胶原血管疾病。大多数des治疗使用人工替代泪液、防止眼液流出的手术和抑制免疫应答的免疫抑制剂环孢菌素a。ucb的多种组分,包括脐带血外泌体和pdp,可能有益于des。
53.如本文所用,术语“子宫内膜萎缩”是指子宫中的子宫内膜层变薄。通常,子宫内膜为约1cm厚。然而,在大龄女性(大于35岁)、绝经后女性和患有卵巢功能障碍、长期口服避孕药和使用他莫昔芬的女性中,子宫内膜厚度小于5mm。在患有子宫内膜萎缩的女性中,体外受精和受精卵的植入常常遭受失败。脐带血外泌体含有包括血管内皮生长因子(vegf)在内的血管因子,其刺激血管生成和子宫内膜生长,以恢复子宫内膜厚度用以体外受精(ivf)。
54.以上概述不旨在定义本公开的每个方面,并且在其他部分中还描述了其他方面,例如以下详述。整个文件作为整体内容而相互关联,并且应该理解,本文所述的特征的所有组合均被考虑在内,即使特征的组合没有一起出现在本文的同一句子或段落或部分中。本发明的其他特征和优势将从以下详述中变得显而易见。然而,应该理解的是,详述和具体的实施例虽然显示了本公开的具体实施方案,但仅以示例的方式给出,因为在本公开的精神和范围内的各种变化和修改对于本详细描述所属领域的技术人员来说将是显而易见的。
55.附图详述
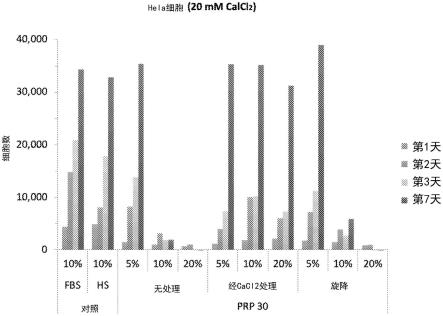
56.图1显示了在没有和有cacl2激活的情况下添加ucb富血小板血浆(prp)对hela细胞的影响。图左侧显示了10%胎牛血清(fbs)和10%成人人血清(hs)的影响。如果将prp应用于未经cacl2处理的培养基,则5%浓度下对细胞数的影响与10%fbs或10%hs相似。然而,10%或20%prp的更高浓度抑制了细胞生长。在用cacl2处理后,添加5%、10%和20%prp(样品prp 30)在7天时具有与10%fbs或10%hs相似的生长效果。向prp添加cacl2导致血小板沉淀。在最左,在对经cacl2处理的prp进行离心(旋转沉降)以使沉淀物沉降后,细胞的生长恢复到没有cacl2处理时所见的效果。该数据显示了向培养基中添加1%prp时显著加强(十倍)的生长刺激作用,这种生长效果与10%fbs或10%hs相等。然而,观察到10%和20%的更高浓度的prp对生长的刺激不如1%prp、10%fbs或10%hs,这表明prp含有抑制hela细胞生长的物质。这种物种很可能是柠檬酸-磷酸-右旋葡萄糖(cpd),其结合钙离子,将细胞外钙离子活性降低至低于细胞生长所需的水平。有趣的是,沉淀物(可能是cpd)的离心使生长效果恢复到添加cacl2之前的水平。cacl2的添加可能会激活血小板并从血小板中释放生长因子并有助于细胞生长。
57.图2显示了在prp和贫血小板血浆(ppp)中添加增加量的5m cacl2(范围从nt(未处理)到20mm、100mm、250mm和500mm钙浓度)后,prp和ppp中的柠檬酸盐浓度。为了评估添加20-100mm cacl2对血浆的柠檬酸盐浓度的影响,通过elisa测定柠檬酸盐水平(mm)。图的最左部分(29prp)显示nt具有约90mm柠檬酸盐。添加20mm cacl2可将柠檬酸盐降至70mm,添加100mm cacl2可将柠檬酸盐降至小于10mm。在另一样品(31prp)中,添加100mm cacl2将柠檬酸盐降低至20mm。在第三个ppp样品(62ppp)中,添加100mm cacl2导致没有柠檬酸盐。在第四个ppp样品(64ppp)中,添加100mm cacl2导致柠檬酸盐小于5mm。在第五个ppp样品(65ppp)中,添加100mm cacl2导致柠檬酸盐小于10mm。cpd-a1是置于采集袋中的柠檬酸-磷酸-右旋葡萄糖(citrate-phosphate-dextrose,cpd)溶液。
58.图3显示了不添加cacl2(nt),或添加足够的5m cacl2(20mm、50mm和100mm ca浓度的相当量),从prp和ppp沉淀cpd。利用20、50和100mm cacl2的相当量对两个prp(38prp、39prp)和两个ppp(61ppp、67ppp)样品进行处理。将cacl2增加至100mm会导致两个prp样品的柠檬酸盐水平小于5mm,2个ppp样品的柠檬酸盐水平小于10mm。cpda-1是含有柠檬酸-磷酸-右旋葡萄糖的阳性对照。
59.图4显示通过添加5m cacl2至100mm的相当量,含有1%至10%激活的去血小板血浆(activated platelet-depleted-plasma,apdp)的培养物中hela细胞的生长。s1是指在2017年10月采集然后在-20℃下冷冻保存至2020年8月的pdp。s2是指在2019年11月采集然后在-20℃下冷冻保存至2020年8月的pdp。将pdp解冻,并通过添加相当于100mm浓度的5m cacl2溶液来激活。fbs是阳性对照,0%fbs是阴性对照。细胞增殖表示为在1%、2.5%、5%和10%apdp中开始3000个细胞在初始培养后1、2、3和7天的细胞计数。
60.图5显示富血小板血浆(prp)和贫血小板血浆(ppp)的cacl2激活对hela细胞生长的影响。ppp是指离心去除血小板的血浆。prp在较低浓度(1-5%)使用时不需要激活,但10%prp则抑制生长。在存在血小板的情况下,即1%、2.5%和5.0%浓度下的prp会增加细胞计数,并且似乎只有10%prp受到抑制。当添加100mm cacl2时,会提高生长速率。在不存在血小板的情况下,即10%ppp在没有cacl2激活的情况下不会刺激那么多的细胞生长。
61.图6显示了在含有prp或pdp的培养基中生长的人脐带内衬层(hcl)间充质细胞的数量。pdp是通过用具有200nm孔的微孔过滤器进行过滤而制备的去血小板血浆。prp和pdp在刺激hcl间充质细胞增殖方面均不如10%fbs有效。与10%fbs相比,未经处理的prp对5%和10%prp浓度的影响延迟且较小。在100mm cacl2处理后,apdp仅在具有5%和10%apdp的培养基中改善了细胞生长。未经处理的pdp不能有效刺激细胞增殖,但经cacl2处理的pdp更有效。
62.图7显示了正常人真皮成纤维细胞(nhdf)生长。未经处理的ppp中等程度地支持生长,但经cacl2处理的pdp在5%和10%的ppp浓度下改善了生长,其中细胞生长超过10%fbs和商业的生长因子混合物(gf)。“脐带血浆”购自stem cell tech,并且其对细胞生长的作用有限。单独的fbs和gf都不如经cacl2处理的ppp。然而,fbs+gf可在7天时刺激生长至44,000个细胞。
63.图8是应用于ucb外泌体的外泌体常见标志物的斑点印迹分析的照片。阳性应答包括icam、anxas、tsg101、cd63、cd81、flot1。
64.图9显示pdp和外泌体对hela细胞培养的效果。右侧是pdp的效果:1%、2.5%、5%
和10%,获得自从2017年10月和2019年11月获得并在-20℃下冷冻保存的s1和s2脐带血血浆样品,然后用于促进hela细胞生长。即使在1%下,apdp也显著刺激了hela细胞生长。左侧,各种浓度的外泌体(从1.2x108个颗粒至1.2x10
10
)的应用刺激了hela细胞生长。单独的peg没有刺激太多生长。
65.发明详述
66.本公开描述了一种从ucb和外周血中分离富血小板血浆(prp)的方法。
67.本公开描述了一种从ucb和外周血中分离、激活并对其冷冻保存的方法。
68.本公开描述了从ucb产生去血小板血浆(pdp)和“激活”ucb pdp以刺激培养中细胞生长的方法。
69.本公开还描述了从ucb、其他生物液体(包括外周血、脑脊液(csf)和尿液)以及来自细胞培养的条件培养基中非常有效地分离外泌体的新方法。
70.本公开还描述了从ucb和外周血中分离球蛋白、白蛋白和纤维蛋白原的有效方法。
71.本公开还描述了使用冷冻干燥的血小板、pdp、外泌体培养哺乳动物(例如人)细胞的细胞培养基和方法。
72.本公开还描述了药物组合物,其包含通过本文所述的方法分离的血小板、外泌体、白蛋白和纤维蛋白原。
73.本公开还描述了用于在受试者中再生组织、用于治疗受试者的纤维蛋白原血症或凝血缺陷以及用于治疗受试者的干眼综合征、骨科疾病或牙科疾病的方法。
74.以下部分定义了与本文所述的方法、试剂盒和组合物相关的血浆组分。
75.ucb血浆组分
76.血浆是ucb和外周血的透明细胞外液体。血浆不同于血清,后者是凝结血液的上清液。为了制备血清,将血液凝结,这导致血细胞分解。当凝块被离心下来时,剩余的上清液是一种淡黄色的液体,含有细胞外液体和细胞内液体。相比之下,血浆是通过例如柠檬酸-磷酸-右旋葡萄糖(cpd)或肝素等化学物质阻止凝血的抗凝血液的上清液,并且仅含有细胞外内容物(包括抗凝剂),但不含凝结细胞的细胞内内容物。
77.根据血液的血细胞比容,ucb血浆的体积范围为血液体积的40-60%。当通过离心分开时,血浆中含有血小板。血小板相对较轻,并且在离心后往往与血浆分级,但由于血小板具有粘性,多达50%的血小板可能被困在rcf或mnc层中。如果分阶段进行离心,使得血液以相对低的速度(100x g)旋转并搅动混合物以将血小板从一层转移到下一层,以更高速度进行第二次离心可导致高达80%的血小板定位在血浆层。
78.血小板
79.具有高浓度血小板的血浆称为富血小板血浆(prp)。血小板的直径为2-3μm,其中充满了生长因子和细胞因子的颗粒,当血小板被激活时会释放这些颗粒。每毫升成人血液具有约200,000个血小板。ucb血小板计数是变化的,但应该接近于成人血液的血小板计数。血小板生成受血小板生成素调控。每个巨核细胞在其一生中产生约1000-3000个血小板。每天平均制造1000亿(10
11
)个血小板。血小板是损伤的“第一反应者”。组织损伤导致血小板粘附在血管上,激活并释放吸引干细胞和炎性/免疫细胞的因子。血小板裂解物用作细胞培物生长的生长因子的来源。
80.外泌体
81.外泌体由胎盘和ucb细胞,尤其是单核细胞、巨噬细胞和血小板释放。它们的直径为30nm到150nm。较大的ev通常含有来自细胞的废物。外泌体在细胞内的多囊泡体(mvb)内形成。外泌体携带“载货”,包括向子宫和胎儿发出信号的μrna和转录因子。细胞通过外泌体相互交流。外泌体与其他ev的不同之处在于其具有用于运输的内体分选复合物(endosomal sorting complexes for transport,escrt)或可溶性n-乙基马来酰亚胺敏感因子(n-ethylmaleimide sensitive factor,nsf)附着蛋白受体(snare)系统以停靠在细胞上。当外泌体停靠在这些受体上时,它们会将其内容物加载到细胞中。外泌体膜还含有胆固醇、鞘磷脂、神经酰胺和磷脂酰丝氨酸,这将它们与脂质体区分开来。外泌体可包含有益和有害因子,包括导致细胞凋亡的信号。
82.血浆蛋白
83.四类蛋白在脐带血浆中占主导地位。第一类是白蛋白,其占血浆蛋白的一半以上(55.2%,2.8-4.5g/dl),分子量为69kd。第二类是纤维蛋白原,其是形成凝块的纤维蛋白的前体蛋白。此外,血浆中含有凝血酶原,即可催化凝块的凝血酶的前体蛋白。第三类是球蛋白,即α-1球蛋白(5.3%,包括α1-抗胰蛋白酶、tbg、运皮质激素蛋白(transcortin)等)、α-2球蛋白(8.6%,包括肝球蛋白、seruloplasmin、α2-巨球蛋白等)、β球蛋白(13.4%,包括β1-转铁蛋白、β脂蛋白等)和γ-球蛋白(11.0%,包括抗体iga、igg和igm)。血清球蛋白的总浓度为约0.42g/dl。第四类是纤维蛋白原(6.5%),其是血液的凝血蛋白。纤维蛋白原的分子量为340kd,具有6条多肽链,可通过凝血酶和其他凝血纤维转化为纤维蛋白。
84.从血液中分离和冷冻保存血小板的方法
85.在分离血小板的多个实施方案中,第一阶段的离心速度应当是低速,产生约100g,持续10-20分钟。调整速度以达到将rcf与mnc分开所需的最小离心时间。rcf的红色清楚地将rcf和mnc通过mnc的“血沉棕黄层(buffy coat layer)”区分开来。将rcf从管的底部去除。剩余的mnc和prp有时称为白血(white blood,wb)。搅动使粘附mnc的血小板松动以进入prp。
86.在分离血小板的多个实施方案中,第二阶段的离心以更高的速度进行,产生500-1000x g,持续20-30分钟,以将mnc和prp分开。通过mnc的光散射可以将mnc和prp区分开来。从离心机顶部去除prp,以浓缩或分离血小板。为了浓缩血小板,将prp置于单独的离心管中并以高速进行离心以达到1000-3000g's,将血小板沉淀到管底部。去除上清液会在管底部留下更浓缩的血小板悬浮液。
87.过滤可用于从prp中分离血小板。如果样品在prp中具有细胞碎片、ev和外泌体,则可以分阶段进行过滤。使用1μm过滤器进行预过滤帮助清理混合物,然后使用具有0.22μ孔的微孔过滤器。另外,prp含有可直接通过具有0.22μ孔的微孔过滤器的混合物。除细菌和大多数病毒外,微孔过滤器将捕获所有血小板。血小板的直径为2-3μm,可通过所述过滤器。
88.在本文所述的方法中,术语“处理”意指将血浆滤出物添加到含有peg的溶液中以分离外泌体。这样的方法可以进一步包括以下步骤:将培养基添加到容器中以解冻和溶解生长因子,从而产生包含生长因子的生长溶液,以及从容器中取出生长溶液。然后可以将这种生长溶液用于在下文更详细描述的细胞培养基和方法中。
89.从组织来源中分离外泌体、球蛋白、纤维蛋白原和白蛋白中的一种或多种的方法包括:提供外泌体、球蛋白、纤维蛋白原和白蛋白的组织来源;用具有直径为0.22μm的孔的
微孔过滤器对组织来源进行过滤,从而产生包含外泌体、球蛋白、纤维蛋白原、白蛋白和cpd的血浆滤出物;将血浆滤出物添加到第一离心管中的包含peg(例如,超声处理的peg)的溶液中,使得外泌体分配到peg泡中;将第一离心管冷却至2℃至8℃(例如,约4℃);将第一离心管离心,使得外泌体和peg形成第一沉淀物,并形成第一上清液,第一上清液包含白蛋白、球蛋白、cpd和纤维蛋白原;将第一上清液转移到第二离心管中,并冷冻包含外泌体和peg的第一沉淀物以进行储存,将沉淀剂与第一上清液混合以沉淀cpd;过滤沉淀剂和第一上清液的混合物以去除cpd,从而产生没有cpd的第二上清液;将第二上清液冷却至2℃至8℃(例如,约4℃),以形成包含纤维蛋白原的冷沉淀物;在第三离心管中离心冷沉淀物,以形成第二沉淀物和第三上清液,去除包含白蛋白的第三上清液,并将包含纤维蛋白原的冷沉淀物冷冻干燥;和将含有白蛋白的第三上清液冷冻干燥。在该方法中,通过peg分离外泌体后,剩余的ppp用于分离白蛋白、纤维蛋白原、球蛋白和凝血因子。
90.在从组织来源分离外泌体、球蛋白、纤维蛋白原和白蛋白中的一种或多种的方法中,可以使用包含外泌体、球蛋白、纤维蛋白原和白蛋白中的一种或多种的任何合适的组织来源(例如,ucb)。在典型的方法中,将组织来源用具有直径为0.22μm的孔的微孔过滤器过滤(进行过滤)。在多个实施方案中可以使用可以从组织来源中分出直径大于约220nm的颗粒的任何合适的过滤器。在多个实施方案中,包含peg的溶液可以是10%peg的溶液。在一些实施方案中,使用经超声处理的peg。经超声处理的peg可以使用已知方法生产或商业获得。当将第一离心管离心以使外泌体和peg形成第一沉淀物并形成第一上清液时,离心速度通常为约3000g(通常为每分钟1000至约5000转(rpm))并且进行离心约20分钟(通常在5到30分钟的范围内)。在多个实施方案中,在该离心之后,第一上清液包含白蛋白、球蛋白、cpd和纤维蛋白原。在所述方法中,沉淀剂通常是cacl2,但可以使用任何合适的沉淀剂。分离外泌体、纤维蛋白原和白蛋白后,将它们各自储存在合适的条件下。
91.所公开的方法可用于从ucb中分离血小板、ev、外泌体、球蛋白、纤维蛋白原和白蛋白。脐带血是血小板、ev、外泌体、球蛋白、纤维蛋白原、白蛋白以及prp、pdp、apdp等的有吸引力的来源。
92.所公开的方法也可应用于从除ucb外的其他组织中分离血小板、ev、外泌体、球蛋白、纤维蛋白原和白蛋白。此类来源的非限制性实例包括外周血、脐带、脐带基质细胞(华通氏胶)、可包括羊膜细胞的羊水、胎盘、脐带内衬层、尿液和经血。
93.血浆制品由富血小板血浆(prp)生产,所述prp通过从单核细胞(mnc)和prp(也称为白血,white blood)分离出红细胞(rbc)或红细胞部分(rcf)而产生的。从ucb和成人血液中将红细胞(rbc)与mnc和prp(称为白血)分离开的标准方法是,将血液慢速离心以将rcf与wb分离,然后以较高速度离心以将mnc与prp分离。
94.以下实施例显示了用两种类型的离心机分离prp的方法:
95.1.可以将ucb在摆动支架中具有多个离心管的水平转子中离心。30分钟后,红细胞(rbc)将沉降在管底部以形成红细胞部分(rcf)。初始离心以低速进行,通常以900rpm(11cm转子半径)进行,产生约100x g,以将红细胞部分(rcf)与mnc和prp或wb中分离开。将rcf从管底部去除,并搅动剩余的mnc和prp以便任何粘在mnc层中的血小板能够流到血浆中。以2000-2500rpm(产生492-769x g)离心20-30分钟能分开mnc和prp层,它们可以被单独移开。
96.2.可以将ucb在旋转圆筒离心机中离心。红细胞(rbc)将对着圆筒内表面形成rcf
外层,mnc形成中层,prp形成圆筒最内侧中心区。圆筒中的上升活塞将旋转的混合物向上推,而中心管则收集细胞。旋转圆筒可以在旋转过程中反向以摇动细胞使附着的血小板脱壁,从而它们能够迁移到血浆中。prp第一个出来。可使用光散射传感器确定有核细胞何时出来并更换收集容器收集mnc。最后,可以很容易地根据rbc的红色血红蛋白颜色检测rcf。
97.在实践中,阶段之间进行摇动的连续两阶段离心法产生了具有小于5%血细胞比容的mnc和具有大于80%血小板的prp。将rfc和mnc分别冷冻保存。可以将prp高效且快速地分离成几种具有重要治疗作用的组分,尤其是冷冻干燥血小板(fdp)、去血小板血浆(pdp)、外泌体、富外泌体血浆(erp),以及血浆球蛋白、白蛋白和凝血蛋白。所述离心方法通过修改可用于将组织组分和其他生物液体分离成可加工的组分。
98.用具有0.22μm孔的微孔过滤器过滤prp将从prp以及大多数细菌和病毒中提取99%的血小板。产生的无菌滤出物称为去血小板血浆(pdp)。根据来源,组织溶液或prp可能需要离心或预过滤以避免堵塞微孔过滤器。尽管过滤长期以来一直被用于分离血小板(细胞和其他生物组分),但所描述的方法的新颖之处在于将血小板冷冻干燥(冻干)以将其颗粒分解为可溶性蛋白。
99.含有冷冻干燥的血小板粉末的过滤器可以储存在带盖的无菌微孔过滤器中,密封在塑料中,并在-20℃下储存多年。当需要刺激培养中的细胞生长时,可以注射培养基通过过滤器,这会溶解冷冻干燥的颗粒化学物质并将滤出物灭菌。每个过滤器上的血小板数量可以通过血小板浓度和所过滤的prp体积来估算。
100.由prp的微孔过滤产生的滤出物(filtrate)称为去血小板血浆(pdp)。在其他实施方案中,可以使用离心来分离血小板。在prp的高速离心(大于2500xg)下,血小板将形成沉淀物。由于离心可能无法沉淀所有血小板,因此离心的prp的上清液是贫血小板血浆(ppp),而不是pdp,如图5所示。将沉淀物冷冻干燥或储存在密封小瓶中。
101.使磷酸盐缓冲盐水或细胞培养基通过具有冷冻干燥的血小板的微孔过滤器将提取可溶性蛋白,包括生长因子和细胞因子。使用0.22μ微孔过滤器具有多个优势。第一,无菌微孔过滤器广泛可用且价格低廉。第二,0.22μ微孔过滤器将清除大部分细胞碎片并捕获大于0.22μm的ev。第三,冷冻干燥的具有血小板的微孔过滤器可以在-20℃或更低温度下储存而不会降解。最后,为了使用冷冻干燥的血小板,用户只需简单地注射室温培养基通过过滤器,溶解冷冻蛋白,并且滤出物是无菌的。
102.大多数商业微孔过滤器具有无菌外壳,其经设计而适应具有鲁尔锁(luer lock)的注射器。过滤器可以在其外壳中直接冷冻干燥,加盖,用塑料包裹膜真空密封,并在-20℃下储存。注射培养基通过过滤器会将冷冻干燥的生长因子和细胞因子直接溶解到培养基容器中。在其他实施方案中,冷冻干燥的过滤器可以放置在无菌小瓶内。将培养溶液注射在小瓶中以溶解过滤器物质,产生生长因子和细胞因子的储备溶液,后者然后被注射入培养基中。另一种方法是将过滤器从其外壳中取出并将过滤器放入小瓶中,然后将其真空密封以更有效地储存。
103.与通过冷冻和解冻血小板3-4次来裂解血小板的传统方法相比,冷冻干燥的血小板具有许多优势。血小板在接触胶原蛋白和血管性血友病(von willebrand)因子、凝血酶或带负电荷的表面(如玻璃)时会被激活。血小板具有蛋白酶激活受体(par),其可通过多种途径被激活(yun sh,et al.(2016).biomed.res.intl.9060143)。传统的冻融方法需要数
小时且耗能量大。最终产物是部分溶解的血小板的冷冻的或湿的浆体,其在冷冻储存中可能不会像冷冻干燥的物质那么持久。冷冻干燥的物质可以通过重量快速且简单地定量。
104.激活pdp以用作细胞培养的生长培养基
105.ucb含有高浓度的抗凝剂柠檬酸-磷酸-右旋葡萄糖(cpd)。柠檬酸盐和磷酸盐两者均结合钙离子,降低培养基中的钙离子活性并抑制细胞生长,而后者需要钙离子。当将ucb pdp或prp以高于5%(ml/分升)的浓度添加到培养基中时,cpd的量将降低细胞外钙浓度,而这足以抑制细胞生长。出于这个原因,必须先由pdp或prp沉淀钙离子,然后才能将其添加到培养基中以刺激细胞生长。
106.一些研究人员将氯化钙(cacl2)添加到pdp或prp中以沉淀cpd。这有时称为pdp或prp的“激活”。添加cacl2不仅会沉淀cpd,还会沉淀其他钙结合蛋白和血小板。必须向pdp或prp中添加惊人高的cacl2量以沉淀足够的cpd来“激活”pdp或prp以刺激细胞生长。为确定向pdp或prp添加的5m cacl2溶液的量,测定pdp或prp中的柠檬酸盐浓度(使用结合柠檬酸盐的抗体的elisa),同时添加20mm、50mm和100mm cacl2浓度的相当量。如图3所示,添加达到100mm的5m cacl2的量是降低柠檬酸盐浓度至接近零所必需的。
107.向prp添加cacl2使许多其他钙结合蛋白和分子以及血小板沉淀。出于这个原因,在添加cacl2之前应先过滤出血小板,并且在用于细胞培养基之前,应通过离心或过滤去除沉淀物。激活的pdp在刺激细胞生长方面非常有效,即使在培养基中浓度为1%或更低时也是如此。图1-5显示了不同apdp浓度对hela细胞培养的影响。激活的pdp还促进人脐带内衬层细胞(图6)和正常人真皮成纤维细胞(图7)的生长。
108.从去血小板血浆中分离和冷冻保存外泌体的方法
109.通过过滤产生的去血小板血浆(pdp)或通过离心产生的贫血小板血浆(ppp)含有外泌体和血浆蛋白,提供了从中提取外泌体的基础材料。从血浆和组织中分离外泌体的传统方法效率很低。这些方法分为两类:
110.1.超速离心。外泌体是含有mrna、μrna和核因子的膜包裹的细胞外囊泡。外泌体在其表面具有与靶细胞上的受体结合并将其内容物加载到细胞中的蛋白。由于外泌体具有与血浆相似的低密度,因此需要在高渗透溶液(蔗糖梯度)中以100,000x g超速离心24-48小时才能将外泌体与血浆分离。溶液的渗透压和离心力会破坏外泌体,从而减少可回收的未被破坏的外泌体的数量。
111.2.将外泌体分配到疏水环境中。表面蛋白结合水并增加外泌体在水性环境中的溶解度。如果从外泌体表面去除水,外泌体将优先分配到更疏水的环境中,例如聚乙二醇(peg)。peg部分溶于水、乙醇、乙腈、苯和二氯甲烷,但不溶于更疏水的环境,如乙醚或己烷。
112.用于外泌体的商业试剂盒使用peg,但收集的外泌体少于20%。在2016年,deregibus等人(deregibus,et al.,2016)使用鱼精蛋白来结合带负电荷的蛋白质并捕获更多的外泌体(genschmer,et al.,2019)。fujifilm1使用磁珠通过磷脂酰丝氨酸受体捕获外泌体(miyanishi,et al.,2007;nakai,et al.,2016)。
113.大多数商业试剂盒将制备10%peg溶液(10ml peg与90ml磷酸盐缓冲盐水)并使用涡旋装置混合。由于peg泡,溶液看起来是浑浊的。在这些试剂盒中,然后将具有外泌体的pdp添加到10%peg溶液中。通常,在室温下一个或两个小时后,10-20%的外泌体会分配到peg中。混合物将以2500xg离心,并且由于peg的分子量较高,具有外泌体的密度较高的peg
将在管底部形成沉淀物。去除上清液并将pbs或pdp添加到沉淀物中以获得富外泌体血浆(erp)。
114.本文描述的新方法在多个方面有所不同。例如,使用超声将peg破碎成具有大得多的表面-体积比的微泡,这大大增加了外泌体与泡之间的相互作用。例如,将50ml peg(10,000分子量)混合到50ml pbs中会产生50%的peg溶液。该溶液在光下是混浊的,因为peg是直径大于340nm的泡的形式。混合物的超声处理迅速澄清溶液,因为经超声处理的微泡直径小于340nm,因此不可见。
115.另一个实例是将溶液冷却至4℃并将溶液在冰箱中保存过夜。随着温度接近0℃,水倾向于离开外泌体表面以参与形成冰,从而降低外泌体在水相中的溶解度并增加外泌体移动到peg微泡中。在4℃下8小时后,大于90%的外泌体已分配到peg中。
116.另一个实例是将peg混合物以2500x g离心30分钟,去除上清液,然后将peg中的外泌体冷冻至-170℃。peg溶液用于汽车的防冻液,其防止可能破坏外泌体的冰形成。当外泌体的冷冻沉淀物(外泌体沉淀物)在室温下解冻时,添加pbs或pdp以产生合适外泌体浓度的富外泌体血浆(exosome-rich plasma)。
117.从去外泌体血浆中分离球蛋白、白蛋白/纤维蛋白原的方法
118.按普及度排列,去外泌体血浆(exosome depleted plasma,edp)主要含有白蛋白、球蛋白和纤维蛋白原。
119.i.白蛋白是脐带血和外周血中最普遍的蛋白,其占血浆蛋白的50%以上。生长因子、激素和细胞因子被白蛋白结合。
120.ii.球蛋白包括免疫球蛋白,例如iga、igg和igm,其经常用于治疗自身免疫疾病。许多球蛋白是信号传导分子。一些球蛋白是冷敏感的冷球蛋白(cryoglobulin),其结合并交联其他球蛋白。
121.iii.凝血蛋白纤维蛋白原可广泛地从外周血中获得,与成人纤维蛋白原应该没有太大区别,但它可以通过诱导凝块形成、将凝块离心而容易地移出。这可以通过添加凝血酶和钙来完成。
122.因为分离外泌体的第二步是将pdp冷却至4℃过夜并离心混合物以形成peg沉淀物,所以大部分球蛋白将被冷却至形成凝胶的程度。可以将球蛋白凝胶倒入小瓶中,然后将白蛋白-纤维蛋白原溶液移液到小瓶中,并冷冻干燥凝胶和白蛋白-纤维蛋白原两者。然后可以将含有外泌体的peg沉淀物(外泌体沉淀物)置于小瓶中并冷冻。
123.如果用户想要得到不含纤维蛋白原的白蛋白,这可以通过添加凝血酶溶液并诱导离心、将凝块离心下来并使用主要含有白蛋白的上清液来完成。pdp当然可以直接用作生长培养基,直接添加到培养基中,如fbs一样。也可以将外泌体、白蛋白和冷冻干燥的血小板单独或一起添加到培养基中。
124.在其他实施方案中,血浆球蛋白和白蛋白-纤维蛋白原的所有上述组分均可以用于研究和临床治疗。
125.使用ucb血浆组分来培养哺乳动物细胞的方法
126.培养哺乳动物细胞的方法的实施方案包括在包含根据上述方法制备的生长溶液的细胞培养基中培养哺乳动物细胞群体。生长溶液可以包含prp、pdp、冷冻干燥的血小板、外泌体和/或白蛋白和/或生长因子。在所述方法中,哺乳动物细胞通常是人细胞,且组织来
源通常是ucb。可以使用本文所述的方法和生长溶液来培养任何类型的哺乳动物细胞,作为非限制性实例包括hela细胞、间充质干细胞、正常真皮细胞、肝细胞和受精卵。
127.术语“培养”是指将细胞维持在它们可以增殖的条件下。例如,将细胞在具有一种ucb组分和额外的生长因子或细胞因子(即生长因子或细胞因子的混合物)的培养基中培养。培养和生长哺乳动物细胞的方法是本领域公知的。
128.根据本文所述的方法、细胞培养基和生长溶液,经cacl2处理的ucb pdp可用作培养用于移植的人细胞的培养基。用100mm cacl2相当量处理的ucb pdp是一种有效且安全的用于人细胞培养的生长佐剂。ucb比可能感染许多疾病的成人血清更无菌。这部分是由于母体-胎盘屏障在妊娠期间将许多母体感染排除在胎儿之外。将采集到的ucb单位(ucb unit)针对许多常见疾病进行检测,并且还将母亲的血液针对常见疾病的抗体进行检测。ucb pdp可能是使用于移植的细胞生长的最安全的人血浆来源。
129.在一些实施方案中,一些人原代细胞可能需要向本文所述的生长培养基添加添加剂。在这样的实施方案中,本文所述的ucb pdp生长溶液用作可添加额外因子的极好基础。这种方法为生长用于移植的人细胞提供了一种经济且高效的无异源生长培养基。对于在激活的pdp中生长不佳的细胞,添加血小板可能会有所帮助。对于某些细胞,例如ucb和骨髓细胞,某些生长因子、细胞因子和其他因子(例如锂——参见美国专利8,852,938,其通过引用并入本文)可能是有用的。
130.ucb与从牛获得的fbs相比具有几个主要优势,例如,作为细胞培养的生长因子来源。首先,由于“疯牛病”或牛海绵状脑病(bse)影响美洲、欧洲和非洲的牛,fbs变得越来越昂贵。目前经认证没有bse的fbs的仅有的来源是澳大利亚和新西兰。如果bse出现在这两个国家中的任何一个国家,全世界的fbs供应可能会受到严重削减。然而,ucb pdp是可用的,因为每年有超过3000万婴儿出生。脐带血单位的平均大小为80ml,且血浆体积为约40ml,或约12亿升ucb血浆,这对于满足细胞培养的需要是绰绰有余的。在印度,将奶牛视为圣物的占大多数人口的印度教群体憎恶将fbs用于细胞培养,因为这需要从妊娠奶牛收获700万头幼牛来获得它们的血清。在印度,每天有9千万个婴儿出生,这对于满足细胞培养行业对所有生长因子的需求是绰绰有余的。印度目前仅采集约5%的脐带血。如果在印度采集20%的脐带血或每天360万毫升血浆,这对于满足目前全世界所有细胞培养对fbs的需求是绰绰有余的。由于使用本文所述的方法将用1-5%的ucb pdp替代10%fbs,因此预估ucb pdp可以以$20/ml的价格替代fbs;fbs目前的费用为约$5/ml。
131.组合物和治疗方法
132.通过上述方法分离的血小板、外泌体、球蛋白、纤维蛋白原和白蛋白对许多情况都具有有益作用并且可以以许多方式应用。例如,外泌体促进了包括神经退行和自身免疫在内的组织损伤的修复。ucb球蛋白可作为静脉内免疫球蛋白治疗的替代品。纤维蛋白原和凝血因子用于治疗患有凝血缺陷的患者,并且可用作手术胶。白蛋白是用于运输细胞的有用赋形剂。
133.本公开还提供了药物组合物,包括通过上述方法分离的冷冻干燥的血小板、外泌体、纤维蛋白原和白蛋白。药物组合物可以包含用于将血小板、外泌体、纤维蛋白原和/或白蛋白递送至有此需要的受试者的合适媒介物。在一些实施方案中,组合物还可以包含冷冻保存剂和/或药学上可接受的载体。
134.因此,本公开提供了一种用于在受试者中再生组织的方法。所述方法包括向受试者施用有效量的通过本文所述的方法分离的外泌体。在所述方法中,受试者通常是患有至少一种以下疾病的人:组织损伤、脑退行(degeneration)、中枢神经系统损伤和退行以及心血管退行。
135.本公开还提供了一种治疗受试者中的纤维蛋白原血症或凝血缺陷的方法。所述方法包括向患有纤维蛋白原血症或凝血缺陷的受试者施用有效量的通过本文所述的方法分离的纤维蛋白原。
136.本公开进一步提供了一种治疗受试者的干眼综合征、骨科疾病或牙科疾病的方法。所述方法包括向患有干眼综合征、骨科疾病或牙科疾病的受试者施用有效量的通过本文的所述方法分离的血小板。
137.剂量和施用频率将取决于临床体征,由这些临床体征确认处于缓解期,其中至少一种或更优选多于一种本领域技术人员已知的急性期临床体征减少或不存在。更普遍地,剂量和频率将部分取决于预期用上述组合物进行治疗的疾病状况或病症的病理体征以及临床和亚临床症状的退减。本领域技术人员理解,剂量和施用方案可以根据施用的年龄、性别、身体状况以及缀合物的益处和在待治疗的患者或哺乳动物受试者中的副作用以及医生的判断进行调整。
138.如本文所用,术语“受试者”是指脊椎动物,并且在一些示例性方面,是指哺乳动物。此类哺乳动物包括但不限于啮齿目哺乳动物例如小鼠和大鼠,和兔形目哺乳动物例如兔,食肉目哺乳动物包括猫科(猫)和犬科(狗),偶蹄目哺乳动物包括牛科(奶牛)和猪科(猪),或奇蹄目哺乳动物包括马科(马),灵长目哺乳动物ceboids或simoids(猴),以及类人猿目哺乳动物(人类和猿)。在多个示例性方面,哺乳动物是小鼠。在更多示例性方面,哺乳动物是人。
139.如本文所用,术语“施用”是指通过多种途径递送外泌体、纤维蛋白原或血小板,所述途径包括但不限于经口、鼻内、眼内、静脉内、骨内、腹膜内、脊柱内、肌内、关节内、心室内、颅内、病灶内、气管内、鞘内、皮下、皮内、透皮或透粘膜施用。
140.如本文所用,术语“有效量”或“治疗有效量”是指导致特定疾病的至少一种症状或参数的可测量改善的量。上述血浆外泌体、血小板、细胞外囊泡、纤维蛋白原和凝血因子的治疗有效量可以通过本领域已知的方法确定。治疗疾病的有效量可以通过本领域普通技术人员已知的经验方法确定。施用给患者的确切量将根据疾病的状态和严重程度以及患者的身体状况而变化。任何症状或参数的可测量改善都可以由本领域技术人员确定或由患者向医师报告。应当理解,上述疾病的任何症状或参数的任何临床或统计学上的显著减弱或改善均在本发明的范围内。临床上的显著减弱或改善意指对于患者和/或医师是可感知的。
141.药物组合物可以通过将治疗有效量的外泌体、纤维蛋白原或血小板以及任选的其他活性剂/化合物与药学上可接受的载体混合来制备。载体是指与治疗剂一起施用的稀释剂、赋形剂或媒介物。载体可以具有不同的形式,这取决于施用途径。载体可以是无菌液体,例如水和油。水或水性溶液、盐溶液以及水性右旋葡萄糖和甘油溶液优选用作载体,尤其是对于可注射溶液。合适的药物载体描述在e.w.martin的“remington's pharmaceutical sciences”第18版中。例如,可以通过与常规药物赋形剂混合和制备方法来制备组合物。赋形剂可以与崩解剂、溶剂、成粒剂、保湿剂和粘合剂混合。
142.短语“药学上可接受的”是指当施用给人时在生理上可耐受并且通常不会产生不希望的反应的分子实体和此类组合物的其他成分。优选地,术语“药学上可接受的”意指由联邦或州政府的监管机构批准或列于美国药典或其他公认的药典中用于哺乳动物,更具体地用于人。药学上可接受的盐、酯、酰胺和前药是指在合理的医学判断范围内,适合与患者组织接触使用而没有过度毒性、刺激、过敏反应等,与合理的收益/风险比相称,并对其预期用途有效的那些盐(例如羧酸盐、氨基酸加成盐)、酯、酰胺和前药。
143.本文提供的任何和所有实例或示例性语言(例如,“例如”)的使用仅旨在更好地说明本发明并且不对本发明的范围构成限制,除非另有声明。说明书中的任何语言都不应被解释为表示任何未要求保护的要素对于本发明的实施是必不可少的。
144.本文所述的所有方法均以任何合适的顺序进行,除非本文另有说明或与上下文明显矛盾。关于所提供的任何方法,所述方法的步骤可以同时或顺序发生。当所述方法的步骤顺序发生时,这些步骤可以以任何顺序发生,除非另有说明。
145.在方法包括步骤的组合的情况下,除非本文另有说明,否则步骤的各种和每种组合或子组合均涵盖在本公开的范围内。
146.本文中引用的每个出版物、专利申请、专利和其他参考文献均以不与本公开内容不一致的程度通过引用整体并入。本文中公开的出版物仅因为其在本发明申请日之前公开而提供。本文中的任何内容都不应被解释为承认本发明无权因在先发明而早于此类出版物。此外,所提供的公开日期可能与实际公开日期不同,这可能需要单独确认。
147.应当理解,本文所述的实例和实施方案仅用于说明目的,并且鉴于其的各种修改或变化是本领域技术人员能想到到并且包括在本技术的精神和范畴以及所附权利要求的范围内。
148.ucb去血小板血浆和外泌体的使用
149.ucb血浆和外泌体与成人血液的血浆和外泌体在几个重要方面不同。ucb由胎盘产生,是胎盘、子宫和胎儿之间的主要交流方式,并通过血浆中的激素、细胞因子、趋化因子和外泌体传递信息。所以,ucb血浆含有成人血液所没有的因子。ucb还具有比成人血液更多且不同的干细胞和祖细胞,包括更高比例的单核细胞。单核细胞是巨噬细胞以及树突细胞的祖细胞。这些细胞分泌不同于成人血液的因子和外泌体。ucb血小板和血浆可替代fbs作为用于人间充质干细胞(msc)培养的生长培养基。已知ucb血浆含有非常高浓度的转化生长因子β-1(tgf-b1)、血管内皮生长因子(vegf)、血小板衍生的生长因子(pdgf-aaa、pdgf-bbb)和内皮生长因子(egf)以及趋化因子(rantes、gro、mcp-1、eotaxin、fractakline)和免疫因子(il-12p70、ifny、il-4、il-17a、il-10和il13)。这些因子中的许多被用在用于培养人msc细胞的特定培养基中。使用ucb血浆作为生长培养基的主要问题是脐带血中存在cpd。cpd是一种抗凝血剂,其结合并降低钙离子活性足以导致停止血液凝结。降低钙离子活性也会导致细胞生长停止。这就是为什么ucb血浆仅在采用足够的cacl2将钙恢复到细胞生长所需的水平时才能促进生长。在下文描述的实验中,添加20mm cacl2不足以结合和沉淀培养物中的cpd,而添加100mm cacl2的相当量将钙离子活性恢复至足以使细胞生长。这些结果表明,1%的“激活的”pdp刺激hela细胞生长的程度与10%fbs相同。
150.下文描述的实验中显示,一旦钙离子活性得到恢复,已知存在于血浆中的生长因子、趋化因子和免疫因子将刺激细胞生长。实验还表明,pdp中的外泌体有助于生长,因为将
每毫升1.2x10
11
个颗粒以10%的浓度添加到培养基中也刺激了细胞生长,尽管程度不如10%pdp。用100mm cacl2的相当量处理pdp会消除cdp的细胞生长抑制作用,并表明了pdp强烈刺激hela细胞生长。hela细胞需要生长因子才能生长,因为它们在仅有培养基的情况下不会生长。大多数实验室目前使用fbs作为生长培养基的来源来培养细胞。许多研究已表明,在fbs中生长的细胞表达牛蛋白并且会被免疫排斥。美国食品和药物管理局(fda)建议,旨在用于人的细胞不得在含有动物蛋白且尤其是fbs的培养基中生长或储存,因为超过一半的人因饮用奶而具有抗fbs的抗体。人生长因子的唯一来源是来自成人血液的裂解的血小板。本文所述的新方法纳入ucb pdp作为更好且更安全的来源。
151.ucb外泌体可在治疗中发挥主要有益作用的病况的一个实例是缺氧缺血性脑病(hie),这是一种影响约0.4%的婴儿的病况,由于脐带血缠绕在颈部、缓慢而长时间地通过产道或严重贫血而可能无法将氧气输送给婴儿。外泌体可以通过血脑屏障(bbb)并且可以静脉内给予(perets et al.nano lett.2019;19(6):3422-31;osorio-querejeta et al.,front mol neurosci.2018;11:434)。有几项临床试验(tsuji et al.sci rep.2020;10(1):4603)和动物研究已表明,在患有hie的新生儿中输注ucb可以改善hie的神经性恢复。ucb外泌体可在治疗中产生益处的病况的另一个实例是卒中。ucb外泌体可在治疗中产生益处的病况的第三个实例是子宫内膜不佳(hypo-endometria),即子宫内膜内衬层薄,这是受精卵不能植入小于0.5cm的薄内膜内衬层的女性的主要原因。由于ucb外泌体携带许多刺激血管形成和血流的信号,将ucb外泌体置于子宫腔内可以刺激内膜生长。这可以在从卵巢中取出卵子时完成。可以在植入前一周将浓缩的富外泌体血浆(erp)注入子宫腔。内膜内衬层可以通过超声容易地监测。可用ucb外泌体治疗的病况的第四个实例是自身免疫疾病。ucb外泌体含有许多抑制免疫系统的因子,因此注射根据本文所述方法分离的ucb外泌体可抑制自身免疫病况,例如多发性硬化、系统性红斑狼疮、风湿性关节炎、银屑病关节炎以及其他。静脉内注射ucb外泌体可以缓解急性自身免疫性攻击。
实施例
152.实施例1
153.i.血小板、ev、外泌体、白蛋白、纤维蛋白原、球蛋白和凝血因子的分离
154.从ucb prp中分离血小板、ev和外泌体的新方法的实施例包括:
155.(a)一种分离血小板和ev并形成冷冻干燥的血小板的方法。将prp用0.22μ过滤器过滤以捕获血小板和细胞外囊泡,将其冷冻干燥作为生长因子的来源。
156.(b)一种分离外泌体并沉淀抗凝血剂cpd的方法。为了分离外泌体,将去血小板血浆(pdp)添加到10%peg和100mm cac12溶液中。外泌体分配到peg中,而cac12将抗凝剂cpd沉淀。将溶液冷却至4℃并以3000g离心20分钟。
157.(c)一种分离白蛋白、纤维蛋白原、球蛋白和凝血因子的方法。将ppp冷却至4℃会激活血浆中对温度敏感的球蛋白,以结合和交联纤维蛋白原和纤维蛋白。纤维蛋白原和球蛋白以及其他凝血因子的冷沉淀物是凝胶样的。将含有白蛋白和其他血浆蛋白的上清液倒入单独的容器中进行冷冻干燥。将冷沉淀物吸入另一容器中进行冷冻干燥。将外泌体/peg沉淀物在-20℃下冷冻,peg保护外泌体免受冷冻损伤。
158.实施例2
159.ii.ucb冷冻干燥的血小板
160.在分离ucb prp的新方法中,首先使用例如syngen(thermogenesis)装置分阶段离心ucb,将ucb分成prp、mnc和rcf,以最大化血浆中的血小板浓度。用60ml注射器取出prp层,并用0.22μmillipore过滤器过滤以去除直径大于220nm的颗粒。将含有ev和血小板的millipore过滤器置于无菌容器中并冷冻干燥,以释放生长因子。容器可在-20℃下储存。
161.在该方法中,过滤和冷冻干燥血小板是新的。相比之下,大多数实验室和行业将prp离心以收集血小板,移出上清液,然后反复冻-融沉淀物以释放生长因子。过滤会收集含有生长因子的血小板和ev。在本文所述的方法中,冷冻干燥比多次冻-融更好地释放和浓缩生长因子。该过程需要对样品的操作较少,并且可以在完全封闭的系统中完成。为了解冻和溶解冷冻干燥的生长因子,将培养基注入容器中以溶解过滤器上的生长因子,然后将所得的生长溶液从容器中取出并置于细胞培养皿中。
162.实施例3
163.ucb血浆外泌体、纤维蛋白原和白蛋白
164.在从ucb prp分离血浆外泌体、纤维蛋白原和白蛋白的新方法中,将pdp添加到含有10%聚乙二醇(peg,10,000mw)和100mm cacl2溶液的离心管中并冷却至4℃。外泌体分配到peg中,而cacl2沉淀cpd,并且冷却激活了血浆中对冷敏感的球蛋白,其结合纤维蛋白原形成冷沉淀物。以3000g离心20分钟后,外泌体在管底部形成peg沉淀物,冷诱导的球蛋白凝胶,上清液含有白蛋白和其他血浆蛋白。倒出上清液后,吸出凝胶样冷沉淀物,并对其进行冷冻干燥以获得纤维蛋白原和凝血因子。外泌体沉淀物可在-20℃下冷冻,其中peg用作冷冻保存剂。
165.这种新方法使用peg和cacl2的组合来分离外泌体并在一个短(20分钟)且低速的离心步骤中沉淀cpd。所述新方法提供了以下优势:
166.i.该过程在一个步骤中沉淀cpd并分离外泌体。由于低速离心,一次可处理大量体积,即来自一个单位的60ml血浆。这比以120,000g重复旋转小体积的血浆18小时要高效得多。
167.ii.peg将防止外泌体结晶并冷冻保存(cryopreserve)外泌体。
168.iii.所述过程分离纤维蛋白原和白蛋白以进行冷冻干燥。
169.实施例4
170.从ucb和pdp中分离外泌体
171.离心ucb分离出ucb的三个主要组分:prp、单核细胞(mnc)和rcf。将prp从ucb中分出,并用0.22μm微孔过滤器过滤以去除血小板,产生pdp。过滤器将去除直径大于220nm的血小板和细胞外囊泡。外泌体得到保留。在生产pdp的方法的一个实施方案中,将ucb解冻,将ucb离心以产生prp部分,将prp部分分离,并通过离心ppp或过滤pdp和细胞碎片以及大于220nm的细胞外囊泡来去除血小板,产生包含cdp、外泌体和血浆蛋白的pdp部分。
172.根据prp中的血小板浓度,可以使用0.22μm过滤器进行过滤,离心prp以获得血小板的沉淀物,并使用1.0μ过滤器过滤以去除血小板,然后使用0.22μm过滤器过滤以去除直径大于220nm的细胞外囊泡。将经离心沉淀的血小板或过滤后的血小板冷冻干燥(冻干),使得血小板中的所有生长因子均被冷冻并可溶解到培养基中。
173.将脐带血用降低细胞培养基中细胞外钙活性的cpd进行抗凝。cpd通过结合钙离子
并将细胞外钙离子活性降至低于凝血所需水平来防止凝血。钙离子活性的降低足以阻止培养物中细胞的生长。为了将cpd降至不阻止细胞生长的水平,将20mm cacl2添加到prp中。cacl2将结合cpd。结果如图1所示。
174.向prp添加20mm cacl2对hela细胞生长具有复杂的影响。在图1中左侧图,10%fbs和10%人血清(hs)在铺板后第1、2、4和7天导致细胞快速生长。当添加了ucb prp时,5%prp浓度的效果被延迟,但在7天时达到相同水平。然而,10-20%浓度的prp抑制了细胞的生长。这解释为意味着5%prp刺激培养中hela细胞的生长的效果如10%fbs或10%hs一样,但10-20%prp的更高浓度则抑制生长,因为它们添加的cpd足以降低细胞外钙从而阻止了细胞生长。
175.将20mm cacl2添加至prp恢复了10mm和20mm prp下的细胞生长。然而,当将经cacl2处理的prp离心下来(旋降)时,在10%和20%prp浓度下的生长抑制得到回复。这可能是由于cpd结合了钙离子并降低了细胞外钙活性,从而抑制了细胞生长。添加20mm cacl2阻止了这种抑制,但它显然还不够,因为对经cacl2处理的prp进行离心并去除沉淀物恢复了10-20%prp的生长抑制(图1最右部分)。
176.未经处理和经cacl2处理的pdp和prp对培养物中细胞生长的影响:
177.向prp添加20mm cacl2的复杂影响和发现旋降沉淀物恢复了10-20%经cacl2处理的prp的生长抑制(图1最右部分),这表明,20mm并没有消除所有cpd。为了确定cpd是否已被消除,不能使用钙特异性离子选择性电极来测定细胞外钙,因为cpd会干扰钙离子活性测定。相反,使用酶联免疫吸附测定(elisa)来测定柠檬酸盐浓度。添加增加量的cacl2以将cacl2的浓度增加至20、100、250和500mm,这将显示哪个cacl2添加量将柠檬酸盐水平降至接近零。图2显示了这些结果。
178.prp和pdp的cacl2激活:
179.图2中显示的实验结果表明,添加cacl2以将血浆中的ca浓度升至100mm的相当量将使prp中的柠檬酸盐降至低水平,并使ppp中的柠檬酸盐降至接近零的水平。ppp是指经离心以沉淀血小板并去除上清液的血小板,其中可能还有一些血小板残留。pdp是指消除了所有血小板的经过滤血浆。尽管添加了100mm的的相当量的柠檬酸盐后血浆中可能仍存在一些柠檬酸盐,但柠檬酸盐的量不足以将ca离子浓度降至足够阻止细胞生长。为了使添加到溶液中的体积最小化,使用最高浓度的cacl2(5m)以向血浆中添加钙。
180.请注意,仅当pdp用于为细胞培养提供生长培养基时,才需要添加cacl2来沉淀prp或ppp中的cpd。如果将pdp静脉内注射到人体内,则体液中钙的量对于中和cpd是绰绰有余的。请注意,即使当添加500mm的相当量的cacl2时,它也没有消除所有的柠檬酸盐,这表明所述测定没有准确地测定零柠檬酸盐。为了确认,重复所述实验以在添加足够的cacl2以达到20、50和100mm后测定柠檬酸盐,如图3所示。
181.数据表明,添加100mm的相当量的cacl2足以将prp样品(38prp和39prp)中的柠檬酸盐水平降至低水平。然而,在ppp样品(61ppp和67ppp)中,添加足够的cacl2达到100mm浓度时将柠檬酸盐降至小于10mm。在未接受处理(nt)的血浆中,prp中的柠檬酸盐浓度似乎接近60mm,但ppp中的柠檬酸盐浓度接近40mm,这表明prp中可能存在一些背景柠檬酸盐活性。
182.cacl2的分子量是110.98克,100mm cacl2是11.098克/升,5m cacl2是554.9克/升。例如,如果有100ml血浆,那么将向98ml血浆中添加1.1098克cacl2或约2.0ml的5m cacl2。大
多数脐带血袋具有cpd,但有些具有cpd加0.25mm腺嘌呤(cpda),其可延长红细胞寿命。
183.常规300ml脐带血采集单位具有27ml cpd溶液(gibson et al.bibl haematol.1968;29:758-63),其含有0.92g柠檬酸钠(二水合物)usp,0.89g右旋葡萄糖(一水合物)usp,114.5mg柠檬酸(一水合物)usp,87.9mg磷酸二氢钠(二水合物),usp。柠檬酸三钠二水合物的分子量为294.1g/摩尔,磷酸二氢钠(二水合物)的分子量为156.01g/摩尔,右旋葡萄糖一水合物的分子量为198.17g/摩尔。
184.经cacl2处理的pdp对hela细胞生长的影响:
185.hela细胞来源于人宫颈癌细胞系。这些细胞需要fbs才能生长。图4中最右图显示了第一天有3000个细胞,然后在第2、3和7天很少或没有细胞。在10%fbs的情况下,细胞在第一天生长至大于4000个细胞,在第二天生长至5000个细胞,在第3天生长至15,000个细胞,在第7天生长至18,000个细胞。
186.在2017年10月收集并在-20℃下储存3年直至2017年8月的1%浓度的s1 apdp,其刺激细胞增殖在开始时较慢,但在第7天即赶上。在2.5%和5%浓度时,2.5%和5%apdp在7天时优于10%fbs。在10%时,apdp在7天时不如10%fbs有效。
187.在1-5%浓度时,在2017年11月收集并储存约10个月的s2 apdp也刺激hela增殖,也具有应答延迟,并且在第7天的结果达到与10%fbs相似。数据显示了两个令人惊讶的发现:1%apdp有效刺激hela细胞生长,并且其与10%fbs一样有效,而无论细胞是在-20℃下冷冻储存3年还是2020年保存3年。
188.表1:在四个血浆样品中添加钙、ph和总蛋白(mg/ml)。prp是富血小板血浆,ppp是贫血小板血浆,通过离心制备。请注意,添加cacl2降低了脐带血的ph值。在所有样品中,添加cacl2都增加了总蛋白的重量(以mg/ml计)。
[0189][0190]
表1显示了在用cacl2处理之前和之后的prp和ppp样品中的血浆ph和总蛋白重量。处理前,ph值为正常(7.4-7.6)。cacl2处理后,ph降至6.4,这可能导致培养物生长降低。参见图5,实验表明,在存在血小板的情况下,即1%、2.5%和5.0%浓度的prp使细胞计数增加,而似乎只有10%prp受到抑制。当添加100mm cacl2时,其提高了生长速率。在不存在血小板的情况下,即10%ppp在没有cacl2激活的情况下似乎表现不佳。
[0191]
用cacl2处理prp和ppp对人脐带内衬层细胞的影响:
[0192]
hcl细胞是具有多达10%的间充质干细胞的间充质细胞(cd105+)。低浓度(1%和2.5%)的未经处理的pdp将支持hcl生长。较高浓度(5%和10%)的未经处理的pdp没有效果(参见图6)。利用100mm cacl2的激活确实改善了细胞生长,尤其是在较高的5%和10%prp
浓度时。
[0193]
这些结果表明,pdp在10%浓度和100ml cacl2激活下对间充质干细胞生长具有最佳效果。生长效果不如10%fbs。约6%的脐带内衬层细胞是muse细胞,它们的细胞生长速率并不高。另一方面,10%浓度的经cacl2激活的ppp在7天时仅产生与10%fbs相比一半数量的细胞。
[0194]
cacl2激活改善了细胞生长,尤其是在较高剂量的ppp时。在1%和2.5%的浓度下,未经处理的prp优于未经处理的ppp,但在5%或10%浓度下则不然。间充质细胞的最佳人生长培养基是经cacl2激活的10%ppp。
[0195]
用cacl2处理prp和ppp对正常人真皮成纤维细胞的影响:
[0196]
成纤维细胞显然需要10%fbs和生长因子两者来实现最佳生长。10%fbs本身确实以明显的剂量-反应曲线刺激生长,但不如10%经cacl2激活的ppp。脐带血浆的商业来源(未经处理)无法大幅改善生长;尽管在较高脐带血浆浓度下减少细胞生长的模式表明存在cpd效应,但cacl2并未被用于激活脐带血浆。
[0197]
人真皮成纤维细胞在单独的10%fbs或单独的生长因子(gf)中生长不佳。然而,fbs+gf的组合在7天具有最佳结果,产生快速且最多的细胞生长(图7右侧)。与hela细胞不同,人真皮成纤维细胞需要更高浓度的ppp和被cacl2激活来刺激细胞生长。
[0198]
与经cacl2激活的ppp相比,fbs+gf能更早和更快地刺激细胞生长。到第3天,细胞数量是利用激活的ppp的培养物的两倍还多。然而,在7天时,经cacl2激活的ppp细胞计数正在赶上。生长因子立即刺激生长,而外泌体需要时间来刺激细胞产生生长因子。
[0199]
激活的ppp和pdf可能主要通过外泌体来刺激生长。外泌体需要时间来刺激培养的细胞产生它们自己的生长因子,因此生长曲线可能会滞后几天。如果在开始时使用冷冻干燥的血小板来补充细胞生长,则这种早期生长差异会得到最小化。
[0200]
验证经cacl2激活的ppp对细胞生长的研究:
[0201]
对经cacl2激活的pdp在多种细胞上进行了测试,包括hela细胞、hep细胞(人肝细胞)、nhdf细胞(正常人真皮成纤维细胞)和miha细胞(永生化人肝细胞系)。在1%和5%ppp中生长4天的hela细胞与在10%fbs和10%人血清(hs)中培养的细胞相比具有相似的细胞计数,这意味着1%和5%ppp与10%fbs和10%hs一样好。同样,在1%、2.5%和5%prp中生长7天的hela细胞具有与在10%fbs下相似的计数或超过在10%fbs下的计数。hep细胞在1%ppp中和在1%fbs中的生长一样好。nhdf在10%ppp中生长的细胞比在10%脐带血浆(商业)中多10倍。nhdf和miha在1%fbs中和在1%ppp中生长得一样好。
[0202]
实施例5
[0203]
新且有效的外泌体分离方法
[0204]
本文描述了通过添加peg(分子量10,000)从ucb pdp中分离外泌体的新且有效的方法。ucb血浆中的外泌体是可溶的,因为水分子与外泌体表面脂质膜上的蛋白结合。如果较少的水与外泌体结合,则外泌体在水中的溶解性较低,并且偏好在疏水性peg中。peg部分溶于水。当将peg添加到水或磷酸盐缓冲盐水中然后搅拌混合物时,peg形成泡。如果泡大于(直径大于)可见光的波长,则可以用肉眼看到peg泡并且溶液会变得混浊。但是,如果它们小于可见光的波长,则溶液对于肉眼来说是透明且清澈的。对peg溶液进行超声处理会产生直径小于380纳米的微泡。可见光谱是从380纳米至700纳米。经超声处理的溶液对于肉眼来
说变为透明。
[0205]
较低的温度降低了外泌体在水性溶液中的溶解性,并增加了外泌体对peg的偏好。在接近冰点的较低温度下(例如4℃),水分子从外泌体表面脱离转而开始形成冰。当这种情况发生时,外泌体将变得更不溶于水,并优先分配到peg泡中。在添加含外泌体的血浆之前对peg进行超声处理会将peg泡分解成直径小于380纳米的更小泡。这会澄清溶液,从而使浑浊消失。在4℃时,约50%的血浆外泌体在约1小时的时间内分配到peg微泡中。用于提取外泌体的经超声处理的peg溶液的最佳终浓度为约10%。如果随后将血浆和peg在4℃下保持过夜,则90-95%的外泌体分配到peg中。
[0206]
上述方法可以在每10ml ucb血浆中收集多达10
12
个外泌体大小的颗粒(30-150nm)。这是从10ml外周血血清中可收集到的10
10
个外泌体的100多倍,是从10ml细胞培养基中收集到的10
10
个外泌体的100多倍。这有几个影响。首先,10%peg对于从10ml脐带血浆中收集90-95%的10
12
个外泌体是绰绰有余的。其次,如果peg悬浮液未经过超声处理或保持在4℃,则少于20%的外泌体将分配到peg中。超声处理大大增加了peg微泡的表面积,使外泌体和peg微泡之间有更多的相互作用。在4℃时,外泌体的溶解性降低,因此更有可能移动到peg中。
[0207]
对血浆和经超声处理的peg溶液进行离心(2500x g)将在管底部形成peg沉淀,其含有大于90%的外泌体。如果使用更高分子量的peg,即10,000分子量,则peg比水重,并将在3000x g下离心30分钟后沉降到管底。通过使用10,000分子量的peg和过夜(例如,8小时)孵育血浆和peg溶液,实现了从ucb血浆中提取95%或更多的外泌体。尽管销售有用于分离外泌体的商业化peg试剂盒,但这些试剂盒通常从血液和血浆以及条件培养基中分离出仅20%的外泌体。本文所述的新方法不仅从ucb血浆中,而且还从培养基和成人外周血浆中分离出大于90%的外泌体。
[0208]
总之,分离外泌体的方法的一些实施方案包括在4℃下将经超声处理的10,000分子量peg(10%浓度)与pdp孵育过夜(8小时),以将大于90%的外泌体从血浆中提取至peg中。以3000x g离心30分钟会产生含有大于90%外泌体的peg沉淀物。由于peg是一种冷冻保存剂,因此可以将peg沉淀物直接在-80℃或-180℃下冷冻。
[0209]
用于从pdp中提取或分离外泌体的典型方案
[0210]
设备和试剂:
[0211]
超声仪(fisherbrand
tm 705型sonic dismembrator或等同物)
[0212]
具有吊桶式转子(swinging bucket rotor)的冷冻离心机
[0213]
peg(10kd,sigma目录号81280-1kg)
[0214]
0.22μm过滤系统(corning目录号430767或等同物)
[0215]
0.1μm过滤系统(nalgene目录号565-0010或等同物)
[0216]
50ml锥形管(bd falcon 352098或等同物)
[0217]
过滤通过0.1μm过滤器单元的盐水
[0218]
起始材料
[0219]
冷冻的人ucb pdp或新鲜的人ucb pdp
[0220]
过程
[0221]
a-peg储备溶液:
[0222]
·
在去离子水中制备50%(w/v)的peg
[0223]
·
将peg溶液在冰上超声处理1小时以获得均质的水性溶液(设置取决于体积和仪器推荐。)
[0224]
·
在4℃下以5,000x g离心20分钟
[0225]
·
用0.22μm过滤器单元过滤上清液并在室温下储存
[0226]
b-外泌体分离:
[0227]
1.在冰上或在4℃过夜解冻hucbpdp。
[0228]
2.用微孔(0.22μm)过滤器过滤pdp。
[0229]
3.将经过滤的pdp与适量的peg储备溶液混合至混合物中的终浓度(其具有10%的终peg浓度)。
[0230]
4.在4℃下孵育过夜(无需搅拌)
[0231]
5.在4℃下以3,000x g离心30分钟。
[0232]
6.吸出并保存上清液(去外泌体血浆(edp))。
[0233]
7.将外泌体沉淀物重悬于体积为pdp体积的1/10的盐水中,使用搅拌棒溶解沉淀物。
[0234]
8.分装并在-80℃下冷冻。
[0235]
生物液体每毫升含有数十亿个外泌体。根据所使用的方法,通过p/peg方法收集的血清中的颗粒数量的范围从2.5x109(25亿)至2.0x10
10
(200亿)不等。颗粒计数的范围从唾液中的6x10
10
(600亿)到来自人肝细胞培养的条件培养基中的2.5x109(25亿)。
[0236]
表2:用在磷酸盐缓冲盐水中的20%peg浓度的经超声处理的peg(分子量10,000)收集的颗粒计数、回收率和粒径分布。pdp=去血小板血浆。peg(2h)是指在离心前于4℃下孵育2小时,peg(8h)是指在4℃下孵育过夜8小时。d/10是粒径的最低10%,d/50是粒径的第50百分位数,d/90是颗粒直径的第90百分位数。回收率是peg(8h)计数的总计数除以pdp的总计数的比率。
[0237][0238]
用微孔过滤器过滤pdp以消除大的细胞外囊泡和碎片。pdp中的粒径分布在第10百分位数(d/10)较低,为90.6nm,在第90百分位数(d/90)较高,为171.0nm。一旦颗粒分配到peg中,在4℃下孵育2小时后,d/10下降至69.5nm,d/90下降至124.8nm。在4℃下孵育8小时后,d10为67.9nm,d90为135.8nm。计数表明,所收集的外泌体比已发表的报告多一个数量级。pdp的每毫升颗粒数为8.2x10
10
或820亿/ml。总计数为8200亿/10ml。与20%peg一起孵育,然后从peg沉淀物的样品中计数,浓度增加至8.0x10
11
/ml或8000亿/ml peg沉淀物。所述沉淀物含有pdp中48.7%的外泌体。孵育8小时后,颗粒数量几乎翻了一倍,表明外泌体的回收率为91%。
[0239]
微泡可以在限制可以分配到peg中的外泌体的大小方面发挥作用。直径超过150nm的细胞外囊泡。使用0.22μ过滤器进行过滤可以消除pdp中所有大于0.22μ的碎片,而d/90从
171.0下降至135.8nm,无需进一步过滤。微泡可排除因太大而无法适配的较大囊泡。peg微泡小于可见光的波长(350nm),因为超声处理清除了因peg泡导致的混浊。从10ml pdp收集的外泌体的总计数为7500亿个,这远远超过了deregibus,et al.2016(int j mol med.2016;38(5):1359-66)研究中的计数(在唾液中超过650亿)。我们对商业外泌体试剂盒的非正式研究表明,其中最好的试剂盒从pdp收集了20%的外泌体,而许多试剂盒可能收集了少于10%的外泌体。
[0240]
实施例6
[0241]
ucb外泌体中标志物的鉴定和外泌体对细胞生长的影响
[0242]
外泌体表达许多标志物。选择了一些更常见的外泌体标志物并进行“斑点印迹(dot blot)”以测定ucb pdp外泌体标志物(参见图8)。最显著的标志物是icam。第二显著的标志物是anxas。第四是cd81或tapa-1(抗增殖抗体的靶标)和四次跨膜蛋白(tetraspanin),第五是cd63,第六是flot1。
[0243]
ucb外泌体对细胞生长具有显著影响,如图9所示。如所示,ucb外泌体支持hela细胞的生长。外泌体进行彻底洗涤,并且不具有任何血浆蛋白。请注意,pdp已经具有外泌体,并且代表了血浆蛋白和外泌体的组合生长刺激作用。阴性对照是仅peg,并且这些培养物显示没有生长。阳性对照是1-10%pdp和10%fbs。这些数据表明,通过经超声处理的peg和冷提取收集的外泌体具有活性并且支持细胞生长。
[0244]
参考文献
[0245]
deregibus,m.c.,f.figliolini,s.d'antico,p.m.manzini,c.pasquino,m.de lena,c.tetta,m.f.brizzi and g.camussi,2016.charge-based precipitation of extracellular vesicles.int j mol med.38,1359-1366.38.
[0246]
ehrhart,j.,p.r.sanberg and s.garbuzova-davis,2018.plasma derived from human umbilical cord blood:potential cell-additive or cell-substitute therapeutic for neurodegenerative diseases.j cell mol med.22,6157-6166.22.
[0247]
genschmer,k.r.,d.w.russell,c.lal,t.szul,p.e.bratcher,b.d.noerager,m.abdul roda,x.xu,g.rezonzew,l.viera,b.s.dobosh,c.margaroli,t.h.abdalla,r.w.king,c.m.mcnicholas,j.m.wells,m.t.dransfield,r.tirouvanziam,a.gaggar and j.e.blalock,2019.activated pmn exosomes:pathogenic entities causing matrix destruction and disease in the lung.cell.176,113-126e15.176.
[0248]
miyanishi,m.,k.tada,m.koike,y.uchiyama,t.kitamura and s.nagata,2007.identification of tim4 as a phosphatidylserine receptor.nature.450,435-9.450.
[0249]
nakai,w.,t.yoshida,d.diez,y.miyatake,t.nishibu,n.imawaka,k.naruse,y.sadamura and r.hanayama,2016.a novel affinity-based method for the isolation of highly purified extracellular vesicles.sci rep.6,33935.6.
[0250]
缩写
[0251]
apdp
ꢀꢀꢀ
激活的pdp(通过向pdp添加cacl2)
[0252]
cacl2ꢀꢀ
氯化钙
[0253]
cpd
ꢀꢀꢀꢀ
柠檬酸-磷酸-右旋葡萄糖
[0254]
cpda1
ꢀꢀ
用于ucb抗凝的柠檬酸-磷酸-右旋葡萄糖溶液
[0255]
csf
ꢀꢀꢀꢀ
脑脊液
[0256]
des
ꢀꢀꢀꢀ
干眼综合征
[0257]
egf
ꢀꢀꢀꢀ
表皮生长因子
[0258]
erp
ꢀꢀꢀꢀ
富外泌体血浆
[0259]
ev
ꢀꢀꢀꢀꢀ
细胞外囊泡
[0260]
fbs
ꢀꢀꢀꢀ
胎牛血清
[0261]
fda
ꢀꢀꢀꢀ
食品和药物管理局(美国)
[0262]
fgf
ꢀꢀꢀꢀ
成纤维细胞生长因子
[0263]
g-csf
ꢀꢀ
粒细胞集落刺激因子
[0264]
hela
ꢀꢀꢀ
henrietta lack(来自此人的宫颈癌细胞系)
[0265]
hs
ꢀꢀꢀꢀꢀ
人血清(成人)
[0266]
ifn-γ 干扰素-γ
[0267]
il-2
ꢀꢀꢀ
白细胞介素-2,一种控制白细胞活性的细胞因子
[0268]
il-6
ꢀꢀꢀ
白细胞介素6(il-6),一种促炎细胞因子
[0269]
iga
ꢀꢀꢀꢀ
免疫球蛋白a
[0270]
igg
ꢀꢀꢀꢀ
免疫球蛋白g
[0271]
igm
ꢀꢀꢀꢀ
免疫球蛋白m
[0272]
ivf
ꢀꢀꢀꢀ
体外受精
[0273]
mm
ꢀꢀꢀꢀꢀ
毫摩尔(浓度)
[0274]
mrna
ꢀꢀꢀ
信使rna
[0275]
μrna
ꢀꢀ
microrna
[0276]
mnc
ꢀꢀꢀꢀ
单核细胞
[0277]
mvb
ꢀꢀꢀꢀ
多囊泡体
[0278]
nt
ꢀꢀꢀꢀꢀ
无处理(组)
[0279]
pdp
ꢀꢀꢀꢀ
去血小板血浆
[0280]
peg
ꢀꢀꢀꢀ
聚乙二醇
[0281]
ppp
ꢀꢀꢀꢀ
贫血小板血浆(经离心的prp的上清液)
[0282]
prp
ꢀꢀꢀꢀ
富血小板血浆
[0283]
rcf
ꢀꢀꢀꢀ
红细胞部分
[0284]
s1
ꢀꢀꢀꢀꢀ
在2017年10月收集的pdp样本1
[0285]
s2
ꢀꢀꢀꢀꢀ
在2019年11月收集的pdp样本2
[0286]
sci
ꢀꢀꢀꢀ
脊髓损伤
[0287]
tnf-α 肿瘤坏死因子-α
[0288]
ucb
ꢀꢀꢀꢀ
脐带血
[0289]
vegf
ꢀꢀꢀ
血管内皮生长因子
[0290]
其他实施方案
[0291]
本说明书中公开的所有特征均可以以任意组合进行组合。本说明书中公开的每个特征均可以被用于相同、等价或类似目的的另外的特征所替换。因此,除非另有明确说明,
否则所公开的每个特征仅是一些通用的等价或类似特征的实例。通过以上描述,本领域的技术人员能够容易地确定本发明的本质特征,并且在不脱离本发明精神和范围的情况下,能够对本发明进行各种变化和修改以使其适应各种用途和情况。因此,其他实施方案也在所附权利要求的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1