一类用于诱导软骨形成的化合物及其应用
1.本发明属于生物医药领域,具体涉及一类用于诱导软骨形成的化合物及其应用。
背景技术:
2.骨关节炎(oa)是一种关节软骨退化损伤,且伴有关节边缘和软骨下骨肥大的缓慢性的退行性病变。目前骨关节炎发病率仅次于冠心病,2015年在中国大陆地区患病人数已超过1.2亿人,且由于人口老龄化和预期寿命延长,这一数字呈不断增长的趋势,预计到2021年成为第四大致残原因(current rheumatology reports,2017,19(7):42)。此外,oa给人们带来沉重的社会负担,如在高收入国家oa治疗的医疗费用已经达到了国民生产总值的1.0~2.5%。目前临床上缺少安全有效的骨关节炎治疗方法,目前oa的疗法主要有口服非甾体抗炎药(nsaid)或选择性环加氧酶2(cox-2)抑制剂、关节内(ia)注射如皮质类固醇和透明质酸等药剂缓解疼痛,以及采用微骨折,关节置换,软骨镶嵌成形术等手术来治疗。但这些治疗方法都存在不同程度的不足,不能修复不可逆损伤的软骨,临床结果大多不理想。因此,需要发展新型的治疗手段来满足日益严峻的oa临床现状。
3.间充质干细胞(mscs)存在于成年人滑膜、骨髓和脂肪,以及新生儿脐带血中。mscs是多能干细胞,可以在体外进行分离和增殖,其可以分化成几种不同类型的细胞,也具有三系分化能力,通过分化过程,专门的细胞类型由专门程度较低的细胞类型形成,例如来自mscs的软骨细胞。mscs可分化成包括但不限于成骨细胞、软骨细胞和脂肪细胞;也可以通过诱导在体外分化成软骨细胞。cartistem由韩国medipost生产,2012年1月19日韩国fda批准,是目前全世界唯一通过国家级批准的干细胞治疗骨性关节炎的药物。该药物是从脐带血中分离出干细胞进行诱导培养,培养后注入到关节腔内,干细胞会在关节腔内分化为关节软骨,修复关节软骨损伤,从而从根本上治好骨性关节炎。上市以来,cartistem销售额呈指数级增长,证明了oa干细胞治疗市场前景广阔。
4.胶原蛋白是表皮的主要结构成分,胶原蛋白对于皮肤健康非常重要,且广泛地应用于皱纹和皮肤衰老的表皮治疗并且可以作为烧伤患者的愈合助剂。胶原蛋白一般在成纤维细胞中表达产生,表皮治疗或者愈合助剂所施用的一般为人和牛的胶原蛋白。
5.但干细胞移植治疗oa仍然存在一定的缺陷。由于oa属于异质性疾病,个体差异大,临床效果不稳定,同时,干细胞移植体内分化效果低,且干细胞直接移植存在致瘤性的风险。因此,开发一类药物,通过在体外将干细胞诱导分化为软骨前体细胞再进行移植,或者通过关节腔注射诱导骨髓间充质干细胞(bmscs)分化成软骨细胞,能够规避干细胞药物存在的问题。小分子药物相对于生物制剂,具有规避免疫排斥,稳定,低成本,且跨物种分险低等优势。因此开发一类诱导间充质干细胞成为软骨细胞而改善骨关节炎或关节损伤的相关疾病的药物,具有重要的意义。
6.wo2011/008773、wo2014/138687描述了一类肽组合物及其用于治疗或预防关节炎和关节损伤的用于诱导间充质细胞分化为软骨细胞的用途。此外wo2012/129562、wo2014/151953、wo2015/175487与wo2018/225009描述了不同小分子化合物、组合物和那些组合物
在改善关节炎和关节损伤并且诱导间充质细胞分化成软骨细胞中的用途。2012年science报道的化合物kartogenin是第一个机制明确能够诱导间充质干细胞成为软骨细胞的小分子药物,但由于其成药性较差,不具备开发成药物的潜力。其后续开发药物ka34已于2017年被fda批准进入临床i期研究。2019年诺华公司的研发日活动(r&d day)上,公布了其公司软骨修复候选药物lna043和lrx712已进入临床i期研究,rhh466已进入预临床研究阶段。总体而言,利用小分子诱导干细胞成软骨分化促进软骨修复治疗骨关节炎为oa这一难治性疾病的治疗带来了新的希望。
7.目前针对关节炎的药物主要用于炎症和疼痛的缓解,不能修复软骨损伤。日益发展的组织再生技术在软骨修复等方面取得了一定的进展,但临床研究表明,通过以上方法修复的软骨组织多为纤维状软骨组织,而不是满足力学要求的透明软骨组织。令人欣慰的是,研究报道通过药物诱导间充质干细胞成软骨分化所修复的软骨组织为透明软骨,在组织修复上更能够模拟人体正常软骨,从而达到从根本上修复关节软骨损伤的作用(advanced drug delivery reviews,2019,146:289-305)。但目前针对软骨修复的药物研发仍然稀少,对化合物结构多样性的探究与生物学机制的摸索并不充分。因此,设计合成新型高效的诱导mscs成软骨分化促软骨修复的小分子诱导剂对于oa治疗的基础研究与临床应用具有重大的研发空间和研究意义。且由于骨关节炎的发病率的持续上升,社会对于有效的骨关节再生的组合物和方法存在持续的需求,具有巨大的市场前景,需要研究者们开发出更多高效低毒并具有良好成药性的化合物。
技术实现要素:
8.为了解决现有技术存在的不足,本发明的目的是提供了一类用于治疗和/或改善和/或预防骨关节炎或关节损伤,或用于诱导间充质干细胞分化成软骨细胞的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物,及其在制备治疗和/或改善和/或预防哺乳动物的关节炎或关节软骨损伤药物中,和/或在制备诱导间充质干细胞分化为软骨细胞药物中的应用。
9.本发明提供了一类如下式(i)所示的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,其由下述结构(i)表示:
[0010][0011]
其中:
[0012]
m为0、1、2、3或4;优选地,为0、1;
[0013]
n为0、1、2、3或4;优选地,为0、1;
[0014]
j为0、1、2、3或4;优选地,为1、2;
[0015]
k为0、1、2、3、4或5;优选地,为0、1;
[0016]
x为氧、c
1-6
烷基、乙烯基、乙炔基、-nr3r
4-、-c(o)-、-nhc(o)-、-c(o)nh-、-nr3c(o)-、-c(o)nr
3-、-nhc(o)nh-、-nhs(o)nh-、-so2nh-、-nhso
2-、-n=n-等;优选地,为-c(o)nh-;
[0017]
(r1)k指a环上连接的k个取代基r1,各自独立地选自h、卤素、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
烷氧基、c
1-6
卤代烷基、c
1-6
烷基氰基、氰基、硝基、羧基、氨基、叠氮基、c
1-6
烷基羟基、or3、sr3、s(o)r3、so2r3、nr3r4、cor3、c(o)r3、co2r3、-nr3c(o)r4、-c(o)nr3r4、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基,c
1-6
烷基-环烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基等;优选地,为h、卤素、硝基、羧基、氨基、-nr3c(o)r4、-c(o)nr3r4。
[0018]
其中,所述杂环烷基选自含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基选自苯基,蒽基,萘基,菲基等;所述杂环芳基选自吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基等;优选地,为苯环;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;
[0019]
(r2)j指b环上连接的j个取代基r2,各自独立地选自h、卤素、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
烷氧基、c
1-6
卤代烷基、c
1-6
烷基氰基、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基,c
1-6
烷基-环烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基、氰基、硝基、羧基、氨基、sr3、s(o)r3、so2r3、n r3r4、cor3、c(o)r3、co2r3、c(o)r3、c(o)nr3r4、c
1-6
烷基氧基、(cr5r6)or3、(cr5r6)nr3r4、(cr5r6)(cr7r8)or3、y(cr5r6)(cr7r8)or3、y(cr5r6)(cr7r8)nr3r4、(cr5r6)c(o)r3、(cr5r6)c(o)or3、(cr5r6)c(o)nr3r4、y(cr5r6)c(o)r3、y(cr5r6)c(o)or3、y(cr5r6)c(o)nr3r4、y(cr5r6)(cr7r8)c(o)r3、y(cr5r6)(cr7r8)c(o)or3、y(cr5r6)(cr7r8)c(o)nr3r4、(cr5r6)nr3so2r3或c(=nor3)r3等;优选地,为芳基、c
1-6
烷基氧基。其中,所述杂环烷基包括含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基选自苯基,蒽基,萘基,菲基等;所述杂环芳基选自吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基等;优选地,为苯环、c
1-6
烷氧基、y(cr5r6)(cr7r8)or3;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;
[0020]
y为o或cr9r
10
;
[0021]
r3选自h、c
1-6
烷基、c
1-6
烷基nhc(o)r4、c
1-6
烷基c(o)nhr4、p(c2烷基氧基)c2烷基nhc(o)r4、p(c2烷基氧基)c2烷基c(o)nhr4等;优选地,为h、c
1-6
烷基c(o)nhr4;其中p为0、1、2、3、4;
[0022]
r4为h、c
1-6
烷基、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基,c
1-6
烷基-环烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基等;其中,所述杂环烷基选自含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基选自苯基,蒽基,萘基,菲基等;所述杂环芳基选自吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基等;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;
[0023]
r5、r6、r7、r8、r9和r
10
独立地选自h、卤素、c
1-6
烷基、oh、co2r3、nr3r4、c
1-6
烷基氧基等;优选地,为h;
[0024]
a、b环各自独立选自下列基团中的任意一个:c
3-8
环烷基、c
7-c
10
桥环、含一个或多个o、n、s原子的杂环烷基、芳基、含一个或多个o、n、s原子的五元或六元杂芳环、含一个或多个o、n、s原子的苯并杂环;其中,所述杂环烷基选自含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基选自苯基,蒽基,萘基,菲基;所述杂环芳基选自吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基;所述苯并杂环选自苯并吡唑基,苯并吡喃基,哒嗪基,苯并嘧啶基,苯并咪唑基,苯并噻唑基,苯并异噻唑基,苯并哌嗪基,吲哚基,喹啉基,吡嗪基,异喹啉基,苯并噁唑基,苯并异噁唑基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基。
[0025]
上述式(i)中,当b环为苯环时,其由下述结构(ii)表示:
[0026][0027]
其中:
[0028]
m为0、1、2、3或4;优选地,为0、1;
[0029]
n为0、1、2、3或4;优选地,为0、1;
[0030]
j为0、1、2、3或4;优选地,为1、2;
[0031]
k为0、1、2、3、4或5;优选地,为0、1;
[0032]
x为氧、c
1-6
烷基、乙烯基、乙炔基、-nr3r
4-、-c(o)-、-nhc(o)-、-c(o)nh-、-nr3c(o)-、-c(o)nr
3-、-nhc(o)nh-、-nhs(o)nh-、-so2nh-、-nhso
2-、-n=n-等;优选地,为-c(o)nh-;
[0033]
(r1)k指a环上连接的k个取代基r1,各自独立地为h、卤素、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
烷氧基、c
1-6
卤代烷基、c
1-6
烷基氰基、氰基、硝基、羧基、氨基、叠氮基、c
1-6
烷基羟基、or3、sr3、s(o)r3、so2r3、nr3r4、cor3、c(o)r3、co2r3、-nr3c(o)r4、-c(o)nr3r4、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基,c
1-6
烷基-环烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基等;优选地,为h、卤素、硝基、羧基、氨基、-nr3c(o)r4、-c(o)nr3r4。
[0034]
其中,所述杂环烷基包括含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基选自苯基,蒽基,萘基,菲基等;所述杂环芳基选自吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基等;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;
[0035]
(r2)j指苯环上连接的j个取代基r2,各自独立地选自h、卤素、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
烷氧基、c
1-6
卤代烷基、c
1-6
烷基氰基、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基,c
1-6
烷基-环烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基、氰基、硝基、羧基、氨基、sr3、s(o)r3、so2r3、n r3r4、cor3、c(o)r3、co2r3、c(o)r3、co2r3、c(o)nr3r4、c
1-6
烷基氧基、(cr5r6)or3、(cr5r6)nr3r4、(cr5r6)(cr7r8)
or3、y(cr5r6)(cr7r8)or3、y(cr5r6)(cr7r8)nr3r4、(cr5r6)c(o)r3、(cr5r6)c(o)or3、(cr5r6)c(o)nr3r4、y(cr5r6)c(o)r3、y(cr5r6)c(o)or3、y(cr5r6)c(o)nr3r4、y(cr5r6)(cr7r8)c(o)r3、y(cr5r6)(cr7r8)c(o)or3、y(cr5r6)(cr7r8)c(o)nr3r4、(cr5r6)nr3so2r3或c(=nor 3
)r3等;优选地,为苯环、c
1-6
烷氧基、y(cr5r6)(cr7r8)or3;其中,所述杂环烷基包括含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基选自苯基,蒽基,萘基,菲基等;所述杂环芳基选自吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基等;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;
[0036]
y为o或cr9r
10
;
[0037]
r3选自h、c
1-6
烷基、c
1-6
烷基nhc(o)r4、c
1-6
烷基c(o)nhr4、p(c2烷基氧基)c2烷基nhc(o)r4、p(c2烷基氧基)c2烷基c(o)nhr4等;优选地,为h、c
1-6
烷基c(o)nhr4;其中p为0、1、2、3、4;
[0038]
r4为h、c
1-6
烷基、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基,c
1-6
烷基-环烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基等;其中,所述杂环烷基包括含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基包括苯基,蒽基,萘基,菲基等;所述杂环芳基包括吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基等;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;
[0039]
r5、r6、r7、r8、r9和r
10
独立地选自h、卤素、c
1-6
烷基、oh、co2r3、nr3r4、c
1-6
烷基氧基等;优选地,为h;
[0040]
a环选自下列基团中的任意一个:c
3-8
环烷基、c
7-c
10
桥环、含一个或多个o、n、s原子的杂环烷基、芳基、含一个或多个o、n、s原子的五元或六元杂芳环、含一个或多个o、n、s原子的苯并杂环;其中,所述杂环烷基选自含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基选自苯基,蒽基,萘基,菲基;所述杂环芳基选自吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基;所述苯并杂环选自苯并吡唑基,苯并吡喃基,哒嗪基,苯并嘧啶基,苯并咪唑基,苯并噻唑基,苯并异噻唑基,苯并哌嗪基,吲哚基,喹啉基,吡嗪基,异喹啉基,苯并噁唑基,苯并异噁唑基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基。
[0041]
上述式(ii)中,当x为-c(o)nh-时,其由下述结构(iii)表示:
[0042][0043]
其中:
[0044]
m为0、1、2、3或4;优选地,为0、1;
[0045]
n为0、1、2、3或4;优选地,为0、1;
[0046]
j为0、1、2、3或4;优选地,为1、2;
[0047]
k为0、1、2、3、4或5;优选地,为0、1;
[0048]
(r1)k指a环上连接的k个取代基r1,各自独立地为h、卤素、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
烷氧基、c
1-6
卤代烷基、c
1-6
烷基氰基、氰基、硝基、羧基、氨基、叠氮基、c
1-6
烷基羟基、or3、sr3、s(o)r3、so2r3、nr3r4、cor3、c(o)r3、co2r3、-nr3c(o)r4、-c(o)nr3r4、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基,c
1-6
烷基-环烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基等;优选地,为h、卤素、硝基、羧基、氨基、-nr3c(o)r4、-c(o)nr3r4。
[0049]
其中,所述杂环烷基包括含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基选自苯基,蒽基,萘基,菲基等;所述杂环芳基选自吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基等;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;
[0050]
(r2)j指苯环上连接的j个取代基r2,各自独立地选自h、卤素、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
烷氧基、c
1-6
卤代烷基、c
1-6
烷基氰基、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基,c
1-6
烷基-环烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基、氰基、硝基、羧基、氨基、sr3、s(o)r3、so2r3、n r3r4、cor3、c(o)r3、co2r3、c(o)r3、co2r3、c(o)nr3r4、c
1-6
烷基氧基、(cr5r6)or3、(cr5r6)nr3r4、(cr5r6)(cr7r8)or3、y(cr5r6)(cr7r8)or3、y(cr5r6)(cr7r8)nr3r4、(cr5r6)c(o)r3、(cr5r6)c(o)or3、(cr5r6)c(o)nr3r4、y(cr5r6)c(o)r3、y(cr5r6)c(o)or3、y(cr5r6)c(o)nr3r4、y(cr5r6)(cr7r8)c(o)r3、y(cr5r6)(cr7r8)c(o)or3、y(cr5r6)(cr7r8)c(o)nr3r4、(cr5r6)nr3so2r3或c(=nor 3
)r3等;优选地,为苯环、c
1-6
烷氧基、y(cr5r6)(cr7r8)or3;其中,所述杂环烷基包括含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基选自苯基,蒽基,萘基,菲基等;所述杂环芳基选自吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基等;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;
[0051]
y为o或cr9r
10
;
[0052]
r3选自h、c
1-6
烷基、c
1-6
烷基nhc(o)r4、c
1-6
烷基c(o)nhr4、p(c2烷基氧基)c2烷基nhc(o)r4、p(c2烷基氧基)c2烷基c(o)nhr4等;优选地,为h、c
1-6
烷基c(o)nhr4;其中p为0、1、2、3、4;
[0053]
r4为h、c
1-6
烷基、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基,c
1-6
烷基-环烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基等;其中,所述杂环烷基包括含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基包括苯基,蒽基,萘基,菲基等;所述杂环芳基包括吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基中的一种或几种;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;
[0054]
r5、r6、r7、r8、r9和r
10
独立地选自h、卤素、c
1-6
烷基、oh、co2r3、nr3r4、c
1-6
烷基氧基等;优选地,为h;
[0055]
a环选自下列基团中的任意一个:c
3-8
环烷基、c
7-c
10
桥环、含一个或多个o、n、s原子的杂环烷基、芳基、含一个或多个o、n、s原子的五元或六元杂芳环、含一个或多个o、n、s原子的苯并杂环;其中,所述杂环烷基选自含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基选自苯基,蒽基,萘基,菲基;所述杂环芳基选自吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基;所述苯并杂环选自苯并吡唑基,苯并吡喃基,哒嗪基,苯并嘧啶基,苯并咪唑基,苯并噻唑基,苯并异噻唑基,苯并哌嗪基,吲哚基,喹啉基,吡嗪基,异喹啉基,苯并噁唑基,苯并异噁唑基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基。
[0056]
上述式(iii)中,当m为0,且n为0时,其由下述结构(iv)表示:
[0057][0058]
其中:
[0059]
j为0、1、2、3或4;优选地,为1、2;
[0060]
k为0、1、2、3、4或5;优选地,为0、1;
[0061]
(r1)k指a环上连接的k个取代基r1,各自独立地为h、卤素、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
烷氧基、c
1-6
卤代烷基、c
1-6
烷基氰基、氰基、硝基、羧基、氨基、叠氮基、c
1-6
烷基羟基、or3、sr3、s(o)r3、so2r3、nr3r4、cor3、c(o)r3、co2r3、-nr3c(o)r4、-c(o)nr3r4、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基,c
1-6
烷基-环烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基等;优选地,为h、卤素、硝基、羧基、氨基、-nr3c(o)r4、-c(o)nr3r4。
[0062]
其中,所述杂环烷基包括含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基选自苯基,蒽基,萘基,菲基等;所述杂环芳基选自吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基等;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;
[0063]
(r2)j指苯环上连接的j个取代基r2,各自独立地选自h、卤素、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
烷氧基、c
1-6
卤代烷基、c
1-6
烷基氰基、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基,c
1-6
烷基-环烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基、氰基、硝基、羧基、氨基、sr3、s(o)r3、so2r3、n r3r4、cor3、c(o)r3、co2r3、c(o)r3、co2r3、c(o)nr3r4、c
1-6
烷基氧基、(cr5r6)or3、(cr5r6)nr3r4、(cr5r6)(cr7r8)or3、y(cr5r6)(cr7r8)or3、y(cr5r6)(cr7r8)nr3r4、(cr5r6)c(o)r3、(cr5r6)c(o)or3、(cr5r6)c(o)nr3r4、y(cr5r6)c(o)r3、y(cr5r6)c(o)or3、y(cr5r6)c(o)nr3r4、y(cr5r6)(cr7r8)c(o)r3、y(cr5r6)(cr7r8)c(o)or3、y(cr5r6)(cr7r8)c(o)nr3r4、(cr5r6)nr3so2r3或c(=nor 3
)r3等;优选
地,为苯环、c
1-6
烷氧基、y(cr5r6)(cr7r8)or3;其中,所述杂环烷基包括含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基选自苯基,蒽基,萘基,菲基等;所述杂环芳基选自吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基等;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;
[0064]
y为o或cr9r
10
;
[0065]
r3选自h、c
1-6
烷基、c
1-6
烷基nhc(o)r4、c
1-6
烷基c(o)nhr4、p(c2烷基氧基)c2烷基nhc(o)r4、p(c2烷基氧基)c2烷基c(o)nhr4等;优选地,为h、c
1-6
烷基c(o)nhr4;其中p为0、1、2、3、4;
[0066]
r4为h、c
1-6
烷基、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基,c
1-6
烷基-环烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基等;其中,所述杂环烷基包括含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基包括苯基,蒽基,萘基,菲基等;所述杂环芳基包括吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基等;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;
[0067]
r5、r6、r7、r8、r9和r
10
独立地选自h、卤素、c
1-6
烷基、oh、co2r3、nr3r4、c
1-6
烷基氧基等;优选地,为h;
[0068]
a环选自下列基团中的任意一个:c
3-7
环烷基、c
7-c
10
桥环、含一个或多个o、n、s原子的杂环烷基、芳基、含一个或多个o、n、s原子的五元或六元杂芳环、含一个或多个o、n、s原子的苯并杂环;其中,所述杂环烷基选自含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基选自苯基,蒽基,萘基,菲基;所述杂环芳基选自吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基;所述苯并杂环选自苯并吡唑基,苯并吡喃基,哒嗪基,苯并嘧啶基,苯并咪唑基,苯并噻唑基,苯并异噻唑基,苯并哌嗪基,吲哚基,喹啉基,吡嗪基,异喹啉基,苯并噁唑基,苯并异噁唑基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基。
[0069]
上述式(iv)中,当a环为噻吩环时,其由下述结构(v)表示:
[0070][0071]
其中:
[0072]
j为0、1、2、3或4,优选地,为1、2;
[0073]
k为0、1、2、3,优选地,为0、1、2;
[0074]
(r1)k指噻吩环上连接的k个取代基r1,各自独立地为h、卤素、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
烷氧基、c
1-6
卤代烷基、c
1-6
烷基氰基、氰基、硝基、羧基、氨基、叠氮基、c
1-6
烷基
羟基、or3、sr3、s(o)r3、so2r3、nr3r4、cor3、c(o)r3、co2r3、-nr3c(o)r4、-c(o)nr3r4、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基,c
1-6
烷基-环烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基等;优选地,为h、卤素、硝基、羧基、氨基、-nr3c(o)r4、-c(o)nr3r4。
[0075]
其中,所述杂环烷基包括含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基选自苯基,蒽基,萘基,菲基等;所述杂环芳基选自吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基等;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;
[0076]
(r2)j指苯环上连接的j个取代基r2,各自独立地选自h、卤素、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
烷氧基、c
1-6
卤代烷基、c
1-6
烷基氰基、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基,c
1-6
烷基-环烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基、氰基、硝基、羧基、氨基、sr3、s(o)r3、so2r3、n r3r4、cor3、c(o)r3、co2r3、c(o)r3、co2r3、c(o)nr3r4、c
1-6
烷基氧基、(cr5r6)or3、(cr5r6)nr3r4、(cr5r6)(cr7r8)or3、y(cr5r6)(cr7r8)or3、y(cr5r6)(cr7r8)nr3r4、(cr5r6)c(o)r3、(cr5r6)c(o)or3、(cr5r6)c(o)nr3r4、y(cr5r6)c(o)r3、y(cr5r6)c(o)or3、y(cr5r6)c(o)nr3r4、y(cr5r6)(cr7r8)c(o)r3、y(cr5r6)(cr7r8)c(o)or3、y(cr5r6)(cr7r8)c(o)nr3r4、(cr5r6)nr3so2r3或c(=nor 3
)r3等;优选地,为苯环、c
1-6
烷氧基、y(cr5r6)(cr7r8)or3;其中,所述杂环烷基包括含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基选自苯基,蒽基,萘基,菲基等;所述杂环芳基选自吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基等;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;
[0077]
y为o或cr9r
10
;
[0078]
r3选自h、c
1-6
烷基、c
1-6
烷基nhc(o)r4、c
1-6
烷基c(o)nhr4、p(c2烷基氧基)c2烷基nhc(o)r4、p(c2烷基氧基)c2烷基c(o)nhr4等;优选地,为h、c
1-6
烷基c(o)nhr4;其中p为0、1、2、3、4;
[0079]
r4为h、c
1-6
烷基、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基,c
1-6
烷基-环烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基等;其中,所述杂环烷基包括含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基包括苯基,蒽基,萘基,菲基等;所述杂环芳基包括吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基等;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;
[0080]
r5、r6、r7、r8、r9和r
10
独立地选自h、卤素、c
1-6
烷基、oh、co2r3、nr3r4、c
1-6
烷基氧基等;优选地,为h;
[0081]
上述式(v)中,当r1通过w基团和噻吩环相连时,其由下述结构(vi)表示:
[0082][0083]
其中:
[0084]
j为0、1、2、3或4,优选地,为1、2;
[0085]
w为氧、c
1-6
烷基、乙烯基、乙炔基、-nr3r
4-、-c(o)-、-nhc(o)-、-c(o)nh-、-nr3c(o)-、-c(o)nr
3-、-nhc(o)nh-、-nhs(o)nh-、-so2nh-、-nhso
2-、-n=n-等;优选地,为-nhc(o)-、-c(o)nh-;
[0086]
r1为h、卤素、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
烷氧基、c
1-6
卤代烷基、c
1-6
烷基氰基、氰基、硝基、羧基、氨基、叠氮基、c
1-6
烷基羟基、or3、sr3、s(o)r3、so2r3、nr3r4、cor3、c(o)r3、co2r3、-nr3c(o)r4、-c(o)nr3r4、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基、c
1-6
烷基-c(o)nr3r4、c
1-6
烷基
‑‑
nr3c(o)r4、c
1-6
烷基-环烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基等;优选地,为c
1-6
烷基羟基、c
1-6
烷基-c(o)nr3r4、c
1-6
烷基
‑‑
nr3c(o)r4。其中,所述杂环烷基包括含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基选自苯基,蒽基,萘基,菲基等;优选地,为c
1-6
烷基羟基;所述杂环芳基选自吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基等;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;
[0087]
(r2)j指苯环上连接的j个取代基r2,各自独立地选自h、卤素、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
烷氧基、c
1-6
卤代烷基、c
1-6
烷基氰基、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基,c
1-6
烷基-环烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基、氰基、硝基、羧基、氨基、sr3、s(o)r3、so2r3、n r3r4、cor3、c(o)r3、co2r3、c(o)r3、co2r3、c(o)nr3r4、c
1-6
烷基氧基、(cr5r6)or3、(cr5r6)nr3r4、(cr5r6)(cr7r8)or3、y(cr5r6)(cr7r8)or3、y(cr5r6)(cr7r8)nr3r4、(cr5r6)c(o)r3、(cr5r6)c(o)or3、(cr5r6)c(o)nr3r4、y(cr5r6)c(o)r3、y(cr5r6)c(o)or3、y(cr5r6)c(o)nr3r4、y(cr5r6)(cr7r8)c(o)r3、y(cr5r6)(cr7r8)c(o)or3、y(cr5r6)(cr7r8)c(o)nr3r4、(cr5r6)nr3so2r3或c(=nor 3
)r3等;优选地,为苯环、c
1-6
烷氧基、y(cr5r6)(cr7r8)or3;其中,所述杂环烷基包括含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基选自苯基,蒽基,萘基,菲基等;所述杂环芳基选自吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基等;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;y为o或cr9r
10
;
[0088]
r3选自h、c
1-6
烷基、c
1-6
烷基nhc(o)r4、c
1-6
烷基c(o)nhr4、p(c2烷基氧基)c2烷基nhc(o)r4、p(c2烷基氧基)c2烷基c(o)nhr4等;优选地,为h、c
1-6
烷基c(o)nhr4;其中p为0、1、2、3、4;
[0089]
r4为h、c
1-6
烷基、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基,c
1-6
烷基-环
烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基等;其中,所述杂环烷基包括含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基包括苯基,蒽基,萘基,菲基等;所述杂环芳基包括吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基等;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;
[0090]
r5、r6、r7、r8、r9和r
10
独立地选自h、卤素、c
1-6
烷基、oh、co2r3、nr3r4、c
1-6
烷基氧基等;优选地,为h;
[0091]
上述式(v)中,当w为6-酰胺基己酰胺时,其由下述结构(vii)表示:
[0092][0093]
其中:
[0094]
j为0、1、2、3或4,优选地,为1、2;
[0095]
(r2)j指苯环上连接的j个取代基r2,各自独立地选自h、卤素、c
1-6
烷基、c
2-6
烯基、c
2-6
炔基、c
1-6
烷氧基、c
1-6
卤代烷基、c
1-6
烷基氰基、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基,c
1-6
烷基-环烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基、氰基、硝基、羧基、氨基、sr3、s(o)r3、so2r3、n r3r4、cor3、c(o)r3、co2r3、c(o)r3、co2r3、c(o)nr3r4、c
1-6
烷基氧基、(cr5r6)or3、(cr5r6)nr3r4、(cr5r6)(cr7r8)or3、y(cr5r6)(cr7r8)or3、y(cr5r6)(cr7r8)nr3r4、(cr5r6)c(o)r3、(cr5r6)c(o)or3、(cr5r6)c(o)nr3r4、y(cr5r6)c(o)r3、y(cr5r6)c(o)or3、y(cr5r6)c(o)nr3r4、y(cr5r6)(cr7r8)c(o)r3、y(cr5r6)(cr7r8)c(o)or3、y(cr5r6)(cr7r8)c(o)nr3r4、(cr5r6)nr3so2r3或c(=nor 3
)r3等;优选地,为苯环、c
1-6
烷氧基、y(cr5r6)(cr7r8)or3;其中,所述杂环烷基包括含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基选自苯基,蒽基,萘基,菲基等;所述杂环芳基选自吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基等;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;
[0096]
y为o或cr9r
10
;
[0097]
r3选自h、c
1-6
烷基、c
1-6
烷基nhc(o)r4、c
1-6
烷基c(o)nhr4、p(c2烷基氧基)c2烷基nhc(o)r4、p(c2烷基氧基)c2烷基c(o)nhr4等;优选地,为h、c
1-6
烷基c(o)nhr4;其中p为0、1、2、3、4;
[0098]
r4为h、c
1-6
烷基、c
3-8
环烷基、c
7-10
桥环烷基、杂环烷基、芳基、杂环芳基,c
1-6
烷基-环烷基、c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-o-芳基、c
1-6
烷基-杂环芳基、杂环芳基-芳基等;优选地,为c
1-6
烷基-杂环烷基、c
1-6
烷基-芳基、c
1-6
烷基-杂环芳基;其中,所述杂环烷基包括含有1-5个氮、氧、硫原子的c
3-8
环烷基;所述芳基包括苯基,蒽基,萘基,菲基等;所述杂环芳基包括吡啶基,呋喃基,吡唑基,吡喃基,哒嗪基,嘧啶基,咪唑基,噻唑基,异噻唑
基,哌嗪基,喹啉基,吡嗪基,异喹啉基,噻吩基,噁唑基,异噁唑基,吲哚基,苯并呋喃基,苯并噻吩基,嘌呤基,咔唑基,吖啶基,吩基嗪,吩噻嗪基,喋啶基,等;其中,所述环烷基,杂环烷基,芳基,杂环芳基可被1-2个r3基团进一步取代;
[0099]
r5、r6、r7、r8、r9和r
10
独立地选自h、卤素、c
1-6
烷基、oh、co2r3、nr3r4、c
1-6
烷基氧基等;优选地,为h;
[0100]
如式(i)—(vii)所述的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,所述化合物具体可以选自:
[0101]
n-([1,1'-联苯]-4-基)噻吩-2-甲酰胺;
[0102]
n-([1,1'-联苯]-3-基)噻吩-2-甲酰胺;
[0103]
n-([1,1'-联苯]-2-基)噻吩-2-甲酰胺;
[0104]
5-([1,1'-联苯]-4-基氨基甲酰基)噻吩-2-羧酸;
[0105]
5-([1,1'-联苯]-3-基氨基甲酰基)噻吩-2-羧酸;
[0106]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)呋喃-2-甲酰胺;
[0107]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-1h-吡咯-2-甲酰胺;
[0108]
5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-羧酸;
[0109]n2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-(3-羟丙基)噻吩-2,5-二甲酰胺;
[0110]n2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-(4-羟丁基)噻吩-2,5-二甲酰胺;
[0111]n2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-(6-羟基己基)噻吩-2,5-二甲酰胺;
[0112]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-硝基噻吩-2-甲酰胺;
[0113]
5-氨基-n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺;
[0114]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(2-氯乙酰胺基)噻吩-2-甲酰胺;
[0115]n2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-环丙基噻吩-2,5-二甲酰胺;
[0116]n2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-(2-羟乙基)噻吩-2,5-二甲酰胺;
[0117]n2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-(5-(5-((3ar,4r,6as)-2-氧六氢-1h-噻吩并[3,4-d]咪唑-4-基)戊酰胺基)戊基噻吩-2,5-二甲酰胺;
[0118]n2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n5-(2-(2-羟基乙氧基)乙基)噻吩-2,5-二甲酰胺;
[0119]
5-(2-氨基乙酰氨基)-n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺;
[0120]
n-(2-氯-5-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺;
[0121]
n-(4-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺;
[0122]
n-([1,1'-联苯]-3-基)噻吩-3-甲酰胺;
[0123]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(6-(5-((3ar,4r,6as)-2-氧六氢-1h-噻吩并[3,4-d]咪唑-4-基)戊酰胺基)六氨基)噻吩-2-甲酰胺;
[0124]
n-(4-(2-甲氧基乙基)苯基)噻吩-2-甲酰胺;
[0125]
n-(3-(2-甲氧基乙基)苯基)噻吩-2-甲酰胺;
[0126]
n-(3-(1-甲基-1h-吡唑-4-基)苯基)噻吩-2-甲酰胺;
[0127]
n-(3-(1h-吡唑-4-基)苯基)噻吩-2-甲酰胺;
[0128]
n-(3-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺;
[0129]
n-(2-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺;
[0130]
n-(3-(1-(2-羟乙基)-1h-吡唑-4-基)苯基)噻吩-2-甲酰胺;
[0131]
n-([[1,1'-联苯]-3-基)-5-(6-(5-((3ar,4r,6as)-2-氧六氢-1h-噻吩并[3,4-d]咪唑-4-基)戊酰胺基)六氨基)噻吩-2-甲酰胺;
[0132]
n2-([1,1'-联苯]-3-基)-n5-(5-(5-(((3ar,4r,6as)-2-氧六氢-1h-噻吩并[3,4-d]咪唑-4-基)戊酰胺基)戊基噻吩-2,5-二甲酰胺;
[0133]n2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-(((2r,3r,4s,5r)-3,4,5,6-四羟基-1-氧己基-2-基)噻吩-2,5-二甲酰胺;
[0134]
n-(1-(2-羟乙基)-1h-吡唑-4-基)噻吩-2-甲酰胺;
[0135]
n-(5-甲基-1h-吡唑-3-基)噻吩-2-甲酰胺;
[0136]
n-(1-甲基-1h-吡唑-4-基)噻吩-2-甲酰胺;
[0137]
n-([1,1'-联苯]-3-基)-1h-1,2,4-三唑-5-甲酰胺;
[0138]
n-([1,1'-联苯]-3-基)噻唑-2-甲酰胺;
[0139]
n-([1,1'-联苯]-3-基)噻唑-4-甲酰胺;
[0140]
n-([1,1'-联苯]-3-基)-1h-吡唑-5-甲酰胺;
[0141]
n-([1,1'-联苯]-3-基)噻唑-5-甲酰胺;
[0142]
n-([1,1'-联苯]-3-基)-1-羟基-1h-1,2,3-三唑-4-甲酰胺;
[0143]
n-([1,1'-联苯]-3-基)异噻唑-5-甲酰胺;
[0144]
n-(噻吩-2-基)-[1,1'-联苯]-3-甲酰胺;
[0145]
n-([1,1'-联苯]-3-基)异噻唑-5-甲酰胺;
[0146]
1-([1,1'-联苯]-3-基)-3-(噻吩-2-基)脲;
[0147]
n-([1,1'-联苯]-3-基甲基)噻吩-2-甲酰胺;
[0148]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻唑-5-羧酰胺;
[0149]
n-(4-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺;
[0150]
n-(3-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺;
[0151]
4-溴-n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2-羧酰胺;
[0152]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-1-甲基-1h-吡唑-3-甲酰胺;
[0153]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(甲基磺酰基)噻吩-2-甲酰胺;
[0154]
3-溴-n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2-羧酰胺;
[0155]
n-(5-氯-2-(2-羟乙基)苯基)噻吩-2-甲酰胺;
[0156]
n-(5-氯-2-(戊氧基)苯基)噻吩-2-甲酰胺;
[0157]
n-(5-氯-2-乙氧基苯基)噻吩-2-甲酰胺;
[0158]
4-氯-2-(噻吩-2-甲酰胺基)苯基乙酸;
[0159]
n-(2-(2-甲氧基乙氧基)-5-甲基苯基)噻吩-2-甲酰胺;
[0160]
n-(2-丁氧基-5-氯苯基)噻吩-2-甲酰胺;
[0161]
n-(5-氯-2-丙氧基苯基)噻吩-2-甲酰胺;
[0162]
n-(5-氯-2-(3-甲氧基丙氧基)苯基)噻吩-2-甲酰胺;
[0163]
n-(5-氯-2-(2-乙氧基乙氧基)苯基)噻吩-2-甲酰胺;
[0164]
n-(5-氯-2-(2-羟基乙氧基)苯基)噻吩-2-甲酰胺;
[0165]
n-(5-氯-2-(2,2,2-三氟乙氧基)苯基)噻吩-2-甲酰胺;
[0166]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻唑-2-羧酰胺;
[0167]
n-(5-氯-2-(庚氧基)苯基)噻吩-2-甲酰胺;
[0168]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-6-乙炔基烟酰胺;
[0169]
4-氯-2-(噻吩-2-甲酰胺基)苯甲酸甲酯;
[0170]
n-(2-(2-甲氧基乙基)苯基)噻吩-2-甲酰胺;
[0171]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(环丙烷甲酰胺基)噻吩-2-甲酰胺;
[0172]
n-(5-氯-2-(丙-2-炔-1-基氧基)苯基)噻吩-2-甲酰胺;
[0173]
(5-((5-氯-2-(2-甲氧基乙氧基)苯基氨基甲酰基)噻吩-2-羰基)甘氨酸;
[0174]
n-(5-甲氧基-2-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺;
[0175]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-甲氧基吡嗪-2-羧酰胺;
[0176]
n-(5-溴-2-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺;
[0177]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-4-苯基噻唑-2-羧酰胺;
[0178]
n-(5-氟-2-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺;
[0179]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2-磺酰胺;
[0180]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-1-羟基-1h-苯并[d][1,2,3]三唑-6-甲酰胺;
[0181]
叔丁基(5-(5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-甲酰胺基)戊基)氨基甲酸酯;
[0182]n2-(5-氨基戊基)-n
5-(5-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2,5-二甲酰胺;
[0183]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-甲氧基吡啶甲酸酰胺;
[0184]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(2-(2-(2-(5-(((3ar,6as)-2-氧代六氢-1h-噻吩并[3,4-d]咪唑-4-基)戊酰胺基)乙氧基)乙氧基)乙酰氨基)噻吩-2-羧酰胺;
[0185]n2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-(2-(2-(2-(5-(((3ar,6as)-2-氧代六氢-1h-噻吩并[3,4-d]咪唑-4-基)戊酰胺基乙氧基)乙氧基)乙基噻吩-2,5-二甲酰胺;
[0186]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)嘧啶-4-羧酰胺;
[0187]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)哒嗪-3-羧酰胺;
[0188]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-2-苯基环丙烷-1-羧酰胺;
[0189]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻唑-4-羧酰胺;
[0190]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)异噻唑-5-羧酰胺;
[0191]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-1h-1,2,4-三唑-5-羧酰胺;
[0192]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-4-羟基吡咯烷-2-羧酰胺;
[0193]
2-(5-氯-2-(2-甲氧基乙氧基)苯基)噻吩;
[0194]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-3-(噻吩-2-基)丙酰胺;
[0195]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-4-(噻吩-2-基)丁酰胺;
[0196]
n-([[1,1'-联苯]-3-基)-2-(噻吩-2-基)乙酰胺;
[0197]n2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-(2-(2-(2-(2-(2-苯基乙酰胺基)乙氧基)乙氧基)乙基)噻吩-2,5-二甲酰胺;
[0198]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(6-(噻吩-2-甲酰胺基)六氨基)噻吩-2-甲酰胺;
[0199]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(6-(2-苯基乙酰胺基)六氨基)噻吩-2-羧酰胺;
[0200]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(6-(2-(噻吩-2-基)乙酰氨基)六氨基)噻吩-2-甲酰胺;
[0201]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(6-(3-(4-氟苯基)丙酰胺基)己酰胺基)噻吩-2-甲酰胺;
[0202]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(6-(4-(噻吩-2-基)丁酰胺基)六氨基)噻吩-2-甲酰胺;
[0203]
2-氯-n-(6-((5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-基)氨基)-6-氧己基)嘧啶-5-羧酰胺;
[0204]
3-溴-n-(6-((5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-基)氨基)-6-氧己基)呋喃-2-羧酰胺;
[0205]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(6-(4-氯-2-甲基苯甲酰胺基)六氨基)噻吩-2-甲酰胺;
[0206]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(6-(3-(噻吩-2-基)丙酰胺基)六氨基)噻吩-2-甲酰胺;
[0207]n2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-(6-((5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-基)氨基)-6-氧己基)噻吩-2,5-二甲酰胺;
[0208]
n-(6-((5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-基)氨基)-6-氧己基)苯并呋喃-2-羧酰胺;
[0209]
n-(6-((5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-基)氨基)-6-氧己基)噻唑-5-羧酰胺;
[0210]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(6-(2-(吡啶-2-基)乙酰氨基)六氨基)噻吩-2-甲酰胺;
[0211]
n-(6-((5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-基)氨基)-6-氧己基)-1h-吡唑-5-羧酰胺;
[0212]
5-(6-(2-(1h-四唑-1-基)乙酰氨基)六氨基)-n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺;
[0213]
n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(6-(4-苯基丁酰胺基)六氨基)噻吩-2-羧酰胺。
[0214]
本发明还提供了一种药物组合物,所述药物组合物包含了本发明前述的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体以及药学上可接受的赋形剂。
[0215]
在某些实施方案中,该药物组合物进一步包含了能有效预防、治疗、改善哺乳动物的关节炎或关节损伤和/或与关节炎或关节损伤相关症状的额外化合物。
[0216]
在某些实施方案中,该额外的化合物选自nsaids、镇痛药、血管生成素样3蛋白(angptl3)或其软骨形成变体、口服鲑鱼降钙素、sd-6010(inos抑制剂)、维生素d3(胆骨化醇)、凋亡/胱天蛋白酶抑制剂(恩利卡生)、胶原水解物、fgf18、bmp7、鳄梨大豆不皂化物(avocado soy unsaponifiables)(asu)、透明质酸中的一种或几种;优选地,为fgf18、
bmp7、透明质酸。
[0217]
本发明还提供了前述的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物在制备预防和/或治疗和/或改善哺乳动物的关节炎或关节损伤和/或与关节炎或关节损伤相关症状的药物组合物中的用途。
[0218]
所述关节炎是骨关节炎、创伤性关节炎、自身免疫性关节炎等中的一种或几种。
[0219]
所述化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体、药物组合物可通过在基质和生物相容性骨架中施用于所需的对象;所施用的组合物中还包含透明质酸。
[0220]
本发明还提供了预防、治疗、或改善哺乳动物的关节炎或关节损伤的方法,该方法包括对所述哺乳动物施用治疗有效量的本发明的化合物或组合物,其中,所述哺乳动物具有关节损害或关节炎或处于其风险中。
[0221]
本发明还提供了预防、治疗、或改善人类患者的关节炎或关节损伤的方法,该方法包含:对所述患者的关节施用包含有效量的本发明化合物或组合物,由此治疗、改善或预防患者的关节炎或关节损伤。
[0222]
所述患者具有关节炎或关节损伤;或不具有关节炎或关节损伤,但处于其风险中。
[0223]
其中,所述关节炎是骨关节炎、创伤性关节炎、自身免疫性关节炎;所施用的组合物还包含透明质酸。
[0224]
本发明还提供了一种前述化合物用于诱导间充质干细胞(mscs)分化成软骨细胞的方法。所述方法包括使间充质干细胞接触足量的本发明的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体、或药物组合物,由此诱导干细胞分化成软骨细胞。
[0225]
所述诱导间充质干细胞(mscs)分化成软骨细胞的方法可以在体外进行,也可以在哺乳动物体内进行,且干细胞存在于哺乳动物中。
[0226]
在一些实施方案中,该哺乳动物是驯养动物或家畜。在某些实施方案中,该哺乳动物是人、鼠、兔、狗、猫或马。
[0227]
上述方法中所述接触在基质或生物相容性骨架中进行;所述接触也可以通过所述化合物结合一种或多种另外的软骨形成因子进行;所述接触还可以通过所述化合物结合一种活性剂进行,所述活性剂选自血管生成素样3蛋白(angptl3)、口服鲑鱼降钙素、sd-6010(inos抑制剂)、维生素d3(胆骨化醇)、胶原蛋白水解物、fgf18、bmp7、醋酸芦沙拉肽、鳄梨大豆不皂化物(asu)、类固醇和类固醇抗炎药(nsaid)、透明质酸等中的一种或几种。
[0228]
任意适量的本发明化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物可以诱导mscs分化成软骨细胞,根据活性成分的特定应用和效能,本发明的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物的使用量范围为0.1mg至10000mg,例如1.0mg至1000mg、例如10mg至5000mg的量存在等。在一些实施方案中,在对膝盖的关节内注射中,本发明的化合物可以以0.1μm至约100μm的浓度存在。
[0229]
本发明提供的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物可以用于治疗、改善或预防任意类型的关节软骨损害(例如关节损伤或损伤),包括,例如,来源于创伤事件或肌腱或韧带撕裂的损害。在一些
实施方案中,施用本发明的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物可预防或改善关节炎或关节损害,例如,其中在关节手术之前或过程中存在关节炎或关节损害或关节损伤的遗传或家族史;也可用于治疗关节损害;所述关节损害是创伤性关节损害;也可以是因年龄或不活动导致的损害;也可以是因自身免疫性疾病导致的损害。在本发明的一些实施方案中,本发明的化合物、组合物和方法可以用于治疗、改善或预防骨关节炎(实施例3-1)。在一些实施方案中,所述化合物、组合物和方法用于改善或预防处于具有或获得性关节炎风险中的受试者中的关节炎(实施例3-2、3)。在一些实施方案中,所述化合物、组合物和方法用于改善或预防处于具有或获得性关节损伤的风险中的受试者的关节损伤(实施例3-2、3-3)。
[0230]
本发明提供的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物可用于刺激例如因跌打损伤或软骨病导致的受损的软骨组织中软骨细胞增殖和软骨产生的方法。具体地,本发明提供的的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物可用于治疗关节中的软骨损害,例如关节连接面上的软骨损害,例如脊骨、肩嘈中腕、指、髋、膝、踝关节和足关节;可以得益于治疗的疾病或障碍的实例包括骨关节炎、类风湿性关节炎、其它的自身免疫病或骨软骨炎病。此外,软骨损害或破坏还会作为一些遗传性或代谢性障碍的结果发生,软骨畸形通常在人的侏儒症中观察到,和/或治疗软骨损害或破坏通常是重建外科手术的结果;因此,本发明提供的前述的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物无论是单独使用或与其它方法结合使用,都是对患者有用的疗法。
[0231]
本发明可通过直接注入关节的滑液、全身施用(口服或静脉内)或直接注入软骨缺陷来施用本发明提供的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物,其可以单独施用或与延长蛋白质释放的适合的载体复合施用;在一些实施方案中,可以将化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物在生物相容性材质或骨架中施用。本发明的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物还可以与手术操作结合在受损关节处使用。本发明的实施,可以在手术操作之前、过程中或与之结合、和/或手术操作之后进行。例如,本发明的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物可以用于使培养物中的软骨细胞群扩充,以便自体或异体软骨细胞植入(aci);可以在施用本发明化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物的同时治疗植入软骨细胞。在这些方法中,例如,可以任选地在本发明化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物和/或另外的生长因子的存在下通过关节内镜从受损关节的带有少量未受损负荷的区域中收集软骨细胞,且在体外孵育以便增加细胞数量,然后移植。然后任选地将扩充的培养物与本发明的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物混合,并且放入关节间隙或直接放入缺陷。在一些实施方案中,可以将扩充的培养物与本发明的化合物一起放入悬浮于基质或膜中的关节间隙。在另外的实施方案中,本发明的化合物或其药学上可接受的盐、多晶
型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物还可以与一种或多种包含软骨形成细胞的骨膜或软骨膜移植物结合使用,有助于将植入的软骨细胞或软骨细胞前体细胞保持就位。在一些实施方案中,使用本发明的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物结合其它方法也可以修复软骨损害,所述其它方法包括但不限于灌洗关节、刺激骨髓、磨削性关节成形术、软骨下钻孔术或近端软骨下骨微小骨折等。在施用本发明的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物,并且软骨生长后,再进行手术治疗可以有益于适当地使新形成的软骨表面形成轮廓。
[0232]
本发明的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物可以促进人表皮成纤维细胞中的胶原蛋白表达;本发明由此提供增加成纤维细胞中胶原蛋白产生的方法,通过使成纤维细胞接触本发明的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物来进行,由此增加成纤维细胞中胶原蛋白的产生。所述接触可以通过将所述化合物直接注入待治疗的区域在体内进行,也可以在体外进入成纤维细胞群。
附图说明
[0233]
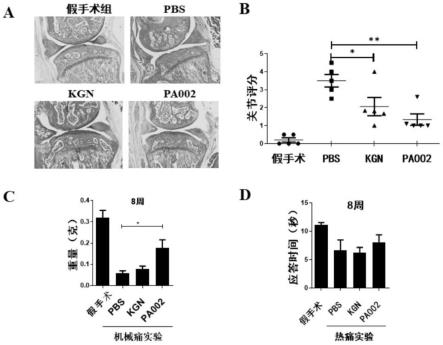
图1为本发明pa002对c57小鼠急性损伤手术模型的软骨损伤修复效果示意图。其中,图1a为小鼠膝关节石蜡切片番红固绿染色结果;图1b为软骨损伤胫骨外侧平台关节评分统计结果;图1c为承重测试评价pa002缓解小鼠oa诱导疼痛结果;图1d为热板实验评价pa002缓解小鼠oa诱导疼痛结果。
[0234]
图2为本发明pa002对c57小鼠软骨缺损模型的软骨修复效果示意图。其中,图2a为显微成像下小鼠关节处软骨缺损修复情况(画圈处为软骨缺损部位);图2b为小鼠关节切片番红固绿染色结果。
[0235]
图3为本发明pa002对sd大鼠软骨缺损模型的软骨修复效果示意图。其中,图3a为pa002体外诱导的uc-mscs体内软骨缺损修复效果以及与对照组的对比;图3b为pa002诱导水凝胶包裹后的uc-mscs体内修复软骨缺损效果以及与对照组的对比。
具体实施方式
[0236]
结合以下具体实施例和附图,对发明作进一步的详细说明。实施本发明的过程、条件、实验方法等,除以下专门提及的内容之外,均为本领域的普遍知识和公知常识,本发明没有特别限制内容。
[0237]
本发明提供了一类化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物,其可刺激间充质干细胞中的软骨细胞分化。本发明还提供了一种诱导间充质干细胞分化为软骨细胞的方法。进一步地,本发明提供了通过向关节、脊椎、椎间盘内或全身性地施用本发明的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物,以治疗、预防或改善关节炎或关节损伤和/或与关节炎或关节损伤相关症状。
[0238]
在以下描述中,对某些具体的细节进行了阐述,以便透彻地理解各实施方案。然而,本领域技术人员将理解,本发明可以在没有这些细节的情况下实施。在其他情形下,没
有详细示出或描述公知的结构,以避免对实施方案的不必要的模糊描述。除非上下文另有要求,在整个说明书及其后的权利要求书中,词语“包含”及其变体,诸如“包括”和“含有”应当解释为开放式、包括性含义,即作为“包括但不限于”。此外,本发明提供的标题仅为了方便,并不解释所请求保护的发明的范围或含义。
[0239]
除非另有说明,如本文所使用的下列术语具有以下含义:
[0240]“氨基”指-nh2基团。
[0241]“氰基”或“腈”指-cn基团。
[0242]“羟基(hydroxy或hydroxyl)”指-oh基团。
[0243]“硝基”指-no2基团。
[0244]“氧代”指=o取代基。
[0245]“肟”指=n-oh取代基。
[0246]“硫代”指=s取代基。
[0247]“烷基”指完全饱和或包含不饱和键的直链或支链的烃链基团,其具有1至30个碳原子,并且通过单键与分子的其余部分连接。涵盖包含1至30个中的任何数目的碳原子的烷基。包含最高达30个碳原子的烷基被称为c
1-30
烷基,同样地,例如,包含最高达12个碳原子的烷基为c
1-12
烷基。包含其他数目的碳原子的烷基(和本发明所定义的其他部分)以相似的方式表示。
[0248]“芳基”指由包含氢、6至30个碳原子和至少一个芳香环的烃环体系衍生的基团。该芳基可为单环、双环、三环或四环环系,可包括稠合或桥接的环系。除非在说明书中另外具体说明,术语“芳基”或前缀“芳”(如在“芳烷基”中)意在包括任选取代的芳基。
[0249]“环烷基”或“碳环”指稳定的、非芳族的单环或多环碳环状环,其可包括稠合或桥接的环系,其为饱和或不饱和的。代表性的环烷基或碳环包括但不限于,具有3至15个碳原子、3至10个碳原子、3至8个碳原子、3至6个碳原子、3至5个碳原子或3至4个碳原子的环烷基。除非在说明书中另外具体说明,环烷基或碳环可任选地被取代。
[0250]“稠合的”指与存在的环结构稠合的本文所述的任何环结构。当稠环为杂环基环或杂芳基环时,在成为稠合的杂环基环或稠合的杂芳基环的一部分的该存在的环结构上的任何碳原子可被氮原子所替代。
[0251]“卤(卤代)”或“卤素”指溴、氯、氟或碘。
[0252]“卤代烷基”指被如上所定义的一个或多个卤素基团取代的如上所定义的烷基。
[0253]
类似地,“卤代烷氧基”指式-ora的基团,其中ra为如上所定义的卤代烷基。除非在说明书中另外具体说明,卤代烷氧基可任选地如下所述被取代。
[0254]“杂环烷基”或“杂环基”或“杂环状环”或“杂环”指包含2至23个碳原子和1至8个选自氮、氧、磷和硫的杂原子的稳定的3至24元非芳香族环基团。除非在说明书中另外具体说明,所述杂环基可为单环、双环、三环或四环环系,可包括稠合或桥接的环系;并且杂环基中的氮、碳或硫原子可任选地被氧化;氮原子可任选地被季铵化;且杂环基可以是部分或完全饱和的。除非在说明书中另外具体说明,杂环基可任选地被取代。杂环烷基的说明性实例也称为非芳香族杂环。术语杂环烷基还包括所有环形式的碳水化合物,包括但不限于单糖、二糖和寡糖。除非另有说明,杂环烷基在环中具有2至10个碳。应理解,当提到杂环烷基中的碳原子的数目时,在该杂环烷基中的碳原子的数目不同于构成杂环烷基(即杂环烷基环的骨
架原子)的原子(包括杂原子)的总数。除非在说明书中另外具体说明,杂环烷基可任选地被取代。
[0255]“杂芳基”指包含氢原子、1至13个碳原子、1至6个选自氮、氧、磷和硫的杂原子以及至少一个芳环的5至14元环系基团。为达到本发明的目的,杂芳基可以是单环、双环、三环或四环环系,可包括稠合或桥接的环系;且在杂芳基中的氮、碳或硫原子可任选地被氧化;氮原子可任选地被季铵化。除非在说明书中另外具体说明,杂芳基可任选地被取代。
[0256]
术语“任选的”或“任选地”意指随后描述的事件或情况可能发生或可能不发生,并且该描述包括其中所述事件或情况发生的情形和所述事件或情况不发生的情形。
[0257]“有效量”或“治疗有效量”指作为单剂量或作为系列剂量的一部分施用于哺乳动物受试者并有效地产生所需治疗效果的化合物的量。
[0258]
对个体(例如,哺乳动物,如人)或细胞的“治疗(处理)”是在试图改变个体或细胞的自然进程中使用的任何类型的干预。在一些实施方案中,治疗包括在病理性事件或与病原体接触开始后施用药物组合物,并包括病况的稳定化(例如,病况不恶化或病况的缓解。在其他实施方案中,治疗还包括预防性处理(例如当个体被怀疑为患有细菌感染时,施用本文所述的组合物)。
[0259]“互变异构体”指从分子的一个原子到同一分子的另一个原子的质子转移。本文提供的化合物可作为互变异构体存在。互变异构体为通过氢原子的迁移(伴随单键和相邻双键的转换)可相互转化的化合物。在可能发生互变异构的键合排列中,将存在互变异构体的化学平衡。考虑了本文所公开的化合物的所有互变异构形式。互变异构体的确切比例取决于若干因素,包括温度、溶剂和ph。
[0260]
本发明所公开的化合物的“代谢物”为当化合物被代谢时所形成的该化合物的衍生物。术语“活性代谢物”指化合物被代谢时所形成的该化合物的生物活性衍生物。如本文所使用的,术语“代谢”指通过其使特定物质被生物体所改变的过程的总和。因此,酶可产生化合物的特定结构改变。本文所公开的化合物的代谢物可通过以下方法来鉴定:将化合物施用于宿主并对来自该宿主的组织样品进行分析,或将化合物与肝细胞在体外温育并对所得化合物进行分析。这两种方法都是本领域公知的。在一些实施方案中,化合物的代谢物通过氧化过程形成,并对应于相应的含羟基化合物。在一些实施方案中,化合物被代谢成药理活性代谢物。
[0261]
本发明提供了用于诱导间充质干细胞分化为软骨细胞以及用于预防、治疗、改善哺乳动物的关节炎或关节损伤和/或与关节炎或关节损伤相关症状的化合物以及这类化合物的制备方法。本发明还提供了这类化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,以及包含至少一种这样的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体以及药学上可接受的赋形剂的药物组合物。
[0262]
本发明提供的化合物可使用本领域技术人员已知的标准合成反应或使用本领域已知的方法来合成。可以以线性顺序采用反应来提供所述化合物,或者可使用这些反应来合成片段,随后通过本领域已知的方法进行连接。
[0263]
如果需要,可使用包括但不限于过滤、蒸馏、结晶及色谱法等常规技术来分离和纯化反应产物。这类材料可使用包括物理常数和波谱数据在内的常规手段来表征。
[0264]
本发明所使用的低温反应装置为eyela(psl-1810)磁力搅拌低温恒温水槽;eyela(n-1100)旋转蒸发仪;实验所得化合物的纯度结果均来自于agilent 1200series lc system高效液相色谱分析仪(色谱条件:zorbax xdb-c18(4.6
×
150mm,5μm),柱温40℃,流动相为meoh/h2o,运行流速为1.5ml/min,紫外检测波长为254nm,进样量为10μl);核磁共振波谱仪为bruker 300型或500型(内标:tms,使用溶剂为cdcl3或dmso-d6);反应中间体以及终产物的纯化均使用层析色谱柱(所用硅胶200-300目),所使用的硅胶购买于青岛海洋化工厂。所有溶剂在使用前均经过重新蒸馏,所使用的无水溶剂均是按标准方法干燥处理获得;除特别说明外,所有反应均是在氮气保护下进行并用tlc跟踪反应进度,后处理均经过饱和食盐水洗和无水硫酸钠干燥。
[0265]
所述哺乳动物部分没有患有关节炎或关节损伤,但其患关节炎或关节损伤的风险增加。
[0266]
本发明提供的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物可以用于预防、治疗、改善任何类型的关节炎或关节损伤或各种软骨病症;在一些实施方案中,施用本发明的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物以预防关节炎或关节损伤,例如在存在关节炎或关节损伤的遗传或家族史或先前进行过关节手术的情况下,或在关节炎或关节损伤风险增加的其他情况下。本发明提供的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物可治疗或预防的示例性的病况或病症包括但不限于系统性类风湿性关节炎、幼年型慢性关节炎、骨关节炎、椎间盘退变性疾病、脊椎关节病和系统性硬化症(硬皮病)。所述关节炎可以是骨关节炎、创伤性关节炎、椎间盘退变性疾病、迪皮特朗病(dupuytren disease)或腱疾病。
[0267]
本发明还提供了一种利用前述化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物刺激已经由于创伤性损伤或软骨病而损伤的软骨组织中的软骨细胞增殖和软骨产生的方法。创伤性损伤可以包括但不限于关节的钝伤或韧带的损伤,如前交叉韧带、内侧副韧带撕裂或半月板撕裂;展现出关节联接表面,因此对治疗特别敏感的组织的实例包括但不限于脊柱、肩、肘、腕、手指关节、髋、膝、踝、足关节等。可以受益于治疗的疾病的实例包括骨关节炎、类风湿性关节炎、其他自身免疫性疾病、分离性骨软骨炎等。另外,软骨畸形在人类侏儒形式中常见,因此本发明能够用于帮助治疗软骨畸形的患者。
[0268]
本发明所述的“哺乳动物”是指被分类为哺乳动物的任何哺乳动物,包括人,驯养动物和农畜,陪伴动物或家畜以及动物园饲养、竞技活动所用的动物;所述“陪伴动物”是指狗、猫、啮齿动物和兔。具体地,可以是人、牛(例如母牛)、马、狗、绵羊、猪、兔、山羊、猫等。动物的选择根据实际情况确定。
[0269]
本发明还提供了一种诱导间充质干细胞(msc)分化为软骨细胞的方法。该方法包括使间充质干细胞接触足量的本发明的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物,由此诱导干细胞分化为软骨细胞。
[0270]
msc是多能干细胞,其能够分化成数种不同类型的细胞,包括但不限于成骨细胞、软骨细胞和脂肪细胞。分化过程是由特化程度较低的细胞类型形成特化的细胞类型,例如
由msc形成软骨细胞的过程。所述诱导间充质干细胞(msc)分化为软骨细胞的方法可以在体外进行,也可以在哺乳动物的体内进行,并且所述干细胞存在于该哺乳动物中。在某些实施方案中,该哺乳动物是人、狗、猫或马等中的一种或几种。
[0271]
诱导msc分化为软骨细胞可以使用任何适量的本发明的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物来完成,根据活性组分的特定应用和效力,本发明的化合物或其药学上可接受的盐、多晶型物、前药、酯、代谢物、n-氧化物、立体异构体或异构体,或药物组合物的使用量范围为0.1mg至10000mg,例如1.0mg至1000mg或例如10mg至500mg等。在一些实施方案中,本发明的化合物也可以以0.1μm
–
100μm的浓度存在于针对膝盖的关节内注射液中。
[0272]
实施例一:各化合物的制备
[0273]
实施例1-1、n-([1,1'-联苯]-4-基)噻吩-2-甲酰胺(pa001)的制备
[0274]
将4-氨基联苯(169mg,1mmol),2-噻吩甲酸(141mg,1.1mmol),n,n-二异丙基乙胺(388mg,3mmol)和hatu(418mg,1.1mmol)溶于3ml的n,n-二甲基甲酰胺中,室温搅拌反应6h。tlc检测反应完全后,用乙酸乙酯萃取反应液,有机相用水洗涤两次,饱和食盐水洗一次,无水硫酸钠干燥。蒸干有机相后,通过柱层析分离纯化得到产物pa001(220mg,79%)。
[0275]1h nmr(500mhz,chloroform-d)δ7.72(s,1h),7.70(d,j=8.6hz,2h),7.65(dd,j=3.8,1.2hz,1h),7.63
–
7.58(m,4h),7.56(dd,j=5.0,1.2hz,1h),7.47
–
7.41(m,2h),7.37
–
7.31(m,1h),7.15(dd,j=5.0,3.7hz,1h)。
[0276]
实施例1-2、n-([1,1'-联苯]-3-基)噻吩-2-甲酰胺(pa002)的制备
[0277]
采用与制备化合物pa001类似的方法,将4-氨基联苯替换为3-氨基联苯,最终得到化合物pa002,产率75%。
[0278]1h nmr(500mhz,chloroform-d)δ7.90
–
7.86(m,1h),7.75(s,1h),7.67
–
7.64(m,1h),7.61(ddd,j=11.9,8.6,1.1hz,3h),7.56(dd,j=5.0,1.0hz,1h),7.47
–
7.41(m,3h),7.42
–
7.32(m,2h),7.15(dd,j=4.9,3.8hz,1h)。
[0279]
实施例1-3、n-([1,1'-联苯]-2-基)噻吩-2-甲酰胺(pa003)的制备
[0280]
采用与制备化合物pa001类似的方法,将4-氨基联苯替换为2-氨基联苯,最终得到化合物pa003,产率77%。
[0281]1h nmr(500mhz,chloroform-d)δ8.50(dd,j=8.3,1.2hz,1h),7.89
–
7.85(m,1h),7.57
–
7.50(m,2h),7.50
–
7.35(m,5h),7.30(dd,j=7.6,1.7hz,1h),7.24
–
7.18(m,1h),7.16(dd,j=3.8,1.2hz,1h),7.02(dd,j=5.0,3.7hz,1h)。
[0282]
实施例1-4、5-([1,1'-联苯]-4-基氨基甲酰基)噻吩-2-羧酸(pa004)的制备
[0283]
将4-氨基联苯(169mg,1mmol),5-羧酸-2-噻吩甲酸甲酯(205mg,1.1mmol),n,n-二异丙基乙胺(388mg,3mmol)和hatu(418mg,1.1mmol)溶于3ml的n,n-二甲基甲酰胺中,室温搅拌反应6h。tlc检测反应完全后,用乙酸乙酯萃取反应液,有机相用水洗涤两次,饱和食盐水洗一次,无水硫酸钠干燥。蒸干有机相后,通过柱层析分离纯化得到化合物5-([1,1'-联苯]-4-基氨基甲酰基)噻吩-2-羧酸甲酯(270mg,产率80%)。
[0284]
将化合物5-([1,1'-联苯]-4-基氨基甲酰基)噻吩-2-羧酸甲酯(270mg,0.8mmol),lioh
·
h2o(336mg,8mmol)溶于甲醇/水(8ml/2ml)中,80℃反应2h。tlc检测反应完全后,旋去有机溶剂,水相用稀盐酸调成酸性,抽滤后滤饼放入真空干燥箱内干燥,得终产物pa004
(212mg,产率82%)。
[0285]1h nmr(500mhz,dmso-d6)δ10.24(s,1h),7.84(d,j=8.4hz,3h),7.67(dd,j=7.9,4.0hz,4h),7.48
–
7.42(m,2h),7.37
–
7.30(m,1h),7.27(d,j=3.7hz,1h)。
[0286]
实施例1-5、5-([1,1'-联苯]-3-基氨基甲酰基)噻吩-2-羧酸(pa005)的制备
[0287]
采用与制备化合物pa004类似的方法,将4-氨基联苯替换为3-氨基联苯,最终得到化合物pa005,产率85%。
[0288]1h nmr(500mhz,dmso-d6)δ10.23(s,1h),7.90
–
7.86(m,1h),7.73(s,1h),7.62(ddd,j=11.9,8.6,1.1hz,3h),7.52(dd,j=5.0,1.0hz,1h),7.47
–
7.40(m,3h),7.43
–
7.33(m,2h),7.16(dd,j=4.9,3.8hz,1h)。
[0289]
实施例1-6、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-甲氧基吡啶甲酸酰胺(pa006)的制备
[0290]
将4-氯-2-硝基苯酚(1.74g,10mmol),2-溴乙基甲基醚(4.17g,30mmol),碳酸钾(4.14g,30mmol)溶于n,n-二甲基甲酰胺(30ml)中,80℃反应2小时。tlc检测反应完全后,用乙酸乙酯萃取反应液,有机相用水洗涤两次,饱和食盐水洗一次,无水硫酸钠干燥。蒸干有机相后,通过柱层析分离纯化得到化合物4-氯-1-(2-甲氧基乙氧基)-2-硝基苯(2.2g,产率95%)
[0291]
将4-氯-1-(2-甲氧基乙氧基)-2-硝基苯(2.2g,9.5mmol)溶于甲醇(30ml)中,加入钯碳,通入氢气,室温反应2小时。tlc检测反应完全后,用硅藻土抽滤,滤液旋干得到化合物5-氯-2-(2-甲氧基乙氧基)苯胺(1.8g,产率94%)。
[0292]
将5-氯-2-(2-甲氧基乙氧基)苯胺(202mg,1mmol),5-甲氧基吡啶甲酸(168mg,1.1mmol),n,n-二异丙基乙胺(388mg,3mmol)和hatu(418mg,1.1mmol)溶于3ml的n,n-二甲基甲酰胺中,室温搅拌反应6小时。tlc检测反应完全后,用乙酸乙酯萃取反应液,有机相用水洗涤两次,饱和食盐水洗一次,无水硫酸钠干燥。蒸干有机相后,通过柱层析分离纯化得到产物pa006,产率70%。
[0293]1h nmr(500mhz,chloroform-d)δ10.51(s,1h),8.66(d,j=2.5hz,1h),8.32
–
8.18(m,2h),7.33(dd,j=8.7,2.9hz,1h),7.01(dd,j=8.7,2.6hz,1h),6.86(d,j=8.7hz,1h),4.30
–
4.17(m,2h),3.94(s,3h),3.89
–
3.82(m,2h),3.52(s,3h)。
[0294]
实施例1-7、n-(5-氯-2-(2-甲氧基乙氧基)苯基)嘧啶-4-羧酰胺(pa007)的制备
[0295]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为嘧啶-4-羧酸,最终得到化合物pa007,产率73%。
[0296]1h nmr(500mhz,chloroform-d)δ10.58(s,1h),9.31(d,j=1.4hz,1h),9.04(d,j=5.0hz,1h),8.63(d,j=2.5hz,1h),8.21(dd,j=5.0,1.4hz,1h),7.07(dd,j=8.7,2.6hz,1h),6.89(d,j=8.7hz,1h),4.37
–
4.16(m,2h),3.98
–
3.72(m,2h),3.52(s,3h)。
[0297]
实施例1-8、n-(5-氯-2-(2-甲氧基乙氧基)苯基)哒嗪-3-羧酰胺(pa008)的制备
[0298]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为哒嗪-3-羧酸,最终得到化合物pa008,产率70%。
[0299]1h nmr(500mhz,chloroform-d)δ9.67(dd,j=2.4,1.3hz,1h),9.45(dd,j=5.2,1.2hz,1h),9.15(s,1h),8.56(d,j=2.5hz,1h),7.97(dd,j=5.3,2.4hz,1h),7.11(dd,j=8.7,2.5hz,1h),6.98(d,j=8.6hz,1h),4.27
–
4.18(m,2h),3.77
–
3.68(m,2h),3.40(s,3h)。
[0300]
实施例1-9、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-2-苯基环丙烷-1-羧酰胺(pa009)的制备
[0301]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为2-苯基环丙烷-1-羧酸,最终得到化合物pa009,产率78%。
[0302]1h nmr(500mhz,chloroform-d)δ8.51(d,j=2.5hz,1h),8.44(s,1h),7.30(t,j=7.6hz,2h),7.24
–
7.19(m,1h),7.17
–
7.09(m,2h),6.96(dd,j=8.6,2.6hz,1h),6.86(d,j=8.6hz,1h),4.19
–
4.05(m,2h),3.72
–
3.63(m,2h),3.34(s,3h),2.60(ddd,j=9.0,6.5,4.0hz,1h),1.81(ddd,j=8.1,5.2,4.1hz,1h),1.73(dt,j=9.5,4.8hz,1h),1.38(ddd,j=8.2,6.5,4.5hz,1h)。
[0303]
实施例1-10、n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻唑-4-羧酰胺(pa010)的制备
[0304]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为噻唑-4-羧酸,最终得到化合物pa010,产率69%。
[0305]1h nmr(500mhz,chloroform-d)δ9.97(s,1h),8.80(d,j=2.1hz,1h),8.62(d,j=2.6hz,1h),8.27(d,j=2.1hz,1h),7.03(dd,j=8.7,2.6hz,1h),6.87(d,j=8.7hz,1h),4.28
–
4.17(m,2h),3.86
–
3.78(m,2h),3.49(s,3h)。
[0306]
实施例1-11、n-(5-氯-2-(2-甲氧基乙氧基)苯基)异噻唑-5-羧酰胺(pa011)的制备
[0307]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为异噻唑-5-羧酸,最终得到化合物pa011,产率72%。
[0308]1h nmr(500mhz,chloroform-d)δ8.82(s,1h),8.56(d,j=1.8hz,1h),8.51(d,j=2.6hz,1h),7.65(d,j=1.7hz,1h),7.07(dd,j=8.7,2.5hz,1h),6.93(d,j=8.7hz,1h),4.32
–
4.12(m,2h),3.78
–
3.66(m,2h),3.41(s,3h)。
[0309]
实施例1-12、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-1h-1,2,4-三唑-5-羧酰胺(pa012)的制备
[0310]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为1h-1,2,4-三唑-5-羧酸,最终得到化合物pa012,产率74%。
[0311]1h nmr(500mhz,chloroform-d)δ9.73(s,1h),8.54(d,j=2.5hz,1h),8.26(s,1h),7.08(dd,j=8.7,2.5hz,1h),6.91(d,j=8.7hz,1h),4.29
–
4.21(m,2h),3.86
–
3.78(m,2h),3.49(s,3h)。
[0312]
实施例1-13、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-4-羟基吡咯烷-2-羧酰胺(pa013)的制备
[0313]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为4-羟基吡咯烷-2-羧酸,最终得到化合物pa013,产率71%。
[0314]1h nmr(500mhz,chloroform-d)δ9.73(s,1h),8.54(d,j=2.5hz,1h),8.26(s,1h),7.08(dd,j=8.7,2.5hz,1h),6.91(d,j=8.7hz,1h),4.29
–
4.21(m,2h),3.86
–
3.78(m,2h),3.49(s,3h)。
[0315]
实施例1-14、2-(5-氯-2-(2-甲氧基乙氧基)苯基)噻吩(pa014)的制备
[0316]
将2-溴-4-氯苯酚(207mg,1mmol),2-溴乙基甲基醚(417mg,3mmol),碳酸钾(414mg,3mmol)溶于n,n-二甲基甲酰胺(5ml)中,80℃反应2h。tlc检测反应完全后,用乙酸
乙酯萃取反应液,有机相用水洗涤两次,饱和食盐水洗一次,无水硫酸钠干燥。蒸干有机相后,通过柱层析分离纯化得到化合物2-溴-4-氯-1-(2-甲氧基乙氧基)苯(245mg,产率92%)。
[0317]
将2-溴-4-氯-1-(2-甲氧基乙氧基)苯(133mg,0.5mmol),2-噻吩硼酸(70mg,0.55mmol),双三苯基膦二氯化钯(35mg,0.05mmol),碳酸钾(104mg,0.75mmol)溶于乙二醇二甲醚(4ml)与水(1ml)中,90℃反应2h。tlc检测反应完全后,用乙酸乙酯萃取反应液,有机相用水洗涤两次,饱和食盐水洗一次,无水硫酸钠干燥。蒸干有机相后,通过柱层析分离纯化得到产物pa014,产率45%。
[0318]1h nmr(500mhz,chloroform-d)δ7.63(d,j=2.6hz,1h),7.53(dd,j=3.7,1.2hz,1h),7.35(dd,j=5.1,1.2hz,1h),7.17(dd,j=8.7,2.6hz,1h),7.09(dd,j=5.1,3.7hz,1h),6.91(d,j=8.8hz,1h),4.20(dd,j=5.6,4.2hz,2h),3.95
–
3.75(m,2h),3.46(s,3h)。
[0319]
实施例1-15、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-3-(噻吩-2-基)丙酰胺(pa015)的制备
[0320]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为3-(噻吩-2-基)丙酸,最终得到化合物pa015,产率74%。
[0321]1h nmr(500mhz,chloroform-d)δ8.48(d,j=2.6hz,1h),8.19(s,1h),7.13(dd,j=5.1,1.2hz,1h),6.97(dd,j=8.6,2.6hz,1h),6.92(dd,j=5.1,3.4hz,1h),6.88
–
6.83(m,2h),4.18
–
4.03(m,2h),3.74
–
3.62(m,2h),3.43(s,3h),3.32
–
3.21(m,2h),2.75(dd,j=8.3,6.8hz,2h)。
[0322]
实施例1-16、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-4-(噻吩-2-基)丁酰胺(pa016)的制备
[0323]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为4-(噻吩-2-基)丁酸,最终得到化合物pa016,产率75%。
[0324]1h nmr(500mhz,chloroform-d)δ8.48(d,j=2.5hz,1h),8.14(s,1h),7.13(dd,j=5.2,1.2hz,1h),6.96(dd,j=8.7,2.6hz,1h),6.92(dd,j=5.2,3.3hz,1h),6.85(d,j=8.7hz,1h),6.84
–
6.81(m,1h),4.19
–
4.03(m,2h),3.73
–
3.65(m,2h),3.39(s,3h),3.02
–
2.91(m,2h),2.51
–
2.36(m,2h),2.11(p,j=7.4hz,2h)。
[0325]
实施例1-17、n-([[1,1'-联苯]-3-基)-2-(噻吩-2-基)乙酰胺(pa017)的制备
[0326]
采用与制备化合物pa002类似的方法,将2-羧基噻吩替换为2-(噻吩-2-基)乙酸,最终得到化合物pa017,产率74%。
[0327]1h nmr(500mhz,chloroform-d)δ7.64(t,j=1.9hz,1h),7.59
–
7.52(m,2h),7.50
–
7.39(m,3h),7.39
–
7.29(m,5h),7.06(d,j=3.9hz,2h),3.98(s,2h)。
[0328]
实施例1-18、n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2-磺酰胺(pa018)的制备
[0329]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为噻吩-2-磺酰氯,最终得到化合物pa018,产率72%。
[0330]1h nmr(500mhz,chloroform-d)δ7.86(s,1h),7.63(d,j=2.5hz,1h),7.55(dd,j=3.8,1.3hz,1h),7.52(dd,j=5.0,1.3hz,1h),7.03
–
6.97(m,2h),6.78(d,j=8.7hz,1h),3.97
–
3.92(m,2h),3.63
–
3.58(m,2h),3.46(s,3h)。
[0331]
实施例1-19、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-1-羟基-1h-苯并[d][1,2,3]三
唑-6-甲酰胺(pa019)的制备
[0332]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为1-羟基-1h-苯并[d][1,2,3]三唑-6-羧酸,最终得到化合物pa019,产率53%。
[0333]1h nmr(500mhz,dmso-d6)δ14.02(s,1h),9.75(s,1h),8.30(s,1h),8.14(d,j=8.5hz,1h),7.99(d,j=2.2hz,1h),7.92(d,j=8.4hz,1h),7.27
–
7.18(m,2h),4.24
–
4.18(m,2h),3.70
–
3.65(m,2h),3.28(s,3h)。
[0334]
实施例1-20、n-(5-氯-2-(2-甲氧基乙氧基)苯基)呋喃-2-甲酰胺(pa020)的制备
[0335]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为糠酸,最终得到化合物pa020,产率81%。
[0336]1h nmr(500mhz,chloroform-d)δ8.91(s,1h),8.56(d,j=2.5hz,1h),7.54
–
7.50(m,1h),7.24(d,j=3.5hz,1h),7.02(dd,j=8.7,2.6hz,1h),6.87(d,j=8.7hz,1h),6.59
–
6.54(m,1h),4.25
–
4.19(m,2h),3.79
–
3.75(m,2h),3.46(s,3h)。
[0337]
实施例1-21、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-1h-吡咯-2-甲酰胺(pa021)的制备
[0338]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为吡咯-2-羧酸,最终得到化合物pa021,产率83%。
[0339]1h nmr(500mhz,chloroform-d)δ9.50(s,1h),8.57(s,1h),8.53(d,j=2.5hz,1h),7.07
–
6.96(m,2h),6.88(d,j=8.6hz,1h),6.79
–
6.74(m,1h),6.33
–
6.27(m,1h),4.23
–
4.17(m,2h),3.77
–
3.71(m,2h),3.45(s,3h)。
[0340]
实施例1-22、5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-羧酸(pa022)的制备
[0341]
将5-氯-2-(2-甲氧基乙氧基)苯胺(202mg,1mmol),5-羧酸-2-噻吩甲酸甲酯(205mg,1.1mmol),n,n-二异丙基乙胺(388mg,3mmol)和hatu(418mg,1.1mmol)溶于3ml的n,n-二甲基甲酰胺中,室温搅拌反应6h。tlc检测反应完全后,用乙酸乙酯萃取反应液,有机相用水洗涤两次,饱和食盐水洗一次,无水硫酸钠干燥。蒸干有机相后,通过柱层析分离纯化得到化合物5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-羧酸甲酯(315mg,产率85%)。
[0342]
将化合物5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-羧酸甲酯(315mg,0.85mmol),lioh
·
h2o(357mg,8.5mmol)溶于甲醇/水(8ml/2ml)中,80℃反应2h。tlc检测反应完全后,旋去有机溶剂,水相用稀盐酸调成酸性,抽滤后滤饼放入真空干燥箱内干燥,得产物pa022(280mg,产率92%)。
[0343]1h nmr(500mhz,dmso-d6)δ13.54(s,1h),9.74(s,1h),7.92(d,j=3.9hz,1h),7.82(d,j=2.3hz,1h),7.78(d,j=3.9hz,1h),7.24(dd,j=8.8,2.4hz,1h),7.19(d,j=8.8hz,1h),4.21
–
4.16(m,2h),3.70
–
3.64(m,2h),3.28(s,3h)。
[0344]
实施例1-23、n
2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-(3-羟丙基)噻吩-2,5-二甲酰胺(pa023)的制备
[0345]
将5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-羧酸(356mg,1mmol),3-氨基-1-丙醇(83mg,1.1mmol),n,n-二异丙基乙胺(388mg,3mmol)和hatu(418mg,1.1mmol)溶于3ml的n,n-二甲基甲酰胺中,室温搅拌反应6h。tlc检测反应完全后,用乙酸乙
酯萃取反应液,有机相用水洗涤两次,饱和食盐水洗一次,无水硫酸钠干燥。蒸干有机相后,通过柱层析分离纯化得到产物pa023(320mg,77%)。
[0346]1h nmr(500mhz,chloroform-d)δ8.79(s,1h),8.52(d,j=2.6hz,1h),7.60(d,j=4.0hz,1h),7.51(d,j=4.0hz,1h),7.04(dd,j=8.6,2.6hz,1h),6.91(d,j=8.7hz,1h),6.73
–
6.66(m,1h),4.24
–
4.18(m,2h),3.78(d,j=6.0hz,2h),3.75
–
3.70(m,2h),3.64(q,j=6.0hz,2h),3.42(s,3h),2.64
–
2.54(m,1h),1.84(p,j=5.7hz,2h)。
[0347]
实施例1-24、n
2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-(4-羟丁基)噻吩-2,5-二甲酰胺(pa024)的制备
[0348]
采用与制备化合物pa023类似的方法,将3-氨基-1-丙醇替换为4-氨基-1-丁醇,最终得到化合物pa024,产率81%。
[0349]1h nmr(500mhz,chloroform-d)δ8.77(s,1h),8.51(d,j=2.6hz,1h),7.59(d,j=3.9hz,1h),7.52(d,j=3.9hz,1h),7.03(dd,j=8.6,2.5hz,1h),6.90(d,j=8.7hz,1h),6.84
–
6.81(m,1h),4.23
–
4.18(m,2h),3.77
–
3.71(m,4h),3.53
–
3.45(m,2h),3.42(s,3h),2.07
–
1.94(m,1h),1.81
–
1.65(m,4h)。
[0350]
实施例1-25、n
2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-(6-羟基己基)噻吩-2,5-二甲酰胺(pa025)的制备
[0351]
采用与制备化合物pa023类似的方法,将3-氨基-1-丙醇替换为6-氨基-1-己醇,最终得到化合物pa025,产率75%。
[0352]1h nmr(500mhz,chloroform-d)δ8.79(s,1h),8.52(d,j=2.6hz,1h),7.60(dd,j=5.2,3.8hz,1h),7.50(d,j=3.9hz,1h),7.44(d,j=2.0hz,1h),7.08
–
7.01(m,1h),6.92(dd,j=8.7,3.9hz,1h),4.34(t,j=6.5hz,1h),4.24
–
4.18(m,2h),3.75
–
3.70(m,2h),3.69
–
3.61(m,2h),3.46(dd,j=14.6,7.1hz,4h),3.42(d,j=2.3hz,3h),1.71
–
1.59(m,2h),1.46
–
1.40(m,4h)。
[0353]
实施例1-26、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-硝基噻吩-2-甲酰胺(pa026)的制备
[0354]
将5-氯-2-(2-甲氧基乙氧基)苯胺(202mg,1mmol),5-硝基噻吩-2-甲酸(190mg,1.1mmol),n,n-二异丙基乙胺(388mg,3mmol)和hatu(418mg,1.1mmol)溶于3ml的n,n-二甲基甲酰胺中,室温搅拌反应6h。tlc检测反应完全后,用乙酸乙酯萃取反应液,有机相用水洗涤两次,饱和食盐水洗一次,无水硫酸钠干燥。蒸干有机相后,通过柱层析分离纯化得到产物pa026(273mg,产率77%)。
[0355]1h nmr(500mhz,chloroform-d)δ8.99(s,1h),8.66(s,1h),8.56(d,j=2.6hz,1h),7.52(d,j=4.2hz,1h),7.02(dd,j=8.7,2.6hz,1h),6.91(d,j=8.6hz,1h),6.82(d,j=4.1hz,1h),4.31(s,2h),4.26
–
4.20(m,2h),3.78
–
3.73(m,2h),3.46(s,3h)。
[0356]
实施例1-27、5-氨基-n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺(pa027)的制备
[0357]
将n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-硝基噻吩-2-甲酰胺(1.78g,5mmol)溶于甲醇(30ml)中,加入钯碳,通入氢气,室温反应2h。tlc检测反应完全后,用硅藻土抽滤,滤液旋干得到产物pa027(800mg,产率94%)。
[0358]1h nmr(500mhz,chloroform-d)δ8.53
–
8.48(m,2h),7.27(d,j=4.1hz,1h),6.95
(dd,j=8.7,2.6hz,1h),6.86(d,j=8.6hz,1h),6.11(d,j=4.0hz,1h),4.30(s,2h),4.21
–
4.08(m,2h),3.74
–
3.69(m,2h),3.42(s,3h)。
[0359]
实施例1-28、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(2-氯乙酰胺基)噻吩-2-甲酰胺(pa028)的制备
[0360]
将5-氨基-n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺(326mg,1mmol),氯乙酰氯(124mg,1.1mmol),三乙胺(303mg,3mmol)溶于二氯甲烷(10ml)中,室温搅拌反应6h。tlc检测反应完全后,用二氯甲烷萃取反应液,有机相用水洗涤两次,饱和食盐水洗一次,无水硫酸钠干燥。蒸干有机相后,通过柱层析分离纯化得到产物pa028(297mg,产率74%)。
[0361]1h nmr(500mhz,chloroform-d)δ8.99(s,1h),8.66(s,1h),8.56(d,j=2.6hz,1h),7.52(d,j=4.2hz,1h),7.02(dd,j=8.7,2.6hz,1h),6.91(d,j=8.6hz,1h),6.82(d,j=4.1hz,1h),4.31(s,2h),4.26
–
4.20(m,2h),3.78
–
3.73(m,2h),3.46(s,3h)。
[0362]
实施例1-29、n
2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-环丙基噻吩-2,5-二甲酰胺(pa029)的制备
[0363]
采用与制备化合物pa023类似的方法,将3-氨基-1-丙醇替换为环丙胺,最终得到化合物pa029,产率68%。
[0364]1h nmr(500mhz,chloroform-d)δ8.78(s,1h),8.52(d,j=2.5hz,1h),7.59(d,j=3.9hz,1h),7.48(s,1h),7.03(dd,j=8.7,2.6hz,1h),6.91(d,j=8.7hz,1h),6.16(s,1h),4.23
–
4.18(m,2h),3.75
–
3.70(m,2h),3.42(s,3h),2.89(tq,j=7.1,3.6hz,1h),0.93
–
0.83(m,2h),0.70
–
0.63(m,2h)。
[0365]
实施例1-30、n
2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-(2-羟乙基)噻吩-2,5-二甲酰胺(pa030)的制备
[0366]
采用与制备化合物pa023类似的方法,将3-氨基-1-丙醇替换为乙醇胺,最终得到化合物pa030,产率72%。
[0367]1h nmr(500mhz,chloroform-d)δ8.80(s,1h),8.52(d,j=2.6hz,1h),7.60(d,j=4.0hz,1h),7.52(d,j=3.9hz,1h),7.04(dd,j=8.7,2.5hz,1h),6.91(d,j=8.6hz,1h),6.53(s,1h),4.24
–
4.18(m,2h),3.88
–
3.84(m,2h),3.75
–
3.70(m,2h),3.67
–
3.60(m,2h),3.42(s,3h),2.27
–
2.23(m,1h)。
[0368]
实施例1-31、n
2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-(5-(5-((3ar,4r,6as)-2-氧六氢-1h-噻吩并[3,4-d]咪唑-4-基)戊酰胺基)戊基噻吩-2,5-二甲酰胺(pa031)的制备
[0369]
采用与制备化合物pa023类似的方法制备叔丁基(5-(5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-甲酰胺基)戊基)氨基甲酸酯。
[0370]
将叔丁基(5-(5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-甲酰胺基)戊基)氨基甲酸酯(270mg,0.5mmol)溶于二氯甲烷(10ml)中,加入盐酸/二氧六环溶液(3ml),室温搅拌反应2h。tlc检测反应完全后,旋去有机溶剂得化合物n
2-(5-氨基戊基)-n
5-(5-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2,5-二甲酰胺(210mg,产率95%)。
[0371]
将n
2-(5-氨基戊基)-n
5-(5-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2,5-二甲酰胺(210mg,0.48mmol),(+)生物素-n-琥珀酰亚胺基酯(180mg,0.53mmol),三乙胺(146mg,1.44mmol)溶于二氯甲烷(10ml)中,室温搅拌反应2h。tlc检测反应完全后,用二氯甲烷萃取反应液,有机相用水洗涤两次,饱和食盐水洗一次,无水硫酸钠干燥。蒸干有机相后,通过柱
层析分离纯化得到产物pa031(253mg,产率80%)。
[0372]1h nmr(500mhz,dmso-d6)δ9.56(s,1h),8.65(s,1h),7.90
–
7.84(m,2h),7.80
–
7.72(m,2h),7.27
–
7.14(m,2h),6.38(d,j=31.4hz,2h),4.29(t,j=6.5hz,1h),4.23
–
4.16(m,2h),4.11(d,j=7.8hz,1h),3.71
–
3.65(m,2h),3.29(s,3h),3.26
–
3.20(m,2h),3.10(d,j=8.9hz,1h),3.05
–
2.99(m,2h),2.81(dd,j=12.3,4.8hz,1h),2.59
–
2.54(m,2h),2.04(t,j=7.0hz,2h),1.60(s,1h),1.55
–
1.38(m,6h),1.35
–
1.25(m,4h)。
[0373]
实施例1-32、n
2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-(2-(2-羟基乙氧基)乙基)噻吩-2,5-二甲酰胺(pa032)的制备
[0374]
采用与制备化合物pa023类似的方法,将3-氨基-1-丙醇替换为二甘醇胺,最终得到化合物pa032,产率72%。
[0375]1h nmr(500mhz,chloroform-d)δ8.78(s,1h),8.52(d,j=2.5hz,1h),7.60(d,j=3.9hz,1h),7.54(d,j=3.9hz,1h),7.03(dd,j=8.6,2.5hz,1h),6.91(d,j=8.6hz,1h),6.69(s,1h),4.24
–
4.18(m,2h),3.81
–
3.78(m,2h),3.76
–
3.62(m,8h),3.42(s,3h),2.17
–
2.06(m,1h)。
[0376]
实施例1-33、5-(2-氨基乙酰氨基)-n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺(pa033)的制备
[0377]
将5-氨基-n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺(326mg,1mmol),boc-甘氨酸(193mg,1.1mmol),n,n-二异丙基乙胺(388mg,3mmol)和hatu(418mg,1.1mmol)溶于3ml的n,n-二甲基甲酰胺中,室温搅拌反应6h。tlc检测反应完全后,用乙酸乙酯萃取反应液,有机相用水洗涤两次,饱和食盐水洗一次,无水硫酸钠干燥。蒸干有机相后,通过柱层析分离纯化得到化合物(2-(((5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-基)氨基)-2-氧乙基)氨基甲酸叔丁酯(386mg,产率80%)。
[0378]
将(2-(((5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-基)氨基)-2-氧乙基)氨基甲酸叔丁酯(386mg,0.8mmol)溶于二氯甲烷(10ml)中,加入盐酸/二氧六环溶液(3ml),室温搅拌反应2h。tlc检测反应完全后,旋去有机溶剂得产物pa033(257mg,产率84%)。
[0379]1h nmr(500mhz,chloroform-d)δ8.51(s,1h),8.50(s,1h),7.27(d,j=4.0hz,1h),6.96(dd,j=8.6,2.6hz,1h),6.87(d,j=8.5hz,1h),6.12(d,j=4.0hz,1h),4.27(s,2h),4.21
–
4.16(m,2h),3.74
–
3.69(m,2h),3.42(s,3h)。
[0380]
实施例1-34、n-(2-氯-5-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺(pa034)的制备
[0381]
采用与制备化合物pa006类似的方法,将4-氯-2-硝基苯酚替换为2-氯-5硝基苯酚,制备化合物2-氯-5-(2-甲氧基乙氧基)苯胺。
[0382]
将2-氯-5-(2-甲氧基乙氧基)苯胺(202mg,1mmol),噻吩-2-羧酸(141mg,1.1mmol),n,n-二异丙基乙胺(388mg,3mmol)和hatu(418mg,1.1mmol)溶于3ml的n,n-二甲基甲酰胺中,室温搅拌反应6小时。tlc检测反应完全后,用乙酸乙酯萃取反应液,有机相用水洗涤两次,饱和食盐水洗一次,无水硫酸钠干燥。蒸干有机相后,通过柱层析分离纯化得到产物pa034(222mg,产率71%)。
[0383]1h nmr(500mhz,chloroform-d)δ8.31(s,1h),8.23(d,j=3.0hz,1h),7.65(dd,j=3.7,1.2hz,1h),7.59(dd,j=5.0,1.1hz,1h),7.28(s,1h),7.16(dd,j=5.0,3.7hz,1h),
溴苯胺制备n-(3-溴苯基)噻吩-2-羧酰胺。
[0401]
将n-(3-溴苯基)噻吩-2-羧酰胺(282mg,1mmol),1-甲基吡唑-4-硼酸频哪醇酯(312mg,1.5mmol),1,1'-双二苯基膦二茂铁二氯化钯(73mg,0.1mmol),碳酸钠(318mg,3mmol)溶于乙二醇二甲醚/水(6ml/3ml)中,90℃反应6h,tlc检测反应完全后,用乙酸乙酯萃取反应液,有机相用水洗涤两次,饱和食盐水洗一次,无水硫酸钠干燥。蒸干有机相后,通过柱层析分离纯化得到产物pa040(191mg,产率67%)。
[0402]1h nmr(500mhz,chloroform-d)δ7.87(s,1h),7.78(s,1h),7.71(s,1h),7.67
–
7.62(m,2h),7.56(dd,j=5.0,1.0hz,1h),7.40
–
7.31(m,2h),7.29
–
7.23(m,1h),7.14(dd,j=4.9,3.8hz,1h),3.94(s,3h)。
[0403]
实施例1-41、n-(3-(1h-吡唑-4-基)苯基)噻吩-2-甲酰胺(pa041)的制备
[0404]
采用与制备化合物pa040类似的方法,将1-甲基吡唑-4-硼酸频哪醇酯替换为4-吡唑硼酸频哪醇酯,最终得到化合物pa039,产率68%。
[0405]1h nmr(500mhz,dmso-d6)δ12.98(s,1h),10.23(s,1h),8.06(d,j=3.6hz,1h),7.92
–
7.84(m,3h),7.56(d,j=7.2hz,2h),7.38
–
7.25(m,2h),7.26
–
7.21(m,1h)。
[0406]
实施例1-42、n-(3-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺(pa042)的制备
[0407]
采用与制备化合物pa034类似的方法,将2-氯-5-(2-甲氧基乙氧基)苯胺替换为3-(2-甲氧基乙氧基)苯胺,最终得到化合物pa042,产率71%。
[0408]1h nmr(500mhz,chloroform-d)δ7.67(s,1h),7.63
–
7.59(m,1h),7.55(dd,j=5.0,0.9hz,1h),7.46
–
7.41(m,1h),7.28
–
7.20(m,1h),7.13(dd,j=4.9,3.8hz,1h),7.08
–
7.03(m,1h),6.74(dd,j=8.3,1.9hz,1h),4.18
–
4.13(m,2h),3.78
–
3.73(m,2h),3.45(s,3h)。
[0409]
实施例1-43、n-(2-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺(pa043)的制备
[0410]
采用与制备化合物pa034类似的方法,将2-氯-5-(2-甲氧基乙氧基)苯胺替换为2-(2-甲氧基乙氧基)苯胺,最终得到化合物pa043,产率71%。
[0411]1h nmr(500mhz,chloroform-d)δ8.77(s,1h),8.51
–
8.44(m,1h),7.66(d,j=3.7hz,1h),7.54(d,j=5.0hz,1h),7.15
–
7.11(m,1h),7.08
–
7.02(m,2h),6.98(dd,j=6.0,3.5hz,1h),4.23(dd,j=5.3,3.7hz,2h),3.75(dd,j=5.2,3.9hz,2h),3.43(s,3h)。
[0412]
实施例1-44、n-(3-(1-(2-羟乙基)-1h-吡唑-4-基)苯基)噻吩-2-甲酰胺(pa044)的制备
[0413]
采用与制备化合物pa040类似的方法,将1-甲基吡唑-4-硼酸频哪醇酯替换为4-(4,4,5,5-四甲基-1,3,2-二噁硼烷-2-基)-1h-吡唑-1-乙醇,最终得到化合物pa044,产率65%。
[0414]1h nmr(500mhz,chloroform-d)δ7.87(s,1h),7.80(s,1h),7.76(s,1h),7.73(s,1h),7.65(d,j=3.6hz,1h),7.56(d,j=5.0hz,1h),7.39
–
7.31(m,2h),7.28
–
7.23(m,1h),7.14(dd,j=4.9,3.8hz,1h),4.34
–
4.24(m,2h),4.14
–
3.96(m,2h),3.12
–
2.97(m,1h)。
[0415]
实施例1-45、n-([[1,1'-联苯]-3-基)-5-(6-(5-((3ar,4r,6as)-2-氧六氢-1h-噻吩并[3,4-d]咪唑-4-基)戊酰胺基)六氨基)噻吩-2-甲酰胺(pa045)的制备
[0416]
采用与制备化合物pa037类似的方法,将5-氯-2-(2-甲氧基乙氧基)苯胺替换为3-氨基联苯,最终得到化合物pa045,产率58%。
[0417]1hnmr(500mhz,dmso-d6)δ11.45(s,1h),10.08(s,1h),8.03(s,1h),7.83(d,j=4.1hz,1h),7.74(d,j=6.2hz,2h),7.64(d,j=7.2hz,2h),7.53
–
7.46(m,2h),7.45
–
7.34(m,3h),6.69(d,j=4.1hz,1h),6.38(d,j=31.2hz,2h),4.31
–
4.25(m,1h),4.15
–
4.08(m,1h),4.03(q,j=7.1hz,1h),3.09(d,j=3.4hz,1h),3.05
–
2.99(m,2h),2.80(dd,j=12.4,4.9hz,1h),2.59
–
2.54(m,2h),2.41
–
2.34(m,2h),2.04(t,j=7.3hz,2h),1.65
–
1.57(m,4h),1.55
–
1.36(m,6h)。
[0418]
实施例1-46、n
2-([1,1'-联苯]-3-基)-n
5-(5-(5-(((3ar,4r,6as)-2-氧六氢-1h-噻吩并[3,4-d]咪唑-4-基)戊酰胺基)戊基噻吩-2,5-二甲酰胺(pa046)的制备
[0419]
采用与制备化合物pa031类似的方法,将5-氯-2-(2-甲氧基乙氧基)苯胺替换为3-氨基联苯,最终得到化合物pa046,产率60%。
[0420]1h nmr(500mhz,dmso-d6)δ10.41(s,1h),8.64(s,1h),8.05(s,1h),8.02
–
7.92(m,2h),7.79(d,j=3.9hz,1h),7.75(d,j=8.7hz,2h),7.65(d,j=7.3hz,2h),7.54
–
7.47(m,2h),7.46
–
7.36(m,2h),6.38(d,j=32.4hz,2h),4.31
–
4.26(m,1h),4.12(s,1h),3.24(d,j=6.0hz,2h),3.05(dd,j=22.4,8.1hz,4h),2.80(dd,j=12.3,4.9hz,1h),2.57(d,j=12.3hz,2h),2.04(t,j=7.2hz,2h),1.55
–
1.38(m,6h),1.35
–
1.26(m,4h)。
[0421]
实施例1-47、n
2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-(((2r,3r,4s,5r)-3,4,5,6-四羟基-1-氧己基-2-基)噻吩-2,5-二甲酰胺(pa047)的制备
[0422]
采用与制备化合物pa023类似的方法,将3-氨基-1-丙醇替换为d-氨基葡萄糖,最终得到化合物pa024,产率81%。
[0423]1h nmr(500mhz,chloroform-d)δ8.81(s,1h),8.48
–
8.42(m,1h),7.55(d,j=4.0hz,1h),7.45(d,j=3.9hz,1h),7.07(ddd,j=7.0,4.3,2.0hz,2h),7.01
–
6.96(m,1h),6.38(s,1h),4.61(dt,j=13.6,6.6hz,1h),4.26
–
4.21(m,2h),3.97
–
3.89(m,4h),3.87
–
3.79(m,5h),3.76
–
3.71(m,2h),3.42(s,3h)。
[0424]
实施例1-48、n-(1-(2-羟乙基)-1h-吡唑-4-基)噻吩-2-甲酰胺(pa048)的制备
[0425]
采用与制备化合物pa034类似的方法,将2-氯-5-(2-甲氧基乙氧基)苯胺替换为2-(4-氨基-1h-吡唑-1-基)乙醇,最终得到化合物pa048,产率71%。
[0426]1h nmr(500mhz,chloroform-d)δ8.06(s,1h),7.60(d,j=2.9hz,2h),7.56
–
7.53(m,2h),7.16
–
7.11(m,1h),4.27
–
4.21(m,2h),4.04
–
3.99(m,2h)。
[0427]
实施例1-49、n-(5-甲基-1h-吡唑-3-基)噻吩-2-甲酰胺(pa049)的制备
[0428]
采用与制备化合物pa034类似的方法,将2-氯-5-(2-甲氧基乙氧基)苯胺替换为3-氨基-5-甲基吡唑,最终得到化合物pa049,产率68%。
[0429]1h nmr(500mhz,chloroform-d)δ8.35(dd,j=3.9,1.3hz,1h),7.73(dd,j=5.0,1.3hz,1h),7.15(dd,j=5.0,4.0hz,1h),5.61(s,2h),5.30(s,1h),2.23(s,3h)。
[0430]
实施例1-50、n-(1-甲基-1h-吡唑-4-基)噻吩-2-甲酰胺(pa050)的制备
[0431]
采用与制备化合物pa034类似的方法,将2-氯-5-(2-甲氧基乙氧基)苯胺替换为1-甲基-4-氨基吡唑,最终得到化合物pa050,产率64%。
[0432]1h nmr(500mhz,chloroform-d)δ7.98(s,1h),7.95(s,1h),7.64
–
7.59(m,1h),7.52(dd,j=5.0,1.0hz,1h),7.47(s,1h),7.10(dd,j=4.9,3.8hz,1h),3.87(s,3h)。
[0433]
实施例1-51、n-([1,1'-联苯]-3-基)-1h-1,2,4-三唑-5-甲酰胺(pa051)的制备
[0434]
采用与制备化合物pa002类似的方法,将2-噻吩甲酸替换为1h-1,2,4-三氮唑-3-羧酸,最终得到化合物pa051,产率64%。
[0435]1h nmr(500mhz,dmso-d6)δ14.64(s,1h),10.44(s,1h),8.80(s,1h),8.17(s,1h),7.88(d,j=7.4hz,1h),7.69
–
7.63(m,2h),7.54
–
7.36(m,5h)。
[0436]
实施例1-52、n-([1,1'-联苯]-3-基)噻唑-2-甲酰胺(pa052)的制备
[0437]
采用与制备化合物pa002类似的方法,将2-噻吩甲酸替换为噻唑-2-甲酸,最终得到化合物pa052,产率70%。
[0438]1h nmr(500mhz,chloroform-d)δ9.18(s,1h),8.01
–
7.96(m,1h),7.94(d,j=3.1hz,1h),7.70(ddd,j=7.9,2.0,1.1hz,1h),7.65(d,j=3.1hz,1h),7.64
–
7.61(m,2h),7.49
–
7.40(m,4h),7.39
–
7.34(m,1h)。
[0439]
实施例1-53、n-([1,1'-联苯]-3-基)噻唑-4-甲酰胺(pa053)的制备
[0440]
采用与制备化合物pa002类似的方法,将2-噻吩甲酸替换为噻唑-4-甲酸,最终得到化合物pa053,产率64%。
[0441]1h nmr(500mhz,chloroform-d)δ9.34(s,1h),8.83(d,j=2.1hz,1h),8.30(d,j=2.1hz,1h),8.00
–
7.96(m,1h),7.75
–
7.69(m,1h),7.66
–
7.61(m,2h),7.51
–
7.42(m,3h),7.41
–
7.33(m,2h)。
[0442]
实施例1-54、n-([1,1'-联苯]-3-基)-1h-吡唑-5-甲酰胺(pa054)的制备
[0443]
采用与制备化合物pa002类似的方法,将2-噻吩甲酸替换为吡唑-3-甲酸,最终得到化合物pa054,产率71%。
[0444]1h nmr(500mhz,chloroform-d)δ10.28(s,1h),8.79(s,1h),7.95(s,1h),7.69(d,j=8.0hz,1h),7.66(d,j=2.4hz,1h),7.63(d,j=7.4hz,2h),7.47
–
7.41(m,3h),7.36(dd,j=12.4,6.6hz,2h),7.00(d,j=2.3hz,1h)。
[0445]
实施例1-55、n-([1,1'-联苯]-3-基)噻唑-5-甲酰胺(pa055)的制备
[0446]
采用与制备化合物pa002类似的方法,将2-噻吩甲酸替换为噻唑-5-甲酸,最终得到化合物pa055,产率61%。
[0447]1h nmr(500mhz,chloroform-d)δ8.96(s,1h),8.40(s,1h),7.88
–
7.84(m,1h),7.80(s,1h),7.64
–
7.56(m,3h),7.49
–
7.40(m,4h),7.39
–
7.33(m,1h)。
[0448]
实施例1-56、n-([1,1'-联苯]-3-基)-1-羟基-1h-1,2,3-三唑-4-甲酰胺(pa056)的制备
[0449]
采用与制备化合物pa002类似的方法,将2-噻吩甲酸替换为1-羟基-1h-1,2,3-三唑-4-羧酸,最终得到化合物pa056,产率78%。
[0450]1h nmr(500mhz,dmso-d6)δ9.98(s,1h),8.15(s,1h),7.84(d,j=7.6hz,1h),7.65(d,j=7.3hz,2h),7.54(s,1h),7.51
–
7.44(m,2h),7.42
–
7.30(m,4h)。
[0451]
实施例1-57、n-([1,1'-联苯]-3-基)异噻唑-5-甲酰胺(pa057)的制备
[0452]
采用与制备化合物pa002类似的方法,将2-噻吩甲酸替换为1-羟基-1h-1,2,3-三唑-4-羧酸,最终得到化合物pa057,产率70%。
[0453]1h nmr(500mhz,chloroform-d)δ8.56(d,j=1.5hz,1h),7.86(s,1h),7.79(s,1h),7.64(d,j=1.5hz,1h),7.63
–
7.56(m,3h),7.49
–
7.41(m,4h),7.40
–
7.34(m,1h)。
[0454]
实施例1-58、n-(噻吩-2-基)-[1,1'-联苯]-3-甲酰胺(pa058)的制备
[0455]
将噻吩胺(99mg,1mmol),3-氨基联苯(186mg,1.1mmol),n,n-二异丙基乙胺(388mg,3mmol)和hatu(418mg,1.1mmol)溶于3ml的n,n-二甲基甲酰胺中,室温搅拌反应6h。tlc检测反应完全后,用乙酸乙酯萃取反应液,有机相用水洗涤两次,饱和食盐水洗一次,无水硫酸钠干燥。蒸干有机相后,通过柱层析分离纯化得到产物pa058(181mg,产率65%)。
[0456]1h nmr(500mhz,chloroform-d)δ8.75(dd,j=4.5,1.3hz,1h),8.55
–
8.51(m,1h),8.48(dd,j=8.4,1.3hz,1h),8.33
–
8.26(m,1h),8.02
–
7.97(m,1h),7.73
–
7.63(m,4h),7.53
–
7.45(m,3h),7.42(dd,j=8.4,6.4hz,1h)。
[0457]
实施例1-59、n-([1,1'-联苯]-3-基)异噻唑-5-甲酰胺(pa059)的制备
[0458]
采用与制备化合物pa002类似的方法,将2-噻吩甲酸替换为5-异噻唑羧酸,最终得到化合物pa059,产率71%。
[0459]1h nmr(500mhz,chloroform-d)δ8.56(d,j=1.5hz,1h),7.86(s,1h),7.79(s,1h),7.64(d,j=1.5hz,1h),7.63
–
7.56(m,3h),7.49
–
7.41(m,4h),7.40
–
7.34(m,1h)。
[0460]
实施例1-60、1-([1,1'-联苯]-3-基)-3-(噻吩-2-基)脲(pa060)的制备
[0461]
将噻吩胺(99mg,1mmol),氯甲酸苯酯(235mg,1.5mmol),碳酸钾(414mg,3mmol)溶于甲苯/水(10ml/5ml),室温反应5h。tlc检测反应完全后,用乙酸乙酯萃取反应液,有机相用水洗涤两次,饱和食盐水洗一次,无水硫酸钠干燥。蒸干有机相后,通过柱层析分离纯化得到化合物苯基噻吩-2-基氨基甲酸酯(210mg,产率96%)。
[0462]
将苯基噻吩-2-基氨基甲酸酯(210mg,0.96mmol),3-氨基联苯(178mg,1.06mmol)溶于n,n-二甲基甲酰胺(10ml)中,80℃反应2h。tlc检测反应完全后,用乙酸乙酯萃取反应液,有机相用水洗涤两次,饱和食盐水洗一次,无水硫酸钠干燥。蒸干有机相后,通过柱层析分离纯化得到产物pa060,产率70%。
[0463]1h nmr(500mhz,dmso-d6)δ8.84(s,1h),7.82(d,j=1.7hz,1h),7.66
–
7.60(m,3h),7.51
–
7.45(m,3h),7.45
–
7.38(m,3h),7.37(d,j=7.7hz,2h),7.30
–
7.24(m,1h)。
[0464]
实施例1-61、n-([1,1'-联苯]-3-基甲基)噻吩-2-甲酰胺(pa061)的制备
[0465]
采用与制备化合物pa002类似的方法,将3-氨基联苯替换为3-苯基苯甲基胺,最终得到化合物pa061,产率71%。
[0466]1h nmr(500mhz,chloroform-d)δ7.60
–
7.55(m,3h),7.52(dd,j=8.2,5.6hz,2h),7.48(d,j=5.0hz,1h),7.46
–
7.39(m,3h),7.39
–
7.32(m,2h),7.09
–
7.04(m,1h),6.34(s,1h),4.69(d,j=5.7hz,2h)。
[0467]
实施例1-62、n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻唑-5-羧酰胺(pa062)的制备
[0468]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为噻唑-5-羧酸,最终得到化合物pa062,产率74%。
[0469]1h nmr(500mhz,chloroform-d)δ8.96(s,1h),8.82(s,1h),8.50(d,j=2.5hz,1h),8.40(s,1h),7.05(dd,j=8.7,2.5hz,1h),6.93(d,j=8.7hz,1h),4.24
–
4.17(m,2h),3.76
–
3.70(m,2h),3.44(s,3h)。
[0470]
实施例1-63、n-(4-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺(pa063)的制备
[0471]
采用与制备化合物pa034类似的方法,将2-氯-5-(2-甲氧基乙氧基)苯胺替换为4-氯-6-(2-甲氧基乙氧基)苯胺,最终得到化合物pa063,产率71%。
[0472]1h nmr(500mhz,chloroform-d)δ8.64(s,1h),8.42(d,j=8.7hz,1h),7.66
–
7.61
(m,1h),7.58
–
7.53(m,1h),7.13(dd,j=4.9,3.8hz,1h),7.03(dd,j=8.7,2.2hz,1h),6.96(d,j=2.2hz,1h),4.25
–
4.19(m,2h),3.78
–
3.72(m,2h),3.43(s,3h)。
[0473]
实施例1-64、n-(3-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺(pa064)的制备
[0474]
采用与制备化合物pa034类似的方法,将2-氯-5-(2-甲氧基乙氧基)苯胺替换为3-氯-6-(2-甲氧基乙氧基)苯胺,最终得到化合物pa064,产率70%。
[0475]1h nmr(500mhz,chloroform-d)δ9.21(s,1h),8.46(p,j=3.9hz,1h),7.75(dd,j=3.7,1.1hz,1h),7.57(dd,j=5.0,1.1hz,1h),7.13(dd,j=4.9,3.8hz,1h),7.09(d,j=4.5hz,2h),4.31
–
4.26(m,2h),3.72
–
3.67(m,2h),3.31(s,3h)。
[0476]
实施例1-65、4-溴-n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2-羧酰胺(pa065)的制备
[0477]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为4-溴噻吩-2-甲酸,最终得到化合物pa065,产率70%。
[0478]1h nmr(500mhz,chloroform-d)δ8.96(s,1h),8.82(s,1h),8.50(d,j=2.5hz,1h),8.40(s,1h),7.05(dd,j=8.7,2.5hz,1h),6.93(d,j=8.7hz,1h),4.24
–
4.17(m,2h),3.76
–
3.70(m,2h),3.44(s,3h)。
[0479]
实施例1-66、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-1-甲基-1h-吡唑-3-甲酰胺(pa066)的制备
[0480]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为1-甲基吡唑-3-甲酸,最终得到化合物pa066,产率73%。
[0481]1h nmr(500mhz,chloroform-d)δ9.41(s,1h),8.60(d,j=2.5hz,1h),7.40(d,j=2.3hz,1h),6.98(dd,j=8.7,2.6hz,1h),6.87(d,j=2.3hz,1h),6.83(d,j=8.7hz,1h),4.23
–
4.18(m,2h),3.96(s,3h),3.85
–
3.80(m,2h),3.51(s,3h)。
[0482]
实施例1-67、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(甲基磺酰基)噻吩-2-甲酰胺(pa067)的制备
[0483]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为5-甲磺酰噻吩-2-羧酸,最终得到化合物pa067,产率75%。
[0484]1h nmr(500mhz,chloroform-d)δ8.89(s,1h),8.50(d,j=2.5hz,1h),7.71(d,j=4.0hz,1h),7.62(d,j=4.0hz,1h),7.07(dd,j=8.7,2.5hz,1h),6.94(d,j=8.7hz,1h),4.24
–
4.19(m,2h),3.75
–
3.69(m,2h),3.41(s,3h),3.23(s,3h)。
[0485]
实施例1-68、3-溴-n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2-羧酰胺(pa068)的制备
[0486]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为3-溴噻吩-2-甲酸,最终得到化合物pa068,产率70%。
[0487]1h nmr(500mhz,chloroform-d)δ9.70(s,1h),8.61(d,j=2.4hz,1h),7.52(dd,j=5.3,1.1hz,1h),7.10(dd,j=5.3,1.1hz,1h),7.03(dt,j=8.7,1.8hz,1h),6.83(d,j=8.7hz,1h),4.27
–
4.16(m,2h),3.83
–
3.72(m,2h),3.42(d,j=1.1hz,3h)。
[0488]
实施例1-69、n-(5-氯-2-(2-羟乙基)苯基)噻吩-2-甲酰胺(pa069)的制备
[0489]
采用与制备化合物pa034类似的方法,将2-氯-5-(2-甲氧基乙氧基)苯胺替换为2-(2-氨基-4-氯苯基)乙-1-醇,最终得到化合物pa069,产率72%。
[0490]1h nmr(500mhz,dmso-d6)δ9.31(s,1h),7.89
–
7.84(m,2h),7.67(d,j=2.2hz,1h),7.26
–
7.21(m,1h),7.03(d,j=8.3hz,1h),6.95(dd,j=8.4,2.2hz,1h),4.17
–
4.11(m,2h),3.69
–
3.63(m,2h)。
[0491]
实施例1-70、n-(5-氯-2-(戊氧基)苯基)噻吩-2-甲酰胺(pa070)的制备
[0492]
采用与制备化合物pa006类似的方法,将2-溴乙基甲基醚替换为溴代正戊烷,制备化合物4-氯-2-(戊氧基)苯胺。
[0493]
将4-氯-2-(戊氧基)苯胺(214mg,1mmol),2-羧基噻吩(141mg,1.1mmol),n,n-二异丙基乙胺(388mg,3mmol)和hatu(418mg,1.1mmol)溶于3ml的n,n-二甲基甲酰胺中,室温搅拌反应6小时。tlc检测反应完全后,用乙酸乙酯萃取反应液,有机相用水洗涤两次,饱和食盐水洗一次,无水硫酸钠干燥。蒸干有机相后,通过柱层析分离纯化得到产物pa070(233mg,产率72%)。
[0494]1h nmr(500mhz,chloroform-d)δ8.54(d,j=2.5hz,1h),8.45(s,1h),7.60(dd,j=3.7,1.0hz,1h),7.56(dd,j=5.0,1.0hz,1h),7.14(dd,j=4.9,3.8hz,1h),7.01(dd,j=8.7,2.5hz,1h),6.81(d,j=8.7hz,1h),4.06(t,j=6.5hz,2h),1.88(dt,j=14.5,6.5hz,2h),1.53
–
1.48(m,2h),1.46
–
1.40(m,2h),0.96(t,j=7.2hz,3h)。
[0495]
实施例1-71、n-(5-氯-2-乙氧基苯基)噻吩-2-甲酰胺(pa071)的制备
[0496]
采用与制备化合物pa070类似的方法,将溴代正戊烷替换为溴乙烷,最终得到化合物pa071,产率70%。
[0497]1h nmr(500mhz,chloroform-d)δ8.53(d,j=2.5hz,1h),8.45(s,1h),7.57(dd,j=17.6,4.2hz,2h),7.17
–
7.12(m,1h),7.00(dd,j=8.7,2.5hz,1h),6.80(d,j=8.7hz,1h),4.13(q,j=7.0hz,2h),1.50(t,j=7.0hz,3h)。
[0498]
实施例1-72、4-氯-2-(噻吩-2-甲酰胺基)苯基乙酸(pa072)的制备
[0499]
采用与制备化合物pa070类似的方法,将溴代正戊烷替换为乙酸酐,最终得到化合物pa072,产率81%。
[0500]1h nmr(500mhz,chloroform-d)δ8.35(s,1h),8.03(d,j=3.0hz,1h),7.77
–
7.72(m,1h),7.28(s,1h),7.25
–
7.22(m,1h),7.21(d,j=8.7hz,1h),7.13(d,j=8.2hz,1h),2.16(s,3h)。
[0501]
实施例1-73、n-(2-(2-甲氧基乙氧基)-5-甲基苯基)噻吩-2-甲酰胺(pa073)的制备
[0502]
采用与制备化合物pa034类似的方法,将2-氯-5硝基苯酚替换为2-硝基-4-甲苯酚,最终得到化合物pa073,产率73%。
[0503]1h nmr(500mhz,chloroform-d)δ7.40
–
7.36(m,2h),7.32(dd,j=5.0,1.1hz,1h),7.08
–
7.03(m,3h),6.84(dd,j=4.9,3.9hz,1h),4.64(s,3h),2.44(t,j=2.4hz,2h),2.24(t,j=2.5hz,2h),1.57(s,3h)。
[0504]
实施例1-74、n-(2-丁氧基-5-氯苯基)噻吩-2-甲酰胺(pa074)的制备
[0505]
采用与制备化合物pa070类似的方法,将溴代正戊烷替换为正溴丁烷,最终得到化合物pa074,产率81%。
[0506]1h nmr(500mhz,chloroform-d)δ8.54(d,j=2.5hz,1h),8.45(s,1h),7.60
–
7.58(m,1h),7.56(d,j=5.0hz,1h),7.15(dd,j=4.9,3.8hz,1h),7.01(dd,j=8.7,2.5hz,1h),
6.81(d,j=8.7hz,1h),4.07(t,j=6.5hz,2h),1.86(dt,j=14.4,6.5hz,2h),1.57
–
1.52(m,2h),1.03(t,j=7.4hz,3h)。
[0507]
实施例1-75、n-(5-氯-2-丙氧基苯基)噻吩-2-甲酰胺(pa075)的制备
[0508]
采用与制备化合物pa070类似的方法,将溴代正戊烷替换为溴代正丙烷,最终得到化合物pa075,产率81%。
[0509]1h nmr(500mhz,chloroform-d)δ8.56(d,j=2.5hz,1h),8.49(s,1h),7.62(dd,j=3.7,1.0hz,1h),7.58(dd,j=5.0,1.0hz,1h),7.17(dd,j=4.9,3.8hz,1h),7.03(dd,j=8.7,2.6hz,1h),6.83(d,j=8.7hz,1h),4.05(t,j=6.5hz,2h),1.93(h,j=7.3hz,2h),1.14(t,j=7.4hz,3h)。
[0510]
实施例1-76、n-(5-氯-2-(3-甲氧基丙氧基)苯基)噻吩-2-甲酰胺(pa076)的制备
[0511]
采用与制备化合物pa070类似的方法,将溴代正戊烷替换为1-溴-3-甲氧基丙烷,最终得到化合物pa076,产率74%。
[0512]1h nmr(500mhz,chloroform-d)δ8.53(d,j=2.5hz,1h),8.52(s,1h),7.62(dd,j=3.7,1.1hz,1h),7.56(dd,j=5.0,1.1hz,1h),7.14(dd,j=5.0,3.8hz,1h),7.01(dd,j=8.7,2.6hz,1h),6.83(d,j=8.7hz,1h),4.17(t,j=6.2hz,2h),3.60(t,j=5.9hz,2h),3.33(s,3h),2.13(p,j=6.1hz,2h)。
[0513]
实施例1-77、n-(5-氯-2-(2-乙氧基乙氧基)苯基)噻吩-2-甲酰胺(pa077)的制备
[0514]
采用与制备化合物pa070类似的方法,将溴代正戊烷替换为2-溴乙基乙基醚,最终得到化合物pa077,产率71%。
[0515]1h nmr(500mhz,chloroform-d)δ8.68(s,1h),8.54(d,j=2.5hz,1h),7.65(dd,j=3.7,1.1hz,1h),7.56(dd,j=5.0,1.1hz,1h),7.13(dd,j=5.0,3.8hz,1h),7.01(dd,j=8.7,2.6hz,1h),6.88(d,j=8.7hz,1h),4.24
–
4.19(m,2h),3.82
–
3.74(m,2h),3.59(q,j=7.0hz,2h),1.21(t,j=7.0hz,3h)。
[0516]
实施例1-78、n-(5-氯-2-(2-羟基乙氧基)苯基)噻吩-2-甲酰胺(pa078)的制备
[0517]
采用与制备化合物pa070类似的方法,将溴代正戊烷替换为2-溴乙醇,最终得到化合物pa078,产率76%。
[0518]1h nmr(500mhz,chloroform-d)δ8.61(s,1h),8.49(d,j=2.4hz,1h),7.65(dd,j=3.7,1.2hz,1h),7.54(dd,j=5.0,1.2hz,1h),7.12(dd,j=5.0,3.7hz,1h),7.02(dd,j=8.7,2.5hz,1h),6.88(d,j=8.8hz,1h),4.24
–
4.14(m,2h),4.06
–
3.96(m,2h),1.95(s,1h)。
[0519]
实施例1-79、n-(5-氯-2-(2,2,2-三氟乙氧基)苯基)噻吩-2-甲酰胺(pa079)的制备
[0520]
采用与制备化合物pa070类似的方法,将溴代正戊烷替换为一溴三氟乙烷,最终得到化合物pa079,产率76%。
[0521]1h nmr(500mhz,chloroform-d)δ8.65(s,1h),8.52(d,j=2.5hz,1h),7.65(dd,j=3.7,1.1hz,1h),7.56(dd,j=5.0,1.1hz,1h),7.12(dd,j=5.0,3.8hz,1h),7.01(dd,j=8.7,2.6hz,1h),6.88(d,j=8.8hz,1h),4.78(q,j=8.5hz,2h)。
[0522]
实施例1-80、n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻唑-2-羧酰胺(pa080)的制备
[0523]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为噻唑-2-羧酸,最终得到化合物pa080,产率68%。
[0524]1h nmr(500mhz,chloroform-d)δ8.96(s,1h),8.82(s,1h),8.50(d,j=2.5hz,1h),8.40(s,1h),7.05(dd,j=8.7,2.5hz,1h),6.93(d,j=8.7hz,1h),4.24
–
4.17(m,2h),3.76
–
3.70(m,2h),3.44(s,3h)。
[0525]
实施例1-81、n-(5-氯-2-(庚氧基)苯基)噻吩-2-甲酰胺(pa081)的制备
[0526]
采用与制备化合物pa070类似的方法,将溴代正戊烷替换为1-溴代庚烷,最终得到化合物pa081,产率63%。
[0527]1h nmr(500mhz,chloroform-d)δ8.53(d,j=2.5hz,1h),8.45(s,1h),7.59(dd,j=3.7,1.1hz,1h),7.56(dd,j=5.0,1.1hz,1h),7.14(dd,j=4.9,3.8hz,1h),7.00(dd,j=8.7,2.6hz,1h),6.80(d,j=8.7hz,1h),4.06(t,j=6.4hz,2h),1.87(dt,j=14.4,6.5hz,2h),1.55
–
1.45(m,2h),1.43
–
1.36(m,2h),1.35
–
1.29(m,4h),0.95
–
0.87(m,3h)。
[0528]
实施例1-82、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-6-乙炔基烟酰胺(pa082)的制备
[0529]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为6-乙炔基烟酸,最终得到化合物pa082,产率71%。
[0530]1h nmr(500mhz,chloroform-d)δ9.23(dd,j=2.3,0.9hz,1h),9.08(s,1h),8.56(d,j=2.5hz,1h),8.42(dd,j=8.1,2.2hz,1h),7.85(dd,j=8.1,0.8hz,1h),7.09(dd,j=8.7,2.5hz,1h),6.97(d,j=8.6hz,1h),4.27
–
4.17(m,2h),4.12(q,j=7.1hz,1h),3.79
–
3.66(m,2h),3.39(s,3h)。
[0531]
实施例1-83、4-氯-2-(噻吩-2-甲酰胺基)苯甲酸甲酯(pa083)的制备
[0532]
采用与制备化合物pa034类似的方法,将2-氯-5-(2-甲氧基乙氧基)苯胺替换为甲基2-胺-4-氯苯酚酯,最终得到化合物pa083,产率76%。
[0533]1h nmr(500mhz,chloroform-d)δ8.35(s,1h),8.03(d,j=3.0hz,1h),7.77
–
7.72(m,1h),7.28(s,1h),7.25
–
7.22(m,1h),7.21(d,j=8.7hz,1h),7.13(d,j=8.2hz,1h),3.96(s,3h)。
[0534]
实施例1-84、n-(2-(2-甲氧基乙基)苯基)噻吩-2-甲酰胺(pa084)的制备
[0535]
采用与制备化合物pa034类似的方法,将2-氯-5-(2-甲氧基乙氧基)苯胺替换为2-(2-甲氧基乙基)苯胺,最终得到化合物pa084,产率74%。
[0536]1h nmr(500mhz,chloroform-d)δ9.77(s,1h),8.01(d,j=8.0hz,1h),7.64(dd,j=3.7,1.0hz,1h),7.53(dd,j=5.0,1.1hz,1h),7.33
–
7.26(m,1h),7.18(dd,j=7.6,1.5hz,1h),7.15
–
7.07(m,2h),3.77
–
3.71(m,2h),3.45(s,3h),2.95
–
2.89(m,2h)。
[0537]
实施例1-85、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(环丙烷甲酰胺基)噻吩-2-甲酰胺(pa085)的制备
[0538]
采用与制备化合物pa028类似的方法,将氯乙酰氯替换为环丙基甲酰氯,最终得到化合物pa085,产率74%。
[0539]1h nmr(500mhz,chloroform-d)δ8.57(s,1h),8.53(d,j=2.5hz,1h),8.35(s,1h),7.46(d,j=4.1hz,1h),6.98(dd,j=8.7,2.5hz,1h),6.87(d,j=8.6hz,1h),6.65(d,j=4.1hz,1h),4.22
–
4.15(m,2h),3.75
–
3.70(m,2h),3.43(s,3h),1.71
–
1.65(m,1h),1.20
–
1.14(m,2h),0.95
–
0.92(m,2h)。
[0540]
实施例1-86、n-(5-氯-2-(丙-2-炔-1-基氧基)苯基)噻吩-2-甲酰胺(pa086)的制
备
[0541]
采用与制备化合物pa070类似的方法,将溴代正戊烷替换为3-溴丙炔,最终得到化合物pa086,产率74%。
[0542]1h nmr(500mhz,chloroform-d)δ7.41
–
7.35(m,2h),7.32(dd,j=5.0,1.1hz,1h),7.08
–
7.02(m,3h),6.84(dd,j=4.9,3.9hz,1h),4.64(s,2h),2.44(t,j=2.4hz,1h)。
[0543]
实施例1-87、(5-((5-氯-2-(2-甲氧基乙氧基)苯基氨基甲酰基)噻吩-2-羰基)甘氨酸(pa087)的制备
[0544]
采用与制备化合物pa023类似的方法,将3-氨基-1-丙醇替换为甘氨酸,最终得到化合物pa087,产率69%。
[0545]1h nmr(500mhz,dmso-d6)δ9.63(s,1h),8.99
–
8.96(m,1h),7.90(d,j=3.8hz,1h),7.88
–
7.82(m,2h),7.25
–
7.15(m,2h),4.21
–
4.17(m,2h),3.89
–
3.84(m,2h),3.70
–
3.66(m,2h),3.28(s,3h)。
[0546]
实施例1-88、n-(5-甲氧基-2-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺(pa088)的制备
[0547]
采用与制备化合物pa034类似的方法,将2-氯-5-(2-甲氧基乙氧基)苯胺替换为5-甲氧基-2-(2-甲氧基乙基)苯胺,最终得到化合物pa088,产率70%。
[0548]1h nmr(500mhz,chloroform-d)δ8.89(s,1h),8.21(d,j=3.0hz,1h),7.68(dd,j=3.7,1.1hz,1h),7.55(dd,j=5.0,1.1hz,1h),7.13(dd,j=4.9,3.8hz,1h),6.93(d,j=8.9hz,1h),6.59(dd,j=8.9,3.0hz,1h),4.19
–
4.14(m,2h),3.81(s,3h),3.71
–
3.65(m,2h),3.39(s,3h)。
[0549]
实施例1-89、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-甲氧基吡嗪-2-羧酰胺(pa089)的制备
[0550]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为5-甲氧基吡嗪-2-羧酸,最终得到化合物pa089,产率70%。
[0551]1h nmr(500mhz,chloroform-d)δ10.20(s,1h),9.01(d,j=1.3hz,1h),8.65(d,j=2.5hz,1h),8.15(d,j=1.3hz,1h),7.03(dd,j=8.7,2.6hz,1h),6.86(d,j=8.7hz,1h),4.25
–
4.20(m,2h),4.07(s,3h),3.82(dd,j=5.3,3.9hz,2h),3.49(s,3h)。
[0552]
实施例1-90、n-(5-溴-2-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺(pa090)的制备
[0553]
采用与制备化合物pa034类似的方法,将2-氯-5-(2-甲氧基乙氧基)苯胺替换为5-溴-2-(2-甲氧基乙氧基)苯胺,最终得到化合物pa090,产率76%。
[0554]1h nmr(500mhz,chloroform-d)δ8.72(s,1h),8.69(d,j=2.4hz,1h),7.65(dd,j=3.7,1.0hz,1h),7.56(dd,j=5.0,1.0hz,1h),7.19
–
7.11(m,2h),6.86
–
6.82(m,1h),4.23
–
4.18(m,2h),3.76
–
3.71(m,2h),3.42(s,3h)。
[0555]
实施例1-91、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-4-苯基噻唑-2-羧酰胺(pa091)的制备
[0556]
采用与制备化合物pa006类似的方法,将5-甲氧基吡啶甲酸替换为4-苯基噻唑-2-羧酸,最终得到化合物pa091,产率70%。
[0557]1h nmr(500mhz,chloroform-d)δ9.98(s,1h),8.59(d,j=2.5hz,1h),8.01
–
7.95(m,2h),7.78(s,1h),7.50
–
7.43(m,2h),7.43
–
7.36(m,1h),7.06(dd,j=8.7,2.5hz,1h),
二甲酰胺(pa096)的制备
[0571]
采用与制备化合物pa031类似的方法,将n-(5-氨基戊基)氨基甲酸叔丁酯替换为2-[2-(2-氨基乙氧基)乙氧基]乙基氨基甲酸叔丁酯n-boc-3,6-二氧杂-1,8-辛二胺,最终得到化合物pa096,产率62%。
[0572]1h nmr(500mhz,dmso-d6)δ9.60(s,1h),8.84
–
8.77(m,1h),7.88(d,j=3.2hz,2h),7.85
–
7.74(m,2h),7.27
–
7.17(m,2h),6.42(s,1h),6.37(s,1h),4.34
–
4.28(m,1h),4.22
–
4.18(m,2h),4.15
–
4.10(m,1h),3.69(t,j=4.6hz,2h),3.56
–
3.51(m,4h),3.44
–
3.37(m,4h),3.37
–
3.32(m,2h),3.29(s,3h),3.18(q,j=5.9hz,2h),3.12
–
3.06(m,1h),2.81(dd,j=12.4,5.1hz,1h),2.61
–
2.55(m,1h),2.06(t,j=7.5hz,2h),1.65
–
1.41(m,4h),1.32
–
1.22(m,2h)。
[0573]
实施例1-97、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(6-(噻吩-2-甲酰胺基)六氨基)噻吩-2-甲酰胺(pa097)的制备
[0574]
采用与制备化合物pa031类似的方法,将d-生物素替换为噻吩-2-羧酸,最终得到化合物pa097,产率71%。
[0575]1h nmr(500mhz,chloroform-d)δ9.51(s,1h),8.63(s,1h),8.50
–
8.34(m,1h),7.59
–
7.54(m,1h),7.45(dd,j=5.9,4.4hz,2h),7.07(dd,j=5.0,3.7hz,1h),7.05
–
6.99(m,1h),6.99
–
6.93(m,1h),6.72(d,j=4.1hz,1h),6.51(t,j=5.9hz,1h),4.22(dd,j=5.3,3.8hz,2h),3.80
–
3.67(m,2h),3.44(s,3h),2.43(t,j=7.2hz,2h),1.86
–
1.71(m,2h),1.47
–
1.19(m,4h),0.98
–
0.82(m,2h)。
[0576]
实施例1-98、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(6-(2-苯基乙酰胺基)六氨基)噻吩-2-羧酰胺(pa098)的制备
[0577]
采用与制备化合物pa031类似的方法,将d-生物素替换为苯乙酸,最终得到化合物pa098,产率75%。
[0578]1h nmr(500mhz,chloroform-d)δ9.41(s,1h),8.61(s,1h),8.49
–
8.38(m,1h),7.46(d,j=4.1hz,1h),7.37
–
7.26(m,3h),7.26
–
7.20(m,2h),7.07
–
6.99(m,2h),6.99
–
6.92(m,1h),6.70(d,j=4.1hz,1h),4.25
–
4.19(m,2h),3.79
–
3.71(m,2h),3.56(s,2h),3.44(s,3h),3.22(q,j=6.8hz,2h),2.38(t,j=7.3hz,2h),1.73(p,j=7.4hz,2h),1.47(p,j=7.2hz,2h),0.95
–
0.83(m,2h)。
[0579]
实施例1-99、n
2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-(2-(2-(2-(2-(2-苯基乙酰胺基)乙氧基)乙氧基)乙基)噻吩-2,5-二甲酰胺(pa099)的制备
[0580]
采用与制备化合物pa098类似的方法,将n-(5-氨基戊基)氨基甲酸叔丁酯替换为2-(2-(2-氨基乙氧基)乙氧基)乙基氨基甲酸叔丁酯,最终得到化合物pa099,产率70%。
[0581]1h nmr(500mhz,chloroform-d)δ8.80(s,1h),8.51(d,j=2.5hz,1h),7.61
–
7.54(m,2h),7.37
–
7.25(m,4h),7.25(s,1h),7.04(dd,j=8.6,2.6hz,1h),6.95
–
6.83(m,2h),5.99(s,1h),4.24
–
4.18(m,2h),3.75
–
3.69(m,2h),3.62(d,j=2.6hz,4h),3.57(s,6h),3.53(t,j=5.3hz,2h),3.47
–
3.40(m,2h),3.41(s,3h)。
[0582]
实施例1-100、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(6-(2-(噻吩-2-基)乙酰氨基)六氨基)噻吩-2-甲酰胺(pa100)的制备
[0583]
采用与制备化合物pa098类似的方法,将苯乙酸替换为2-噻吩乙酸,最终得到化合
物pa100,产率71%。
[0584]1h nmr(500mhz,chloroform-d)δ9.33(s,1h),8.59(s,1h),8.52(d,j=2.5hz,1h),7.46(d,j=4.1hz,1h),7.23(dd,j=5.2,1.2hz,1h),7.01
–
6.95(m,2h),6.92(d,j=3.1hz,1h),6.87(d,j=8.6hz,1h),6.72(d,j=4.2hz,1h),5.86(s,1h),4.21
–
4.14(m,2h),3.77(s,2h),3.75
–
3.71(m,2h),3.44(s,3h),3.25(q,j=6.7hz,2h),2.41(t,j=7.3hz,2h),1.75(p,j=7.4hz,2h),1.50(p,j=7.2hz,2h),0.96
–
0.83(m,2h)。
[0585]
实施例1-101、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(6-(3-(4-氟苯基)丙酰胺基)己酰胺基)噻吩-2-甲酰胺(pa101)的制备
[0586]
采用与制备化合物pa098类似的方法,将苯乙酸替换为3-(4-氟苯基)丙酸,最终得到化合物pa101,产率75%。
[0587]1h nmr(500mhz,chloroform-d)δ9.09(s,1h),8.59(s,1h),8.53(d,j=2.5hz,1h),7.46(d,j=4.2hz,1h),7.16
–
7.09(m,2h),7.01
–
6.91(m,3h),6.88(d,j=8.7hz,1h),6.72(d,j=4.2hz,1h),5.61(s,1h),4.23
–
4.17(m,2h),3.80
–
3.66(m,2h),3.43(s,3h),3.22(q,j=6.7hz,2h),2.92(t,j=7.5hz,2h),2.43(dt,j=19.5,7.4hz,4h),1.78
–
1.70(m,2h),1.51
–
1.43(m,2h),0.95
–
0.89(m,2h)。
[0588]
实施例1-102、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(6-(4-(噻吩-2-基)丁酰胺基)六氨基)噻吩-2-甲酰胺(pa102)的制备
[0589]
采用与制备化合物pa098类似的方法,将苯乙酸替换为4-(噻吩-2-基)丁酸,最终得到化合物pa102,产率69%。
[0590]1h nmr(500mhz,dmso-d6)δ11.50(s,1h),9.11(s,1h),8.00(d,j=2.3hz,1h),7.78(t,j=5.6hz,1h),7.65(d,j=4.1hz,1h),7.29(dd,j=5.1,1.2hz,1h),7.21
–
7.09(m,2h),6.93(dd,j=5.1,3.4hz,1h),6.85
–
6.79(m,1h),6.68(d,j=4.1hz,1h),4.25
–
4.13(m,2h),3.74
–
3.63(m,2h),3.31(s,3h),3.03(q,j=6.6hz,2h),2.76(t,j=7.6hz,2h),2.37(t,j=7.4hz,2h),2.10(t,j=7.4hz,2h),1.81(t,j=7.5hz,2h),1.68
–
1.53(m,2h),1.41(p,j=7.1hz,2h),1.33
–
1.16(m,2h)。
[0591]
实施例1-103、2-氯-n-(6-((5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-基)氨基)-6-氧己基)嘧啶-5-羧酰胺(pa103)的制备
[0592]
采用与制备化合物pa098类似的方法,将苯乙酸替换为2-氯嘧啶-5-羧酸,最终得到化合物pa103,产率69%。
[0593]1h nmr(500mhz,dmso-d6)δ11.52(dd,j=12.2,6.5hz,1h),9.24
–
9.02(m,2h),8.90
–
8.65(m,1h),7.99(d,j=7.0hz,1h),7.65(dd,j=9.5,4.3hz,1h),7.16(d,j=3.0hz,2h),6.75
–
6.62(m,2h),4.20(t,j=4.6hz,2h),3.69(dd,j=5.9,3.1hz,2h),3.30(d,j=2.0hz,3h),2.40(p,j=7.2hz,2h),1.73
–
1.45(m,4h),1.34(td,j=17.8,16.4,7.1hz,2h),1.28
–
1.15(m,2h)。
[0594]
实施例1-104、3-溴-n-(6-((5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-基)氨基)-6-氧己基)呋喃-2-羧酰胺(pa104)的制备
[0595]
采用与制备化合物pa098类似的方法,将苯乙酸替换为3-溴-2-呋喃甲酸,最终得到化合物pa104,产率78%。
[0596]1h nmr(500mhz,chloroform-d)δ9.18(s,1h),8.58(s,1h),8.53(d,j=2.5hz,
1h),7.46(d,j=4.2hz,1h),7.43(d,j=1.9hz,1h),6.98(dd,j=8.6,2.5hz,1h),6.87(d,j=8.6hz,1h),6.73(d,j=4.2hz,1h),6.61(d,j=6.5hz,1h),6.57(d,j=1.9hz,1h),4.23
–
4.17(m,2h),3.76
–
3.70(m,2h),3.44(s,3h),2.45(t,j=7.4hz,2h),1.82(p,j=7.5hz,2h),1.65(s,2h),1.51
–
1.37(m,2h),1.39
–
1.17(m,2h)。
[0597]
实施例1-105、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(6-(4-氯-2-甲基苯甲酰胺基)六氨基)噻吩-2-甲酰胺(pa105)的制备
[0598]
采用与制备化合物pa098类似的方法,将苯乙酸替换为4-氯-2-甲基苯甲酸,最终得到化合物pa105,产率71%。
[0599]1h nmr(500mhz,chloroform-d)δ9.45(s,1h),8.58(s,1h),8.53
–
8.44(m,1h),7.40(d,j=4.1hz,1h),7.23(d,j=8.2hz,1h),7.17(s,1h),7.11(s,1h),6.98(dd,j=8.6,2.5hz,1h),6.87(d,j=8.7hz,1h),6.64(d,j=4.2hz,1h),6.18(s,1h),4.23
–
4.15(m,2h),3.79
–
3.66(m,2h),3.42(s,3h),2.45(t,j=7.3hz,2h),2.38(s,3h),1.80(d,j=8.0hz,2h),1.66(d,j=7.5hz,2h),1.43(dt,j=21.0,7.4hz,2h),1.38
–
1.19(m,2h)。
[0600]
实施例1-106、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(6-(3-(噻吩-2-基)丙酰胺基)六氨基)噻吩-2-甲酰胺(pa106)的制备
[0601]
采用与制备化合物pa098类似的方法,将苯乙酸替换为(噻吩-2-基)丙酸,最终得到化合物pa106,产率70%。
[0602]1h nmr(500mhz,chloroform-d)δ9.45(s,1h),8.58(s,1h),8.53
–
8.44(m,1h),7.40(d,j=4.1hz,1h),7.23(d,j=8.2hz,1h),7.17(s,1h),7.11(s,1h),6.98(dd,j=8.6,2.5hz,1h),6.87(d,j=8.7hz,1h),6.64(d,j=4.2hz,1h),6.18(s,1h),4.23
–
4.15(m,2h),3.79
–
3.66(m,2h),3.42(s,3h),2.45(t,j=7.3hz,2h),2.38(s,3h),1.80(d,j=8.0hz,2h),1.66(d,j=7.5hz,2h),1.43(dt,j=21.0,7.4hz,2h),1.38
–
1.19(m,2h)。
[0603]
实施例1-107、n
2-(5-氯-2-(2-甲氧基乙氧基)苯基)-n
5-(6-((5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-基)氨基)-6-氧己基)噻吩-2,5-二甲酰胺(pa107)的制备
[0604]
采用与制备化合物pa098类似的方法,将苯乙酸替换为5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-羧酸,最终得到化合物pa107,产率71%。
[0605]1h nmr(500mhz,dmso-d6)δ11.47(s,1h),9.55(s,1h),9.06(s,1h),8.68(d,j=7.5hz,1h),7.96
–
7.82(m,2h),7.77(d,j=4.1hz,1h),7.62(d,j=4.2hz,1h),7.29
–
7.15(m,2h),7.15
–
7.06(m,2h),7.03
–
6.91(m,1h),6.68(d,j=4.1hz,1h),4.18(q,j=5.0hz,4h),3.68(dt,j=6.2,3.0hz,4h),3.36
–
3.21(m,6h),2.39(q,j=9.9,8.6hz,2h),1.68
–
1.61(m,2h),1.56(t,j=7.7hz,2h),1.41
–
1.31(m,2h),1.28
–
1.14(m,2h)。
[0606]
实施例1-108、n-(6-((5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-基)氨基)-6-氧己基)苯并呋喃-2-羧酰胺(pa108)的制备
[0607]
采用与制备化合物pa098类似的方法,将苯乙酸替换为苯并呋喃-2-羧酸,最终得到化合物pa108,产率73%。
[0608]1h nmr(500mhz,dmso-d6)δ11.47(s,1h),9.55(s,1h),9.06(s,1h),8.68(d,j=7.5hz,1h),7.96
–
7.82(m,2h),7.77(d,j=4.1hz,1h),7.62(d,j=4.2hz,1h),7.29
–
7.15(m,2h),7.15
–
7.06(m,2h),7.03
–
6.91(m,1h),6.68(d,j=4.1hz,1h),4.18(q,j=5.0hz,
4h),3.68(dt,j=6.2,3.0hz,4h),3.36
–
3.21(m,6h),2.39(q,j=9.9,8.6hz,2h),1.68
–
1.61(m,2h),1.56(t,j=7.7hz,2h),1.41
–
1.31(m,2h),1.28
–
1.14(m,2h)。
[0609]
实施例1-109、n-(6-((5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-基)氨基)-6-氧己基)噻唑-5-羧酰胺(pa109)的制备
[0610]
采用与制备化合物pa098类似的方法,将苯乙酸替换为噻唑-5-羧酸,最终得到化合物pa109,产率73%。
[0611]1h nmr(500mhz,chloroform-d)δ8.88(s,1h),8.84(s,1h),8.62(s,1h),8.50(d,j=2.5hz,1h),8.31(s,1h),7.46(d,j=4.1hz,1h),6.99(dd,j=8.7,2.6hz,1h),6.88(d,j=8.7hz,1h),6.70(d,j=4.1hz,1h),6.51(s,1h),4.20(d,j=2.7hz,2h),3.78
–
3.69(m,2h),3.52
–
3.45(m,2h),3.43(s,3h),2.47(t,j=7.2hz,2h),1.80(q,j=7.5hz,2h),1.70
–
1.64(m,4h)。
[0612]
实施例1-110、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(6-(2-(吡啶-2-基)乙酰氨基)六氨基)噻吩-2-甲酰胺(pa110)的制备
[0613]
采用与制备化合物pa098类似的方法,将苯乙酸替换为2-吡啶基乙酸,最终得到化合物pa110,产率71%。
[0614]1h nmr(500mhz,chloroform-d)δ9.33(s,1h),8.58(s,1h),8.57
–
8.50(m,2h),7.67(td,j=7.7,1.8hz,1h),7.48(d,j=4.2hz,1h),7.43(d,j=16.4hz,1h),7.26
–
7.18(m,2h),6.98(dd,j=8.7,2.5hz,1h),6.88(d,j=8.7hz,1h),6.73(d,j=4.1hz,1h),4.20(d,j=5.0hz,2h),3.75
–
3.72(m,2h),3.72(s,2h),3.44(s,3h),3.28(q,j=6.6hz,2h),2.41(t,j=7.3hz,2h),1.77(p,j=7.4hz,2h),1.57
–
1.50(m,2h),1.46
–
1.37(m,2h)。
[0615]
实施例1-111、n-(6-((5-((5-氯-2-(2-甲氧基乙氧基)苯基)氨基甲酰基)噻吩-2-基)氨基)-6-氧己基)-1h-吡唑-5-羧酰胺(pa111)的制备
[0616]
采用与制备化合物pa098类似的方法,将苯乙酸替换为1h-吡唑-5-羧酸,最终得到化合物pa111,产率71%。
[0617]1h nmr(600mhz,dmso-d6)δ13.17(s,1h),11.50(s,1h),9.11(s,1h),8.08(t,j=6.1hz,1h),8.00(d,j=2.3hz,1h),7.79(t,j=1.8hz,1h),7.64(d,j=4.2hz,1h),7.17
–
7.14(m,2h),6.68(d,j=4.2hz,1h),6.60(t,j=2.2hz,1h),4.25
–
4.12(m,2h),3.76
–
3.59(m,2h),3.31(s,3h),3.22(p,j=6.5hz,2h),2.42
–
2.35(m,2h),1.63(p,j=7.5hz,2h),1.52(p,j=7.4hz,2h),1.32(dd,j=15.1,7.5hz,2h)。
[0618]
实施例1-112、5-(6-(2-(1h-四唑-1-基)乙酰氨基)六氨基)-n-(5-氯-2-(2-甲氧基乙氧基)苯基)噻吩-2-甲酰胺(pa112)的制备
[0619]
采用与制备化合物pa098类似的方法,将苯乙酸替换为四氮唑乙酸,最终得到化合物pa112,产率77%。
[0620]1h nmr(500mhz,dmso-d6)δ11.52(s,1h),9.35(s,1h),9.12(s,1h),8.42(t,j=5.6hz,1h),7.99(d,j=2.2hz,1h),7.65(d,j=4.3hz,1h),7.28
–
7.05(m,2h),6.69(d,j=4.2hz,1h),5.21(s,2h),4.25
–
4.14(m,2h),3.74
–
3.64(m,2h),3.31(s,3h),3.11(d,j=6.3hz,2h),2.39(t,j=7.5hz,2h),1.69
–
1.57(m,2h),1.52
–
1.39(m,2h),1.32(tt,j=9.5,6.1hz,2h)。
[0621]
实施例1-113、n-(5-氯-2-(2-甲氧基乙氧基)苯基)-5-(6-(4-苯基丁酰胺基)六氨
基)噻吩-2-羧酰胺(pa113)的制备
[0622]
采用与制备化合物pa098类似的方法,将苯乙酸替换为4-苯基丁酸,最终得到化合物pa113,产率71%。
[0623]1h nmr(500mhz,chloroform-d)δ9.54(s,1h),8.68
–
8.44(m,2h),7.45(d,j=4.1hz,1h),7.26(t,j=7.5hz,2h),7.16(dd,j=19.7,7.3hz,3h),7.00
–
6.95(m,1h),6.87(d,j=8.6hz,1h),6.73(d,j=4.1hz,1h),5.88
–
5.59(m,1h),4.29
–
4.10(m,2h),3.85
–
3.65(m,2h),3.43(d,j=0.8hz,3h),3.24(q,j=6.7hz,2h),2.63(t,j=7.5hz,2h),2.43(t,j=7.3hz,2h),2.18(t,j=7.6hz,2h),1.96(p,j=7.5hz,2h),1.76(p,j=7.4hz,2h),1.51(q,j=7.2hz,2h),1.35(p,j=7.3,6.9hz,2h)。
[0624]
表1实施例1-113(pa001-113)所示化合物制备汇总
[0625]
[0626]
[0627]
[0628]
[0629]
[0630]
[0631]
[0632]
[0633]
[0634]
[0635]
[0636]
[0637]
[0638][0639]
本发明的化合物可使用多种试验来鉴定;最初的筛选鉴定了刺激人间充质干细胞(hmscs)以发展成软骨细胞结节的化合物。
[0640]
实施例二:生物实验
[0641]
实施例2-1、细胞的培养与分化
[0642]
选用人骨髓间充质干细胞(hbmscs),脐带间充质干细胞(hucmscs)与脂肪间充质干细胞(hadmscs)。在间充质干细胞生长培养基(mscgm)中培养,培养获得的状态良好的2-8代间充质干细胞可用于实验。使用荧光激活细胞分选法对细胞进行分选,并证明其对cd29,cd44,cd166和cd105的阳性率》98%,对cd45的阳性率《0.1%。
[0643]
实施例2-2、免疫细胞化学染色与定量
[0644]
为让mscs向软骨分化,将5000个细胞/孔在corning 384孔板中铺板。24小时后,除去mscgm并且用25μl包含1%fbs的dmem替换。然后向每个孔中加入所示剂量的测试化合物。使培养物在37℃生长7天。
[0645]
为检测潜在的促进向软骨分化的蛋白,用4%pfa固定细胞15分钟,用包含0.1%的triton x-100、0.25g/ml的胶原酶2的pbs渗透10分钟,在室温用包含5%bsa的pbst封闭1小时,然后再4℃与包含1%bsa的pbs中的ii型胶原蛋白抗体一起温浴过夜。用pbs将细胞洗涤3次,在室温与荧光团缀合的二级抗体一起温浴1小时,然后用pbs洗涤3次,再与dapi一起孵育3分钟,然后用pbs洗涤3次。使用imagexpress micro根据高容量推定定量。使用专用多波长细胞评分脚本进行数据分析,计算本发明实施例一制备的化合物刺激ii型胶原蛋白表达水平。
[0646]
在化合物活性评价上,使用阴性对照(dmso)作为mscs成软骨分化的基础水平。选择显示出染色强度相比阴性对照增加30%或更多本发明实施例一制备的的化合物作为活性命中物。代表性数据在表1中示出(a:与阴性对照相比染色强度增加》200%;b:与阴性对照相比染色强度增加100-200%;c:与阴性对照相比染色强度增加30-100%;d:与阴性对照相比染色强度增加《30%)
[0647]
结果如表2所示,绝大部分本发明实施例一制备的化合物都能够显著促进间充质干细胞中ii型胶原蛋白的表达,多个化合物表现出在10μm浓度下活性优于阳性化合物kgn。这些结果表明本发明实施例一制备的化合物能够诱导间充质干细胞成软骨分化。
[0648]
表2.本发明化合物在诱导软骨发生中的活性
[0649]
[0650][0651]
实施例三:动物实验
[0652]
实施例3-1c57小鼠手术诱发急性损伤骨关节炎模型
[0653]
在oa的小鼠急性损伤手术,即内侧半月板不稳定手术(dmm)模型中,该方法通过对c57小鼠(每组小鼠个数n=7)通过手术切断右膝盖前十字韧带(acl),内侧半月板胫骨韧带(mmtl),内侧副韧带(mcl),造成膝关节的失稳从而损伤关节软骨,导致oa的表型形成。为评价代测化合物促软骨修复能力,实验共分为四组,依次为sham假手术组(仅切开皮肤未伤害关节韧带),阴性对照(关节腔注射pbs),kgn给药组(kgn溶于生理盐水,配成33μm溶液,进行关节腔注射),代测化合物pa002给药组(代测化合物溶于生理盐水,配成33μm溶液,进行关节腔注射)。在术后3天,各组进行关节腔注射给药,每周注射一次。在6周后,处死小鼠,取出关节样本,进行包埋切片,观察组织学改善情况并进行统计分析。
[0654]
结果如图1所示,从中可以发现本发明化合物pa002在给药33μm剂量下能够显著逆转软骨损伤的进程,关节评分结果pa002表现出更好的软骨修复效果,并有明显的统计学意义。在对小鼠的行为学测痛实验中,pa002给药组的小鼠表现出很好的应对术后骨关节炎引起的疼痛,且效果优于kgn给药组。表明pa002能够很好的减缓骨关节炎引起的疼痛。
[0655]
实施例3-2c57小鼠关节软骨缺损骨关节炎模型
[0656]
用1ml一次性无菌注射器针头(26g)诱发软骨损伤,针头提前打磨使其变钝,将10μl透明枪头套在上述针头上,使尖端露出1毫米。手术前将针头暴露于紫外线辐射15分钟灭菌。小鼠生长到4周,开始进行手术,使用阿弗丁(220μl/15g)麻醉雄性c57bl/6小鼠。用棉球擦拭75%的酒精对后肢及手术桌面进行消毒,尽量减轻手术过程中小鼠的痛苦。用外科手术刀在股骨近端内侧切开长度略小于1cm的皮肤切口及肌肉层,将关节囊打开,把髌骨移到侧面,然后将关节完全弯曲以露出滑车沟的关节面。使用上述针头在髌骨沟中造成纵向软骨损伤,将针尖放在髌骨凹槽的前面,并沿股骨的整个长度轻轻移动,通过软骨损伤部位的出血来确认穿透到软骨下骨。用小鼠缝合线将关节囊和皮肤缝合。对侧膝关节不做手术(假手术对照组)。将小鼠放置在37摄氏度恒温加热板上,苏醒后放入鼠笼继续放在spf级屏障环境中饲养7、10、14天。实验共分为四组(每组小鼠个数n=7),依次为假手术组,pbs组,kgn给药组与待测化合物pa002给药组。两组给药组均将药物用生理盐水配成33μm的浓度用于关节腔注射。造模完成3天后,进行关节腔注射给药,每周一次。4周后,采用颈椎脱臼法将小鼠处死,剥出其股骨,体式显微镜拍照观察之后,固定组织,之后脱钙切片,番红固绿染色观测软骨损伤修复的过程。
[0657]
结果如图2所示,从中可以发现阳性化合物kgn并没有很好的软骨损伤修复效果,而本发明化合物pa002在给药33μm剂量下能够显著促进软骨缺损部位的软骨修复,表明化合物pa002具有很好的应对软骨损伤修复效果。
[0658]
实施例3-3sd大鼠关节软骨损伤模型的构建
[0659]
所有手术均在无菌环境下进行,实验器械均已灭菌。本研究使用雄性sd大鼠(8周龄);注射4%水合氯醛(1ml/100g)麻醉大鼠,备皮、消毒,铺巾;依次切开皮肤和肌肉,暴露膝关节;用电钻钻出了直径为2毫米、深度为1.5毫米的全厚度圆柱状软骨缺损;动物实验共分为四组(每组小鼠个数n=7),依次为假手术组,pbs对照组,uc-mscs直接注射组,以及5k(10μm)体外诱导后uc-mscs注射组。模型建立5天后,关节腔注射干细胞;术后9周,过量注射4%水合氯醛处死大鼠,收集所有标本;修复期完成以后,每个样品的软骨修复状态通过数码相机获得(图3a)。本发明还拟借助生物材料,即利用明胶包裹干细胞,将其固定到软骨缺
损部位,定点修复关节软骨,采用与上述实验相同的造模与给药方法,术后9周后采取大鼠股骨关节样本(图3b)。
[0660]
结果如图3所示。图3a结果显示,未经过干细胞治疗的pbs组软骨缺损区的再生软骨组织较少,仍能观察到明显的软骨缺损。而直接注射uc-mscs的实验组,可以明显观察到关节软骨缺损部位得到修复,但关节表面较为粗糙,表现出了轻微的骨质增生的现象,这对于软骨修复不利。而通过pa002体外诱导的uc-mscs实验组,软骨异常增生现象较弱,能够观察到软骨缺损部位得到了很好的修复。可以观察到,在缺损表面形成完整的软骨组织,并与周围原有的软骨组织形成平滑的表面。这一实验结果表明,通过化合物pa002提前体外诱导,能够提升mscs的体内软骨修复效果。图3b结果显示,未经给药的水凝胶组仍能够在关节表面观察到明显的软骨缺损存在。而在水凝胶包裹的未经分化uc-mscs组中,可以观察到在关节软骨缺损部位形成了一层透明软骨样组织,能够明显观察到软骨缺损部位。推测可能是形成软骨较薄,且软骨下骨部位未得到很好的修复。而经化合物pa002诱导后的实验组,可以观察到软骨缺损部位已经完全覆盖平滑组织,且新生组织颜色与周围的正常软骨组织并无太大差异。这一结果表明,化合物pa002能够更好的促进uc-mscs体内的成软骨分化,且经pa002诱导后的uc-mscs经水凝胶包裹后,能够更好的促进软骨缺损的修复,能够避免直接注射干细胞导致的组织异常增生问题。
[0661]
本发明的保护内容不局限于以上实施例。在不背离发明构思的精神和范围下,本领域技术人员能够想到的变化和优点都被包括在本发明中,并且以所附的权利要求书为保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1