黄精半乳聚糖及其制备方法和应用
1.本发明涉及食品和医药技术领域,特别是涉及一种黄精半乳聚糖及其制备方法和应用。
背景技术:
2.黄精是百合科黄精属植物,因有补益功效而得名。该属植物主要包括黄精(polygonatum sibiricum)、滇黄精(polygonatum kingianum)、多花黄精(polygonatum cyrtonema)、棒丝黄精(polygonatum cathcartii)、玉竹(polygonatum odoratum)、康定玉竹(polygonatum prattii)、小玉竹(polygonatum humile)、毛筒玉竹(polygonatum inflatum)、垂叶黄精(polygonatum curvistylum)、长苞黄精(polygonatum desoulayi)、长梗黄精(polygonatum filipes)、粗毛黄精(polygonatum hirtellum)、大苞黄精(polygonatum megaphyllum)、点花黄精(polygonatum punctatum)、短筒黄精(polygonatum altelobatum)、互卷黄精(polygonatum alternicirrhosum)、距药黄精(polygonatum franchetii)、独花黄精(polygonatum hookeri)、二苞黄精(polygonatum involucratum)、节根黄精(polygonatum nodosum)、对叶黄精(polygonatum oppositifolium)、湖北黄精(polygonatum zanlanscianense)、格脉黄精(polygonatum tessellatum)、五叶黄精(polygonatum acuminatifolium)、卷叶黄精(polygonatum cirrhifolium)、细根茎黄精(polygonatum gracile)、热河黄精(polygonatum macropodium)、新疆黄精(polygonatum roseum)、轮叶黄精(polygonatum verticillatum)和狭叶黄精(polygonatum stenophyllum)等。黄精药用部位为根茎,味甘,平。可补气养阴,健脾,润肺,益肾。用于脾虚胃弱,体倦乏力,口干食少,肺虚燥咳,精血不足,内热消渴。黄精属植物的根茎可作药用,其根茎中的化学成分主要有:黄精多糖、粘液质、淀粉、甾体皂苷、蒽醌类化合物、生物碱、强心苷、木脂素、维生素、脂肪、蛋白质以及多种对人体有用的氨基酸等化合物,而其中的黄精多糖正是黄精属植物中最具有药用功效的成分。
3.然而,植物多糖的化学结构极其复杂,同一植物中往往含有多种不同类型的多糖,多糖的生物学功效研究开展的也较少,因而植物多糖在生物医药和食品领域的应用研发进展缓慢。
技术实现要素:
4.本发明的目的在于:针对现有技术对于黄精研究深度不足,黄精中植物多糖成分复杂,其植物多糖研究进展缓慢的问题,提供一种黄精半乳聚糖及其制备方法和应用。
5.为了实现上述目的,本发明采用的技术方案为:
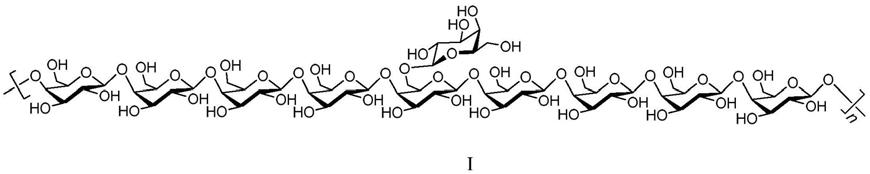
6.一种黄精半乳聚糖,所述黄精半乳聚糖具有如下通式i表示的化学结构:
[0007][0008]
式(i)中,n表示糖重复单元数,n为自然数。
[0009]
本发明结构新颖的黄精半乳聚糖成分,经药理学研究发现可以促进包括乳酸杆菌和双歧杆菌在内的益生菌的增殖,且在2到12小时效果显著;随着药物浓度的增加,黄精半乳聚糖促进益生菌增殖的能力明显增强,表明所述黄精半乳聚糖能促进益生菌的生长。
[0010]
作为本发明的优选方案,在其中一个实施例中,所述黄精半乳聚糖的重均分子量为4000da~15000da,多分散系数为1~3。
[0011]
进一步,所述黄精半乳聚糖的多分散系数可以是1.5、2、2.5等,或者上述分散系数点值上下浮动20%的范围内。
[0012]
为了获得上述黄精半乳聚糖成分,本发明还提供以下制备工艺方法,以便于从天然黄精药材中分离提取得到黄精半乳糖。
[0013]
一种上述黄精半乳聚糖的制备方法,包括以下步骤:
[0014]
提取炮制品黄精中的黄精粗多糖;
[0015]
纯化所述黄精粗多糖中重均分子量为4000da~15000da的组分,得到所述黄精半乳聚糖。
[0016]
进一步,上述黄精半乳聚糖的制备方法,具体包括以下步骤:
[0017]
步骤1、提取炮制品黄精的50
‑
65v%醇浓度下的粗多糖,得黄精粗多糖;
[0018]
步骤2、纯化分离所述黄精粗多糖中,重均分子量为4000da~15000da的组分,得到所述黄精半乳聚糖。
[0019]
本发明提供工艺方法采用炮制品黄精,提取约60v%的醇浓度的粗多糖,经过纯化分离得到黄精半乳聚糖。通过选择炮制品黄精将传统炮制工艺加工的制黄精进行分离提纯,获得具有特定活性的天然药物化学成分,具有重大的生物医药应用价值。
[0020]
进一步,炮制品黄精是黄精根茎的炮制品,通过炮制品黄精对进行提取,分离得到黄精粗多糖。
[0021]
进一步,所述炮制品黄精是黄精属植物经过6
‑
9次蒸晒炮制得到的。
[0022]
进一步,提取炮制品黄精的60%醇浓度下的粗多糖。
[0023]
在其中一个实施例中,步骤1、提取粗多糖具体包括以下步骤:将炮制品黄精加水回流提取,提取液用乙醇沉淀,筛选醇浓度达50
‑
65v%的醇沉物,离心并收集醇沉沉淀。最好是采用60v%乙醇沉淀物。
[0024]
进一步,将炮制品黄精经热水提取后,再分别用乙醇分级沉淀黄精多糖,使其醇浓度分别达到36
‑
45v%、55
‑
65v%,然后离心收集55
‑
65v%乙醇浓度时的沉淀。优选地,两次乙醇浓度分别为40%和60%。
[0025]
进一步,从黄精属各黄精的根茎中提取所述黄精半乳聚糖,其步骤包括以下步骤:将黄精植物的根茎用热水提取后,再分别用乙醇分级沉淀黄精多糖,使其醇浓度分别达到40%和60%,然后离心收集60%乙醇浓度时的沉淀。
[0026]
在其中一个实施例中,步骤2、纯化分离过程,选自凝胶排阻层析柱法、透析法和超滤法中的一种或多种。分离得到所述黄精多糖中重均分子量为4000da~15000da的组分,具有独特的活性特点。
[0027]
即,纯化所述黄精根茎粗多糖的重均分子量为4000da~15000da的组分的方法选自醇沉再分级、凝胶排阻层析柱法、透析法和超滤法中的一种或多种。
[0028]
在其中一个实施例中,所述黄精属植物包括黄精、滇黄精、多花黄精、棒丝黄精、玉竹、康定玉竹、小玉竹、毛筒玉竹、垂叶黄精、长苞黄精、长梗黄精、粗毛黄精、大苞黄精、点花黄精、短筒黄精、互卷黄精、距药黄精、独花黄精、二苞黄精、节根黄精、对叶黄精、湖北黄精、格脉黄精、五叶黄精、卷叶黄精、细根茎黄精、热河黄精、新疆黄精、轮叶黄精和狭叶黄精中的一种或多种。在制备过程中可以选择上述黄精属植物中的一种或多种,主要可以使用上述黄精属植物的根茎。
[0029]
一种药物组合物,所述药物组合物含有有效量的黄精半乳聚糖。
[0030]
进一步,所述药物组合物还包括有效量的黄精半乳聚糖和/或药用和/或食品用辅料或赋型剂或矫味剂。
[0031]
进一步,所述黄精半乳聚糖与药学载体组合作为密切的掺和物中的活性成分。
[0032]
进一步,所述黄精半乳聚糖采用口服或肠胃外给药的剂型。具体而言,可以举例的,其剂型可以是包含黄精半乳聚糖作为活性成分的胶囊、扁囊剂或片剂。
[0033]
进一步,所述黄精半乳聚糖采用还可以采用局部使用,例如,可以制成以下剂型之一:气雾剂、霜剂、软膏剂、洗剂、隔离剂、漱口水、含漱剂等。
[0034]
进一步,所述黄精半乳聚糖还可以是直肠施用、阴道施用的形式。例如,可以添加必要载体材料混合形成栓剂。合适的载体包括可可脂和其它本领域常用的材料,栓剂通过首先将黄精半乳聚糖与软化或融化的载体混合,然后在模具中冷却并塑型而便利地形成。
[0035]
一种上述黄精半乳聚糖、或药物组合物在促进益生菌生长的产品中的应用。
[0036]
在其中一个实施例中,所述药物组合物的剂型为冻干粉、口服液、胶囊、片剂、膏剂、栓剂等。
[0037]
一种上述药物组合物在制备用于促进消化、肠道蠕动的食品和药物中的应用。具体而言,所述黄精半乳聚糖的应用,包括至少以下之一,在调节胃肠道菌群、促进肠道蠕动和/或促消化的食品和/或药物制备中的应用。
[0038]
综上所述,由于采用了上述技术方案,本发明的有益效果是:
[0039]
1、本发明分离得到的黄精半乳聚糖尚属首次报道,经过发明人动物实验研究确定具有促进肠道益生菌群活性的作用,具有重要的保健品应用潜力。
[0040]
2、本发明黄精半乳聚糖经过益生菌分解以后,可以是使得乳酸、乙酸等短链脂肪酸代谢产物有所增加,从而使培养基ph值显著降低,更加有利于益生菌的生存,达到抑制有害菌群繁殖的作用。
附图说明:
[0041]
图1为黄精半乳聚糖的hplc图;
[0042]
图2为黄精半乳聚糖的单糖组成分析hplc图,其中图a为单糖标准品的hplc图,图b为黄精半乳聚糖的单糖组成分析hplc图,gal表示半乳糖;
[0043]
图3为黄精半乳聚糖的红外光谱图;
[0044]
图4为黄精半乳聚糖的核磁共振谱图,其中图a为1h nmr谱、图b为
13
c nmr谱;
[0045]
图5为黄精半乳聚糖的核磁共振谱图,其中图a为hsqc
‑
tocsy nmr图,图b为hmbc nmr图;
[0046]
图6为不同时间黄精半乳聚糖对接种包括乳酸杆菌和双歧杆菌在内的益生菌的培养基ph值的影响(n=3);
[0047]
图7为不同时间黄精半乳聚糖对接种包括乳酸杆菌和双歧杆菌在内的益生菌的培养基od值的影响(n=3);
[0048]
图8为不同时间黄精半乳聚糖对接种包括乳酸杆菌和双歧杆菌在内的益生菌的培养基中细菌数量的影响(n=3)。
具体实施方式
[0049]
为了便于理解本发明,下面将对本发明进行更全面的描述,并给出了本发明的较佳实施例。但是,本发明可以以许多不同的形式来实现,并不限于本发明所描述的实施例。相反地,提供这些实施例的目的是使对本发明的公开内容的理解更加透彻全面。
[0050]
除非另有定义,本发明所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。本发明所使用的术语“和/或”包括一个或多个相关的所列项目的任意的和所有的组合。
[0051]
本发明一实施例的黄精半乳聚糖,具有如下通式i表示的结构:
[0052][0053]
式(i)中,n表示糖重复单元数,n为自然数。
[0054]
所述黄精半乳聚糖以β(1
→
4)糖苷键为主链,侧链为半乳糖以β(1
→
6)糖苷键连接到此主链上。
[0055]
本发明人对黄精多糖经过深入研究惊奇地发现,从多花黄精等黄精属植物中,应用创新性方法提取纯化可获得一种结构新颖的黄精半乳聚糖。通过进一步的药理活性研究发现,所述新发现的黄精半乳聚糖能够显著促进益生菌的增殖,因而所述黄精半乳聚糖具有用于肠道调节和助消化药物和/或食品的制备的用途。因此,本发明提供的一种结构新颖的黄精半乳聚糖及其制备方法和药用组合物,以及在制备肠道调节和助消化药物中的应用,均为首次公开报道。
[0056]
进一步,n的取值范围1
‑
40,例如可以是1
‑
30、1
‑
20、1
‑
15、1
‑
10、2
‑
5,更具体的距离可以是1、2、4、6、8、10、14、18、22等。根据不同的天然黄精原料、炮制方法、分离情况可能略有不同。
[0057]
在一个具体示例中,黄精半乳聚糖的重均分子量为4000da~15000da,多分散系数为1~3。优选地,黄精半乳聚糖的重均分子量为6000da~10000da。
[0058]
在一个具体示例中,当通式i中的n=1,黄精半乳聚糖具有如下化学式ii表示的结构:
[0059][0060]
本发明一实施例的上述黄精半乳聚糖的制备方法,包括以下步骤s1~s2:
[0061]
s1:提取黄精属植物炮制后的多糖。
[0062]
s2:纯化黄精多糖中重均分子量为4000da~15000da的组分,得到黄精半乳聚糖。
[0063]
进一步,所述黄精属植物炮制后的原料为炮制品黄精(或称黄精炮制品)。
[0064]
在一个具体示例中,黄精属植物包括但不限于黄精、滇黄精、多花黄精、棒丝黄精、玉竹、康定玉竹、小玉竹、毛筒玉竹、垂叶黄精、长苞黄精、长梗黄精、粗毛黄精、大苞黄精、点花黄精、短筒黄精、互卷黄精、距药黄精、独花黄精、二苞黄精、节根黄精、对叶黄精、湖北黄精、格脉黄精、五叶黄精、卷叶黄精、细根茎黄精、热河黄精、新疆黄精、轮叶黄精和狭叶黄精。鉴于黄精属植物的种植资源情况,优选地,上述黄精属植物为黄精、滇黄精、多花黄精和玉竹中的一种和/或多种。
[0065]
进一步,所述炮制品黄精是多花炮制品黄精。以多花黄精作为原料进行蒸晒炮制,得到炮制品黄精即为多花炮制品黄精。
[0066]
进一步,所述炮制品黄精是“九蒸九晒”黄精、“八蒸八晒”黄精、“七蒸七晒”黄精、“六蒸六晒”黄精。
[0067]
进一步,所述炮制品黄精通过以下方法制备得到:
[0068]
将黄精去除杂质及须根,洗净晾干,切片。随后置于蒸锅内,盒盖,加热,待蒸锅内的水煮沸后,将蒸锅功率调小,并开始计时,文火蒸5
‑
10小时,优选4
‑
7h。
[0069]
蒸好后,将黄精取出,置于65
‑
77℃烘箱内,10
‑
15小时后取出,即为一蒸一晒黄精。重复上述方法6
‑
9次,分别可以制得“六蒸六晒”黄精、“七蒸七晒”黄精、“八蒸八晒”黄精、“九蒸九晒”黄精。
[0070]
具体的,将新鲜的多花黄精10kg去除杂质及须根,洗净晾干,切厚片。随后置于蒸锅内,待蒸锅内的水煮沸后,将蒸锅功率调小,并开始计时,文火蒸6h。蒸好后,将黄精取出,置于70℃烘箱内,12h后取出即为一蒸一晒黄精。重复上述方法制得“九蒸九晒”黄精。
[0071]
进一步,s1包括以下步骤:称取炮制品黄精,5
‑
15倍水回流提取1
‑
4次,每次1
‑
5h,过滤,合并提取液,离心,得上清液,浓缩多花黄精重量的5
‑
10倍,得浓缩液。
[0072]
然后,向浓缩液中加入乙醇,调节醇浓度为35
‑
45v%,离心,得第一醇沉物以及第一醇沉上清液。上述第一醇沉上清液中,加入乙醇调节醇浓度至55
‑
65v%,离心,得第二醇沉物和第二醇沉上清液,体积浓度92v%以上的乙醇洗涤第二醇沉物1
‑
4次,挥发脱除乙醇后,得粗黄精半乳聚糖。
[0073]
在一个具体示例中,提取黄精多糖的步骤包括以下步骤:称取多花炮制品黄精200g,10倍水回流提取2次,每次4h,过滤,合并提取液,离心,得上清液,浓缩至1300ml。浓缩液中加入95%乙醇945ml至醇浓度为40%,离心,得40%醇沉物以及1000ml醇沉上清液。上
述40%醇沉上清液中,搅拌下加入1714ml95%乙醇,离心,得60%醇沉物和醇沉上清液,95%乙醇洗涤60%醇沉物3次,挥醇后得粗黄精半乳聚糖。
[0074]
在一个具体示例中,纯化黄精多糖中重均分子量为4000da~15000da的组分的方法选自阴离子交换柱层析法、凝胶排阻层析柱法、透析法和超滤法中的一种或多种。
[0075]
具体地,可将粗黄精半乳聚糖组分加去离子水复溶后,离心除去少量不溶物,任选醇沉分级、凝胶排阻层析法、透析法或超滤法等方法中至少一种进行纯化,收集含有半乳聚糖的流份或截留液或透过液,若含有盐需脱盐后,直接真空冷冻干燥或减压浓缩后醇沉减压干燥,即得纯化的黄精半乳聚糖。
[0076]
本领域技术人员容易理解,对于凝胶排阻层析法,是根据黄精多糖组分中多糖物质的分子量,合理选择凝胶材料,例如葡聚糖凝胶sephadex系列、琼脂糖凝胶sepharose系列、聚丙烯酰胺bio
‑
gel p系列以及它们相互交联形成的凝胶填料,然后按照各个填料的实际性能进行装柱、上样以及用含盐或不含盐洗脱溶液依次洗脱并收集流份。合并各个流出峰,流出液可浓缩或不需要浓缩,装入透析袋透析或超滤膜包超滤脱盐,收集脱盐后的截留液,经真空冷冻干燥或真空减压干燥,即得纯化的黄精半乳聚糖。或者采用透析法或超滤法等方法进行纯化黄精多糖组分时,选择适当分子量的超滤膜包进行切向流超滤截留处理。例如,黄精多糖组分水溶液先经一个大于黄精半乳聚糖的分子量的透析袋或超滤膜包充分透析或超滤,收集透过液或流出液,除去大分子量的物质,然后再经小于黄精半乳聚糖的分子量的透析袋或超滤膜包充分透析或超滤,收集截留液,浓缩后经真空冷冻干燥或真空减压干燥,即得纯化的黄精半乳聚糖。
[0077]
本发明还提供一种上述黄精半乳聚糖的结构解析方法,包括以下步骤:
[0078]
(1)分子量测定:取黄精半乳聚糖样品,采用高效凝胶排阻色谱
‑
示差检测器检测法。
[0079]
(2)单糖组成分析:取黄精半乳聚糖样品,用浓度较低的酸使之部分水解为单糖,经pmp衍生化后,进如c18的色谱柱,经高效液相色谱仪分析黄精半乳聚糖的单糖组成。
[0080]
(3)甲基化分析:取黄精半乳聚糖样品,用如碘甲烷等卤代甲烷试剂在碱性条件下,进行多糖甲基化,在碱性条件下水解后用硼氢化钠还原,用酸酐对甲基化糖醇进行乙酰化,萃取定容后,进行气相色谱仪联用质谱仪(gc
‑
ms)分析,判断黄精半乳聚糖的糖苷键连接方式。
[0081]
(4)红外光谱分析:取黄精半乳聚糖样品,充分干燥后,采用固体溴化钾压片法,在红外光谱仪上测定样品的红外光谱。
[0082]
(5)核磁共振分析:取黄精半乳聚糖样品溶解于氘代重水中,冷冻真空干燥,重复三次重水交换后,溶解到重水中,检测样品的核磁共振谱包括一维1h和
13
c谱和1h
‑1h cosy、1h
‑1h tocsy、1h
‑1h roesy、1h
‑
13
c hsqc、1h
‑
13
c hmbc二维相关谱。
[0083]
(6)综合数据解析:综合分析上述步骤的分析数据,解析黄精半乳聚糖的化学结构。
[0084]
按照上述结构解析方法,对应用本发明的制备方法从多花黄精中提取纯化的黄精半乳聚糖进行结构分析。结果显示,所述黄精半乳聚糖在hpgpc凝胶色谱峰上只显示一个对称性良好的色谱峰,而其重均分子量为~7kda,其多分散指数为1.15;单糖组成显示所述黄精半乳聚糖由半乳糖组成;甲基化分析显示,该黄精半乳聚糖存在β(1
→
4)糖苷键和β(4,6
→
1)糖苷键;红外光谱分析显示,糖环和环上的羟基吸收峰,以及在指纹图谱区有吡喃糖吸收信号峰都符合半乳聚糖的吸收峰;根据核磁共振谱数据,可以清晰地归属黄精半乳聚糖的1h和
13
c的信号。综合上述数据,所述黄精半乳聚糖具有如通式i所示的结构特征:以β(1
→
4)糖苷键为主链,而侧链半乳糖以β(1
→
6)糖苷键连接到此主链上。
[0085][0086]
式(i)中,n表示糖重复单元数,n为自然数。
[0087]
按照本发明上述结构解析方法,黄精属植物中含有具有化学式ii所示结构的黄精半乳聚糖。
[0088][0089]
显然,如化学式ii所示结构的黄精半乳聚糖是如通式i所示黄精半乳聚糖当n=1时的结构。
[0090]
本发明经药理学研究惊奇地发现,所述黄精半乳聚糖可以促进益生菌的增殖,且在2到12小时效果显著;随着药物浓度的增加,黄精半乳聚糖促进益生菌的能力明显增强,表明所述黄精半乳聚糖能够促进益生菌的增殖。因此,所述结构新颖的黄精半乳聚糖具有促进益生菌增殖,因而具有调节肠道菌群的实际应用价值。
[0091]
为此,进一步本发明还提供所述黄精半乳聚糖在制备调节肠道菌群、促进消化和增强肠道蠕动药物和/或食品中的应用。
[0092]
本发明一实施例的药物组合物,包括所述黄精半乳聚糖及其药学上可接受的盐或药学上可接受的溶剂合物,和药学上和/或食品上可接受的辅料。可选地,上述辅料包括药用赋形剂、载体和/或稀释剂和/或矫味剂等。
[0093]
在一个具体示例中,上述药物组合物的剂型为注射剂或固体制剂,例如水针剂和注射用冻干粉针剂和胶囊剂和泡腾剂等,辅料包括赋型剂和/或矫味剂等。
[0094]
本发明还提供上述药物组合物在制备用于调节肠道菌群、促进消化和增强肠道蠕动药物和/或功能食品中的应用。
[0095]
以下结合附图以特定的具体实施例来详细说明本发明内容,但这些具体实施例对本发明的权利要求的范围不构成任何限制。
[0096]
实施例1黄精半乳聚糖的提取纯化
[0097]
1.黄精粗多糖的提取
[0098]
将新鲜的多花黄精10kg去除杂质及须根,洗净晾干,切厚片。随后置于蒸锅内,待蒸锅内的水煮沸后,将蒸锅功率调小,并开始计时,文火蒸6h。蒸好后,将黄精取出,置于70℃烘箱内,12h后取出即为一蒸一晒黄精。重复上述方法制得“九蒸九晒”黄精。
[0099]
取上述炮制后的多花黄精200g,10倍水回流提取2次,过滤,合并提取液,离心,得上清液,浓缩得1300ml浓缩液。加入95%乙醇945ml至醇浓度为40%,离心(4000rpm
×
15min),得40%醇沉物和上清液。搅拌下,40%醇沉上清液加入1714ml 95%乙醇,至醇浓度达60%,离心(4000rpm
×
15min),得60%醇沉物和上清液,95%乙醇洗涤60%醇沉物3次,挥醇后得粗黄精半乳聚糖。
[0100]
2.黄精半乳聚糖纯化
[0101]
取上述粗黄精半乳聚糖,溶解于去离子水中,上deae
‑
52(3.2cm
×
30cm)弱阴离子交换柱,分别用去离子水和0.1、0.5和1.0m nacl溶液洗脱,每管约10ml收集洗脱流份。苯酚硫酸法检测,绘制流出曲线,收集流份后,减压浓缩,冷冻真空干燥,即得纯化的黄精半乳聚糖1.78g。
[0102]
实施例2黄精半乳聚糖的结构解析
[0103]
1.实验过程
[0104]
1.1.分子量及其分布
[0105]
采用高效凝胶排阻色谱
‑
示差检测器检测法(hpgpc
‑
ri)分析实施例1制备的黄精半乳聚糖的分子量及其分布。
[0106]
色谱仪器:agilent technologies 1260series高效液相色谱仪;
[0107]
色谱条件:shodex ohpak sb
‑
804hq(7.8mm
×
300mm)柱;柱温为35℃;示差检测器;流动相为0.1m nacl,流速0.5ml/min;
[0108]
测定过程:各取5mg半乳聚糖样品或已知分子量的右旋糖酐对照品加流动相配制为5mg/ml的溶液,过0.22μm微孔滤膜,滤过液50μl进高效液相色谱仪分析,记录色谱图。数据采用gpc软件处理,绘制标准曲线,将数据带入方程,计算分子量。
[0109]
1.2单糖组成分析
[0110]
取黄精半乳聚糖样品2.0mg,加水溶解至2mg/ml,取300μl,加入300μl 4m的三氟乙酸溶液溶解,充n2,封管,110℃条件下水解反应4h后,在70℃水浴锅中蒸干水解液,除去三氟乙酸。加入100μl水溶解蒸干物后,加入50μl 0.6m的氢氧化钠溶液和100μl 0.5m的3
‑
甲基
‑1‑
苯基
‑2‑
吡唑啉
‑5‑
酮(pmp)甲醇溶液,涡旋混匀,于70℃烘箱中衍生化反应60min,反应结束后冷却至室温,加入100μl 0.3m的盐酸溶液中和后,溶液加入500μl三氯甲烷萃取,离心(15000rpm
×
15min),用0.22μm微孔滤膜过滤后供色谱分析。
[0111]
色谱条件:仪器:agilent technologies 1260series高效液相色谱仪;色谱柱:agilent zorbax sb c18(150mm
×
4.6mm,5μm);柱温为30℃;流动相为0.1m乙酸铵(ph 5.5)缓冲液:乙腈(83:17);流速:1ml/min;进样体积为20μl;dad检测器,检测波长为250nm。
[0112]
1.3甲基化分析
[0113]
甲基化反应:称取黄精半乳聚糖样品10mg溶解于4ml dmso中,依次加入100mg氢氧化钠和600μl碘甲烷,充氮气超声反应1小时。反应结束后,加入2ml纯水,用1m盐酸溶液调节溶液ph值至中性,加入6ml三氯甲烷对甲基化后样品进行萃取,取有机相40℃减压干燥并真空干燥12h除有机溶剂。
[0114]
酸水解:上述干燥后样品,溶解于2ml 2m tfa溶液,封管120℃下酸水解5h。
[0115]
还原:上述水解液用1m naoh调ph为10~12,加入50mg硼氢化钠,50℃水浴搅拌2h后,加入250μl冰乙酸终止反应,反应液冻干。
[0116]
乙酰化:上述冻干样品中加入1ml吡啶和1ml乙酸酐于试管中,100℃封管反应1h。冷却后,加入1ml水,每次2ml二氯甲烷萃取3次,有机相用n2吹干后,加入100μl二氯甲烷溶解,进行gc
‑
ms分析。
[0117]
gc条件:hp
‑
5ms石英毛细管柱(50mm
×
0.25mm,0.25μm);柱温:起始温度80℃,保持11min,程序升温5℃/min至250℃,保持5min;载气为高纯氦气;载气流量为1.5ml/min;进样口温度270℃;柱前压100kpa;不分流;进样量:2μl。
[0118]
ms条件:电离方式ei;电子能量70;传输线温度290℃;离子源温度230℃;四极杆温度150℃;质量范围50~600;采用ccrc标准谱库计算机检索定性。
[0119]
1.4红外光谱分析
[0120]
按照2020版《中国药典》第四部分采用固体压片法:取2mg样品经40℃真空干燥24h,采用kbr压片法,使用tensor 27傅立叶变换中红外光谱仪对样品进行4000~400cm
‑1扫描,记录光谱图。
[0121]
1.5核磁共振分析
[0122]
取黄精半乳聚糖样品10mg溶于0.5ml d2o中,冷冻干燥,d2o交换三次后,将冷冻干燥样品溶于0.5ml d2o(99.9atom%d,含有内标物0.05wt.%3
‑
(trimethylsilyl)propionic
‑
2,2,3,3
‑
d
4 acid,sodium salt)中。使用bruker 800mhz核磁共振波谱仪测定1h/
13
c nmr谱图以及二维图谱(1h
‑1h cosy、1h
‑1h tocsy、1h
‑1h roesy、1h
‑
13
c hmbc和1h
‑
13
c hsqc),采用mestrenova软件进行分析处理。
[0123]
2.实验结果
[0124]
本发明的黄精半乳聚糖的性状为:白色或类白色固体,无味,易溶于水,微溶于乙醇等有机溶剂,有引湿性。
[0125]
高效凝胶排阻色谱法分析结果表明(附图1),黄精半乳聚糖仅有一个对称的色谱峰,其重均分子量(mw)为7019da,多分散系数为1.14。
[0126]
单糖组成分析结果显示(附图2),所述黄精半乳聚糖经pmp柱前衍生后的hplc图显示仅有一个半乳糖的峰,说明所述黄精半乳聚糖单糖组成中仅含有半乳糖。
[0127]
甲基化分析结果表明,所述黄精半乳聚糖存在β(1
→
4)半乳糖糖苷键、β(1
→
4,6)半乳糖糖苷键和β(
→
1)半乳糖糖苷键。
[0128]
红外光谱(cm
‑1)数据(附图3)为:3416cm
‑1为糖环上羟基o
‑
h伸缩振动的特征吸收;2922~2897cm
‑1为糖环上亚甲基c
‑
h伸缩振动;1025cm
‑1为糖环上c
‑
o
‑
c伸缩振动;889cm
‑1为β型单糖的构型特征吸收。
[0129]
核磁共振nmr检测分析部分结果见附图4和附图5,详细的1h和
13
c nmr信号的归属见表1和2。质子化学位移4.65ppm、4.61ppm和4.46ppm分别为1,4
‑
β
‑
d
‑
半乳糖(1,4
‑
β
‑
d
‑
galp,简写为b)、1,4,6
‑
β
‑
d
‑
半乳糖(1,4,6
‑
β
‑
d
‑
galp,简写为d)和1
‑
β
‑
d
‑
半乳糖(1
‑
β
‑
d
‑
galp,简写为a)异头1h质子信号,1,4
‑
β
‑
d
‑
galp的4位(h
‑
4)质子信号为4.19ppm以及其对应的c
‑
4的化学位移为80.5ppm;1,4,6
‑
β
‑
d
‑
galp的4位(h
‑
4)和6位质子信号分别为4.22ppm和3.90ppm(4.12ppm)以及其对应的c
‑
4和c
‑
6的化学位移为80.5ppm和73.1ppm。上述化学位移相对于无取代半乳糖的相应的化学位移显著向低场移动,说明半乳糖基b的1位和4位的羟基有取代,半乳糖基d的1位、4位和6位的羟基有取代。半乳糖基b的异头c
‑
h的耦合常数为148hz,显示其异头位构型应为β型。在nmr谱中有3个异头氢信号(化学位移值均小于
4.90ppm),3个异头碳信号从低到高分别为106.5、107.1和107.2ppm,分别对应1
‑
β
‑
d
‑
半乳糖(1
‑
β
‑
d
‑
galp)、1,4,6
‑
β
‑
d
‑
半乳糖(1,4,6
‑
β
‑
d
‑
galp)和1,4
‑
β
‑
d
‑
半乳糖(1,4
‑
β
‑
d
‑
galp)的c
‑
1,说明三个糖基片段的异头位构型均为β型。1h和
13
c远程相关hmbc谱清晰的显示,半乳糖基a的h
‑
1(a1)和d的c
‑
6(d6)有明显的相关信号(附图5),而半乳糖基b的h
‑
1(b1)和半乳糖基d的c
‑
4(d4),半乳糖基d的h
‑
1(d1)和半乳糖基b的c
‑
4(b4),半乳糖基b的h
‑
4(b4)和半乳糖基a的c
‑
1(a1)也有相关信号。因此,半乳聚糖的连接方式为:半乳糖基b以β(1
→
4)糖苷键形成主链,而半乳糖基a以β(1
→
6)糖苷键连接到半乳糖基d的6位上。
[0130]
综合上述数据可知,这个结构新颖的黄精半乳聚糖的化学结构式如通式i所示。
[0131][0132]
式(i)中,n表示糖重复单元数,n为自然数。
[0133]
其结构特征为:(1)所述黄精半乳聚糖是从黄精的根茎提取的新结构的半乳聚糖;(2)所述黄精半乳聚糖的单糖连接方式为:以β(1
→
4)糖苷键为主链,而侧链半乳糖以β(1
→
6)糖苷键连接到此主链上。经国内外公开文献检索,所述黄精半乳聚糖的这种排列方式和化学结构未见公开报道,为本发明人首次发现。
[0134]
表1.黄精半乳聚糖的1h nmr的归属
[0135] 1
‑
β
‑
d
‑
galp(a)1,4
‑
β
‑
d
‑
galp(b)1,4,6
‑
β
‑
d
‑
galp(d)h
‑
14.464.654.61h
‑
23.623.693.53h
‑
33.673.793.79h
‑
43.954.194.22h
‑
53.733.674.00h
‑
63.833.73,3.853.90,4.12
[0136]
表2.黄精半乳聚糖的
13
c nmr的归属
[0137][0138][0139]
注:
[0140]
其中,1
‑
β
‑
d
‑
galp表示β
‑
d
‑
galp
‑
(1
→
;
[0141]
1,4
‑
β
‑
d
‑
galp表示
→
4)
‑
β
‑
d
‑
galp
‑
(1
→
;
[0142]
1,4,6
‑
β
‑
d
‑
galp表示
→
4,6)
‑
β
‑
d
‑
galp
‑
(1
→
。
[0143]
实施例3黄精半乳聚糖的促进益生菌生长实验
[0144]
1.受试品、试剂和菌株
[0145]
黄精半乳聚糖,简写为pp1,按照实施例1制备的半乳聚糖;无糖de man
‑
rogosa
‑
sharpe(mrs)培养基,北京coolaber公司;4种菌株分别为动物双歧杆菌乳亚种(bifidobacterium animalis subsp.lactis)、两歧双歧杆菌(bifidobacterium bifidum)、嗜酸乳杆菌(lactobacillus acidophilus)和植物乳杆菌(lactobacillus plantarum)均购自北京北纳创联生物技术研究院。
[0146]
2.实验方法
[0147]
2.1溶液配制
[0148]
称取低聚果糖fos、黄精半乳聚糖pp1各600mg以及700mg葡萄糖(glucose),分别用无菌水配制成10mg/ml溶液,在超净工作台中用0.22μm的无菌滤器过滤后,每种溶液均以5mg/ml的浓度添加到无糖的mrs培养基中。取56ml灭菌好的mrs培养基,加56ml无菌水稀释过滤的样品,混合后,配制成5mg/ml mrs培养基。b.bifidum和l.plantarum在相应的培养基上接种1
×
107cfu/ml的量,b.animalis subsp.lactis和l.acidophilus在相应的培养基上接种1
×
108cfu/ml的量。
[0149]
2.2细菌培养
[0150]
细菌培养基:mrs(l
‑
半胱氨酸)培养基含0.05%的l
‑
半胱氨酸;
[0151]
细菌复苏:准备1支相对液体培养基及2个平板,在超净台中用小砂轮在管身1/2处划圈,然后用75%的酒精擦拭管壁,用镊子敲断。将0.3
‑
0.5ml的液体培养基注入冻干管中,轻轻吹打混匀,充分溶解成菌悬液,吸取1/3加入液体培养基中,剩余平均加入到2个平板上,在相应的条件下培养至长出菌落。
[0152]
扩菌:从平板上挑取单个菌落于液体培养基中,37℃相应条件下摇床上培养。
[0153]
保种:取25ml菌液4℃下离心(4100rmp
×
10min),去上清液,加2.5ml液体培养基悬起沉淀,加等体积的甘油混匀分装置
‑
80℃冻存。
[0154]
2.3各细菌培养基的培养
[0155]
各细菌菌株置于厌氧环境(85%n2,10%co2和5%h2,体积浓度)中培养,在0h、2h、4h、6h、8h、12h、24h、36h和48h各时间点取样。
[0156]
2.4ph值的检测
[0157]
在各取样时间点取出培养液,平行取三份,离心后(4000rpm
×
10min),测定ph值,每个时间点测3次。
[0158]
2.4od值的检测
[0159]
在各取样时间点取出培养液,平行取三份,上下振摇15s后,倒入比色皿内,于600nm波长处用紫外分光光度计测定od值,每个时间点测3次。
[0160]
2.6细菌数目的检测
[0161]
在各取样时间点取出培养液,平行取三份,上下振摇15s后,从中取出一定量培养液,以一定倍数稀释后在血球计数板上数,每个时间点测3次。
[0162]
3.实验结果
[0163]
3.1对各细菌培养基中ph值的影响
[0164]
如附图6所示,与空白组相比,黄精半乳聚糖和其他各处理组的ph值均有不同程度的降低,表明各细菌株在黄精半乳聚糖、低聚果糖和葡萄糖的存在下,其如乳酸、乙酸等短链脂肪酸代谢产物有所增加,从而使培养基ph值显著降低。
[0165]
3.2对各细菌培养基中od值的影响
[0166]
如附图7所示,以不同培养基培养得到的培养液中od值在0到12小时整体快速上升,12h后各培养液的od值基本保持不变;黄精半乳聚糖、低聚果糖和葡萄糖组的od值在相应时间内均显著高于空白。黄精半乳聚糖、低聚果糖和葡萄糖均可促进各细菌菌株的增殖,而黄精半乳聚糖处理后细菌增殖数量与空白组有显著差异(p<0.01)。
[0167]
3.3对各细菌培养基中细菌菌株数目的影响
[0168]
如附图8所示,在含有黄精半乳聚糖的培养基中,4个细菌菌株均在2
‑
12小时进入指数期,快速增殖;对4种不同菌种的增殖情况随菌种不同而有差异,对动物双歧杆菌乳亚种(b.animalis subsp.lactis)促增殖活性显著高于嗜酸乳杆菌(l.acidophilus)。
[0169]
上述结果证实,本发明所述黄精半乳聚糖具有显著的促进益生菌生长活性,因而所述结构新颖的黄精半乳聚糖具有改善肠道菌群、促进消化和增强肠道蠕动的实际应用价值。
[0170]
实施例4黄精半乳聚糖冻干粉针的制备
[0171]
1.材料
[0172]
同实施例1方法所得黄精半乳聚糖,药用级氯化钠。
[0173]
2.处方
[0174]
原辅料名称用量黄精半乳聚糖50g氯化钠4.5g注射用水500ml共制成1000支
[0175]
3.制备工艺
[0176]
称取处方量的黄精半乳聚糖和氯化钠加注射用水至全量,搅拌使溶解完全,间歇式热压法灭菌。加入0.3%的药用活性炭,搅拌20min;使用布氏漏斗及3.0μm微孔滤膜脱炭过滤除去热源。含量合格后用0.22μm的微孔滤膜过滤;分装于管制西林瓶中,每瓶0.5ml,半压塞,置冷冻干燥箱内,按设定的冻干曲线进行冻干,压塞,出箱,轧盖,目检合格,包装得成品。
[0177]
冻干过程:将样品进箱,降隔板温至
‑
40℃,保持4h;冷阱降至
‑
50℃,开始抽真空至250μbar。开始升华:1h匀速升温至
‑
20℃,保持3h;3h匀速升温至
‑
10℃,保持8h,真空保持100~250μbar;再进行干燥:2h升温至
‑
5℃,保持2h,真空保持150~200μbar;0.5h升温至10℃,保持2h,真空保持80~100μbar;0.5h升温至40℃,保持4h,真空抽至最低。
[0178]
实施例5黄精半乳聚糖胶囊剂的制备
[0179]
1.材料
[0180]
同实施例1方法所得黄精半乳聚糖,食品或药品级淀粉。
[0181]
2.处方
[0182]
原辅料名称用量黄精半乳聚糖300g淀粉500g共制成5000粒
[0183]
3.制备工艺
[0184]
称取处方量的黄精半乳聚糖和淀粉,搅拌使混合完全。加入适量滑石粉,用乙醇湿法制粒,过筛干燥后,装入2号胶囊壳中,每个胶囊体装填60mg的黄精半乳聚糖,制得黄精半乳聚糖胶囊。
[0185]
实施例6黄精半乳聚糖口服液的制备
[0186]
1.材料
[0187]
同实施例1方法所得黄精半乳聚糖,食品或药品级矫味剂为和焦糖香精。
[0188]
2.处方
[0189]
原辅料名称用量黄精半乳聚糖50g蔗糖0.3g焦糖香精0.05g纯化水1000ml共制成500支
[0190]
3.制备工艺
[0191]
称取处方量的黄精半乳聚糖、蔗糖和焦糖香精,加纯化水完全溶解后,0.22μm的微孔滤膜过滤,滤液按每瓶2ml的量,经口服液罐装机罐装,封口后灭菌,即得。
[0192]
实施例7黄精半乳聚糖洁面乳制备
[0193]
1.材料
[0194]
同实施例1方法所得黄精半乳聚糖,采用化妆品级别或食品级的原料。
[0195]
2.处方
[0196]
黄精半乳聚糖7g、甘油2.0g、丁二醇4.0g、丙二醇0.5g、edta钠0.1g、瓜尔胶0.3g、二氧化锌2.0g、c12
‑
15醇苯甲酸酯4.0g、c12
‑
20烷基葡糖苷3.0g、c14
‑
22醇0.5g、鲸蜡硬脂醇1.2g、尼泊金酯0.2g、硬脂酸钠0.3g、聚二甲基硅氧烷醇0.5g、聚山梨醇酯0.2g、去离子水55g。
[0197]
3.制备工艺
[0198]
称取处方量的黄精半乳聚糖,加纯化水完全溶解;取甘油、丁二醇、丙二醇、edta钠、瓜尔胶、二氧化锌、硬脂酸钠、c12
‑
15醇苯甲酸酯、c12
‑
20烷基葡糖苷、c14
‑
22醇、鲸蜡硬脂醇,加纯化水完全溶解;取尼泊金酯、聚二甲基硅氧烷醇、聚山梨醇酯,加纯化水完全溶解。将前述准备的溶液混合,充分搅拌均匀,0.22μm的微孔滤膜过滤,滤液按每瓶30ml的量罐装,封口后灭菌,即得。
[0199]
实施例8黄精半乳聚糖面膜制备
[0200]
1.材料
[0201]
同实施例1方法所得黄精半乳聚糖,采用化妆品级别或食品级的原料。
[0202]
2.处方
[0203]
黄精半乳聚糖12g、透明汉生胶3.5g、水解透明质酸2.0g、透明质酸钠2.0g、丙二醇0.3g、卡波姆0.5g、尼泊金酯0.1、ppg
‑
10甲基葡糖醚0.25g、甘油葡糖苷1.0g、去离子水45g。
[0204]
3.面膜制备工艺
[0205]
步骤1、取去离子水、透明汉生胶、水解透明质酸、透明质酸钠、丙二醇、卡波姆、尼泊金酯加入乳化锅内,一边搅拌一边加热至75℃,达到温度以后保温并继续搅拌直至溶液呈透明均一,然后保温20分钟后,降温至42℃。
[0206]
步骤2、调节ph=7.6
±
0.2。
[0207]
步骤3、继续降温至35℃,加入ppg
‑
10甲基葡糖醚、黄精半乳聚糖、甘油葡糖苷,继续搅拌均匀,检验合格后即可出料。以无纺布底材进行涂布,涂布量为2.1g每平方厘米。
[0208]
本申请所引用的各专利、专利申请和出版文的说明全部纳入本申请参考。引用的任何参考文献不应认为是允许这些参考文献可以用来作为本申请的“现有技术”。
[0209]
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
[0210]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1