抗人CD40抗体及其用途的制作方法
抗人cd40抗体及其用途
技术领域
1.本技术大体涉及基因工程和抗体药物领域;具体而言,涉及抗人cd40抗体领域及其用途。本技术开发了新的抗人cd40抗体,并提供了所述抗体在预防或治疗cd40介导的疾病中的用途。
背景技术:
2.cd40是分子量为50kda的i型跨膜蛋白,是肿瘤坏死因子受体(tnfr)超家族的成员1,主要在b细胞和其他抗原递呈细胞(apc)(如树突状细胞和巨噬细胞)上表达。cd40也可以由内皮细胞、平滑肌细胞、成纤维细胞和上皮细胞表达,在细胞免疫反应和体液免疫反应中具有不可替代的作用。cd40的配体cd40l(又称为cd154、gp39或trap)是一种ii型跨膜蛋白,属于肿瘤坏死因子(tnf)超家族成员,cd40l主要表达于激活的cd4
+
t细胞及一小亚群cd8
+
t细胞表面2。
3.cd40和cd40l的相互作用是t细胞激活的共刺激信号。t细胞完全激活需要两个不同但协同的信号。由抗原递呈细胞(apc)上的抗原-mhc复合物提供的第一信号,通过t细胞抗原受体(tcr)传递,并负责免疫应答的特异性。第二或共刺激信号则是通过cd28与b7-1(cd80)/b7-2(cd86),以及cd40与cd40l相互作用来传递,这是达到完全t细胞应答所必需的。在缺乏共刺激信号时,t细胞可能发生无应答或持续特异性免疫应答,从而产生耐受。因此第二信号通路在机体免疫应答的整个过程中起着非常关键的调节作用。
4.静息b细胞上的cd40-cd40l相互作用能诱导b细胞增殖、分化为抗体分泌细胞及同种型转换,并且对生发中心的发展和记忆性b细胞的存活都有影响,所有这一切都是体液免疫应答必不可少的3。树突状细胞(dc)上cd40与cd40l的结合可诱导dc完全成熟为有效apc,这表现在共刺激分子(如b7家族(cd80、cd86))的表达增加,以及促炎细胞因子(如白细胞介素12)的产生,这将导致显著的t细胞应答
4,5
。
5.cd40信号由多聚化受体经一系列tnf受体相关因子(traf)的募集而转导6。cd40信号转导激活多种通路,包括nf-κb(核因子-κb)、mapk(丝裂原活化蛋白激酶)和stat3(信号转导子和转录激活子-3)7,其通过激活活化蛋白、c-jun、atf2(激活转录因子-2)和rel转录因子8调节基因表达。通过cd40信号应答而激活的基因包括各种细胞因子和趋化因子,如il-1、il-6、il-8、il-10、il-12、tnf-α和巨噬细胞炎性蛋白-1α(mip1α)。在某些细胞类型中,cd40激活可能会导致产生细胞毒性自由基、cox-2(环氧合酶-2),并产生no(一氧化氮)8。
6.cd40不仅在正常的免疫细胞上表达,还可以在许多恶性细胞上表达。例如,cd40在以下疾病中过表达:b系非霍奇金淋巴瘤(nhl)、慢性淋巴细胞性白血病(cll)、毛细胞白血病(hcl)、霍奇金病
9,10
、多发性骨髓瘤
11
以及膀胱癌、肾癌、卵巢癌、宫颈癌、乳腺癌、肺癌、鼻咽癌、恶性黑色素瘤
12
,13
,14
等。
7.目前已知cd40的激活可有效触发抗肿瘤反应,包括肿瘤特异性t细胞反应的免疫激活、对cd40阳性肿瘤直接的细胞凋亡作用,以及刺激导致adcc的体液反应,且观察到的肿瘤根除与肿瘤特异性细胞毒性t淋巴细胞的出现强烈相关
15,16
。据报道,cd40激动剂能克服
荷瘤小鼠的t细胞耐受,激起针对肿瘤相关抗原的有效的细胞毒t细胞应答,并增强抗肿瘤疫苗的效力
17,18
。
8.因此,鉴于抗cd40抗体具有广泛的适用性,基于临床需求,探索和研发cd40靶向抗体具有重要的生物学和医学意义。
9.发明概述
10.第一方面,本技术提供了结合人cd40的抗体,其包含含hcdr1、hcdr2和hcdr3氨基酸序列的重链可变区和含lcdr1、lcdr2和lcdr3氨基酸序列的轻链可变区,其中
11.所述hcdr1氨基酸序列如seq id no:28、34或37所示,所述hcdr2氨基酸序列如seq id no:29、35或38所示,所述hcdr3氨基酸序列如seq id no:30或39所示,所述lcdr1氨基酸序列如seq id no:31或40所示,所述lcdr2氨基酸序列如seq id no:32所示,所述lcdr3氨基酸序列如seq id no:33、36或41所示;
12.其中hcdr和lcdr氨基酸序列根据kabat定义。
13.在一些实施方案中,所述抗体的重链可变区的氨基酸如seq id no:17、19、21、25或者26所示。
14.在一些实施方案中,所述抗体的轻链可变区的氨基酸如seq id no:18、20、22或者27所示。
15.在一些实施方案中,所述抗体的重链可变区的氨基酸序列如seq id no:17所示,所述抗体的轻链可变区的氨基酸序列如seq id no:18所示;或者
16.所述抗体的重链可变区的氨基酸序列如seq id no:19所示,所述抗体的轻链可变区的氨基酸序列如seq id no:20所示;或者
17.所述抗体的重链可变区的氨基酸序列如seq id no:21所示,所述抗体的轻链可变区的氨基酸序列如seq id no:22所示;或者
18.所述抗体的重链可变区的氨基酸序列如seq id no:25所示,所述抗体的轻链可变区的氨基酸序列如seq id no:27所示;或者
19.所述抗体的重链可变区的氨基酸序列如seq id no:26所示,所述抗体的轻链可变区的氨基酸序列如seq id no:27所示。
20.第二方面,本技术提供了结合人cd40的抗体,其中所述抗体的重链可变区的氨基酸序列与seq id no:17、19、21、25和26中任何一项具有至少90%的同源性,并且所述抗体的轻链可变区的氨基酸序列与seq id no:18、20、22和27中任何一项具有至少90%的同源性。
21.在第一方面和第二方面的一些实施方案中,所述抗体能够结合重组人cd40(seq id no:1)和重组猴cd40(seq id no:4)。
22.在第一方面和第二方面的一些实施方案中,所述抗体为所述抗体为全抗体、fab片段、f(ab')2片段或单链fv片段(scfv)。
23.在第一方面和第二方面的一些实施方案中,所述抗体为人源化抗体。
24.在第一方面和第二方面的一些实施方案中,所述抗体为单克隆抗体。
25.在第一方面和第二方面的一些实施方案中,所述抗体还包含选自igg1亚型、igg2亚型或igg4亚型的重链恒定区。
26.在第一方面和第二方面的一些实施方案中,所述抗体还包含选自κ亚型或者λ亚型
的轻链恒定区。
27.第三方面,本技术提供了核酸分子,其编码第一方面或第二方面所述的抗体。
28.第四方面,本技术提供了药物组合物,其包含第一方面或第二方面所述的抗体和药学上可接受的赋形剂、稀释剂或载体。
29.在一些实施方案中,所述药物组合物用于预防或治疗cd40相关的疾病或病症。
30.在一些实施方案中,所述cd40相关的疾病或病症为为癌症,例如选自:淋巴癌、乳腺癌、膀胱癌、肾癌、卵巢癌、宫颈癌、肺癌、鼻咽癌、食管癌、恶性黑色素瘤、白血病、多发性骨髓瘤等。
31.第五方面,本技术提供了第一方面或第二方面所述的抗体在制备用于预防或治疗cd40相关的疾病或病症的药物中的用途。
32.在第五方面的一些实施方案中,所述cd40相关的疾病或病症的药物中的用途;优选地,所述疾病或病症为癌症,例如选自:淋巴癌、乳腺癌、膀胱癌、肾癌、卵巢癌、宫颈癌、肺癌、鼻咽癌、食管癌、恶性黑色素瘤、白血病、多发性骨髓瘤等。
33.第六方面,本技术提供了预防或治疗cd40相关的疾病或病症的方法,包括向有需要的个体给予第一方面或第二方面所述的抗体或第四方面所述的药物组合物。
34.在第六方面的一些实施方案中,所述治疗cd40相关的疾病或病症的药物中的用途;优选地,所述疾病或病症为癌症,例如选自:淋巴癌、乳腺癌、膀胱癌、肾癌、卵巢癌、宫颈癌、肺癌、鼻咽癌、食管癌、恶性黑色素瘤、白血病、多发性骨髓瘤等。
附图说明
35.图1显示elisa分析抗cd40单克隆抗体与不同种属cd40的结合能力。
36.图2显示使用流式细胞仪分析不同抗cd40单克隆抗体结合cd40阳性细胞daudi表面cd40的能力。
37.图3显示化学发光法测定分析抗cd40单克隆抗体激活jurkat-dual hcd40细胞中的nf-κb信号通路的能力。
38.图4显示使用流式细胞仪分析人源化抗cd40单克隆抗体结合cd40阳性细胞jurkat-dual hcd40表面cd40的能力。
39.图5显示化学发光法细胞活力测定分析人源化抗cd40单克隆抗体激活jurkat-dual hcd40细胞中的nf-κb信号通路的能力。
40.图6显示cd40人源化小鼠mc38-hupd-l1皮下移植瘤模型中抗cd40抗体治疗组和对照组小鼠肿瘤体积的生长变化情况。
41.图7显示cd40人源化小鼠mc38-hupd-l1皮下移植瘤模型中抗cd40抗体治疗组和对照组小鼠体重的变化情况。
42.序列说明
43.seq id no:1显示人(homo sapiens)cd40胞外区(hcd40)的氨基酸序列。
44.seq id no:2显示小鼠(mus musculus)cd40胞外区(mcd40)的氨基酸序列。
45.seq id no:3显示人cd40半胱氨酸富集结构域1(crd1)和小鼠cd40半胱氨酸富集结构域2,3,4(crd2-4)嵌合的cd40胞外区(cd40-hcrd1+mcrd2-4)的氨基酸序列。
46.seq id no:4显示食蟹猴(macaca fascicularis)cd40胞外区(mfcd40)的氨基酸
序列。
47.seq id no:5显示his标签(his)的氨基酸序列。
48.seq id no:6显示人(homo sapiens)igg1抗体的fc段(hfc)的氨基酸序列。
49.seq id no:7显示小鼠(mus musculus)igg2a抗体的fc段(mfc)的氨基酸序列。
50.seq id no:8显示人(homo sapiens)igg1亚型重链恒定区的氨基酸序列。
51.seq id no:9显示人(homo sapiens)igg2亚型重链恒定区的氨基酸序列。
52.seq id no:10显示人(homo sapiens)igg4亚型重链恒定区的氨基酸序列。
53.seq id no:11显示小鼠(mus musculus)igg1亚型重链恒定区的氨基酸序列。
54.seq id no:12显示小鼠(mus musculus)igg2a亚型重链恒定区的氨基酸序列。
55.seq id no:13显示人(homo sapiens)κ亚型轻链恒定区的氨基酸序列。
56.seq id no:14显示人(homo sapiens)λ亚型轻链恒定区的氨基酸序列。
57.seq id no:15显示小鼠(mus musculus)κ亚型轻链恒定区的氨基酸序列。
58.seq id no:16显示小鼠(mus musculus)λ亚型轻链恒定区的氨基酸序列。
59.seq id no:17显示鼠单克隆抗体s1h5重链可变区序列的氨基酸序列。
60.seq id no:18显示鼠单克隆抗体s1h5轻链可变区序列的氨基酸序列。
61.seq id no:19显示鼠单克隆抗体s2a7重链可变区序列的氨基酸序列。
62.seq id no:20显示鼠单克隆抗体s2a7轻链可变区序列的氨基酸序列。
63.seq id no:21显示鼠单克隆抗体s6g2重链可变区序列的氨基酸序列。
64.seq id no:22显示鼠单克隆抗体s6g2轻链可变区序列的氨基酸序列。
65.seq id no:23显示人(homo sapiens)抗cd40对照抗体cp-870893重链的氨基酸序列。
66.seq id no:24显示人(homo sapiens)抗cd40对照抗体cp-870893轻链的氨基酸序列。
67.seq id no:25显示鼠单克隆抗体s2a7重链人源化版本s2a7vh-h2的氨基酸序列。
68.seq id no:26显示鼠单克隆抗体s2a7重链人源化版本s2a7vh-h3的氨基酸序列。
69.seq id no:27显示鼠单克隆抗体s2a7轻链人源化版本s2a7vk-h2的氨基酸序列。
70.seq id no:28和29分别显示s2a7、s2a7vh-h2和s2a7vh-h3的hcdr1和hcdr2的氨基酸序列。
71.seq id no:30显示s2a7、s2a7vh-h2、s2a7vh-h3和s1h5的hcdr3的氨基酸序列。
72.seq id no:31显示s2a7、s2a7vk-h2和s1h5的lcdr1的氨基酸序列。
73.seq id no:32显示s2a7、s2a7vk-h2、s1h5和s6g2的lcdr2的氨基酸序列。
74.seq id no:33显示s2a7和s2a7vk-h2的lcdr3的氨基酸序列。
75.seq id no:34-36分别显示s1h5的hcdr1、hcdr2和lcdr3的氨基酸序列。
76.seq id no:37-41分别显示s6g2的hcdr1、hcdr2、hcdr3、lcdr1和lcdr3的氨基酸序列。
77.seq id no:42显示引物pmcgr的核苷酸序列。
78.seq id no:43显示引物pmckr的核苷酸序列。
79.发明详细描述
80.本技术的发明人通过抗体工程技术得到了新的抗人cd40抗体。在本技术的多个方
面,提供了新的抗人cd40抗体,编码该抗体的核酸分子、包含所述核酸分子的载体、包含所述核酸分子或载体的宿主细胞、制备和纯化该抗体的方法及所述抗体的医学和生物学应用。根据本技术提供的抗体的可变区的序列,可构建全长的抗体分子作为药物用于治疗临床上cd40相关的疾病或病症。
81.除非另外指明,本技术的实施采用本领域常规的分子生物学、微生物学、细胞生物学、生物化学以及免疫学技术。
82.除非另外指明,本技术中所用的术语具有本领域技术人员通常所理解的含义。
83.定义
84.如本文所用术语“抗体”是指能够经由至少一个位于免疫球蛋白分子的可变区中的抗原识别位点特异性结合到靶标的免疫球蛋白分子。靶标包括但不限于碳水化合物、多聚核苷酸、脂质、多肽等。本文所使用的“抗体”不仅包括完整的(即全长的)抗体,而且还包括其抗原结合片段(例如fab、fab'、f(ab')2、fv)、其变异体、包含抗体部分的融合蛋白、人源化抗体、嵌合抗体、双抗体、线性抗体、单链抗体、多特异性抗体(例如双特异性抗体)及任何其他包含所需特异性的抗原识别位点的免疫球蛋白分子的修改配置,包括抗体的糖基化变体、抗体的氨基酸序列变体及共价修饰的抗体。
85.通常,完整或全长的抗体包含两个重链和两个轻链。每个重链含有重链可变区(vh)和第一、第二及第三恒定区(ch1、ch2及ch3)。每个轻链含有轻链可变区(vl)和恒定区(cl)。全长的抗体可以是任何种类的抗体,例如igd、ige、igg、iga或igm(或上述的子类),但抗体不需要属于任何特定的类别。根据重链的恒定域的抗体氨基酸序列,可以将免疫球蛋白指定为不同的类别。通常,免疫球蛋白有五种主要的类别:iga、igd、ige、igg及igm,而且这些类别中有几个可以再被进一步区分成子类(同型),例如igg1、igg2、igg3、igg4、iga1及iga2。对应于不同免疫球蛋白类别的重链恒定域分别称为α、δ、ε、γ、以及μ。不同类别的免疫球蛋白的子单元结构和三维结构是公知的。
86.如本文所用术语“抗原结合片段或抗原结合部分”是指负责结合抗原的完整抗体分子的一部分或区域。抗原结合域可以包含重链可变区(vh)、轻链可变区(vl)或上述两者。vh和vl中的每个通常含有三个互补决定区cdr1、cdr2及cdr3。
87.本领域技术人员公知,互补决定区(cdr,通常有cdr1、cdr2及cdr3)是可变区中对抗体的亲和力和特异性影响最大的区域。vh或vl的cdr序列有两种常见的定义方式,即chothia定义和kabat定义。(参阅例如kabat,“sequences of proteins of immunological interest”,national institutes of health,bethesda,md.(1991);a1-lazikani等人,j.mol.biol.273:927-948(1997);以及martin等人,proc.natl.acad.sci.usa86:9268-9272(1989)。对于给定抗体的可变区序列,可以根据chothia定义或者kabat定义来确定vh和vl序列中的cdr序列。在本技术的实施方案中,利用kabat定义cdr序列。
88.对于给定抗体的可变区序列,可以通过多种方式分析可变区序列中的cdr序列,例如可以利用在线软件abysis确定(http://www.abysis.org/)。
89.抗原结合片段的实例包括但不限于:(1)fab片段,其可以是具有vl-cl链和vh-ch1链的单价片段;(2)f(ab')2片段,其可以是具有两个fab'片段的二价片段,该两个fab'片段由铰链区的二硫桥(即fab'的二聚物)连接;(3)具有抗体的单臂的vl和vh域的fv片段;(4)单链fv(scfv),其可以是由vh域和vl域经由胜肽连接符组成的单一多胜肽链;以及(5)
(scfv)2,其可以包含两个由胜肽连接符连接的vh域和两个vl域,该两个vl域是经由二硫桥与该两个vh域组合。
90.在本文描述抗体结构时,涉及氨基酸位置编号的描述参照人igg1抗体的eu numbering定义,这是本领域技术人员公知且容易查询到的。此外,在本文结合eu numbering位置描述突变时,是指相对于天然抗体序列产生的突变。
91.如本文所用术语“fc片段”、“fc结构域”、“fc部分”或类似的术语是指抗体重链恒定区的一部分,包括铰链区(hinge)、恒定区的ch2片段和ch3片段。参照人igg1抗体的eu numbering定义,fc片段是抗体恒定区中第216-447位的氨基酸序列。
92.如本文所用术语“特异性结合”是指两个分子之间的非随机结合反应,例如抗体至抗原表位的结合。
93.如本文所用术语“人源化抗体”主要指鼠源单克隆抗体以基因克隆及dna重组技术改造,重新表达的抗体,其大部分氨基酸序列被人源序列取代,基本保留亲本鼠单克隆抗体的亲和力和特异性,又降低了其异源性,有利应用于人体。人源化抗体的恒定区部分(即ch和cl区)或抗体所有全部由人类抗体基因所编码。人源化抗体可以大大减少异源抗体对人类机体造成的免疫副反应。人源化抗体包括嵌合抗体、改型抗体和全人源化抗体等几类。
94.如本文所用术语“单克隆抗体”指由基本同质的抗体群体获得的抗体,即,除了可能在少量个体中存在自然发生的突变以外,组成群体的各个抗体是相同的。本文所述单克隆抗体特别包括“嵌合”抗体,其中重链和/或轻链的一部分与来源于具体物种或属于具体抗体类或亚类的抗体中的对应序列相同或同源,而重链和/或轻链的余下部分与来源于另一物种或属于另一抗体类或亚类的抗体中的对应序列相同或同源,并且还包括这样的抗体的片段,只要它们能表现出所期望的生物学活性(美国专利号4,816,567;和morrison等人,proc.natl.acad.sci.usa 81:6851-6855(1984)。
95.如本文所用术语“同源性”被定义为经过序列比对和引入空位后,氨基酸或核苷酸序列变体中相同的残基的百分比,如果需要,达到最大百分比的同源性。用于比对的方法和计算机程序在本领域内是公知的。
96.第一方面,本技术提供了结合人cd40的抗体,其包含含hcdr1、hcdr2和hcdr3氨基酸序列的重链可变区和含lcdr1、lcdr2和lcdr3氨基酸序列的轻链可变区,其中
97.所述hcdr1氨基酸序列如seq id no:28、34或37所示,所述hcdr2氨基酸序列如seq id no:29、35或38所示,所述hcdr3氨基酸序列如seq id no:30或39所示,所述lcdr1氨基酸序列如seq id no:31或40所示,所述lcdr2氨基酸序列如seq id no:32所示,所述lcdr3氨基酸序列如seq id no:33、36或41所示;
98.其中hcdr和lcdr氨基酸序列根据kabat定义。
99.在一些实施方案中,所述抗体的重链可变区的氨基酸如seq id no:17、19、21、25或者26所示。
100.在一些实施方案中,所述抗体的轻链可变区的氨基酸如seq id no:18、20、22或者27所示。
101.在一些实施方案中,所述抗体的重链可变区的氨基酸序列如seq id no:17所示,所述抗体的轻链可变区的氨基酸序列如seq id no:18所示;或者
102.所述抗体的重链可变区的氨基酸序列如seq id no:19所示,所述抗体的轻链可变
区的氨基酸序列如seq id no:20所示;或者
103.所述抗体的重链可变区的氨基酸序列如seq id no:21所示,所述抗体的轻链可变区的氨基酸序列如seq id no:22所示;或者
104.所述抗体的重链可变区的氨基酸序列如seq id no:25所示,所述抗体的轻链可变区的氨基酸序列如seq id no:27所示;或者
105.所述抗体的重链可变区的氨基酸序列如seq id no:26所示,所述抗体的轻链可变区的氨基酸序列如seq id no:27所示。
106.第二方面,本技术提供了结合人cd40的抗体,其中所述抗体的重链可变区的氨基酸序列与seq id no:17、19、21、25和26中任何一项具有至少90%的同源性,并且所述抗体的轻链可变区的氨基酸序列与seq id no:18、20、22和27中任何一项具有至少90%的同源性。
107.在第二方面的一些实施方案中,所述抗体的重链可变区的氨基酸序列与seq id no:17、19、21、25和26中任何一项具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高的同源性。
108.在第二方面的一些实施方案中,所述抗体的轻链可变区的氨基酸序列与seq id no:18、20、22和27中任何一项具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高的同源性。
109.在第二方面的一些实施方案中,所述抗体的重链可变区的氨基酸序列与seq id no:17、19、21、25和26中任何一项所示的氨基酸序列相差约1、2、3、4、5、6、7、8、9、或10个氨基酸的取代、缺失和/或添加。
110.在第二方面的一些实施方案中,所述抗体的轻链可变区的氨基酸序列与seq id no:18、20、22和27中任何一项所示的氨基酸序列相差约1、2、3、4、5、6、7、8、9、或10个氨基酸的取代、缺失和/或添加。
111.在第二方面的一些实施方案中,seq id no:17、19、21、25和26中任何一项所示的氨基酸序列的c端或n端区域还可以被截短约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、20、25或更多个氨基酸,而仍然保持类似的所述抗体的重链可变区的功能。
112.在第二方面的一些实施方案中,还可以在seq id no:17、19、21、25和26中任何一项所示的氨基酸序列的c端或n端区域添加1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、20、25或更多个氨基酸,得到的氨基酸序列仍然保持类似的所述抗体的重链可变区的功能。
113.在第二方面的一些实施方案中,还可以在seq id no:17、19、21、25和26中任何一项所示的氨基酸序列的c端或n端以外的区域添加或缺失1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、20、25或更多个氨基酸,只要改变后的氨基酸序列基本上保持类似的所述抗体的重链可变区的功能。
114.在第二方面的一些实施方案中,seq id no:18、20、22和27中任何一项所示的氨基酸序列的c端或n端区域还可以被截短约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、20、25或更多个氨基酸,而仍然保持类似的所述抗体的轻链可变区的功能。
115.在第二方面的一些实施方案中,还可以在seq id no:18、20、22和27中任何一项所示的氨基酸序列的c端或n端区域添加1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、20、25或更多个氨基酸,得到的氨基酸序列仍然保持类似的所述抗体的轻链可变区的功能。
116.在第二方面的一些实施方案中,还可以在seq id no:18、20、22和27中任何一项所示的氨基酸序列的c端或n端以外的区域添加或缺失1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、20、25或更多个氨基酸,只要改变后的氨基酸序列基本上保持类似的所述抗体的轻链可变区的功能。
117.在第一方面和第二方面的一些实施方案中,所述抗体能够结合重组人cd40(seq id no:1)和重组猴cd40(seq id no:4)。
118.在第一方面和第二方面的一些实施方案中,所述抗体为全抗体、fab片段、f(ab')2片段或单链fv片段(scfv)。
119.在第一方面和第二方面的一些实施方案中,所述抗体为人源化抗体。
120.在第一方面和第二方面的一些实施方案中,所述抗体为单克隆抗体。
121.在第一方面和第二方面的一些实施方案中,所述抗体还包含选自igg1亚型、igg2亚型或igg4亚型的重链恒定区。
122.在第一方面和第二方面的一些实施方案中,所述抗体的重链恒定区可以是人igg1亚型、人igg2亚型、人igg4亚型、鼠igg1亚型或鼠igg2a亚型。
123.在第一方面和第二方面的一些具体实施方案中,所述重链恒定区为igg1亚型。
124.在第一方面和第二方面的一些具体实施方案中,所述抗体的重链恒定区包含人igg1亚型重链恒定区的fc段序列并且所述fc序列的第234、235和331位的氨基酸序列分别为f、e和s,其中抗体恒定区氨基酸序列顺序按照eu numbering来确定。
125.在第一方面和第二方面的一些实施方案中,所述抗体还包含选自κ亚型或者λ亚型的轻链恒定区。
126.在第一方面和第二方面的一些实施方案中,所述抗体的轻链恒定区可以是人κ亚型、人λ亚型、鼠κ亚型或者鼠λ亚型。
127.第三方面,本技术提供了核酸分子,其编码第一方面或第二方面所述的抗体。
128.在一些实施方案中,所述核酸分子可操作地连接到调控序列,调控序列可以被用所述载体转化过的宿主细胞识别。
129.第四方面,本技术提供了药物组合物,其包含第一方面或第二方面所述的抗体和药学上可接受的赋形剂、稀释剂或载体。
130.在一些实施方案中,所述药物组合物用于预防或治疗cd40相关的疾病或病症。
131.在一些实施方案中,所述cd40相关的疾病或病症的药物中的用途;优选地,所述疾病或病症为癌症,例如选自:淋巴癌、乳腺癌、膀胱癌、肾癌、卵巢癌、宫颈癌、肺癌、鼻咽癌、食管癌、恶性黑色素瘤、白血病、多发性骨髓瘤等。
132.在一些实施方案中,所述药物组合物还可包含下述中的一种或多种:润滑剂,如滑石粉、硬脂酸镁和矿物油;润湿剂;乳化剂;悬浮剂;防腐剂,如苯甲酸、山梨酸和丙酸钙;增甜剂和/或调味剂等。
133.在一些实施方案中,可将本技术中的药物组合物配制为片剂、丸剂、粉剂、锭剂、酏剂、悬液、乳剂、溶液、糖浆、栓剂或胶囊等形式。
134.在一些实施方案中,可以利用任何生理上可接受的给药方式递送本技术的药物组合物,这些给药方式包括但不限于:口服给药、肠胃外给药、经鼻给药、直肠给药、腹膜内给药、血管内注射、皮下给药、经皮给药、吸入给药等。
135.在一些实施方案中,可以通过混合具有所需纯度的试剂与视情况的药学上可接受的载体、赋形剂等,以冻干制剂或水溶液的形式配制用于治疗用途的药物组合物用于存储。
136.第五方面,本技术提供了第一方面或第二方面所述的抗体在制备用于预防或治疗cd40相关的疾病或病症的药物中的用途。
137.在一些实施方案中,所述cd40相关的疾病或病症的药物中的用途;优选地,所述疾病或病症为癌症,例如选自:淋巴癌、乳腺癌、膀胱癌、肾癌、卵巢癌、宫颈癌、肺癌、鼻咽癌、食管癌、恶性黑色素瘤、白血病、多发性骨髓瘤等。
138.第六方面,本技术提供了预防或治疗cd40相关的疾病或病症的方法,包括向有需要的个体给予第一方面或第二方面所述的抗体或第四方面所述的药物组合物。
139.在一些实施方案中,所述cd40相关的疾病或病症的药物中的用途;优选地,所述疾病或病症为癌症,例如选自:淋巴癌、乳腺癌、膀胱癌、肾癌、卵巢癌、宫颈癌、肺癌、鼻咽癌、食管癌、恶性黑色素瘤、白血病、多发性骨髓瘤等。
140.在其他方面,本技术还提供编码本技术抗体或其轻链或重链的分离的核酸分子以及包含所述核酸分子的载体、包含所述载体的宿主细胞以及产生所述抗体的方法。在一些实施方案中,所述核酸分子可操作地连接到调控氨基酸序列,调控氨基酸序列可以被用所述载体转化过的宿主细胞识别。在一些实施方案中,产生抗体的方法包括培养宿主细胞以便于表达核酸。在一些实施方案中,产生抗体的方法还包括从宿主细胞培养基中回收抗体。
141.此外,本文所述的特异性结合人cd40的抗体也可用于检测生物样品中cd40的存在。基于抗体的检测方法在本领域是众所周知的,并且包括例为elisa、免疫印迹、放射免疫试验、免疫荧光、免疫沉淀以及其它相关技术。
142.应当理解,以上详细描述仅为了使本领域技术人员更清楚地了解本技术的内容,而并非意图在任何方面加以限制。本领域技术人员能够对所述实施方案进行各种改动和变化。
实施例
143.以下实施例仅用于说明而非限制本技术范围的目的。
144.实施例1:重组蛋白的制备
145.制备抗cd40单克隆抗体的过程中需要用到多种不同的重组蛋白,包括人cd40胞外区(hcd40,seq id no:1)、小鼠cd40胞外区(mcd40,seq id no:2)、人cd40半胱氨酸富集结构域1(crd1)和小鼠cd40半胱氨酸富集结构域2,3,4(crd2-4)嵌合的cd40胞外区(cd40-hcrd1+mcrd2-4,seq id no:3)、食蟹猴cd40胞外区(mfcd40,seq id no:4)。这些蛋白都有大量的翻译后修饰(如:糖基化或二硫键等),因而利用哺乳动物细胞表达系统将更有利于保持重组蛋白的结构和功能。此外,在这些重组蛋白的c端添加his标签(his,seq id:5)、人抗体igg1的fc段(fc,seq id:6)或者鼠抗体igg2a的fc段(mfc,seq id:7),将更有利于重组蛋白的纯化和单克隆抗体功能的鉴定。抗体重链恒定区可以是人igg1亚型(seq id no:8)、人igg2亚型(seq id no:9)、人igg4亚型(seq id no:10)、鼠igg1亚型(seq id no:11)或者鼠igg2a亚型(seq id no:12),轻链恒定区可以是人κ亚型(seq id no:13)、人λ亚型(seq id no:14)、鼠κ亚型(seq id no:15)或者鼠λ亚型(seq id no:16)。根据uniprot数据库的各种目的重组蛋白的氨基酸序列,设计并合成上述各种重组蛋白的基因(包含his标签或者
fc、mfc编码基因)。利用常规的分子生物学技术将合成的各种重组蛋白基因克隆至合适的真核表达载体(如invitrogen公司的pcdna3.1等),然后利用脂质体(如invitrogen公司的293fectin等)或者其他阳离子转染试剂(如pei等)将制备的重组蛋白表达质粒转染入hek293细胞(如invitrogen公司的hek293f),在无血清悬浮培养条件下培养3-4天,然后通过离心等方式收获培养上清。
146.his标签融合表达的重组蛋白利用金属螯合亲和层析柱(如ge公司的histrap ff等)对培养上清中的重组蛋白进行一步纯化,fc和mfc融合表达的重组蛋白用proteina/g亲和层析柱(如ge公司的mabselect sure等)进行一步纯化。利用脱盐柱(如ge公司的hitrap desaulting等)将重组蛋白保存缓冲液置换为pbs(ph7.0)或者其他合适的缓冲液。必要时,可以对抗体样品进行过滤除菌,然后分装保存于-20℃。
147.实施例2:小鼠免疫库的构建
148.取6-8周龄balb/c小鼠,首次免疫每只小鼠腹腔注射100μg融合蛋白cd40-hcrd1+mcrd2-4-his,之后间隔两周加强免疫,每只小鼠腹腔注射50μg重组蛋白,共加强4次。末次免疫,以不加佐剂的cd40-hcrd1+mcrd234-his重组蛋白作为免疫原,每只小鼠腹腔注射100μg,冲击免疫后3天处死小鼠,收集脾细胞。
149.使用小鼠淋巴细胞分离液(达科为生物技术股份有限公司,cat#dkw33-r0100)分离小鼠脾脏淋巴细胞,利用细胞总rna提取试剂盒(天根生化科技(北京)有限公司,cat#dp430)提取淋巴细胞总rna。以提取的总rna为模板,利用第一链cdna合成试剂盒(thermo scientific,cat#k1621)分别合成编码重链可变区和轻链可变区的基因,反转录引物采取基因特异性引物,引物配对区分别位于抗体重链恒定区和抗体轻链恒定区,具体序列分别为pmcgr:tgcatttgaactccttgcc(seq id no:42)和pmckr:ccatcaatcttccacttgac(seq id no:43)。合成的cdna立即存放于-70℃保存备用。然后以反转录得到的cdna为模板,参考文献(journal of immunological methods,201(1997),35
–
55,通过引用方式将上述文献的全部内容并入本文中)合成引物,并利用pcr分别扩增编码鼠抗体vh和vk的基因,然后利用重叠延伸pcr技术,构建单链抗体(scfv)基因。最后将制备的小鼠单链抗体基因克隆至载体padscfv-s构建scfv库(实验技术流程可参见中国专利申请第201510097117.0号的实施例1,通过引用方式将上述专利申请的全部内容并入本文中)。此抗体库的库容达到4.2e+07,正确率为65%。
150.实施列3:鼠抗人cd40单链抗体库的筛选和鉴定
151.3.1小鼠免疫库的筛选
152.参照文献(中国专利申请第201510097117.0号,通过引用方式将上述专利申请的全部内容并入本文中),以实施例1制备的重组人cd40-his为抗原,利用固相筛选策略(实验方案参考噬菌体展示:通用实验指南/(美)克拉克森(clackson,t.),(美)洛曼(lowman,h.b.)编,马岚等译,化学工业出版社,2008年5月)筛选上述构建的展示小鼠单链抗体的噬菌体库,通过结合、洗脱、中和、感染、扩增的方式共进行三轮筛选,最终获得多株序列不同,但均能结合人cd40的单链抗体,包括克隆s2a7、s1h5和s6g2。
153.利用常规分子生物学方法,分别将编码s1h5(重链氨基酸序列如seq id no:17所示,轻链氨基酸序列如seq id no:18所示)、s2a7(重链氨基酸序列如seq id no:19所示,轻链氨基酸序列如seq id no:20所示)和s6g2(重链氨基酸序列如seq id no:21所示,轻链氨
基酸序列如seq id no:22所示)三个分子的轻重链基因克隆至真核表达载体,制备重组人igg1m3-κ形式鼠-人嵌合抗体。同时,参照imgt公布序列制备人源抗cd40单抗cp-870893作为阳性对照(重链氨基酸序列如seq id no:23所示,轻链氨基酸序列如seq id no:24所示)。
154.3.2重组抗cd40单克隆抗体的亲和力分析
155.利用biacore x100通过表面等离子共振技术测定抗cd40抗体的亲和力。氨基偶联试剂盒(br-1000-50)、人抗体捕获试剂盒(br-1008-39)、cm5芯片(br100012)和ph7.4的10
×
hbs-ep(br100669)等相关试剂和耗材均购自ge healthcare。依照试剂盒中的说明书,用1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(1-ethyl-3-(3-dimethylaminopropyl)carbodiimide hydrochloride,edc)和n-羟基琥珀酰亚胺(n-hydroxysuccinimide,nhs)对羧基化cm5芯片表面进行活化,将抗人igg(fc)抗体(捕获抗体)用10mm ph5.0乙酸钠稀释至25μg/ml,之后以10μl/min的流速注射以实现大约10000个响应单位(ru)的偶联量。注射捕获抗体之后,注射1m乙醇胺以封闭未反应的基团。对于动力学测量,稀释抗cd40抗体至0.5-1μg/ml,以10μl/min的流速注射,保证130-150ru左右的抗体被抗人fc的抗体捕获。然后将hcd40-his设置一系列的浓度梯度(例如0.62nm、1.85nm、5.56nm、16.7nm、50nm),于25℃下以30μl/min的流速从低浓度到高浓度进行注射,结合时间为120s,解离时间为300s-1200s,以10μl/min的流速注射3m的mgcl
2 30s以对芯片表面进行再生。使用biacore x100评估软件第2.0.1版,通过1:1结合模型拟合结合和解离传感图来计算结合速率(ka)和解离速率(kd),以比率kd/ka计算解离平衡常数(kd),拟合结果如表1所示。
156.表1.重组抗cd40单克隆抗体结合hcd40的亲和力常数
[0157] kakdkdcp-8708931.369e+52.058e-31.503e-8s1h54.848e+66.669e-31.376e-9s2a75.312e+63.037e-35.717e-10s6g29.952e+53.556e-23.573e-8
[0158]
3.3重组抗cd40单克隆抗体与不同种属cd40的结合
[0159]
分别用制备的人cd40(hcd40-his)、食蟹猴cd40(mfcd40-his)和小鼠cd40(mcd40-his)包被96孔elisa板(3μg/ml、100μl/孔),4℃包被过夜。利用封闭液pbs-0.1%吐温20-3%牛奶在37℃封闭1小时后,分别加入各重组抗cd40单克隆抗体(10μg/ml,100μl/孔,2个复孔),37℃结合1小时。用pbs-0.1%吐温20缓冲液洗涤elisa板,然后100μl/孔加入1:5000稀释的hrp鼠抗人igg(bioss,bsm-0297m-hrp),37℃结合1小时。使用pbs-0.1%吐温20缓冲液洗涤elisa板,加入opd底物显色液,5-10分钟后用1m的h2so4终止显色,使用酶标仪测定492nm/630nm的双波长光密度值。elisa分析结果(图1)显示,所有分子都识别hcd40-his并交叉识别mfcd40-his,所有分子都不识别mcd40-his。
[0160]
3.4重组抗cd40单克隆抗体结合细胞表面cd40抗原的鉴定
[0161]
取生长对数期的daudi(人burkitt's淋巴瘤细胞,中国人民解放军军事医学研究院赠送),离心后用含1%bsa的pbs缓冲液重悬至3
×
106个/ml,100μl/孔铺于96孔v底板中。用pbs将待测样品s1h5、s2a7、s6g2和对照抗体cp-870893以及igg1m3-κ同型对照抗体进行梯度稀释,抗cd40单克隆抗体起始浓度20μg/ml,3倍梯度稀释,共11个浓度点。分别取100μl
抗cd40单克隆抗体加入含细胞的孔中,4℃孵育1小时。然后用200μl pbs溶液洗3遍,孵育羊抗人igg-fitc(北京中杉金桥生物技术有限公司,zf-0308),100μl/孔,4℃避光30分钟后用200μl pbs溶液洗3遍,并用100μl pbs溶液重悬后用流式细胞仪(acea,novocyte)检测fitc通道。结果显示,抗cd40单克隆抗体s1h5、s2a7、s6g2和对照抗体cp-870893均能很好的结合cd40阳性细胞daudi(图2)。
[0162]
3.5重组抗cd40单克隆抗体激活nf-κb信号通路的鉴定
[0163]
jurkat-dual细胞(购自invivogen)具有lucia荧光素酶基因,由ifn-β最小启动子驱动,该启动子融合了5个nf-κb的转录应答元件和3个c-rel结合位点。jurkat-dual hcd40细胞为本公司构建,是基于jurkat-dual细胞转入人cd40基因得到的。
[0164]
取生长对数期的jurkat-dual hcd40细胞,离心后用测试培养基(rpmi1640+10%热灭活fbs+1%p.s.)重悬至5
×
105个/ml,100μl/孔铺于96孔细胞板中。用测试培养基将待测样品s1h5、s2a7、s6g2、对照抗体cp-870893以及igg1m3-κ同型对照抗体进行梯度稀释,抗cd40单克隆抗体起始浓度为20μg/ml,3倍梯度稀释,共11个浓度点。分别取100μl抗cd40单克隆抗体加入含细胞的孔中,将细胞板置于co2培养箱37℃正常培养。孵育20小时后,取上清,参照quanti-luc
tm
说明书(quanti-luc
tm
,invivogen,rep-qlc2)检测和分析抗cd40单克隆抗体对jurkat-dual hcd40细胞的特异性激活。结果(图3)显示,抗cd40单克隆抗体s1h5、s2a7、s6g2和对照抗体cp-870893均能很好的激活jurkat-dual hcd40细胞中的nf-κb信号通路。
[0165]
实施例4:s2a7鼠单克隆抗体的人源化改造
[0166]
4.1s2a7鼠单克隆抗体的人源化改造
[0167]
对鼠源单克隆抗体s2a7(重链可变区序列为seq id no:19;轻链可变区序列为seq id no:20)进行人源化研究以降低其免疫原性。将编码s2a7的重链可变区(vh)和轻链可变区(vl)的基因分别与imgt数据库中的人抗体胚系基因序列相比较,选择合适的胚系基因序列以提供抗体的框架区1至3(fr1+fr2+fr3),选择合适的j区基因序列以提供框架区4(fr4)。这个模板可以根据多种因素选出,如:抗体的相对总长度、cdr区的大小、位于抗体框架区(fr)和超变区(cdr)之间连接处的氨基酸残基、序列整体的同源性等。所选的模板可以是多个序列的嵌合版本或者可以是共有模板(consensus sequence),目的是尽可能维持亲本互补决定区(cdr)的合适构象。对s2a7的重链进行cdr移植得到两个人源化版本s2a7vh-h2(seq id no:25)和s2a7vh-h3(seq id no:26);对s2a7的轻链进行cdr移植得到一个人源化版本s2a7vk-h2(seq id no:27)。根据人源化抗体的氨基酸序列设计并合成抗体可变区基因并克隆至真核表达载体。将s2a7vh-h2、s2a7vh-h3分别配合s2a7vk-h2组合表达人igg1m3版本全抗体s2a7vh-h2+s2a7vk-h2和s2a7vh-h3+s2a7vk-h2。
[0168]
4.2 s2a7人源化单克隆抗体的亲和力分析
[0169]
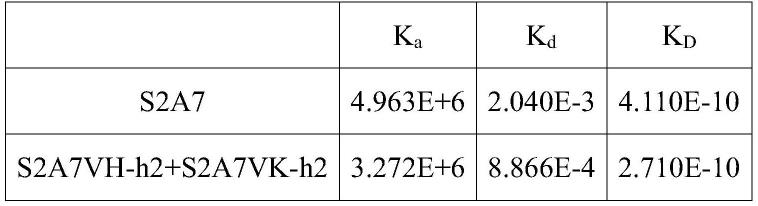
参照实施例3.2,用biacore x100对s2a7人源化单克隆抗体(s2a7vh-h2+s2a7vk-h2和s2a7vh-h3+s2a7vk-h2)进行亲和力分析。将抗人igg(fc)抗体(捕获抗体)偶联至cm5芯片表面,捕获s2a7及其人源化单克隆抗体,将hcd40-his作为流动相(cd40浓度梯度为0.247nm、0.74nm、2.22nm、6.67nm、20nm),结合120s,解离1200s。使用biacore x100评估软件第2.0.1版,通过1:1结合模型拟合结合和解离传感图来计算结合速率(ka)和解离速率(kd),以比率kd/ka计算解离平衡常数(kd),拟合结果如表2所示。
[0170]
表2.s2a7人源化单克隆抗体结合hcd40的亲和力常数
[0171][0172][0173]
4.3人源化抗cd40单克隆抗体结合细胞表面cd40抗原的鉴定
[0174]
取生长对数期的jurkat-dual hcd40细胞,离心后用含1%bsa的pbs缓冲液重悬至3
×
106个/ml,100μl/孔铺于96孔v底板中。用pbs将待测样品s2a7、s2a7vh-h2+s2a7vk-h2和s2a7vh-h3+s2a7vk-h2进行梯度稀释,抗cd40单克隆抗体的起始浓度20μg/ml,3倍梯度稀释,共11个浓度点。分别取100μl抗cd40单克隆抗体加入含细胞的孔中,4℃孵育1小时。然后用200μl pbs溶液洗3遍,孵育羊抗人igg-fitc(北京中杉金桥生物技术有限公司,zf-0308),100μl/孔,4℃避光30分钟。后用200μl pbs溶液洗3遍,100μl pbs溶液重悬后用流式细胞仪(acea,novocyte)检测fitc通道。结果(图4)显示,人源化抗cd40单克隆抗体保持了亲本分子结合cd40阳性细胞jurkat-dual hcd40的活性,ec
50
值见表3。
[0175]
表3.人源化抗cd40单克隆抗体结合jurkat-dual hcd40细胞的ec
50
值
[0176] ec
50
(nm)s2a70.7566s2a7vh-h2+s2a7vk-h20.7608s2a7vh-h3+s2a7vk-h20.8126
[0177]
4.4人源化抗cd40单克隆抗体激活nf-kb信号通路的鉴定
[0178]
取生长对数期的jurkat-dual hcd40细胞,离心后用测试培养基(rpmi1640+10%热灭活fbs+1%p.s.)重悬至5
×
105个/ml,100μl/孔铺于96孔细胞板中。用测试培养基将待测样品s2a7、s2a7vh-h2+s2a7vk-h2和s2a7vh-h3+s2a7vk-h2进行梯度稀释,抗cd40单克隆抗体的起始浓度为20μg/ml,3倍梯度稀释,共11个浓度点。分别取100μl抗cd40单克隆抗体加入含细胞的孔中,细胞板置于co2培养箱37℃正常培养。孵育20小时后,取上清,参照quanti-luc
tm
说明书(quanti-luc
tm
,invivogen,rep-qlc2)检测和分析抗cd40单克隆抗体对jurkat-dual hcd40细胞的特异性激活。结果(图5)显示,人源化抗cd40单克隆抗体较亲本分子激活强度下降,但ec
50
值相当(表4),均能很好的激活jurkat-dual hcd40细胞中的nf-κb信号通路。
[0179]
表4.人源化抗cd40单克隆抗体激活jurkat-dual hcd40细胞中nf-kb信号通路的ec
50
值
[0180] ec
50
(nm)s2a70.05946s2a7vh-h2+s2a7vk-h20.05017
cd40 antigen expression with discrete stages[j].2011.
[0195]
10.o'grady j t,stewart s,lowrey j,et al.cd40 expression in hodgkin's disease[j].the american journal of pathology,1994,144(1):21.
[0196]
11.pellat-deceunynck c,bataille r,robillard n,et al.expression of cd28 and cd40 in human myeloma cells:a comparative study with normal plasma cells[j].1994.
[0197]
12.young l s,eliopoulos a g,gallagher n j,et al.cd40 and epithelial cells:across the great divide[j].immunology today,1998,19(11):502-506.
[0198]
13.ziebold j l,hixon j,boyd a,et al.differential effects of cd40 stimulation on normal and neoplastic cell growth[j].archivum immunologiae et therapiae experimentalis,2000,48(4):225-233.
[0199]
14.gladue r p,cole s h,donovan c,et al.in vivo efficacy of the cd40 agonist antibody cp-870,893against a broad range of tumor types:impact of tumor cd40 expression,dendritic cells,and chemotherapy[j].journal of clinical oncology,2006,24(18_suppl):2514-2514.
[0200]
15.grewal i s,flavell r a.cd40 and cd154 in cell-mediated immunity[j].annual review of immunology,1998,16(1):111-135.
[0201]
16.tong a w,stone m j.prospects for cd40-directed experimental therapy of human cancer[j].cancer gene therapy,2003,10(1):1-13.
[0202]
17.eliopoulos a g,davies c,knox p g,et al.cd40 induces apoptosis in carcinoma cells through activation of cytotoxic ligands of the tumor necrosis factor superfamily[j].molecular and cellular biology,2000,20(15):5503-5515.
[0203]
18.tong a w,papayoti m h,netto g,et al.growth-inhibitory effects of cd40 ligand(cd154)and its endogenous expression in human breast cancer[j].clinical cancer research,2001,7(3):691-703.
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1