一种重组融合蛋白及其在结核诊断中应用的制作方法
1.本发明涉及生物技术领域,具体涉及一种新型重组融合蛋白及其在结核诊断中应用。
2.背景信息
3.结核病是慢性传染性疾病。目前全球已有20亿人感染结核菌,活动性结核患者达1500万,每年新发结核患者达800万~1000万,有180万人因结核病死亡。据who《2008年全球结核病控制报告》估计,2006年我国结核病发病人数为131万,占全球的14.3%,位居全球第二位,是全球22个结核病高负担国家之一。2010年全国结核病流行病学抽样调查结果显示,我国结核病疫情特点是:感染人数多,全国有5亿人口已感染结核菌,明显高于全球平均感染水平;患者数多,全国有活动性肺结核患者约500
‑
600万,其中传染性肺结核患者约86万;死亡人数多,农村患者多,全国约80%肺结核患者在农村,而且主要集中在中西部地区;耐药患者多,特别是耐多药和广泛耐药患者人数多。
4.在我国传染病疫情网络报告中,肺结核报告发病和报告死亡数位居甲、乙类传染病前列。肺结核患者中的3/4为最具有劳动能力的青壮年。结核病仍是制约农村地区特别是贫困地区经济和社会发展的重大疾病之一。同时,我国结核病防治工作还面临着流动人口结核病,耐多药结核病和结核菌/艾滋病病毒双重感染等新的挑战。
5.结核菌可能侵入人体全身各种器官,但主要侵犯肺脏,称为肺结核病。结核病是青年人容易发生的一种慢性和缓发的传染病。潜伏期4~8周。其中80%发生在肺部,其他部位(颈淋巴、脑膜、腹膜、肠、皮肤、骨骼)也可继发感染。人与人之间呼吸道传播是本病传染的主要方式。传染源是接触排菌的肺结核患者。随着环境污染和艾滋病的传播,结核病发病率越发强烈。除少数发病急促外,临床上多呈慢性过程。常有低热、乏力等全身症状和咳嗽、咯血等呼吸系统表现。
6.who估计每年大约有300万的结核患者未被检测到,不仅使得结核感染患者不能及时诊治,同时也加大了家庭和社会群体之间的传播风险。不利因素提醒我们在结核病控制中早期筛查尤为重要,在《柳叶刀》的一篇结核相关文献中,提出了一个重要的观念变革
‑‑
在世界范围内推广“在高危群体中去主动发现病人。”结核的高危人群主要包括两类。一是和结核确诊患者有密切接触的亲属和在共同生活环境中的人员;二是基于各国结核病流行趋势不同的特定人群。现存的发现结核病例的方式主要是被动的发现,即等着患者(如果经济条件和医疗条件允许)自己来寻求医疗救治。这种方式虽然能发现大量的患者,但寻求救治的患者一般已有了明显的症状,可能早就在家庭、群体之间发生了传播。大量没有寻医的患者对公众健康存在极大的隐患。
7.针对确诊的患者的亲属和与其密切接触的人员:一旦发现了结核患者,就应该要求其亲属和与其有密切接触的人员到医疗机构进行结核病筛查。同时,也需在条件允许的情况下主动到患者的家庭及其生活环境中进行筛查。
8.根据结核病感染的特点,具体选择高危人群进行筛查。1)hiv患者:虽然我国整体的hiv发病率达不到5%,但因为hiv感染的人数逐年上升,临床中应该提高门诊hiv患者的
重视程度,尽可能对其进行结核病筛查。2)选择结核病高发区域进行普查。我国是结核病高负荷国家之一,且是人口大国,进行结核病普查显然是不现实的。因此,基于各地区结核发病率的差异,选择发病率高的地区(经济欠发达地区、下级乡镇等)进行普查是一项值得考虑的举措。3)做好医院感控工作,防止结核院内感染。目前我国各级医院经常出现人满为患的情况,应该做好医院感控工作,防止结核院内感染。保证候诊区的通风,及时发现、隔离疑似病例都是有效的手段。
9.传统的结核确诊手段,需要考虑影像学、细菌学、临床表现、分子生物技术等许多方面,如:(1)询问病史和症状,体格检查。(2)胸片、ct等影像学检查。(3)痰涂片抗酸染色查抗酸杆菌。(4)痰培养找结核杆菌。近年发展起来的分枝杆菌快速培养、鉴定和药物敏感性检测技术使原来培养所需时间大大缩短。(5)结核菌素(现一般用tb
‑
ppd试验)。(6)抽血查结核抗体。(7)结核特异性反应t细胞的细胞因子释放试验如t
‑
spot及quantiferon
‑
tb检测方法,有助于鉴别结核分枝杆菌感染,区别于卡介苗接种和其他大多数非结核分枝杆菌感染。(8)结核杆菌聚合酶链反应(tb
‑
pcr)+探针检查。近年开展的分枝杆菌基因芯片检查技术、巢式pcr+反向点杂交分枝杆菌鉴定及耐药基因检测技术,使结核菌鉴定及药物敏感试验时间缩短到只需几个小时,为耐药结核病的及时合理治疗提供了方便。(9)纤维支气管镜检查,包经支气管镜活检、刷检,支气管肺泡灌洗或冲洗液获取标本进行细菌学、细胞学及病理学等检查。(10)临床标本的噬菌体分析方法。(11)经皮穿剌肺组织病理活检。(12)肺外淋巴结或其它器官的病理活检。
10.比较在上述诊断方法中,虽然经典的结核菌素试验已经应用了100年,但是该方法敏感性低,特异性差,不能鉴别卡介苗接种者,血清结核抗体检测等方法的敏感性和特异性不理想;近几年兴起的γ干扰素释放试验的试剂昂贵,技术复杂,需要特殊的设备和培训,不适合基层医疗单位或者现场应用。
11.结核菌素是结核分枝杆菌培养滤液蛋白,作用于人体会激发致敏机体产生iv型超敏反应,iv型超敏反应是由t淋巴细胞介导,通常在抗原攻击后48小时才能表现出来,其核心是cd4+和/或cd8+效应t细胞在识别靶抗原后造成的以淋巴细胞浸润为主要病理特征的炎症损伤。患过结核或者接种过卡介苗的人在皮下注射tb
‑
ppd 24小时会出现炎性硬结,48
‑
72小时达到高峰,有时会出现全身反应。通常反应强度与细胞免疫呈平行关系。tb
‑
ppd已经成为临床上最常用且最简便的一种结核菌感染诊断方法,反应越强,表示结核感染可能性越大,我国一直使用硬结≥5mm为阳性,≥20mm或有水泡、坏死、淋巴结炎等为强阳性,3岁以下儿童≥15mm为强阳性的标准。
12.用于结核病皮肤试验的主要试剂有以下几种:(1)旧结核菌素,不易标准化和易发生非特异性反应,已经被淘汰;(2)tb
‑
ppd,人型结核菌素;(3)bcg
‑
ppd,牛型结核菌素,是卡介苗培养液纯蛋白衍生物,主要用于卡介苗接种是否成功;(4)结核菌重组38kd蛋白,是一种新的皮试抗原,有结核感染者反应强,卡介苗接种者反应弱的特点。
13.当前大规模人群筛查主要手段是tb
‑
ppd筛查。但是,tb
‑
ppd不能区分卡介苗(bcg)接种或是结核杆菌感染,假阳性的结果影响结核病筛查。因此,临床急需一种价格合适的,应用简便,无需特殊仪器,适合基层医疗单位的皮肤诊断试剂。
14.来源于致病性结核杆菌的esat
‑
6和cfp
‑
10两个抗原,在所有的bcg疫苗株中缺失,使得esat
‑
6和cfp
‑
10有望成为新一代诊断试剂的核心抗原,人群中特异性可以达到93%,
远高于tb
‑
ppd的7%
1.。
15.2004年中国药品生物制品检定所申请了esat
‑
6蛋白在诊断结核病中的用途,该发明公开了esat
‑
6蛋白作为一种结核病鉴别诊断用变态反应原的用途。用于卡介苗接种或结核杆菌既往感染但是体内已经无结核活菌者与结核杆菌感染且体内仍有结核活菌者的鉴别,尤其可用于结核高危人群的筛选。该项目在2017年开展了iii期临床,数据表明esat
‑
6特异性很高,但是敏感性低于80%。
16.2015年12月安徽智飞龙科马生物制药有限公司启动了“重组结核杆菌esat6
‑
cfp10融合蛋白”诊断试剂的iii期临床试验。试验剂量为1μg/0.1ml的ec蛋白(clinicaltrials.gov number nct02623556)。采用的技术是e.coli表达esat
‑
6和cfp
‑
10融合蛋白,将esat
‑
6的终止子和cfp起始密码子替换为kpn i的粘性末端(ggtacc),由此制备的融合蛋白是:resat6
‑‑
甘氨酸(gly)
‑
苏氨酸(thr)
‑‑
rcfp10,2015年9月申请了发明专利
2.,该重组蛋白可用于结核菌潜伏感染人群的筛查以及结核病的辅助诊断,克服了通用的特异性γ
‑
ifn检测方法价格昂贵、设备及操作人员要求高的缺点,使用方便、易于推广、适合于大规模普及。该产品与2020年下半年上市。
17.2008年丹麦血清研究所发表了对重组蛋白rdesat
‑
6和tb
‑
ppd结核感染临床诊断(i期:单中心剂量爬坡,双盲随机)比较研究(trial code:tesat
‑
01,eudract no.2005
‑
001850
‑
26)
3.。研究的目的是比较重组二聚体rdesat
‑
6(0.01μg、0.1μg、1μg、10μg)和tb
‑
ppd(2tu)皮内注射的安全性以及确定人用剂量。结果为0.1μg的rdesat
‑
6的反应程度与tb
‑
ppd(2tu)相当。该研究采用了esat
‑
6单一抗原,同时也提出,正如在γ干扰素释放试验(igra)中所观察的那样,增加特异性的cfp
‑
10抗原会提高敏感性。
18.2010年丹麦血清研究所发布了另一个i期临床试验结果(clinicaltrials.gov nct00793702,trial code tesec
‑
01,eudract no.:2008
‑
001489
‑
96)。动物试验表明,在rdesat
‑
6体系中增加cfp
‑
10组分可以提高诊断的敏感度而不会损失特异性。本次临床是在42名健康志愿者中测试rdesat
‑
6和cfp
‑
10皮内注射的安全性,按照1:1(wt/wt)比例,剂量为0.01μg和0.1μg,间隔6或12周。结论是该制剂是安全的,将进入ii期临床。作者同时表示开发这样一组特异性抗原的目标是保持较高的特异性、敏感性同时又低致敏性,将来替代tb
‑
ppd
[4,9]
。
[0019]
2013年丹麦血清研究所在同一篇文章中发布了针对rdesat
‑
6和cfp
‑
10组合抗原c
‑
tb的另一个i期临床试验(clinicaltrials.gov nct01033929)和ii期临床试验(clinicaltrials.gov nct01241188;nct01242475)结果。i期试验在38名病人上验证c
‑
tb安全性,剂量为0.01μg和0.1ug。ii期临床试验在151名未感染结核菌的bcg疫苗免疫的人群中比较c
‑
tb 0.1ug和tb
‑
ppd(2tu)的特异性,结论:c
‑
tb不受bcg疫苗免疫影响,是一种简单、便利的针对结核菌感染的特异性皮试诊断试剂
[5]
。
[0020]
2015年12月份丹麦血清研究所发表了c
‑
tb临床(ii期)敏感性试验数据。253名病人入组,与tb
‑
ppd试剂和quantiferon
‑
tb gold in
‑
tube(qft
‑
git;cellestis/qiagen,venlo,the netherlands)试剂盒一同比较敏感性,结果c
‑
tb与qft
‑
git敏感性相当(73.9%vs 75.1%)
[6]
。
[0021]
2017年4月份丹麦血清研究所在《柳叶刀》杂志上发表了iii期临床试验结果。在西班牙13个试验中心,979名入组,263名阴性对照,299名偶然接触者,316名密切接触者和101
名结核病人,970人(99%)完成了全程试验。在接种部位c
‑
tb和tb
‑
ppd形成的硬结相当,但是tb
‑
ppd阳性受到bcg免疫状态影响。研究者发现c
‑
tb阳性组随着感染风险的增加,有强阳性的趋势,从阴性对照组3%,偶然接触组16%,到密切接触组43%。在834名5岁以上的受试者中,c
‑
tb和qft试剂盒结果一致(785人,94%)。c
‑
tb的安全性与tst相当
[7]
。研究者计划在南非开展另一个iii期临床(clinicaltrials.gov nct1642888)
[7]
。
[0022]
2016年浙江海正药业股份有限公司申请了一项专利,申请号:201610011182.1,是一种含有结核菌变态反应原cfp
‑
10和esat
‑
6的组合物,实质上是一个重组融合蛋白,该蛋白第1
‑
100位为cfp
‑
10抗原表位序列,第101
‑
108位为连接臂,第109
‑
203位为esat
‑
6抗原表位,连接臂是8个氨基酸残基ggggsggg,cfp
‑
10(100a.a.)和esat
‑
6(95a.a.)与结核杆菌h37rv株的rv3874和rv3875的基因完全一致。
[0023]
中检所esat
‑
6多肽序列与龙科马以及海正药业的序列相比较,在第2位的苏氨酸(thr)改变为缬氨酸(val),其他序列含有94a.a.均相同。该技术转让给了北京祥瑞生物制品有限公司。
[0024]
2019年扩增生物科技(北京)有限公司申请了“结核分支杆菌重组蛋白eecc及其制备方法和应用”该发明设计的是结核分枝杆菌重组融合蛋白eecc,具体是esat6
‑
esat6
‑
cfp10
‑
cfp10,但是设计中带有his标签,可能引入了其他表位。降低了特异性。
[0025]
2019年北京祥瑞生物制品有限公司获得一项tb
‑
4s专利授权,该发明是将cfp
‑
10串联表达,再将esat
‑
6等比例混合制备诊断试剂,设计思路与丹麦血清所相似。
[0026]
1、发明人对现有技术进行对比分析
[0027]
1.1龙科马公司采用的是resat6
‑
cfp10融合蛋白,ii期临床确定的剂量是1μg/0.1ml;而丹麦血清所采用的是串联rdesat
‑
6加等重量的rcfp
‑
10蛋白抗原(c
‑
tb),临床确定的剂量是0.1μg/0.1ml。中检所采用的resat
‑
6抗原,1μg/0.1ml。显然,丹麦血清所的抗原用量低(1/10),并且比中检所多一种特异性抗原cfp
‑
10。龙科马和海正设计的抗原包含了esat
‑
6和cfp
‑
10两种抗原,区别在于两条多肽连接的前后顺序。
[0028]
1.2 c
‑
tb多肽分子设计是n末端连接5个氨基酸asp
‑
thr
‑
arg
‑
ser
‑
met(dtrsm),在2个单体之间连接3个氨基酸arg
‑
ser
‑
met(rsm),即:dtrsm
‑
resat6
‑
rsm
‑
resat6,再添加等重量的rcfp
‑
10,最终rdesat
‑
6与rcfp
‑
10的mol数比是1:1。龙科马的是resat6
‑‑
甘氨酸(gly)
‑
苏氨酸(thr)
‑‑
rcfp10融合蛋白,resat
‑
6和rcfp
‑
10的分子mol比也是1:1,两者相同。海正药业是rcfp10
‑‑
甘氨酸(gly)
‑‑
甘氨酸(gly)
‑‑
甘氨酸(gly)
‑‑
甘氨酸(gly)
‑‑
丝氨酸(ser)
‑‑
甘氨酸(gly)
‑‑
甘氨酸(gly)
‑‑
甘氨酸(gly)
‑‑
resat6,resat
‑
6和rcfp
‑
10的分子mol比也是1:1。
[0029]
1.3 esat
‑
6和cfp
‑
10在溶液中易形成1:1的结合物
[10]
,当模拟多肽分子在溶液中的微观状态时就会发现海正和龙科马公司的重组分子设计与c
‑
tb的重组分子设计不同,c
‑
tb呈现4个亚单位结构组合的大分子,而海正和龙科马的融合蛋白是2个亚单位组合的分子
[11]
。多肽链亚单位结构不同可能反映在激活t细胞的效率不同
[8,12]
。
[0030]
1.4鉴于c
‑
tb的设计思路,祥瑞生物采用另一种设计策略,既规避丹麦血清所的专利,又达到c
‑
tb的特异性和敏感性。串联cfp
‑
10,融合表达二聚体的cfp
‑
10多肽链,按照等重量比添加resat
‑
6多肽单链,形成与c
‑
tb类似的结构,同时规避了对方的专利。
[0031]
2、c
‑
tb、tb
‑
4s和ec产品的缺陷分析
[0032]
丹麦的c
‑
tb与祥瑞tb
‑
4s均是接近100%特异性,经过临床测试确定的人用剂量为0.1μg/人,但是敏感性低于80%。为了提高敏感性,可以采取提高接种剂量的方法,但是试验表明剂量提高同时不良反应也增加,分析原因可能是esat
‑
6和cfp
‑
10在溶液中形成天然结构,具有很强的毒性。除敏感性较低外,c
‑
tb制备过程需分别表达esat
‑6‑
esat
‑
6和cfp
‑
10两种抗原,再将二者按1:1比例混匀,制备工艺较融合表达类抗原复杂,成本较高。智飞龙科马的ec产品将esat
‑
6和cfp
‑
10串联在一起,两个抗原之间引入了两个氨基酸的连接子,有可能形成未知抗原表位而降低其安全性。临床试验表明,虽然ec的敏感性超过80%,特异性也接近100%,但是每人份剂量较tb
‑
ppd和c
‑
tb提高了10倍(批准上市的产品剂量确定为1.0μg/人),导致不良反应较高。海正和龙科马公司的简单融合表达存在同样的问题,使用剂量有可能是c
‑
tb剂量10倍。中检所的单一esat
‑
6多肽抗原方案,忽略了cfp
‑
10有增效的作用。
[0033]
总之,降低ec类产品使用剂量,提高其安全性的同时保持100%特异性和大于80%敏感性,是开发这种新型结核诊断试剂的关键点。
技术实现要素:
[0034]
针对上述存在的问题,本发明目的在于提供一种重组结核分枝杆菌融合蛋白及其制备方法,并将其应用到结核诊断中,既能避免tb
‑
ppd的低特异性,又具有较ec更高的敏感性和安全性,且制备工艺简单,成本较低。
[0035]
本发明所提供的重组融合蛋白,是将来自于结核分枝杆菌的esat
‑
6和cfp
‑
10两种多肽串联融合,具体是串联2条esat
‑
6肽链和1条cfp
‑
10肽链。
[0036]
在一种实施例中,本发明所述的重组融合蛋白,多肽串联融合方式为esat6
‑
esat6
‑
cfp10(简写为eec)。
[0037]
在一种具体的实施例中,本发明所述的重组融合蛋白,多肽之间没有连接子。即氨基酸序列是t细胞表位的串联,多肽相连接时均删除接头的甲硫氨酸(m)直接衔接,共删除两个m,多肽之间没有连接子。发明人发现,这种连接方式可以有效避免出现未知抗原表位,有效提高安全性。
[0038]
在一种具体的实施例中,本发明所述的重组融合蛋白,其氨基酸序列如seq id no.1所示。
[0039]
本发明所述的重组融合蛋白两端不添加其他标签等非天然序列,或者仅添加利于表达纯化的his标签。可进一步提高安全性。
[0040]
本发明还提供编码所述重组融合蛋白的核苷酸。
[0041]
在一些实施例中,所述核苷酸序列如seq id no.2所示。
[0042]
本发明还提供所述重组融合蛋白在结核诊断中的应用。
[0043]
本发明还提供本发明所述的重组融合蛋白在制备结核诊断试剂或检测试剂盒中的应用。
[0044]
本发明还提供一种结核诊断试剂,所述诊断试剂中含有本发明所述的重组融合蛋白。
[0045]
本发明所述的重组融合蛋白,将esat
‑
6和cfp
‑
10融合表达,制备工艺简单,成本较低。
[0046]
在一种具体的实施方式中,本发明还提供所述重组融合蛋白的一种具体的制备方法:用原核表达系统制备。在一种具体的实施方式中,本发明所述的重组融合蛋白的制备方法,将本发明所述的重组融合蛋白的编码基因序列插入原核表达载体,转入菌株扩增和纯化。
[0047]
本发明还提供一种本发明所述的重组融合蛋白的纯化方法,用(15~25)%和(35~45)%饱和度的硫酸铵使蛋白梯度沉淀,随后进行超滤,将蛋白溶液体系更换为ph=7.8~8.2的tris
‑
尿素;超滤结束后进行阴离子层析,7%~9%的nacl去除杂蛋白,11%~13%的nacl收集目的蛋白。
[0048]
在本发明的一种实施例中,阴离子层析选用qhp型填料(ge公司)。
[0049]
本发明所述的重组融合蛋白采用原核表达体系,经表达纯化后,用于结核杆菌潜伏感染人群的筛查和辅助诊断。在低剂量应用中,特异性接近100%,敏感性与同类产品相比大幅提高,安全性和依从性好,可用作tb
‑
ppd的替代品。具体而言,本发明所述的重组融合蛋白相对于现有技术,具有如下优势:
[0050]
①
选择esat
‑
6和cfp
‑
10两种结核分枝杆菌特有抗原,特异性较tb
‑
ppd有显著提高。
[0051]
②
抗原esat
‑
6和cfp
‑
10的比例为2:1,较ec等抗原比例为1:1类的方案具有更高的敏感性,同时安全性也有所提高(剂量更低);native电泳均一性更好,安全性和有效性更佳。
[0052]
③
本发明所述的esat
‑
6和cfp
‑
10的连接方式,安全性更高。
[0053]
④
抗原esat
‑
6和cfp
‑
10融合表达,较c
‑
tb制备工艺简单,成本更低,本发明所述的纯化方法,最终蛋白纯度更高。
[0054]
说明书附图
[0055]
图1重组蛋白表达质粒图谱;
[0056]
图2.重组蛋白eec纯化流程;
[0057]
图3.重组蛋白eec电泳纯度分析;
[0058]
图4.重组蛋白eec的hplc纯度;
[0059]
图5重组蛋白ec、ece、ecce、ecec和ececc电泳纯度分析;
[0060]
图6 sds
‑
page检测蛋白eec与ece表达量;
[0061]
图7 eec、ece、ecce、ecec和ececc的native电泳分析。
具体实施方式
[0062]
以下结合具体实施例,对本发明进行进一步说明,若无特别说明,实施例中用到的试剂均为本领域的常规试剂,所用的方法均为本领域的常规方法。
[0063]
以下实施例中使用的cfp
‑
10蛋白,氨基酸序列如seq id no.3所示;esat
‑
6的氨基酸序列如seq id no.4所示。cfp
‑
10和esat
‑
6的氨基酸序列设计参考来源于结核杆菌h37rv株,该株中含有毒力因子cfp
‑
10和esat
‑
6基因,参考基因编号为rv3874和rv3875。cfp
‑
10的核酸序列如seq id no.5所示;esat
‑
6核酸序列如seq id no.6所示。
[0064]
作为对比例,本发明设计了多种esat
‑
6(简称e)和cfp
‑
10(简称c)串联方案,包括ec、ece、ecce、ecec、ececc。
[0065]
五种对比例加本发明所述的重组融合蛋白eec,本发明的六种串联方案,两条多肽相连接时均删除了接头的甲硫氨酸(m)。其中两条多肽串联方案是ec,三条多肽串联方案是ece和eec,四条多肽串联方案是ecec和ecce,五条多肽串联方案是ececc。按照上述设计合成基因序列,转入大肠杆菌或者乳酸菌(革兰氏阳性菌)等原核表达系统,表达蛋白质,作为皮试反应原,用于结核病感染的诊断等相关领域的应用。
[0066]
实施例1:eec重组蛋白表达质粒与工程菌的构建
[0067]
从ncbi数据库中查询mycobacterium tuberculosis h37rv基因组数据(ncbi索取号:al123456),选取cfp
‑
10和esat
‑
6的基因序列(seq id no.5和6),按照eec的串联组合方案设计基因序列并交由第三方基因合成公司(如上海生工)进行基因合成,将合成的基因插入原核表达载体(pet
‑
30a,如图1所示)。表达载体构建成功后,先将该载体转入大肠杆菌dh5α菌株内,进行质粒扩增,扩增后用质粒提取纯化试剂提取质粒。最后将提取的质粒转化蛋白表达菌株(如bl
‑
21(de3))。将转化成功后的第一代菌种作为原始种子,分别建立主种子批和工作种子批,用于重组蛋白的表达制备。
[0068]
实施例2:eec重组蛋白的制备
[0069]
1.工程菌发酵及重组蛋白表达:取一支菌种,室温融化后,按1%接种至含5ml lb培养基的中管内,37℃过夜培养12
‑
16h,使菌种复苏;将复苏的菌液按1%接种至250ml lb培养基内,37℃摇床培养至od600=0.6~0.8时,加iptg(终浓度为0.4mmol/l)诱导,继续培养4h。离心收集菌体,用0.01m pbs缓冲液洗涤两次,将洗涤后的菌体放置于4℃冰箱备用。
[0070]
2.菌体破碎:将菌体用0.01m pbs缓冲液重悬,用高压均质机破碎菌体,破碎压力为800bar,破碎两次。随后12000
×
g离心30min,收集上清液备用。,
[0071]
3.蛋白纯化:蛋白纯化流程图如图2所示,首先用20%和40%饱和度的硫酸铵使蛋白梯度沉淀,随后进行超滤,将蛋白溶液体系更换为tris
‑
尿素(ph=8.0);超滤结束后进行阴离子层析,选用qhp型填料(ge公司),8%nacl去除杂蛋白,12%的nacl收集目的蛋白。纯化后用sds
‑
page电泳法检测重组蛋白纯度,最终蛋白纯度大于98%(图3,通道1为mark,通道2为eec电泳,图4为hplc纯度),本发明所述的纯化方法获得的蛋白纯度更高。
[0072]
实施例3:ec、ece、ecce、ecec和ececc重组蛋白的制备
[0073]
按照ec、ece、ecce、ecec和ececc的串联组合方案设计基因序列(蛋白序列分别为seq id no.7~11;核酸序列分别为seq id no.12~16),并交由第三方基因合成公司(如上海生工)进行基因合成(部分方案可能含有his标签,以便于蛋白纯化),按照实施例1和实施例2同样的方法将合成的基因分别插入原核表达载体。表达载体构建成功后,将各方案质粒分别转化蛋白表达菌株(如bl
‑
21(de3))。转化成功后,将菌液按1%接种至250ml lb培养基内,37℃摇床培养至od600=0.6~0.8时,加iptg(终浓度为0.4mmol/l)诱导,继续培养4h。离心收集菌体,用超声或高压均质机将菌体破碎。离心去沉淀后用镍柱对目的蛋白进行纯化。纯化后的蛋白用sds
‑
page电泳法检测重组蛋白纯度,最终蛋白纯度大于95%(图5)。
[0074]
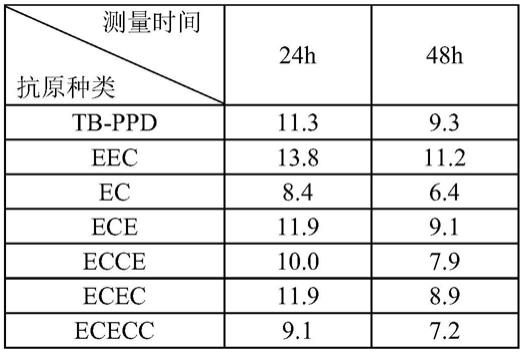
实施例4:不同串联方式重组蛋白药效对比
[0075]
用结核分枝杆菌减毒株(h37ra)将豚鼠致敏。详细操作步骤如下:用注射器吸取结核分枝杆菌减毒株(h37ra)菌液0.5ml(含h37ra 1mg),于豚鼠后腿注射,每组致敏8只。三周后,将豚鼠背部脊柱两侧去毛,用酒精棉消毒去毛部位的皮肤,以轮圈法分别用1ml一次性注射器于皮内注射重组蛋白(eec、ec、ece、ecce、ecec和ececc)和tb
‑
ppd各0.1ml。其中,重
组蛋白剂量为0.5μg/只,tb
‑
ppd 5iu/只。分别于24h和48h测量红晕或硬结大小(纵横直径相加除2)。结果如表1所示。数据表明,重组蛋白eec在24h和48h产生的红晕或硬结直径均大于其余重组蛋白方案或tb
‑
ppd,表明eec的敏感性明显优于其他抗原(eec与ec、ecce、ececc差异显著(p<0.05))。
[0076]
表1.不同抗原产生的红晕或硬结直径/mm对比(均值,n=8)
[0077][0078]
实施例5:eec与tb
‑
ppd特异性对比
[0079]
分别用结核分枝杆菌减毒株(h37ra)和卡介菌菌株将豚鼠致敏。详细操作步骤如下:用注射器吸取结核分枝杆菌减毒株(h37ra)或卡介菌菌液0.5ml(含h37ra 1mg或卡介菌12mg),于豚鼠后腿注射,各致敏4只。三周后,将豚鼠背部脊柱两侧去毛,用酒精棉消毒去毛部位的皮肤,以轮圈法分别用1ml一次性注射器于皮内注射重组蛋白eec和tb
‑
ppd各0.1ml。其中,重组蛋白eec剂量为0.5μg/只,ppd 5iu/只,于24h测量红晕或硬结大小(纵横直径相加除2)。结果见表2。由结果可见,eec对卡介菌致敏的豚鼠无反应,而tb
‑
ppd对卡介菌致敏的豚鼠有反应,因此eec的特异性优于tb
‑
ppd,可区分卡介苗接种和结核分枝杆菌感染,即可实现100%的特异性。
[0080]
表2.eec与tb
‑
ppd特异性对比结果
[0081][0082]
实施例6:eec与ece表达量对比
[0083]
分别将含有多肽串联方案eec和ece的载体质粒转入原核表达菌株(如大肠杆菌
bl
‑
21(de3)),用250ml摇瓶培养至od600=0.6~0.8时,加入iptg至终浓度0.4mmol/l,诱导4h,收集菌体并提取蛋白,sds
‑
page检测蛋白表达量,结果见下图6。结果显示,在同样的表达体系内,eec的表达量明显高于ece。
[0084]
实施例7:eec与ece、ecce、ecec和ececc的结构均一性对比
[0085]
分别对抗原eec、ece、ecce、ecec和ececc进行native电泳分析,电泳缓冲液为3g/l tris,14.4g/l甘氨酸,ph 8.3。低温下电泳,电压80v,12%分离胶,5%浓缩胶。电泳结果如图7显示,ece、ecce、ecec和ececc均有多个条带,而eec仅有两个条带,表明eec抗原的构象较其他方案更加均一,在安全性和有效性方面可能会具有更好的优势。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1