化合物、聚合物、液晶取向剂、液晶取向膜、液晶显示元件、以及制造方法与流程
1.本发明涉及一种有效用作液晶取向剂中所使用的聚合物的原料单体的二胺化合物及其制造方法、将所述二胺化合物用于原料单体的聚合物、有效用作所述二胺化合物的合成中间体的二硝基化合物及其制造方法以及保护二氨基化合物。进而涉及一种包含所述聚合物的液晶取向剂、使用所述液晶取向剂而形成的光取向方式的液晶取向膜(光取向膜)及其制造方法、以及具有所述液晶取向膜的液晶显示元件。
背景技术:
2.液晶显示元件已知有扭转向列(twisted nematic,tn)模式、超扭转向列(super twisted nematic,stn)模式、共面切换(in
‑
plane switching,ips)模式、边缘场切换(fringe field switching,ffs)模式、垂直取向型的垂直取向(vertical alignment,va)(多域垂直取向(multi
‑
domain vertical alignment))模式等各种驱动方式的液晶显示元件。这些液晶显示元件采用于电视、移动电话等各种电子机器的图像显示装置,以进一步提高显示品质为目标而正在进行开发。具体而言,液晶显示元件的性能的提高不仅可通过驱动方式、元件结构的改良来达成,而且还可通过元件中所使用的结构构件来达成。而且,液晶显示元件中所使用的结构构件中,特别是液晶取向膜是与显示品质相关的重要材料之一,为了应对液晶显示元件的高品质化的要求,正在积极进行研究。
3.此处,液晶取向膜在设置于液晶显示元件的液晶层的两侧的一对基板上与所述液晶层相接设置,具有使构成液晶层的液晶分子相对于基板具有一定规则性地进行取向的功能。通过使用液晶取向性高的液晶取向膜,可实现对比度高且残像特性得到改善的液晶显示元件(例如,参照专利文献1及专利文献2)。
4.在此种液晶取向膜的形成中,目前主要使用使聚酰胺酸、可溶性的聚酰亚胺或聚酰胺酸酯溶解于有机溶剂中而成的溶液(清漆)。在利用这些清漆来形成液晶取向膜时,将清漆涂布于基板后,通过加热等而将涂膜固化来形成各种液晶取向膜,视需要实施适合于所述显示模式的取向处理。
5.具体而言,例如作为在基板上形成用以制成液晶取向膜的聚酰亚胺膜的方法,除将含有作为聚酰亚胺前体的聚酰胺酸的液晶取向剂涂布在基板上后进行煅烧来制成聚酰亚胺膜的方法、或将含有溶剂可溶性聚酰亚胺的液晶取向剂涂布在基板上去除溶剂来制成聚酰亚胺膜的方法以外,已知有将含有由含酰亚胺基的二胺获得的含酰亚胺基的聚酰胺酸的液晶取向剂涂布在基板上的方法(例如,参照专利文献3)。
6.另外,作为取向处理方法,已知有:利用布等摩擦取向膜的表面来调整聚合物分子的方向的摩擦法;及通过对取向膜照射直线偏光的紫外线而在聚合物分子中引起光异构化或二聚化等光化学变化,对膜赋予各向异性的光取向法。其中,与摩擦法相比,光取向法的取向的均匀性高,为非接触的取向处理法,因此具有不损伤膜、可减低起尘或静电等使液晶显示元件产生显示不良的原因等优点。
7.另外,作为所述光取向法之一,已知有分解型的光取向法。所述分解型光取向法例如为通过对聚酰亚胺膜照射偏光紫外线,利用分子结构的紫外线吸收的偏光方向依存性产生各向异性的分解,利用未分解而残留的聚酰亚胺使液晶取向的方法(例如,参照专利文献4)。
8.[现有技术文献]
[0009]
[专利文献]
[0010]
[专利文献1]日本专利特开2010
‑
197999号公报
[0011]
[专利文献2]国际公开第2013/157463号
[0012]
[专利文献3]日本专利特开平9
‑
185064号公报
[0013]
[专利文献4]日本专利特开平9
‑
297313号公报
技术实现要素:
[0014]
[发明所要解决的问题]
[0015]
且说,随着近年来的液晶显示元件的利用形态的变化,要求进一步实现高对比度的液晶显示元件。此处,为了实现高对比度,液晶层的液晶分子必须取得有规则地排列的状态,为此,对液晶层赋予取向性的液晶取向膜具有高的液晶取向性变得重要。但是,利用现有的光取向法获得的液晶取向膜的液晶取向性不充分,因此实际情况是无法充分满足近年来对比度提高的要求。
[0016]
因此,本发明人等人为了解决此种现有技术的课题,以提供可形成液晶取向性高的液晶取向膜的材料及其原料为目的而进行了研究。
[0017]
[解决问题的技术手段]
[0018]
本发明人等人为了解决所述课题而进行了努力研究,结果发现:通过将聚酰胺酸或其衍生物用于液晶取向剂,可获得液晶取向性高的液晶取向膜,所述聚酰胺酸或其衍生物是将具有特定环丙烷结构的二胺化合物用于二胺单体而合成,通过使用所述液晶取向膜,实现显示出高的对比度的液晶显示元件。本发明是基于此种见解而完成,具体而言具有以下的结构。
[0019]
[1]一种二胺化合物,由下述通式(1)表示。
[0020]
[化1]
[0021][0022]
(式中,r1及r2各自独立地表示氢原子、卤素原子、碳数1至6的烷基、碳数1至6的卤代烷基或碳数1至6的烷氧基。r1与r2可成为一体而形成可经取代的亚甲基。x各自独立地表示卤素原子、碳数1至6的烷基、碳数1至6的卤代烷基或碳数1至6的烷氧基,n表示0至4的整数)
[0023]
[2]根据[1]所述的二胺化合物,由下述通式(1
‑
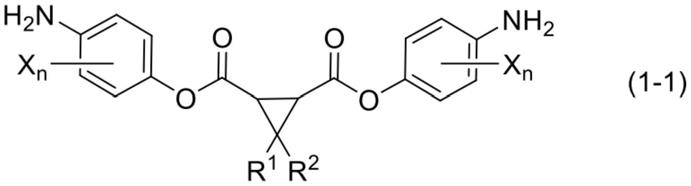
1)表示。
[0024]
[化2]
[0025][0026]
(式中,r1、r2、x及n分别与所述通式(1)的r1、r2、x及n为相同含义)
[0027]
[3]根据[1]或[2]所述的二胺化合物,由下述通式(1
‑
2)表示。
[0028]
[化3]
[0029][0030]
(式中,r1及r2分别与所述通式(1)的r1及r2为相同含义)
[0031]
[4]根据[1]至[3]中任一项所述的二胺化合物,其中两个酯以反式构型在环丙烷环进行取代。
[0032]
[5]一种聚合物,是使包含二胺类与四羧酸二酐类的原料组合物聚合而成的聚合物或其衍生物,所述聚合物中,所述二胺类的至少一种为根据[1]至[4]中任一项所述的二胺化合物。
[0033]
[6]一种液晶取向剂,包含根据[5]所述的聚合物。
[0034]
[7]一种液晶取向膜,由根据[6]所述的液晶取向剂形成。
[0035]
[8]一种液晶显示元件,具有根据[7]所述的液晶取向膜。
[0036]
[9]一种液晶取向膜的制造方法,包括:将根据[6]所述的液晶取向剂涂布在基板而形成涂膜的工序;以及对所述涂膜照射偏光紫外线的工序。
[0037]
[10]一种二胺化合物的制造方法,将下述通式(2)所表示的二硝基化合物还原来获得下述通式(1)所表示的二胺化合物。
[0038]
[化4]
[0039][0040]
(式中,r1及r2各自独立地表示氢原子、卤素原子、碳数1至6的烷基、碳数1至6的卤代烷基或碳数1至6的烷氧基。r1与r2可成为一体而形成可经取代的亚甲基。x各自独立地表示氢原子、卤素原子、碳数1至6的烷基、碳数1至6的卤代烷基或碳数1至6的烷氧基,n表示0至4的整数)
[0041]
[化5]
[0042][0043]
(式中,r1、r2、x及n分别与所述通式(1)的r1、r2、x及n为相同含义)
[0044]
[11]一种二胺化合物的制造方法,对下述通式(7
‑
1)所表示的保护二氨基化合物进行脱保护来获得下述通式(1
‑
1)所表示的二胺化合物。
[0045]
[化6]
[0046][0047]
(式中,r1及r2各自独立地表示氢原子、卤素原子、碳数1至6的烷基、碳数1至6的卤代烷基或碳数1至6的烷氧基。r1与r2可成为一体而形成可经取代的亚甲基。x各自独立地表示卤素原子、碳数1至6的烷基、碳数1至6的卤代烷基或碳数1至6的烷氧基,n表示0至4的整数。boc表示叔丁氧基羰基)
[0048]
[化7]
[0049][0050]
(式中,r1、r2、x及n分别与所述通式(1)的r1、r2、x及n为相同含义)
[0051]
[12]一种二胺化合物的制造方法,使下述通式(3)所表示的环丙烷衍生物与下述通式(6
‑
1)所表示的保护氨基苯酚化合物发生缩合反应,合成下述通式(7
‑
1)所表示的保护二氨基化合物后进行脱保护,来获得下述通式(1
‑
1)所表示的二胺化合物。
[0052]
[化8]
[0053][0054]
(式中,r1及r2各自独立地表示氢原子、卤素原子、碳数1至6的烷基、碳数1至6的卤代烷基或碳数1至6的烷氧基。r1与r2可成为一体而形成可经取代的亚甲基。y表示脱离基)
[0055]
[化9]
[0056][0057]
(式中,x表示卤素原子、碳数1至6的烷基、碳数1至6的卤代烷基或碳数1至6的烷氧基,n表示0至4的整数。当n为2以上时,多个x可相互相同也可不同。boc表示叔丁氧基羰基)
[0058]
[化10]
[0059][0060]
(式中,r1、r2、x、n及boc分别与所述通式(7
‑
1)的r1、r2、x、n及boc为相同含义)
[0061]
[化11]
[0062][0063]
(式中,r1、r2、x及n分别与所述通式(1)的r1、r2、x及n为相同含义)
[0064]
[13]一种二硝基化合物,由下述通式(2)表示。
[0065]
[化12]
[0066][0067]
(式中,r1、r2、x及n分别与所述通式(2)的r1、r2、x及n为相同含义)
[0068]
[14]根据[13]所述的二硝基化合物,由下述通式(2
‑
1)表示。
[0069]
[化13]
[0070][0071]
(式中,r1、r2、x及n分别与所述通式(2)的r1、r2、x及n为相同含义)
[0072]
[15]根据[13]或[14]所述的二硝基化合物,由下述通式(2
‑
2)表示。
[0073]
[化14]
[0074][0075]
(式中,r1及r2分别与所述通式(2)的r1及r2为相同含义)
[0076]
[16]根据[13]至[15]中任一项所述的二硝基化合物,其中两个酯以反式构型在环丙烷环进行取代。
[0077]
[17]一种二硝基化合物的制造方法,使下述通式(3)所表示的环丙烷衍生物与下述通式(4)所表示的硝基化合物发生缩合反应,来合成下述通式(2)所表示的二硝基化合物。
[0078]
[化15]
[0079][0080]
(式中,r1及r2各自独立地表示氢原子、卤素原子、碳数1至6的烷基、碳数1至6的卤代烷基或碳数1至6的烷氧基。r1与r2可成为一体而形成可经取代的亚甲基。y表示脱离基)
[0081]
[化16]
[0082][0083]
(式中,x表示氢原子、卤素原子、碳数1至6的烷基、碳数1至6的卤代烷基或碳数1至6的烷氧基,n表示0至4的整数。当n为2以上时,多个x可相互相同也可不同)
[0084]
[化17]
[0085][0086]
(式中,r1、r2、x及n分别与所述通式(2)的r1、r2、x及n为相同含义)
[0087]
[18]一种保护二氨基化合物,由下述通式(7
‑
1)表示。
[0088]
[化18]
[0089][0090]
(式中,r1、r2、x、n及boc分别与所述通式(7
‑
1)的r1、r2、x、n及boc为相同含义)
[0091]
[19]根据[18]所述的保护二氨基化合物,其中两个酯以反式构型在环丙烷环进行取代。
[0092]
以下,对各通式的r1、r2及x中的卤素原子、碳数1至6的烷基、碳数1至6的卤代烷基、碳数1至6的烷氧基、及y中的脱离基进行说明。
[0093]
作为卤素原子,可列举:氟原子、氯原子、溴原子、碘原子。
[0094]
碳数1至6的烷基可为直链状、分支链状、环状的任一种。
[0095]
作为烷基的具体例,可例示:甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基、异戊基、新戊基、叔戊基、1
‑
甲基丁基、1
‑
乙基丙基、己基、异己基、1
‑
甲基戊基、1
‑
乙基丁基、环戊基、环己基等。
[0096]
作为碳数1至6的卤代烷基,可列举所述碳数1至6的烷基中处于任意位置的任意数量的氢原子经卤素原子取代而成的基。关于卤素原子的具体例,可参照r1、r2及x中的卤素原子的具体例。卤代烷基中的卤素原子的数量优选为1至5,更优选为1至4,进而优选为1至3。作为卤代烷基的具体例,可列举:二氟甲基、三氟甲基、1,1
‑
二氟乙基、2,2
‑
二氟乙基、2,2,2
‑
三氟乙基、3
‑
氟丙基、氯甲基、二氯甲基、三氯甲基等。
[0097]
碳数1至6的烷氧基可为直链状、分支链状、环状的任一种。作为烷氧基的具体例,可例示:甲氧基、乙氧基、丙氧基、异丙基氧基、丁基氧基、异丁基氧基、仲丁基氧基、叔丁基氧基、戊基氧基、异戊基氧基、新戊基氧基、叔戊基氧基、1
‑
甲基丁基氧基、1
‑
乙基丙基氧基、己基氧基、异己基氧基、1
‑
甲基戊基氧基、1
‑
乙基丁基氧基、环戊基氧基、环己基氧基等。
[0098]
作为脱离基y,可列举:氯原子、羟基、4
‑
硝基苯基氧基、2,4
‑
二硝基苯基氧基等。
[0099]
[发明的效果]
[0100]
本发明的二胺化合物有效用作液晶取向剂中所使用的聚合物的原料单体。通过将使用所述二胺化合物而合成的聚合物用于液晶取向剂,可形成液晶取向性高的液晶取向膜。而且,通过将所述液晶取向膜适用于液晶显示元件,可对其液晶层赋予高的取向性,以高的对比度进行显示。
具体实施方式
[0101]
以下,对本发明进行详细说明。以下记载的结构要件的说明有时基于具有代表性的实施方式或具体例而成,但本发明并不限定于此种实施方式。再者,本说明书中使用“~”表示的数值范围是指包含“~”前后所记载的数值作为下限值及上限值的范围。
[0102]
另外,本发明中的“液晶取向剂”是当在基板上形成所述的膜时,通过照射偏光紫外线而可赋予各向异性的液晶取向剂,本说明书中若有时也简称为“液晶取向剂”,则有时也称为“光取向用液晶取向剂”。另外,本发明中所谓“四羧酸二酐类”,是指四羧酸二酐、四羧酸二酯或四羧酸二酯二卤化物。另外,本发明中,有时也将二胺及二酰肼称为“二胺类”。
[0103]
另外,以下的说明中,有时将通式(1)所表示的二胺化合物、通式(2)所表示的二硝基化合物、通式(3)所表示的环丙烷衍生物、通式(4)所表示的硝基化合物、通式(6
‑
1)所表示的保护氨基苯酚化合物、通式(7
‑
1)所表示的保护二氨基化合物分别称为二胺化合物(1)、二硝基化合物(2)、环丙烷衍生物(3)、硝基化合物(4)、保护氨基苯酚化合物(6
‑
1)、保护二氨基化合物(7
‑
1)。
[0104]
<二胺化合物>
[0105]
本发明的二胺化合物是通式(1)所表示的化合物。
[0106]
[化19]
[0107][0108]
通式(1)中,r1及r2各自独立地表示氢原子、卤素原子、碳数1至6的烷基、碳数1至6的卤代烷基或碳数1至6的烷氧基。r1与r2可相互相同也可不同。另外,r1与r2可成为一体而形成可经取代的亚甲基。作为亚甲基的取代基,可列举:氟原子或氯原子等卤素原子、可经氟原子或氯原子等卤素原子或碳数1至4的烷氧基取代的烷基、或者可经氟原子或氯原子等卤素原子、碳数1至4的烷基或碳数1至4的烷氧基取代的芳基等。x各自独立地表示卤素原子、碳数1至6的烷基、碳数1至6的卤代烷基或碳数1至6的烷氧基,n表示0至4的整数。当两个n的合计为2以上时,多个x可相互相同也可不同。x及氨基(
‑
nh2)的键结位置分别为其结合键所键结的苯环的能够进行取代的位置的任一处。
[0109]
由将所述通式(1)所表示的二胺化合物(二胺化合物(1))用于单体而合成的聚合物形成涂膜,并照射偏光时,可对所述涂膜赋予高的液晶取向性。推测这是由于以下机制引起的。
[0110]
即,认为本发明的二胺化合物(1)具有苯基酯与环丙烷的相邻的碳键结的结构,由此通过光照射而发生光弗里斯重排反应。因此,若对使用所述二胺化合物(1)而合成的聚合物的涂膜照射光取向用的偏光,则在无规取向的聚合物链中,在与所述偏光方向大致平行的聚合物主链的源于二胺的结构单元上,选择性地发生光化学反应(光弗里斯重排反应)。其结果,源于与偏光方向大致呈直角的聚合物链的取向成分占支配地位,成为在特定方向上高度取向的状态。
[0111]
而且,若将所述取向的膜用作液晶显示元件的液晶取向膜,则液晶取向膜的表面与液晶分子的相互作用的结果是:液晶分子在与照射的偏光的偏光方向大致呈直角的方向上使长轴对齐并均匀地取向,从而对液晶层赋予高的各向异性。
[0112]
根据以上内容,二胺化合物(1)有效用作液晶取向剂中所使用的聚合物的原料单体(二胺单体)。而且,通过将使用所述二胺化合物而合成的聚合物用于液晶取向剂,可形成液晶取向性高的液晶取向膜。而且,通过将所述液晶取向膜适用于液晶显示元件,可对其液晶层赋予高的取向性,以高的对比度进行显示。
[0113]
再者,本说明书中,有时将聚合物链中朝向特定方向的成分占支配地位的状态表
现为聚合物链进行取向,将形成取向膜的聚合物链处于沿特定方向取向的状态表现为产生各向异性。另外,有时将聚合物链在特定方向上进一步对齐表现为具有高的各向异性。
[0114]
以下,对通式(1)所表示的二胺化合物的优选的例子进行说明。
[0115]
[通式(1
‑
1)所表示的二胺化合物]
[0116]
作为通式(1)所表示的二胺化合物的优选的例子,可列举下述通式(1
‑
1)所表示的二胺化合物。
[0117]
[化20]
[0118][0119]
通式(1
‑
1)中,r1、r2、x及n分别与通式(1)中的r1、r2、x及n为相同含义。x的键结位置为其结合键所键结的苯环的能够进行取代的位置的任一处。使用通式(1
‑
1)所表示的二胺化合物而合成的聚合物由于氨基相对于酯位于对位,因此直线性变高,使用所述聚合物的液晶取向膜可表现出高的各向异性。
[0120]
[通式(1
‑
2)所表示的二胺化合物]
[0121]
作为通式(1
‑
1)所表示的二胺化合物的优选的例子,可列举下述通式(1
‑
2)所表示的二胺化合物。
[0122]
[化21]
[0123][0124]
通式(1
‑
2)中,r1及r2分别与通式(1)中的r1及r2为相同含义。通式(1
‑
2)所表示的二胺化合物就其制造中的原料获取的容易度而言是有用的。
[0125]
另外,通式(1)、通式(1
‑
1)或通式(1
‑
2)所表示的化合物中,优选为环丙烷环上的两个酯为反式构型。
[0126]
[通式(1
‑
3)所表示的化合物]
[0127]
作为通式(1
‑
1)所表示的二胺化合物的优选的例子,可列举下述通式(1
‑
3)所表示的二胺化合物及其对映体(镜像异构体)。通式(1
‑
3)所表示的化合物及其对映体可混合而用于聚合物的原料,也可混合当量作为外消旋体而用于聚合物的原料。
[0128]
[化22]
[0129][0130]
通式(1
‑
3)中,r1、r2、x及n分别与通式(1)中的r1、r2、x及n为相同含义。式(1
‑
3)所表示的二胺化合物及其对映体由于环丙烷环上的两个酯为反式构型,因此直线性变高,将
所述二胺化合物用于原料的聚合物的液晶取向膜可表现出高的各向异性。
[0131]
就特性优选的方面而言,r1及r2优选为氢原子、或者r1与r2成为一体而形成亚甲基。
[0132]
作为通式(1)所表示的二胺化合物的具体例,可列举下述式(1
‑2‑
1)、式(1
‑3‑
1)~式(1
‑3‑
13)、及式(1
‑4‑
1)~式(1
‑4‑
13)所表示的二胺化合物。下述式中,me表示甲基。
[0133]
[化23]
[0134]
[0135][0136]
式(1
‑3‑
1)与式(1
‑4‑
1)、式(1
‑3‑
2)与式(1
‑4‑
2)、式(1
‑3‑
3)与式(1
‑4‑
3)、式(1
‑3‑
4)与式(1
‑4‑
4)、式(1
‑3‑
5)与式(1
‑4‑
5)、式(1
‑3‑
6)与式(1
‑4‑
6)、式(1
‑3‑
7)与式(1
‑4‑
7)、式(1
‑3‑
8)与式(1
‑4‑
8)、式(1
‑3‑
9)与式(1
‑4‑
9)、式(1
‑3‑
10)与式(1
‑4‑
10)、式(1
‑3‑
11)与式(1
‑4‑
11)、式(1
‑3‑
12)与式(1
‑4‑
12)、及式(1
‑3‑
13)与式(1
‑4‑
13)分别处于对映体的关系。可将式(1
‑3‑
1)所表示的二胺化合物与式(1
‑4‑
1)所表示的二胺化合物的混合物、式(1
‑3‑
2)所表示的二胺化合物与式(1
‑4‑
2)所表示的二胺化合物的混合物、式(1
‑3‑
3)所
表示的二胺化合物与式(1
‑4‑
3)所表示的二胺化合物的混合物、式(1
‑3‑
4)所表示的二胺化合物与式(1
‑4‑
4)所表示的二胺化合物的混合物、式(1
‑3‑
5)所表示的二胺化合物与式(1
‑4‑
5)所表示的二胺化合物的混合物、式(1
‑3‑
6)所表示的二胺化合物与式(1
‑4‑
6)所表示的二胺化合物的混合物、式(1
‑3‑
7)所表示的二胺化合物与式(1
‑4‑
7)所表示的二胺化合物的混合物、式(1
‑3‑
8)所表示的二胺化合物与式(1
‑4‑
8)所表示的二胺化合物的混合物、式(1
‑3‑
9)所表示的二胺化合物与式(1
‑4‑
9)所表示的二胺化合物的混合物、式(1
‑3‑
10)所表示的二胺化合物与式(1
‑4‑
10)所表示的二胺化合物的混合物、式(1
‑3‑
11)所表示的二胺化合物与式(1
‑4‑
11)所表示的二胺化合物的混合物、式(1
‑3‑
12)所表示的二胺化合物与式(1
‑4‑
12)所表示的二胺化合物的混合物、及式(1
‑3‑
13)所表示的二胺化合物与式(1
‑4‑
13)所表示的二胺化合物的混合物分别作为二胺化合物(1)而用于原料组合物。
[0137]
本说明书中,也有时将式(1
‑3‑
1)所表示的二胺化合物与式(1
‑4‑
1)所表示的二胺化合物的混合物称为“二胺异构体混合物1”,式(1
‑3‑
2)所表示的二胺化合物与式(1
‑4‑
2)所表示的二胺化合物的混合物称为“二胺异构体混合物2”,式(1
‑3‑
3)所表示的二胺化合物与式(1
‑4‑
3)所表示的二胺化合物的混合物称为“二胺异构体混合物3”,式(1
‑3‑
4)所表示的二胺化合物与式(1
‑4‑
4)所表示的二胺化合物的混合物称为“二胺异构体混合物4”,式(1
‑3‑
5)所表示的二胺化合物与式(1
‑4‑
5)所表示的二胺化合物的混合物称为“二胺异构体混合物5”,式(1
‑3‑
6)所表示的二胺化合物与式(1
‑4‑
6)所表示的二胺化合物的混合物称为“二胺异构体混合物6”,式(1
‑3‑
7)所表示的二胺化合物与式(1
‑4‑
7)所表示的二胺化合物的混合物称为“二胺异构体混合物7”,式(1
‑3‑
8)所表示的二胺化合物与式(1
‑4‑
8)所表示的二胺化合物的混合物称为“二胺异构体混合物8”,式(1
‑3‑
9)所表示的二胺化合物与式(1
‑4‑
9)所表示的二胺化合物的混合物称为“二胺异构体混合物9”,式(1
‑3‑
10)所表示的二胺化合物与式(1
‑4‑
10)所表示的二胺化合物的混合物称为“二胺异构体混合物10”,式(1
‑3‑
11)所表示的二胺化合物与式(1
‑4‑
11)所表示的二胺化合物的混合物称为“二胺异构体混合物11”,式(1
‑3‑
12)所表示的二胺化合物与式(1
‑4‑
12)所表示的二胺化合物的混合物称为“二胺异构体混合物12”,及式(1
‑3‑
13)所表示的二胺化合物与式(1
‑4‑
13)所表示的二胺化合物的混合物称为“二胺异构体混合物13”。
[0138]
<聚合物>
[0139]
其次,对本发明的聚合物进行说明。
[0140]
本发明的聚合物的特征在于:是使包含二胺类与四羧酸二酐类的原料组合物聚合而成的聚合物或其衍生物,二胺类的至少一种为本发明的通式(1)所表示的二胺化合物。
[0141]
使包含二胺类与四羧酸二酐类的原料组合物聚合而成的聚合物或其衍生物中,二胺类与四羧酸二酐的聚合体为聚酰胺酸,其他聚合物为聚酰胺酸的衍生物。因此,本发明的聚合物也可称为作为聚酰胺酸或其衍生物、且聚酰胺酸的二胺单体的至少一种为本发明的通式(1)所表示的二胺化合物的聚合物。本发明的聚合物包含选自聚酰胺酸或其衍生物的群组中的至少一种聚合物。本发明的聚合物可包括聚酰胺酸或其衍生物的任一种,也可包括选自聚酰胺酸或其衍生物的群组中的两种以上的混合物。另外,本发明的聚合物也可构成选自聚酰胺酸的群组中的一种以上与选自聚酰胺酸的衍生物的群组中的一种以上的混合物。作为聚酰胺酸的衍生物,可列举:聚酰亚胺、部分聚酰亚胺、聚酰胺酸酯、聚酰胺酸
‑
聚酰胺共聚物及聚酰胺酰亚胺。本说明书中,也有时将这些称为聚酰胺酸衍生物。
[0142]
以下,对聚酰胺酸或其衍生物说明详情。
[0143]
如下述反应式所示般,聚酰胺酸为通过式(di)所表示的二胺类与式(an)所表示的四羧酸二酐的聚合反应而合成的聚合物,且具有式(paa)所表示的结构单元。用于聚酰胺酸的合成的二胺类及四羧酸二酐分别可为一种也可为两种以上。包含聚酰胺酸的液晶取向剂当在形成液晶取向膜的工序中进行加热煅烧时,聚酰胺酸进行酰亚胺化,可形成具有式(pi)所表示的结构单元的聚酰亚胺液晶取向膜。
[0144]
[化24]
[0145][0146]
(式中,x1表示四价有机基。x2表示二价有机基)
[0147]
关于x1中的四价有机基的优选的范围与具体例,可参照下述的四羧酸二酐类一栏中记载的四羧酸二酐所对应的结构。关于x2中的二价有机基的优选的范围与具体例,可参照关于式(1)或下述的二胺类一栏中记载的二胺或二酰肼所对应的结构的记载。
[0148]
聚酰胺酸衍生物为将聚酰胺酸的一部分取代为其他原子或原子团而改变了特性的化合物,特别优选为提高了在液晶取向剂中使用的溶剂中的溶解性的聚酰胺酸衍生物。作为此种聚酰胺酸衍生物,具体而言,可列举:1)聚酰胺酸的所有氨基与羧基进行脱水闭环反应而成的聚酰亚胺、2)部分地进行脱水闭环反应而成的部分聚酰亚胺、3)将聚酰胺酸的羧基变换为酯而成的聚酰胺酸酯、4)将四羧酸二酐化合物中包含的酸二酐的一部分取代为有机二羧酸并进行反应而获得的聚酰胺酸
‑
聚酰胺共聚物、以及5)使所述聚酰胺酸
‑
聚酰胺共聚物的一部分或全部进行脱水闭环反应而成的聚酰胺酰亚胺。这些衍生物中,例如作为聚酰亚胺,可列举具有所述式(pi)所表示的结构单元的聚酰亚胺,作为聚酰胺酸酯,可列举具有下述式(pae)所表示的结构单元的聚酰胺酸酯。
[0149]
[化25]
[0150][0151]
(式中,x1表示四价有机基,x2表示二价有机基,z独立地表示烷基)
[0152]
关于x1及x2的优选的范围与具体例,可参照关于式(paa)中的x1及x2的记载。z中优选为碳数1~6的直链状或分支状的烷基,更优选为甲基、乙基、丙基、异丙基、丁基、异丁基或叔丁基。
[0153]
本发明的聚酰胺酸或其衍生物可为包含第一聚合物链及结构与第一聚合物链不同的第二聚合物链的嵌段聚合物。另外,嵌段聚合物也可进而包含结构与第一聚合物链及
第二聚合物链不同的其他聚合物链。例如聚酰胺酸的嵌段聚合物可通过将式(paa)所表示的特定聚酰胺酸(paa1)的溶液与x1及x2的组合和聚酰胺酸(paa1)不同的聚酰胺酸(paa2)的溶液混合并加热来形成。如此所形成的聚酰胺酸的嵌段聚合物包含(paa1)
n1
所表示的嵌段与(paa2)
n2
所表示的嵌段。(paa1)
n1
及(paa2)
n2
中的n1及n2各自独立地为1以上的整数,优选为各自独立地为2以上的整数。嵌段聚合物中,将二胺化合物(1)用于原料组合物的聚合物链可为任一种,也可为两种以上,还可为所有的聚合物链。
[0154]
此处,聚酰胺酸嵌段聚合物可在分别单独制造两种以上的聚酰胺酸后进行混合并加热来合成,也可在相同的反应容器中合成两种以上的聚酰胺酸后进行加热来合成。
[0155]
在将本发明的聚酰胺酸设为作为聚酰胺酸衍生物的聚酰亚胺的情况下,可通过使所获得的聚酰胺酸溶液与作为脱水剂的乙酸酐、丙酸酐、三氟乙酸酐等酸酐、及作为脱水闭环催化剂的三乙胺、吡啶、三甲吡啶等三级胺一起在温度20℃~150℃下进行酰亚胺化反应,来获得聚酰亚胺。或者,也可通过使用大量的不良溶剂(甲醇、乙醇、异丙醇等醇系溶剂或乙二醇等二醇系溶剂)而使聚酰胺酸自所获得的聚酰胺酸溶液析出,并使所析出的聚酰胺酸在甲苯、二甲苯等溶剂中与所述脱水剂及脱水闭环催化剂一起在温度20℃~150℃下进行酰亚胺化反应,来获得聚酰亚胺。
[0156]
酰亚胺化反应中,脱水剂与脱水闭环催化剂的比例优选为0.1~10(摩尔比)。相对于所述聚酰胺酸的合成中使用的四羧酸二酐的摩尔量的合计,脱水剂与脱水闭环催化剂的合计使用量优选为1.5倍摩尔~10倍摩尔。通过调整所述酰亚胺化反应中使用的脱水剂、催化剂量、反应温度及反应时间,可控制酰亚胺化的程度,由此可获得仅聚酰胺酸的一部分酰亚胺化而成的部分聚酰亚胺。所获得的聚酰亚胺也可与反应中使用的溶剂分离并再溶解于其他溶剂中而用作液晶取向剂,或者也可不与溶剂分离而用作液晶取向剂。
[0157]
聚酰胺酸酯可利用以下方法来获得:通过使聚酰胺酸与含羟基的化合物、卤化物、含环氧基的化合物等反应而合成的方法,或者通过使由四羧酸二酐衍生的四羧酸二酯或四羧酸二酯二氯化物与二胺类反应而合成的方法。由四羧酸二酐衍生的四羧酸二酯例如可使四羧酸二酐与2当量的醇反应并开环而获得,四羧酸二酯二氯化物可通过使四羧酸二酯与2当量以上的氯化剂(例如亚硫酰氯等)反应而获得。再者,聚酰胺酸酯可仅具有酰胺酸酯结构,也可为酰胺酸结构与酰胺酸酯结构并存的部分酯化物。通过将通式(1)所表示的二胺化合物用作二胺类的至少一种,可获得本发明的聚酰胺酸酯。
[0158]
将通式(1)所表示的二胺化合物用于原料的聚酰胺酸或其衍生物可与聚酰亚胺膜的形成中所使用的现有的聚酰胺酸或其衍生物同样地制造。
[0159]
相对于二胺类的合计1摩尔,四羧酸二酐类的总投入量优选为设为0.9摩尔~1.1摩尔。
[0160]
本发明的液晶取向剂可仅包含这些聚酰胺酸、聚酰胺酸酯及将这些加以酰亚胺化而获得的聚酰亚胺中的一种,也可包含两种以上。
[0161]
作为本发明的聚合物的聚酰胺酸或其衍生物的分子量以聚苯乙烯换算的重量平均分子量(mw)计,优选为5,000~500,000,更优选为5,000~50,000。聚酰胺酸或其衍生物的分子量可根据利用凝胶渗透色谱(gel permeation chromatography,gpc)法的测定来求出。
[0162]
作为本发明的聚合物的聚酰胺酸或其衍生物可通过以下方式来确认它的存在:利
用红外光谱法(infrared spectroscopy,ir)、核磁共振分析(nuclear magnetic resonance,nmr)对在大量的不良溶剂中沉淀而获得的固体成分进行分析。另外,可通过以下方式来确认所使用的单体:利用气相色谱法(gas chromatography,gc)、高效液相色谱法(high performance liquid chromatography,hplc)或气相色谱质谱法(gas chromatography
‑
mass spectrometry,gc
‑
ms)对使用氢氧化钾或氢氧化钠等强碱的水溶液将聚酰胺酸或其衍生物分解后,使用有机溶剂从其分解物中所提取出的提取物进行分析。
[0163]
四羧酸二酐类
[0164]
作为本发明中聚合物的原料组合物中使用的四羧酸二酐类,可无限制地自现有的四羧酸二酐类中选择。
[0165]
以下列举四羧酸二酐的例子。也可将这些四羧酸二酐衍生为四羧酸二酯或四羧酸二酯二氯化物而用于聚合物的原料。即,设为本发明的“四羧酸二酐类”中除包含四羧酸二酐以外,也包含四羧酸二酐的衍生物例如四羧酸二酯或四羧酸二酯二卤化物。这些中,可将任一种供于聚合,也可将两种以上组合而供于聚合。
[0166]
另外,四羧酸二酐可属于二羧酸酐直接键结于芳香环上的芳香族系(包含杂芳香环系),也可属于二羧酸酐未直接键结于芳香环上的脂肪族系(包含杂环系)。
[0167]
作为此种四羧酸二酐的例子,可列举以下的式(an
‑
1)~式(an
‑
9)、式(an
‑
11)、式(an
‑
12)、式(an
‑
15)、式(an
‑
10
‑
1)、式(an
‑
10
‑
2)、及式(an
‑
16
‑
1)~式(an
‑
16
‑
17)所表示的四羧酸二酐。
[0168]
[式(an
‑
1)所表示的四羧酸二酐]
[0169]
[化26]
[0170][0171]
式(an
‑
1)中,r
11
各自独立地表示氢原子或甲基。g
11
表示单键、碳数1~12的亚烷基、1,4
‑
亚苯基或1,4
‑
亚环己基。x
11
各自独立地表示单键或
‑
ch2‑
。g
12
各自独立地表示下述三价基的任一种。
[0172]
[化27]
[0173][0174]
在g
12
为>ch
‑
时,>ch
‑
的氢原子可经甲基取代。在g
12
为>n
‑
时,g
11
不为单键及
‑
ch2‑
,x
11
不为单键。r
11
各自独立地表示氢原子或甲基。
[0175]
作为式(an
‑
1)所表示的四羧酸二酐的例子,可列举下述式(an
‑1‑
1)~式(an
‑1‑
15)所表示的化合物。
[0176]
[化28]
[0177][0178]
式(an
‑1‑
2)及式(an
‑1‑
14)中,m各自独立地为1~12的整数。
[0179]
[式(an
‑
2)所表示的四羧酸二酐]
[0180]
[化29]
[0181][0182]
式(an
‑
2)中,r
61
各自独立地表示氢原子、碳数1~5的烷基或苯基。
[0183]
作为式(an
‑
2)所表示的四羧酸二酐的例子,可列举下述式(an
‑2‑
1)~式(an
‑2‑
3)所表示的化合物。
[0184]
[化30]
[0185][0186]
[式(an
‑
3)所表示的四羧酸二酐]
[0187]
[化31]
[0188][0189]
式(an
‑
3)中,环a
11
表示环己烷环或苯环。
[0190]
作为式(an
‑
3)所表示的四羧酸二酐的例子,可列举下述式(an
‑3‑
1)、式(an
‑3‑
2)所表示的化合物。
[0191]
[化32]
[0192][0193]
[式(an
‑
4)所表示的四羧酸二酐]
[0194]
[化33]
[0195][0196]
式(an
‑
4)中,g
13
表示单键、
‑
c≡c
‑
、
‑
(ch2)
m
‑
、
‑
o
‑
、
‑
s
‑
、
‑
c(ch3)2‑
、
‑
so2‑
、
‑
co
‑
、
‑
c(cf3)2‑
、下述式(g13
‑
1)或下述式(g13
‑
2)所表示的二价基,m为1~12的整数。环a
11
各自独立地表示环己烷环或苯环。g
13
可键结于环a
11
的任意的位置。此处,“任意的位置”是指其结合键所键结的骨架结构的能够进行取代的位置。以下的说明中的“任意的位置”也设为相同的含义。
[0197]
[化34]
[0198][0199]
式(g13
‑
1)及式(g13
‑
2)中,g
13a
及g
13b
各自独立地表示单键、
‑
o
‑
、
‑
coo
‑
、
‑
oco
‑
、
‑
conh
‑
或
‑
nhco
‑
所表示的二价基。各式表示的亚苯基优选为1,4
‑
亚苯基或1,3
‑
亚苯基。式(g13
‑
2)中,g
13c
为碳数1~4的亚烷基或亚环烷基,g
13d
为甲基,n为0~2的整数。
[0200]
作为式(an
‑
4)所表示的四羧酸二酐的例子,可列举下述式(an
‑4‑
1)~式(an
‑4‑
37)所表示的化合物。
[0201]
[化35]
[0202][0203]
[化36]
[0204][0205]
式(an
‑4‑
17)中,m为1~12的整数。
[0206]
[化37]
[0207][0208]
[化38]
[0209][0210]
[化39]
[0211][0212]
[式(an
‑
5)所表示的四羧酸二酐]
[0213]
[化40]
[0214][0215]
式(an
‑
5)中,r
11
各自独立地表示氢原子或甲基。两个r
11
中苯环上的r
11
键结于苯环的能够进行取代的位置的任一处。
[0216]
作为式(an
‑
5)所表示的四羧酸二酐的例子,可列举下述式(an
‑5‑
1)~式(an
‑5‑
3)所表示的化合物。
[0217]
[化41]
[0218][0219]
[式(an
‑
6)所表示的四羧酸二酐]
[0220]
[化42]
[0221][0222]
式(an
‑
6)中,x
11
各自独立地表示单键或
‑
ch2‑
。x
12
表示
‑
ch2‑
、
‑
ch2ch2‑
或
‑
ch=ch
‑
。n为1或2。当n为2时,两个x
12
可相互相同也可不同。
[0223]
作为式(an
‑
6)所表示的四羧酸二酐的例子,可列举下述式(an
‑6‑
1)~式(an
‑6‑
12)所表示的化合物。
[0224]
[化43]
[0225][0226]
[式(an
‑
7)所表示的四羧酸二酐]
[0227]
[化44]
[0228][0229]
式(an
‑
7)中,x
11
表示单键或
‑
ch2‑
。
[0230]
作为式(an
‑
7)所表示的四羧酸二酐的例子,可列举下述式(an
‑7‑
1)、式(an
‑7‑
2)所表示的化合物。
[0231]
[化45]
[0232][0233]
[式(an
‑
8)所表示的四羧酸二酐]
[0234]
[化46]
[0235][0236]
式(an
‑
8)中,x
11
表示单键或
‑
ch2‑
。r
12
表示氢原子、甲基、乙基或苯基。环a
12
表示环己烷环或环己烯环。
[0237]
作为式(an
‑
8)所表示的四羧酸二酐的例子,可列举下述式(an
‑8‑
1)、式(an
‑8‑
2)所表示的化合物。
[0238]
[化47]
[0239][0240]
[式(an
‑
9)所表示的四羧酸二酐]
[0241]
[化48]
[0242][0243]
式(an
‑
9)中,r各自独立地为0或1。
[0244]
作为式(an
‑
9)所表示的四羧酸二酐的例子,可列举下述式(an
‑9‑
1)~式(an
‑9‑
3)所表示的化合物。
[0245]
[化49]
[0246][0247]
[式(an
‑
10
‑
1)及式(an
‑
10
‑
2)所表示的四羧酸二酐]
[0248]
[化50]
[0249][0250]
[式(an
‑
11)所表示的四羧酸二酐]
[0251]
[化51]
[0252][0253]
式(an
‑
11)中,环a
11
各自独立地表示环己烷环或苯环。
[0254]
作为式(an
‑
11)所表示的四羧酸二酐的例子,可列举下述式(an
‑
11
‑
1)~式(an
‑
11
‑
3)所表示的化合物。
[0255]
[化52]
[0256]
[0257]
[式(an
‑
12)所表示的四羧酸二酐]
[0258]
[化53]
[0259][0260]
式(an
‑
12)中,环a
11
各自独立地表示环己烷环或苯环。
[0261]
作为式(an
‑
12)所表示的四羧酸二酐的例子,可列举下述式(an
‑
12
‑
1)~式(an
‑
12
‑
3)所表示的化合物。
[0262]
[化54]
[0263][0264]
[式(an
‑
15)所表示的四羧酸二酐]
[0265]
[化55]
[0266][0267]
式(an
‑
15)中,w为1~10的整数。
[0268]
作为式(an
‑
15)所表示的四羧酸二酐的例子,可列举下述式(an
‑
15
‑
1)~式(an
‑
15
‑
3)所表示的化合物。
[0269]
[化56]
[0270][0271]
作为所述以外的四羧酸二酐,可列举下述式(an
‑
16
‑
1)~式(an
‑
16
‑
17)所表示的化合物。
[0272]
[化57]
[0273][0274]
[四羧酸二酐类的更优选的例子]
[0275]
对所述四羧酸二酐中提高后述的液晶取向膜的各特性的适宜的材料进行叙述。在重视进一步提高形成液晶取向膜时的各向异性或液晶取向性的情况下,更优选为式(an
‑3‑
2)、式(an
‑4‑
5)、式(an
‑4‑
29)或式(an
‑4‑
37)所表示的化合物。
[0276]
在重视提高液晶显示元件的透过率的情况下,优选为式(an
‑1‑
1)、式(an
‑1‑
2)、式(an
‑2‑
1)、式(an
‑3‑
1)、式(an
‑4‑
17)、式(an
‑4‑
30)、式(an
‑5‑
1)、式(an
‑7‑
2)、式(an
‑
10
‑
1)、式(an
‑
16
‑
3)或式(an
‑
16
‑
4)所表示的化合物,其中式(an
‑1‑
2)中,优选为m=4~8,式(an
‑4‑
17)中,优选为m=4~8。
[0277]
在重视提高液晶显示元件的电压保持率(voltage holding ratio,vhr)的情况
下,优选为式(an
‑1‑
1)、式(an
‑1‑
2)、式(an
‑2‑
1)、式(an
‑3‑
1)、式(an
‑4‑
17)、式(an
‑4‑
30)、式(an
‑7‑
2)、式(an
‑
10
‑
1)、式(an
‑
16
‑
3)、式(an
‑
16
‑
4)或式(an
‑
16
‑
17)所表示的化合物,式(an
‑1‑
2)中,优选为m=4~8,式(an
‑4‑
17)中,优选为m=4~8。
[0278]
作为防止烧痕的方法之一,有效的是通过使液晶取向膜的体积电阻值降低而使液晶取向膜中的残留电荷(残留直流电(direct current,dc))的缓和速度提高。在重视所述目的的情况下,优选为式(an
‑1‑
13)、式(an
‑3‑
2)、式(an
‑4‑
21)、式(an
‑4‑
29)或式(an
‑
11
‑
3)所表示的化合物。
[0279]
式(an
‑4‑
32)、式(an
‑4‑
33)、式(an
‑4‑
34)、式(an
‑4‑
35)、及式(an
‑4‑
36)为有可能发生光弗里斯重排反应的化合物。本发明的二胺化合物(1)具有光反应性,因此与其组合的四羧酸二酐并不一定具有光反应性,但也可与本发明的二胺化合物(1)组合而使用。
[0280]
二胺类
[0281]
本发明中聚合物的原料组合物中使用的二胺类包含本发明的通式(1)所表示的二胺化合物(二胺化合物(1))。关于二胺化合物(1)的说明,可参照<二胺化合物>一栏的记载。二胺类包含的二胺化合物(1)可为一种也可为两种以上。另外,二胺类可仅包含二胺化合物(1),也可包含其他二胺类。
[0282]
以下,对可用于二胺类中的二胺化合物(1)以外的二胺类(其他二胺类)进行说明。
[0283]
作为其他二胺类,可无限制地自现有的二胺类中选择。此处,设为“其他二胺类”中除包含二胺以外,也包含二酰肼。
[0284]
另外,二胺可根据其结构而分成两种。即,具有侧链基的二胺与不具有侧链基的二胺,所述侧链基是在将连结两个氨基的骨架看作主链时,自主链中分支的基。以下的说明中,有时将此种具有侧链基的二胺称为侧链型二胺。而且,有时将此种不具有侧链基的二胺称为非侧链型二胺。所述侧链基是具有增大预倾角的效果的基。
[0285]
原料组合物中使用的其他二胺类的二胺可为侧链型二胺也可为非侧链型二胺,还可将所述两者组合。通过将非侧链型二胺与侧链型二胺适当地分开使用,可对应于各自所需的预倾角。
[0286]
侧链型二胺优选为以不损及本发明的特性的程度来并用。另外,关于侧链型二胺及非侧链型二胺,优选为出于提高对于液晶的垂直取向性、vhr、及残像特性等特性的目的进行取舍选择来使用。
[0287]
[非侧链型二胺]
[0288]
在以下的式(di
‑
1)~式(di
‑
16)中示出已知的不具有侧链的二胺。
[0289]
[化58]
[0290][0291]
[化59]
[0292][0293]
[化60]
[0294][0295]
键结位置未固定在构成环的碳原子上的基表示在所述环上的键结位置为任意。或者,环己烷环或苯环上的氨基的键结位置为除g
21
、g
22
、g
33
、或g
34
的键结位置以外的任意的位置。
[0296]
所述式(di
‑
1)中,g
20
表示
‑
ch2‑
或式(di
‑1‑
a)所表示的基。在g
20
为
‑
ch2‑
时,m个
‑
ch2‑
的至少一个可经取代为
‑
nh
‑
、
‑
o
‑
,m个
‑
ch2‑
的至少一个氢原子可经羟基或甲基取代。m为1~12的整数。在di
‑
1中的m为2以上时,多个g
20
可相互相同也可不同。其中,在g
20
为下述式(di
‑1‑
a)所表示的基时,m为1。
[0297]
[化61]
[0298][0299]
式(di
‑1‑
a)中,v各自独立地为1~6的整数。
[0300]
式(di
‑
3)、式(di
‑
6)及式(di
‑
7)中,g
21
各自独立地表示单键、
‑
nh
‑
、
‑
nch3‑
、
‑
o
‑
、
‑
s
‑
、
‑
s
‑
s
‑
、
‑
so2‑
、
‑
co
‑
、
‑
coo
‑
、
‑
oco
‑
、
‑
conch3‑
、
‑
conh
‑
、
‑
c(ch3)2‑
、
‑
c(cf3)2‑
、
‑
(ch2)
m
‑
、
‑
o
‑
(ch2)
m
‑
o
‑
、
‑
n(ch3)
‑
(ch2)
k
‑
n(ch3)
‑
、
‑
(o
‑
c2h4)
m
‑
o
‑
、
‑
o
‑
ch2‑
c(cf3)2‑
ch2‑
o
‑
、
‑
o
‑
co
‑
(ch2)
m
‑
co
‑
o
‑
、
‑
co
‑
o
‑
(ch2)
m
‑
o
‑
co
‑
、
‑
(ch2)
m
‑
nh
‑
(ch2)
m
‑
、
‑
co
‑
(ch2)
k
‑
nh
‑
(ch2)
k
‑
、
‑
(nh
‑
(ch2)
m
)
k
‑
nh
‑
、
‑
co
‑
c3h6‑
(nh
‑
c3h6)
n
‑
co
‑
或
‑
s
‑
(ch2)
m
‑
s
‑
,m各自独立地为1~12的整数,k各自独立地为1~5的整数,n为1或2。
[0301]
式(di
‑
4)中,s各自独立地为0~2的整数。
[0302]
式(di
‑
4)中,苯环的至少一个氢原子可经选自下述式(di
‑4‑
a)~式(di
‑4‑
i)的任一者所表示的基的群组中的一个取代。
[0303]
[化62]
[0304][0305]
[化63]
[0306][0307]
式(di
‑4‑
a)及式(di
‑4‑
b)中,r
20
各自独立地表示氢原子或甲基。式(di
‑4‑
f)及式(di
‑4‑
g)中,m各自独立地为0~12的整数,boc为叔丁氧基羰基。
[0308]
式(di
‑
5)中,g
33
为单键、
‑
nh
‑
、
‑
nch3‑
、
‑
o
‑
、
‑
s
‑
、
‑
s
‑
s
‑
、
‑
so2‑
、
‑
co
‑
、
‑
coo
‑
、
‑
conch3‑
、
‑
conh
‑
、
‑
c(ch3)2‑
、
‑
c(cf3)2‑
、
‑
(ch2)
m
‑
、
‑
o
‑
(ch2)
m
‑
o
‑
、
‑
n(ch3)
‑
(ch2)
k
‑
n(ch3)
‑
、
‑
(o
‑
c2h4)
m
‑
o
‑
、
‑
o
‑
ch2‑
c(cf3)2‑
ch2‑
o
‑
、
‑
o
‑
co
‑
(ch2)
m
‑
co
‑
o
‑
、
‑
co
‑
o
‑
(ch2)
m
‑
o
‑
co
‑
、
‑
(ch2)
m
‑
nh
‑
(ch2)
m
‑
、
‑
co
‑
(ch2)
k
‑
nh
‑
(ch2)
k
‑
、
‑
(nh
‑
(ch2)
m
)
k
‑
nh
‑
、
‑
co
‑
c3h6‑
(nh
‑
c3h6)
n
‑
co
‑
、
‑
s
‑
(ch2)
m
‑
s
‑
、
‑
n(boc)
‑
(ch2)
e
‑
n(boc)
‑
、
‑
nh
‑
(ch2)
e
‑
n(boc)
‑
、
‑
n(boc)
‑
(ch2)
e
‑
、
‑
n(boc)
‑
(ch2)
e
‑
n(ch3)
‑
、
‑
(ch2)
m
‑
n(boc)
‑
conh
‑
(ch2)
m
‑
、
‑
(ch2)
m
‑
n(boc)
‑
(ch2)
m
‑
、下述式(di
‑5‑
a)、下述式(di
‑5‑
b)或下述式(di
‑5‑
c)所表示的基,m各自独立地为1~12的整数,k为1~5的整数,e为2~10的整数,n为1或2。boc为叔丁氧基羰基。
[0309]
[化64]
[0310][0311]
式(di
‑5‑
a)及式(di
‑5‑
c)中,q各自独立地为0~6的整数。r
44
表示氢原子、羟基、碳数1~6的烷基或碳数1~6的烷氧基。
[0312]
式(di
‑
6)中,g
34
各自独立地表示单键、
‑
o
‑
、
‑
s
‑
、
‑
co
‑
、
‑
coo
‑
、
‑
oco
‑
、
‑
c(ch3)2‑
、
‑
c(cf3)2‑
或碳数1~10的亚烷基,环a
12
表示环己烷环或苯环。
[0313]
式(di
‑
7)中,g
22
各自独立地表示单键、
‑
o
‑
、
‑
s
‑
、
‑
co
‑
、
‑
c(ch3)2‑
、
‑
c(cf3)2‑
或碳数1~10的亚烷基。
[0314]
式(di
‑
2)~式(di
‑
7)中的环己烷环及苯环的至少一个氢原子可经氟原子、氯原子、碳数1~3的烷基、甲氧基、羟基、三氟甲基、羧基、氨甲酰基、苯基氨基、苯基或苄基取代。式(di
‑
5)中,g
33
为单键时,苯环的至少一个氢原子可经n
‑
(叔丁氧基羰基)氨基或n,n
‑
双(叔丁氧基羰基)氨基取代。
[0315]
式(di
‑
11)中,r为0或1。式(di
‑
8)~式(di
‑
11)中,键结于环上的氨基的键结位置为任意的位置。
[0316]
式(di
‑
12)中,r
21
及r
22
各自独立地表示碳数1~3的烷基或苯基,g
23
各自独立地表示碳数1~6的亚烷基、亚苯基、或经烷基取代的亚苯基,w为1~10的整数。
[0317]
式(di
‑
13)中,r
23
各自独立地表示碳数1~5的烷基、碳数1~5的烷氧基或氯原子,p各自独立地为0~3的整数,q为0~4的整数。
[0318]
式(di
‑
14)中,环b表示单环的杂环式芳香族基,r
24
表示氢原子、氟原子、氯原子、碳数1~6的烷基、烷氧基、烯基、或炔基,q各自独立地为0~4的整数。当q为2以上时,多个r
24
可相互相同也可不同。式(di
‑
15)中,环c表示杂环式芳香族基或杂环式脂肪族基。式(di
‑
16)中,g
24
表示单键、碳数2~6的亚烷基或1,4
‑
亚苯基,r为0或1。而且,键结位置未固定在构成环的碳原子上的基表示在所述环上的键结位置为任意。式(di
‑
13)~式(di
‑
16)中,键结于环上的氨基的键结位置为任意的位置。
[0319]
其次,列举具体例对已知的不具有侧链的二胺进行更详细的说明。在以下的式(di
‑1‑
1)~式(di
‑1‑
9)中示出式(di
‑
1)所表示的二胺的例子。
[0320]
[化65]
[0321][0322]
式(di
‑1‑
7)及式(di
‑1‑
8)中,k各自独立地为1~3的整数。式(di
‑1‑
9)中,v各自独立地为1~6的整数。
[0323]
在以下的式(di
‑2‑
1)、式(di
‑2‑
2)、式(di
‑3‑
1)~式(di
‑3‑
3)中示出式(di
‑
2)~式(di
‑
3)所表示的二胺的例子。
[0324]
[化66]
[0325][0326]
在以下的式(di
‑4‑
1)~式(di
‑4‑
29)中示出式(di
‑
4)所表示的二胺的例子。
[0327]
[化67]
[0328][0329]
[化68]
[0330][0331]
[化69]
[0332][0333]
[化70]
[0334][0335]
[化71]
[0336][0337]
[化72]
[0338][0339]
式(di
‑4‑
20)及式(di
‑4‑
21)中,m为1~12的整数。在这些式中,boc为叔丁氧基羰基。
[0340]
[化73]
[0341][0342]
在以下的式(di
‑5‑
1)~式(di
‑5‑
50)中示出式(di
‑
5)所表示的二胺的例子。
[0343]
[化74]
[0344][0345]
式(di
‑5‑
1)中,m为1~12的整数。
[0346]
[化75]
[0347][0348]
式(di
‑5‑
12)及式(di
‑5‑
13)中,m各自独立地为1~12的整数。
[0349]
[化76]
[0350][0351]
式(di
‑5‑
16)中,v为1~6的整数。
[0352]
[化77]
[0353][0354]
式(di
‑5‑
30)中,k为1~5的整数。
[0355]
[化78]
[0356][0357]
式(di
‑5‑
35)~式(di
‑5‑
37)及式(di
‑5‑
39)中,m各自独立地为1~12的整数,式(di
‑5‑
38)及式(di
‑5‑
39)中,k各自独立地为1~5的整数,式(di
‑5‑
40)中,n为1或2的整数。
[0358]
[化79]
[0359][0360]
式(di
‑5‑
42)~式(di
‑5‑
44)中,e为2~10的整数,式(di
‑5‑
45)中,r
43
各自独立地为氢原子、n
‑
(叔丁氧基羰基)氨基或n,n
‑
双(叔丁氧基羰基)氨基。式(di
‑5‑
42)~式(di
‑5‑
44)中,boc为叔丁氧基羰基。
[0361]
[化80]
[0362][0363]
[化81]
[0364][0365]
在以下的式(di
‑6‑
1)~式(di
‑6‑
10)中示出式(di
‑
6)所表示的二胺的例子。
[0366]
[化82]
[0367][0368]
在以下的式(di
‑7‑
1)~式(di
‑7‑
11)中示出式(di
‑
7)所表示的二胺的例子。
[0369]
[化83]
[0370][0371]
式(di
‑7‑
3)及式(di
‑7‑
4)中,m为1~12的整数,n各自独立地为1或2。
[0372]
[化84]
[0373][0374]
[化85]
[0375][0376]
在以下的式(di
‑8‑
1)~式(di
‑8‑
4)中示出式(di
‑
8)所表示的二胺的例子。
[0377]
[化86]
[0378][0379]
在以下的式(di
‑9‑
1)~式(di
‑9‑
3)中示出式(di
‑
9)所表示的二胺的例子。
[0380]
[化87]
[0381][0382]
在以下的式(di
‑
10
‑
1)、式(di
‑
10
‑
2)中示出式(di
‑
10)所表示的二胺的例子。
[0383]
[化88]
[0384][0385]
在以下的式(di
‑
11
‑
1)~式(di
‑
11
‑
3)中示出式(di
‑
11)所表示的二胺的例子。
[0386]
[化89]
[0387][0388]
在以下的式(di
‑
12
‑
1)中示出式(di
‑
12)所表示的二胺的例子。
[0389]
[化90]
[0390][0391]
在以下的式(di
‑
13
‑
1)~式(di
‑
13
‑
13)中示出式(di
‑
13)所表示的二胺的例子。
[0392]
[化91]
[0393][0394]
[化92]
[0395][0396]
[化93]
[0397][0398]
在以下的式(di
‑
14
‑
1)~式(di
‑
14
‑
9)中示出式(di
‑
14)所表示的二胺的例子。
[0399]
[化94]
[0400][0401]
在以下的式(di
‑
15
‑
1)~式(di
‑
15
‑
12)中示出式(di
‑
15)所表示的二胺的例子。
[0402]
[化95]
[0403][0404]
[化96]
[0405][0406]
在以下的式(di
‑
16
‑
1)中示出式(di
‑
16)所表示的二胺的例子。
[0407]
[化97]
[0408][0409]
[非侧链型二酰肼]
[0410]
其次,对可用于本发明的聚合物的原料组合物中的二酰肼进行说明。作为已知的不具有侧链的二酰肼,可列举以下的式(dih
‑
1)~式(dih
‑
3)的任一者所表示的化合物。
[0411]
[化98]
[0412][0413]
式(dih
‑
1)中,g
25
表示单键、碳数1~20的亚烷基、
‑
co
‑
、
‑
o
‑
、
‑
s
‑
、
‑
so2‑
、
‑
c(ch3)2‑
或
‑
c(cf3)2‑
。
[0414]
式(dih
‑
2)中,环d表示环己烷环、苯环或萘环,所述基的至少一个氢原子可经甲基、乙基或苯基取代。式(dih
‑
3)中,环e各自独立地表示环己烷环或苯环,所述基的至少一个氢原子可经甲基、乙基或苯基取代。多个环e可相互相同也可不同。式(dih
‑
3)中,y表示单键、碳数1~20的亚烷基、
‑
co
‑
、
‑
o
‑
、
‑
s
‑
、
‑
so2‑
、
‑
c(ch3)2‑
或
‑
c(cf3)2‑
。式(dih
‑
2)及式(dih
‑
3)中,键结于环上的酰肼基的键结位置为任意的位置。
[0415]
在以下的式(dih
‑1‑
1)、式(dih
‑1‑
2)、式(dih
‑2‑
1)~式(dih
‑2‑
3)、式(dih
‑3‑
1)~式(dih
‑3‑
6)中示出式(dih
‑
1)~式(dih
‑
3)的任一者所表示的化合物的例子。
[0416]
[化99]
[0417][0418]
式(dih
‑1‑
2)中,m为1~12的整数。
[0419]
[化100]
[0420][0421]
[化101]
[0422][0423]
[侧链型二胺]
[0424]
对适合于增大预倾角的目的的二胺进行说明。作为适合于增大预倾角的目的且具有侧链基的二胺,可列举式(di
‑
31)~式(di
‑
35)、及式(di
‑
36
‑
1)~式(di
‑
36
‑
8)的任一者所表示的二胺。
[0425]
[化102]
[0426][0427]
式(di
‑
31)中,g
26
表示单键、
‑
o
‑
、
‑
coo
‑
、
‑
oco
‑
、
‑
co
‑
、
‑
conh
‑
、
‑
ch2o
‑
、
‑
och2‑
、
‑
cf2o
‑
、
‑
ocf2‑
或
‑
(ch2)
ma
‑
,ma为1~12的整数。g
26
的优选的例子为单键、
‑
o
‑
、
‑
coo
‑
、
‑
oco
‑
、
‑
ch2o
‑
及碳数1~3的亚烷基,特别优选的例子为单键、
‑
o
‑
、
‑
coo
‑
、
‑
oco
‑
、
‑
ch2o
‑
、
‑
ch2‑
及
‑
ch2ch2‑
。r
25
表示碳数3~30的烷基、苯基、具有类固醇骨架的基或下述式(di
‑
31
‑
a)所表示的基。所述烷基中,至少一个氢原子可经氟原子取代,而且至少一个
‑
ch2‑
可将
‑
o
‑
、
‑
ch=ch
‑
或
‑
c≡c
‑
取代。所述苯基的氢原子可经氟原子、甲基、甲氧基、氟甲基氧基、二氟甲基氧基、三氟甲基氧基、碳数3~30的烷基或碳数3~30的烷氧基取代。键结于苯环上的氨基的键结位置表示在所述环上为任意的位置,所述键结位置优选为相互处于间位或对位的关系的位置。即,在将基“r
25
‑
g
26
‑”
的键结位置设为1位时,两个氨基的键结位置优选为3位与5位、或2位与5位。
[0428]
[化103]
[0429][0430]
式(di
‑
31
‑
a)中,g
27
、g
28
及g
29
为键结基,这些各自独立地为单键或碳数1~12的亚烷基,所述亚烷基的一个以上的
‑
ch2‑
可经
‑
o
‑
、
‑
coo
‑
、
‑
oco
‑
、
‑
conh
‑
或
‑
ch=ch
‑
取代。环
b
21
、环b
22
、环b
23
及环b
24
各自独立地表示1,4
‑
亚苯基、1,4
‑
亚环己基、1,3
‑
二噁烷
‑
2,5
‑
二基、嘧啶
‑
2,5
‑
二基、吡啶
‑
2,5
‑
二基、萘
‑
1,5
‑
二基、萘
‑
2,7
‑
二基或蒽
‑
9,10
‑
二基,环b
21
、环b
22
、环b
23
及环b
24
中,至少一个氢原子可经氟原子或甲基取代,s、t及u各自独立地为0~2的整数,这些的合计为1~5,在s、t或u为2时,各个括号内的两个键结基可相同也可不同,而且,两个环可相同也可不同。r
26
表示氢原子、氟原子、羟基、碳数1~30的烷基、碳数1~30的氟取代烷基、碳数1~30的烷氧基、氰基、氟甲基氧基、二氟甲基氧基或三氟甲基氧基,所述碳数1~30的烷基、或碳数1~30的烷氧基的至少一个
‑
ch2‑
可经下述式(di
‑
31
‑
b)所表示的二价基取代。
[0431]
[化104]
[0432][0433]
式(di
‑
31
‑
b)中,r
27
及r
28
各自独立地为碳数1~3的烷基,v为1~6的整数。
[0434]
[化105]
[0435][0436]
式(di
‑
32)及式(di
‑
33)中,g
30
各自独立地表示单键、
‑
co
‑
或
‑
ch2‑
,r
29
各自独立地表示氢原子或甲基,r
30
各自独立地表示氢原子、碳数1~20的烷基或碳数2~20的烯基。式(di
‑
33)中的苯环的至少一个氢原子可经碳数1~20的烷基或苯基取代。而且,键结位置未固定在构成环的任一个碳原子上的基表示在所述环上的键结位置为任意。优选为式(di
‑
32)中的两个基“氨基苯基
‑
g
30
‑
o
‑”
的其中一个键结于类固醇核的3位,另一个键结于类固醇核的6位。式(di
‑
33)中的两个基“氨基苯基
‑
g
30
‑
o
‑”
在苯环上的键结位置优选为相对于类固醇核的键结位置,分别为间位或对位。式(di
‑
32)及式(di
‑
33)中,键结于苯环上的氨基表示在所述环上的键结位置为任意。
[0437]
[化106]
[0438][0439]
式(di
‑
34)及式(di
‑
35)中,g
31
各自独立地表示
‑
o
‑
或碳数1~6的亚烷基,g
32
表示单键或碳数1~3的亚烷基。r
31
表示氢原子或碳数1~20的烷基,所述烷基的至少一个
‑
ch2‑
可经
‑
o
‑
、
‑
ch=ch
‑
或
‑
c≡c
‑
取代。r
32
表示碳数6~22的烷基,r
33
表示氢原子或碳数1~22的烷基。环b
25
为1,4
‑
亚苯基或1,4
‑
亚环己基,r为0或1。而且,键结于苯环上的氨基表示在所述环上的键结位置为任意,优选为各自独立地相对于g
31
的键结位置而为间位或对位。
[0440]
更具体而言,在以下的式(di
‑
31
‑
1)~式(di
‑
31
‑
55)中示出式(di
‑
31)所表示的化合物的例子。
[0441]
[化107]
[0442][0443]
式(di
‑
31
‑
1)~式(di
‑
31
‑
11)中,r
34
各自独立地表示碳数1~30的烷基或碳数1~30的烷氧基,优选为碳数5~25的烷基或碳数5~25的烷氧基。r
35
各自独立地表示碳数1~30的烷基或碳数1~30的烷氧基,优选为碳数3~25的烷基或碳数3~25的烷氧基。
[0444]
[化108]
[0445][0446]
式(di
‑
31
‑
12)~式(di
‑
31
‑
17)中,r
36
各自独立地表示碳数4~30的烷基,优选为碳
数6~25的烷基。r
37
各自独立地表示碳数6~30的烷基,优选为碳数8~25的烷基。
[0447]
[化109]
[0448][0449]
[化111]
[0450][0451]
[化112]
[0452][0453]
[化113]
[0454][0455]
式(di
‑
31
‑
18)~式(di
‑
31
‑
43)中,r
38
各自独立地表示碳数1~20的烷基或碳数1~20的烷氧基,优选为碳数3~20的烷基或碳数3~20的烷氧基。r
39
各自独立地表示氢原子、氟原子、碳数1~30的烷基、碳数1~30的烷氧基、氰基、氟甲基氧基、二氟甲基氧基或三氟甲基氧基,优选为碳数3~25的烷基或碳数3~25的烷氧基。而且g
33
表示碳数1~20的亚烷基。
[0456]
[化114]
[0457][0458]
[化115]
[0459][0460]
[化116]
[0461][0462]
[化117]
[0463][0464]
在以下的式(di
‑
32
‑
1)~式(di
‑
32
‑
4)中示出式(di
‑
32)所表示的化合物的例子。
[0465]
[化118]
[0466][0467]
在以下的式(di
‑
33
‑
1)~式(di
‑
33
‑
8)中示出式(di
‑
33)所表示的化合物的例子。
[0468]
[化119]
[0469][0470]
[化120]
[0471][0472]
在以下的式(di
‑
34
‑
1)~式(di
‑
34
‑
12)中示出式(di
‑
34)所表示的化合物的例子。
[0473]
[化121]
[0474][0475]
[化122]
[0476][0477]
[化123]
[0478][0479]
[化124]
[0480][0481]
式(di
‑
34
‑
1)~式(di
‑
34
‑
12)中,r
40
各自独立地表示氢原子或碳数1~20的烷基,优选为表示氢原子或碳数1~10的烷基,而且r
41
各自独立地表示氢原子或碳数1~12的烷基。
[0482]
在以下的式(di
‑
35
‑
1)~式(di
‑
35
‑
3)中示出式(di
‑
35)所表示的化合物的例子。
[0483]
[化125]
[0484]
[0485]
式(di
‑
35
‑
1)~式(di
‑
35
‑
3)中,r
37
各自独立地表示碳数6~30的烷基,r
41
各自独立地表示氢原子或碳数1~12的烷基。
[0486]
以下示出式(di
‑
36
‑
1)~式(di
‑
36
‑
8)所表示的化合物。
[0487]
[化126]
[0488][0489]
式(di
‑
36
‑
1)~式(di
‑
36
‑
8)中,r
42
各自独立地表示碳数3~30的烷基。
[0490]
[其他二胺类的更优选的例子]
[0491]
对所述二胺类中提高后述的液晶取向膜的各特性的适宜的材料进行叙述。在重视提高形成光取向膜时的各向异性或液晶取向性的情况下,优选为使用式(di
‑1‑
3)、式(di
‑5‑
1)、式(di
‑5‑
5)、式(di
‑5‑
9)、式(di
‑5‑
12)、式(di
‑5‑
13)、式(di
‑5‑
29)、式(di
‑6‑
7)、式(di
‑7‑
3)或式(di
‑
11
‑
2)所表示的化合物。式(di
‑5‑
1)中,优选为m=2~8,更优选为m=2~4。式(di
‑5‑
12)中,优选为m=2~6,更优选为m=2~4。式(di
‑5‑
13)中,优选为m=1或2,更优选为m=1。
[0492]
在重视提高透过率的情况下,优选为使用式(di
‑1‑
3)、式(di
‑2‑
1)、式(di
‑5‑
1)、式(di
‑5‑
5)、式(di
‑5‑
24)或式(di
‑7‑
3)所表示的二胺,更优选为式(di
‑2‑
1)所表示的化合物。式(di
‑5‑
1)中,优选为m=2~8,更优选为m=8。式(di
‑7‑
3)中,优选为m=2或3且n=1或2,更优选为m=3且n=1。
[0493]
在重视提高液晶显示元件的vhr的情况下,优选为使用式(di
‑2‑
1)、式(di
‑4‑
1)、式(di
‑4‑
2)、式(di
‑4‑
10)、式(di
‑4‑
15)、式(di
‑4‑
22)、式(di
‑5‑
1)、式(di
‑5‑
28)、式(di
‑5‑
30)或式(di
‑
13
‑
1)所表示的化合物,更优选为式(di
‑2‑
1)、式(di
‑5‑
1)或式(di
‑
13
‑
1)所表示的二胺。式(di
‑5‑
1)中,优选为m=1。式(di
‑5‑
30)中,优选为k=2。
[0494]
作为防止烧痕的方法之一,有效的是通过使液晶取向膜的体积电阻值降低而使液
晶取向膜中的残留电荷(残留dc)的缓和速度提高。在重视所述目的的情况下,优选为使用式(di
‑4‑
1)、式(di
‑4‑
2)、式(di
‑4‑
10)、式(di
‑4‑
15)、式(di
‑5‑
1)、式(di
‑5‑
12)、式(di
‑5‑
13)、式(di
‑5‑
28)、式(di
‑4‑
20)、式(di
‑4‑
21)、或式(di
‑
16
‑
1)所表示的化合物,更优选为式(di
‑4‑
1)、式(di
‑5‑
1)或式(di
‑5‑
13)所表示的化合物。式(di
‑5‑
1)中,优选为m=2~8,更优选为m=4~8。式(di
‑5‑
12)中,优选为m=2~6,更优选为m=5。式(di
‑5‑
13)中,优选为m=1或2,更优选为m=1。
[0495]
[其他光反应性二胺类]
[0496]
如所述般,本发明的二胺化合物(1)显示出光反应性,因此与其并用的其他二胺类并不一定具有光反应性,但也可将显示出光反应性的二胺类与二胺化合物(1)并用。例如作为有可能发生光弗里斯重排反应的其他光反应性二胺化合物,可列举式(di
‑5‑
32)、式(di
‑5‑
33)、式(di
‑5‑
35)、式(di
‑5‑
36)、式(di
‑6‑
8)、式(di
‑6‑
9)、式(di
‑6‑
10)所表示的化合物。
[0497]
[化127]
[0498][0499]
式(di
‑5‑
35)、式(di
‑5‑
36)中,m为1~12的整数。
[0500]
[原料组合物中的通式(1)所表示的二胺化合物的调配量]
[0501]
本发明中使用的聚合物的原料组合物中,相对于用作原料的二胺类的总量,将二胺化合物(1)用于原料组合物中的聚合物的二胺化合物(1)的调配量优选为40摩尔%~100摩尔%,更优选为50摩尔%~100摩尔%。相对于用作原料的二胺类的总量,本发明中使用的聚合物为嵌段聚合物时的二胺化合物(1)的调配量优选为10摩尔%~100摩尔%,更优选为20摩尔%~70摩尔%。
[0502]
本发明中使用的聚合物的原料组合物中,二胺类的一部分可经取代为选自由单胺及单酰肼所组成的群组中的至少一种。关于取代的比例,优选为选自由单胺及单酰肼所组
成的群组中的至少一种相对于二胺类的比率为40摩尔%以下的范围。此种取代可引起生成聚酰胺酸时的聚合反应的终止,可抑制聚合反应的进一步进行。因此,通过此种取代,可容易控制所获得的聚合物(聚酰胺酸或其衍生物)的分子量,例如可不损及本发明的效果而改善液晶取向剂的涂布特性。只要不损及本发明的效果,则可经单胺或单酰肼取代的二胺类可为一种也可为两种以上。作为所述单胺,例如可列举:苯胺、4
‑
羟基苯胺、环己胺、丁胺、戊胺、己胺、庚胺、辛胺、壬胺、癸胺、十一胺、十二胺、十三胺、十四胺、十五胺、十六胺、十七胺、十八胺、二十胺、对氨基苯基三甲氧基硅烷、及3
‑
氨基丙基三乙氧基硅烷。
[0503]
本发明中使用的聚合物的原料组合物也可进而包含单异氰酸酯化合物作为单体。通过单体中包含单异氰酸酯化合物,所获得的聚酰胺酸或其衍生物的末端得到修饰,分子量得到调节。通过使用所述末端修饰型的聚酰胺酸或其衍生物,例如可不损及本发明的效果地改善液晶取向剂的涂布特性。就所述观点而言,相对于单体中的二胺及四羧酸二酐的总量,单体中的单异氰酸酯化合物的含量优选为1摩尔%~10摩尔%。作为单异氰酸酯化合物,例如可列举苯基异氰酸酯、及萘基异氰酸酯。
[0504]
本发明的聚合物可用于液晶取向膜、光学各向异性体、相位差膜、光学补偿膜、防反射膜、各种膜、或光学构件等材料。此处,在将本发明的聚合物用于液晶取向膜、光学各向异性体、相位差膜、光学补偿膜、防反射膜、各种膜、或光学构件等的情况下,这些聚合物可包括一种本发明的聚合物,也可将本发明的聚合物混合两种以上。在这些用途中,在更重视取向性的用途、例如相位差膜中,优选为包括一种本发明的聚合物。
[0505]
<液晶取向剂>
[0506]
以下,对由本发明的聚合物所得的液晶取向剂进行详细说明。
[0507]
本发明的液晶取向剂以包含本发明的聚合物为特征。关于本发明的聚合物的说明,可参照<聚合物>一栏的记载。
[0508]
本发明的液晶取向剂包含的本发明的聚合物可为一种也可为两种以上。另外,本发明的液晶取向剂包含的聚合物可仅为本发明的聚合物,也可为在本发明的聚合物中混合本发明的聚合物以外的聚合物(其他聚合物)的混合物。再者,本说明书中,有时将仅含有一种聚合物的液晶取向剂称为单层型液晶取向剂。有时将含有两种以上聚合物的液晶取向剂称为掺合型液晶取向剂。掺合型液晶取向剂特别用于重视vhr可靠性或其他电性特性的情况。
[0509]
作为掺合型液晶取向剂中使用的其他聚合物,优选为聚酰胺酸或其衍生物的任一种以上。作为其他聚合物的聚酰胺酸或其衍生物中可使用将包含通式(1)所表示的二胺化合物以外的二胺类(其他二胺类)与四羧酸二酐类的原料组合物聚合而成的聚合物。关于四羧酸二酐类及其他二胺类的说明,可参照所述<聚合物>一栏的对应的记载。
[0510]
在使用两成分的聚合物的情况下,例如有如下形态:其中一者选择在液晶取向能力方面具有优异的性能的聚合物,另一者选择对于改善液晶显示元件的电性特性而言具有优异的性能的聚合物,因获得液晶取向性与电气特性的平衡良好的液晶取向剂而适宜。
[0511]
另外,在所述情况下,通过控制各个聚合物的结构或分子量,可使其中一聚合物偏析于薄膜的上层,使另一聚合物偏析于薄膜的下层。即,通过此种聚合物的结构或分子量的控制,在对将两种聚合物溶解于溶剂而制备的液晶取向剂的涂膜进行预干燥来形成薄膜的过程中,可使液晶取向能力优异的聚合物偏析于薄膜的上层,使液晶显示元件的电性特性
改善能力优异的聚合物偏析于薄膜的下层。其中,在混合存在的聚合物中,可应用表面能量小的聚合物分离于上层,表面能量大的聚合物分离于下层的现象。此种相分离的确认可通过以下方式来确认:所形成的液晶取向膜的表面能量为与由仅含有意图偏析于上层的聚合物的液晶取向剂形成的膜的表面能量相同或与其相近的值。
[0512]
作为显现层分离的方法,可列举使偏析于上层的聚合物的分子量较偏析于下层的聚合物的分子量而言更小的方法、或者将偏析于上层的聚合物设为聚酰亚胺的方法。
[0513]
此处,通式(1)所表示的二胺化合物可用作偏析于薄膜的上层的聚合物的原料单体,也可用作偏析于薄膜的下层的聚合物的原料单体,另外还可用作两种聚合物的原料单体,但优选为用作偏析于薄膜的上层的聚合物的原料单体。
[0514]
作为偏析于薄膜的上层的聚酰胺酸或其衍生物的原料组合物中使用的四羧酸二酐,可无限制地自所述例示的现有的四羧酸二酐中选择。
[0515]
偏析于薄膜的上层的聚酰胺酸或其衍生物的原料组合物中使用的四羧酸二酐优选为式(an
‑1‑
1)、式(an
‑1‑
2)、式(an
‑2‑
1)、式(an
‑3‑
1)、式(an
‑4‑
5)、式(an
‑4‑
17)或式(an
‑4‑
21)所表示的化合物,更优选为式(an
‑4‑
17)或式(an
‑4‑
21)。式(an
‑4‑
17)中,优选为m=4~8。
[0516]
作为偏析于薄膜的上层的聚酰胺酸或其衍生物的原料组合物中使用的、且式(1)所表示的二胺化合物以外的二胺类,可无限制地自所述例示的现有的二胺类中选择。
[0517]
作为偏析于薄膜的上层的聚酰胺酸或其衍生物的原料组合物中使用的、且式(1)所表示的二胺化合物以外的二胺类,优选为使用式(di
‑4‑
1)、式(di
‑4‑
13)、式(di
‑4‑
15)、式(di
‑5‑
1)、式(di
‑7‑
3)或式(di
‑
13
‑
1)所表示的化合物。其中,更优选为使用式(di
‑4‑
13)、式(di
‑4‑
15)、式(di
‑5‑
1)或式(di
‑
13
‑
1)所表示的化合物。式(di
‑5‑
1)中,优选为m=4~8。式(di
‑7‑
3)中,优选为m=3且n=1。
[0518]
作为偏析于薄膜的下层的聚酰胺酸或其衍生物的原料组合物中使用的四羧酸二酐,可无限制地自所述例示的现有的四羧酸二酐中选择。
[0519]
作为偏析于薄膜的下层的聚酰胺酸或其衍生物的原料组合物中使用的四羧酸二酐,优选为式(an
‑1‑
1)、式(an
‑1‑
13)、式(an
‑2‑
1)、式(an
‑3‑
2)或式(an
‑4‑
21)所表示的化合物,更优选为式(an
‑1‑
1)、式(an
‑2‑
1)或式(an
‑3‑
2)所表示的化合物。
[0520]
偏析于薄膜的下层的聚酰胺酸或其衍生物的原料组合物中使用的四羧酸二酐优选为在四羧酸二酐的总量中包含10摩尔%以上的芳香族四羧酸二酐,更优选为包含30摩尔%以上。
[0521]
作为偏析于薄膜的下层的聚酰胺酸或其衍生物的原料组合物中使用的、且式(1)所表示的二胺化合物以外的二胺类,可无限制地自所述例示的现有的二胺类中选择。
[0522]
作为偏析于薄膜的下层的聚酰胺酸或其衍生物的原料组合物中使用的、且式(1)所表示的二胺化合物以外的二胺类,优选为式(di
‑4‑
1)、式(di
‑4‑
2)、式(di
‑4‑
10)、式(di
‑4‑
18)、式(di
‑4‑
19)、式(di
‑5‑
1)、式(di
‑5‑
9)、式(di
‑5‑
28)、式(di
‑5‑
30)、式(di
‑
13
‑
1)或式(dih
‑1‑
2)所表示的化合物。式(di
‑5‑
1)中,优选为m=1或2的化合物,式(di
‑5‑
30)中,优选为k=2的化合物。其中,更优选为式(di
‑4‑
1)、式(di
‑4‑
18)、式(di
‑4‑
19)、式(di
‑5‑
9)、式(di
‑
13
‑
1)或式(dih
‑1‑
2)所表示的化合物。
[0523]
相对于所有二胺类,偏析于薄膜的下层的聚酰胺酸或其衍生物的原料组合物中使
用的二胺类优选为包含30摩尔%以上的选自由芳香族二胺及芳香族二酰肼所组成的群组中的至少一种,更优选为包含50摩尔%以上。
[0524]
偏析于薄膜的上层的聚酰胺酸或其衍生物相对于偏析于薄膜的上层的聚酰胺酸或其衍生物与偏析于薄膜的下层的聚酰胺酸或其衍生物的合计量的比例优选为5重量%~50重量%,进而优选为10重量%~40重量%。
[0525]
另外,就液晶取向剂的涂布性、或聚酰胺酸或其衍生物的浓度的调整的观点而言,本发明的液晶取向剂也可进而含有溶剂。溶剂只要为具有溶解高分子成分的能力的溶剂,则可无特别限制地使用,例如可根据使用目的而自聚酰胺酸、可溶性聚酰亚胺等聚合物成分的制造工序或各用途中通常所使用的溶剂、聚酰胺酸或其衍生物的亲溶剂、以改善涂布性为目的的其他溶剂中适宜选择。溶剂可为一种也可为两种以上的混合溶剂。
[0526]
作为相对于聚酰胺酸或其衍生物而为亲溶剂的非质子性极性有机溶剂,可列举:n
‑
甲基
‑2‑
吡咯烷酮、n
‑
乙基
‑2‑
吡咯烷酮、二甲基咪唑烷酮、n
‑
甲基己内酰胺、n
‑
甲基丙酰胺、n,n
‑
二甲基乙酰胺、二甲基亚砜、n,n
‑
二甲基甲酰胺、n,n
‑
二乙基甲酰胺、二乙基乙酰胺、n,n
‑
二甲基异丁基酰胺、γ
‑
丁内酯、γ
‑
戊内酯等。这些溶剂中,优选为n
‑
甲基
‑2‑
吡咯烷酮、二甲基咪唑烷酮、γ
‑
丁内酯或γ
‑
戊内酯。
[0527]
作为以改善涂布性等为目的的其他溶剂的例子,可列举:乙二醇单丁醚、乙二醇单叔丁基醚等乙二醇单烷基醚、二乙二醇单乙醚等二乙二醇单烷基醚、二乙二醇乙基甲基醚、二乙二醇二乙醚、二乙二醇丁基甲基醚等二乙二醇二烷基醚。另外,可列举:丙二醇单甲醚、1
‑
丁氧基
‑2‑
丙醇等丙二醇单烷基醚、二丙二醇单甲醚等二丙二醇单烷基醚、三乙二醇单烷基醚、苯基乙酸酯、及这些乙酸酯类等酯化合物。进而,可列举:丙二酸二乙酯等丙二酸二烷基酯、乳酸烷基酯、二异丁基酮、二丙酮醇、3
‑
甲基
‑3‑
甲氧基丁基醇、4
‑
甲基
‑2‑
戊醇、2,6
‑
二甲基
‑4‑
庚醇、四氢萘、及异佛尔酮。
[0528]
这些溶剂中,优选为二异丁基酮、4
‑
甲基
‑2‑
戊醇、2,6
‑
二甲基
‑4‑
庚醇、乙二醇单丁醚、乙二醇单叔丁基醚、二乙二醇单乙醚、二乙二醇乙基甲基醚、二乙二醇二乙醚、二乙二醇丁基甲基醚、1
‑
丁氧基
‑2‑
丙醇、丙二醇单甲醚、二丙二醇单甲醚或丁基溶纤剂乙酸酯。
[0529]
本发明的液晶取向剂中的聚合物浓度并无特别限定,只要结合下述各种涂布法来选择最合适的值即可。通常,为了抑制涂布时的不均或针孔等,相对于液晶取向剂重量,优选为0.1重量%~30重量%,更优选为1重量%~10重量%。
[0530]
本发明的液晶取向剂的粘度根据涂布的方法、聚酰胺酸或其衍生物的浓度、所使用的聚酰胺酸或其衍生物的种类、溶剂的种类与比例而优选的范围不同。例如,在利用印刷机进行涂布的情况下为5mpa
·
s~100mpa
·
s(更优选为10mpa
·
s~80mpa
·
s)。若为5mpa
·
s以上,则容易获得充分的膜厚,若为100mpa
·
s以下,则容易抑制印刷不均。在利用旋涂进行涂布的情况下,适合的是5mpa
·
s~200mpa
·
s(更优选为10mpa
·
s~100mpa
·
s)。在使用喷墨涂布装置来进行涂布的情况下,适合的是5mpa
·
s~50mpa
·
s(更优选为5mpa
·
s~20mpa
·
s)。液晶取向剂的粘度可通过旋转粘度测定法来测定,例如使用旋转粘度计(东机产业制造的tve
‑
20l型)来测定(测定温度:25℃)。
[0531]
本发明的液晶取向剂可仅包括聚合物成分,也可进而含有各种添加剂。为了提高取向膜的各种特性,各种添加剂可根据各自的目的来选择使用。以下示出可用于液晶取向剂中的添加剂的例子。
[0532]
(烯基取代纳迪克酰亚胺化合物)
[0533]
例如,就使液晶显示元件的电气特性长期稳定的目的而言,本发明的液晶取向剂也可进而含有烯基取代纳迪克酰亚胺化合物。烯基取代纳迪克酰亚胺化合物可使用一种,也可并用两种以上。就所述目的而言,相对于聚酰胺酸或其衍生物,烯基取代纳迪克酰亚胺化合物的含量优选为1重量%~50重量%,更优选为1重量%~30重量%,进而优选为1重量%~20重量%。烯基取代纳迪克酰亚胺化合物优选为可溶解于溶解本发明中所使用的聚酰胺酸或其衍生物的溶剂中的化合物。优选的烯基取代纳迪克酰亚胺化合物可列举日本专利特开2008
‑
096979号公报、日本专利特开2009
‑
109987号公报、日本专利特开2013
‑
242526号公报中所公开的烯基取代纳迪克酰亚胺化合物。作为特别优选的烯基取代纳迪克酰亚胺化合物,可列举:双{4
‑
(烯丙基双环[2.2.1]庚
‑5‑
烯
‑
2,3
‑
二羧基酰亚胺)苯基}甲烷、n,n'
‑
间苯二甲基
‑
双(烯丙基双环[2.2.1]庚
‑5‑
烯
‑
2,3
‑
二羧基酰亚胺)或n,n'
‑
六亚甲基
‑
双(烯丙基双环[2.2.1]庚
‑5‑
烯
‑
2,3
‑
二羧基酰亚胺)。
[0534]
(具有自由基聚合性不饱和双键的化合物)
[0535]
例如,就使液晶显示元件的电气特性长期稳定的目的而言,本发明的液晶取向剂也可进而含有具有自由基聚合性不饱和双键的化合物。具有自由基聚合性不饱和双键的化合物可为一种化合物,也可为两种以上的化合物。再者,在具有自由基聚合性不饱和双键的化合物中不包含烯基取代纳迪克酰亚胺化合物。关于具有自由基聚合性不饱和双键的化合物中,作为优选的化合物,可列举:n,n'
‑
亚甲基双丙烯酰胺、n,n'
‑
二羟基亚乙基
‑
双丙烯酰胺、亚乙基双丙烯酸酯、4,4'
‑
亚甲基双(n,n
‑
二羟基亚乙基丙烯酸酯苯胺)、氰脲酸三烯丙酯、以及日本专利特开2009
‑
109987号公报、日本专利特开2013
‑
242526号公报、国际公开第2014/119682号、国际公开第2015/152014号中所公开的具有自由基聚合性不饱和双键的化合物。就所述目的而言,相对于聚酰胺酸或其衍生物,具有自由基聚合性不饱和双键的化合物的含量优选为1重量%~50重量%,更优选为1重量%~30重量%。
[0536]
(噁嗪化合物)
[0537]
例如,就使液晶显示元件的电气特性长期稳定的目的而言,本发明的液晶取向剂也可进而含有噁嗪化合物。噁嗪化合物可为一种化合物,也可为两种以上的化合物。就所述目的而言,相对于聚酰胺酸或其衍生物,噁嗪化合物的含量优选为0.1重量%~50重量%,更优选为1重量%~40重量%,进而优选为1重量%~20重量%。
[0538]
噁嗪化合物优选为可溶于使聚酰胺酸或其衍生物溶解的溶剂中且具有开环聚合性的噁嗪化合物。关于优选的噁嗪化合物,可列举式(ox
‑3‑
1)、式(ox
‑3‑
9)、式(ox
‑3‑
10)所表示的噁嗪化合物、以及日本专利特开2007
‑
286597号公报、日本专利特开2013
‑
242526号公报中所公开的噁嗪化合物。
[0539]
[化128]
[0540][0541]
(噁唑啉化合物)
[0542]
例如,就使液晶显示元件的电气特性长期稳定的目的而言,本发明的液晶取向剂也可进而含有噁唑啉化合物。噁唑啉化合物为具有噁唑啉结构的化合物。噁唑啉化合物可为一种化合物,也可为两种以上的化合物。就所述目的而言,相对于聚酰胺酸或其衍生物,噁唑啉化合物的含量优选为0.1重量%~50重量%,更优选为1重量%~40重量%,进而优选为1重量%~20重量%。优选的噁唑啉化合物可列举日本专利特开2010
‑
054872号公报、日本专利特开2013
‑
242526号公报中所公开的噁唑啉化合物。更优选为可列举1,3
‑
双(4,5
‑
二氢
‑2‑
噁唑基)苯。
[0543]
(环氧化合物)
[0544]
例如,就使液晶显示元件的电气特性长期稳定的目的、提高膜的硬度的目的、或提高与密封剂的密接性的目的而言,本发明的液晶取向剂也可进而含有环氧化合物。环氧化合物可为一种化合物,也可为两种以上的化合物。就所述目的而言,相对于聚酰胺酸或其衍生物,环氧化合物的含量优选为0.1重量%~50重量%,更优选为1重量%~20重量%,进而优选为1重量%~10重量%。
[0545]
作为环氧化合物,可使用在分子内具有一个或两个以上环氧环的各种化合物。
[0546]
为了提高膜的硬度的目的、或提高与密封剂的密接性的目的,优选为在分子内具有两个以上的环氧环的化合物,更优选为在分子内具有三个或四个环氧环的化合物。
[0547]
作为环氧化合物,可列举日本专利特开2009
‑
175715号公报、日本专利特开2013
‑
242526号公报、日本专利特开2016
‑
170409号公报、国际公开第2017/217413号中所公开的环氧化合物等。作为优选的环氧化合物,可列举:n,n,n',n'
‑
四缩水甘油基
‑
4,4'
‑
二氨基二苯基甲烷、3
‑
缩水甘油氧基丙基三甲氧基硅烷、2
‑
(3,4
‑
环氧环己基)乙基三甲氧基硅烷、2
‑
(3,4
‑
环氧环己基)乙基三乙氧基硅烷、(3,3',4,4'
‑
二环氧基)双环己基、1,1'
‑
双
‑7‑
氧杂双环[4.1.0]庚烷、1,4
‑
丁二醇缩水甘油醚、异氰脲酸三(2,3
‑
环氧丙基)酯、1,3
‑
双(n,n
‑
二缩水甘油基氨基甲基)环己烷或n,n,n',n'
‑
四缩水甘油基
‑
间二甲苯二胺。
[0548]
除所述以外,也可添加具有环氧环的寡聚物或聚合体。具有环氧环的寡聚物或聚合体可使用日本专利特开2013
‑
242526号公报中所公开的寡聚物或聚合体。
[0549]
(硅烷化合物)
[0550]
例如,就提高与基板及密封剂的密接性的目的而言,本发明的液晶取向剂也可进而含有硅烷化合物。就所述目的而言,相对于聚酰胺酸或其衍生物,硅烷化合物的含量优选为0.1重量%~30重量%,更优选为0.5重量%~20重量%,进而优选为0.5重量%~10重
量%。
[0551]
作为硅烷偶合剂,可使用日本专利特开2013
‑
242526号公报、日本专利特开2015
‑
212807号公报、日本专利特开2018
‑
173545号公报、国际公开第2018/181566号中所公开的硅烷偶合剂。
[0552]
作为优选的硅烷偶合剂,可列举:3
‑
缩水甘油氧基丙基三甲氧基硅烷、3
‑
缩水甘油氧基丙基三乙氧基硅烷、2
‑
(3,4
‑
环氧环己基)乙基三甲氧基硅烷、对氨基苯基三甲氧基硅烷、3
‑
氨基丙基三乙氧基硅烷、3
‑
缩水甘油氧基丙基甲基二乙氧基硅烷、3
‑
异氰酸酯基丙基三乙氧基硅烷或3
‑
脲基丙基三乙氧基硅烷。
[0553]
除所述记载的添加剂以外,就提高取向膜的强度的目的、或使液晶显示元件的电气特性长期稳定的目的而言,也可添加具有环碳酸酯基的化合物、具有羟基烷基酰胺部位或羟基的化合物。作为具体的化合物,可列举日本专利特开2016
‑
118753号公报、国际公开第2017/110976号中所公开的化合物。作为优选的化合物,可列举以下的式(hd
‑
1)~式(hd
‑
4)。相对于聚酰胺酸或其衍生物,这些化合物优选为0.5重量%~50重量%,更优选为1重量%~30重量%,进而优选为1重量%~10重量%。
[0554]
[化129]
[0555][0556]
另外,在需要提高抗静电时,也可使用抗静电剂,当在低温下进行酰亚胺化的情况下,也可使用酰亚胺化催化剂。作为酰亚胺化催化剂,可列举日本专利特开2013
‑
242526号公报中所公开的酰亚胺化催化剂。
[0557]
<液晶取向膜>
[0558]
其次,对本发明的液晶取向膜进行说明。
[0559]
本发明的液晶取向膜是使用本发明的液晶取向剂而形成。关于本发明的液晶取向剂的说明,可参照所述<液晶取向剂>一栏的记载。
[0560]
在本发明的液晶取向剂包含聚酰胺酸的情况下,在形成液晶取向膜的过程中对所述液晶取向剂的涂膜进行加热煅烧时,聚酰胺酸可引起酰亚胺化反应而形成聚酰亚胺系液晶取向膜。本发明的液晶取向剂适合于光取向用的液晶取向剂,在形成液晶取向膜的过程中的取向处理中,可适用光取向法。
[0561]
<液晶取向膜的制造方法>
[0562]
以下,对本发明的液晶取向膜的制造方法进行说明。
[0563]
本发明的液晶取向膜可通过由光取向用液晶取向剂制作液晶取向膜的通常的方法而获得。具体而言,本发明的液晶取向膜可使用如下工序来形成,即:将本发明的液晶取向剂涂布于基板而形成涂膜的工序、以及对所述涂膜照射光的工序。进而本发明的液晶取向膜优选为例如通过经过如下工序来制造,即:将本发明的液晶取向剂涂布于基板而形成涂膜的工序、对涂膜进行加热干燥而形成液晶取向剂的膜的工序、对液晶取向剂的膜照射光而赋予各向异性的工序、以及对赋予了各向异性的液晶取向剂的膜进行加热煅烧的工序。即,针对本发明的液晶取向膜,优选为在涂膜工序、加热干燥工序后照射光来赋予各向异性,之后经过加热煅烧工序。另外,为了赋予各向异性而照射的光优选为偏光紫外线。
[0564]
涂膜可与通常的液晶取向膜的制作同样地,通过将本发明的液晶取向剂涂布于液晶显示元件中的基板上来形成。基板可列举可设置有氧化铟锡(indium tin oxide,ito)、氧化铟锌(in2o3‑
zno,izo)、氧化铟镓锌(in
‑
ga
‑
zno4,igzo)电极等电极或彩色滤光片等的玻璃制、氮化硅制、丙烯酸制、聚碳酸酯制、聚酰亚胺制等的基板。
[0565]
作为将液晶取向剂涂布于基板上的方法,一般已知有旋转器法、印刷法、浸渍法、滴加法、喷墨法等。这些方法也可同样地适用于本发明中。
[0566]
加热干燥工序一般已知有在烘箱或红外炉中进行加热处理的方法、在热板上进行加热处理的方法等。加热干燥工序优选为在溶剂可蒸发的范围内的温度下实施,更优选为在相对于加热煅烧工序中的温度为比较低的温度下实施。具体而言,加热干燥温度优选为30℃~150℃的范围,进而优选为50℃~120℃的范围。
[0567]
加热煅烧工序可在聚酰胺酸或其衍生物呈现酰亚胺化反应所需的条件下进行。涂膜的煅烧一般已知有在烘箱或红外炉中进行加热处理的方法、在热板上进行加热处理的方法等。这些方法也可同样地适用于本发明中。一般优选为在90℃~300℃左右的温度下进行1分钟~3小时,更优选为120℃~280℃,进而优选为150℃~250℃。
[0568]
在重视提高膜的各向异性、或提高制作液晶显示元件时的残像特性的情况下,优选为缓慢地进行加热工序的升温,例如可一面阶段性地提高温度,一面在不同的温度下进行多次加热煅烧,或者使温度自低温变化为高温来进行加热。另外,也可组合两种加热方法来进行。
[0569]
当在不同的温度下进行多次加热煅烧的情况下,可使用设定为不同的温度的多个加热装置,也可使用一台加热装置,一面依次变化为不同的温度一面进行加热煅烧。
[0570]
当在不同的温度下进行多次加热煅烧的情况下,优选为在初次的煅烧温度为90℃~180℃下进行,优选为在最后的温度为185℃~300℃下进行。例如,优选为在110℃下加热煅烧后在220℃下加热煅烧,在110℃下加热煅烧后在230℃下加热煅烧,在130℃下加热煅烧后在220℃下加热煅烧,在150℃下加热煅烧后在200℃下加热煅烧,在150℃下加热煅烧后在220℃下加热煅烧,在150℃下加热煅烧后在230℃下加热煅烧,或者在170℃下加热煅烧后在200℃下加热煅烧。进而,也优选为一面增加阶段并缓慢地升温,一面进行加热煅烧。在改变加热温度而以两阶段以上进行加热煅烧的情况下,各加热工序中的加热时间优选为5分钟~30分钟。
[0571]
在使温度自低温度变化为高温来进行煅烧的情况下,初始温度优选为90℃~180℃。最终温度优选为185℃~300℃,更优选为190℃~230℃。加热时间优选为5分钟~60分
钟,更优选为20分钟~60分钟。升温速度例如可设为0.5℃/min~40℃/min。升温中的升温速度也可不固定。
[0572]
本发明的液晶取向膜的形成方法中,为了使液晶相对于水平方向和/或垂直方向在一方向上进行取向,可适宜地使用现有的光取向法作为对薄膜赋予各向异性的方法。
[0573]
对利用光取向法的本发明的液晶取向膜的形成方法进行详细说明。使用光取向法的本发明的液晶取向膜可通过以下方式而形成:通过向对涂膜进行加热干燥后的薄膜照射光的直线偏光或无偏光,而对薄膜赋予各向异性,并对所述膜进行加热煅烧。或者,可通过对涂膜进行加热干燥,并进行加热煅烧,然后对薄膜照射光的直线偏光或无偏光而形成。就液晶取向性的方面而言,光的照射工序优选为在加热煅烧工序前进行。
[0574]
进而,为了提高液晶取向膜的液晶取向能力,也可一面对涂膜进行加热一面照射光的直线偏光或无偏光。光的照射可在对涂膜进行加热干燥的工序、或进行加热煅烧的工序中进行,也可在加热干燥工序与加热煅烧工序之间进行。
[0575]
在对涂膜进行加热干燥的工序、或进行加热煅烧的工序中照射光时的加热温度可参考所述加热干燥工序、或加热煅烧工序的记载。在加热干燥工序与加热煅烧工序之间照射光时的加热温度优选为30℃~150℃的范围,进而优选为50℃~110℃的范围。
[0576]
作为光,例如可使用包含150nm~800nm的波长的光的紫外线或可见光,优选为包含200nm~400nm的光的紫外线。另外,可使用直线偏光或无偏光。这些光只要为可对所述薄膜赋予液晶取向能力的光,则并无特别限定,在欲对液晶显现强的取向限制力的情况下,优选为直线偏光。
[0577]
本发明的液晶取向膜即便在低能量的光照射下也可显示出高的各向异性。所述光照射工序中的直线偏光的照射量优选为0.05j/cm2~10j/cm2,更优选为0.1j/cm2~5j/cm2。直线偏光对膜表面的照射角度并无特别限定,在欲显现对于液晶的强取向限制力的情况下,就取向处理时间缩短的观点而言,优选为相对于膜表面尽量垂直。另外,本发明的液晶取向膜通过照射直线偏光,可在相对于直线偏光的偏光方向而呈直角的方向上使液晶取向。
[0578]
在照射光的直线偏光或无偏光的工序中使用的光源中,可无限制地使用超高压水银灯、高压水银灯、低压水银灯、深紫外线(deep uv)灯、卤素灯、金属卤化物灯、大功率金属卤化物灯、氙灯、水银氙灯、准分子灯、krf准分子激光、荧光灯、发光二极管(light emitting diode,led)灯、钠灯、微波激发无极灯(microwave discharged electrodeless lamp)等。
[0579]
本发明的液晶取向膜可通过进而包括所述工序以外的其他工序的方法而适宜地获得。
[0580]
本发明的液晶取向膜虽然不将利用清洗液对煅烧或光照射后的膜进行清洗的工序设为必需,但可根据其他工序的情况而设置清洗工序。作为利用清洗液的清洗方法,可列举:刷洗(brushing)、喷雾(jet spray)、蒸气清洗或超声波清洗等。这些方法可单独进行,也可并用。作为清洗液,可使用:纯水、或甲醇、乙醇、异丙醇等醇、苯、甲苯、二甲苯等芳香族烃、二氯甲烷等卤化烃、丙酮、甲基乙基酮等酮,但并不限定于这些。当然,这些清洗液可使用经充分纯化的杂质少的清洗液。此种清洗方法也可适用于本发明的液晶取向膜的形成中的所述清洗工序中。
[0581]
为了提高本发明的液晶取向膜的液晶取向能力,可在加热煅烧工序的前后或者偏光或无偏光的光照射的前后使用利用热或光的退火处理。所述退火处理中,退火温度为30℃~180℃,优选为50℃~150℃,时间优选为1分钟~2小时。另外,退火处理中使用的退火光可列举uv灯、荧光灯、led灯等。光的照射量优选为0.3j/cm2~10j/cm2。
[0582]
本发明的液晶取向膜的膜厚并无特别限定,但优选为10nm~300nm,更优选为30nm~150nm。本发明的液晶取向膜的膜厚可通过轮廓仪或椭偏计(ellipsometer)等现有的膜厚测定装置来测定。
[0583]
本发明的液晶取向膜以具有特别大的取向的各向异性为特征。此种各向异性的大小可通过日本专利特开2005
‑
275364号公报等中记载的使用偏光ir的方法来评价。另外,也可通过使用椭偏测量术(ellipsometry)的方法来评价。详细而言,可通过分光椭偏计来测定液晶取向膜的延迟值。膜的延迟值与聚合物主链的取向度成比例地增大。即,认为具有大的延迟值的聚合物的膜具有大的取向度,在用作液晶取向膜的情况下,具有更大的各向异性的液晶取向膜相对于液晶组合物而具有更大的取向限制力。
[0584]
本发明的液晶取向膜可用于智能手机、输入板、车载监视器、电视等液晶显示器用的液晶组合物的取向控制。除液晶显示器用的液晶组合物的取向用途以外,还可用于光学补偿材料或使用液晶的微波/毫米波带的宽频可变移相器等的其他所有液晶材料的取向控制。另外,本发明的液晶取向膜具有大的各向异性,因此可单独用于光学补偿材料用途。
[0585]
<液晶显示元件>
[0586]
其次,对本发明的液晶显示元件进行说明。
[0587]
本发明的液晶显示元件的特征在于具有本发明的液晶取向膜的方面,因其对比度的高度而可实现高显示品质。
[0588]
对本发明的液晶显示元件进行详细说明。本发明中,在如下液晶显示元件中,液晶取向膜包含本发明的液晶取向膜,所述液晶显示元件包括相向配置的一对基板、形成于所述一对基板各自的相向面的其中一者或两者上的电极、形成于所述一对基板各自的相向面上的所述液晶取向膜、形成于所述一对基板间的液晶层、以夹持所述相向基板的方式设置的一对偏光膜、背光及驱动装置。
[0589]
电极只要为形成于基板的一面上的电极,则并无特别限定。此种电极例如可列举ito或金属的蒸镀膜等。另外,电极可形成于基板的其中一面的整个面上,也可呈例如经图案化的所期望的形状形成。电极的所述所期望的形状例如可列举梳型或锯齿结构等。电极可形成于一对基板中的其中一基板上,也可形成于两基板上。电极的形成形态根据液晶显示元件的种类而不同,例如在ips型液晶显示元件(横向电场型液晶显示元件)的情况下,将电极配置于所述一对基板的其中一者上,在其他液晶显示元件的情况下,将电极配置于所述一对基板两者上。在所述基板或电极上形成所述液晶取向膜。
[0590]
在平行取向的液晶显示元件(例如ips、ffs等)的情况下,作为结构,自背光侧起至少具有背光、第一偏光膜、第一基板、第一液晶取向膜、液晶层、第二基板、第二偏光膜,所述偏光膜的偏光轴是以第一偏光膜的偏光轴(偏光吸收的方向)与第二偏光膜的偏光轴交差(优选为正交)的方式设置。此时,可以第一偏光膜的偏光轴与液晶取向方向平行的方式、或正交的方式设置。将以第一偏光膜的偏光轴与液晶取向方向平行的方式设置的液晶显示元件称为o
‑
模式,将以正交的方式设置的液晶显示元件称为e
‑
模式。本发明的液晶取向膜也
可适用于o
‑
模式、e
‑
模式的任一者中,可根据目的而选择。
[0591]
当使为了对液晶取向剂附加各向异性而照射的偏光的偏光轴与源自配置于背光侧的偏光膜的偏光的偏光轴平行且一致(在使用本发明的液晶取向剂的情况下,设为o
‑
模式的配置)时,液晶取向膜的光吸收波长区域的透过率上升。因此,可进一步改善液晶显示元件的透过率。
[0592]
所述液晶层是以利用形成有液晶取向膜的面相向的所述一对基板来夹持液晶组合物的形式形成。在液晶层的形成中,视需要可使用微粒子或树脂片等介隔存在于所述一对基板之间并形成适当的间隔的间隔物。
[0593]
作为液晶层的形成方法,已知有真空注入法与液晶滴注(one drop fill,odf)法。
[0594]
真空注入法中,以液晶取向膜面相向的方式设置空隙(单元间隙),且留下液晶的注入口而印刷密封剂并粘合基板。在由基板表面及密封剂划分的单元间隙内利用真空差压来注入填充液晶,然后封闭注入口,从而制造液晶显示元件。
[0595]
odf法中,在一对基板中的其中一者的液晶取向膜面的外周印刷密封剂并在密封剂的内侧的区域滴加液晶,然后以液晶取向膜面相向的方式粘合另一基板。然后,将液晶按压扩展于基板的整个面上,继而对基板的整个面照射紫外光而使密封剂硬化,从而制造液晶显示元件。
[0596]
关于基板的粘合中所使用的密封剂,除uv硬化型以外也已知有热硬化型。密封剂的印刷例如可通过网版印刷法来进行。
[0597]
液晶组合物并无特别限制,可使用介电常数各向异性为正或负的各种液晶组合物。介电常数各向异性为正的优选的液晶组合物(正型液晶组合物)可列举:日本专利第3086228号公报、日本专利第2635435号公报、日本专利特表平5
‑
501735号公报、日本专利特开平8
‑
157826号公报、日本专利特开平8
‑
231960号公报、日本专利特开平9
‑
241644号公报(欧洲专利申请公开第885272号说明书)、日本专利特开平9
‑
302346号公报(欧洲专利申请公开第806466号说明书)、日本专利特开平8
‑
199168号公报(欧洲专利申请公开第722998号公报)、日本专利特开平9
‑
235552号公报、日本专利特开平9
‑
255956号公报、日本专利特开平9
‑
241643号公报(欧洲专利申请公开第885271号公报)、日本专利特开平10
‑
204016号公报(欧洲专利申请公开第844229号公报)、日本专利特开平10
‑
204436号公报、日本专利特开平10
‑
231482号公报、日本专利特开2000
‑
087040号公报、日本专利特开2001
‑
48822号公报等中所公开的液晶组合物。
[0598]
作为所述具有负的介电常数各向异性的液晶组合物(负型液晶组合物)的优选的例子,可列举:日本专利特开昭57
‑
114532号公报、日本专利特开平2
‑
4725号公报、日本专利特开平4
‑
224885号公报、日本专利特开平8
‑
40953号公报、日本专利特开平8
‑
104869号公报、日本专利特开平10
‑
168076号公报、日本专利特开平10
‑
168453号公报、日本专利特开平10
‑
236989号公报、日本专利特开平10
‑
236990号公报、日本专利特开平10
‑
236992号公报、日本专利特开平10
‑
236993号公报、日本专利特开平10
‑
236994号公报、日本专利特开平10
‑
237000号公报、日本专利特开平10
‑
237004号公报、日本专利特开平10
‑
237024号公报、日本专利特开平10
‑
237035号公报、日本专利特开平10
‑
237075号公报、日本专利特开平10
‑
237076号公报、日本专利特开平10
‑
237448号公报(欧洲专利申请公开第967261号公报)、日本专利特开平10
‑
287874号公报、日本专利特开平10
‑
287875号公报、日本专利特开平10
‑
291945号公报、日本专利特开平11
‑
029581号公报、日本专利特开平11
‑
080049号公报、日本专利特开2000
‑
256307号公报、日本专利特开2001
‑
019965号公报、日本专利特开2001
‑
072626号公报、日本专利特开2001
‑
192657号公报、日本专利特开2010
‑
037428号公报、国际公开第2011/024666号、国际公开第2010/072370号、日本专利特表2010
‑
537010号公报、日本专利特开2012
‑
077201号公报、日本专利特开2009
‑
084362号公报等中所公开的液晶组合物。
[0599]
即便在介电常数各向异性为正或负的液晶组合物中添加一种以上的光学活性化合物来使用,也无任何影响。
[0600]
另外,例如就提高取向性的观点而言,例如本发明的液晶显示元件中使用的液晶组合物也可进而添加添加物。此种添加物为光聚合性单体、光学活性化合物、抗氧化剂、紫外线吸收剂、色素、消泡剂、聚合引发剂、聚合抑制剂等。优选的光聚合性单体、光学活性化合物、抗氧化剂、紫外线吸收剂、色素、消泡剂、聚合引发剂、聚合抑制剂可列举国际公开第2015/146330号等中所公开的化合物。
[0601]
为了适合于聚合物稳定取向(polymer sustained alignment,psa)模式的液晶显示元件,可在液晶组合物中混合可聚合的化合物。可聚合的化合物的优选的例子为丙烯酸酯、甲基丙烯酸酯、乙烯基化合物、乙烯基氧基化合物、丙烯基醚、环氧化合物(氧杂环丙烷、氧杂环丁烷)、乙烯基酮等具有可聚合的基的化合物。优选的化合物可列举国际公开第2015/146330号等中所公开的化合物。
[0602]
<二硝基化合物>
[0603]
其次,对本发明的二硝基化合物进行说明。
[0604]
本发明的二硝基化合物为下述通式(2)所表示的化合物。
[0605]
[化130]
[0606][0607]
通式(2)中,r1及r2各自独立地表示氢原子、卤素原子、碳数1至6的烷基、碳数1至6的卤代烷基或碳数1至6的烷氧基。r1与r2可相互相同也可不同。另外,r1与r2可成为一体而形成可经取代的亚甲基。关于取代基的说明与优选的范围、具体例,可参照关于可对通式(1)的亚甲基进行取代的取代基的说明与优选的范围、具体例。x各自独立地表示卤素原子、碳数1至6的烷基、碳数1至6的卤代烷基或碳数1至6的烷氧基,n表示0至4的整数。当两个n的合计为2以上时,多个x可相互相同也可不同。x及硝基(
‑
no2)的键结位置分别为其结合键所键结的苯环的能够进行取代的位置的任一处。
[0608]
通式(2)所表示的二硝基化合物(二硝基化合物(2))可通过其还原容易地变换为通式(1)所表示的二胺化合物(二胺化合物(1))。因此,二硝基化合物(2)有效用作二胺化合物(1)的合成中间体。关于将二硝基化合物(2)作为合成中间体来制造二胺化合物(1)的方法,可参照下述<二胺化合物的制造方法>一栏的记载。
[0609]
作为二硝基化合物(2)的优选的例子,可列举通式(2
‑
1)所表示的二硝基化合物,作为更优选的例子,可列举通式(2
‑
2)所表示的二硝基化合物。另外,二硝基化合物(2)、二硝基化合物(2
‑
1)、二硝基化合物(2
‑
2)中,优选为环丙烷环上的两个酯为反式构型。
[0610]
[化131]
[0611][0612]
通式(2
‑
1)的x及n、以及通式(2
‑
1)及通式(2
‑
2)的r1及r2分别与通式(2)的r1、r2、x及n为相同含义。通式(2
‑
1)中,x的键结位置为其结合键所键结的苯环的能够进行取代的位置的任一处。
[0613]
关于二硝基化合物(2)的优选的范围与具体例,可参照所述<二胺化合物>一栏中的二胺化合物(1)的优选的范围与具体例并将两个氨基置换为硝基。
[0614]
<保护二氨基化合物>
[0615]
其次,对本发明的保护二氨基化合物进行说明。
[0616]
本发明的保护二氨基化合物为下述通式(7
‑
1)所表示的化合物。
[0617]
[化132]
[0618][0619]
通式(7
‑
1)中,r1及r2各自独立地表示氢原子、卤素原子、碳数1至6的烷基、碳数1至6的卤代烷基或碳数1至6的烷氧基。r1与r2可相互相同也可不同。另外,r1与r2可成为一体而形成可经取代的亚甲基。关于取代基的说明与优选的范围、具体例,可参照关于可对通式(1)的亚甲基进行取代的取代基的说明与优选的范围、具体例。x各自独立地表示卤素原子、碳数1至6的烷基、碳数1至6的卤代烷基或碳数1至6的烷氧基,n表示0至4的整数。当两个n的合计为2以上时,多个x可相互相同也可不同。x的键结位置为其结合键所键结的苯环的能够进行取代的位置的任一处。boc表示叔丁氧基羰基。
[0620]
通式(7
‑
1)所表示的保护二氨基化合物(保护二氨基化合物(7
‑
1))可通过对经boc
基保护的氨基进行脱保护,容易地变换为通式(1
‑
1)所表示的二胺化合物(二胺化合物(1
‑
1))。因此,保护二氨基化合物(7
‑
1)有效用作二胺化合物(1
‑
1)的合成中间体。关于将保护二氨基化合物(7
‑
1)作为合成中间体来制造二胺化合物(1
‑
1)的方法,可参照下述<二胺化合物的制造方法>一栏的记载。
[0621]
保护二氨基化合物(7
‑
1)中,优选为环丙烷环上的两个酯为反式构型。
[0622]
关于保护二氨基化合物(7
‑
1)的优选的范围与具体例,可参照所述<二胺化合物>一栏中的二胺化合物(1)的优选的范围与具体例并将两个氨基置换为经boc基保护的氨基。
[0623]
<二胺化合物的制造方法>
[0624]
其次对本发明的二胺化合物的制造方法进行说明。
[0625]
[经由二硝基化合物(2)的二胺化合物的制造方法]
[0626]
如下述反应流程所示,本发明的通式(1)所表示的二胺化合物(二胺化合物(1))可通过将通式(2)所表示的二硝基化合物(二硝基化合物(2))的硝基还原来制造。关于二硝基化合物(2)的说明与优选的范围,可参照所述<二硝基化合物>一栏的记载。
[0627]
[化133]
[0628][0629]
式中,r1、r2、x及n分别与所述通式(1)及通式(2)的r1、r2、x及n为相同含义。
[0630]
此处,二硝基化合物(2)可通过使通式(3)所表示的环丙烷衍生物与通式(4)所表示的硝基化合物发生缩合反应来制造。
[0631]
[化134]
[0632][0633]
通式(3)中,r1及r2分别与通式(2)的r1及r2为相同含义。y表示脱离基。
[0634]
[化135]
[0635][0636]
通式(4)中,x及n分别与通式(2)的x及n为相同含义。当n为2以上时,多个x可相互相同也可不同。
[0637]
作为本发明的二胺化合物的制造方法的优选的例子,可列举如下方法:如下述反应流程所示,通过以下工序来合成二胺化合物(1),即:获得将由丙烯酸酯类与卤代乙酸酯类制备的1,2
‑
环丙烷二羧酸二酯(3
‑
0)水解合成而得的二羧酸化合物(3
‑
1)的工序(第一工
序);制成羧酸氯化物化合物(3
‑
2)的工序(第二工序);使硝基化合物(4)与所述二羧酸氯化物化合物(3
‑
2)反应而获得作为中间体的二硝基化合物(2)的工序(第三工序);以及将所述中间体的硝基还原的工序(第四工序)。
[0638]
[化136]
[0639][0640]
式中,r1、r2、x及n分别与通式(1)及通式(2)的r1、r2、x及n为相同含义。et表示乙基。
[0641]
在第一工序的反应中,作为合成二羧酸化合物(3
‑
1)的方法,也可采用《美国化学会志(j.am.chem.soc.)》,114(24),9401
‑
9408(1992)等中所记载的现有的方法,例如可列举如下方法,即:使丙烯酸酯化合物(5
‑
1)与卤代乙酸酯(5
‑
2)在氢化钠或叔丁醇钠的存在下反应获得二羧酸酯化合物(3
‑
0)后,在氢氧化钠水溶液的存在下将酯部位水解,由此获得二羧酸化合物(3
‑
1)。再者,在所述反应时也可使用有机溶剂。作为所使用的有机溶剂,例如可列举二甲基亚砜或二甲基甲酰胺等,就收率良好的方面而言,优选为使用二甲基甲酰胺。另外,在r1及r2成为一体而成为亚甲基的情况下,作为获得二羧酸化合物(3
‑
1)的工序(第一工序),也可采用《瑞士化学学报(helvetica chimica acta)》,95(2),268
‑
277(2012)等中所记载的现有的方法。
[0642]
在第二工序的反应中,作为合成二羧酸氯化物化合物(3
‑
2)的方法,只要采用国际公开第2008/112251号或《四面体(tetrahedron)》,56(29),5225
‑
5239(2000)等中所记载的现有的方法即可,并无特别限制,例如可列举将二羧酸化合物(3
‑
1)在过剩的亚硫酰氯的存在下且回流条件下搅拌的方法。再者,所述反应时,有机溶剂可有也可无,在使用有机溶剂的情况下,只要在反应后在蒸馏去除亚硫酰氯的同时去除有机溶剂即可。另外,二羧酸氯化物化合物(3
‑
2)也可通过在乙二酰氯的存在下搅拌二羧酸化合物(3
‑
1)来获得。此时,可以促进反应为目的来添加催化剂。
[0643]
作为第二工序的反应中使用的有机溶剂,只要为不影响反应的溶剂,则并无特别限定,可使用:苯、甲苯、二甲苯等芳香族烃;己烷、庚烷、环己烷等脂肪族烃;n,n
‑
二甲基甲酰胺(以下,称为dmf(n,n
‑
dimethyl formamide))、n,n
‑
二甲基乙酰胺(以下,称为dmac(n,
n
‑
dimethyl acetamide))、n
‑
甲基
‑2‑
吡咯烷酮(以下,称为nmp(n
‑
methyl
‑2‑
pyrrolidone))等酰胺;二乙醚、四氢呋喃(以下,称为thf(tetrahydrofuran))、1,4
‑
二噁烷、1,2
‑
二甲氧基乙烷(以下,称为dme(1,2
‑
dimethoxy ethane))、环戊基甲醚等醚;2
‑
丁酮、4
‑
甲基
‑2‑
戊酮等酮;乙腈、丙腈等腈;二甲基亚砜(以下,称为dmso(dimethyl sulfoxide));氯仿、二氯甲烷、二氯乙烷等卤化烃等。这些溶剂可以单体使用,也可将两种以上组合而使用。
[0644]
反应温度只要为使用溶剂的沸点以下即可,可设为0℃至200℃左右,优选为0℃至150℃,更优选为0℃至80℃。
[0645]
作为使用亚硫酰氯或乙二酰氯时所使用的催化剂,只要促进反应,则并无特别限定,例如可列举dmf。另外,作为使用量,并无特别限定,相对于二羧酸化合物(3
‑
1),通常为0.01摩尔%至50摩尔%,优选为0.1摩尔%至20摩尔%。
[0646]
反应后,蒸馏去除溶剂等,在粗产物的状态下或者进行纯化而用于下一工序。纯化方法任意,只要自再结晶、蒸馏、硅胶色谱等现有的方法中适宜选择即可。
[0647]
在第三工序的反应中,作为由二羧酸氯化物化合物(3
‑
2)合成二硝基化合物(2)的方法,并无特别限制,例如可列举在有机溶剂中、碱的存在下使硝基化合物(4)与二羧酸氯化物化合物(3
‑
2)反应的方法。
[0648]
作为第三工序的反应中使用的有机溶剂,只要为不影响反应的溶剂,则并无特别限定,可使用:苯、甲苯、二甲苯等芳香族烃;己烷、庚烷、环己烷等脂肪族烃;dmf、dmac、nmp等酰胺;二乙醚、thf、1,4
‑
二噁烷、dme、环戊基甲醚等醚;2
‑
丁酮、4
‑
甲基
‑2‑
戊酮等酮;乙腈、丙腈等腈;dmso;氯仿、二氯甲烷、二氯乙烷等卤化烃等。这些溶剂可以单体使用,也可将两种以上组合而使用。再者,在硝基化合物(4)与二羧酸氯化物化合物(3
‑
2)迅速反应而缩合的情况下,可使用将所述有机溶剂与水组合的肖顿鲍曼(schotten
‑
baumann)条件。
[0649]
反应温度只要为使用溶剂的沸点以下即可,可设为0℃至200℃左右,优选为0℃至100℃,更优选为0℃至50℃。
[0650]
所使用的碱只要可捕捉副产生的酸,则并无特别限定,例如可列举:吡啶、二甲基氨基吡啶(以下,设为dmap(dimethyl amino pyridine))、三乙胺、三丁胺等有机碱;氢氧化钠、氢氧化钾、碳酸氢钠、碳酸钠、碳酸钾等无机碱。
[0651]
反应后,蒸馏去除溶剂,在粗生成的状态下或者进行纯化而用于下一工序。纯化方法任意,只要自再结晶、蒸馏、提取、利用酸性或碱性水溶液的清洗、硅胶柱色谱法等现有的方法中适宜选择即可。
[0652]
在第四工序的反应中,作为将二硝基化合物(2)的硝基还原为氨基的方法,只要采用现有的方法即可。
[0653]
作为用于还原的氢源,可列举:氢气、肼、氯化氢、氯化铵、甲酸铵等。
[0654]
作为用于接触氢化的催化剂,可列举:铂、钯、钌、铑、镍、铁、锌、锡等金属粉末,也可为金属粉末担载在活性体上而成的催化剂。催化剂的种类可根据氢源的种类或反应条件而适宜决定,因此并无特别限定,只要为可仅还原硝基的催化剂即可,优选为可列举:钯
‑
碳、氧化铂、拉尼镍、铂
‑
碳、铑
‑
氧化铝、硫化铂碳等。
[0655]
例如有时将钯
‑
碳、氧化铂、拉尼镍、铂
‑
碳、铑
‑
氧化铝、硫化铂碳、还原铁、氯化铁、锡、氯化锡、锌等用作催化剂,将氢气、肼、氯化氢、氯化铵等用作氢源。特别是就不易引起由
二硝基化合物(2)的酯部位引起的副反应、可容易地获得目标物而言,优选为接触氢化或使用氯化锡或者其水合物等的贝尚(bechamp)还原反应。
[0656]
另外,催化剂量可根据氢源的种类或反应条件而适宜决定,因此并无特别限定,相对于作为原料的二硝基化合物(2),以金属换算计通常为0.01摩尔%至50摩尔%,优选为0.1摩尔%至20摩尔%。例如,作为氯化锡的使用量,可根据反应条件而适宜决定,因此并无特别限定,相对于作为原料的二硝基化合物,通常为1摩尔当量至50摩尔当量,优选为5摩尔当量至20摩尔当量。另外,也可使用氯化锡二水合物代替氯化锡。
[0657]
作为反应溶剂,可使用不影响反应的溶剂。例如可使用:乙酸甲酯、乙酸乙酯、乙酸丙酯等酯;苯、甲苯、二甲苯等芳香族烃;己烷、庚烷、环己烷等脂肪族烃;dmf、dmac、nmp等酰胺;thf、1,4
‑
二噁烷、dme、环戊基甲醚等醚;2
‑
丁酮、4
‑
甲基
‑2‑
戊酮等酮;甲醇、乙醇、丙醇等醇;dmso;水等。这些溶剂可以单体使用,也可将两种以上组合而使用。
[0658]
反应温度只要为原料或产物不发生分解、且所使用的溶剂的沸点以下的温度即可,可自此种温度范围选择反应高效进行的温度进行反应。具体而言,反应温度优选为
‑
78℃至溶剂的沸点以下的温度,就合成的简易性的观点而言,更优选为0℃至溶剂的沸点以下的温度。
[0659]
就提高反应速度以及能够在低温下进行反应等观点而言,接触氢化也可使用高压釜等在加压条件下进行。
[0660]
然后,自所获得的反应混合物中蒸馏去除溶剂后,使用再结晶、蒸馏、硅胶色谱等现有的方法进行纯化,由此可获得本发明的二胺化合物(1)。
[0661]
另外,作为本发明的二胺化合物的制造方法的优选的例子,也可列举如下方法:如下述反应流程所示,通过以下工序来合成二胺化合物(1),即:使二羧酸化合物(3
‑
1)与硝基化合物(4)反应来获得作为中间体的二硝基化合物(2)的工序(第五工序);以及将所述二硝基化合物(2)的硝基还原的工序。
[0662]
[化137]
[0663][0664]
式中,r1、r2、x及n分别与通式(2)的r1、r2、x及n为相同含义。关于二羧酸化合物(3
‑
1)的合成方法、及自二硝基化合物(2)还原为二胺化合物(1)的方法的说明与具体的条件,可参照关于所述第一工序及第四工序的记载。
[0665]
在第五工序中,例如使利用《瑞士化学学报(helvetica chimica acta)》,95(2),268
‑
277(2012)中记载的方法合成的二羧酸化合物(3
‑
1)在有机溶剂中、缩合剂的存在下与硝基化合物(4)反应,由此可获得二硝基化合物(2)(中间体)。再者,二羧酸化合物(3
‑
1)也可利用所述第一工序的说明中列举的其他合成方法合成。
[0666]
在第五工序的反应中,作为使二羧酸化合物(3
‑
1)与硝基化合物(4)缩合的方法,只要采用现有的方法(施特格利希(steglich)酯化反应等)即可,并无特别限制,例如可列举在缩合剂的存在下进行反应的方法。
[0667]
作为反应中使用的有机溶剂,只要为不影响反应的溶剂,则并无特别限定,可使用:苯、甲苯、二甲苯等芳香族烃;己烷、庚烷、环己烷等脂肪族烃;dmf、dmac、nmp等酰胺;二乙醚、thf、1,4
‑
二噁烷、dme、环戊基甲醚等醚;2
‑
丁酮、4
‑
甲基
‑2‑
戊酮等酮;乙腈、丙腈等腈;dmso;氯仿、二氯甲烷、二氯乙烷等卤化烃等。这些溶剂可以单体使用,也可将两种以上组合而使用。
[0668]
反应温度只要为使用溶剂的沸点以下即可,可设为0℃至200℃左右,优选为
‑
10℃至100℃,更优选为0℃至50℃。
[0669]
反应后,在粗生成的状态下或者进行纯化而用于下一工序。纯化方法任意,只要自再结晶、蒸馏、硅胶柱色谱法等现有的方法中适宜选择即可。
[0670]
使用的缩合剂只要可促进酯化,则并无特别限定,例如可列举:二环己基碳二酰亚胺(以下,称为dcc(dicyclohexyl carbodiimide))、二异丙基碳二酰亚胺(以下,称为dic(diisopropyl carbodiimide))、1
‑
乙基
‑3‑
(3
‑
二甲基氨基丙基)碳二酰亚胺(以下,称为edc(1
‑
ethyl
‑3‑
(3
‑
dimethyl amino propyl)carbodiimide)或wsci(1
‑
ethyl
‑3‑
(3
‑
dimethyl amino propyl)carbodiimide))、1
‑
乙基
‑3‑
(3
‑
二甲基氨基丙基)碳二酰亚胺盐酸盐(以下,称为edc
‑
hcl(1
‑
ethyl
‑3‑
(3
‑
dimethyl amino propyl)carbodiimide hydrochloride))等。
[0671]
作为使用的催化剂,只要促进反应,则并无特别限定,例如可列举dmap、吡啶等。另外,作为使用量,并无特别限定,相对于二羧酸化合物(3
‑
1),通常为1摩尔%至100摩尔%,优选为10摩尔%至50摩尔%。
[0672]
[经由保护二氨基化合物(7)的二胺化合物的制造方法]
[0673]
进而,作为本发明的二胺化合物的制造方法的优选的例子,也可列举如下方法:如下述反应流程所示,通过以下工序来合成二胺化合物(1),即:使环丙烷衍生物(3)与具有经boc保护的氨基的酚化合物(6)反应来获得作为中间体的保护二氨基化合物(7)的工序(第六工序);以及对所述中间体的保护基进行脱保护的工序(第七工序)。
[0674]
[化138]
[0675][0676]
式中,r1、r2、x、n及y分别与通式(1)及通式(2)的r1、r2、x及n、通式(3)的y为相同含义。boc表示叔丁氧基羰基。环丙烷衍生物(3)中可优选地使用二羧酸化合物(3
‑
1)。关于二羧酸化合物(3
‑
1)的合成方法的说明与具体的条件,可参照关于所述第一工序的记载。
[0677]
第六工序为例如使二羧酸化合物(3
‑
1)与具有boc保护氨基的苯酚化合物(6)进行缩合反应来获得保护二氨基化合物(7)的工序,使用具有经boc保护的氨基的苯酚化合物(6)代替硝基化合物(4),除此以外可与所述第五工序同样地进行。即,第六工序中只要采用
现有的缩合方法(施特格利希酯化反应等)即可,并无特别限制。
[0678]
此处,作为具有经boc保护的氨基的苯酚化合物(6)的优选的例子,可列举下述通式(6
‑
1)所表示的保护氨基苯酚化合物(保护氨基苯酚化合物(6
‑
1))。通过使用保护氨基苯酚化合物(6
‑
1),可合成在相对于酯基的对位上具有保护氨基的保护二氨基化合物(7
‑
1),通过对其进行脱保护,可制造所述二胺化合物(1
‑
1)。关于保护二氨基化合物(7
‑
1)的说明与优选的范围,可参照所述<保护二氨基化合物>一栏的记载,关于二氨基化合物(1
‑
1)的说明与优选的范围、具体例,可参照所述<二胺化合物>一栏的记载。
[0679]
[化139]
[0680][0681]
通式(6
‑
1)中,x、n及boc分别与通式(6)的x、n及boc为相同含义。
[0682]
第六工序中使用的具有经boc保护的氨基的苯酚化合物(6)例如只要利用日本专利特开2015
‑
176110号公报中记载的方法来制备即可。
[0683]
第七工序为对第六工序中获得的保护二氨基化合物(7)的boc基进行脱保护来获得二胺化合物(1)的工序。boc基的脱保护可通过使用酸的现有的脱保护方法进行,脱保护用的酸例如可使用三氟乙酸等。
[0684]
[实施例]
[0685]
以下,列举实施例与比较例来对本发明的特征进行更具体的说明。以下的实施例中所示的材料、使用量、比例、处理内容、处理程序等只要不脱离本发明的主旨,则可适宜变更。因此,本发明的范围不应由以下所示的具体例进行限定性解释。
[0686]
二硝基化合物、二胺化合物及二胺异构体混合物的合成
[0687]
各合成例中示出的反应式中,me表示甲基,et表示乙基。另外,各反应式中,在化合物为反式体的情况下,设为仅示出其中一个对映体,但另一对映体也包含在原料、产物中。
[0688]
[合成例1]二硝基化合物1的合成
[0689]
[化140]
[0690][0691]
将反式
‑
1,2
‑
环丙烷二羧酸二乙酯(10.0g、53.7mmol)的乙醇(100ml)溶液冰浴冷却后,加入氢氧化钠(8.60g、215mmol)的水(100ml)溶液。历时1小时将所述混合物慢慢升温至室温后,搅拌15小时。反应结束后,将反应混合物在减压下浓缩,并蒸馏去除乙醇。将残渣再次冰浴冷却,加入浓盐酸(20ml)后,加入过量的食盐,利用乙酸乙酯(100ml
×
8次)进行提取。利用无水硫酸钠将有机层干燥后,在减压下浓缩,由此获得反式
‑
1,2
‑
环丙烷二羧酸的白色固体(产量6.44g、收率92%)。
[0692]1h
‑
nmr(400mhz,dmso
‑
d6):δ1.89
‑
1.77(m,2h),1.26
‑
1.14(m,2h).
[0693]
[化141]
[0694][0695]
向反式
‑
1,2
‑
环丙烷二羧酸(6.00g、46.1mmol)中加入亚硫酰氯(30ml),在70℃下搅拌4小时后,在减压下浓缩,蒸馏去除亚硫酰氯,由此获得粗制的反式
‑
1,2
‑
环丙烷二羧酸氯化物。所述羧酸氯化物设为thf(90ml)溶液,全部用于以下的反应。
[0696]
在氩环境下,向4
‑
硝基苯酚(13.5g、96.8mmol)的thf(100ml)溶液中加入三乙胺(16.3g、161mmol)并进行冰浴冷却。一面激烈搅拌所述混合物,一面历时5分钟加入所述制备的羧酸氯化物的thf溶液后,升温至室温,在室温下搅拌两个半小时。向所述反应混合物中加入饱和氯化铵水溶液(100ml),并在减压下浓缩。利用乙酸乙酯(300ml
×
3次)提取残渣后,利用饱和碳酸氢钠(300ml)加以清洗。利用无水硫酸钠使有机层干燥后,在减压下浓缩,由此获得反式
‑
1,2
‑
环丙烷二羧酸二(4
‑
硝基苯基)酯的淡黄色固体(7.36g)。进而,过滤分离残留在水层中的固体,并利用水进行清洗,由此回收反式
‑
1,2
‑
环丙烷二羧酸二(4
‑
硝基苯基)酯的淡黄色固体(6.72g),与所述7.36g合并,由此获得二硝基化合物1(反式
‑
1,2
‑
环丙烷二羧酸二(4
‑
硝基苯基)酯)(合计产量14.1g、收率82%)。
[0697]1h
‑
nmr(400mhz,cdcl3):δ8.31(d,j=9.2hz,4h),7.35(d,j=9.2hz,4h),2.66
‑
2.59(m,2h),1.86
‑
1.78(m,2h).
[0698]
[合成例2]二胺异构体混合物1(二胺化合物(1
‑4‑
1)及其对映体的混合物)的合成
[0699]
[化142]
[0700][0701]
在氩环境下,向二硝基化合物1(14.0g、37.6mmol)的乙酸乙酯(370ml)溶液中加入氯化锡(ii)二水合物(84.8g、376mmol),在加热回流下搅拌4小时。反应结束后,将反应混合物冷却至室温,将反应混合物加入至饱和碳酸氢钠水溶液(1l)中后,利用乙酸乙酯(300ml
×
3次)进行提取。利用饱和碳酸氢钠水溶液(300ml)、饱和食盐水(300ml)对所获得的有机层进行清洗后,利用无水硫酸钠加以干燥,并在减压下浓缩。对于所获得的残渣,将氯仿:甲醇的混合溶剂用于洗脱液,一面使其比例在100:0~95:5的范围内变化,一面利用硅胶柱色谱法进行纯化,由此获得作为目标的二胺异构体混合物1(二胺化合物(1
‑4‑
1)及其对映体的混合物)的白色固体(产量8.50g、收率72%)。
[0702]1h
‑
nmr(400mhz,cdcl3):δ6.90(d,j=8.8hz,4h),6.67(d,j=8.8hz,4h),3.64(brs,4h),2.53
‑
2.47(m,2h),1.71
‑
1.65(m,2h).
[0703]
[合成例3]二硝基化合物2的合成
[0704]
[化143]
[0705][0706]
将3
‑
氧杂双环[3.1.0]己烷
‑
2,4
‑
二酮(10.0g、81.9mmol)的水(160ml)悬浮液在加热回流下搅拌3小时。冷却至室温后,在减压下浓缩,由此获得顺式
‑
1,2
‑
环丙烷二羧酸的淡黄色固体(产量10.7g)。
[0707]1h
‑
nmr(400mhz,dmso
‑
d6):δ12.26(brs,2h),2.53(dd,j=8.3,6.6hz,2h),2.01(td,j=6.6,4.2hz,1h),1.64(td,j=8.3,4.2hz,1h).
[0708]
[化144]
[0709][0710]
向顺式
‑
1,2
‑
环丙烷二羧酸(8.02g、61.6mmol)的甲苯(40ml)悬浮液中加入亚硫酰氯(40ml)及dmf(0.4ml),在100℃下搅拌4小时后,在减压下浓缩,由此获得粗制的顺式
‑
1,2
‑
环丙烷二羧酸氯化物。所述羧酸氯化物设为thf(80ml)溶液,全部用于以下的反应。
[0711]
在氩环境下,向4
‑
硝基苯酚(17.9g、129mmol)的thf(160ml)溶液中加入三乙胺(21.9g、216mmol)并进行冰浴冷却。一面激烈搅拌所述混合物,一面历时5分钟加入所述制备的羧酸氯化物的thf溶液后,升温至室温,在室温下搅拌两个半小时。向所述反应混合物中加入饱和氯化铵水溶液(200ml),并在减压下浓缩。利用乙酸乙酯(300ml
×
3次)提取残渣后,利用饱和碳酸氢钠(300ml)加以清洗。过滤分离产生的固体,并利用水(100ml)、饱和碳酸氢钠水溶液(100ml)进行清洗后,再次利用水(100ml)进行清洗。将所获得的固体在减压下干燥,由此获得作为目标的二硝基化合物2(顺式
‑
1,2
‑
环丙烷二羧酸二(4
‑
硝基苯基)酯)的淡黄色固体(产量12.6g、收率55%)。
[0712]1h
‑
nmr(400mhz,cdcl3):δ8.26(d,j=9.2hz,4h),7.29(d,j=9.2,4h),2.53(dd,j=8.5,6.7hz,2h),2.01(td,j=6.7,5.4hz,1h),1.64(td,j=8.5,5.4hz,1h).
[0713]
[合成例4]二胺化合物(1
‑2‑
1)的合成
[0714]
[化145]
[0715][0716]
在氩环境下,向二硝基化合物2(14.2g、38.1mmol)的乙酸乙酯(380ml)溶液中加入氯化锡(ii)二水合物(86.0g、381mmol),在加热回流下搅拌3小时。反应结束后,将反应混合物冷却至室温,加入至饱和碳酸氢钠水溶液(1l)中后,利用硅藻土进行过滤。利用乙酸乙酯(300ml
×
3次)提取所获得的混合物后,利用饱和碳酸氢钠水溶液(300ml)、饱和食盐水(300ml)对有机层进行清洗。利用无水硫酸钠对所获得的有机层进行干燥,并在减压下浓缩。对于残渣,将氯仿:甲醇的混合溶剂用于洗脱液,一面使其比例在100:0~95:5的范围内
变化,一面利用硅胶柱色谱法进行纯化后,进而利用乙酸乙酯(50ml)与己烷(50ml)进行再沉淀,由此获得作为目标的二胺化合物(1
‑2‑
1)(顺式
‑
1,2
‑
环丙烷二羧酸二(4
‑
氨基苯基)酯)的白色固体(产量8.52g、收率72%)。
[0717]1h
‑
nmr(400mhz,cdcl3):δ6.87(d,j=8.8hz,4h),6.62(d,j=8.8hz,4h),3.61(brs,4h),2.37(dd,j=8.4,6.7hz,2h),1.91(td,j=6.7,5.2hz,1h),1.45(td,j=8.4,5.2hz,1h).
[0718]
[合成例5]二硝基化合物3的合成
[0719]
[化146]
[0720][0721]
在冰浴冷却下,历时30分钟向浓硫酸(20ml)中滴加乙酰乙酸乙酯(26.6g、204mmol)。在滴加后,将所述混合物升温至室温并搅拌22小时。反应结束后,将反应溶液注入至冰(60g)后,搅拌至冰全部溶解。利用二乙醚(100ml
×
3次)提取所获得的混合物后,利用10wt%碳酸钠水溶液加以清洗。利用无水硫酸镁对有机层进行干燥后,在减压下浓缩。对于所获得的残渣,将己烷:乙酸乙酯的混合溶剂用于洗脱液,一面使其比例在100:0~80:20的范围内变化,一面利用硅胶柱色谱法进行纯化,由此获得4,6
‑
二甲基
‑2‑
氧代
‑
2h
‑
吡喃
‑5‑
羧酸乙酯的淡黄色油状物质(产量6.88g、收率34%)。
[0722]1h
‑
nmr(400mhz,cdcl3):δ6.01(s,1h),4.35(q,j=7.1hz,2h),2.40(s,3h),2.23(s,3h),1.37(t,j=7.1hz,3h).
[0723]
[化147]
[0724][0725]
在氩环境下,将4,6
‑
二甲基
‑2‑
氧代
‑
2h
‑
吡喃
‑5‑
羧酸乙酯(25.0g、127mmol)的氯仿(50ml)溶液冰浴冷却后,一面搅拌一面历时30分钟滴加溴(23.3g、146mmol)的氯仿(50ml)溶液。将所述混合物升温至室温后,搅拌24小时。反应结束后,将反应混合物注入至冰(300g)中后,搅拌至冰全部溶解。利用乙酸乙酯(150ml
×
3次)提取混合物后,利用10wt%碳酸钠水溶液(300ml)、饱和食盐水(100ml)加以清洗。利用无水硫酸镁将有机层干燥后,在减压下浓缩而生成粗固体,利用己烷(100ml)对所生成的粗固体进行清洗,由此获得3
‑
溴
‑
4,6
‑
二甲基
‑2‑
氧代
‑
2h
‑
吡喃
‑5‑
羧酸乙酯的淡黄色固体(产量33.1g、收率95%)。
[0726]1h
‑
nmr(400mhz,cdcl3):δ4.37(q,j=7.1hz,2h),2.35(s,3h),2.34(s,3h),1.38(q,j=7.1hz,3h).
[0727]
[化148]
[0728][0729]
在油浴(110℃)下对3
‑
溴
‑
4,6
‑
二甲基
‑2‑
氧代
‑
2h
‑
吡喃
‑5‑
羧酸乙酯(34.0g、124mmol)的1,4
‑
二噁烷(70ml)溶液进行加温后,在加热回流下,历时20分钟滴加7m氢氧化钾水溶液(171ml)。滴加后,在所述温度下搅拌1小时后进行冰浴冷却,慢慢加入50%硫酸(68ml)。对反应混合物进行过滤,利用二乙醚(150ml)加以清洗。利用二乙醚(150ml
×
3次)提取混合物后,利用饱和食盐水(100ml)加以清洗。利用硫酸镁将有机层干燥后,在减压下浓缩,由此获得粗产物。将其利用乙酸乙酯(10ml)
‑
己烷(100ml)进行再结晶,由此获得反式
‑3‑
亚甲基
‑
1,2
‑
环丙烷二羧酸的褐色结晶(产量5.92g、收率34%)。
[0730]1h
‑
nmr(400mhz,dmso
‑
d6):δ12.8(brs,2h),5.66
‑
5.62(m,2h),2.63
‑
2.59(m,2h).
[0731]
[化149]
[0732][0733]
在氩环境下,向反式
‑3‑
亚甲基
‑
1,2
‑
环丙烷二羧酸(10.0g、70.4mmol)的二氯甲烷(700ml)溶液中加入4
‑
硝基苯酚(24.5g、176mmol)后,在冰浴冷却下一面搅拌一面加入edc
‑
hcl(33.7g、176mmol)、dmap(1.72g、14.1mmol)。一面将所述混合物慢慢升温至室温,一面搅拌6小时后,加入水(150ml)。利用乙酸乙酯(500ml
×
3次)提取所述反应混合物,利用硫酸钠将有机层干燥后,在减压下浓缩。利用乙醇(5ml)
‑
乙酸乙酯(20ml)
‑
己烷(20ml)对所获得的粗固体进行再沉淀后,利用80℃的热水(500ml)加以清洗,由此获得二硝基化合物3(反式
‑3‑
亚甲基
‑
1,2
‑
环丙烷二羧酸二(4
‑
硝基苯基)酯)的淡黄色固体(产量16.7g、收率62%)。
[0734]1h
‑
nmr(400mhz,dmso
‑
d6):δ8.31(d,j=9.2hz,4h),7.35(d,j=9.2hz,4h),5.98
‑
5.94(m,2h),3.32
‑
3.28(m,2h).
[0735]
[合成例6]二胺异构体混合物2(二胺化合物(1
‑3‑
2)及其对映体的混合物)的合成
[0736]
[化150]
[0737][0738]
在氩环境下,向二硝基化合物3(15.0g、39.0mmol)的乙酸乙酯(300ml)溶液中加入氯化锡(ii)二水合物(88.0g、390mmol),在加热回流下搅拌4小时。反应结束后,将反应混合物冷却至室温,加入至饱和碳酸氢钠水溶液(1.1l)中后,利用硅藻土进行过滤。利用乙酸乙酯(300ml
×
3次)提取滤液后,利用饱和食盐水(300ml)加以清洗。利用无水硫酸钠对所获得的有机层进行干燥,并在减压下浓缩。对于所获得的残渣,将氯仿:甲醇=90:10的混合溶剂用于洗脱液,并利用硅胶柱色谱法进行纯化,由此获得作为目标的二胺异构体混合物2(二
胺化合物(1
‑3‑
2)及其对映体的混合物)的白色固体(产量7.05g、收率56%)。
[0739]1h
‑
nmr(400mhz,cdcl3):δ6.81(d,j=8.8hz,4h),6.54(d,j=8.8hz,4h),5.90
‑
5.85(m,2h),5.08(brs,4h),3.12
‑
3.08(m,2h).
[0740]
[合成例7]二硝基化合物4的合成
[0741]
[化151]
[0742][0743]
将反式
‑
1,2
‑
环丙烷二羧酸(2.00g、15.4mmol)、4
‑
硝基
‑
邻甲酚(4.93g、31.6mmol)溶解在二氯甲烷(154ml)中,并进行冰浴冷却。向其中加入1
‑
(3
‑
二甲基氨基丙基)
‑3‑
乙基碳二酰亚胺盐酸盐(6.18g、31.6mmol)与4
‑
二甲基氨基吡啶(0.38g、3.1mmol),升温至室温并搅拌24小时。反应结束后,向反应混合物中加入水(50ml),利用乙酸乙酯(50ml
×
3次)进行提取。利用无水硫酸镁将合并后的有机层干燥后,在减压下浓缩。利用甲醇(40ml)对所获得的粗产物进行清洗,由此获得二硝基化合物4[反式
‑
1,2
‑
环丙烷二羧酸双(2
‑
甲基
‑4‑
硝基苯基)酯]的黄色固体(产量5.03g、收率82%)。
[0744]1h
‑
nmr(400mhz,dmso
‑
d6):δ8.27(dd,j=2.8,0.6hz,2h),8.16(ddd,j=8.8,2.8,0.6hz,2h),7.51(d,j=8.8hz,2h),2.71
‑
2.67(m,2h),2.29(s,6h),1.85
‑
1.81(m,2h).
[0745]
[合成例8]二胺异构体混合物3(二胺化合物(1
‑3‑
3)及其对映体的混合物)的合成
[0746]
[化152]
[0747][0748]
在氩环境下,在室温下将反式
‑
1,2
‑
环丙烷二羧酸双(2
‑
甲基
‑4‑
硝基苯基)酯(5.02g、12.5mmol)、10%钯碳(0.53g、0.50mmol)、四氢呋喃(200ml)的混合物搅拌17小时。反应结束后,一面利用四氢呋喃(200ml)清洗反应混合物,一面进行硅藻土过滤,在减压下对滤液进行浓缩。利用甲醇(30ml)对所获得的固体进行清洗,由此获得作为目标的二胺异构体混合物3(二胺化合物(1
‑3‑
3)及其对映体的混合物)的淡黄色固体(产量2.47g、收率58%)。
[0749]1h
‑
nmr(400mhz,dmso
‑
d6):δ6.73(d,j=8.5hz,2h),6.43(d,j=2.5hz,2h),6.38(dd,j=8.5,2.5hz,2h),4.98(brs,4h),2.44
‑
2.40(m,2h),1.97(s,6h),1.65
‑
1.61(m,2h).
[0750]
[合成例9]二硝基化合物5的合成
[0751]
[化153]
[0752]
[0753]
向反式
‑
1,2
‑
环丙烷二羧酸(3.03g、23.2mmol)中加入亚硫酰氯(15.4ml),在70℃下搅拌4小时。反应结束后在减压下浓缩,由此蒸馏去除亚硫酰氯,获得粗生成的反式
‑
1,2
‑
环丙烷二羧酸氯化物。所述酸氯化物设为thf(46ml)溶液,全部用于以下的反应。
[0754]
在氩环境下,向4
‑
硝基
‑
间甲酚(7.64g、48.9mmol)的thf(50ml)溶液中加入三乙胺(11.3ml、81.5mmol)并进行冰浴冷却。历时5分钟向所述溶液中滴加之前制备的酸氯化物的thf溶液后,升温至室温并搅拌18小时。反应结束后,向反应混合物中加入水(100ml),并在减压下浓缩。利用乙酸乙酯(100ml
×
3)提取残渣后,利用饱和氯化钠水溶液(100ml)加以清洗。利用无水硫酸镁将有机层干燥后,在减压下浓缩。利用甲醇(50ml)对所获得的残渣进行清洗,由此获得二硝基化合物5[反式
‑
1,2
‑
环丙烷二羧酸双(3
‑
甲基
‑4‑
硝基苯基)酯]的黄土色固体(产量8.09g、收率87%)。
[0755]1h
‑
nmr(400mhz,dmso
‑
d6):δ8.10(d,j=8.9hz,2h),7.42(d,j=2.4hz,2h),7.35(dd,j=2.4,8.9hz,2h),2.62
‑
2.59(m,2h),2.54(s,6h),1.80
‑
1.76(m,2h).
[0756]
[合成例10]二胺异构体混合物4(二胺化合物(1
‑3‑
4)及其对映体的混合物)的合成
[0757]
[化154]
[0758][0759]
在氩环境下,向反式
‑
1,2
‑
环丙烷二羧酸双(3
‑
甲基
‑4‑
硝基苯基)酯(3.02g、7.55mmol)的乙酸乙酯(76ml)溶液中加入氯化锡(ii)二水合物(17.6g、75.5mmol),在加热回流下搅拌2小时。反应结束后冷却至室温,将反应混合物加入至饱和碳酸氢钠水溶液(300ml)后,进行硅藻土过滤,利用乙酸乙酯(100ml
×
3)提取滤液。利用饱和碳酸氢钠水溶液(200ml)、饱和食盐水(200ml)对合并后的有机层进行清洗后,利用无水硫酸镁加以干燥,并在减压下浓缩。对于所获得的残渣,将氯仿:甲醇的混合溶剂用于洗脱液,一面使其比例在95:5~85:15的范围内变化,一面利用硅胶色谱法进行纯化,由此获得作为目标的二胺异构体混合物4(二胺化合物(1
‑3‑
4)及其对映体的混合物)的淡黄色固体(产量2.09g、收率81%)。
[0760]1h
‑
nmr(400mhz,dmso
‑
d6):δ6.74(d,j=2.4hz,2h),6.69(dd,j=2.4,8.5hz,2h),6.58(d,j=8.5hz,2h),4.82(brs,4h),2.38
‑
2.34(m,2h),2.04(s,6h),1.61
‑
1.57(m,2h).
[0761]
[合成例11]二硝基化合物6的合成
[0762]
[化155]
[0763][0764]
向反式
‑
1,2
‑
环丙烷二羧酸(1.81g、13.9mmol)中加入亚硫酰氯(9.2ml),在70℃下搅拌4小时。反应结束后在减压下浓缩,由此蒸馏去除亚硫酰氯,获得粗生成的反式
‑
1,2
‑
环丙烷二羧酸氯化物。所述酸氯化物设为thf(28ml)溶液,全部用于以下的反应。
[0765]
在氩环境下,向2,6
‑
二甲基
‑4‑
硝基苯酚(4.97g、29.2mmol)的thf(30ml)溶液中加
入三乙胺(6.7ml、48.6mmol)并进行冰浴冷却。历时30分钟向所述溶液中滴加之前制备的酸氯化物的thf溶液后,升温至室温并搅拌21小时。反应结束后,向反应混合物中加入水(150ml),过滤分离沉淀物后,利用甲醇(30ml)加以清洗,由此获得二硝基化合物6[反式
‑
1,2
‑
环丙烷二羧酸双(2,6
‑
二甲基
‑4‑
硝基苯基)酯]的浅茶色固体(产量5.58g、收率94%)。
[0766]1h
‑
nmr(400mhz,dmso
‑
d6):δ8.10(s,4h),2.78
‑
2.75(m,2h),2.26(s,12h),1.89
‑
1.85(m,2h).
[0767]
[合成例12]二胺异构体混合物5(二胺化合物(1
‑3‑
5)及其对映体的混合物)的合成
[0768]
[化156]
[0769][0770]
在氩环境下,向反式
‑
1,2
‑
环丙烷二羧酸双(2,6
‑
二甲基
‑4‑
硝基苯基)酯(2.55g、6.0mmol)的乙酸乙酯(60ml)溶液中加入氯化锡(ii)二水合物(13.8g、59.5mmol),在加热回流下搅拌1小时。反应结束后冷却至室温,将反应混合物加入至饱和碳酸氢钠水溶液(300ml)中后,进行硅藻土过滤,利用乙酸乙酯(100ml
×
3)提取滤液。利用饱和碳酸氢钠水溶液(200ml)、饱和食盐水(200ml)对合并后的有机层进行清洗后,利用无水硫酸镁加以干燥,并在减压下浓缩。对于所获得的残渣,将氯仿:甲醇的混合溶剂用于洗脱液,一面使其比例在95:5~85:15的范围内变化,一面利用硅胶色谱法进行纯化后,利用甲醇(50ml)进行清洗,由此获得作为目标的二胺异构体混合物5[二胺化合物(1
‑3‑
5)及其对映体的混合物]的淡黄色固体(产量1.41g、收率64%)。
[0771]1h
‑
nmr(400mhz,dmso
‑
d6):δ6.26(s,4h),4.88(brs,4h),2.47
‑
2.44(m,2h),1.94(s,12h),1.69
‑
1.66(m,2h).
[0772]
[合成例13]二硝基化合物7的合成
[0773]
[化157]
[0774][0775]
向反式
‑
1,2
‑
环丙烷二羧酸(1.91g、14.7mmol)中加入亚硫酰氯(9.8ml),在70℃下搅拌4小时后在减压下浓缩,由此蒸馏去除亚硫酰氯,获得粗生成的反式
‑
1,2
‑
环丙烷二羧酸氯化物。所述酸氯化物设为thf(30ml)溶液,全部用于以下的反应。
[0776]
在氩环境下,向2
‑
氟
‑4‑
硝基苯酚(4.98g、30.8mmol)的thf(32ml)溶液中加入三乙胺(7.10ml、51.3mmol)并进行冰浴冷却。历时10分钟向所述溶液中滴加之前制备的酸氯化物的thf溶液后,升温至室温并搅拌16小时。反应结束后,向反应混合物中加入水(100ml),并在减压下浓缩。利用乙酸乙酯(100ml
×
3)提取残渣后,利用饱和氯化钠水溶液(100ml)加以清洗,利用无水硫酸镁将有机层干燥,并在减压下浓缩。利用甲醇(50ml)对所获得的残渣进行清洗,由此获得二硝基化合物7[反式
‑
1,2
‑
环丙烷二羧酸双(2
‑
氟
‑4‑
硝基苯基)酯]的
白色固体(产量5.29g、收率88%)。
[0777]1h
‑
nmr(400mhz,dmso
‑
d6):δ8.39(d,j=2.6hz,1h),8.37(d,j=2.6hz,1h),8.22
‑
8.19(m,2h),7.78(d,j=7.7hz,1h),7.75(d,j=7.7hz,1h),2.76
‑
2.72(m,2h),1.89
‑
1.85(m,2h).
19
f
‑
nmr(376mhz,dmso
‑
d6):δ
‑
124.4(s,2f).
[0778]
[合成例14]二胺异构体混合物6(二胺化合物(1
‑3‑
6)及其对映体的混合物)的合成
[0779]
[化158]
[0780][0781]
在氩环境下,向反式
‑
1,2
‑
环丙烷二羧酸双(2
‑
氟
‑4‑
硝基苯基)酯(3.20g、7.83mmol)的乙酸乙酯(78ml)溶液中加入氯化锡(ii)二水合物(18.2g、78.3mmol),在加热回流下搅拌1小时。反应结束后冷却至室温,将反应混合物加入至饱和碳酸氢钠水溶液(300ml)中后,进行硅藻土过滤,利用乙酸乙酯(100ml
×
3)提取滤液。利用饱和碳酸氢钠水溶液(200ml)、饱和食盐水(200ml)对合并后的有机层进行清洗后,利用无水硫酸镁加以干燥,并在减压下浓缩。对于所获得的残渣,将氯仿:甲醇的混合溶剂用于洗脱液,一面使其比例在95:5~85:15的范围内变化,一面利用硅胶色谱法进行纯化,由此获得作为目标的二胺异构体混合物6[二胺化合物(1
‑3‑
6)及其对映体的混合物]的淡黄色固体(产量2.34g、收率86%)。
[0782]1h
‑
nmr(400mhz,dmso
‑
d6):δ6.94(t,j=8.8hz,2h),6.43(dd,j=8.8,2.5hz,2h),6.34(dd,j=8.8,2.5hz,2h),5.39(brs,4h),2.48
‑
2.44(m,2h),1.68
‑
1.64(m,2h).
19
f
‑
nmr(376mhz,dmso
‑
d6):δ
‑
130.1(s,2f).
[0783]
[合成例15]二硝基化合物8的合成
[0784]
[化159]
[0785][0786]
向反式
‑
1,2
‑
环丙烷二羧酸(1.90g、14.6mmol)中加入亚硫酰氯(9.8ml),在70℃下搅拌4小时后在减压下浓缩,由此蒸馏去除亚硫酰氯,获得粗生成的反式
‑
1,2
‑
环丙烷二羧酸氯化物。所述酸氯化物设为thf(30ml)溶液,全部用于以下的反应。
[0787]
在氩环境下,向3
‑
氟
‑4‑
硝基苯酚(4.92g、30.7mmol)的thf(32ml)溶液中加入三乙胺(7.10ml、51.2mmol)并进行冰浴冷却。历时5分钟向所述溶液中滴加之前制备的酸氯化物的thf溶液后,升温至室温并搅拌16小时。反应结束后,向反应混合物中加入水(100ml),过滤分离沉淀物并加以干燥,由此获得二硝基化合物8[反式
‑
1,2
‑
环丙烷二羧酸双(3
‑
氟
‑4‑
硝基苯基)酯]的白色固体(产量2.87g、收率48%)。
[0788]1h
‑
nmr(400mhz,dmso
‑
d6):δ8.28(t,j=8.9hz,2h),7.67(dd,j=12.0,2.4hz,2h),7.38(ddd,j=12.0,8.9,2.4hz,2h),2.66
‑
2.62(m,2h),1.84
‑
1.80(m,2h).
19
f
‑
nmr(376mhz,
dmso
‑
d6):δ
‑
115.3(s,2f).
[0789]
[合成例16]二胺异构体混合物7(二胺化合物(1
‑3‑
7)及其对映体的混合物)的合成
[0790]
[化160]
[0791][0792]
在氩环境下,向反式
‑
1,2
‑
环丙烷二羧酸双(3
‑
氟
‑4‑
硝基苯基)酯(2.81g、6.89mmol)的乙酸乙酯(70ml)溶液中加入氯化锡(ii)二水合物(16.0g、68.9mmol),在加热回流下搅拌1小时。反应结束后冷却至室温,将反应混合物加入至饱和碳酸氢钠水溶液(200ml)中后,进行硅藻土过滤,利用乙酸乙酯(100ml
×
3)提取滤液。利用饱和碳酸氢钠水溶液(150ml)、饱和食盐水(150ml)对合并后的有机层进行清洗后,利用无水硫酸镁加以干燥,并在减压下浓缩。对于所获得的残渣,将氯仿:甲醇的混合溶剂用于洗脱液,一面使其比例在95:5~85:15的范围内变化,一面利用硅胶色谱法进行纯化,由此获得作为目标的二胺异构体混合物7[二胺化合物(1
‑3‑
7)及其对映体的混合物]的淡黄色固体(产量1.08g、收率45%)。
[0793]1h
‑
nmr(400mhz,dmso
‑
d6):δ6.97
‑
6.93(m,2h),6.78
‑
6.71(m,4h),2.42
‑
2.39(m,2h),1.65
‑
1.61(m,2h).
19
f
‑
nmr(376mhz,dmso
‑
d6):δ
‑
132.8(s,2f).
[0794]
[合成例17]二硝基化合物9的合成
[0795]
[化161]
[0796][0797]
向反式
‑
1,2
‑
环丙烷二羧酸(3.01g、23.2mmol)中加入亚硫酰氯(15.4ml),在70℃下搅拌4小时后在减压下浓缩,由此蒸馏去除亚硫酰氯,获得粗生成的反式
‑
1,2
‑
环丙烷二羧酸氯化物。所述酸氯化物设为thf(46ml)溶液,全部用于以下的反应。
[0798]
在氩环境下,向2
‑
氯
‑4‑
硝基苯酚(8.61g、48.6mmol)的thf(50ml)溶液中加入三乙胺(11.2ml、81.0mmol)并进行冰浴冷却。历时5分钟向所述溶液中滴加之前制备的酸氯化物的thf溶液后,升温至室温并搅拌18小时。反应结束后,向反应混合物中加入水(150ml),过滤分离沉淀物并加以干燥,由此获得二硝基化合物9[反式
‑
1,2
‑
环丙烷二羧酸双(2
‑
氯
‑4‑
硝基苯基)酯]的白色固体(产量9.96g、收率98%)。
[0799]1h
‑
nmr(400mhz,dmso
‑
d6):δ8.51(d,j=2.7hz,2h),8.32(dd,j=9.0,2.7hz,2h),7.77(d,j=9.0hz,2h),2.77
‑
2.73(m,2h),1.92
‑
1.88(m,2h).
[0800]
[合成例18]二胺异构体混合物8(二胺化合物(1
‑3‑
8)及其对映体的混合物)的合成
[0801]
[化162]
[0802][0803]
在氩环境下,向反式
‑
1,2
‑
环丙烷二羧酸双(2
‑
氯
‑4‑
硝基苯基)酯(2.10g、4.76mmol)的乙酸乙酯(48ml)溶液中加入氯化锡(ii)二水合物(11.1g、47.6mmol),在加热回流下搅拌1小时。反应结束后冷却至室温,将反应混合物加入至饱和碳酸氢钠水溶液(200ml)中后,进行硅藻土过滤,利用乙酸乙酯(100ml
×
3)提取滤液。利用饱和碳酸氢钠水溶液(200ml)、饱和食盐水(200ml)对合并后的有机层进行清洗后,利用无水硫酸镁加以干燥,并在减压下浓缩。对于所获得的残渣,将氯仿:甲醇的混合溶剂用于洗脱液,一面使其比例在95:5~85:15的范围内变化,一面利用硅胶色谱法进行纯化,由此获得作为目标的二胺异构体混合物8[二胺化合物(1
‑3‑
8)及其对映体的混合物]的白色固体(产量1.19g、收率65%)。
[0804]1h
‑
nmr(400mhz,dmso
‑
d6):δ6.97(d,j=8.7hz,2h),6.67(d,j=2.6hz,2h),6.51(dd,j=8.7,2.6hz,2h),5.38(brs,4h),2.49
‑
2.45(m,2h),1.71
‑
1.68(m,2h).
[0805]
[合成例19]二硝基化合物10的合成
[0806]
[化163]
[0807][0808]
向反式
‑
1,2
‑
环丙烷二羧酸(1.75g、13.5mmol)中加入亚硫酰氯(9.0ml),在70℃下搅拌4小时后在减压下浓缩,由此蒸馏去除亚硫酰氯,获得粗生成的反式
‑
1,2
‑
环丙烷二羧酸氯化物。所述酸氯化物设为thf(27ml)溶液,全部用于以下的反应。
[0809]
在氩环境下,向3
‑
氯
‑4‑
硝基苯酚(5.01g、28.3mmol)的thf(30ml)溶液中加入三乙胺(6.50ml、47.2mmol)并进行冰浴冷却。历时5分钟向其中滴加所述制备的酸氯化物的thf溶液后,升温至室温并搅拌18小时。反应结束后,向反应混合物中加入水(100ml),过滤分离沉淀物,由此获得二硝基化合物10[反式
‑
1,2
‑
环丙烷二羧酸双(3
‑
氯
‑4‑
硝基苯基)酯]的淡黄色固体(产量3.48g、收率58%)。
[0810]1h
‑
nmr(400mhz,dmso
‑
d6):δ8.21(d,j=8.9hz,2h),7.83(d,j=2.4hz,2h),7.52(dd,j=8.9,2.4hz,2h),2.66
‑
2.62(m,2h),1.83
‑
1.80(m,2h).
[0811]
[合成例20]二胺异构体混合物9(二胺化合物(1
‑3‑
9)及其对映体的混合物)的合成
[0812]
[化164]
[0813][0814]
在氩环境下,向反式
‑
1,2
‑
环丙烷二羧酸双(3
‑
氯
‑4‑
硝基苯基)酯(3.43g、
7.77mmol)的乙酸乙酯(78ml)溶液中加入氯化锡(ii)二水合物(18.1g、77.7mmol),在加热回流下搅拌1小时。反应结束后冷却至室温,将反应混合物加入至饱和碳酸氢钠水溶液(200ml)中后,进行硅藻土过滤,利用乙酸乙酯(50ml
×
3)提取滤液。利用饱和碳酸氢钠水溶液(150ml)、饱和食盐水(150ml)对合并后的有机层进行清洗后,利用无水硫酸镁加以干燥,并在减压下浓缩。对于所获得的残渣,将己烷:乙酸乙酯=50:50的混合溶剂用于洗脱液,利用硅胶色谱法进行纯化后,利用甲醇(30ml)加以清洗,由此获得作为目标的二胺异构体混合物9[二胺化合物(1
‑3‑
9)及其对映体的混合物]的白色固体(产量2.09g、收率70%)。
[0815]1h
‑
nmr(400mhz,dmso
‑
d6):δ7.12(d,j=2.6hz,2h),6.87(dd,j=8.7,2.6hz,2h),6.78(d,j=8.7hz,2h),5.34(brs,4h),2.43
‑
2.39(m,2h),1.65
‑
1.61(m,2h).
[0816]
[合成例21]二硝基化合物11的合成
[0817]
[化165]
[0818][0819]
向反式
‑
1,2
‑
环丙烷二羧酸(2.022g、15.5mmol)中加入亚硫酰氯(10.4ml),在70℃下搅拌4小时后在减压下浓缩,由此蒸馏去除亚硫酰氯,获得粗生成的反式
‑
1,2
‑
环丙烷二羧酸氯化物。所述酸氯化物设为thf(31ml)溶液,全部用于以下的反应。
[0820]
在氩环境下,向2
‑
甲氧基
‑4‑
硝基苯酚(5.63g、32.6mmol)的thf(31ml)溶液中加入三乙胺(7.5ml、54.4mmol)并进行冰浴冷却。历时15分钟向所述溶液中滴加之前制备的酸氯化物的thf溶液后,升温至室温并搅拌16小时。反应结束后,向反应混合物中加入水(80ml),过滤分离沉淀物,由此获得二硝基化合物11[反式
‑
1,2
‑
环丙烷二羧酸双(2
‑
甲氧基
‑4‑
硝基苯基)酯]的白色固体(产量6.34g、收率94%)。
[0821]1h
‑
nmr(400mhz,dmso
‑
d6):δ7.95(d,j=2.6hz,2h),7.92(dd,j=8.6,2.6hz,2h),7.54(d,j=8.6hz,2h),3.95(s,6h),2.63
‑
2.59(m,2h),1.80
‑
1.76(m,2h).
[0822]
[合成例22]二胺异构体混合物10(二胺化合物(1
‑3‑
10)及其对映体的混合物)的合成
[0823]
[化166]
[0824][0825]
在氩环境下,向反式
‑
1,2
‑
环丙烷二羧酸双(2
‑
甲氧基
‑4‑
硝基苯基)酯(3.16g、7.30mmol)的乙酸乙酯(73ml)溶液中加入氯化锡(ii)二水合物(17.0g、73.0mmol),在加热回流下搅拌2小时。反应结束后冷却至室温,将反应混合物加入至饱和碳酸氢钠水溶液(300ml)中后,进行硅藻土过滤,利用乙酸乙酯(100ml
×
3)提取滤液。利用饱和碳酸氢钠水溶液(200ml)、饱和食盐水(200ml)对合并后的有机层进行清洗后,利用无水硫酸镁加以干燥,并在减压下浓缩。对于所获得的残渣,将氯仿:甲醇的混合溶剂用于洗脱液,一面使其比例在95:5~85:15的范围内变化,一面利用硅胶色谱法进行纯化,由此获得作为目标的二胺
异构体混合物10[二胺化合物(1
‑3‑
10)及其对映体的混合物]的白色固体(产量1.68g、收率62%)。
[0826]1h
‑
nmr(400mhz,dmso
‑
d6):δ6.74(d,j=8.5hz,2h),6.31(d,j=2.4hz,2h),6.09(dd,j=8.5,2.4hz,2h),5.08(brs,4h),3.67(s,6h),2.35
‑
2.32(m,2h),1.60
‑
1.57(m,2h).
[0827]
[合成例23]二硝基化合物12的合成
[0828]
[化167]
[0829][0830]
向反式
‑
1,2
‑
环丙烷二羧酸(2.27g、17.5mmol)中加入亚硫酰氯(11.6ml),在70℃下搅拌4小时后在减压下浓缩,由此蒸馏去除亚硫酰氯,获得粗生成的反式
‑
1,2
‑
环丙烷二羧酸氯化物。所述酸氯化物设为thf(35ml)溶液,全部用于以下的反应。
[0831]
在氩环境下,向3
‑
甲氧基
‑4‑
硝基苯酚(6.20g、36.7mmol)的thf(35ml)溶液中加入三乙胺(8.5ml、61.1mmol)并进行冰浴冷却。历时40分钟向所述溶液中滴加之前制备的酸氯化物的thf溶液后,升温至室温并搅拌18小时。反应结束后,向反应混合物中加入水(100ml),利用乙酸乙酯(50ml
×
3)进行提取。利用饱和食盐水(50ml
×
2)对合并后的有机层进行清洗后,利用无水硫酸镁加以干燥,并在减压下浓缩。对于所获得的残渣,将氯仿:甲醇=99:1的混合溶剂用于洗脱液,利用硅胶色谱法进行纯化,由此获得二硝基化合物12[反式
‑
1,2
‑
环丙烷二羧酸双(3
‑
甲氧基
‑4‑
硝基苯基)酯]的白色固体(产量1.94g、收率26%)。
[0832]1h
‑
nmr(400mhz,dmso
‑
d6):δ8.01(d,j=8.8hz,2h),7.33(d,j=2.3hz,2h),7.01(dd,j=8.8,2.3hz,2h),3.92(s,6h),2.64
‑
2.60(m,2h),1.82
‑
1.78(m,2h).
[0833]
[合成例24]二胺异构体混合物11(二胺化合物(1
‑3‑
11)及其对映体的混合物)的合成
[0834]
[化168]
[0835][0836]
在氩环境下,向反式
‑
1,2
‑
环丙烷二羧酸双(3
‑
甲氧基
‑4‑
硝基苯基)酯(1.90g、4.40mmol)的乙酸乙酯(44ml)溶液中加入氯化锡(ii)二水合物(10.2g、44.0mmol),在加热回流下搅拌1小时。反应结束后冷却至室温,将反应混合物加入至饱和碳酸氢钠水溶液(200ml)中后,进行硅藻土过滤,利用乙酸乙酯(100ml
×
3)提取滤液。利用饱和碳酸氢钠水溶液(100ml)、饱和食盐水(100ml)对合并后的有机层进行清洗后,利用无水硫酸镁加以干燥,并在减压下浓缩。对于所获得的残渣,将氯仿:甲醇=90:10的混合溶剂用于洗脱液,利用硅胶色谱法进行纯化,由此获得作为目标的二胺异构体混合物11[二胺化合物(1
‑3‑
11)及其对映体的混合物]的淡黄色固体(产量1.18g、收率72%)。
[0837]1h
‑
nmr(400mhz,dmso
‑
d6):δ6.68(d,j=2.4hz,2h),6.60(d,j=8.4hz,2h),6.49(dd,j=8.4,2.4hz,2h),4.68(brs,4h),3.74(s,6h),2.42
‑
2.38(m,2h),1.64
‑
1.61(m,2h).
[0838]
[合成例25]二硝基化合物13的合成
[0839]
[化169]
[0840][0841]
向反式
‑
1,2
‑
环丙烷二羧酸(2.04g、15.7mmol)中加入亚硫酰氯(10.5ml),在70℃下搅拌4小时后在减压下浓缩,由此蒸馏去除亚硫酰氯,获得粗生成的反式
‑
1,2
‑
环丙烷二羧酸氯化物。所述酸氯化物设为thf(30ml)溶液,全部用于以下的反应。
[0842]
在氩环境下,向3
‑
硝基苯酚(4.68g、33.0mmol)的thf(34ml)溶液中加入三乙胺(7.6ml、54.9mmol)并进行冰浴冷却。历时10分钟向所述溶液中滴加之前制备的酸氯化物的thf溶液后,升温至室温并搅拌25小时。反应结束后,向反应混合物中加入水(100ml),并在减压下浓缩。利用乙酸乙酯(100ml
×
3)提取残渣后,利用饱和氯化钠水溶液(100ml)加以清洗,利用无水硫酸镁将有机层干燥,并在减压下浓缩。对于所获得的残渣,将氯仿:甲醇的混合溶剂用于洗脱液,一面使其比例在95:5~85:15的范围内变化,一面利用硅胶色谱法进行纯化,由此获得二硝基化合物13[反式
‑
1,2
‑
环丙烷二羧酸双(3
‑
硝基苯基)酯]的黄色固体(产量4.27g、收率73%)。
[0843]1h
‑
nmr(400mhz,dmso
‑
d6):δ8.21
‑
8.16(m,4h),7.79
‑
7.72(m,4h),2.67
‑
2.63(m,2h),1.83
‑
1.80(m,2h).
[0844]
[合成例26]二胺异构体混合物12(二胺化合物(1
‑3‑
12)及其对映体的混合物)的合成
[0845]
[化170]
[0846][0847]
在氩环境下,向反式
‑
1,2
‑
环丙烷二羧酸双(3
‑
硝基苯基)酯(2.04g、5.47mmol)的乙酸乙酯(55ml)溶液中加入氯化锡(ii)二水合物(12.7g、54.7mmol),在加热回流下搅拌4小时。反应结束后冷却至室温,将反应混合物加入至饱和碳酸氢钠水溶液(200ml)中后,进行硅藻土过滤,利用乙酸乙酯(100ml
×
3)提取滤液。利用饱和碳酸氢钠水溶液(200ml)、饱和食盐水(200ml)对合并后的有机层进行清洗后,利用无水硫酸镁加以干燥,并在减压下浓缩。对于所获得的残渣,将氯仿:甲醇的混合溶剂用于洗脱液,一面使其比例在95:5~85:15的范围内变化,一面利用硅胶色谱法进行纯化,由此获得作为目标的二胺异构体混合物12[二胺化合物(1
‑3‑
12)及其对映体的混合物]的淡黄色油状物(产量1.34g、收率79%)。
[0848]1h
‑
nmr(400mhz,dmso
‑
d6):δ7.02(t,j=8.0hz,2h),6.44(ddd,j=8.0,2.2,0.8hz,2h),6.32(t,j=2.1hz,2h),6.27(ddd,j=8.0,2.2,0.8hz,2h),5.29(brs,4h),2.43
‑
2.39(m,2h),1.64
‑
1.60(m,2h).
[0849]
[合成例27]二胺异构体混合物13(二胺化合物(1
‑3‑
13)及其对映体的混合物)的合成
[0850]
[化171]
[0851][0852]
向反式
‑3‑
亚甲基
‑
1,2
‑
环丙烷二羧酸(3.20g、22.5mmol)的甲醇(48ml)溶液中加入浓硫酸(0.1ml),在40℃下搅拌4个半小时。通过在减压下浓缩而蒸馏去除溶剂后,加入水(100ml),利用乙酸乙酯(30ml
×
3)进行提取。利用饱和碳酸氢钠水溶液(50ml)与饱和氯化钠水溶液(50ml)对所获得的有机层进行清洗后,利用无水硫酸镁加以干燥,并在减压下浓缩,由此获得反式
‑3‑
亚甲基
‑
1,2
‑
环丙烷二甲酯的黄色油状物(产量3.74g、收率98%)。
[0853]1h
‑
nmr(400mhz,cdcl3):δ5.68(t,j=2.4hz,2h),3.72(s,6h),2.89(t,j=2.4h,2h).
[0854]
[化172]
[0855][0856]
向反式
‑3‑
亚甲基
‑
1,2
‑
环丙烷二甲酯(1.28g、9.02mmol)中加入肼一水合物(1.1ml、22.6mmol)、乙腈(75ml)。在氧环境下,一面照射低压水银灯(uvl
‑
20ph
‑
6)一面搅拌42小时。反应结束后,通过短柱色谱法(乙酸乙酯100ml)对反应液进行纯化,由此获得反式
‑3‑
甲基
‑
1,2
‑
环丙烷二甲酯的茶色油状物(产量1.20g、收率77%)。
[0857]1h
‑
nmr(400mhz,cdcl3):δ3.71(s,3h),3.69(s,3h),2.29(dd,j=9.6,4.6hz,1h),2.11(dd,j=5.6,4.6hz,1h),1.88
‑
1.79(m,1h),1.26(d,j=6.4hz,3h).
[0858]
[化173]
[0859][0860]
在冰浴冷却下,历时5分钟向反式
‑3‑
甲基
‑
1,2
‑
环丙烷二甲酯(1.20g、6.97mmol)的乙醇(14ml)溶液中滴加氢氧化钠(1.12g、27.9mmol)的水(14ml)溶液。反应结束后在减压下浓缩,由此蒸馏去除溶剂。在冰浴冷却下向残渣中加入浓盐酸(3.0ml)后,利用乙酸乙酯(30ml
×
3)进行提取。利用无水硫酸镁将合并后的有机层干燥,在减压下浓缩,由此获得反式
‑3‑
甲基
‑
1,2
‑
环丙烷二羧酸的淡黄色固体(产量0.91g、收率91%)。
[0861]1h
‑
nmr(400mhz,dmso
‑
d6):δ12.5(brs,2h),2.01(dd,j=9.6,4.6hz,1h),1.78(dd,j=5.8,4.6hz,1h),1.73
‑
1.65(m,1h),1.17(d,j=6.2hz,3h).
[0862]
[化174]
[0863][0864]
在氩环境下,将反式
‑3‑
甲基
‑
1,2
‑
环丙烷二羧酸(867mg、6.02mmol)与叔丁基n
‑
(4
‑
羟基苯基)氨基甲酸酯(2.64g、12.6mmol)溶解于二氯甲烷(60ml)并进行冰浴冷却。向所述中加入1
‑
(3
‑
二甲基氨基丙基)
‑3‑
乙基碳二酰亚胺盐酸盐(2.47g、12.6mmol)与4
‑
二甲基氨基吡啶(147mg、1.20mmol),升温至室温并搅拌64小时。反应结束后,加入水(100ml),利用氯仿(30ml
×
3)进行提取。利用无水硫酸镁将所获得的有机层干燥,并在减压下浓缩。利用甲醇(20ml)对残渣进行清洗,由此获得反式
‑3‑
甲基
‑
1,2
‑
环丙烷二羧酸二叔丁基n
‑
(4
‑
羟基苯基)酯的白色固体(产量2.33g、收率73%)。
[0865]1h
‑
nmr(400mhz,dmso
‑
d6):δ9.41(brs,2h),7.49
‑
7.45(m,4h),7.08
‑
7.05(m,4h),2.57(dd,j=9.7,4.6hz,1h),2.27(dd,j=5.9,4.6hz,1h),2.09(m,1h),1.48(s,18h),1.31(d,j=6.3hz,3h).
[0866]
[化175]
[0867][0868]
在冰浴冷却下,历时10分钟以上向反式
‑3‑
甲基
‑
1,2
‑
环丙烷二羧酸二叔丁基n
‑
(4
‑
羟基苯基)酯(2.27g、4.30mmol)的二氯甲烷(43ml)溶液中滴加三氟乙酸(8.4ml)后,升温至室温。反应结束后,在冰浴冷却下加入饱和碳酸氢钠水溶液(200ml),利用氯仿(50ml
×
3)进行提取。利用无水硫酸镁将合并后的有机层干燥,并在减压下浓缩,由此获得反式
‑3‑
甲基
‑
1,2
‑
环丙烷二羧酸二
‑4‑
氨基苯基酯的白色固体(产量1.13g、收率80%)。
[0869]1h
‑
nmr(400mhz,cdcl3):δ6.92
‑
6.88(m,4h),6.69
‑
6.64(m,4h),2.61(dd,j=9.7,4.6hz,1h),2.39(dd,j=5.9,4.6hz,1h),2.11
‑
2.03(m,1h),1.40(d,j=6.4hz,3h).1h
‑
nmr(400mhz,dmso
‑
d6):δ6.82
‑
6.77(m,4h),6.57
‑
6.52(m,4h),5.06(brs,4h),2.49
‑
2.47(m,1h),2.20(dd,j=5.9,4.6hz,1h),2.06
‑
1.97(m,1h),1.28(d,j=6.2hz,3h).
[0870]
反式
‑
1,2
‑
环丙烷二羧酸的合成
[0871]
二硝基化合物的合成中使用的反式
‑
1,2
‑
环丙烷二羧酸可通过下述合成例28~合成例31来合成。
[0872]
[合成例28]
[0873]
[化176]
[0874][0875]
将在dmf(30ml)中加入氢化钠(5.24g、120mmol)的混合溶液冷却至2℃后,历时45分钟滴加丙烯酸乙酯(10.0g、99.9mmol)与氯乙酸乙酯(12.2g、99.9mmol)的dmf(20ml)溶液。2小时后升温至室温,在所述状态下搅拌20小时。反应结束后,在冰浴冷却下,向反应混
合物中缓慢滴加5m盐酸(30ml)后,加入水(50ml)并搅拌,利用二乙醚(50ml
×
3)进行提取。利用饱和碳酸氢钠水溶液(50ml)、饱和食盐水(50ml
×
2)对合并后的有机层进行清洗后,利用硫酸镁加以干燥,并在减压下浓缩。所获得的残渣(12.1g)的反式体:顺式体为97:3。将所述残渣制成乙醇(200ml)溶液,总量用于以下的反应。
[0876]
在冰浴冷却下向通过之前的反应而获得的乙醇溶液中缓慢滴加氢氧化钠(16.0g、400mmol)的水(200ml)溶液。滴加结束后,将反应液慢慢升温至室温,搅拌15小时。反应结束后在减压下浓缩,由此蒸馏去除乙醇。利用己烷(150ml
×
3)对所获得的水层进行清洗后,在冰浴冷却下,向水层中滴加浓盐酸(40ml)。搅拌一会儿后,利用乙酸乙酯(50ml
×
3)进行提取。利用硫酸镁将合并后的有机层干燥,并在减压下浓缩。利用乙酸乙酯(40ml)、己烷(200ml)对所获得的粗产物进行清洗,由此获得反式
‑
1,2
‑
环丙烷二羧酸的白色固体(产量5.88g、收率45%)。
[0877]1h
‑
nmr(400mhz,dmso
‑
d6):δ12.6(brs,2h),1.91
‑
1.87(m,2h),1.29
‑
1.25(m,2h).
[0878]
[合成例29]
[0879]
将氢化钠(2.62g、59.9mmol)的dmf(10ml)溶液冷却至
‑
10℃,历时20分钟滴加丙烯酸乙酯(5.00g、49.9mmol)与氯乙酸乙酯(6.12g、49.9mmol)的dmf(15ml)溶液,搅拌24小时。在冰浴冷却下,向所述反应液中缓慢滴加5m盐酸(15ml),加入水(30ml)并搅拌后,利用二乙醚(50ml
×
3)进行提取。利用饱和碳酸氢钠水溶液(50ml)、饱和食盐水(50ml
×
2)对合并后的有机层进行清洗后,利用硫酸镁加以干燥,并在减压下浓缩。所获得的残渣(8.50g)的反式体:顺式体为98:2。将所述残渣制成乙醇(100ml)溶液,全部用于以下的反应。
[0880]
在冰浴冷却下向通过之前的反应而获得的乙醇溶液中缓慢滴加氢氧化钠(8.00g、200mmol)的水(100ml)溶液。滴加结束后,将反应液慢慢升温至室温,搅拌15小时。反应结束后在减压下浓缩,由此蒸馏去除乙醇。利用己烷(100ml
×
3)对所获得的水层进行清洗后,在冰浴冷却下,向水层中滴加浓盐酸(20ml)。搅拌一会儿后,利用乙酸乙酯(50ml
×
3)进行提取。利用硫酸镁将合并后的有机层干燥,并在减压下浓缩。利用乙酸乙酯(18ml)、己烷(30ml)对所获得的粗产物进行清洗,由此获得反式
‑
1,2
‑
环丙烷二羧酸的白色固体(产量3.08g、收率48%)。
[0881]1h
‑
nmr(400mhz,dmso
‑
d6):δ12.6(brs,2h),1.91
‑
1.87(m,2h),1.29
‑
1.25(m,2h).
[0882]
[合成例30]
[0883]
将在dmf(50ml)中加入氢化钠(4.30g、98.44mmol)的混合溶液冷却至2℃后,历时40分钟滴加丙烯酸乙酯(10.0g、99.9mmol)与氯乙酸乙酯(12.2g、99.9mmol、1.0eq.)。2小时后升温至室温,搅拌20小时。反应结束后,在冰浴冷却下,向所述反应混合物中缓慢滴加5m
‑
盐酸(30ml)后,加入水(50ml)并搅拌,利用二乙醚(50ml
×
3)进行提取。利用饱和碳酸氢钠水溶液(50ml)、饱和食盐水(50ml
×
2)对合并后的有机层进行清洗后,利用硫酸镁加以干燥,并在减压下浓缩。所获得的残渣(18.8g)的反式体与顺式体的比率为反式:顺式=85:15。将所述残渣制成乙醇(200ml)溶液,全部用于以下的反应。
[0884]
在冰浴冷却下向通过之前的反应而获得的乙醇溶液中缓慢滴加氢氧化钠(16.0g、400mmol)的水(200ml)溶液。滴加结束后,将反应液慢慢升温至室温,搅拌15小时。反应结束后在减压下浓缩,由此蒸馏去除乙醇。利用己烷(150ml
×
3)对所获得的水层进行清洗后,在冰浴冷却下,向水层中滴加浓盐酸(40ml)。搅拌一会儿后,利用乙酸乙酯(50ml
×
3)进行提
取。利用硫酸镁将合并后的有机层干燥,并在减压下浓缩。利用乙酸乙酯(48ml)、己烷(40ml)对所获得的粗产物进行清洗,由此获得反式
‑
1,2
‑
环丙烷二羧酸的白色固体(产量6.46g、收率50%)。
[0885]1h
‑
nmr(400mhz,dmso
‑
d6):δ12.6(brs,2h),1.91
‑
1.87(m,2h),1.29
‑
1.25(m,2h).
[0886]
[合成例31]
[0887]
将叔丁醇钠(11.8g、120mmol)的dmf(30ml)混合溶液冷却至2℃后,历时40分钟滴加丙烯酸乙酯(10.0g、99.9mmol)与氯乙酸乙酯(12.2g、99.9mmol)的dmf(20ml)溶液。2小时后升温至室温,在所述状态下搅拌20小时。反应结束后,在冰浴冷却下,向所述反应混合物中缓慢滴加5m盐酸(30ml)后,加入水(50ml)并搅拌,利用二乙醚(50ml
×
3)进行提取。利用饱和碳酸氢钠水溶液(50ml)、饱和食盐水(50ml
×
2)对合并后的有机层进行清洗后,利用硫酸镁加以干燥,并在减压下浓缩。所获得的残渣(17.8g)制成乙醇(200ml)溶液,全部用于以下的反应。
[0888]
在冰浴冷却下向通过之前的反应而获得的乙醇溶液中缓慢滴加氢氧化钠(16.0g、400mmol)与水(200ml)溶液。滴加结束后,将反应液慢慢升温至室温,搅拌15小时。反应结束后在减压下浓缩,由此蒸馏去除乙醇。在冰浴冷却下,向所获得的水层中滴加浓盐酸(40ml)。搅拌一会儿后,利用乙酸乙酯(50ml
×
3)进行提取。利用硫酸镁将合并后的有机层干燥,并在减压下浓缩。利用乙酸乙酯(22ml)、己烷(20ml)对所获得的粗产物进行清洗,由此获得反式
‑
1,2
‑
环丙烷二羧酸的白色固体(产量7.50g、收率58%)。
[0889]1h
‑
nmr(400mhz,dmso
‑
d6):δ12.6(brs,2h),1.91
‑
1.87(m,2h),1.29
‑
1.25(m,2h).
[0890]
测定法与评价法
[0891]
下述示出本实施例中使用的测定法与评价法。
[0892]
[重量平均分子量(mw)的测定]
[0893]
聚酰胺酸的重量平均分子量是通过以下方式来求出:使用2695分离模块
·
2414示差折射计(沃特世(waters)制造)利用gpc法测定,并进行聚苯乙烯换算。利用磷酸
‑
dmf混合溶液(磷酸/dmf=0.6/100:重量比),以聚酰胺酸浓度成为约2重量%的方式对所获得的聚酰胺酸进行稀释。管柱使用hspgel rt mb
‑
m(沃特世(waters)制造),将所述混合溶液作为展开剂,在管柱温度50℃、流速0.40ml/min的条件下进行测定。标准聚苯乙烯使用东曹(tosoh)(股)制造的tsk标准聚苯乙烯。
[0894]
[对比度的测定]
[0895]
测定所制作的液晶单元的亮度
‑
电压特性(b
‑
v特性),使用最小亮度与最大亮度的比来求出对比度(contrast ratio,cr)。cr的值越大,是指明暗显示越鲜明,对比度越良好,为3000以上时,可以说具有优异的对比度。
[0896]
cr=b
max
/b
min
[0897]
式中,b
max
表示b
‑
v特性中的最大亮度,b
min
表示b
‑
v特性中的最小亮度。
[0898]
[交流电(alternating current,ac)残像的测定]
[0899]
ac残像是依据国际公开2000/43833号小册子中记载的方法来测定。具体而言,测定所制作的液晶单元的亮度
‑
电压特性(b
‑
v特性),将其设为施加应力前的亮度
‑
电压特性:b(前(before))。其次,对液晶单元施加20分钟4.5v、60hz的交流电,然后短路1秒钟,再次测定亮度
‑
电压特性(b
‑
v特性)。将其设为施加应力后的亮度
‑
电压特性:b(后(after))。此处,
作为b(前(before))及b(后(after))的特性值,使用所测定的各亮度
‑
电压特性的电压1.3v下的亮度,并利用下述式来求出亮度变化率δb(%)。δb(%)的值越小,是指越可抑制ac残像的产生,即残像特性越良好。若δb未满3%,则评价为
“○”
,若为3%以上,则评价为
“×”
,若为
“○”
,则可以说残像特性良好。
[0900]
δb(%)={[b(后(after))
‑
b(前(before))]/b(前(before))}
×
100
[0901]
本实施例中使用的化合物
[0902]
[通式(1)所表示的二胺化合物]
[0903]
下述示出本实施例中用于清漆的制备的通式(1)所表示的二胺化合物。
[0904]
[化177]
[0905]
[0906][0907]
[其他二胺化合物]
[0908]
下述示出本实施例及比较例中用于清漆的制备的其他二胺化合物。这些中,化合物(di
‑5‑
32)、化合物(di
‑5‑
35)及化合物(di
‑6‑
8)为光反应性二胺化合物。关于下述式中的m,表1~表5中记载了值。
[0909]
[化178]
[0910][0911]
[四羧酸二酐]
[0912]
下述示出本实施例及比较例中用于清漆的制备的四羧酸二酐。关于下述式中的m,表1~表5中记载了值。
[0913]
[化179]
[0914][0915]
下述示出本实施例及比较例中用于清漆的制备的溶剂。
[0916]
nmp:n
‑
甲基
‑2‑
吡咯烷酮
[0917]
bc:丁基溶纤剂(乙二醇单丁醚)
[0918]
下述示出本实施例及比较例中用于清漆的制备的添加剂。
[0919]
ad.1:3
‑
氨基丙基三乙氧基硅烷
[0920]
ad.2:2
‑
(3,4
‑
环氧环己基)乙基三甲氧基硅烷
[0921]
ad.3:(3,3',4,4'
‑
二环氧基)双环己基
[0922]
ad.4:1,3
‑
双(4,5
‑
二氢
‑2‑
噁唑基)苯
[0923]
清漆的制备
[0924]
本实施例中使用的清漆是按照下述程序来制备。此处,清漆的制备例1~制备例7、及制备例21~制备例37中制备的清漆a1~清漆a7、及清漆a21~清漆a37是将二胺化合物(1)的至少一种用作二胺单体的聚酰胺酸的溶液,在清漆的制备例8~制备例10中制备的清漆a8~清漆a10是使用其他光反应性二胺化合物(di
‑5‑
32)、光反应性二胺化合物(di
‑5‑
35)、或光反应性二胺化合物(di
‑6‑
8)而合成的聚酰胺酸的溶液。清漆的制备例11~制备例13、及制备例41~制备例43中制备的清漆b1~清漆b6是在原料中不使用光反应性二胺化合物而合成的聚酰胺酸的溶液,且与清漆a1~清漆a10、清漆a21~清漆a37、及清漆c1~清漆c6掺合而使用。清漆的制备例14~制备例19中制备的清漆c1~清漆c6是不使用光反应性二胺化合物而合成的第一聚酰胺酸、与使用二胺化合物(1)而合成的第二聚酰胺酸的嵌段聚合物的溶液。
[0925]
[清漆的制备例1]清漆a1的制备
[0926]
在安装有搅拌翼、氮气导入管的100ml三口烧瓶中放入二胺异构体混合物1(0.883g),加入nmp(10.0g)并加以搅拌。向所述溶液中加入四羧酸二酐(an
‑3‑
2)(0.617g)
与nmp(2.5g),在室温下搅拌12小时。向其中加入nmp(6.0g)及bc(5.0g),在80℃下对所述溶液进行加热搅拌,直至作为溶质的聚合物的重量平均分子量成为目标重量平均分子量为止,从而获得溶质的重量平均分子量为约18,000且树脂成分浓度为6重量%的清漆a1。
[0927]
[清漆的制备例2~制备例13、制备例21~制备例37]清漆a2~清漆a10、清漆a21~清漆a37、清漆b1~清漆b6的制备
[0928]
除如表1~表3所示般变更用作二胺类及四羧酸二酐类的化合物以外,与制备例1同样地制备聚合物浓度为6重量%的清漆a2~清漆a10、及清漆a21~清漆a37。另外,除如表4所示般变更用作二胺类及四羧酸二酐类的化合物以外,与制备例1同样地制备清漆b1~清漆b6。清漆b1~清漆b6中,调整加热搅拌的条件,以使聚合物的重量平均分子量成为50,000左右。将所生成的聚合物的重量平均分子量(mw)示于表1~表4中。再者,表1~表4中,关于作为二胺类记载有两种以上的化合物的制备例,是指将所述所有的化合物合并用作二胺类,关于作为四羧酸二酐类记载有两种以上的化合物的制备例,是指将所述所有的化合物合并用作四羧酸二酐类。方括号内的数值表示调配比(摩尔%),空栏是指不使用与所述栏对应的化合物。下述表5中也同样。
[0929]
[表1]
[0930][0931]
[表2]
[0932][0933]
[表3]
[0934][0935]
[表4]
[0936][0937]
[清漆的制备例14]清漆c1的制备
[0938]
本制备例中,进行两阶段的聚合工序来合成聚酰胺酸的嵌段聚合物。
[0939]
(1)第一阶段的聚合工序
[0940]
在安装有搅拌翼、氮气导入管的200ml的三口烧瓶中加入二胺化合物(di
‑4‑
1)(0.408g)、二胺化合物(di
‑
13
‑
1)(1.011g)、及nmp(20.0g)并加以搅拌。向所述溶液中放入四羧酸二酐(an
‑4‑
21)(1.17g)、四羧酸二酐(an
‑1‑
1)(0.747g)、及nmp(10.0g),在室温下持续搅拌6小时,获得第一聚酰胺酸的溶液。
[0941]
(2)第二阶段的聚合工序
[0942]
在进行了第一阶段的聚合的烧瓶中放入二胺异构体混合物1(1.57g)、四羧酸二酐(an
‑3‑
2)(1.10g)、以及nmp(34.0g),在室温下持续搅拌24小时,获得第一聚酰胺酸与第二聚酰胺酸的混合溶液。向所述反应溶液中加入bc(30.0g),一面加热至60℃,一面进行8小时搅拌,获得聚合物固体成分浓度为6重量%的聚酰胺酸嵌段聚合物溶液。将所述聚酰胺酸嵌段聚合物溶液设为清漆c1。
[0943]
[清漆的制备例15~制备例19]清漆c2~清漆c6的制备
[0944]
除如表5所示般变更用作二胺类及四羧酸二酐类的化合物以外,与制备例14同样地制备树脂成分浓度为6重量%的清漆c2~清漆c6。
[0945]
[表5]
[0946][0947]
[实施例1]
[0948]
<液晶取向剂的制备及对比度的测定>
[0949]
利用nmp/bc混合溶液(nmp/bc=7/3重量比)将清漆a1以成为4重量%的方式进行稀释、搅拌,从而制备液晶取向剂1。
[0950]
通过旋转器法将液晶取向剂1涂布于带ffs电极的玻璃基板及带柱间隔物(column spacer)的玻璃基板。在涂布后,将基板在60℃下加热80秒钟,使溶剂蒸发,然后使用牛尾电机(股)制造的姆奇莱特(multi
‑
light)ml
‑
501c/b,自相对于基板而铅垂的方向经由偏光板来照射紫外线的直线偏光。此时的曝光能量是使用牛尾电机(股)制造的紫外线累计光量计uit
‑
150(光接收器:uvd
‑
s254)来测定光量,以在波长254nm下成为1.0j/cm2的方式调整曝光时间。之后,在220℃下进行30分钟煅烧处理,从而形成膜厚约100nm的取向膜。
[0951]
继而,将这些形成有取向膜的两片基板以使形成有液晶取向膜的面相向、且在相向的液晶取向膜之间设置用以注入液晶组合物的空隙的方式加以贴合。此时,使对各个液晶取向膜照射的直线偏光的偏光方向平行。在这些单元中注入正型液晶组合物a,制作单元厚度5μm的液晶单元(液晶显示元件)。
[0952]
<正型液晶组合物a>
[0953]
[化180]
[0954][0955]
(物性值)
[0956]
相转变温度ni:100.1℃、介电常数各向异性δε:5.1、折射率各向异性δn:0.093、粘度η:25.6mpa
·
s.
[0957]
使用所制成的液晶单元,如所述记载般进行对比度的测定。其结果,对比度为
3800。
[0958]
[实施例2]~[实施例17]、[实施例21]~[实施例62]、[比较例1]~[比较例3]
[0959]
除使用表6~表7所示的清漆代替清漆a1以外,与实施例1同样地制备液晶取向剂2~液晶取向剂17、液晶取向剂21~液晶取向剂62、及比较液晶取向剂1~比较液晶取向剂3。再者,在表6~表7中,在记载有两种以上清漆的制备例中,将所述所有的清漆按照表6~表7所示的调配比(重量比)进行混合,制备液晶取向剂。另外,在液晶取向剂8~液晶取向剂17、液晶取向剂38~液晶取向剂40、液晶取向剂50、液晶取向剂51、液晶取向剂54、及液晶取向剂57中,相对于清漆中的聚合物重量,以表6~表7所示的重量份加入表6~表7所示的添加剂。使用所制备的各液晶取向剂,与实施例1同样地制作带液晶取向膜的基板,并对组装有所述基板的液晶单元进行了对比度的测定。其中,液晶取向膜形成时的紫外线的照射条件以表6~表7所示的曝光量进行。将各实施例中使用的液晶取向剂与对比度的评价结果示于表6~表7。
[0960]
[表6]
[0961][0962]
[表7]
[0963][0964]
如表6~表7所示,液晶取向膜中使用了二胺化合物(1)的聚合物的实施例1~实施例17、及实施例21~实施例62的液晶单元中对比度均为3300以上,是对比度较使用了二胺化合物(1)以外的光反应性二胺化合物即化合物(di
‑5‑
32)的聚合物的比较例1、使用了化合物(di
‑5‑
35)的聚合物的比较例2、及使用了化合物(di
‑6‑
8)的聚合物的比较例3的液晶单元而言更高的值。由此可知,源于二胺化合物(1)的结构单元较源于其他光反应性二胺化合物的结构单元而言更有效果地有助于赋予膜的取向性。
[0965]
[实施例80]
[0966]
<ac残像的测定>
[0967]
利用使用液晶取向剂23而制作的实施例23的液晶单元,如所述记载般进行了ac残像的评价。其结果,δb为1.8%,因此评价为
“○”
。
[0968]
[实施例81]~[实施例87]、[比较例4]
[0969]
利用使用表8所示的液晶取向剂代替液晶取向剂23的液晶单元、即实施例24~实施例26、实施例21、实施例29、实施例48、实施例49、及比较例1的液晶单元,与实施例80同样地进行了ac残像的评价。将各实施例中使用的液晶取向剂与液晶取向膜的形成条件、ac残像的评价结果示于表8。
[0970]
[表8]
[0971][0972]
如表8所示,液晶取向膜中使用了二胺化合物(1)的聚合物的实施例80~实施例87的液晶单元中ac残像的评价均为
“○”
,较使用了二胺化合物(1)以外的光反应性二胺化合物即化合物(di
‑5‑
32)的聚合物的比较例4的液晶单元而言ac残像更优异。由此可知,较源于其他光反应性二胺化合物的结构单元而言,源于二胺化合物(1)的结构单元可制作显示出更优异的ac残像的液晶单元。
[0973]
[产业上的可利用性]
[0974]
通过将使用本发明的二胺化合物而合成的聚合物用于液晶取向剂,实现液晶取向性高的液晶取向膜。而且,通过使用所述液晶取向膜,可提供对比度高、可以各种利用形态使用的液晶显示元件。因此,本发明的产业上的可利用性高。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1