新型全人源抗人B7H3抗体、包含所述抗体的组合物及其应用
antitumor activity.clin cancer res.2012 jul 15;18(14):3834
‑
45.;ahmed m,cheng m,zhao q,et al.humanized affinity
‑
matured monoclonal antibody 8h9 has potent antitumor activity and binds to fg loop of tumor antigen b7
‑
h3[j].journal of biological chemistry,2015,290(50):30018
‑
30029.),虽然已有抗b7h3抗体的相关报道,但均是鼠源或人源化改造的鼠源抗体,目前本领域仍然亟需靶向b7h3的新型全人源抗体及靶向并杀伤表达b7h3的肿瘤细胞的治疗剂。
技术实现要素:
[0005]
鉴于此,本发明的目的在于提供一种新型的全人源抗人b7h3抗体、包含所述抗体的组合物及其应用。
[0006]
为了实现上述目的,本发明采用了如下技术方案:
[0007]
本发明的第一方面提供了一种分离的全人源单克隆抗体或其抗原结合片段。
[0008]
进一步,所述抗体或其抗原结合片段与b7h3特异性地结合;
[0009]
优选地,所述抗体或其抗原结合片段包含hcvr、lcvr;
[0010]
更优选地,所述hcvr包含hcdr1、hcdr2、hcdr3;
[0011]
更优选地,所述lcvr包含lcdr1、lcdr2、lcdr3;
[0012]
最优选地,所述hcdr1含有seq id no:1所述的氨基酸序列或与seq id no:1具有至少95%、至少96%、至少97%、至少98%、至少99%同一性的氨基酸序列;
[0013]
最优选地,所述hcdr2含有seq id no:2所述的氨基酸序列或与seq id no:2具有至少95%、至少96%、至少97%、至少98%、至少99%同一性的氨基酸序列;
[0014]
最优选地,所述hcdr3含有seq id no:3所述的氨基酸序列或与seq id no:3具有至少95%、至少96%、至少97%、至少98%、至少99%同一性的氨基酸序列;
[0015]
最优选地,所述lcdr1含有seq id no:6所述的氨基酸序列或与seq id no:6具有至少95%、至少96%、至少97%、至少98%、至少99%同一性的氨基酸序列;
[0016]
最优选地,所述lcdr2含有seq id no:7所述的氨基酸序列或与seq id no:7具有至少95%、至少96%、至少97%、至少98%、至少99%同一性的氨基酸序列;
[0017]
最优选地,所述lcdr3含有seq id no:8所述的氨基酸序列或与seq id no:8具有至少95%、至少96%、至少97%、至少98%、至少99%同一性的氨基酸序列;
[0018]
最优选地,所述抗体或其抗原结合片段hcvr的氨基酸序列如seq id no:4所示;
[0019]
最优选地,所述抗体或其抗原结合片段lcvr的氨基酸序列如seq id no:9所示;
[0020]
最优选地,所述抗体或其抗原结合片段的氨基酸序列如seq id no:13所示。
[0021]
进一步,所述抗体或其抗原结合片段hcvr的核苷酸序列如seq id no:5所示。
[0022]
进一步,所述抗体或其抗原结合片段lcvr的核苷酸序列如seq id no:10所示。
[0023]
进一步,所述全人源单克隆抗体或其抗原结合片段还包含连接hcvr和lcvr的linker;
[0024]
优选地,所述linker为g4s短肽;
[0025]
更优选地,所述g4s短肽的氨基酸序列如seq id no:11所示;
[0026]
更优选地,所述g4s短肽的氨基酸序列如seq id no:12所示。
[0027]
进一步,所述抗体或抗原结合片段的核苷酸序列如seq id no:14所示。
[0028]
本发明的第二方面提供了一种药物组合物。
[0029]
进一步,所述药物组合物包含有效量的本发明第一方面所述的抗体或其抗原结合片段;
[0030]
优选地,所述药物组合物还包含一种或多种药学上可接受的赋形剂;
[0031]
优选地,所述药物组合物用于治疗卵巢癌、肾癌、肺癌、乳腺癌、结直肠癌、食管癌、前列腺癌、口腔癌、胃癌、胰腺癌、子宫内膜癌、肝癌、膀胱癌、骨肉瘤、急性髓系白血病;
[0032]
更优选地,所述药物组合物可与第二治疗剂联用;
[0033]
最优选地,所述药物组合物与第二治疗剂联用用于增强治疗效果;
[0034]
最优选地,所述第二治疗剂包括瑞戈非尼、甲苯磺酸索拉非尼、曲妥珠单抗、甲磺酸阿帕替尼、甲磺酸伊马替尼、维莫非尼、依维莫司、培唑帕尼、西达本胺、沙利度胺、芦可替尼、硼替佐米、西妥昔单抗、贝伐珠单抗、达沙替尼、尼洛替尼、利妥昔单抗、伊布替尼、曲妥珠单抗、甲苯磺酸拉帕替尼、尼妥珠单抗、甲苯磺酸索拉非尼。
[0035]
进一步,所述有效量的本发明第一方面所述的抗体或其抗原结合片段是指作为单次剂量或者根据多次剂量方案单独或与缓解不利疾患的其他物质联合使用,足以清除患者受治疗区域中b7h3阳性细胞但在毒理学上耐受的抗体量。
[0036]
进一步,所述患者包括人类、非人类动物,其中,非人类动物包括兔、大鼠、小鼠、猴或其他低等灵长类。
[0037]
本发明的第三方面提供了一种抗体
‑
药物偶联物。
[0038]
进一步,所述抗体
‑
药物偶联物包含本发明第一方面所述的抗体或其抗原结合片段;
[0039]
优选地,所述抗体
‑
药物偶联物还包括小分子药物;
[0040]
更优选地,所述抗体
‑
药物偶联物是通过本发明第一方面所述的抗体或其抗原结合片段共价附着至小分子药物上得以形成的;
[0041]
更优选地,所述小分子药物包括烷化剂、抗代谢物、抗肿瘤抗生素、有丝分裂抑制剂、染色质功能抑制剂、抗血管生成剂、抗雌激素、抗雄激素、免疫调节剂;
[0042]
最优选地,所述烷化剂包括双氯乙基甲胺、苯丁酸氮芥、苯丙氨酸氮芥、溴丙哌嗪、松龙苯芥、磷雌氮芥、环磷酰胺、六甲密胺、氯乙环磷酰胺、异磷酰胺、三胺硫磷、卡氮芥、链唑霉素、福替目丁、环己亚硝脲、白消安、苏消安、英丙舒凡、氮烯咪胺、顺铂、奥沙利铂、卡铂;
[0043]
最优选地,所述抗代谢物包括甲氨喋呤、5
‑
氟脲嘧啶、氟苷、5
‑
氟脱氧尿嘧啶、卡培他滨、阿糖胞苷、氟达拉滨、阿糖胞苷、6
‑
巯基嘌呤(6
‑
mp)、6
‑
巯基鸟嘌呤(6
‑
tg)、2
‑
氯脱氧腺苷、5
‑
氮杂胞苷、2,2
‑
二氟脱氧胞嘧啶核苷、克拉屈滨、脱氧柯福霉素、喷司他丁;
[0044]
最优选地,所述抗肿瘤抗生素包括阿霉素、柔红霉素、去甲氧正定霉素、戊柔比星、盐酸米托蒽醌、更生霉素、光辉霉素、光神霉素、丝裂霉素c、博来霉素、甲基苄肼;
[0045]
最优选地,所述有丝分裂抑制剂包括紫杉醇、紫杉萜、长春碱、长春新碱、长春酰胺、长春瑞滨;
[0046]
最优选地,所述染色质功能抑制剂包括托泊替康、依立替康、依托扑沙、磷酸依托扑沙、鬼臼噻吩甙;
[0047]
最优选地,所述抗血管生成剂包括丙亚胺、马马司他、巴马司他、普啉司他、坦诺司
他、伊洛马司他、cgs
‑
27023a、溴氯哌喹酮、col
‑
3、新伐司他、bms
‑
275291、沙立度胺;
[0048]
最优选地,所述抗雌激素包括它莫西芬、托瑞米芬、雷洛昔芬、屈洛昔芬、奥多昔芬、阿纳托唑、来曲唑、依西美坦;
[0049]
最优选地,所述抗雄激素包括氟他米特、尼鲁米特、比卡鲁胺、安体舒通、醋酸环丙氯地孕酮、非那司提、西咪替丁;
[0050]
最优选地,所述免疫调节剂包括干扰素、白介素、肿瘤坏死因子、蘑菇多糖、西佐糖、罗喹美克、匹多莫特、甲氧聚乙二醇琥珀酰胺腺甙脱氨酶、胸腺肽制剂。
[0051]
本发明的第四方面提供了一种分离的多核苷酸分子。
[0052]
进一步,所述多核苷酸分子包括编码本发明第一方面所述抗体或其抗原结合片段的hcvr的核苷酸序列、编码本发明第一方面所述抗体或其抗原结合片段的lcvr的核苷酸序列;
[0053]
优选地,所述多核苷酸分子的核苷酸序列如seq id no:5所示;
[0054]
优选地,所述多核苷酸分子的核苷酸序列如seq id no:10所示;
[0055]
优选地,所述多核苷酸分子的核苷酸序列如seq id no:14所示。
[0056]
本发明的第五方面提供了一种表达载体。
[0057]
进一步,所述表达载体包含本发明第四方面所述的多核苷酸分子;
[0058]
优选地,所述载体包括质粒、病毒来源的载体;
[0059]
更优选地,所述病毒来源的载体包括慢病毒载体、逆转录病毒载体、腺病毒载体、腺相关病毒载体。
[0060]
本发明的第六方面提供了一种宿主细胞。
[0061]
进一步,所述宿主细胞包含本发明第五方面所述的表达载体;
[0062]
优选地,所述宿主细胞包括原核细胞、真核细胞;
[0063]
更优选地,所述原核细胞包括细菌、放线菌、蓝细菌、支原体、衣原体、立克次氏体;
[0064]
最优选地,所述细菌包括大肠杆菌、枯草杆菌、鼠伤寒沙门氏菌、假单胞菌属、链霉菌、葡萄球菌;
[0065]
更优选地,所述真核细胞包括哺乳动物细胞、昆虫细胞、植物细胞、酵母细胞。
[0066]
本发明第七方面提供了一种宿主细胞群体。
[0067]
进一步,所述宿主细胞群体包含本发明第六方面所述的宿主细胞;
[0068]
优选地,所述宿主细胞群体还包含不包含本发明第五方面所述的表达载体的宿主细胞;
[0069]
更优选地,所述宿主细胞包括原核细胞、真核细胞;
[0070]
最优选地,所述原核细胞包括细菌、放线菌、蓝细菌、支原体、衣原体、立克次氏体;
[0071]
最优选地,所述细菌包括大肠杆菌、枯草杆菌、鼠伤寒沙门氏菌、假单胞菌属、链霉菌、葡萄球菌;
[0072]
最优选地,所述真核细胞包括哺乳动物细胞、昆虫细胞、植物细胞、酵母细胞。
[0073]
本发明的第八方面提供了一种试剂盒。
[0074]
进一步,所述试剂盒包含本发明第一方面所述的抗体或其抗原结合片段、本发明第四方面所述的多核苷酸分子、本发明第五方面所述的表达载体、本发明第六方面所述的宿主细胞、本发明第七方面所述的宿主细胞群体。
[0075]
本发明的第九方面提供了如下任一种方法:
[0076]
(1)一种生产本发明第一方面所述的抗体或其抗原结合片段的方法,其特征在于,所述方法包括如下步骤:培养本发明第六方面所述的宿主细胞或本发明第七方面所述的宿主细胞群体,从培养物中分离出本发明第一方面所述的抗体或其抗原结合片段;
[0077]
(2)一种非诊断和非治疗目的地检测待测样品中b7h3的方法,其特征在于,所述方法包括如下步骤:将待测样品与本发明第一方面所述的抗体或其抗原结合片段接触,检测所述抗体或其抗原结合片段与b7h3的复合物的形成;
[0078]
优选地,所述抗体或其抗原结合片段是被可用于检测的标记物标记的抗体或其抗原结合片段;
[0079]
更优选地,所述可用于检测的标记物包括荧光色素、亲和素、顺磁原子、放射性同位素;
[0080]
最优选地,所述荧光色素为荧光素、罗丹明、texas红、藻红蛋白、藻蓝蛋白、别藻蓝蛋白、多甲藻黄素
‑
叶绿素蛋白;
[0081]
最优选地,所述亲和素为生物素、卵白亲和素、链亲和素、卵黄亲和素、类亲和素;
[0082]
最优选地,所述放射性同位素为放射性碘、放射性铯、放射性铱、放射性钴;
[0083]
(3)一种制备本发明第六方面所述的宿主细胞的方法,其特征在于,所述方法包括如下步骤:将本发明第五方面所述的表达载体导入到宿主细胞中;
[0084]
优选地,所述导入的方式包括磷酸钙转染、deae、右旋糖介导的转染、电穿孔、噬菌体感染;
[0085]
(4)一种特异性地抑制b7h3活性的方法,其特征在于,所述方法包括如下步骤:将本发明第四方面所述的多核苷酸分子导入到生物体细胞中,通过表达本发明第一方面所述的抗体或其抗原结合片段抑制b7h3的活性。
[0086]
本发明还提供了一种诊断受试者是否患有表达b7h3的癌症的方法。
[0087]
进一步,所述方法包括如下步骤:使用本发明第一方面所述的抗体或其抗原结合片段检测b7h3在来自所述受试者的样品中的量;
[0088]
优选地,所述方法还包括:将所述b7h3在来自所述受试者的样品中的量与其在已知标准品或参照样品中的量进行比较,并确定来自所述受试者的样品的b7h3的水平是否落入与癌症相关的b7h3的水平内;
[0089]
更优选地,所述样品可选自:尿液、血液、血清、血浆、唾液、腹水、循环肿瘤细胞、非组织缔合的细胞、组织、组织学制备物。
[0090]
本发明还提供了一种治疗患有表达b7h3的癌症的受试者的方法。
[0091]
进一步,所述方法包括给有需要的受试者施用本发明第二方面所述的药物组合物、本发明第三方面所述的抗体
‑
药物偶联物。
[0092]
本发明的第十方面提供了如下任一方面的应用:
[0093]
(1)本发明第一方面所述的抗体或其抗原结合片段、本发明第四方面所述的多核苷酸分子、本发明第五方面所述的表达载体、本发明第六方面所述的宿主细胞、本发明第七方面所述的宿主细胞群体在制备用于预防和/或治疗肿瘤的药物中的应用;
[0094]
(2)本发明第一方面所述的抗体或其抗原结合片段、本发明第四方面所述的多核苷酸分子、本发明第五方面所述的表达载体、本发明第六方面所述的宿主细胞、本发明第七
方面所述的宿主细胞群体在制备用于预防和/或治疗肿瘤的抗体
‑
药物偶联物中的应用;
[0095]
(3)本发明第一方面所述的抗体或其抗原结合片段、本发明第四方面所述的多核苷酸分子、本发明第五方面所述的表达载体、本发明第六方面所述的宿主细胞、本发明第七方面所述的宿主细胞群体在制备用于检测待测样品中的b7h3和/或诊断受试者是否患有肿瘤的试剂盒中的应用;
[0096]
(4)本发明第二方面所述的药物组合物在预防和/或治疗肿瘤的药物中的应用;
[0097]
(5)本发明第三方面所述的抗体
‑
药物偶联物在预防和/或治疗肿瘤的药物中的应用;
[0098]
(6)本发明第八方面所述的试剂盒在检测待测样品中的b7h3和/或诊断受试者是否患有肿瘤中的应用;
[0099]
(7)本发明第一方面所述的抗体或其抗原结合片段在制备多核苷酸分子、表达载体、宿主细胞、宿主细胞群体中的应用;
[0100]
(8)本发明第四方面所述的多核苷酸分子在制备表达载体、宿主细胞、宿主细胞群体中的应用;
[0101]
(9)本发明第五方面所述的表达载体在制备宿主细胞、宿主细胞群体中的应用;
[0102]
(10)本发明第六方面所述的宿主细胞在制备宿主细胞群体中的应用;
[0103]
优选地,所述肿瘤为表达b7h3的肿瘤;
[0104]
更优选地,所述肿瘤包括卵巢癌、肾癌、肺癌、乳腺癌、结直肠癌、食管癌、前列腺癌、口腔癌、胃癌、胰腺癌、子宫内膜癌、肝癌、膀胱癌、骨肉瘤、急性髓系白血病;
[0105]
优选地,所述多核苷酸分子为本发明第四方面所述的多核苷酸分子;
[0106]
优选地,所述表达载体为本发明第五方面所述的表达载体;
[0107]
优选地,所述宿主细胞为本发明第六方面所述的宿主细胞;
[0108]
优选地,所述宿主细胞群体为本发明第七方面所述的宿主细胞群体。
[0109]
本发明的优点和有益效果如下:
[0110]
本发明提供了一种新型全人源抗人b7h3抗体、以及包含所述抗体的药物组合物和抗体
‑
药物偶联物、编码所述抗体的多核苷酸分子、包含所述多核苷酸分子的表达载体、包含所述表达载体的宿主细胞和宿主细胞群体,本发明提供的全人源抗人b7h3抗体检测b7h3的灵敏度高、与b7h3的亲和力高、特异性强,为抗肿瘤药物的开发、抗肿瘤治疗、肿瘤机制的研究等奠定了基础。
附图说明
[0111]
以下,结合附图来详细说明本发明的实施方案,其中:
[0112]
图1显示筛选特异性结合抗体的噬菌体克隆富集结果统计图;
[0113]
图2显示利用elisa检测b7h3
‑
02单克隆噬菌体识别并结合b7h3靶抗原的显色反应结果图;
[0114]
图3显示利用elisa检测b7h3
‑
02单克隆噬菌体识别并结合b7h3靶抗原的显色反应数据统计图;
[0115]
图4显示利用dna电泳检测pcr扩增b7h3
‑
02 scfv及其原核表达载体鉴定结果图,其中,a图:b7h3
‑
02 scfv,b图:pet22b
‑
b7h3
‑
02 scfv;
[0116]
图5显示原核表达b7h3
‑
02 scfv蛋白纯化结果图;
[0117]
图6显示利用elisa检测纯化的b7h3
‑
02 scfv蛋白识别b7h3靶抗原能力的显色反应结果图;
[0118]
图7显示利用elisa检测纯化的b7h3
‑
02 scfv蛋白识别b7h3靶抗原能力的显色反应数据统计图;
[0119]
图8显示利用biacore检测纯化的b7h3
‑
02抗体与b7h3靶抗原的结合常数与解离常数结果图,其中,a图:结果图,b图:结果统计图;
[0120]
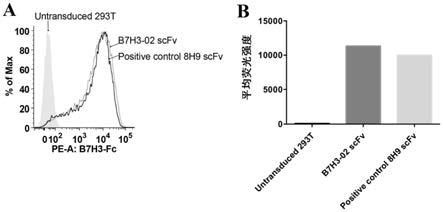
图9显示流式细胞术检测真核细胞表面表达的b7h3
‑
02 scfv结合b7h3靶抗原的能力的结果图及平均荧光强度统计图,其中,a图:流式细胞术检测结果图,b图:平均荧光强度统计图。
具体实施方式
[0121]
下面结合具体实施例,进一步阐述本发明,仅用于解释本发明,而不能理解为对本发明的限制。本领域的普通技术人员可以理解为:在不脱离本发明的原理和宗旨的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由权利要求及其等同物限定。下列实施例中未注明具体条件的实验方法,通常按照常规条件或按照厂商所建议的条件实施检测。
[0122]
实施例1全人源b7h3单链抗体(b7h3 scfv)的筛选
[0123]
1、实验条件设置
[0124]
分别设置实验组、对照组1、对照组2,所述各组的实验条件分别如下:
[0125]
实验组:b7h3抗原+b7h3
‑
phage
[0126]
对照组1:其它无biotin抗原(prps1)+b7h3
‑
phage
[0127]
对照组2:无抗原+b7h3
‑
phage
[0128]
2、实验方法
[0129]
经过四轮筛选富集特异性结合抗体序列,每一轮中改变投入噬菌体总量、加入抗原量、反应时间等条件;
[0130]
最终结果通过计算实验组对照组每100μl中0.1m hcl(ph=2.0)洗脱液中含有的具有感染能力的噬菌体个数,判断富集情况。
[0131]
3、实验结果
[0132]
(1)筛选结果分析:实验结果分别见表1和图1,结果显示,第三轮筛选出现富集,实验组洗脱下来的phage个数(抗原抗体特异性结合)与对照组(抗原抗体之间非特异性结合,或者无亲和力的)比值接近10倍;在第四轮改变实验条件后,实验组和对照组依然保持10倍差距,表明筛选得到的phage有与b7h3目的蛋白具有亲和力的scfv;
[0133]
(2)scfv序列分析:挑选24个单克隆测序,其中13条完整表达scfv序列,富集序列:
[0134]
克隆02(克隆b7h3
‑
02):vh:ighv3
‑
23*01/ighv3
‑
23d*01、ighj4*02/ighj4*0303;vk:igkv1
‑
39*01/igkv1d
‑
39*01、ikj1*01;
[0135]
经测序,克隆02的scfv氨基酸序列如seq id no:13所示;
[0136]
其中,克隆02的重链可变区(hcvr)的hcdr1的氨基酸序列如seq id no:1所示,hcdr2的氨基酸序列如seq id no:2所示,hcdr3的氨基酸序列如seq id no:3所示,hcvr的
氨基酸序列如seq id no:4所示,hcvr的核苷酸序列如seq id no:5所示,克隆02的轻链可变区(lcvr)的lcdr1的氨基酸序列如seq id no:6所示,lcdr2的氨基酸序列如seq id no:7所示,lcdr3的氨基酸序列如seq id no:8所示,lcvr的氨基酸序列如seq id no:9所示,lcvr的核苷酸序列如seq id no:10所示,克隆02的linker的氨基酸序列如seq id no:11所示,核苷酸序列如seq id no:12所示,克隆02的核苷酸序列seq id no:14所示。
[0137]
表1筛选结果
[0138][0139][0140]
实施例2全人源b7h3 scfv的结合靶抗原能力的检测
[0141]
1、检测条件设置
[0142]
实验组:b7h3抗原+phage
[0143]
阴性对照组:bcma抗原及phage scfv
‑
bcma
[0144]
阴性对照组1:其它无biotin抗原(prps1)+phage
[0145]
阴性对照组2:无抗原+phage
[0146]
2、实验方案
[0147]
分别制备单克隆phage,b7h3
‑
02,通过elisa实验显色反应和od值初步判断其与靶抗原是否有亲和力。
[0148]
3、实验步骤
[0149]
每组实验孔及对照孔中加入等量抗原包被,其后加入等量phage,孵育之后,多次清洗去除未结合的phage,加入phage检测抗体和二抗后,进行tmb显色,酶标仪测od
450nm
读数。
[0150]
4、实验结果
[0151]
实验结果分别见表2、图2和图3,通过elisa显色反应的结果图和od
450nm
读值可看出克隆b7h3
‑
02能识别并结合b7h3靶抗原。
[0152]
表2 b7h3
‑
02统计结果
[0153][0154]
实施例3全人源b7h3 scfv识别靶抗原能力的验证
[0155]
一、实验一
[0156]
1、scfv抗体表达纯化
[0157]
利用pet
‑
22b构建b7h3
‑
02 scfv抗体表达载体,鉴定结果如图4a和b所示,通过诱导表达和纯化,得到纯化的b7h3
‑
02 scfv蛋白,纯化结果图如图5所示。
[0158]
b7h3
‑
02 scfv抗体:0.456μg/μl。
[0159]
2、实验方案
[0160]
每组实验孔及对照孔中加入等量抗原包被,其后加入纯化的scfv抗体,孵育之后,多次洗涤,加入his抗体和二抗后,进行tmb显色,酶标仪测od
450nm
读数。
[0161]
3、elisa结果分析
[0162]
结果如图6、图7和表4所示,b7h3
‑
02具有较高的亲和力,当纯化的scfv抗体稀释1000倍时,b7h3
‑
02依然有较好的亲和力。
[0163]
表4亲和力统计结果
[0164][0165][0166]
二、实验二
[0167]
1、实验方案
[0168]
采用预设偶联量模式,纯化得到的b7h3
‑
02抗体用ph=7.5的pbs缓冲液稀释至1μg/ml,用生物传感芯片protein a亲和捕获一定量的待测抗体,以乙醇胺封闭未结合的活化基团。b7
‑
h3抗原采用一系列浓度梯度流经芯片表面,结合时间120s,解离时间120s,循环解
离完成后采用甘氨酸
‑
盐酸(ph=1.5)缓冲液将生物芯片洗净,30μl/min进样,再生30s。利用biacore仪器实时检测反应信号从而获得结合和解离曲线。
[0169]
2、结果分析
[0170]
实验得到的数据用ge软件以langmuir模型进行拟合,实验结果见图8a和b,结果显示b7h3
‑
02抗体与b7h3抗原的亲和力为27.8nm,表明了b7h3
‑
02抗体与b7h3抗原具有较好的亲和力。
[0171]
三、实验三
[0172]
1、实验方案
[0173]
将b7h3
‑
02 scfv构建至含有gpi锚定序列的真核表达载体中,转染293t细胞,通过b7h3
‑
fc(r&d systems,1027
‑
b3
‑
100)和pe
‑
anti
‑
human igg fc(thermo,12
‑
4998
‑
82)进行流式检测表达在细胞膜表面的scfv是否能结合靶抗原。
[0174]
2、结果分析
[0175]
通过流式检测结果可见b7h3
‑
02 scfv能识别并结合b7h3靶抗原,其中b7h3
‑
02 scfv结合能力较强,其与阳性对照8h9克隆scfv结合抗原能力相当(见图9a),通过分析细胞表面scfv结合靶抗原b7h3的平均荧光强度可见b7h3
‑
02 scfv较强(见图9b),说明每个细胞膜表面该scfv结合的靶抗原数量较多即荧光基团较多,以上结果均表明了b7h3
‑
02 scfv与b7h3的亲和力高、特异性强。
[0176]
以上已对本发明创造的较佳实施例进行了具体说明,但本发明创造并不限于所述实施例,熟悉本领域的技术人员在不违背本发明创造精神的前提下还可做出种种的等同的变型或替换,这些等同的变型或替换均包含在本申请权利要求所限定的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1