一种用于药物皮下注射制剂的透明质酸酶突变体的制作方法
1.本发明涉及基因工程技术领域,特别是涉及一种用于药物皮下注射制剂的透明质酸酶突变体。
背景技术:
2.透明质酸是一种粘性多糖,它是由双糖单位重复连接组成的直链高分子多糖,其双糖单位是由n
‑
乙酰葡萄糖胺和d
‑
葡萄糖醛酸构成,以β
‑
1,3糖苷键连接,这两种单糖是按照1:1的摩尔比构成,双糖单位之间是以β
‑
1,4糖苷键相连,广泛存在于动物结缔组织的细胞外基质中。它是组织基质中具有限制水分和其它细胞外的物质扩散的成分,在进行药物治疗时,透明质酸会阻碍药物分子的扩散作用。透明质酸酶(hyaluronidase,haase)是能使透明质酸产生低分子化作用的酶的总称,它能降低透明质酸的活性和粘度,提高组织中液体渗透能力。目前haase在临床上被广泛用作药物的一种渗透剂(扩散因子),与药物共同作用,可促进药物吸收。
3.目前市场上透明质酸酶的获取主要是从牛、羊组织内提取,由酵母表达及cho表达系统表达的重组人透明质酸酶这三种方法,从动物组织中提取的透明质酸酶纯度较低,免疫原性较高,酵母表达量较低,而cho表达系统成本较高,目前缺少廉价的原核表达体系,主要原因是透明质酸酶需要进行n
‑
糖基化才能够具有活性,而糖基化过程只能在真核表达体系中完成,原核表达体系不能进行糖基化修饰过程。
4.透明质酸酶目前已经应用在多个领域,美国fda已经批准透明质酸酶作为分散剂,可用于促进药物的扩散和吸收,现透明质酸酶已被用于麻醉辅助剂,常与麻醉药物合用,增强麻醉效果。透明质酸酶也用于注射液的快速吸收,除此以外,由于肿瘤细胞能同时分泌ha和haase,并且随着肿瘤细胞转移而增强分泌,所以透明质酸酶也被用于肿瘤检测的理想标记物。透明质酸酶可以促进代谢进程,减轻血管破坏和细胞及组织水肿,增加侧循环等作用,所以透明质酸酶也可用于减轻缺血损伤,降低心肌梗死概率。由于现在市场上使用的haase大多数从哺乳动物睾丸中提取的,来源有限,产量较低,并且成本较高,由于其糖基化的限制,缺少有效的原核表达体系,而且由于受到免疫原性和纯度的限制,在临床应用时就会发生过敏反应和快速清除反映,在临床应用受到极大限制。
技术实现要素:
5.本发明的目的是提供一种用于药物皮下注射制剂的透明质酸酶突变体,以解决上述现有技术存在的问题,本发明选用哺乳动物细胞293t细胞表达人透明质酸酶ph20并通过分析它的一级结构以及二级结构预测,选出对透明质酸酶活性影响较大的氨基酸位点,通过氨基酸定点突变技术,进行透明质酸酶突变体的构建,并通过pei转染试剂,进行透明质酸酶突变体蛋白重组表达质粒瞬转入细胞,进行蛋白表达。最后在通过活性分析,对比透明质酸酶各突变体之间活性变化情况,最终获得不需要进行糖基化也有活性的透明质酸酶。
6.为实现上述目的,本发明提供了如下方案:
7.本发明提供一种用于药物皮下注射制剂的透明质酸酶突变体,对人透明质酸酶ph20进行氨基酸定点突变,构建透明质酸酶突变体,突变顺序为:n47s/n131d/n200s/n219k/q234l/i228v/t293l/k279t/v53i/v302i/t306s;其中所述透明质酸突变体糖基化数量减少,且保留催化活性。
8.优选的是,所述透明质酸酶突变体分别为:
9.n1:ph20
‑
n47s/n131d/n200s/n219k/q234l/i228v
10.n2:ph20
‑
n47s/n131d/n200s/n219k/q234l/i228v/t293l/k279t
11.n3:ph20
‑
n47s/n131d/n200s/n219k/q234l/i228v/t293l/k279t/v53i
12.n4:ph20
‑
n47s/n131d/n200s/n219k/q234l/i228v/t293l/k279t/v53i/v302i/t306s
13.优选的是,所述n1
‑
n4的目标基因扩增引物如seq id no.5
‑
26所示。
14.本发明还提供所述的透明质酸酶突变体的应用,可用于制备治疗透明质酸酶底物累积的疾病或病症的药物组合物。
15.优选的是,所述药物组合物配制为用于口服,或静脉内(iv)、皮下、肌内、肿瘤内、真皮内、局部、透皮、经直肠或表皮下注射给药。
16.优选的是,所述药物组合物包含免疫球蛋白(ig)、重组蛋白、合成多肽、rna、dna或化学药物。
17.优选的是,所述药物组合物配制为皮下注射给药形式,所述药物组合物中透明质酸酶突变体的量足以使得该药物组合物在治疗上有效。
18.本发明公开了以下技术效果:
19.本发明选取了来源不同的四个物种,运用bioxm进行四个物种透明质酸酶蛋白序列的比较,确定了11个影响透明质酸酶活性的重要氨基酸位点,根据这些位点在透明质酸酶二级结构预测上的分布位置,和这些位点氨基酸的性质,最终获得n1
‑
n4一共4个透明质质酸酶突变体。
20.本发明对透明质酸酶进行分子改造主要是运用氨基酸定点突变技术。首先通过pcr扩增人透明质酸酶序列,再根据所要突变的氨基酸位点设计引物,运用点突变技术依次构建各个透明质酸酶突变体。用双酶切ptt5质粒与目的基因进行同源重组连接,构建突变体蛋白重组表达载体,将构建好的重组表达载体质粒瞬转入293t细胞进行连续传代培养,将培养后的细胞收集起来,用pbs适当重悬,进行超声破碎后,将破碎上清通过his柱纯化,最终得到突变体蛋白。利用dns法测突变体蛋白的活性变化情况。dns在碱性溶液中被透明质酸酶降解ha产物中的还原糖还原为氨基化合物,沸水浴后可以发生显色反应,测a540处的吸光值可以测得酶促反应液中的还原糖当量,用此方法进行透明质酸酶活性测定。进而筛选出对透明质酸酶活性影响较大的氨基酸位点,最终获得不需要糖基化也有活性的人的透明质酸酶。
附图说明
21.图1为透明质酸酶分子改造技术路线图;
22.图2为透明质酸酶二级结构分析,a透明质酸酶糖基化位点分布,b四个物种二级结构比对,c四个物种进化树构建,d四个物种序列比对等同性分析;
23.图3为四个物种透明质酸酶序列比对结果;
24.图4为透明质酸酶同源建模二级结构预测;
25.图5为蛋白活性中心位点氨基酸(d111、e113、e249)c
α
原子轨迹变化情况图;
26.图6为各突变体活性口袋变化情况统计;
27.图7为突变体蛋白电荷变化情况;
28.图8为透明质酸酶及其突变体构建技术路线;
29.图9为各突变体示意图;
30.图10为ph20蛋白重组表达载体构建菌落pcr结果,其中,1
‑
5泳道为ph20蛋白重组表达载体构建菌落pcr琼脂糖凝胶分离结果;
31.图11为透明质酸酶及其突变体活性。
具体实施方式
32.现详细说明本发明的多种示例性实施方式,该详细说明不应认为是对本发明的限制,而应理解为是对本发明的某些方面、特性和实施方案的更详细的描述。
33.本发明所用试剂和设备如无特殊说明,均为普通市售产品,或本领域技术人员通过公开途径可以获得。
34.本发明主要是为了获得原核表达体系表达的不进行糖基化也有活性的透明质酸酶,图1为本发明的技术路线,从genbank数据库中获得人透明质酸酶的序列,将其作为模板,与不需要糖基化也有活性的牛和蜜蜂的透明质酸酶序列进行一级序列比对,成功发现了与活性有关的4个糖基化位点和7个氨基酸位点,通过分析这些突变位点氨基酸的性质和文献查阅最终确定这11个氨基酸位点的突变顺序:n47s/n131d/n200s/n219k/q234l/i228v/t293l/k279t/v53i/v302i/t306s,按照突变顺序对透明质酸酶进行分子改造。
35.对透明质酸酶进行分子改造主要是运用氨基酸定点突变技术。首先通过pcr扩增人透明质酸酶序列,再根据所要突变的氨基酸位点设计引物,运用点突变技术依次构建各个透明质酸酶突变体。用双酶切ptt5质粒与目的基因进行同源重组连接,构建突变体蛋白重组表达载体,将构建好的重组表达载体质粒瞬转入293t细胞进行连续传代培养,将培养后的细胞收集起来,用pbs适当重悬,进行超声破碎后,将破碎上清通过his柱纯化,最终得到突变体蛋白。利用dns法测突变体蛋白的活性变化情况。dns在碱性溶液中被透明质酸酶降解ha产物中的还原糖还原为氨基化合物,沸水浴后可以发生显色反应,测a540处的吸光值可以测得酶促反应液中的还原糖当量,用此方法进行透明质酸酶活性测定。进而筛选出对透明质酸酶活性影响较大的氨基酸位点,最终获得不需要糖基化也有活性的人的透明质酸酶。
36.实施例1透明质酸酶突变位点的选择
37.1、突变位点的确定
38.根据已知文献,已知透明质酸酶含有6个糖基化位点(asn47、131、200、219、333、358),这六个糖基化位点在糖基化修饰种类和比例上有较大的区别,这六个糖基化位点在透明质酸酶二级结构图上的位置如下图2a所示,其中asn333和asn358位糖基化修饰位点位于透明质酸酶c末端,高露糖修饰比例较高。本发明选用了牛(>aap5571.1),大胡蜂(>cby83816.1),蜜蜂(>aaap55713.1)三种活性较高的透明质酸酶物种序列与人ph20(>np
‑
001167516.1)序列进行比对并构建进化树(图2c)进行同源性分析。
39.四个物种透明质酸酶序列比对结果如图3所示。根据四个不同物种的透明质酸酶序列比对结果所示,暗灰色部分为透明质酸酶活性位点氨基酸和透明质酸酶六个糖基化位点的位置,要完成透明质酸酶不进行糖基化的过程必须将这几个糖基化位点突变掉,根据进化树同源性分析结果,人与牛的透明质酸酶同源性较高,蜜蜂与大胡蜂的透明质酸酶同源性较高,所以选择突变位点氨基酸时要以同源性较高的牛的透明质酸酶序列为主,以蜜蜂和大胡蜂的透明质酸酶序列为辅进行糖基化位点突变体的设计。所以n47、131、219突变氨基酸选择为与牛透明质酸该位点处的氨基酸一致,及将n47突变为s、n131突变为d、n219突变为k。n200突变氨基酸选择与蜜蜂透明质酸该位点处氨基酸一致,及将n200突变为s。另外n333、358处糖基化位点位于人透明质酸酶序列尾端,且位于活性口袋的背面,故舍弃这两个糖基化位点,最终确定突变的糖基化位点为n47s、n131d、n200s、n219k这四个位点。
40.灰色高光处氨基酸为筛选出的与透明质酸酶活性可能有影响的位点,这些位点在牛、蜜蜂、大胡蜂的透明质酸酶序列上有较高的同源性,并且这些位点在二级结构上离催化口袋很近。通过对透明质酸酶各个突变体同源建模模型结构分析,各个突变体活性口袋变化情况不一,存在活性变高的可能性。
41.四个物种透明质酸酶二级结构进行比对,如图2b,在活性口袋处有较大部分的重叠,并且序列比对等同性e<10
‑5如图2d,则说明四个物种具有较高的同源性,而其中人与牛的同源性最高,根据序列比对来选择可能提高透明质酸酶的氨基酸位点是可信的。
42.2、突变顺序的确定
43.如图4所示,根据同源建模二级结构预测分析(蓝色为α螺旋结构,绿色为β折叠结构)透明质酸酶活性口袋为111
‑
118位氨基酸肽段形成的无规卷曲与240
‑
245肽段形成的α螺旋及其附近β片层折叠构成,离活性口袋越近的氨基酸位点突变后影响透明质酸酶活性的可能性越大,除此以外,突变位点氨基酸的性质变化,也会影响透明质酸酶突变体蛋白的活性。根据透明质酸酶二级结构预测,将糖基化位点47,131,200,219定义为一级突变位点,228,234两个氨基酸位点为影响催化反应域
‑
α螺旋折叠的权重最高的位点,将其定义为二级突变位点,53,279,293,302,306为影响活性口袋β片层结构折叠的权重较高的氨基酸位点,定义为三级突变位点。除此以外载人透明质酸酶序列上还有一些氨基酸位点在牛、蜜蜂和大胡蜂序列上具有高度同源性,如i83、s84、e285、m323,这些位点都位于形成活性口袋的α螺旋和β片层之间的无规卷曲结构上,所以不考虑这些位点,最后根据氨基酸的性质,亲疏水性,带电荷情况以及查阅相关文献分析,初步确定三级突变位点突变顺序为:t293l
‑
k279t
‑
v53i
‑
v302i
‑
t306s。
44.确定构建以下四个突变体:
45.n1:ph20
‑
n47s/n131d/n200s/n219k/q234l/i228v
46.n2:ph20
‑
n47s/n131d/n200s/n219k/q234l/i228v/t293l/k279t
47.n3:ph20
‑
n47s/n131d/n200s/n219k/q234l/i228v/t293l/k279t/v53i
48.n4:ph20
‑
n47s/n131d/n200s/n219k/q234l/i228v/t293l/k279t/v53i/v302i/t306s
49.3、突变体活性口袋变化情况分析
50.从ncbi上找到人ph20基因序列,去掉n末端35个氨基酸序列的信号肽部分,去掉c
末端糖基磷脂酰肌醇修饰位点,选择第35个氨基酸到482个氨基酸中间序列共447个氨基酸作为目的蛋白表达序列。
51.本发明中ph20核苷酸序列如seq id no.1所示。
52.按照突变顺序,将4个突变体蛋白序列输入https://swissmodel.expasy.org/interactive网站进行模型构建,将pdb格式模型文件用pdb
‑
viewer打开,分析各蛋白活性中心位点氨基酸(d111、e113、e249)c
α
原子轨迹变化情况如图5所示。
53.将以上4个糖基化位点突变体蛋白活性口袋变化情况进行统计如下图6所示。经分析,各突变体活性口袋变化情况不一,蛋白活性变化情况不可预测。通过实验来验证透明质酸酶活性变化情况。
54.4、分析突变体蛋白的电荷变化情况
55.通过将突变体蛋白输入discovery分析突变体蛋白电荷变化情况如图7所示,ph20与n1蛋白的表面电荷变化情况较大(红色代表正电荷,蓝色代表负电荷),ph20与n1蛋白的等电点没有变化都是8.6,但是静电势发生了变化,n0:1710.43,n1:1780.52电势将底物对接到透明质酸酶的活性中心,蛋白电势升高,与底物结合的可能性更高,其余突变体对接也按照上述方法进行分析,根据突变体表面电荷变化情况。最终确定构建以上4个糖基化位点突变体。
56.实施例2透明质酸酶及其突变体的构建、表达及活性研究
57.1、实验材料
58.细胞:293t细胞本实验室提供;菌种:大肠杆菌tg1实验室提供;质粒:ptt5质粒,淼灵生物购买;目的基因:金斯瑞公司合成人ph20基因。
59.2、实验方法
60.2.1透明质酸酶及其突变体蛋白的构建技术路线
61.本发明主要通过同源重组连接构建透明质酸酶重组表达载体,并通过菌落pcr和测序进行验证,透明质酸酶及其突变体蛋白构建的技术路线如图8所示。
62.2.2ph20蛋白重组表达载体构建
63.2.2.1ph20基因的优化及合成
64.从ncbi上下载的ph20基因序列,去掉n
‑
端信号肽部分及c
‑
端gpi位点,在n末端加上荧光素酶信号肽,氨基酸序列为mgvkvlfaliciavaea。并在c末端加上his标签,方便后续蛋白表达检测及纯化操作。按照哺乳动物细胞密码子偏好性对ph20基因进行密码子优化,优化后序列氨基酸未发生变化。将优化后的目的基因序列送南京金斯瑞生物公司进行基因合成,并将目的基因构建到puc
‑
57质粒载体上,优化后的目的基因序列如seq id no.2所示。
65.本发明利用同源重组连接构建透明质酸酶表达载体,同源重组连接是一种dna定向克隆技术,利用这种定向克隆技术,可以将插入片段的pcr回收产物定向克隆至任意载体的任意位置,简单、快速且高效。
66.(5)对得到的人透明质酸酶突变体蛋白,利用dns法进行活性测定。
67.具体步骤如下:
68.(1)获得编码人透明质酸酶的基因片段,基因序列(seq id no.1,genbankaccession number:>np
‑
001167516.1)
69.(2)将glu信号肽序列连接到人透明质酸酶序列的5’端,去掉3’端gpi位点,得到的seq id no.2基因序列,连接到ptt5(seq id no.3)载体上,转入293t细胞中进行表达,得到人透明质酸酶蛋白。
70.(3)通过定点突变对seq id no.2基因序列进行改造,得到糖基化全缺失突变体(seq id no.4),连接到ptt5载体上,转入293t细胞中进行表达,得到人透明质酸酶突变体蛋白。
71.(4)在seq id no.4基因序列基础上,进行特定位点氨基酸的改造,得到突变株n1
‑
n4基因序列,连接到ptt5载体上,转入293t细胞中进行表达,得到人透明质酸酶突变体蛋白。
72.(5)对得到的人透明质酸酶突变体蛋白,利用dns法进行活性测定。
73.实施例3质粒ptt5
‑
ph20的构建
74.所用质粒ptt5购自淼灵生物公司,将表达人透明质酸酶的基因进行pcr扩增,再将扩增产物掺入ptt5质粒上的ecori/hindⅲ位点之间,得到质粒ptt5
‑
ph20。所构建的序列送生工生物工程有限公司进行测序验证。
75.构建过程如下:
76.1、以引物ph20
‑
f(seq id no.5)和ph20
‑
r(seq id no.6)为引物,以人透明质酸酶序列seq id no.2为模板,扩增获取人透明质酸酶基因片段。
77.pcr循环过程(kod
‑
plus
‑
neo酶):
78.step1:94℃2min
79.step2:98℃10s
80.step3:63℃30s
81.step4:68℃45s(至step2,40个循环)
82.step5:68℃5min
83.pcr产物的检测:取3μl pcr产物,琼脂糖凝胶电泳检测(如图10所示),结果显示成功扩增出人透明质酸酶基因片段。
84.2、将上述获得的pcr产物利用同源重组酶连接到ptt5载体上,转入tg1感受态细胞中,具体操作方法如下:
85.使用ecori和hindⅲ双酶切质粒ptt5,使用同源重组酶将pcr扩增的seq id no.2序列连接到双酶切后的ptt5载体上,得到ptt5
‑
ph20,取10μl酶连产物,加入到200mltg1感受态细胞中,冰浴30min,42℃热激90s,热激完成后,再冰浴2min,加入800μllb液体培养基(无抗性),37℃,140rpm复苏45min,5000rpm离心收集菌体,弃掉900μl培养基上清,将菌体重悬后进行涂布平板(氨苄青霉素抗性,100ng/μl),通过菌落pcr选出重组菌,并进行测序验证。
86.3、挑取上述测序正确的菌落于5ml lb液体培养基(氨苄青霉素抗性,100ng/μl)中,37℃,180rpm培养15h,利用去内毒素试剂盒进行质粒提取,将提取好的质粒利用lip2000瞬转入293t细胞中进行蛋白表达,具体操作如下:
87.将20μg的质粒与20μl的lip2000分别加入48μl的培养基(dmem高糖培养基)中混合均匀,静置20min,将混合液滴加入细胞培养皿中,连续培养3天,收集细胞,进行超声破碎处理,将细胞破碎上清收集起来,用0.22μm膜进行抽滤,用his亲和层析柱进行纯化,将得到的
蛋白进行透析、冻干等操作,得到纯度达到90%以上的人透明质酸酶蛋白。
88.4、将得到的人透明质酸酶蛋白进行活性测定,本发明采用dns法进行人透明质酸酶活性测定,具体操作如下:
89.利用2mg/l葡萄糖溶液做标准曲线。葡萄糖溶液体积分别为:0、5、7.5、10、12.5、15、17.5、20μl,按照要求向1.5ml离心管中加入葡萄糖溶液,用pbs缓冲液补足到100μl,将溶液混合均匀后,在分别向离心管中加入200μl dns试剂混合均匀后,煮沸10min,加入700μl超纯水混合均匀,各吸取200μl混合液,加入96孔板中,用多功能酶标仪测a
540
吸光值。
90.将得到的人透明质酸酶蛋白用pbs缓冲液进行稀释,取一定量的蛋白稀释液20μl,在向其中加入20μl 0.5%ha溶液,用pbs补足到100μl,对照用pbs代替酶稀释液。充分混和均匀后37℃反应10min。反应后将酶促反应液置于100℃金属浴上,金属浴5min,让蛋白失活。向酶促反应液中立即加入200μl dns试剂,混匀后100℃加热10min,加入700μl的超纯水,充分混和均匀后,吸取200μl混合液,加入96孔板中,用多功能酶标仪测a
540
吸光值。
91.以葡萄糖浓度作为横坐标,以a
540
处的吸光值为纵坐标,绘制标葡萄糖量准曲线。按照a
540
吸光值计算出酶促反应液中的还原糖当量产物,进而测出透明质酸酶活性。
92.实施例4糖基化位点全缺失突变体的构建及活性测定
93.利用定点突变技术,向ph20目的基因(seq id no.2)引入氨基酸突变,通过重叠延伸pcr进行突变体蛋白全长目的基因模板扩增,并构建重组表达载体。糖基化位点变体构建所需引物由上海生工生物有限公司合成:
94.引物设计:47
‑
f(seq id no.7),47
‑
r(seq id no.8),131
‑
f(seq id no.9),131
‑
r(seq id no.10),200
‑
f(seq id no.11),200
‑
r(seq id no.12),219
‑
f(seq id no.13),219
‑
r(seq id no.14)。
95.以seq id no.2为模板,以上述引物进行pcr反应,得到seq id no.4,pcr循环过程及后续构建、纯化、活性测定操作同实施例3。
96.实施例3活性回复突变体的构建及活性测试
97.利用定点突变技术,向seq id no.4序列中分别引入七位点突变,通过重叠延伸pcr进行突变体蛋白全长目的基因模板扩增,并构建重组表达载体。突变体构建所需引物由上海生工生物有限公司合成:
98.引物设计:234
‑
228
‑
f(seq id no.15),234
‑
228
‑
r293
‑
f(seq id no.16),293
‑
f(seq id no.17),293
‑
r(seq id no.18),279
‑
f(seq id no.19),279
‑
r(seq id no.20),53
‑
f(seq id no.21),53
‑
r(seq id no.22),302
‑
f(seq id no.23),302
‑
r(seq id no.24),306
‑
f(seq id no.25),306
‑
r(seq id no.26)。
99.以seq id no.4为模板,以上述引物进行pcr反应,得到n1
‑
n4蛋白核苷酸序列(如seq id no:27
‑
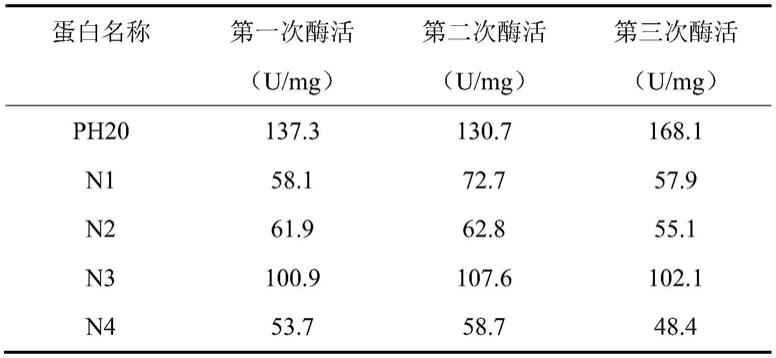
30),各突变体构建示意图如图9所示。pcr循环过程及后续构建、纯化、活性测定操作同实施例3。各突变体活性如图11及表1所示,测得活性回复突变体n3活性最高为103.5u/mg,达到野生型人透明质酸酶活性的70%。
100.表1透明质酸酶以及各个突变体酶活性
[0101][0102]
实施例4应用放射性示踪显像比较研究生物促渗剂人透明质酸酶强化组织药物吸收的效果。
[0103]
人透明质酸酶突变体n3与阴性对照生理盐水经静脉分别注入健康icr小鼠,注射后2小时,在左或右大腿部位皮下注射99mtc标记的示踪剂甲氧基异丁基异腈(99mtc-sestamibi),应用高分辨小动物专用γ相机获取活体鼠全身成像,观测放射性标记的药物模拟化合物皮下注射后吸收速度和全身组织分布。
[0104]
结果显示,静脉注射人透明质酸酶突变体n3动物(a)经皮下注射部位吸收99mtc-sestamibi的放射性吸收分布情况显示,人透明质酸酶突变体n3治疗组小鼠体内99mtc-sestamibi的放射性分布及主要器官放射水平明显高于生理盐水对照组动物。
[0105]
本发明提出了人透明质酸酶ph20突变株,通过实施例进行详细描述,相关技术人员能在本发明内容和范围内对本文所述的方法进行适当变动,来实现本发明技术。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1