具有预防或治疗糖尿病作用的新型乳杆菌YUYINGW的制作方法
具有预防或治疗糖尿病作用的新型乳杆菌yuyingw
技术领域
1.本发明属于微生物技术领域,具体涉及一株具有预防或治疗糖尿病作用的新型乳杆菌yuyingw。
背景技术:
2.糖尿病(diabetes,td)作为世界第三大慢性非传染性疾病,随着社会老龄化和城市化的进程,患病人数逐年上升。国际糖尿病联合会(international diabetes federation, idf)的数据显示,2019 年估计有 4.63 亿人患有糖尿病,占全球总人数的9.3%,到2045年患病人数预计上升至7亿。根据 1999 年世界卫生组织 (world health organization,who) 和idf公布的定义,糖尿病主要分为胰岛素依赖型糖尿病 (1 型糖尿病) 和非胰岛素依赖型糖尿病 (2型糖尿病),妊娠糖尿病和其它类型,其中2型糖尿病占总患病数的90%以上。
3.肥胖、高脂高盐饮食和缺乏体育锻炼使td发病率趋于年轻化,td不仅归因于基因组、营养习惯、日常体育锻炼等因素,糖脂代谢紊乱以及肠道微生态平衡紊乱均会加重胰岛素抵抗的发生。肠道微生物及其代谢产物与宿主细胞共同维持正常生理功能,肠道屏障、胆汁酸代谢、抗生素的使用以及微生物代谢产物多效能共同影响肠道菌群平衡,菌群失调继发肠道炎症和代谢性内毒素血症,研究显示,其肠道微生态失衡与肠道菌群中的益生菌减少和有害菌增加有关 。高脂饮食、肥胖、血脂异常、糖耐受不良和肝损伤与肠道微生态紊乱协同作用于胰岛素抵抗的发生,加重糖尿病病情。
4.因此,急需通过有效措施来预防和治疗糖尿病。目前用于治疗糖尿病的方式,除可施予胰岛素外,另分为非药物治疗与药物治疗两种。在非药物治疗方面,主要是通过饮食调控和运动的方式来加以治疗。而在药物治疗方面,主要目的是使不足的胰岛素上升、调降进食后的高血糖和改善胰岛素抵抗性等。目前用于治疗糖尿病的药物主要分为 :磺酰尿素类 (sulfonylurea) 、α
‑ꢀ
葡萄糖苷酶 (α
‑
glucosidase) 抑制剂、噻唑烷二酮类 (thiazolidinedione) 衍生物和双胍类 (biguanides)。但这些药物都具有副作用,初服可能有肠胃不适,如厌食,恶心、呕吐或腹泻等,少数人可能出现皮疹,且长期使用后可能会有失活的现象发生。
5.益生菌能够帮助消化,有助人体肠道健康。乳杆菌作为定居肠道中的有益菌群具有多种作用 :1. 能维持微生态平衡和肠管机能 ;2. 有抗菌作用,能抑制腐败菌,如可杀灭李斯特菌,葡萄球菌和明串珠菌,以抑制和消灭革兰氏阴性菌、过氧化氢酶阳性菌,大肠杆菌和沙门氏菌等 ;3. 能改善肝功能 ;4. 乳杆菌能使肠道减少对胆固醇的吸收,并能将一部分胆固醇转变成胆酸盐排出体外 ;5. 能增强免疫功能和抗肿瘤病。近年来,有研究报道乳杆菌对糖尿病治疗有积极地影响。乳杆菌可以预防和延迟不同类型糖尿病的发生。目前大量研究表明,乳杆菌具有减少糖尿病发病率的潜力,但是对于乳杆菌作为糖尿病治疗剂的研究还是很少。
6.本发明从小鼠粪便中筛选获得一株新型乳杆菌yuyingw(cgmcc no.21661),该菌
株通过调节肠微生态系统,减轻代谢性内毒素血症的发生,达到降糖降脂、改善胰岛素抵抗的作用,具有预防或治疗糖尿病的作用。
技术实现要素:
7.本发明的目的在于提供一株具有预防或治疗糖尿病作用的新型乳杆菌yuyingw。新型乳杆菌yuyingw筛选自小鼠粪便,该菌株通过调节肠微生态系统,减轻代谢性内毒素血症的发生,达到降糖降脂、改善胰岛素抵抗的作用,具有预防或治疗糖尿病的作用。
8.为实现上述目的,本发明采用如下技术方案:一株新型乳杆菌yuyingw,所述新型乳杆菌yuyingw,其分类命名为乳杆菌(lactobacillus sp.),已于2021年1月18日保藏于中国微生物菌种保藏管理委员会普通微生物中心,地址为:北京市朝阳区北辰西路1号院3号,中国科学院微生物研究所;保藏编号为cgmcc no.21661。
9.上述新型乳杆菌yuyingw在预防或治疗肠道疾病中的应用。
10.上述新型乳杆菌yuyingw在预防或治疗糖尿病及其相关并发症中的应用。
11.上述应用,其中新型乳杆菌yuyingw具有通过调节肠微生态系统,减轻代谢性内毒素血症的发生,达到降糖、改善胰岛素抵抗的作用,进而预防或治疗糖尿病及其相关并发症。
12.上述新型乳杆菌yuyingw在预防或治疗脂质代谢异常中的应用。
13.上述应用,其中新型乳杆菌yuyingw通过调节肠微生态系统,减轻代谢性内毒素血症的发生,达到降脂的作用,进而预防或治疗脂质代谢异常相关疾病。
14.一种含有上述新型乳杆菌yuyingw的制剂。
15.上述一种含有上述新型乳杆菌yuyingw的制剂,其中,所述制剂包含但不限于新型乳杆菌yuyingw,新型乳杆菌yuyingw和/或其代谢产物;所述代谢产物包括但不限于:培养新型乳杆菌yuyingw时,经新型乳杆菌yuyingw代谢后所分泌至培养液中的物质;或者经新型乳杆菌yuyingw代谢后的细胞内容物;或者经新型乳杆菌yuyingw代谢后所分泌至培养液中的物质和培养此新型乳杆菌yuyingw的培养液。
16.上述一种含有上述新型乳杆菌yuyingw的制剂,其中,所述制剂包含新型乳杆菌yuyingw的片段,所述片段包括:新型乳杆菌yuyingw细胞的部分;包括新型乳杆菌yuyingw 的dna、rna、蛋白质、肽、脂类、糖,细胞膜、细胞壁中的一种或几种,不仅限于以上组分。
17.上述一种含有上述新型乳杆菌yuyingw的制剂,其中,所述制剂包含但不限于新型乳杆菌yuyingw的突变体或衍生物,所述突变体或衍生物包括:通过基因工程技术、物理诱变及化学修改所致的对表达/转录/翻译产生影响的突变体或衍生物。
18.上述新型乳杆菌yuyingw是分离自小鼠粪便的乳杆菌属菌株。该菌株的培养及形态特征、生理生化特性如下:新型乳杆菌yuyingw的培养及形态特征:无芽孢、革兰氏染色呈阳性、过氧化氢实验呈阴性;菌体杆状,单个或成链,有时成丝状,产生假分枝;细胞罕见以周生鞭毛运动。菌落在营养琼脂上有凸起、乳白色、边缘光滑,直径2mm
‑
5mm。该乳酸菌在固体培养基上菌落较小,生长缓慢,在液体发酵培养基内可以很快的生长,离心洗涤后可以获得纯度较高的菌
体,且兼具需氧和厌氧的性能。
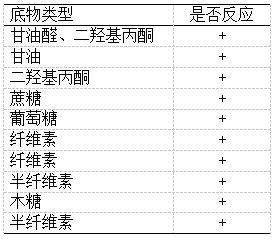
19.新型乳杆菌yuyingw的生理生化特征见表1:表1本发明的有益效果:(1)本发明提供了一株新型乳杆菌yuyingw,该菌株分离自小鼠的粪便。经全基因组测序鉴定,现有技术中并未发现在种水平上有与之相似的菌株。
20.(2)本发明分离的新型乳杆菌yuyingw作为肠道原生益生菌,在降低血糖方面表现出优于已知益生菌(双歧杆菌、粪便菌群)的优秀作用,能显著降低血糖和糖化血红蛋白的含量。
21.(3)本发明分离的新型乳杆菌yuyingw作为肠道原生益生菌,能显著改善脂质代谢。经新型乳杆菌yuyingw菌群移植后,由td造成的体重亏损得到一定程度的恢复;饮食量由td期间的生理打击状态恢复至恒定水平;肝细胞结构有明显正常化趋势并在一定程度上得到修复,肝小叶结构趋于正常化,假小叶减少;肝脂肪变程度减轻,肝细胞脂滴明显减少;血脂指标降低。乳杆菌yuyingw菌群移植通过改善肠道微生态环境,改变了肠道微生物代谢水平,调节脂质代谢,减少异常脂肪堆积,降低了血脂水平。乳杆菌yuyingw菌群移植对逆转非酒精性脂肪肝和脂质代谢异常情况有明显组织学和血清学效果。
22.(4)本发明分离的新型乳杆菌yuyingw作为肠道原生益生菌,能有效改善谢性内毒素血症。血清学炎症因子il
‑
6和tnf
‑
α的降低,肠alcian染色提示乳杆菌yuyingw组杯状细胞增加和肠粘膜层增厚,证实乳杆菌yuyingw移植对修复肠屏障系统,改善肠腔炎症环境有优异的作用。
23.(5)本发明分离的新型乳杆菌yuyingw作为肠道原生益生菌,能有效预防或治疗糖尿病。通过给予高丰度新型乳酸菌yuyingw,调节菌群失调改变了肠道微生态系统;通过修复肠粘膜屏障系统,减少炎症因子释放入血,减轻机体代谢性内毒素血症,改善机体整体的炎症状态。新型乳酸菌yuyingw调节肠腔微环境,增加降糖激素glp
‑
1的产生,增加胰岛素敏感性;减轻肝脏、胰腺等脏器脂肪化负担,一定程度恢复胰岛β细胞功能,促进胰岛细胞再生。新型乳酸菌yuyingw总体作用达到降低血糖、改善胰岛素抵抗的作用,是用于制备预防或治疗糖尿病制剂的优秀组分。
24.附图说明:
图1乳杆菌yuyingw革兰氏染色和和过氧化氢实验结果图。图a为棒状的革兰氏染色阳性细菌图(200x);图b为过氧化氢实验结果阴性图。
25.图2乳杆菌yuyingw基于16s rrna的系统发育树。
26.图3乳杆菌yuyingw同源物种分布饼图。
27.图4乳杆菌yuyingw kegg代谢通路分类。
28.图5乳杆菌yuyingw对小鼠血糖的影响。图中control为菌群移植治疗组,normal(nc)为普通饮食对照组,td为糖尿病对照组,lab为粪便筛选优势菌株组(即新型乳杆菌yuyingw),bio为双歧杆菌组,fmt为粪菌移植组,i.p. stz表示腹腔注射链脲佐菌素,pbs(phosphate buffered saline)为磷酸盐缓冲盐溶液;图a为造模干预流程图;图b为造模后小鼠空腹血糖值;图c为干预后空腹血糖值;图d为干预后血浆糖化血红蛋白(hba1c)浓度。
29.图6 乳杆菌yuyingw对小鼠血脂的影响。图a为干预后饮食量(平均5只/周),已恢复至正常水平;图b为干预后体重;图c为肝脏he染色(200x)和油红o染色(200x)切片;图d为血清总胆固醇(tc);图e为血清甘油三酯(tg);图f为血清低密度脂蛋白(ldl
‑
c)。
30.图7 乳杆菌yuyingw对小鼠内毒素的影响。 图a为结肠alcian染色(100x),;图b
‑
e依次为血清炎症因子(il
‑
6、il
‑
10、tnf
‑
α)、胰岛素(ins)。
具体实施方式
31.通过以下实施实例更加详细地说明本发明。以下实施实例仅是说明性的,本发明并不受这些实施实例的限制。
32.本说明书中所述的所有技术性及科学术语,除非另外有所定义,皆为该所属领域具有通常技艺者可共同了解的意义。
33.新型乳杆菌(lactobacillus sp.)yuyingw是分离自小鼠粪便的乳杆菌属菌株。新型乳杆菌(lactobacillus sp.)yuyingw已于2021年1月18日保藏于中国微生物菌种保藏管理委员会普通微生物中心,地址为:北京市朝阳区北辰西路1号院3号,中国科学院微生物研究所;保藏编号为cgmcc no.21661。通过糖尿病动物模型实验验证,发现新型乳杆菌yuyingw可有效改善、降低、控制、治疗及预防患有糖尿病的对象体内的高血糖值、高血糖值变化量、高糖化血红素比例、高总胆固醇浓度、高甘油三酯浓度、高炎症因子浓度,进而改善其病情及其相关并发症的病情。
34.其中该乳杆菌还包含其继代培养的后代,或突变株,但仍与本发明所述的菌种特性、基因、或用途 ( 用于预防或治疗肠道疾病、脂质代谢和糖尿病症状 ) 相同。
35.本发明提供一株新型乳杆菌yuyingw在预防或治疗肠道疾病中的应用。所述“肠道疾病”包括肠道危害细菌感染、以及炎症性肠道疾病,例如,包括由病原性微生物 ( 大肠杆菌、沙门氏菌、梭菌等 ) 引起的感染性腹泻、肠胃炎、炎症性肠道疾病、神经性肠炎综合症、小肠细菌过度生长、急性腹泻等,但是并不限于这些。
36.本发明提供一株新型乳杆菌yuyingw在预防或治疗糖尿病及其相关并发症中的应用。术语“糖尿病”包括所有形式的糖尿病,其特征为由于胰岛素激素水平不足而导致的代谢紊乱和异常高血糖 ( 高血糖症 )。该术语由此包括 1 型糖尿病、2 型糖尿病、妊娠糖尿病以及葡萄糖耐受不良。术语“糖尿病相关并发症”,包含但不限于 :糖尿病性神经病 ( 包含但不限于膀胱无力、腹胀、便秘、泻肚、阳萎、对冷热感觉差 )、肾疾病 ( 包含但不限于丝
球体性肾炎、肾小球硬化症、肾病征候群、高血压性肾硬化、肾疾病末期、尿毒症 )、发炎反应、心血管或胆固醇过高并发症 ( 包含但不限于脑中风、心肌梗塞、冠状动脉栓塞、心绞痛、心衰竭、心律不稳、末梢血液循环不良、足部感染等 )、眼疾 ( 视网膜病变、白内障、青光眼、弱视 ( 视力衰弱 ))、肝脏疾病 ( 包含但不限于肝脏纤维化、脂肪肝、非酒精性脂肪肝、及肝硬化 )。
37.本发明提供一株新型乳杆菌yuyingw在预防或治疗脂质代谢异常相关疾病中的应用。术语“脂质代谢异常”包含但不限于具有比正常水平更高血脂水平的状态 (高脂血症)、血液中脂蛋白的性质改变和异常和游离脂肪酸增加。具体地,作为高脂血症,包含但不限于高胆固醇血症、高低密度脂蛋白血症、低高密度脂蛋白血症、高甘油三酯血症、脂肪肝(如非酒精性脂肪肝和酒精性脂肪肝)、餐后高脂血症等。
38.本发明提供一种含有上述新型乳杆菌yuyingw的制剂。术语“制剂”可以作为术语“组合物”的同义词使用。所述制剂包括但不限于药用、兽用、化妆品用或食品用制剂。所述制剂包括但不限于粉剂、棒剂、乳膏剂、分散体剂、乳剂、泡沫剂、软膏剂、喷雾剂、气溶胶剂、毛巾剂、洗剂、混悬剂、溶液剂、凝胶剂的形式。所述新型乳杆菌yuyingw,其菌体包括但不限于:新型乳杆菌菌液、冻干粉或任意形式作为其他产品添加剂或成分中的菌体。
39.本发明提供一种含有上述新型乳杆菌yuyingw的制剂;所述制剂包含但限于新型乳杆菌yuyingw,新型乳杆菌yuyingw和/或其代谢产物。术语“代谢产物”意为培养新型乳杆菌yuyingw时,经新型乳杆菌yuyingw代谢后所分泌至培养液中的物质;或者经新型乳杆菌yuyingw代谢后的细胞内容物;或者经新型乳杆菌yuyingw代谢后所分泌至培养液中的物质和培养此新型乳杆菌yuyingw的培养液。
40.本发明提供一种含有上述新型乳杆菌yuyingw的制剂;所述制剂包含新型乳杆菌yuyingw的片段,所述片段包括:新型乳杆菌yuyingw细胞的部分;包括新型乳杆菌yuyingw 的dna、rna、蛋白质、肽、脂类、糖,细胞膜、细胞壁中的一种或几种,不仅限于以上组分。
41.本发明提供一种含有上述新型乳杆菌yuyingw的制剂;所述制剂包含但不限于新型乳杆菌yuyingw的突变体或衍生物,所述突变体或衍生物包括:通过基因工程技术、物理诱变及化学修改所致的对表达/转录/翻译产生影响的突变体或衍生物。
42.实施例1 糖尿病小鼠造模雄性 c57bl/6 小鼠(5周龄)购自北京华阜康生物科技股份有限公司(中国 北京)。动物饲养在福建医科大学(中国 福州)的实验动物中心。每5只小鼠圈养在笼中,12小时光照/黑暗周期下保持(早晨08:00开灯,温度和湿度控制的环境(21
±
2℃、60%),自由获得食物和水。所有实验程序均按照国家机构实验室动物护理和使用卫生指南进行,动物方案经动物使用和保护伦理委员会批准。
43.5周龄雄性c57bl/6小鼠55只,适应性喂养一周后随机分为普通饲料对照组(normal, n=10)和td造模组(n=45),造模组采用高脂饮食(hfd)4周后加低剂量链脲佐菌素(stz)40
‑
50mg
·
kg
‑1/只腹腔注射5天,测一周后禁食过夜空腹血糖值若在16.27
±
0.99mmol/l,造模成功。
44.实施例2 菌株的筛选、分离与鉴定1.1 配制改良mrs琼脂平板
(1)将干净的培养皿拆包后平铺于无菌操作台中,紫外灭菌30min。
45.(2)取清洗好的500ml容量锥形瓶,加入mrs肉汤培养粉10.48g,agar粉3g,加热溶解于200ml蒸馏水中,110℃高压灭菌15分钟,待培养液降至55℃以下,加入l
‑
半胱氨酸盐酸盐1支(0.1g/支)、莫匹罗星锂盐2支(5mg/支),摇晃均匀。
46.(3)立即将尚热的培养液以平均每10ml一个平板的量倒板,待培养皿稍微凝固后盖培养皿盖后倒置于无菌操作台,过夜后收于4℃冰箱密封保存,备用。
47.1.2配制改良mrs培养液取清洗好的500ml容量锥形瓶,加入mrs肉汤培养粉10.48g,加热溶解于200ml蒸馏水中,110℃高压灭菌15分钟,待培养液温度降至常温加入l
‑
半胱氨酸盐酸盐1支(0.1g/支)、莫匹罗星锂盐2支(5mg/支),摇晃均匀,放于4℃冰箱保存,封口备用。
48.1.3野生粪便菌株筛选(1)收集对照组(普通饲料喂养)6
‑
7周龄小鼠粪便于1.5ml试管内,并在2h内加1ml的1
×
pbs溶液稀释,研磨棒将其搅匀,4℃低温离心机3000r/30s离心。
49.(2)吸弃一部分上清液,取100μl悬浊液涂于改良mrs琼脂平板上,涂布棒将其均匀平铺于改良mrs琼脂平板上,立即装入2.5l圆底立式厌氧培养袋中,袋中加入一包2.5l厌氧产气包及一瓶氧气指示剂后封口。
50.(3)将厌氧培养袋平放于37℃恒温培养箱培养72h。
51.(4)待培养皿长满白色独立菌落后,取出培养皿,将单个菌落挑出涂于新的改良mrs琼脂平板划线培养,再次37℃恒温厌氧培养72h,以纯化单一菌株。
52.(5)培养出单一菌落接种于mrs液体培养基中培养72h,37℃恒温摇床150r/h,以增殖菌落,最终获得单一菌落增殖的粪便菌液。
53.1.4过氧化氢酶实验将0.3ml的3vol%过氧化氢滴于培养好的粪便单一菌落平板上,观察1
‑
2分钟,镜检,含有过氧化氢酶的细菌会分解过氧化氢产生气泡。
54.1.5革兰氏染色革兰氏染色法一般包括初染、媒染、脱色、复染等四个步骤,具体操作方法是:(1)涂片火焰固定,加结晶紫液染10秒,水洗,沥干。
55.(2)加碘液染10秒,水洗,沥干。
56.(3)加脱色液(乙醇),脱色10
‑
20秒,沥干。
57.(4)加复染液(碱性品红)染10秒,水洗。
58.(5)干后镜检,革兰氏阳性菌呈紫色,革兰氏阴性菌呈红色。
59.1.6菌落计数(1)培养上述制备的单菌落菌株。
60.(2)以8000rpm/4℃离心10分钟后收集上述微生物菌落,并加入3ml1
×
pbs溶液稀释沉淀,吹打均匀。
61.(3)取1ml菌液于1.5ml试管内,用枪吹打均匀,取100μl于一新试管内,加入900μl的1
×
pbs溶液,依次做梯度稀释(10
‑1、10
‑2、10
‑3、10
‑4、10
‑5)。
62.(4)每一支试管取吹打均匀的100μl菌液培养于mrs平板上,在厌氧培养袋中密封,37℃培养箱培养72h后计数产生的菌落个数,菌落计数以菌落形成单位(colony
‑
forming
units,cfu)表示。
63.(5)每一支试管中菌液吹打均匀后立即检测od
600
值。
64.(6)将菌落计数od
600
值为横坐标,菌落计数为纵坐标做菌液浓度梯度回归曲线,以备后续菌液浓度计算。
65.1.7 菌株冻存与复苏(1)冻存:将纯化增殖后的菌落离心8000rpm/4℃离心10min,弃上清加2.7ml改良mrs培养液重悬,加入0.3ml的100%甘油混匀,每200μl分装于1.5mlep管内,封口膜封口后冻于
‑
80℃冰箱,用于保种。
66.(2)复苏:将分装好的小ep管菌落从
‑
80℃冰箱中拿出,常温复苏1
‑
2分钟,加入改良mrs培养液重悬,分别添加于新的50ml试管内,加入改良mrs培养液5ml,在37℃厌氧环境下扩增培养72h。
67.1.8 筛选结果:经上述步骤从小鼠粪便中筛选获得一株细菌yuyingw。
68.新型乳杆菌yuyingw的培养及形态特征:无芽孢、革兰氏染色呈阳性、过氧化氢实验呈阴性(图1a
‑
b);菌体杆状,单个或成链,有时成丝状,产生假分枝,细胞罕见以周生鞭毛运动。菌落在营养琼脂上有凸起、乳白色、边缘光滑,直径2mm
‑
5mm。该乳酸菌在固体培养基上菌落较小,生长缓慢,在液体发酵培养基内可以很快的生长,离心洗涤后可以获得纯度较高的菌体,且兼具需氧和厌氧的性能。
69.新型乳杆菌yuyingw的生理生化特征如表1所示。
70.扩增菌株yuyingw的16s rna序列,16s rna序列如seq id no.1所示。在ncbi中进行blast分析,绘制系统发育树(图2),结果显示该菌株属于乳杆菌(lactobacillus sp.)属。
71.菌株yuyingw进行全基因组测序,与现有数据库比对,结果表明在现有数据库中,在种水平,并未发现有与之相似菌株(图3)。
72.因此菌株yuyingw,是一株新型乳杆菌,命名为乳杆菌(lactobacillus sp.)yuyingw。该菌株已于2021年1月18日保藏于中国微生物菌种保藏管理委员会普通微生物中心,地址为:北京市朝阳区北辰西路1号院3号,中国科学院微生物研究所;保藏编号为cgmcc no.21661。
73.乳杆菌(lactobacillus sp.)yuyingw全基因组测序数据,进行kegg代谢通路分析(图4),结果表明:乳杆菌(lactobacillus sp.)yuyingw除了主要有糖代谢、核苷酸代谢外,脂质代谢、氨基酸代谢外,产生的微生物代谢产物能直接影响肠内容物的分解消化及产能过程,并通过肠内容物与自身的肠道微生物的相互作用,分解脂肪酸、蛋白质、产生微量元素(必要和非必要维生素及其他功能物质)、为机体提供能量,并通过调节菌群失调,改善机体炎症及高脂高糖代谢状态。
74.实施例3. 菌群移植治疗糖尿病小鼠造模后由于stz毒副作用导致2只小鼠死亡,造模成功的43只小鼠分为4组,分别为:糖尿病(td)对照组、筛选菌株(lab)治疗组、双歧杆菌(bio)治疗组和粪菌移植(fmt)组,各10、9、10、14只。实验期间监测空腹血糖、体重、饮食,测血脂指标、血清炎症因子、结肠、肝脏等组织学水平。
75.双歧杆菌菌株购买于中国微生物菌种保藏管理委员会普通微生物中心(china general microbiological culturecollectioncenter,cgmcc),菌株名称为长双歧杆菌长亚种(bifidobacterium longum subsp. longum),cgmcc编号为1.2186,此菌株通常用于双歧杆菌研究对糖尿病的影响及其机制,选取对象有治疗意义。
76.3.1 灌胃菌株溶液的制备将冻存的粪便筛选菌株乳杆菌yuyingw和双歧杆菌(cgmcc编号为1.2186)复苏,培养于改良 mrs培养液中72h,以8000rpm离心10分钟后收集上述微生物菌落,加入3ml的1
×
pbs溶液重悬沉淀。所述1xpbs缓冲液配方:kh2po
4 0.2g、na2hpo4.12h2o 2.9g、nacl 8.0g、kcl 0.2g,加水定容到1000ml。
77.3.2 菌落计数立即取上述重悬菌液100μl在分光光度计上测定od
600
值:以1
×
pbs溶液作为空白调零,测定稀释后菌液的吸光度,并记录。测od
600
值后根据菌株浓度回归方程计算菌液浓度,并用1
×
pbs溶液将微生物菌落浓度调节至1
×
106cfu/ ml。
78.3.3粪菌制备(1)收集普通饲料喂养正常小鼠的新鲜粪便1
‑
2粒,置于1.5mlep管中,加入1
×
pbs溶液1ml,立即用高压灭菌过的研磨棒研磨至均匀无大颗粒。
79.(2)将研磨好的ep管封口离心机3000rpm/4℃离心30s。
80.(3)将离心好的上清液转移至另一干净试管中,制备获得粪菌悬液。
81.3.4小鼠灌胃(1)将成模后的糖尿病小鼠每天以0.3ml
‑
0.4ml的1
×
106cfu/ ml乳杆菌yuyingw和双歧杆菌菌液灌胃治疗,粪菌移植组以每只小鼠0.3ml粪菌悬液灌胃治疗,对照组小鼠每天以0.3ml
‑
0.4ml的1
×
pbs溶液灌胃处理,连续4周。
82.(2)第5周每3天以0.3ml
‑
0.4ml的1
×
106cfu/ ml乳杆菌yuyingw和双歧杆菌菌液灌胃,粪菌移植组以每只小鼠0.3ml粪菌悬液灌胃治疗,对照组小鼠每3天以0.3ml
‑
0.4ml的1
×
pbs溶液灌胃处理。
83.(3)第6周灌胃1次,以0.3ml
‑
0.4ml的1
×
106cfu/ ml乳杆菌yuyingw和双歧杆菌菌液灌胃,粪菌移植组以每只小鼠0.3ml粪菌悬液灌胃治疗,对照组小鼠以0.3ml
‑
0.4ml的1
×
pbs溶液灌胃处理。
84.3.5小鼠血糖测量每周日禁食过夜,周一早晨取小鼠尾血滴于血糖试纸,血糖仪测小鼠空腹血糖,并记录。
85.3.6小鼠体重测量每周日禁食过夜,周一早晨取小鼠于干净的鼠笼,置于体重仪上测小鼠体重,并记录。
86.3.7小鼠饮食测量每周一给每笼小鼠新鲜饲料称重,周末禁食前称每笼小鼠剩余饲料数,计算平均每周每笼小鼠饮食量。
87.3.8 统计学计算采用spss25.0软件进行统计学分析,graphpad prism8.4软件进行统计图绘制,采
用单因素或多因素方差分析,方差分析采用f检验,实验数据以均数
±
标准差表示, p<0.05认为有统计学意义。
88.实施例4 实验结果4.1 乳杆菌yuyingw治疗td本发明采用高脂饮食联合链脲佐菌素(hfd/stza)建立糖尿病小鼠模型(图5a)。测得其空腹血糖值为16.27
±
0.99mmol/l,p<0.0001,远高于对照组小鼠(4.04
±
0.25mmol/l)(图5b),认定为造模成功。
89.经6周的菌群移植治疗后,测得小鼠禁食过夜后空腹血糖随着治疗进程缓慢下降,其中lab组血糖降至11.84
±
1.29mmol/l,并稳定保持在该血糖水平,bio组(13.58
±
1.02 mmol/l)和fmt组(16.08
±
2.15 mmol/l)的血糖水平较td组(18.68
±
1.21 mmol/l)也有大幅度降低,但相对高于lab组(图5c)。本实验3组菌群移植对hba1c均较td组(9.63
±
0.85)有不同程度的降低效果,但均未降至正常水平,其中lab组(8.1
±
0.61,p<0.001)降幅最大,与血糖结果一致(图5d)。另外,lab组由于高血糖造成的小鼠死亡情况随着治疗进程而减少,小鼠活跃度增加,毛发湿度降低,尿量明显减少,小鼠整体生存状态好转,死亡率低于td组,治疗后期不再出现连续死亡现象。
90.血糖作为检测糖尿病的通用指标,能够准确显示小鼠即刻血糖变化,本发明已经证实菌群移植对于改善td小鼠血糖效果显著,而糖化血红蛋白(glycated hemoglobin,hba1c)是血红蛋白糖化反应的产物,其含量取决于血糖浓度以及与血红蛋白的接触时间,而与空腹、抽血、胰岛素等因素无关。因此,能够有效地反映糖尿病小鼠在过去8
‑
12周平均血糖水平,检测hba1c有助于准确了解各种不同菌群移植对糖尿病的长期影响效果,实验证实乳杆菌yuyingw降低糖化血红蛋白效果最为显著。
91.4.2 乳杆菌yuyingw改善脂质代谢在td小鼠进行6周的菌群移植治疗过程中对体重指标进行监测发现,由于td造成的体重亏损在经菌群移植后得到一定程度的恢复,后期维持在一定水平不再降低并有升高趋势(图6b);饮食量由造模期间的生理打击状态恢复至恒定水平(图6a)。
92.经相同剂量的肠道菌群移植治疗后,小鼠肝组织he染色发现,肝细胞结构有明显正常化趋势并在一定程度上得到修复,肝小叶结构趋于正常化,假小叶减少;油红o染色显示肝脂肪变程度减轻,肝细胞脂滴明显减少(图6c)。在血清学水平上,菌群移植治疗对于肝脂肪化的改善效果同样明显,与非干预组对比,lab组血清学指标tc(2.21
±
0.68 mmol/l,p<0.01)(图6d)、tg(0.4
±
0.15 mmol/l,p<0.01)(图6e)、ldl
‑
c(0.53
±
0.16 mmol/l,p<0.0001)(图6f)水平降低明显,血脂指标的降低说明菌群移植对于脂质代谢的校正作用明显。
93.血脂异常通常与胰岛素抵抗相关,由于胰岛素抵抗和胰岛β细胞损伤造成的过度脂肪在肌肉、肝脏、胰腺等组织中累积,加重了糖尿病的病情。因此,乳酸菌通过改善菌群失调调节脂质代谢,减少异常脂肪堆积,降低血脂水平,减轻肝脏、胰腺等脏器脂肪化负担,有利于改善胰岛素抵抗,恢复胰岛β细胞功能。本发明结果表明,乳杆菌yuyingw菌群移植对改善脂质代谢,逆转非酒精性脂肪肝有明显组织学和血清学效果,脂质代谢的改善作用一定程度改善了胰岛素抵抗,进而表现出优秀的降糖作用。测得血清学胰岛素含量恢复至正常水平,而血糖仍降至中等水平保持稳定并不再进展,是由于益生菌对于肠道微生态环境的
调节作用,改变了肠道微生物代谢水平进而改善了脂质代谢和胰岛素抵抗。
94.4.3 乳杆菌yuyingw改善代谢性内毒素血症肠腔的完整性在维持肠道微生态平衡中发挥重要作用,肠粘液层具有阻挡细菌穿透肠屏障系统进入血液的作用,同时保护肠腔酸碱平衡。定植于肠道粘液层的益生菌可以调节杯状细胞产生粘液,小鼠结肠组织阿利辛蓝粘液染色有助于观察小鼠肠腔粘液层的变化。正常对照组小鼠结肠组织中存在丰厚的蓝色粘液层,杯状细胞体积偏大、排列正常、数量多。糖尿病造模组结肠粘液层消失殆尽,粘液层不完整,肠绒毛变短残缺,褶皱变浅,而经治疗后结肠粘液层厚度均有不同程度的增厚,杯状细胞增加,lab组改善最为显著(图7a)。
95.血清学炎症指标检测小鼠内毒素血症状况发现,经过菌群移植治疗后的小鼠炎症因子有所减轻,其中lab组促炎因子tnf
‑
α(356.41
±
78.6pg/ml,p<0.0001)、il
‑
6(32.88
±
6.45pg/ml)、抑炎因子il
‑
10(18.68
±
3.31 pg/ml ,p<0.0001)较td组(tnf
‑
α:647.21
±
45.41 pg/ml、il
‑
6:37.75
±
5.15pg/ml、il
‑
10:32.97
±
3.52 pg/ml)下降明显(图7bcd),小鼠整体炎症状态好转。血清胰岛素(ins)水平在经过乳酸菌治疗后含量有所升高lab组(47.71
±
7.29mu/l,p>0.05),恢复至正常小鼠水平normal组(47.95
±
7.61 mu/l)(图7e)。
96.肠道菌群中内毒素如 lps引发的内毒素血症会导致多器官炎症损伤,已被证实在胰岛素抵抗和非酒精性脂肪肝的发展中发挥重要作用,促炎因子(如tnf)可诱导胰岛素受体底物 1 (irs
‑
1) 的丝氨酸磷酸化,并在体外将 irs
‑
1 转化为ir酪氨酸激酶活性的抑制剂,增加组织胰岛素抵抗。血清学炎症因子il
‑
6和tnf
‑
α的降低证实乳酸菌移植确实对改善内毒素血症,肠alcian染色提示lab组杯状细胞增加和肠粘膜层增厚,均显示出乳酸菌修复肠屏障系统,改善肠腔炎症环境的优秀作用。肠道菌群中内毒素如 lps引发的内毒素血症会导致多器官炎症损伤,已被证实在胰岛素抵抗和非酒精性脂肪肝的发展中发挥重要作用;促炎因子(如tnf)可诱导胰岛素受体底物 1 (irs
‑
1) 的丝氨酸磷酸化,并在体外将 irs
‑
1 转化为ir酪氨酸激酶活性的抑制剂,增加组织胰岛素抵抗。血清学炎症因子il
‑
6和tnf
‑
α的降低证实乳酸菌移植确实对改善内毒素血症,肠alcian染色提示lab组杯状细胞增加和肠粘膜层增厚,均显示出乳酸菌修复肠屏障系统,改善肠腔炎症环境的优秀作用。测得血清学胰岛素含量恢复至正常水平,而血糖仍降至中等水平保持稳定并不再进展,可能是由于益生菌对于肠道微生态环境的调节作用,改变了肠道微生物代谢水平进而改善了脂质代谢和胰岛素抵抗。
97.上述结果表明,本发明筛选的粪便菌株乳杆菌yuyingw作为肠道原生益生菌,在降糖降脂方面表现出优于已知益生菌和粪菌移植的优秀作用,包括减轻体重,改善脂质代谢、胰岛素抵抗、肠粘膜屏障功能和缓解内毒素血症。通过调节肠微生态系统和肠道炎症状态改善了胰岛功能,达到了降低血糖和改善脂质代谢异常的目的,对预防或治疗糖尿病有明显的积极作用。
98.以上所述仅为本发明的较佳实施例,凡依本发明申请专利范围所做的均等变化与修饰,皆应属本发明的涵盖范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1