一种H9N2亚型禽流感和鸡滑液囊支原体的二联灭活疫苗
一种h9n2亚型禽流感和鸡滑液囊支原体的二联灭活疫苗
技术领域
1.本发明涉及兽用生物制品技术领域,尤其涉及一种h9n2亚型禽流感和鸡滑液囊支原体的二联灭活疫苗。
背景技术:
2.h9n2亚型禽流感病毒(avian influenza virus,aiv)是当前我国禽流感流行的主要亚型,由于病原流行分布范围广,感染鸡群可引起产蛋下降,或降低鸡群抵抗力,引发继发和混合感染现象,h9n2禽流感给养禽业造成了巨大的经济损失,已成为困扰和危害我国规模化养禽场的主要疫病之一。此外,h9n2aiv宿主广泛,可作为其它新型流感病毒的内部基因供体,加快流感病毒的持续性变异,促进新型流感病毒的产生和流行,在公共卫生健康方面同样具有较大的潜在威胁。
3.鸡滑液囊支原体(mycoplasma synoviae,ms)是一种主要引起鸡和火鸡出现呼吸道症状和传染性滑膜炎症状的急性或慢性传染性疾病,其病原可直接侵入鸡类软骨组织,导致家鸡的关节肿大肿胀、滑液囊及腱鞘发炎、跛行和瘫痪,感染该病还会降低蛋鸡产蛋率、影响蛋品质,而且鸡滑液囊支原体可以垂直传播,给病原防控带来很大困难。目前h9n2aiv和ms在全世界鸡场中都广泛存在,而且两种病原均容易发生交叉感染,尤其是在高湿高热的福建省地区,临床常发支原体与流感的混合感染情况,给禽类养殖业造成了严重的经济损失。
4.当前防控禽流感的主要措施之一是使用疫苗免疫接种,但由于经典h9n2亚型商品化疫苗对新发毒株和变异株的免疫效果不佳,导致传统灭活疫苗不能满足当前我国许多地区的免疫防疫需要,所以急需研发与福建省主要流行毒株匹配性更高的疫苗。对于滑液囊支原体引起的疾病和经济损失,目前主要存在三种不同的措施用以预防和控制:鸡场净化,抗生素治疗和预防接种。但由于中国禽业养殖场的规模和管理级别的不同,净化成本高昂,很难建立和维护无ms感染的种鸡群,而抗生素治疗的方法,不仅容易导致菌株产生耐药性,而且存在药物残留影响食品安全的风险。因此疫苗接种同样成为了防控ms的最佳选择。
5.我国目前尚无h9n2亚型禽流感和鸡滑液囊支原体二联灭活疫苗上市。因此研发高效的二联灭活疫苗符合目前养禽业的市场需求,对于我国h9n2亚型禽流感和鸡滑液囊支原体的防控具有重要的意义。
技术实现要素:
6.有鉴于此,本发明的目的在于提出一种实施可靠有效、制备便利且可用于鸡滑液囊支原体病和h9n2的免疫预防的h9n2亚型禽流感和鸡滑液囊支原体的二联灭活疫苗。
7.为了实现上述的技术目的,本发明所采用的技术方案为:
8.一种h9n2亚型禽流感和鸡滑液囊支原体的二联灭活疫苗,其包括抗原和疫苗佐剂。
9.作为一种可能的实施方式,进一步,所述抗原为灭活抗原,其包括灭活的甲型流感
病毒fz株和灭活的滑液囊支原体ms-fj01;其中,甲型流感病毒fz株已保藏于中国典型培养物保藏中心,保藏地址为中国武汉,保藏编号为cctcc no:v 202171,保藏日期为2021年9月26日;滑液囊支原体ms-fj01已保藏于中国典型培养物保藏中心,保藏地址为中国武汉,保藏编号为cctcc no:m 2021210,保藏日期为2021年3月8日。
10.作为一种较优的实施选择,优选的,所述甲型流感病毒fz株和滑液囊支原体ms-fj01采用甲醛灭活。
11.基于上述疫苗组成方案,本发明还提供一种h9n2亚型禽流感和鸡滑液囊支原体的二联灭活疫苗的制备方法,其包括如下步骤:
12.1)将甲型流感病毒fz株用灭菌pbs做1000倍稀释接种于9~11日龄spf鸡胚尿囊腔中,置于37℃孵育,48h后收获鸡胚病毒尿囊液,利用1%鸡红细胞做血凝试验,无菌收集ha效价≥256的病毒尿囊液,再保存于-80℃环境(如低温冰箱)下;然后取用ph值为7.6~7.8的鸡滑液囊支原体培养基,以10比1的比例加入滑液囊支原体ms-fj01,然后置于培养温度为37℃、振荡速度为180r/min的环境下,培养至对数期,即菌液变成橙黄后,再置于4℃保存;
13.2)抗原灭活:向步骤1)制得的鸡胚病毒尿囊液中加入终浓度为0.1%的甲醛溶液,随加随摇,使其充分混合;然后置于37℃恒温摇床中以200~220r/min摇荡灭活12小时后取出,置4℃环境下(如冰箱)保存备用;将含有滑液囊支原体ms-fj01的菌液置于超高数离心机中离心处理菌液,使其浓缩至每毫升活菌含量不低于5
×
10
13
ccu,浓缩后立即在浓缩的菌液中加入终浓度0.2%的甲醛,并在培养温度为37℃、振荡速度为180r/min的条件下,震荡灭活24小时;
14.3)以1:1:5.62的比例分别加入步骤2)灭活的甲型流感病毒fz株病毒液、滑液囊支原体ms-fj01菌液和疫苗佐剂,使用hr-500分散乳化机逐渐从a档到d档开始乳化,令其在低温条件下以15000r/min乳化30分钟。
15.作为一种较优的实施选择,优选的,步骤1)中,所述鸡滑液囊支原体培养基的制备方法为:取脑心浸出液肉汤21g、酵母浸出粉5.6g、1wt%的酚红溶液2ml、50mg/ml的l-半胱氨酸溶液2ml、50mg/ml的精氨酸溶液8ml和250mg/ml的辅酶i溶液0.4ml进行混合,然后定容至900ml,加入灭活的胎牛血清100ml、添加80万单位/l的青霉素,调整ph至7.6~7.8,最后使用0.22μm过滤器过滤至无菌的容器中完成制备。
16.进一步,本发明还提供甲型流感病毒fz株和滑液囊支原体ms-fj01在制备禽流感病毒诊断用阳性血清试剂中的应用。
17.进一步,本发明还提供一种禽类二联灭活疫苗,其包括上述所述的h9n2亚型禽流感和鸡滑液囊支原体的二联灭活疫苗。
18.采用上述的技术方案,本发明与现有技术相比,其具有的有益效果为:
19.1、本发明方案的疫苗能够诱导鸡产生较高水平的抗体,且持续期长,免疫后h9n2禽流感和鸡滑液囊支原体的发病率明显减少,能够有效预防鸡滑液囊支原体的流行。
20.2、国内尚无h9n2亚型禽流感和鸡滑液囊支原体二联灭活疫苗上市,通过本发明的甲型流感病毒fz株与滑液囊支原体ms-fj01制备的二联灭活疫苗可以有效的防控这两种传染病,同时也能弥补养禽行业市场空缺。
附图说明
21.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
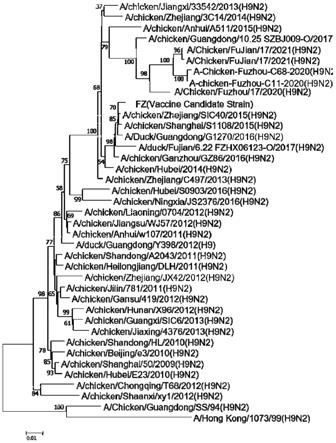
22.图1为本发明方案h9n2亚型禽流感ha基因的进化树分析图;
23.图2为本发明方案h9n2亚型禽流感感染spf鸡后的剖检变化图。
24.图3为本发明方案将鸡滑液囊支原体攻毒至spf鸡后出现的临床症状图;
25.图4为本发明方案鸡滑液囊支原体16s rrna基因的进化树分析图。
具体实施方式
26.下面结合附图和实施例,对本发明作进一步的详细描述。特别指出的是,以下实施例仅用于说明本发明,但不对本发明的范围进行限定。同样的,以下实施例仅为本发明的部分实施例而非全部实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其它实施例,都属于本发明保护的范围。
27.下述实施例中所使用的实验方法如无特殊说明,均为常规方法,同时,下述实施例中所用的材料、试剂,如无特殊说明,均可从商业途径得到。
28.实施例1、h9n2亚型禽流感代表性毒株的鉴定
29.(一)h9n2亚型禽流感毒株的分离鉴定
30.1、样品采集:采集福建省养殖场和家禽门诊的鸡、鸭、番鸭、鹅等的喉头和泄殖腔拭子以及送检病例的肺、气管等脏器。采集的样品保存在加青霉素和链霉素的pbs中,低温运输至实验室,并立即进行病毒的分离鉴定培养。
31.2、h9n2亚型禽流感病毒的分离、鉴定:采集的样品涡旋震荡,12000rpm/min离心1min,取上清接种9日龄spf鸡胚,接种后的鸡胚放置于37℃培养箱培养。48h后收取未致死鸡胚的尿囊液,制作1%鸡红细胞悬液,进行血凝试验,收获具有血凝价的尿囊液,随后利用实验室的h9单因子血清做血凝抑制试验,鉴定ha亚型。经血清鉴定后确定分离到h9亚型禽流感病毒,将尿囊液继续接种10日龄spf鸡胚传代5次,收获稳定的血凝阳性的病毒尿囊液冻存于-80℃冰箱。
32.(二)h9n2亚型禽流感毒株的测序分析
33.1、ha基因组测序:将分离纯化后的h9亚型禽流感病毒,提取病毒rna,用流感病毒保守的12bp引物反转录,获得cdna。然后用片段特异性引物扩增禽流感的ha片段,纯化后用h9n2亚型特异性测序引物进行测序。
34.2、遗传演化分析:测序结果利用dnastar软件包中的seqman软件拼接,序列拼接成完整序列后用mega align分析比较序列的同源性。利用mega 7绘制aiv遗传演化树,根据基因差异性对病毒进行基因型划分。结果如图1所示,该疫苗候选株fz株与近年来福建省h9n2aiv流行毒株遗传关系均较近。
35.(三)h9n2亚型禽流感毒株的致病性分析
36.1、毒株扩繁:将保存的h9n2毒株的尿囊液室温融化,稀释后按照0.1ml/胚接种于10日龄spf鸡胚尿囊腔,接种后置于37℃恒温培养箱孵育。每间隔12h观察一次,弃去24h内
死亡的鸡胚,48h收集血凝效价≥256的鸡胚尿囊液。
37.2、毒株eid
50
测定将含h9n2原毒株fz用pbs进行十倍倍比稀释,稀释度从10-5
至10-9
;每个稀释度接种5枚10日龄spf鸡胚,每枚胚0.1ml;每12h照鸡胚一次,弃去24h内死亡的鸡胚;24h后死亡的鸡胚4℃保存;72h收集尿囊液做血球凝集试验,血凝大于1:8者判定为阳性,根据reed-muench法计算该病毒液鸡胚半数感染量为10
8.5
eid
50
/0.1ml。
38.3、动物感染试验:将h9n2亚型禽流感fz病毒液,通过静脉注射途径每只鸡0.2ml(含有10
6.0
eid
50
),临床观察结果显示观察期内,空白组状况良好,未观察到可见临床症状。fz试验组仅有部分鸡只出现甩头,喷嚏等轻微呼吸道症状,死亡率均为0。剖检变化结果如图2所示,fz试验组鸡气管和喉头内有黏液,喉头有出血点,其它各组织器官均无明显变化。攻毒后5d每组随机采集咽喉拭子,用鸡胚接种的方法检测病毒感染鸡只排毒,结果表明fz试验组5d排毒率达到100%。
39.通过以上各项试验结果表明,所分离的h9n2亚型禽流感毒株属于弱毒株,符合h9n2亚型禽流感病毒特性;将其命名为:甲型流感病毒fz株,其保藏于中国典型培养物保藏中心,保藏地址为中国武汉,保藏编号为cctcc no:v202171,保藏日期为2021年9月26日。
40.实施例2、鸡滑液囊支原体的分离鉴定
41.(一)鸡滑液囊支原体的分离
42.采集福州鸡场疑似感染鸡滑液囊支原体的病鸡肿胀跗关节腔内的关节液及内容物,在无菌操作条件下,接种于改良frey氏液体培养基中,置于37℃恒温振荡培养48h,待菌液由红色变成黄色时,将菌液用0.22μm过滤器过滤,并按滤液与改良frey氏液体培养基体积比为1∶10的比例重新接种到改良frey氏液体培养基中再次培养,收取第2代菌液用于病原菌的鉴定。
43.(二)鸡滑液囊支原体的鉴定
44.1、菌体形态鉴定观察:将分离的第2代菌液涂片,经吉姆萨染色后镜检,观察的菌体形态特征为球形或球杆型。取过滤后的菌种接种于改良frey氏固体培养基上,并置于体积分数为5%的co2培养箱中,37℃条件下培养7d,于显微镜下观察发现细小、光滑、致密的小菌落,表现为“煎蛋样”,半凹陷于培养基内。
45.2、菌体l型鉴定:取分离的第2代菌液接种在不含青霉素和醋酸铊的改良frey氏液体培养基,连续传代培养10次,再将培养菌液接种改良frey氏固体培养基,37℃恒温培养后观察菌落形态并进行涂片镜检。结果表明分离菌为菌体l型阴性。
46.3、人工感染鉴定:取分离的第2代菌液0.5ml,经滴鼻点眼及脚垫内注射接种spf雏鸡,40d后感染鸡出现跛行、瘫痪、关节肿大、龙骨处有干酪样沉积物等明显的临床症状(见图3)。
47.4、16s rrna基因的进化树分析:扩增鸡滑液囊支原体毒株16s rrna基因,对扩增出来的基因序列进行测序,并与其他已知的几种鸡滑液囊支原体毒株进行比对和进化树分析。如图4所示,该鸡滑液囊支原体毒株与亚洲鸡滑液囊支原体毒株具有较高的同源性。
48.通过以上各项鉴定结果表明,所分离的鸡滑液囊支原体毒株均符合鸡滑液囊支原体特性;将其命名为滑液囊支原体ms-fj01;其拉丁名为mycoplasmasynoviae,该滑液囊支原体ms-fj01已保藏于中国典型培养物保藏中心,保藏地址为中国武汉,保藏编号为cctcc no:m 2021210,保藏日期为2021年3月8日。
49.其中,所述改良frey氏液体培养基和改良frey氏固体培养基均为市销常规产品,便不再对其赘述。
50.实施例3、h9n2亚型禽流感和鸡滑液囊支原体二联灭活疫苗
51.(一)种子液制备
52.将纯化后的h9n2毒株fz株病毒尿囊液(实施例1步骤(一)所获得),稀释后按照0.1ml/胚接种于10日龄spf鸡胚尿囊腔,接种后置于37℃恒温培养箱孵育。每间隔12h观察一次,弃去24h内死亡的鸡胚,48h收集血凝效价≥256的鸡胚尿囊液,收集5至15代作为种子批,置于-80℃保存。
53.将滑液囊支原体ms-fj01以1比10的比例加入鸡滑液囊支原体培养基,培养温度为37℃、振荡速度为180r/min、培养至对数期即菌液由红色变成橙黄后收集菌液,记录实际培养时间,收集菌液作为鸡滑液囊支原体种子液,置于4℃保存。
54.其中,所述鸡滑液囊支原体培养基的制备方法为:取脑心浸出液肉汤21g、酵母浸出粉5.6g、1wt%的酚红溶液2ml、50mg/ml的l-半胱氨酸溶液2ml、50mg/ml的精氨酸溶液8ml和250mg/ml的辅酶i溶液0.4ml进行混合,然后定容至900ml,加入灭活的胎牛血清100ml、添加80万单位/l的青霉素,调整ph7.6~7.8,最后使用0.22μm过滤器过滤至无菌的容器中完成制备。
55.(二)毒菌种的扩增培养
56.将保存的h9n2毒株的尿囊液室温融化,按照0.1ml/胚接种于9~11日龄spf鸡胚尿囊腔,接种后置于37℃恒温培养箱孵育。每间隔12h观察一次,弃去24h内死亡的鸡胚,48-72h收集鸡胚尿囊液,结果显示收集的尿囊液血凝效价大于等于256,病毒抗原含量大于等于10
8.5
eid
50
/0.1ml。
57.将鸡滑液囊支原体种子液以1比10的比例加入鸡滑液囊支原体培养基,培养温度为37℃、振荡速度为180r/min、培养至对数期即菌液由红色变成橙黄后收集菌液,取样进行活菌测定:将培养好的ms-fj01株菌液用鸡滑液囊支原体培养基以10倍系列稀释至10
24
,分别将活菌计数试管置于37℃,180r/min振荡培养,观察7日(以培养基颜色由猩红变色到橘黄的最终管作为活菌的最高浓度)。结果显示ms-fj01株活菌量不低于10
12
ccu/ml。
58.(三)支原体菌液浓缩
59.用超高速冷冻离心机于15000g、4℃条件下离心收集的鸡滑液囊支原体菌液30min,最后浓缩鸡滑液囊支原体菌液至每毫升活菌含量不低于5
×
10
13
ccu,浓缩后立即灭活。
60.(四)菌液和毒株灭活
61.向步骤(二)制得的无菌h9n2亚型aiv fz毒株病毒尿囊液中加入终浓度为0.1%的甲醛溶液,随加随摇,使其充分混合。再置于37℃恒温摇床中200~220r/min摇荡灭活12小时后取出,置4℃冰箱保存备用。
62.向步骤(三)制得的浓缩的鸡滑液囊支原体菌液中加入终浓度为0.2%的甲醛,使其充分混合,置于培养温度为37℃、振荡速度为180r/min的培养箱中震荡灭活24小时。
63.(五)灭活检验
64.以3枚/份,0.1ml/枚的标准进行10日龄spf鸡胚尿囊腔接种灭活病毒液,封口标记且置于37℃培养箱培养,连续观察5d,2次/d,5d后收获鸡胚尿囊液,进行ha测定,结果表明,
该病毒液用0.1%的甲醛,置于37℃恒温摇床中200~220r/min摇荡灭活12小时可以充分灭活。
65.将灭活的菌液以1比10的比例接种于鸡滑液囊支原体培养基中,培养14天左右,观察菌体生长情况。结果表明,该菌用0.2%的甲醛,在37℃、振荡速度为180r/min的培养箱中震荡灭活24小时可充分灭活。
66.(六)疫苗制备
67.在无菌的容器中以1:2.81的比例分别加入灭活的h9n2亚型aiv fz株病毒液(疫苗的病毒抗原含量为10
8.0
eid
50
/ml)和疫苗佐剂,使用hr-500分散乳化机逐渐从a档到e档开始乳化,持续30分钟完成疫苗1制备。
68.在无菌的容器中以1:2.81的比例分别加入灭活的滑液囊支原体菌液和疫苗佐剂(疫苗的菌体抗原含量不低于1
×
10
12
ccu/ml),使用hr-500分散乳化机逐渐从a档到e档开始乳化,持续30分钟完成疫苗2制备。
69.在无菌的容器中以1:1:5.62的比例分别加入灭活的h9n2亚型aiv fz株病毒液(疫苗的病毒抗原含量为10
8.0
eid
50
/ml)、鸡滑液囊支原体菌液(疫苗的菌体抗原含量不低于1
×
10
12
ccu/ml)和疫苗佐剂,使用hr-500分散乳化机逐渐从a档到e档开始乳化,持续30分钟完成疫苗3制备。
70.(七)成品检验
71.1、外观:取疫苗各5ml放清洁玻璃管中,观察疫苗的颜色无变化、无杂质等。
72.2、剂型:取清洁吸管,吸取少量疫苗滴入冷水表面,观察疫苗未出现扩散情况。
73.3、稳定性:吸取每批疫苗各10ml加入离心管中,3000r/min离心15分钟,观察疫苗未出现分层情况。
74.4、无菌检验:按现行《中国兽药典》附录进行,均无细菌生长。
75.5、纯粹检验:按现行《中国兽药典》附录进行检验,均符合规定。
76.6、甲醛残留量测定:按现行《中国兽药典》附录进行测定,结果表明符合兽用生物制品通则的规定。
77.7、安全检验:取14日龄spf鸡10只,颈部皮下注射本发明疫苗,每只0.5ml,连续观察14日所有试验鸡精神、采食及饮水均无见明显异常,注射疫苗均未引起的局部或全身不良反应。
78.8、血清抗体效价检验:取14日龄spf鸡40只,随机分成4组,每组10只。第1组颈部皮下注射疫苗1,第2组颈部皮下注射疫苗2,第3组颈部皮下注射疫苗3,第4组不免疫作对照。免疫后每隔一周对第一组、第三组和对照鸡进行采血,分离血清,共采集6周血清后分别测定h9n2亚型禽流感hi抗体和鸡滑液囊支原体elisa抗体效价s/p值。h9n2亚型禽流感hi抗体结果显示,对照组鸡血清,平均hi效价<2,免疫后14天的平均hi效价≥256,免疫后21天的平均hi效价≥512,免疫后21天抗体水平达到峰值,平均hi效价≥512,之后趋于稳定,保持高水平血清抗体。鸡滑液囊支原体elisa抗体结果显示对照组鸡血清,平均s/p值<0.1;免疫组鸡血清,免疫后14天的平均s/p值≥1,免疫后21天的平均s/p值≥1.5,免疫后28天抗体水平达到峰值,平均s/p值≥2.5,之后趋于稳定,符合elisa抗体检测试剂盒标准。
79.9、效力检验:用14日龄spf鸡40只,第1组颈部皮下注射疫苗1,第2组颈部皮下注射疫苗2,第3组颈部皮下注射疫苗3,第4组不免疫作对照。免疫14天后,第1组静脉接种h9n2亚
型禽流感原毒0.2ml(10
6.0
eid
50
/ml),第2组滴鼻点眼接种鸡滑液囊支原体培养物0.5ml(10
12
ccu/ml),第3组分别感染鸡滑液囊支原体培养物0.5ml(10
12
ccu/ml)和h9n2亚型禽流感原毒0.2ml(10
6.0
eid
50
/ml)。攻毒后采集每组鸡咽喉和泄殖腔拭子进行h9n2亚型禽流感的接胚检测,采集每组鸡的咽拭子进行鸡滑液囊支原体的pcr检测。h9n2亚型禽流感的接胚检测结果如表1,鸡滑液囊支原体的pcr检测结果如表2。
80.表1 免疫攻h9n2亚型禽流感后3和5d排毒检测结果统计
[0081][0082]
表2 免疫攻鸡滑液囊支原体的3和5d排毒检测结果统计
[0083][0084]
以上所述仅为本发明的部分实施例,并非因此限制本发明的保护范围,凡是利用本发明说明书及附图内容所作的等效装置或等效流程变换,或直接或间接运用在其他相关的技术领域,均同理包括在本发明的专利保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1