一种羧酸类化合物及其金属盐衍生物的制备方法与流程
1.本发明属于有机合成技术领域,具体涉及一种羧酸类化合物及其金属盐衍生物的制备方法。
背景技术:
2.化合物1和化合物2作为起始原料或重要的中间体,被广泛地应用在一些医药的生产合成中。
3.关于化合物1的制备方法,现有技术中虽有报道,但是不适合工业化生产,例如organic letters,15(6),1266-1269;2013报道如下的合成路线:
[0004][0005]
2-甲基丁内酯经开环、苄基保护,酯化、手性拆分然后再氧化等多步反应得到目标产物,步骤复杂、繁琐;wo2006074940中透露的合成步骤如下:
[0006]
起始原料手性丁二酸单甲酯的价格昂贵,基本也没有实际的产业化意义。
[0007]
关于的制备方法,chemcatchem,9(6),1105-1112;2017报道了化合物2消旋体的制备,
[0008]
该方法需高压和贵金属催化,所以也不是理想的工业化合成方法。
技术实现要素:
[0009]
本发明的目的是提供一种原料易得、步骤简单、安全、且成本低的羧酸类化合物及其金属盐衍生物的制备方法。
[0010]
为达到上述目的,本发明采用的技术方案是:
[0011]
本发明提供一种式iv所示的羧酸类化合物的制备方法,式i所示化合物和式ii所示化合物经缩合反应得到式iii所示化合物,所述的式iii所示化合物经水解脱羧得到iv所示的羧酸类化合物,
[0012][0013]
其中,r1为卤素或磺酸基;
[0014]
r2为c1~c6的烷基;
[0015]
r3为氰基或-coor4,r4为c1~c4烷基。
[0016]
优选地,r1为氯、溴、碘、对甲苯磺酸基或甲基磺酸基;r2为甲基或叔丁基,r3为氰基或-cooch3。
[0017]
优选地,所述的缩合反应在碱性条件下进行,形成所述的碱性条件的碱为强碱,包括钠氢、醇钠、或醇钾中的一种或多种。
[0018]
优选地,所述的缩合反应的温度为40~60℃。
[0019]
进一步地,所述的缩合反应的温度为45~55℃。
[0020]
具体地,所述的制备方法包括:
[0021]
式i所示化合物和式ii所示化合物在碱性条件下和第一有机溶剂存在的条件下发生缩合反应得到式iii所示化合物,
[0022]
式iii所示化合物与碱性化合物在第二有机溶剂存在的条件下反应得到混合物,接着使用酸性化合物调节所述的混合物的ph值为1~2,然后加热回流反应得到含有式iv所示的羧酸类化合物的反应液;
[0023]
进一步地,形成所述的碱性条件的碱为强碱,包括钠氢、醇钠、或醇钾中的一种或多种。
[0024]
进一步地,所述的碱性化合物为氢氧化钠和/或氢氧化钾。
[0025]
进一步地,所述的酸性化合物为盐酸和/或硫酸。
[0026]
进一步地,所述的第一有机溶剂和所述的第二有机溶剂独立地选自四氢呋喃、n,n-二甲基甲酰胺、或甲苯中的一种或多种的混合物。
[0027]
具体地,所述的缩合反应的温度为40~60℃。
[0028]
进一步地,所述的缩合反应的温度为45~55℃。
[0029]
再进一步地,所述的缩合反应的反应时间为2~5小时。
[0030]
再进一步地,式iii所示化合物与碱性化合物反应的反应时间为1~3小时。
[0031]
再进一步地,所述的回流反应的反应时间为0.5~2小时。
[0032]
具体地,式i所示化合物和式ii所示化合物的投料摩尔比为1:0.9~1.2。
[0033]
具体地,所述的式ii所示化合物和所述的第一有机溶剂的投料量之比为0.7~
1.5mol/l。
[0034]
具体地,式i所示化合物以滴加的方式进行投料。
[0035]
式i所示化合物可使用适量的第一有机溶剂溶解或稀释后滴加。
[0036]
进一步地,式i所示化合物在30~40℃下滴加。
[0037]
具体地,所述的制备方法还包括后处理步骤,所述的后处理步骤为反应液分层去水相,有机相浓缩后加入石油醚,析出固体,即为式iv所示的羧酸类化合物。
[0038]
具体地,若式i所示化合物中的r1为磺酸基,所述的制备方法还包括:d-乳酸烷基酯与卤代磺酰在三乙胺和第三溶剂存在的条件下进行d-乳酸烷基酯磺酰化反应。
[0039]
根据一些具体地实施例方式,所述的卤代磺酰为氯代磺酰,具体为对甲苯磺酰氯。
[0040]
具体地,所述的第三溶剂为二氯甲烷、甲苯、四氢呋喃中的一种或多种。
[0041]
具体地,所述的d-乳酸烷基酯磺酰化反应的反应温度为20~50℃。
[0042]
进一步地,所述的d-乳酸烷基酯磺酰化反应的反应温度为30~40℃。
[0043]
进一步地,所述的d-乳酸烷基酯磺酰化反应的反应时间为4~6℃。
[0044]
所述的d-乳酸烷基酯磺酰化反应结束后,加入适量水洗涤有机层,然后加入无水硫酸钠干燥,滤去干燥剂后浓缩得到式i所示化合物。
[0045]
本发明还提供一种式iv所示的羧酸类化合物的金属盐衍生物的制备方法,使用所述的制备方法制备的式iv所示的羧酸类化合物与甲醇盐在第四有机溶剂中反应得到式v所示的羧酸类化合物的金属盐衍生物,m为一价金属离子。
[0046]
具体地,所述的醇盐为甲醇钠和/或乙醇钠。
[0047]
具体地,所述的甲醇盐以质量分数为20~35%的甲醇盐水溶液以滴加的形式进行投料。
[0048]
具体地,所述的第四有机溶剂为甲苯和甲醇的混合溶液。
[0049]
由于上述技术方案运用,本发明与现有技术相比具有下列优点:
[0050]
本发明使用的原料来源广,成本低,反应步骤简单,反应条件温和,无需使用昂贵且危险性高的金属催化剂,本发明的制备方法具有很高的实用价值,尤其适合工业化大规模生产,应用前景广阔。
具体实施方式
[0051]
本说明书中公开了所有特征,或公开的所有方法或过程中的步骤,除了相互排斥的特征或步骤以外,均可以以任何方式组合。
[0052]
由于现有化合物1和化合物2的制备方法存在步骤繁琐、原料昂贵或反应条件苛刻等问题导致生产成本居高不下,不适合工业化生产,制约了一些医药的发展。因此,发明人进行了大量的实验,提出一种新的羧酸类化合物的制备方
法,使用来源广的原料,工艺简单且反应条件温和。
[0053]
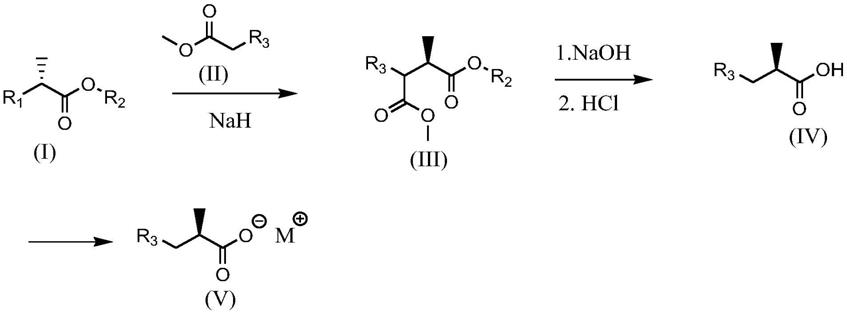
本发明的反应方程为:
[0054][0055]
上述反应式中,r1为卤素或磺酸基;r2为c1~c6的烷基;r3为氰基或-coor4,r4为c1~c4烷基,m为na、k等一价金属离子,羧酸类化合物的收率可达到70%及以上,其金属盐衍生物的收率可达到67%。
[0056]
下面结合具体实施例对本发明的技术方案作进一步的描述,但本发明不应限于这些实施例,除非特别叙述,均可被其他等效或具有类似目的的替代特征加以替换。除非特别叙述,每个特征只是一系列等效或类似特征中一个例子而已。在本发明中所使用的术语,除非另有说明,一般具有本领域普通技术人员通常理解的含义。
[0057]
实施例一、
[0058]
1)d-乳酸叔丁酯磺酰化
[0059][0060]
在反应瓶中加入80ml二氯甲烷、14.2克(100mmol)d-乳酸叔丁酯、12.3克(120mmol)三乙胺,21.9克(115mmol)对甲苯磺酰氯,30℃-35℃反应5小时,加入50克水洗涤有机层,有机层加入无水硫酸钠干燥,滤除干燥剂,浓缩后加入50ml四氢呋喃稀释直接用于下步反应。
[0061]
2)(r)-3-甲基-4-叔丁氧基-4-氧代丁酸的制备
[0062][0063]
在反应瓶中加入80ml四氢呋喃、14.5克(110mmol)丙二酸二甲酯、3.8克60%钠氢(110mmol),35℃滴加实施例一中制备好的的四氢呋喃溶液,滴加完毕,50℃再反应3小时,减压浓缩除去溶剂,加入50ml甲苯和60ml 4n的氢氧化钠溶液,室温反应2小时,滴加盐酸中和至ph=1-2,加热回流1小时,冷却至室温,分去水层,有机层浓缩,加入石油醚析出固体,过滤,干燥得产品13.2克,纯度98%,光学纯度ee%98%。
[0064]
产品氢谱:
[0065]1h nmr(400mhz,cdcl3):11.0(s,1h),2.92-2.77(m,2h),2.64-2.53(m,1h),1.38(s,9h),1.19(s,3h).
[0066]
实施例二、
[0067][0068]
在反应瓶中加入80ml四氢呋喃、14.5克(110mmol)丙二酸二甲酯、3.8克60%钠氢(110mmol),35℃滴加16.6克(100mmol)(r)-2-氯丙酸叔丁酯,滴加完毕,50℃再反应3小时,减压浓缩除去溶剂,加入50ml甲苯和60ml 4n的氢氧化钠溶液,室温反应2小时,滴加盐酸中和至ph=1-2,加热回流1小时,冷却至室温,分去水层,有机层浓缩,加入石油醚析出固体,过滤,干燥得产品14.1克,纯度98%,光学纯度ee%97%
[0069]
产品氢谱:
[0070]1h nmr(400mhz,cdcl3):11.0(s,1h),2.92-2.77(m,2h),2.64-2.53(m,1h),1.38(s,9h),1.19(s,3h).
[0071]
实施例三、(r)-2-甲基-3-氰基丙酸盐的制备
[0072][0073]
在反应瓶中加入80ml二氯甲烷、10.4克(100mmol)d-乳酸甲酯、12.3克(120mmol)三乙胺,21.9克(115mmol)对甲苯磺酰氯,30℃-35℃反应5小时,加入50克水洗涤有机层,有机层加入无水硫酸钠干燥,滤除干燥剂,浓缩后加入50ml四氢呋喃稀释直接用于下步反应。
[0074]
在反应瓶中加入80ml四氢呋喃、10.9克(110mmol)氰乙酸甲酯、3.8克60%钠氢(110mmol),35℃滴加上一步制备好的磺酰化乳酸酯四氢呋喃溶液,滴加完毕,50℃再反应3小时,减压浓缩除去一约半溶剂,加入80ml甲苯和60ml 4n的氢氧化钠溶液,室温反应2小时,滴加盐酸中和至ph=1-2,加热回流1小时,冷却至室温,分去水层,有机层浓缩,加入60ml(1:1)甲苯-甲醇溶液溶解残留物,50℃滴加19克28%甲醇钠溶液,逐渐析出固体钠盐,冷却至室温,过滤,干燥,得产品9.1克,纯度98%光学纯度ee%98%。
[0075]
产品氢谱:
[0076]1h nmr(400mhz,dmso-d6):2.87-2.62(m,2h),2.54-2.43(m,1h),1.14(s,3h).
[0077]
上述实施例只为说明本发明的技术构思及特点,其目的在于让熟悉此项技术的人士能够了解本发明的内容并据以实施,并不能以此限制本发明的保护范围。凡根据本发明精神实质所作的等效变化或修饰,都应涵盖在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1