基于多重扩增子测序技术检测精神类药物相关基因的方法与流程
1.本发明属于基因检测的技术领域,特别是涉及基于多重扩增子测序技术检测精神类药物相关基因的方法。
背景技术:
2.精神疾病已经成为我国的高发疾病,据统计我国成年人中有超过17%的人深受抑郁症、精神分裂症等精神疾病的困扰。药物治疗是目前精神疾病的主要临床手段,但是仍然处于试误法(trial and error)的阶段,药物疗效和不良反应也呈现出显著的个体差异。在精神分裂症患者中,只有33%~50%的患者在足量足疗程的抗精神分裂症药物治疗下可以获得临床症状的完全缓解。导致药物治疗出现巨大个体差异的原因,除了传统上的病理、生理、性别、年龄、身高、体重、依从性等方面外,遗传因素是影响药物反应差异的重要因素。
3.近年来,药物基因组学得到了飞速发展,通过对药物代谢、疗效和不良反应的相关基因检测指导药物的选择和剂量调整,达到个体化治疗的目的。对于临床医生来说如何合理地选择药物、进行剂量调整、临床监测以及合理地控制不良反应显得尤为重要。目前,在美国食品药品监督管理局(fda)批准的药品说明书中,已有超过200种药物被推荐进行药物基因组生物标记物的检测,占据前3位的分别是抗肿瘤药物、精神类药物和心血管类药物。大量的临床数据也都显示了精神科开展个体化药学的紧要性和必要性,但在中国,精神类药物的药物相关基因检测一直没有在临床得到广泛的应用,随着个体化用药基因学检测的临床模式的建立,药物基因组学在指导临床合理用药中将发挥越来越重要的作用,其临床应用和普及将成为趋势。
4.高通量文库构建方法是目前接受度最广、数据表现最稳定、数据偏向性最少的建库方法。本发明基于多重pcr的目标区域捕获及高通量测序技术,检测28个精神类药物治疗相关基因,共68个位点的变异,对受检样品进行精神类药物的种类、剂量、毒副作用、有效性等分析,为临床治疗提供参考。
技术实现要素:
5.本发明的目的在于提供基于多重扩增子测序技术检测精神类药物相关基因的方法,基于多重pcr的目标区域捕获及高通量测序技术,检测28个精神类药物治疗相关基因,共68个位点的变异,对受检样品进行精神类药物的种类、剂量、毒副作用、有效性等分析。
6.为解决上述技术问题,本发明是通过以下技术方案实现的:
7.基于多重扩增子测序技术检测精神类药物相关基因的方法,包括以下几个步骤,
8.(1)提取待测物种样本的基因组dna;
9.(2)对基因组dna进行多重pcr扩增,加入特异性靶向目标区域引物,特异性靶向目标区域引物引导扩增的基因序列针对精神类药物治疗相关基因,特异性靶向目标区域引物对应的5’端分别连接有通用引物序列;
10.以基因组dna为模板,进行第一轮多重pcr反应,得到两端带有通用引物序列的pcr
产物;
11.(3)对第一轮得到的pcr产物进行纯化;
12.(4)以纯化后的第一轮pcr产物为模板,加入测序标签序列引物,测序标签序列引物携带有测序平台可识别的接头序列,测序标签序列引物的两端分别连接与第一轮pcr通用引物序列相匹配的引物序列,进行第二轮pcr反应;
13.(5)纯化步骤(4)得到的第二轮pcr产物,质检合格后上机测序,得到被检测到的基因序列,对比药物基因注释库,得到对受检样品进行精神类药物的种类、剂量、毒副作用、有效性等分析数据。
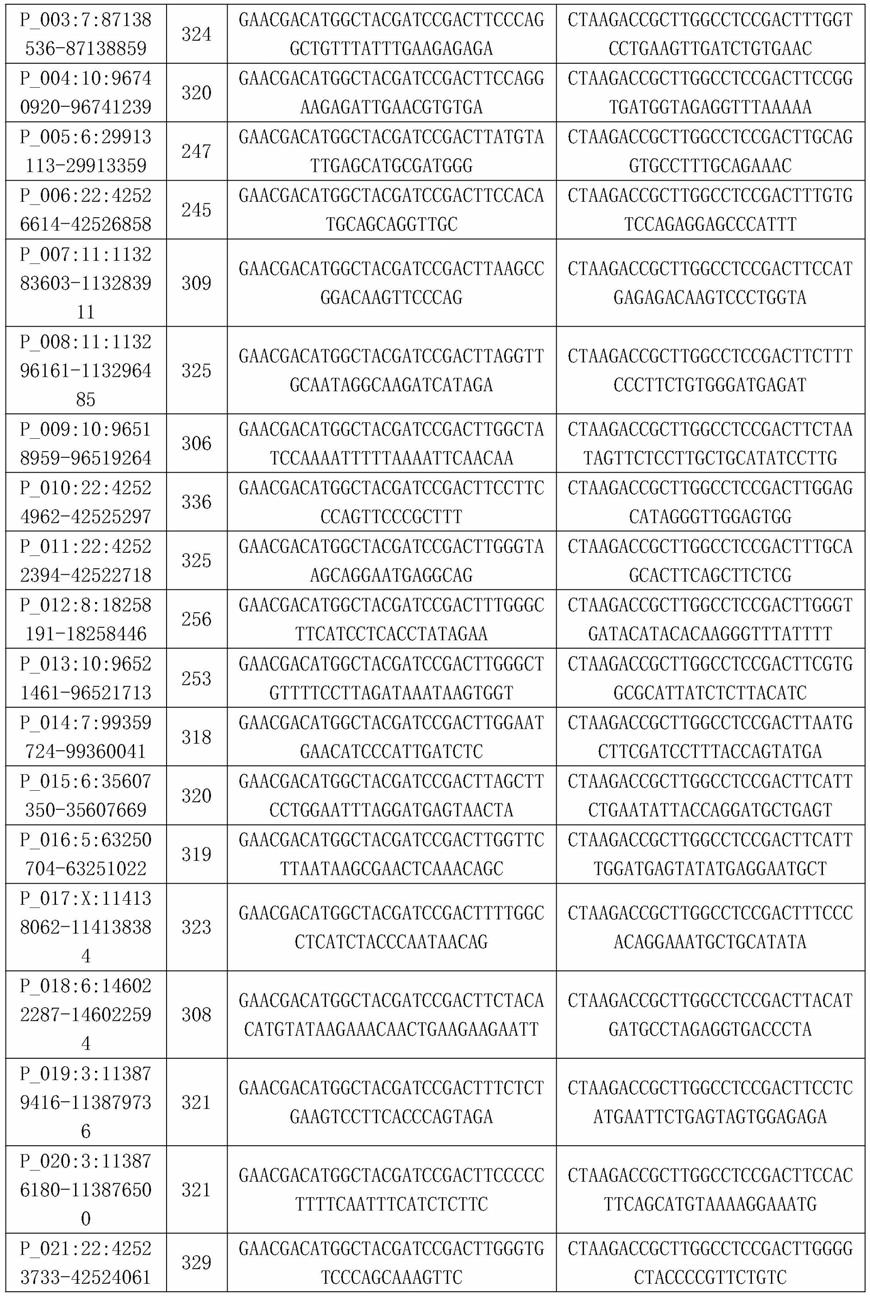
14.进一步地,特异性靶向目标区域引物对应的正向引物f_primer和反向引物r_primer如下:
15.16.17.[0018][0019]
进一步地,特异性靶向目标区域引物对应的正向引物的通用引物序列为f_primer:5
’‑
gaacgacatggctacgatccgactt-特异性靶向目标区域的正向引物-3’,对应的反向引物的通用引物序列为r_primer:5
’‑
ctaagaccgcttggcctccgactt-特异性靶向目标区域的反向引物-3’。
[0020]
进一步地,测序标签序列引物:
[0021]
ad153_pcr2_1:5
’‑
gaacgacatggctacga-3’;index r:5
’‑
tgtgagccaaggagttgnnnnnnnnnnttgtcttcctaagaccgcttggcct-3’,其中,引物ad153_pcr2_1的5
′
端经磷酸化修饰,nnnnnnnnnn为适用于mgiseq-200rs测序平台的接头序列,n代表碱基a、t、g或c。
[0022]
进一步地,第一轮pcr反应的反应条件为:98℃3min;98℃20s,60℃240s,20个循环;72℃2min;
[0023]
第二轮pcr反应的反应条件为:98℃2min;98℃15s,58℃15s,72℃30s,8个循环;72℃2min;4℃保存。98℃进行的是变性,dna解旋阶段,98℃20s,60℃240s,20个循环和58℃15s,72℃30s,8个循环;均为对应的扩增阶段,意思是在对应的两个温度区间不断的循环,最终的72℃均为延伸阶段。
[0024]
进一步地,第一轮得到的pcr产物纯化步骤如下:
[0025]
(1)向反应pcr管加0.6倍原始pcr体积的磁珠(采用agencourt ampure xp)比如:30ul体系加18ul,用移液器上下吹打,充分混匀,室温放置2min;
[0026]
(2)上步骤pcr管,在磁力架上进行磁珠吸附,待溶液澄清,吸取上清至新的pcr管,保留上清,请勿吸到磁珠,将步骤中的磁珠抛弃;
[0027]
(3)上步骤pcr管加入0.5倍体积磁珠,比如:30ul体系加15ul,用移液器上下吹打,充分混匀,室温放置2-5min;
[0028]
(4)将上步骤pcr管,在磁力架上进行磁珠吸附,待溶液澄清,用移液器小心吸取上清抛弃,保留磁珠;
[0029]
(5)将上步骤pcr管,加入100u180%乙醇,用磁力架2-3次快速在pcr管不同的面吸附,以充分洗涤磁珠,静置15s;
[0030]
(6)将上步骤pcr管,在磁力架上进行磁珠吸附,待溶液澄清,用移液器小心吸取上清抛弃,保留磁珠;
[0031]
(7)将上步骤含有磁珠的pcr管,室温静置,待乙醇完全挥发即可。
[0032]
进一步地,第二轮pcr产物纯化步骤如下:
[0033]
(1)向反应pcr管加0.8倍原始pcr体积的磁珠,比如30ul体系加24ul,用移液器上下吹打,充分混匀,室温放置2min;
[0034]
(2)将上步骤pcr管,在磁力架上进行磁珠吸附,待溶液澄清,吸取上清至新的pcr管,保留上清,请勿吸到磁珠,将步骤中的磁珠抛弃;
[0035]
(3)将上步骤pcr管,加入100u180%乙醇,用磁力架2-3次快速在pcr管不同的面吸附,以充分洗涤磁珠,静置15s;
[0036]
(4)将上步骤pcr管,在磁力架上进行磁珠吸附,待溶液澄清,用移液器小心吸取上清抛弃,保留磁珠;
[0037]
(5)将上步骤含有磁珠的pcr管,室温静置,待乙醇完全挥发;
[0038]
(6)向带有磁珠的pcr管,加入20ul te溶液,充分混匀洗涤磁珠,静置2min;
[0039]
(7)向带有磁珠的pcr管,在磁力架上进行磁珠吸附,待溶液澄清,小心吸取上清至新的pcr管中,请勿吸到磁珠,将步骤中的磁珠抛弃即可。
[0040]
进一步地,第一轮pcr反应,采用0.2mlpcr管,在超净台里按照如下体系配置反应:其中基因组dna是一个变量,只要总量在20-200ng之间即可。
[0041][0042][0043]
进一步地,第二轮pcr反应,将带有磁珠的pcr管加入以下pcr体系试剂:
[0044]
第二轮pcr引物
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
1μl
[0045]
不含rnase的水
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
14μl
[0046]2×
kapa热启动hifi高保真酶readymix
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
15μl。
[0047]
本发明具有以下有益效果:
[0048]
本发明方法以药物基因组学和药物遗传学为基础,检测患者的药物相关基因多态性,基于多重pcr的目标区域捕获及高通量测序技术,来源于fda、cfda、pharmgkb、cpic等权威指南、相关数据库和专业文献,对受检样品进行精神类药物的种类、剂量、毒副作用、有效性等分析。较传统的taqman探针-pcr,massarray等检测方法,本方法通量较高,一次检测多个位点的变异信息。
[0049]
当然,实施本发明的任一产品并不一定需要同时达到以上所述的所有优点。
具体实施方式
[0050]
基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其它实施例,都属于本发明保护的范围。
[0051]
用于检测精神类药物的样本来自人源基因组dna,mpcr-js第一、二轮pcr引物由上海何因生物科技有限公司合成,多重pcr mix(kapa热启动hifi高保真酶readymix),agencourt ampure xp(核酸纯化试剂盒)购自美国贝克曼库尔特有限公司,quibt(荧光试剂盒)定量试剂购自南京诺唯赞生物科技有限公司。
[0052]
采用0.2mlpcr管,在超净台里按照如下体系配置反应:
[0053]
第一轮pcr引物8μl人源基因组dna(20-200ng)nμl2
×
kapa热启动hifi高保真酶readymix15μl不含rnase的水add up to 30μl
[0054]
第一轮pcr扩增:pcr反应的反应条件为:98℃3min;98℃20s,60℃240s,20个循环;72℃2min。
[0055]
产物纯化:
[0056]
1)向反应pcr管加0.6倍原始pcr体积的磁珠,30ul体系加18ul,用移液器上下吹打,充分混匀,室温放置2min。
[0057]
2)将上步骤pcr管,在磁力架上进行磁珠吸附,待溶液澄清。吸取上清至新的pcr管,保留上清,请勿吸到磁珠,将步骤中的磁珠抛弃。
[0058]
3)上步骤pcr管加入0.5倍体积磁珠,30ul体系加15ul,用移液器上下吹打,充分混匀,室温放置2-5min。
[0059]
4)将上步骤pcr管,在磁力架上进行磁珠吸附,待溶液澄清,用移液器小心吸取上清抛弃,保留磁珠。
[0060]
5)将上步骤pcr管,加入100u180%乙醇,用磁力架2-3次快速在pcr管不同的面吸附,以充分洗涤磁珠,静置15 sec。
[0061]
6)将上步骤pcr管,在磁力架上进行磁珠吸附,待溶液澄清,用移液器小心吸取上清抛弃,保留磁珠。
[0062]
7)将上步骤含有磁珠的pcr管,室温静置,待乙醇完全挥发。
[0063]
第二轮pcr反应:将带有磁珠的pcr管加入以下pcr体系试剂:
[0064]
mpcr-js第二pcr引物1μl不含rnase的水14μl2
×
kapa热启动hifi高保真酶readymix15μl
[0065]
第二轮pcr扩增:pcr反应的反应条件为:98℃2min;98℃15s,58℃15s,72℃30s,8个循环;72℃2min;4℃保存。
[0066]
第二轮产物纯化:
[0067]
1)向反应pcr管加0.8倍原始pcr体积的磁珠,30ul体系加24ul,用移液器上下吹打,充分混匀,室温放置2min。
[0068]
2)将上步骤pcr管,在磁力架上进行磁珠吸附,待溶液澄清。吸取上清至新的pcr管,保留上清,请勿吸到磁珠,将步骤中的磁珠抛弃。
[0069]
3)将上步骤pcr管,加入100u180%乙醇,用磁力架2-3次快速在pcr管不同的面吸附,以充分洗涤磁珠,静置15 sec。
[0070]
4)将上步骤pcr管,在磁力架上进行磁珠吸附,待溶液澄清,用移液器小心吸取上清抛弃,保留磁珠。
[0071]
5)将上步骤含有磁珠的pcr管,室温静置,待乙醇完全挥发。
[0072]
6)向带有磁珠的pcr管,加入20ul te溶液,充分混匀洗涤磁珠,静置2min。
[0073]
7)向带有磁珠的pcr管,在磁力架上进行磁珠吸附,待溶液澄清,小心吸取上清至新的pcr管中,请勿吸到磁珠,将步骤中的磁珠抛弃。
[0074]
上机测序,数据分析:下机数据质控,结果见表:
[0075]
分别设置不同数据量的样本,以分析不同数据量对两步pcr扩增子建库的影响。根据数据质控结果,q20约为95%以上,q30约为95%以上,超过mgiseq-2000rs测序平台数据质量标准,表明数据结果可靠。
[0076]
检测位点分型结果:
[0077]
检测样本1:试剂盒检测得到如下结果:
[0078]
[0079][0080]
根据上面的结果,我们做出如下判读:
[0081]
药物代谢基因表型
[0082]
[0083][0084]
药物疗效、代谢能力、毒副作用检测结果:
[0085]
[0086]
[0087][0088]
本发明仅受权利要求书及其全部范围和等效物的限制。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1