一种二苯溴甲烷的制备方法与流程
1.本技术涉及有机合成技术领域,尤其涉及一种二苯溴甲烷的制备方法。
背景技术:
2.二苯溴甲烷(bromodiphenylmethane),又名二苯基溴甲烷、溴二苯甲烷、二苯甲基溴、溴化二苯甲烷、溴代二苯甲烷等,其结构式如下:
[0003][0004]
二苯溴甲烷是制备莫达非尼的中间体,是一种重要的医药中间体,与无水哌嗪、苯丙烯氯缩合可得长效多功能的血管收缩拮抗剂桂益嗪,可用于桂益嗪、苯海拉明盐酸盐、百乐利辛、奥沙米特等药物的生产。
[0005]
现有的关于二苯溴甲烷的合成,常以二苯甲烷为原料,二氯甲烷做溶剂,然后加入碱性物质,再与溴化剂进行反应,得到二苯溴甲烷产品。然而采用这种合成路线存在诸多缺点,比如最终得到的产物中含有很多杂质,若直接用于后续医药产物的合成,会对后续反应带来极大干扰,也对医药产物的纯度有影响,此外,这种反应合成路线中所用的物质成本较高,不利于规模化生产销售。
技术实现要素:
[0006]
本技术的目的在于提供一种具有良好经济性且产品纯度高的二苯溴甲烷的制备方法。
[0007]
为实现以上目的,本技术提供了一种二苯溴甲烷的制备方法,包括:
[0008]
以二苯甲烷和溴素为原料,反应得到二苯溴甲烷粗品,提纯得到二苯溴甲烷。
[0009]
优选的,所述反应包括:将所述二苯甲烷加热后,滴加所述溴素,保温搅拌。
[0010]
优选的,所述加热的温度为70℃~130℃;
[0011]
所述滴加的速度为10g/min~100g/min;
[0012]
所述搅拌的时间为50min~80min。
[0013]
优选的,所述提纯包括:
[0014]
将所述二苯溴甲烷粗品与有机溶剂混合,降温后固液分离,收集固体产物。
[0015]
优选的,所述有机溶剂包括甲醇、乙醇和异丙醇中的任意一种。
[0016]
优选的,所述所述有机溶剂与所述二苯甲烷的质量比为(1~3):1。
[0017]
优选的,所述混合之前还包括:将所述二苯溴甲烷粗品冷却至室温,水洗,静置分液,得到有机层。
[0018]
优选的,所述降温后的温度为-15℃~10℃。
[0019]
优选的,所述固液分离的方式为抽滤;
[0020]
优选的,所述固液分离的方式为离心,所述降温之后、所述离心之前还包括第一搅
拌;
[0021]
优选的,所述降温之前还包括第二搅拌;
[0022]
所述第一搅拌的时间为25min~35min;
[0023]
所述第二搅拌的时间为50min~60min。
[0024]
优选的,所述二苯甲烷和所述溴素的摩尔比为1:(1~1.2)。
[0025]
本技术的有益效果:
[0026]
本技术直接采用二苯甲烷和单质溴为原料进行反应得到二苯溴甲烷粗品,然后通过进一步的提纯处理得到二苯溴甲烷纯品。在整个反应过程中,并未引入除反应物以外的其他杂质元素,有助于后续的提纯处理,也有助于二苯溴甲烷产品作为医药中间体进行后续的反应时,不因杂质的存在而干扰后续产品的合成。本技术提供的二苯溴甲烷的制备方法中,反应原料容易获得,价格低廉,反应步骤简单,得到的产品收率较高,纯度较高,具有良好的工业化前景。
附图说明
[0027]
为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对本发明范围的限定。
[0028]
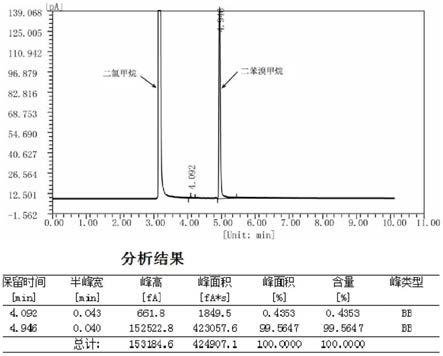
图1为实施例1制备得到的二苯溴甲烷产品的gc谱图;
[0029]
图2为实施例2制备得到的二苯溴甲烷产品的gc谱图;
[0030]
图3为对比例1制备得到的二苯溴甲烷粗品的gc谱图。
具体实施方式
[0031]
如本文所用之术语:
[0032]“由
……
制备”与“包含”同义。本文中所用的术语“包含”、“包括”、“具有”、“含有”或其任何其它变形,意在覆盖非排它性的包括。例如,包含所列要素的组合物、步骤、方法、制品或装置不必仅限于那些要素,而是可以包括未明确列出的其它要素或此种组合物、步骤、方法、制品或装置所固有的要素。
[0033]
连接词“由
……
组成”排除任何未指出的要素、步骤或组分。如果用于权利要求中,此短语将使权利要求为封闭式,使其不包含除那些描述的材料以外的材料,但与其相关的常规杂质除外。当短语“由
……
组成”出现在权利要求主体的子句中而不是紧接在主题之后时,其仅限定在该子句中描述的要素;其它要素并不被排除在作为整体的所述权利要求之外。
[0034]
当量、浓度、或者其它值或参数以范围、优选范围、或一系列上限优选值和下限优选值限定的范围表示时,这应当被理解为具体公开了由任何范围上限或优选值与任何范围下限或优选值的任一配对所形成的所有范围,而不论该范围是否单独公开了。例如,当公开了范围“1~5”时,所描述的范围应被解释为包括范围“1~4”、“1~3”、“1~2”、“1~2和4~5”、“1~3和5”等。当数值范围在本文中被描述时,除非另外说明,否则该范围意图包括其端值和在该范围内的所有整数和分数。
[0035]
在这些实施例中,除非另有指明,所述的份和百分比均按质量计。
[0036]“质量份”指表示多个组分的质量比例关系的基本计量单位,1份可表示任意的单位质量,如可以表示为1g,也可表示2.689g等。假如我们说a组分的质量份为a份,b组分的质量份为b份,则表示a组分的质量和b组分的质量之比a:b。或者,表示a组分的质量为ak,b组分的质量为bk(k为任意数,表示倍数因子)。不可误解的是,与质量份数不同的是,所有组分的质量份之和并不受限于100份之限制。
[0037]“和/或”用于表示所说明的情况的一者或两者均可能发生,例如,a和/或b包括(a和b)和(a或b)。
[0038]
本技术提供了一种二苯溴甲烷的制备方法,包括:以二苯甲烷和溴素为原料,反应得到二苯溴甲烷粗品,提纯得到二苯溴甲烷。
[0039]
只选用二苯甲烷和溴素作为制备二苯溴甲烷的原料,利用卤代烷的反应活性差别,可将二苯甲烷中的一个氢取代为溴原子,得到二苯溴甲烷,反应过程为:
[0040][0041]
在本技术的一个实施例中,该反应具体包括:将二苯甲烷加热后,缓慢滴加溴素,保温搅拌。
[0042]
具体的,将二苯甲烷需要加热至70℃~130℃,例如可以升高至70℃、75℃、80℃、90℃、95℃、100℃、105℃、110℃、115℃、120℃、125℃、130℃或者是70℃~130℃之间的任意值。
[0043]
进一步的,在本技术的一个优选实施例中,将二苯甲烷加热至110℃。
[0044]
需要说明的是,溴素有强氧化性,容易将二苯甲烷中与碳相连的两个氢原子都进行取代,得到二溴二苯基甲烷,为避免二溴二苯基甲烷的产生,在溴素与二苯甲烷进行反应时,尽量将溴素进行缓慢滴加,使得二苯甲烷与溴素先充分进行反应制备得到二苯溴甲烷,而且溴素滴进去后,一般过几分钟才褪色。
[0045]
优选的,在进行缓慢滴加时,滴加速度为10g/min~100g/min,例如可以是10g/min、20g/min、40g/min、60g/min、80g/min、100g/min或者是10g/min~100g/min的任意值。
[0046]
在滴加过程中,整个反应体系要进行保温处理,确保体系温度不下降,同时也要确保体系温度的升高范围不超过5℃。在滴加结束后,需要继续进行保温搅拌,搅拌的时间为50min~80min,例如可以是50min、55min、60min、65min、70min、75min、80min或者是50min~80min之间的任意值。
[0047]
经过研究发现,在以二苯甲烷为原料,以二氯甲烷为溶剂,加入氢氧化钠等碱性物质,再缓慢滴加溴素的合成路线中,氢氧化钠会与溴素发生反应,极大影响了二苯甲烷和溴素之间的反应,所且最终反应结束后的产物中除了二苯溴甲烷之外,还含有其他如二苯甲醇、二溴基二苯甲烷等等杂质产物。然而以二苯甲烷和溴素为原料进行反应时,虽然产物的杂质含量减少,但是依然还是得不到纯度较高的二苯溴甲烷产品,因此需要对反应结束后的二苯溴甲烷粗品进行提纯处理。
[0048]
在本技术的一个实施例中,在进行提纯时,包括:将上述保温搅拌得到的二苯溴甲烷粗品与有机溶剂混合,降温,固液分离,收集固体产物。
[0049]
具体的,在本技术的一个实施例中,本技术所用的有机溶剂包括甲醇、乙醇和异丙
醇中的任意一种。进一步优选的,本技术选用的有机溶剂为甲醇。
[0050]
在整个提纯工艺中,所用的有机溶剂与合成所用原料二苯甲烷的质量比为(1~3):1,例如可以是1:1、1.5:1、2:1、2.5:1、3:1或者是(1~3):1之间的任意值。
[0051]
在进行混合之前,本技术还需要将得到的二苯溴甲烷粗品先冷却至室温,之后向其中加入水,对得到的二苯溴甲烷粗品进行充分洗涤,静置分液后,得到有机层。
[0052]
可以理解的是,用水对二苯溴甲烷粗品进行充分洗涤的原因,就是在整个反应过程中,由于原料中带入的水,或者是外界空气进入的水,会使得产物中会得到一些溶于水的杂质,比如溴化氢等。那么,用水清洗之后,可去除反应产物中的水溶性杂质,只留下可以与有机溶剂混溶的有机层。
[0053]
在将二苯溴甲烷粗品与有机溶剂进行混合后,二苯溴甲烷及其中的杂质可溶解在有机溶剂中,通过进行降温处理,需要将整个混合体系的温度降低至-15℃~10℃,例如可以降温至-15℃、-10℃、-5℃、-4℃、-2℃、0℃、3℃、5℃、8℃、10℃或者是-15℃~10℃之间的任意值。
[0054]
之后,将上述降温后的混合体系进行固液分离。当固液分离的方式为抽滤时,本技术制备方法中的提纯具体包括:将得到的二苯溴甲烷粗品与有机溶剂进行第一搅拌,降温至-15℃~10℃,进行抽滤,收集固体产物。当固液分离的方式为离心时,本技术制备方法中的提纯具体包括:将得到的二苯溴甲烷粗品与有机溶剂进行第一搅拌,降温至-15℃~10℃后,进行第二搅拌,离心,收集固体产物。
[0055]
具体的,第一搅拌的时间为25min~35min,例如可以是25min、27min、30min、33min、35min或者是25min~35min之间的任意值;第二搅拌的时间为50min~60min,例如可以是50min、52min、54min、56min、58min、60min或者是50min~60min之间的任意值。
[0056]
在进行二苯溴甲烷的制备过程中,如果最终制备的产物的产量非常大,为了尽可能减少提纯过程中的损失,常常选用离心的方式,来进行固液分离。
[0057]
需要说明的是,不论是用抽滤还是离心的方式,最终收集的固体产物都是纯度较高的二苯溴甲烷成品,这主要是利用二苯溴甲烷的熔点为33℃~42℃,而选用的有机溶剂以及溶解在有机溶剂中的大多数杂质的熔点都相对比较低,这样就与二苯溴甲烷的熔点有极大差异。当体系温度下降后,有机层中的杂质以及有机溶剂依然会保持为液相,而二苯溴甲烷则根据自身性能,容易析晶变为固相,实现了由二苯溴甲烷粗品到纯度高的二苯溴甲烷成品的转变。
[0058]
在本技术的一个实施例中,本技术制备方法中所用的原料二苯甲烷和溴素的摩尔比为1:(1~1.2),例如可以是1:1、1:1.1、1:1.2或者是1:(1~1.2)之间的任意值。由于1:1的摩尔比,可能会有部分溴素被带走,导致原料反应不完全,影响后续提纯的效果;而1:1.2的摩尔比,又会导致有部分溴素生成二溴产物,使得杂质含量升高,也影响后续提纯效果,所以优选的,二苯甲烷和溴素的最佳摩尔比为1:1.1。
[0059]
为了便于理解本技术,下面将结合具体实施例对本技术的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限制本发明的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
[0060]
实施例1
[0061]
在100l的反应容器里加入30kg二苯甲烷,加热到110℃,然后以100g/min的滴加速度,将31kg溴素缓慢滴加进去,此时温度控制在不超过115℃,滴加结束后,继续保温搅拌1小时,得到二苯溴甲烷粗品。将含二苯溴甲烷粗品的溶液冷却至室温,向其中加入30kg水,进行充分的洗涤,静置后,分离出水层,得到有机层,向有机层中加入60kg的甲醇,充分搅拌30min,然后冷却到-5℃,继续搅拌60min,离心得到33kg的二苯溴甲烷产品。
[0062]
本实施例利用气相色谱仪来测试制备得到的二苯溴甲烷产品纯度,如图1所示,最终产品的gc纯度为99.56%,摩尔收率为74.9%。
[0063]
实施例2
[0064]
在500ml的四口瓶中加入100g二苯甲烷,加热到110℃,然后以80g/min的滴加速度,缓慢将104g溴素滴加进去,此时温度控制在不超过115℃,滴加结束后,继续保温搅拌1小时,得到二苯溴甲烷粗品。将含二苯溴甲烷粗品的溶液冷却至室温,向其中加入100g水,进行充分的洗涤,静置后,分离出水层,得到有机层,向有机层中加入200g的甲醇,充分搅拌30min,然后冷却到-5℃,进行抽滤处理,得到110g的二苯溴甲烷产品。
[0065]
本实施例利用气相色谱仪来测试制备得到的二苯溴甲烷产品,如图2所示,最终产品的gc纯度为98.87%,摩尔收率为74.8%。
[0066]
实施例3
[0067]
在500ml的四口瓶中加入100g二苯甲烷,加热到110℃,然后以80g/min的滴加速度,缓慢将95g溴素滴加进去,温度控制在不超过115℃,滴加结束后,继续保温搅拌1小时,得到二苯溴甲烷粗品。将含二苯溴甲烷粗品的溶液冷却至室温,向其中加入100g水,进行充分的洗涤,静置后,分离出水层,得到有机层,向有机层中加入200g的甲醇,充分搅拌30min,然后冷却到-5℃,进行抽滤处理,得到75g的二苯溴甲烷产品。
[0068]
本实施例制备得到的二苯溴甲烷产品的摩尔收率为51%。
[0069]
实施例4
[0070]
在500ml的四口瓶中加入100g二苯甲烷,加热到110℃,然后以80g/min的滴加速度,缓慢将114g溴素滴加进去,温度控制在不超过115℃,滴加结束后,继续保温搅拌1小时,得到二苯溴甲烷粗品。将含二苯溴甲烷粗品的溶液冷却至室温,向其中加入100g水,进行充分的洗涤,静置后,分离出水层,得到有机层,向有机层中加入200g的甲醇,充分搅拌30min,然后冷却到-5℃,进行抽滤处理,得到70g的二苯溴甲烷产品。
[0071]
本实施例制备得到的二苯溴甲烷产品的摩尔收率为47.6%。
[0072]
实施例5
[0073]
在500ml的四口瓶中加入100g二苯甲烷,加热到110℃,然后以80g/min的滴加速度,缓慢将104g溴素滴加进去,温度控制在不超过115℃,滴加结束后,继续保温搅拌1小时,得到二苯溴甲烷粗品。将含二苯溴甲烷粗品的溶液冷却至室温,向其中加入100g水,进行充分的洗涤,静置后,分离出水层,得到有机层,向有机层中加入200g的乙醇,充分搅拌30min,然后冷却到-5℃,进行抽滤处理,得到108g的二苯溴甲烷产品。
[0074]
本实施例制备得到的二苯溴甲烷产品的摩尔收率为73.5%。
[0075]
实施例6
[0076]
在500ml的四口瓶中加入100g二苯甲烷,加热到110℃,然后以80g/min的滴加速度,缓慢将104g溴素滴加进去,温度控制在不超过115℃,滴加结束后,继续保温搅拌1小时,
得到二苯溴甲烷粗品。将含二苯溴甲烷粗品的溶液冷却至室温,向其中加入100g水,进行充分的洗涤,静置后,分离出水层,得到有机层,向有机层中加入200g的异丙醇,充分搅拌30min,然后冷却到-5℃,进行抽滤处理,得到100g的二苯溴甲烷产品。
[0077]
本实施例制备得到的二苯溴甲烷产品的摩尔收率为68.1%。
[0078]
实施例7
[0079]
在500ml的四口瓶中加入100g二苯甲烷,加热到70℃,然后以80g/min的滴加速度,缓慢将104g溴素滴加进去,温度控制在不超过75℃,滴加结束后,继续保温搅拌1小时,得到二苯溴甲烷粗品。将含二苯溴甲烷粗品的溶液冷却至室温20℃,向其中加入100g水,进行充分的洗涤,静置后,分离出水层,得到有机层,向有机层中加入200g的甲醇,充分搅拌30min,然后冷却到-5℃下,进行抽滤处理,得到108g二苯溴甲烷产品。
[0080]
本实施例制备得到的二苯溴甲烷产品摩尔收率为73.5%。
[0081]
实施例8
[0082]
在500ml的四口瓶中加入100g二苯甲烷,加热到90℃,然后以80g/min的滴加速度,缓慢将104g溴素滴加进去,温度控制在不超过95℃,滴加结束后,继续保温搅拌1小时,得到二苯溴甲烷粗品。将含二苯溴甲烷粗品的溶液冷却至室温20℃,向其中加入100g水,进行充分的洗涤,静置后,分离出水层,得到有机层,向有机层中加入200g的甲醇,充分搅拌30min,然后冷却到-5℃下,进行抽滤处理,得到108.5g二苯溴甲烷产品。
[0083]
本实施例制备得到的二苯溴甲烷产品的摩尔收率为73.8%。
[0084]
实施例9
[0085]
在500ml的四口瓶中加入100g二苯甲烷,加热到110℃,然后以80g/min的滴加速度,缓慢将104g溴素滴加进去,温度控制在不超过115℃,滴加结束后,继续保温搅拌1小时,得到二苯溴甲烷粗品。将含二苯溴甲烷粗品的溶液冷却至室温,向其中加入100g水,进行充分的洗涤,静置后,分离出水层,得到有机层,向有机层中加入200g的甲醇,充分搅拌30min,然后冷却到-15℃,进行抽滤处理,得到109g的二苯溴甲烷产品。
[0086]
本实施例制备得到的二苯溴甲烷产品的摩尔收率为74.1%。
[0087]
实施例10
[0088]
在500ml的四口瓶中加入100g二苯甲烷,加热到110℃,然后以80g/min的滴加速度,缓慢将104g溴素滴加进去,温度控制在不超过115℃,滴加结束后,继续保温搅拌1小时,得到二苯溴甲烷粗品。将含二苯溴甲烷粗品的溶液冷却至室温,向其中加入100g水,进行充分的洗涤,静置后,分离出水层,得到有机层,向有机层中加入200g的甲醇,充分搅拌30min,然后冷却到5℃,进行抽滤处理,得到105g的二苯溴甲烷产品。
[0089]
本实施例制备得到的二苯溴甲烷产品的摩尔收率为71.5%。
[0090]
对比例1
[0091]
在500ml的四口瓶中加入100g二苯甲烷,加热到110℃,然后以80g/min的滴加速度,缓慢将104g溴素滴加进去,温度控制在不超过115℃,滴加结束后,继续保温搅拌1小时,然后用水清洗,得到140g的二苯溴甲烷粗品。
[0092]
本对比例利用气相色谱仪来测试制备得到的二苯溴甲烷粗品,如图3所示,样品的gc纯度为72.44%,样品摩尔收率为95.2%。
[0093]
试验结果分析:
[0094]
实施例2-10中设计了不同的原料摩尔配比、不同有机溶剂、不同反应温度与析晶提纯温度的试验。表1中列出了原料摩尔配比与摩尔收率的关系,表2中列出了不同有机溶剂与摩尔收率的关系,表3中列出了反应温度与摩尔收率的关系,表4列出了析晶提纯温度与摩尔收率的关系。通过比较表中的结果,可以表明本技术在原料摩尔配比为1:1.1、反应温度为110℃、使用甲醇在-5℃下进行提纯时,可以得到收率较高的二苯溴甲烷产品。
[0095]
表1原料摩尔配比与摩尔收率的关系
[0096] 实施例3实施例2实施例4投料配比1:11:1.11:1.2收率51%74.8%47.6%
[0097]
表2不同有机溶剂与摩尔收率的关系
[0098] 实施例2实施例5实施例6溶剂甲醇乙醇异丙醇收率74.8%73.5%68.1%
[0099]
表3反应温度与收率的关系
[0100] 实施例7实施例8实施例2反应温度70℃90℃110℃收率73.5%73.8%74.8%
[0101]
表4析晶提纯温度与收率的关系
[0102] 实施例9实施例2实施例10析晶温度-15℃-5℃5℃收率74.1%74.8%71.5%
[0103]
本技术对实施例1-2以及对比例1中得到的样品利用气相色谱仪进行了检测。其中实施例1的样品检测结果如图1所示,实施例2的样品检测结果如图2所示,在检测这两个样品时,使用了二氯甲烷进行样品的稀释溶解,因此在图1和图2的谱图中出现了非常明显的二氯甲烷的波峰。对比例1的样品检测结果如图3所示,在样品检测时,使用了甲醇进行样品的稀释溶解,因此在图3的谱图中出现了甲醇的波峰。
[0104]
通过将图1、图2和图3进行对比,可以明显发现图3中的杂质峰较多,且二苯溴甲烷的纯度低,表明了本技术对制备得到的二苯溴甲烷粗品进一步地进行提纯后,最终可以得到纯度高的、杂质少的二苯溴甲烷产品。
[0105]
实施例1是在实施例2的基础上大批量进行制备,最终的检测结果以及摩尔收率都表明了本技术的制备方法是稳定的、可靠的,可适用于大规模生产。
[0106]
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
[0107]
此外,本领域的技术人员能够理解,尽管在此的一些实施例包括其它实施例中所包括的某些特征而不是其它特征,但是不同实施例的特征的组合意味着处于本发明的范围
之内并且形成不同的实施例。例如,在上面的权利要求书中,所要求保护的实施例的任意之一都可以以任意的组合方式来使用。公开于该背景技术部分的信息仅仅旨在加深对本发明的总体背景技术的理解,而不应当被视为承认或以任何形式暗示该信息构成已为本领域技术人员所公知的现有技术。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1