一种预防呼吸道合胞病毒的rAAV载体疫苗的制作方法
一种预防呼吸道合胞病毒的raav载体疫苗
技术领域
1.本发明涉及一种预防呼吸道合胞病毒rsv的raav载体疫苗。
背景技术:
2.呼吸道合胞病毒(respiratory syncytial virus,rsv)于1955年首次被发现(morris et al,1956),属于副黏病毒科(paramyxoviridae),肺炎病毒亚科(pneumovirinae),肺炎病毒属(pneumovirus),依据g蛋白的序列分a和b两个亚型。rsv广泛在世界各地广泛流行,是全球范围内引起呼吸道感染(respiratory tract infection,rti)的病毒性病原体,是导致5岁以下儿童和老人呼吸系统疾病住院的最主要原因,感染主要引起下呼吸道感染症状,其中严重症状的患者占有相当高的比例(如毛细支气管炎和肺炎),需要住院治疗,具有较高的死亡率。rsv也可感染成年人,引起的症状及危害比流感还严重。对于患有先天性心脏病、慢性肺病和特异性病史等人群,rsv感染的风险也大大增加。rsv在全球范围内广泛传播和流行,已经成为世界性的公共卫生问题,rsv的危害已经引起了世界卫生组织(who)以及全球各级卫生管理部门的高度关注和重视。
3.rsv为非节段性的负链rna病毒,其基因组长度为15.2kb,有10个基因,共编码11种蛋白,包括非结构蛋白(ns1,ns2)、核蛋白(n)、磷蛋白(p)、基质蛋白(m)、rna 依赖rna 聚合酶(l)、转录延伸因子(m2-1)、调控因子(m2-2)和3种包膜糖蛋白(黏附蛋白(g)、融合蛋白(f)和小疏水蛋白(sh))。病毒为100-350nm的球形颗粒,但通常占主导地位的病毒颗粒是直径为60~200nm,长度大于10μm的丝状结构。rsv可以通过人与人之间接触传播,或者通过咳嗽或打喷嚏而吸入传播,也可通过接触污染物而获得感染,主要感染鼻腔以及肺部大、小气道的上皮细胞,也可能感染肺泡巨噬细胞和肺部其它类型的细胞,可引起细胞融合在一起形成合胞体。
4.rsv包膜下面有n、p、l、m和m2-1蛋白,而f、g和sh蛋白表达在病毒包膜表面,由于f蛋白为融合蛋白,感染细胞后产生独特的细胞融合病变;g蛋白为吸附性蛋白,可与细胞表面的受体结合;f蛋白为典型的副粘病毒融合性糖蛋白,由f1和f2两段蛋白组成,中间由弗林蛋白酶(furin)酶切位点相连;f1的n端是由连续的19个疏水氨基酸组成的具有融合活性的肽段,c端由连续23个疏水氨基酸组成的肽段,介导病毒与细胞膜融合、病毒的穿入及合胞体的形成;而g蛋白与rsv感染的机理有关,并决定了rsv抗原的多样性。
5.rsv感染主要是由病毒表面f、g蛋白引发,刺激机体产生血清中和抗体及呼吸道黏膜的分泌型iga;f蛋白在诱发免疫保护、高水平血清中和抗体方面起着重要作用;同时rsv f和g蛋白,是激发机体产生保护性抗体的最主要的抗原,且g蛋白所诱导的中和抗体具有型特异性;f蛋白高度保守,中和抗体识别位点主要分布于f1片段,且所诱导的中和抗体可同时抑制a、b两个亚型的病毒感染。小疏水蛋白(sh)是另一个可能的疫苗靶点,包含跨膜结构域和胞外结构域,与病毒在体内的复制和炎症激活方面起作用,可能诱导抗体依赖的细胞介导细胞毒作用(adcc),因此,其胞外域已被用作抗原研究也具有潜在的应用价值。
6.疫苗研究是目前rsv防治研究最为集中的领域,早在20世纪60年代,福尔马林灭活
rsv疫苗(fi-rsv)被研制出来进行临床研究,这也是首个进入临床试验的rsv疫苗,但该疫苗不仅没有产生对rsv疾病的保护作用,且在后来的自然感染中,接种过疫苗的儿童发生了严重的疾病增强(erd)现象,住院率明显增加,甚至引起死亡,因此,该疫苗最终未能进入临床应用。
7.近年对rsv疫苗研究的方向更加的广泛和深入,包括减毒活疫苗、灭活疫苗、嵌合载体疫苗、亚单位疫苗、病毒样颗粒疫苗、复制缺陷型病毒载体疫苗、核酸疫苗等作为候选疫苗,目前都处于临床前或临床试验阶段,其中减毒活疫苗、重组蛋白疫苗和嵌合载体疫苗是近年rsv疫苗研究的热点方向;而g蛋白和f蛋白能够诱发良好的体液免疫和细胞免疫反应,是重组蛋白疫苗技术的主要目标抗原。
8.基于rsv的f蛋白和g蛋白开发的亚单位疫苗能够诱导产生中和抗体和保护性抗体,用它们制备的亚单位疫苗包括特异性g蛋白或纯化f蛋白,由于f蛋白相当保守,在疫苗应用研究中更受欢迎,而基于这f和g两种蛋白的亚单位疫苗和减毒活疫苗最有前途,已经被应用于临床研究试验阶段;重组rsv纳米颗粒疫苗,是由f蛋白组成的低聚物颗粒,不仅可诱导高活性的中和抗体,还能够防止肺部感染,可用于母婴传递和老年人预防rsv的感染;表达rsv f蛋白和g蛋白的腺病毒载体和痘病毒载体疫苗,能够诱导良好的体液免疫和细胞免疫反应,且无erd现象,也是理想的疫苗候选疫苗品种;开发编码rsv抗原的dna或mrna的核酸疫苗的目标是能够有效保护儿童和老年人群rsv的感染。
9.目前,rsv疫苗是市场呼声最高的疫苗产品之一,也是who疫苗研发计划大力支持和倡导的品种。近些年,随着反向遗传学、疫苗学、分子病毒学、基因组学、免疫学等技术水平的不断提升和发展,预防rsv感染的疫苗开发也取得了重大的突破,许多的产品在临床研究试验阶段表现出了良好免疫原性和临床应用潜力。
10.腺相关病毒(adeno-associated virus,aav)属于细小病毒属,病毒颗粒直径为22nm左右,属于复制缺陷型二十面体无包膜单链dna病毒,已经发现的aav血清型有12种,目前,还未发现aav对人类致病。但不同的aav载体具有不同的衣壳蛋白空间结构、序列和组织特异性。重组aav以衣壳为载体,将病毒包装的基因组传送到细胞核进行复制。aav具有三层蛋白质外壳(vp1、vp2和vp3),包围并保护一个约4.7kb大小的单链dna基因组。
11.对野生型aav进行基因工程改造的重组型aav是基因传递和表达的一个重要载体,其具有广泛的宿主范围及组织感染能力,既能感染分裂细胞,也能转导外源基因进入非分裂细胞,长期表达外源基因,而不依赖于宿主细胞活跃的分裂能力。
12.raav相对于其它病毒载体具有安全性高、免疫原性低、宿主范围广,能稳定表达和物理性质稳定的优点。目前,已有3款基于aav载体的基因药物在国外批准上市,并且有多个基于aav的药物在临床研究阶段,因此,aav载体被美国fda认为是用于人体基因治疗的最安全的病毒载体之一。而根据文献报道(karen nieto and anna salvetti),基于aav载体的疫苗可以稳定在体内表达抗原,并能够诱导机体产生持久和稳定的免疫反应。
13.rsv疫苗面临的最重要难点目前认为是免疫持续的时间短以及诱导的th1和th2免疫反应不平衡的问题,而基于raav载体的rsv疫苗能够诱导持久的免疫反应和以及病毒载体疫苗在改变th1和th2免疫反应平衡方面具有明显的优势,该疫苗已然成为rsv最有希望的疫苗品种。然而rsv的基因组较大,难以有效被aav载体包裹。
14.一直以来,raav的制备存在生产工艺复杂、限制因素多等方面的技术瓶颈,而基于
raav的疫苗涉及疫苗抗原序列筛选和raav大规模生产两方面的难题,会更具有难度。
技术实现要素:
15.本发明的目的在于克服现有技术的至少一个不足,提供一种预防呼吸道合胞病毒的载体疫苗。
16.本发明所采取的技术方案是:本发明的第一个方面,提供:一种rsv抗原,其氨基酸序列选自如下述氨基酸序列的至少一条,或者至少具有90%、95%、98%、99%同源性的氨基酸序列:rsv f抗原多肽序列,能够诱导针对f蛋白、f1、f2蛋白的特异性抗体及针对rsv的中和抗体和免疫保护效果,选自:使用连接序列gs替代f蛋白furin位点氨基酸得到的融合蛋白;使用连接序列gs替代f蛋白furin位点及其后融合区连接的10个氨基酸得到的融合蛋白;使用2a连接序列替代f蛋白furin位点氨基酸得到的抗原多肽;使用2a连接序列替代f蛋白furin位点及其后融合区连接的10个氨基酸得到的抗原多肽;f1蛋白的c-末端残基添加foldon三聚化结构域得到的抗原多肽;f1蛋白的n-末端添加ige信号肽序列、c-末端残基添加foldon三聚化结构域得到的抗原多肽;f蛋白furin b酶切位点突变为kkqkqq(seq id no.:1)得到的抗原多肽;rsv g抗原多肽序列,能够诱导针对g蛋白的特异性抗体及针对rsv的中和抗体和免疫保护效果,选自:在rsv的g蛋白的n-末端添加ige信号肽序列得到的抗原多肽;rsv sh抗原多肽序列,能够诱导针对sh蛋白的特异性抗体及针对rsv的中和抗体和免疫保护效果,选自:rsv的sh蛋白与免疫球蛋白igg fc区的融合蛋白;优选的,sh蛋白与免疫球蛋白igg fc区通过连接序列偶连;优选的,所述连接序列紧邻sh c-末端与fc的n-末端,选自长度为1~20 aa的合适序列;特别的,所述连接序列的氨基酸序列选自gggsgggsgggsgs(seq id no.:2)、gggsgggs(seq id no.:3)、gggsgggsgg(seq id no.:4)、gggsgggsgggs(seq id no.:5)。
17.在一些实例中,连接序列gs为gs连接子,优选的,其氨基酸序列选自gggsgggsgggsgs、gggsgggs、gggsgggsgg、gggsgggsgggs。
18.在一些实例中,2a连接序列的氨基酸序列为含d-x-e-x-n-p-g-p(seq id no.:6)的氨基酸序列,优选的,其序列为gsgatnfsllkqagdveenpgp(seq id no.:7)所示。
19.本发明的第二个方面,提供:表达本发明第一个方面所述rsv抗原的核苷酸序列。
20.在一些实例中,所述核苷酸序列还包括aav的反向末端重复序列(itr)、信号肽序列中的至少一种。
21.在一些实例中,所述aav的反向末端重复序列(itr)源自aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8、aavrh8、aavrh8r、aav9、aav10、aavrh10、aav11、aav12、aav2r471a、aavdj、aavdj/8血清型,优选的,itr为aav2血清型的itr。
22.在一些实例中,所述信号肽序列选自人白介素2信号肽和/或人免疫球蛋白e(ige)信号肽;优选的信号肽为ige信号肽,具体的氨基酸序列为mdwtwilflvaaatrvhs(seq id no.:8)。
23.在一些实例中,所述核苷酸序列针对人类细胞进行密码子优化。
24.在一些实例中,所述核苷酸序列如seq id no.:9和seq id no.:10所示。
25.本发明的第三个方面,提供:一种预防呼吸道合胞病毒的非复制型重组腺相关病毒载体疫苗,至少具有aav衣壳和rsv 抗原核苷酸序列,所述aav衣壳内包装有本发明第二个方面所述的核苷酸序列,或编码rsv的f蛋白、f1蛋白、f2蛋白、g蛋白、sh蛋白的核苷酸序列。
26.在一些实例中,所述aav衣壳蛋白序列源自aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8、aav9、aavrh10、aavdj/8等血清型,优选的为aav5血清型。
27.在一些实例中,其具有的核酸包括但不限于dna、rna、cdna、gdna、ssdna、dsdna或其任何组合,优选的,所述的重组腺相关病毒为ssaav和scaav。
28.在一些实例中,其表达盒可以携带在递送至包装宿主细胞的任何合适载体上;可以改造用于本发明的质粒,使得它们适于在原核细胞、昆虫细胞、哺乳动物细胞体外复制和包装。
29.在一些实例中,还包括可接受的病毒稀释剂、缓冲液、保护剂、稳定剂、赋形剂中的至少一种组分。
30.在一些实例中,所述非复制型重组腺相关病毒载体疫苗被配制用于肌肉注射或静脉内使用。
31.在一些实例中,所述非复制型重组腺相关病毒载体疫苗被配制用于鼻内接种使用。
32.在一些实例中,所述非复制型重组腺相关病毒载体疫苗还包括容器。
33.在一些实例中,所述非复制型重组腺相关病毒载体疫苗还包括使用说明。
34.本发明的第四个方面,提供:本发明第三个方面所述的非复制型重组腺相关病毒载体疫苗在制备预防rsv制剂中的应用。
35.本发明的第五个方面,提供:一种预防rsv感染的方法,包括使用本发明第三个方面所述的非复制型重组腺相关病毒载体疫苗对适合接种的人群进行接种。
36.在一些实例中,包括使用的有效剂量的要求及使用方法。
37.在一些实例中,接种的剂量约为109~10
12
vg。
38.在一些实例中,接种的次数为1~2次。
39.在一些实例中,接种的途径包括鼻内给药、肌肉接种和静脉注射。
40.本发明的有益效果是:本发明一些实例的抗原,其编码核酸可以有效地被包裹在aav衣壳内,同时其具有
更为稳定的结构。
41.本发明一些实例的抗原,在体内合成后可以酶切/自切为2段,之后通过二硫键连接形成post-f,而后再聚合形成稳定的三聚体结构。
42.本发明一些实例的抗原,可以形成稳定的蛋白多肽/融合蛋白。
43.(1)以rsv f、f1和f2抗原多肽为基础进行优化和突变的多肽序列/融合蛋白,为以下氨基酸中的一种,能够诱导针对f蛋白、f1蛋白、f2蛋白的特异性抗体及针对rsv的中和抗体和免疫保护效果:
①
rsv-f2-gs-f1是用gs连接序列(seq id no.:2)替代f蛋白furin位点氨基酸,形成稳定的pre-f融合蛋白;
②
rsv-f2-2a-f1是用2a连接序列(seq id no.:7)替代f蛋白furin位点氨基酸,2a序列自切为f1和f2,而后f1和f2通过二硫键连接,而后再聚合形成稳定的三聚体抗原蛋白结构;
③
rsv-f1-foldon是f1的c-末端残基添加foldon三聚化结构域( saiggyipeaprdgqayvrkdgewvllstfl,seq id no.:11),而形成更加稳定的抗原蛋白结构;
④
rsv-ige-sp f1-foldon 是f1的n-末端添加ige信号肽序列(seq id no.:8),c-末端残基通过添加foldon三聚化结构域(seq id no.:11);
⑤
rsv-f2-2a-f1-10是用2a连接序列(seq id no.:7)替代f蛋白furin位点氨基酸,同时删除f蛋白furin位点后融合区10个氨基酸(137~146)的抗原多肽;
⑥
rsv-f2-gs-f1-10是用gs连接序列(seq id no.:15)替代f蛋白furin位点氨基酸,同时删除融合区10个氨基酸(137~146)形成稳定的pre-f融合蛋白;
⑦
rsv-f mutation是将f蛋白furin b酶切位点突变为kkqkqq;(3)rsv g抗原多肽序列为以下氨基酸序列中的一种:
①
rsv g 蛋白;
②
rsv-ige sp g是在g蛋白的n-末端添加ige信号肽序列(seq id no.:8); 能够诱导针对g蛋白的特异性抗体及针对rsv的中和抗体和免疫保护效果:(4)rsv sh抗原多肽序列为以下氨基酸序列中的一种:
①
rsv sh蛋白;
②
rsv-sh-fc是sh的c-末端与免疫球蛋白igg fc区(seq id no.:12)通过连接序列(seq id no.:3)相连的融合蛋白;优选的,连接序列为gggsgggs;能够诱导针对sh蛋白的特异性抗体及针对rsv的中和抗体和免疫保护效果。
附图说明
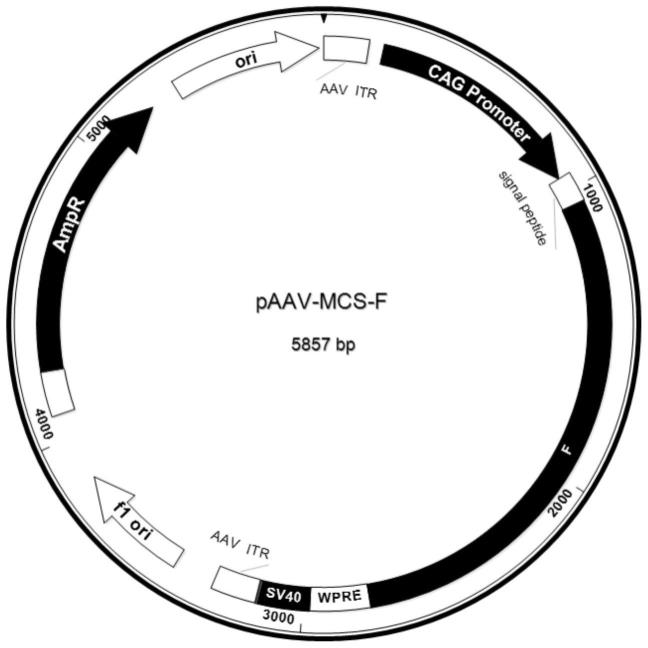
44.图1是paav-mcs-f载体图谱示意图;图2是paav-mcs-g载体图谱示意图;图3是aav-f蛋白中和抗体滴度检测(蚀斑法);图4是raav-g蛋白中和抗体滴度检测(蚀斑法);图5是免疫血清特异性igg检测;图6是肺组织病毒滴度检测(蚀斑法);图7是肺组织病理检查。
具体实施方式
45.下面结合实施实例及附图对本发明进一步详细的描述,但本发明的实施方式不限于此。
46.除非本文中另外明确定义,否则本发明中使用的技术和科学术语具有本领域普遍技术人员通常理解的含义。在本发明的描述中,将使用以下术语,简要说明定义如下。
[0047]“rsv f 蛋白”指rsv f蛋白的所有形式,包括f1多肽和f2多肽,即包括f0前体多肽、f0前体多肽三聚体、成熟f蛋白三聚体等。
[0048]
除非另有说明,负责如文中所用,术语“蛋白”、“蛋白质”和多肽可以互换使用。
[0049]
如文中所用,术语“核酸”、“核酸序列”和“核苷酸序列”可以互换使用;“核酸”是指天然存在的或合成的寡核苷酸或多核苷酸,无论是dna或rna或dna-rna杂交体、单链或双链、有义或反义的,其能够通过watson-crick碱基配对与互补核酸杂交。本发明的核酸还可以包括核苷酸类似物(例如brdu)和非磷酸二酯核苷间连键(例如肽核酸(pna)或硫代二酯键)。具体地说,核酸可以包括但不限于dna、rna、cdna、gdna、ssdna、dsdna或其任何组合。
[0050]
如文中所用,术语“佐剂”是指能够增强、加速或延长机体对免疫原或免疫原性组合物的免疫应答的物质,如氢氧化铝。
[0051]
如文中所用,“aav载体”指腺相关病毒(adeno-associated virus,aav)载体;“raav载体”指重组腺相关病毒(recombinant adeno-associated virus,raav)载体,是指重组非复制型的腺相关病毒,包括血清型蛋白衣壳,并携带重组的基因组,基因组包括功能性的5’和3’反向末端重复序列 (itr),并连接外源核苷酸序列替代野生型aav的 rep或者cap基因。itr 序列提供对raav功能性拯救、复制、包装。在一些实施实例中,itr序列来自aav2。外源核苷酸序列通常由一系列表达调控元件和编码区组成。
[0052]
如文中所用,载体是指用于遗传物质的递送的工具或原件,例如质粒、病毒、噬菌体、脂质体等,且该术语根据应用场景或称为克隆载体、表达载体或骨架载体,以及病毒载体或病毒表达载体。
[0053]
aav血清型质粒包括两个开放的阅读框(orf),编码rep和cap表达产物。cap是指aav的衣壳蛋白,编码vp1、vp2和vp3及aap等功能蛋白,且不同的血清型的aav蛋白衣壳序列有所不同。
[0054]
本技术实施过程中未注明具体的实验方法,通常可按照常规条件执行,如分子克隆手册、冷泉港实验室手册以及制造商提供的说明书执行;实施过程中用到的实验材料如无特别注明,均可从商业化途径购买得到。
[0055]
实施例1:表达rsv抗原多肽质粒构建通过ncbi数据库(www.ncbi.nlm.nih.gov)获取rsv f、g、sh蛋白基因序列(见genbank: ay911262.1)。
[0056]
分析获取的多肽序列特性,选择性的与信号肽序列拼接。优选的,信号肽为人白介素2信号肽和/或人免疫球蛋白e(ige) 信号肽。对序列进行人源密码子优化;基因序列送往基因合成公司完成。
[0057]
将以上所述的基因序列插入到aav表达质粒载体paav-mcs-f和paav-mcs-g,使抗原基因序列插入包含itr序列的质粒载体,形成抗原表达重组质粒;质粒转化大肠杆菌dh5α,涂在含有氨苄抗性的培养基皿,37℃培养箱培养48h以
pfu/100μl。稀释后的病毒液、样品各取100μl,混合均匀,在37℃细胞培养箱放置中和2小时。
[0066]
(3)蚀斑法检测中和抗体:吸弃hep-2细胞培养上清,取200μl混合液加入到6孔板培养的hep-2细胞中,加入阴性对照,放入37℃继续培养2h。每孔加入4 ml 1%的甲基纤维素覆盖培养基,放置于co2培养箱中5天,吸弃培养基,结晶紫染色2h,统计蚀斑情况,能使蚀斑数减少50%的血清稀释度判定为血清的中和抗体滴度,计算各个血清样品分别中和的rsv a2的中和抗体滴度。
[0067]
(4)igg1/igg2a抗体效价测定:96孔板包被rsv-f或rsv-g蛋白(1~2
µ
g/孔),加入200μl封闭液,37℃放置2h进行封闭;加入以倍比稀释的方式(1:2
2-2
25
)进行稀释的待测鼠血清,100μl /孔,以抗体稀释液作为阴性对照,37℃孵育1h;然后取出elisa板,用pbst洗板3次,加入goat anti-mouse igg1(抗体稀释液1:10000稀释)或者goat anti-mouse igg2a(抗体稀释液1:10000稀释),100μl/孔,37℃孵育1h;用pbst洗板6次,加入显色液,100μl /孔,37℃避光显色10-15min;加入2m h2so4终止液,50μl /孔,振荡elisa板进行混匀,于酶标仪读od450nm吸光值;结果判断:若待测孔od值》0.1且大于阴性对照孔的2.1倍(p/n》2.1,其中p为待测血清在某一稀释倍数测定的od值,n为阴性对照测定的od值),则判定为阳性,以判定为阳性的血清最高稀释倍数为血清igg1或者igg2a抗体效价。
[0068]
图3是实施例3:raav载体疫苗免疫原性分析中中和抗体检测结果,即用重组腺相关病毒raav-f(高剂量组滴度为 5
×
10
11
vg/ml和低剂量租滴度1
×
10
11
vg/ml),一针免疫,每只小鼠肌肉注射200μl;采用蚀斑减少法检测小鼠血清中和抗体;结果表明,两个剂量组都能够诱导高水平的中和抗体滴度,raav-f高剂量组中和抗体滴度高于1:10240,raav-f低剂量组中抗体在1:2560左右。
[0069]
图4是实施例3:raav载体疫苗免疫原性分析中中和抗体检测结果,即用重组腺相关病毒raav-g(高剂量组滴度为5
×
10
11
vg/ml和低剂量租滴度1
×
10
11
vg/ml),一针免疫,每只小鼠肌肉注射200μl;采用蚀斑减少法检测小鼠血清中和抗体;结果表明,两个剂量组都能够诱导较高水平的中和抗体滴度,raav-g高剂量组和raav-g低剂量组中抗体滴度都在1:2560左右。
[0070]
图5是实施例3:raav载体疫苗免疫原性分析中igg1/igg2a抗体效价测定结果,即用raav-f高剂量组和低剂量组、raav-g高剂量组合低剂量组一针免疫,每只小鼠肌肉注射200μl;用elisa法检测血清中f蛋白和g蛋白的特异性igg,实验结果显示,该疫苗能够诱导高水平的igg1和igg2a水平,并且免疫反应以th1型为主。
[0071]
实施例4:raav载体疫苗免疫保护效果(1)攻毒保护试验:4~6周龄balb/c小鼠免疫:将纯化获得的raav-f和raav-g分别稀释到5
×
10
11
vg/ml(高剂量组)和1
×
10
11
vg/ml(低剂量组),每只小鼠后腿肌肉注射200μl,每侧注射100μl,一针免疫;并在第42天进行攻毒试验。攻毒时每个剂量组又分为三个组别,分别滴鼻2
×
10
6 pfu rsv a2病毒株或pbs,并在攻毒后第4天,断颈处死小鼠,无菌条件下取左肺和右肺置于无菌的收集管中,并加入1ml预冷的rpmi-1640培养基(2% fbs,双抗),保存于-80℃;或用多聚甲醛固定用于组织病理观察。
[0072]
(2)肺组织病毒滴度检测从-80℃冰箱取出肺组织,称取一定的量,无菌匀浆制备肺组织悬液,4℃,10000
×
g 离心5min,保留上清液。利用蚀斑法对上清液进行病毒滴度测定,并计算肺组织中的病毒量(pfu/g或者pfu/ml)。
[0073]
肺组织病毒清除率计算公式为:病毒清除率=(pbs对照组肺病毒滴度-样品组肺组织病毒滴度)/ pbs对照组肺病毒滴度
×
100%。
[0074]
(3)肺部组织病理观察所取肺部组织在多聚甲醛溶液中固定48 h,经过脱水、透明、浸蜡、包埋、切片、he 染色等步骤制备病理切片,在光学显微镜下进行观察并采集数码图像。
[0075]
(4)肺组织病毒载量检测取一定量的肺组织,提取总rna,逆转录成cdna,设计rsv f蛋白基因pcr扩增引物(ph-f:ccggaatattaatagatcatggaga(seq id no.:13);ph-r:tcattttatgtttcaggttcagggg(seq id no.:14)),按照试剂盒说明书pcr扩增f蛋白基因,电泳检查pcr产物的是否有条带以及条带大小。
[0076]
图6是实施例4:raav载体疫苗免疫保护效果中肺组织病毒滴度检测结果,即用raav-f高剂量组和低剂量组、raav-g高剂量组和低剂量组一针免疫,每只小鼠肌肉注射200μl;通过小鼠攻毒保护实验检测攻毒保护效果,攻毒实验结果表明,2
×
10
6 pfu rsv a2病毒株嘀鼻攻毒后,疫苗组小鼠肺部无病毒检出,说明其对rsv a2病毒攻击具有良好的保护作用。
[0077]
图7是实施例4:raav载体疫苗免疫保护效果中小鼠肺部组织病理变化情况观察结果,疫苗免疫组能够显著保护rsv感染肺部导致的组织病变,对照组(raav-gfp)攻毒后出现明显的肺部病变。
[0078]
综上,结合raav-f蛋白免疫血清、raav-g蛋白免疫血清,本发明获得的基于raav载体的rsv疫苗在小鼠体能能够诱导具有高水平的中和抗体滴度和免疫保护效果,是一种理想的rsv疫苗候选品种。
[0079]
上述实施例仅为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明创造的保护范围之中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1