一种制备罗伊氏乳杆菌冻干的方法与流程
1.本发明属于微生物发酵技术领域,具体涉及一种制备罗伊氏乳杆菌冻干的方法。
背景技术:
2.益生菌是活的微生物,当宿主中摄入足量时,会产生健康益处。近年来在欧盟、美国、日本和中国等国家和地区的市场上,含有益生菌的产品种类逐年增多。大量的科学实验已经证实经常性的摄入益生菌及其制品能够保证肠道的健康。
3.要使益生菌产品可以发挥理想的益生效果,必须要保证产品中活菌的数量足够,所以,目前工业大部分是从益生菌菌生产工艺的后端来进行控制,如采用真空冷冻干燥的方法制备益生菌菌粉,同时添加合适的保护剂来提高益生菌冻干存活率以及保证其储藏稳定性。这种方法确实是在一定程度要可以提升益生菌菌粉的储藏稳定性,但因菌株的差异性,该方法有一定的局限性。而且,目前较少研发人员从前端(如发酵工艺的控制)来研究其益生菌的稳定性。
技术实现要素:
4.本发明第一方面的目的,在于提供一种制备罗伊氏乳杆菌冻干的方法。
5.本发明第二方面的目的,在于提供第一方面的方法得到的罗伊氏乳杆菌冻干。
6.本发明第三方面的目的,在于提供第一方面的方法和/或第二方面的罗伊氏乳杆菌冻干在制备产品中的应用。
7.本发明第四方面的目的,在于提供一种产品。
8.本发明第五方面的目的,在于提供一种试剂。
9.本发明第六方面的目的,在于提供一种培养基。
10.为了实现上述目的,本发明所采取的技术方案是:
11.本发明的第一个方面,提供一种制备罗伊氏乳杆菌冻干的方法,所述方法包括在罗伊氏乳杆菌对数生长中期补加试剂的步骤;
12.所述试剂为海藻糖、蔗糖、甘油、茶多酚、羟乙基淀粉、聚乙烯聚吡咯烷酮、二十二碳六烯酸、抗坏血酸棕榈酸酯和乳酸钠中的至少一种。
13.优选地,所述方法包括如下步骤:将罗伊氏乳杆菌菌液接种至培养基,培养,在罗伊氏乳杆菌对数生长中期补加试剂,在罗伊氏乳杆菌对数生长末期时进行固液分离,得到上清液和菌泥,将菌泥和与冻干保护剂混合,冷冻干燥,得到罗伊氏乳杆菌冻干。
14.优选地,所述罗伊氏乳杆菌菌液的接种量为所述培养基的1v/v%~5v/v%;进一步为1v/v%~2v/v%。
15.优选地,所述培养基为mrs液体培养基、nb液体培养基、lbs液体培养基以及本领域其他用于培养罗伊氏乳杆菌的常规培养基。
16.优选地,所述培养的温度为35~39℃;进一步为36~38℃;更进一步为37℃。
17.优选地,所述罗伊氏乳杆菌菌液的制备方法如下:将保存的罗伊氏乳杆菌活化,扩
大培养,得到罗伊氏乳杆菌菌液。
18.优选地,所述活化的步骤如下:取一环保存的罗伊氏乳杆菌,在活化培养基上划线,35~39℃培养46~50h,得到活化的罗伊氏乳杆菌。
19.优选地,所述活化培养基为mrs固体培养基、nb固体培养基、lbs固体培养基以及本领域其他用于活化罗伊氏乳杆菌的常规培养基。
20.优选地,所述扩大培养的步骤如下:取活化的罗伊氏乳杆菌接种至种子培养基中,35~39℃培养16~20h,得到罗伊氏乳杆菌菌液。
21.优选地,所述种子培养基为mrs液体培养基、nb液体培养基、lbs液体培养基以及本领域其他用于扩大培养罗伊氏乳杆菌的常规培养基。
22.优选地,所述试剂为(1)~(15)中任一种:(1)海藻糖;(2)蔗糖;(3)甘油;(4)茶多酚;(5)羟乙基淀粉;(6)聚乙烯聚吡咯烷酮;(7)二十二碳六烯酸;(8)抗坏血酸棕榈酸酯;(9)乳酸钠;(10)海藻糖和蔗糖;(11)海藻糖和甘油;(12)海藻糖和茶多酚;(13)海藻糖、茶多酚和二十二碳六烯酸;(14)海藻糖、茶多酚和抗坏血酸棕榈酸酯;(15)海藻糖、茶多酚、二十二碳六烯酸和抗坏血酸棕榈酸酯。
23.优选地,(1)中所述海藻糖的终浓度为5~20g/l;进一步为10g/l。
24.优选地,(2)中所述蔗糖的终浓度为5~25g/l;进一步为10g/l。
25.优选地,(3)中所述甘油的终浓度为10~25g/l;进一步为15g/l。
26.优选地,(4)中所述茶多酚的终浓度为1~10g/l;进一步为5g/l。
27.优选地,(5)中所述羟乙基淀粉的终浓度为1~15g/l;进一步为5g/l。
28.优选地,(6)中所述聚乙烯聚吡咯烷酮的终浓度为1~15g/l;进一步为5g/l。
29.优选地,(7)中所述二十二碳六烯酸的终浓度为0.5~5g/l;进一步为2g/l。
30.优选地,(8)中所述抗坏血酸棕榈酸酯的终浓度为0.1~1.5g/l;进一步为1g/l。
31.优选地,(9)中所述乳酸钠的终浓度为5~25g/l;进一步为10g/l。
32.优选地,(10)中所述海藻糖的终浓度为5~20g/l,所述蔗糖的终浓度为5~25g/l;进一步优选地,所述海藻糖的终浓度为10g/l,所述蔗糖的终浓度为10g/l。
33.优选地,(11)中所述海藻糖的终浓度为5~20g/l,所述甘油的终浓度为10~25g/l;进一步优选地,所述海藻糖的终浓度为10g/l,所述甘油的终浓度为15g/l。
34.优选地,(12)中所述海藻糖的终浓度为5~20g/l,所述茶多酚的终浓度为1~10g/l;进一步优选地,所述海藻糖的终浓度为10g/l,所述茶多酚的终浓度为5g/l。
35.优选地,(13)中所述海藻糖的终浓度为5~20g/l,所述茶多酚的终浓度为1~10g/l,所述二十二碳六烯酸的终浓度为0.5~5g/l;进一步优选地,所述海藻糖的终浓度为10g/l,所述茶多酚的终浓度为5g/l,所述二十二碳六烯酸的终浓度为2g/l。
36.优选地,(14)中所述海藻糖的终浓度为5~20g/l,所述茶多酚的终浓度为1~10g/l,所述抗坏血酸棕榈酸酯的终浓度为0.1~1.5g/l;进一步优选地,所述海藻糖的终浓度为10g/l,所述茶多酚的终浓度为5g/l,所述抗坏血酸棕榈酸酯的终浓度为1g/l。
37.优选地,(15)中所述海藻糖的终浓度为5~20g/l,所述茶多酚的终浓度为1~10g/l,所述二十二碳六烯酸的终浓度为0.5~5g/l,所述抗坏血酸棕榈酸酯的终浓度为0.1~1.5g/l;进一步优选地,所述海藻糖的终浓度为10g/l,所述茶多酚的终浓度为5g/l,所述二十二碳六烯酸的终浓度为2g/l,所述抗坏血酸棕榈酸酯的终浓度为1g/l。
38.优选地,所述固液分离的方式为离心。
39.优选地,所述离心的条件为5000~8000r/min下离心15~25min。
40.优选地,所述冻干保护剂包括低聚木糖、菊粉、脱脂奶粉、海藻糖、甘油和麦芽糊精;进一步优选地,所述冻干保护剂包括5~20g/l低聚木糖、10~20g/l菊粉、5~20g/l脱脂奶粉、20~50g/l海藻糖、1~10g/l甘油和5~30g/l麦芽糊精;更进一步优选地,所述冻干保护剂包括5g/l低聚木糖、10g/l菊粉、5g/l脱脂奶粉、20g/l海藻糖、1g/l甘油和5g/l麦芽糊精。
41.优选地,所述菌泥与冻干保护剂的质量比为1:(0.5~2)。
42.优选地,所述冷冻干燥包括如下步骤:(1)-44℃~-55℃预冻3~6h;(2)经过200~380min升温至-29~-13℃后,维持850-980min;(3)经过3~7h升温至0~8℃后,维持3-8h;(4)经过100~250min升温至10~18℃后,维持120~300min;(5)经过60~100min升温至25~30℃后,维持300~480min。
43.优选地,所述方法还包括如下步骤:在罗伊氏乳杆菌对数生长后期进行热胁迫处理,所述热胁迫处理为42~48℃处理30~60min。
44.优选地,所述热胁迫处理为42~45℃处理30~60min;进一步为45℃处理30~45min;更进一步为45℃处理45min。
45.优选地,所述方法还包括如下步骤:在罗伊氏乳杆菌对数生长后期进行低温胁迫处理,所述低温胁迫处理为15~25℃处理30~60min。
46.优选地,所述低温胁迫处理为20~25℃处理30~45min;进一步为20℃处理30~45min;更进一步为20℃处理30min。
47.优选地,所述方法还包括如下步骤:在冷冻干燥前,添加所述上清液。
48.优选地,所述上清液的添加量为所述菌泥的质量的10%~50%;进一步为所述菌泥的质量的30%~50%;更进一步为所述菌泥的质量的40%。
49.优选地,在本发明的第一个方面中,先进行热胁迫处理再进行低温胁迫处理。
50.进一步优选地,在本发明的第一个方面中,进行热胁迫处理后立即进行低温胁迫处理。
51.优选地,在本发明的第一个方面中,所述培养为厌氧培养。
52.优选地,本发明通过在培养过程中通入氮气进行厌氧培养。
53.优选地,在本发明的第一个方面中,所述罗伊氏乳杆菌为罗伊氏乳杆菌ccfm8631。
54.本发明的第二个方面,提供一种罗伊氏乳杆菌冻干,通过本发明第一个方面的方法得到。
55.优选地,所述罗伊氏乳杆菌冻干中罗伊氏乳杆菌的存活率为30%~91%;进一步为43%~91%;更进一步为60%~91%;再进一步为70%~91%。
56.本发明的第三个方面,提供本发明第一个方面的方法或第二个方面的罗伊氏乳杆菌冻干在制备产品中的应用。
57.优选地,所述产品为食品、药品和保健品中的至少一种。
58.本发明的第四个方面,提供一种产品,包含本发明第二个方面的罗伊氏乳杆菌冻干。
59.优选地,所述产品为食品、药品和保健品中的至少一种。
60.优选地,所述产品还包含食品、药品和保健品中可接受的辅料。
61.本发明的第五个方面,提供一种试剂,为(1)~(15)中任一种:(1)海藻糖;(2)蔗糖;(3)甘油;(4)茶多酚;(5)羟乙基淀粉;(6)聚乙烯聚吡咯烷酮;(7)二十二碳六烯酸;(8)抗坏血酸棕榈酸酯;(9)乳酸钠;(10)海藻糖和蔗糖;(11)海藻糖和甘油;(12)海藻糖和茶多酚;(13)海藻糖、茶多酚和二十二碳六烯酸;(14)海藻糖、茶多酚和抗坏血酸棕榈酸酯;(15)海藻糖、茶多酚、二十二碳六烯酸和抗坏血酸棕榈酸酯。
62.本发明的第六个方面,提供一种培养基,包括基础培养基和本发明的第五个方面的试剂。
63.优选地,所述基础培养基为为mrs液体培养基、nb液体培养基、lbs液体培养基以及本领域其他用于培养罗伊氏乳杆菌的常规培养基。
64.优选地,(1)中所述海藻糖的终浓度为5~20g/l;进一步为10g/l。
65.优选地,(2)中所述蔗糖的终浓度为5~25g/l;进一步为10g/l。
66.优选地,(3)中所述甘油的终浓度为10~25g/l;进一步为15g/l。
67.优选地,(4)中所述茶多酚的终浓度为1~10g/l;进一步为5g/l。
68.优选地,(5)中所述羟乙基淀粉的终浓度为1~15g/l;进一步为5g/l。
69.优选地,(6)中所述聚乙烯聚吡咯烷酮的终浓度为1~15g/l;进一步为5g/l。
70.优选地,(7)中所述二十二碳六烯酸的终浓度为0.5~5g/l;进一步为2g/l。
71.优选地,(8)中所述抗坏血酸棕榈酸酯的终浓度为0.1~1.5g/l;进一步为1g/l。
72.优选地,(9)中所述乳酸钠的终浓度为5~25g/l;进一步为10g/l。
73.优选地,(10)中所述海藻糖的终浓度为5~20g/l,所述蔗糖的终浓度为5~25g/l;进一步优选地,所述海藻糖的终浓度为10g/l,所述蔗糖的终浓度为10g/l。
74.优选地,(11)中所述海藻糖的终浓度为5~20g/l,所述甘油的终浓度为10~25g/l;进一步优选地,所述海藻糖的终浓度为10g/l,所述甘油的终浓度为15g/l。
75.优选地,(12)中所述海藻糖的终浓度为5~20g/l,所述茶多酚的终浓度为1~10g/l;进一步优选地,所述海藻糖的终浓度为10g/l,所述茶多酚的终浓度为5g/l。
76.优选地,(13)中所述海藻糖的终浓度为5~20g/l,所述茶多酚的终浓度为1~10g/l,所述二十二碳六烯酸的终浓度为0.5~5g/l;进一步优选地,所述海藻糖的终浓度为10g/l,所述茶多酚的终浓度为5g/l,所述二十二碳六烯酸的终浓度为2g/l。
77.优选地,(14)中所述海藻糖的终浓度为5~20g/l,所述茶多酚的终浓度为1~10g/l,所述抗坏血酸棕榈酸酯的终浓度为0.1~1.5g/l;进一步优选地,所述海藻糖的终浓度为10g/l,所述茶多酚的终浓度为5g/l,所述抗坏血酸棕榈酸酯的终浓度为1g/l。
78.优选地,(15)中所述海藻糖的终浓度为5~20g/l,所述茶多酚的终浓度为1~10g/l,所述二十二碳六烯酸的终浓度为0.5~5g/l,所述抗坏血酸棕榈酸酯的终浓度为0.1~1.5g/l;进一步优选地,所述海藻糖的终浓度为10g/l,所述茶多酚的终浓度为5g/l,所述二十二碳六烯酸的终浓度为2g/l,所述抗坏血酸棕榈酸酯的终浓度为1g/l。
79.本发明的有益效果是:
80.本发明提供了一种制备罗伊氏乳杆菌冻干的方法,通过在罗伊氏乳杆菌对数生长中期补加试剂(试剂为海藻糖、蔗糖、甘油、茶多酚、羟乙基淀粉、聚乙烯聚吡咯烷酮、二十二碳六烯酸、抗坏血酸棕榈酸酯和乳酸钠中的至少一种),提高了罗伊氏乳杆菌的冻干存活
率,相应地,该罗伊氏乳杆菌经过37℃加速2个月和25℃常温1年储藏后的存活率也得到提高。
81.进一步地,本发明在罗伊氏乳杆菌对数生长后期进行热胁迫处理,进一步提高了罗伊氏乳杆菌的冻干存活率,相应地,该罗伊氏乳杆菌经过37℃加速2个月和25℃常温1年储藏后的存活率也可以得到提高。
82.进一步地,本发明在罗伊氏乳杆菌对数生长后期进行低温胁迫处理,进一步提高了罗伊氏乳杆菌的冻干存活率,相应地,该罗伊氏乳杆菌经过37℃加速2个月和25℃常温1年储藏后的存活率也可以得到提高。
83.进一步地,本发明在冷冻干燥前添加上清液,更进一步提高罗伊氏乳杆菌的冻干存活率,相应地,该罗伊氏乳杆菌经过37℃加速2个月和25℃常温1年储藏后的存活率也可以得到提高。
84.本发明方法制备得到的罗伊氏乳杆菌冻干中罗伊氏乳杆菌的存活率显著提升,罗伊氏乳杆菌经过37℃加速2个月和25℃常温1年储藏后的存活率也可以得到提高,该方法及该方法得到的罗伊氏乳杆菌冻干可用于制备食品、药品和保健品。
具体实施方式
85.以下通过具体的实施例对本发明的内容作进一步详细的说明。
86.应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。
87.下述实施例中涉及罗伊氏乳杆菌ccfm8631(lactobacillusreuteri),于2017年07月07日保藏于中国微生物菌种保藏管理委员会普通微生物中心cgmcc,保藏地址为北京市朝阳区北辰西路1号院3号中国科学院微生物研究所,保藏编号为cgmccno.14394;已在专利文献cn107523526a中公开。
88.下述实施例中涉及的培养基如下:
89.mrs液体培养基:蛋白胨10g/l、酵母提取物5g/l、牛肉浸膏10g/l、葡萄糖20g/l、无水乙酸钠2g/l、柠檬酸氢二胺2g/l、k2hpo
4 2.6g/l、mgso
4 0.5g/l、mnso
4 0.25g/l、l-半胱氨酸盐酸盐0.5g/l。
90.mrs固体培养基:蛋白胨10g/l、酵母提取物5g/l、牛肉浸膏10g/l、葡萄糖20g/l、无水乙酸钠2g/l、柠檬酸氢二胺2g/l、k2hpo
4 2.6g/l、mgso
4 0.5g/l、mnso
4 0.25g/l、吐温80 1g/l、琼脂20g/l、l-半胱氨酸盐酸盐0.5g/l。
91.下述实施例中涉及的检测方法如下:
92.罗伊氏乳杆菌活菌数的检测方法:采用国标《gb4789.35-2016食品安全国家标准食品微生物学检测乳酸菌检测》。
93.冻干存活率的计算公式为:存活率(%)=(冻干后活菌数/冻干前活菌数)*100%。
94.实施例1一种制备罗伊氏乳杆菌冻干的方法
95.用接种环蘸取甘油管中的罗伊氏乳杆菌ccfm8631菌液在mrs固体培养基上划线,于37℃恒温厌氧培养48h,得到单菌落;挑取单菌落接种于mrs液体培养基中,37℃恒温厌氧培养18h,得到种子液;将种子液按2%(v/v)的接种量接种至mrs液体培养基中,37℃恒温厌氧培养12h至对数生长中期,添加海藻糖(终浓度为10g/l),待其培养至对数生长末期时,收集菌液;将菌液在6500r/min下离心20min,收集菌泥;将菌泥与冻干保护剂(冻干保护剂配
制方法为准确称量低聚木糖5g,菊粉10g,脱脂奶粉5g,海藻糖20g,甘油1g,麦芽糊精5g,定容至1000ml)按质量比1:1混合,得到乳化液;将乳化液进行冷冻干燥(冷冻干燥的条件包括以下步骤:(1)-50℃预冻4h;(2)经过300min升温至-29℃后,维持900min;(3)经过6h升温至5℃后,维持5h;(4)经过200min升温至14℃后,维持200min;(5)经过80min升温至28℃后,维持400min),得到罗伊氏乳杆菌冻干。
96.实施例2一种制备罗伊氏乳杆菌冻干的方法
97.本实施例的方法与实施例1相同,区别仅在于:37℃恒温厌氧培养12h至对数生长中期,添加蔗糖(终浓度为10g/l)。
98.实施例3一种制备罗伊氏乳杆菌冻干的方法
99.本实施例的方法与实施例1相同,区别仅在于:37℃恒温厌氧培养12h至对数生长中期,添加甘油(终浓度为15g/l)。
100.实施例4一种制备罗伊氏乳杆菌冻干的方法
101.本实施例的方法与实施例1相同,区别仅在于:37℃恒温厌氧培养12h至对数生长中期,添加茶多酚(终浓度为5g/l)。
102.实施例5一种制备罗伊氏乳杆菌冻干的方法
103.本实施例的方法与实施例1相同,区别仅在于:37℃恒温厌氧培养12h至对数生长中期,添加羟乙基淀粉(终浓度为5g/l)。
104.实施例6一种制备罗伊氏乳杆菌冻干的方法
105.本实施例的方法与实施例1相同,区别仅在于:37℃恒温厌氧培养12h至对数生长中期,添加聚乙烯聚吡咯烷酮(分子式:(c6h9no)n,分子量:111.14,终浓度为5g/l)。
106.实施例7一种制备罗伊氏乳杆菌冻干的方法
107.本实施例的方法与实施例1相同,区别仅在于:37℃恒温厌氧培养12h至对数生长中期,添加二十二碳六烯酸(终浓度为2g/l)。
108.实施例8一种制备罗伊氏乳杆菌冻干的方法
109.本实施例的方法与实施例1相同,区别仅在于:37℃恒温厌氧培养12h至对数生长中期,添加抗坏血酸棕榈酸酯(终浓度为1g/l)。
110.实施例9一种制备罗伊氏乳杆菌冻干的方法
111.本实施例的方法与实施例1相同,区别仅在于:37℃恒温厌氧培养12h至对数生长中期,添加乳酸钠(终浓度为10g/l)。
112.实施例10一种制备罗伊氏乳杆菌冻干的方法
113.本实施例的方法与实施例1相同,区别仅在于:37℃恒温厌氧培养12h至对数生长中期,添加海藻糖和蔗糖(海藻糖和蔗糖的终浓度均为10g/l)。
114.实施例11一种制备罗伊氏乳杆菌冻干的方法
115.本实施例的方法与实施例1相同,区别仅在于:37℃恒温厌氧培养12h至对数生长中期,添加海藻糖和甘油(海藻糖和甘油的终浓度分别为10g/l、15g/l)。
116.实施例12一种制备罗伊氏乳杆菌冻干的方法
117.本实施例的方法与实施例1相同,区别仅在于:37℃恒温厌氧培养12h至对数生长中期,添加海藻糖和茶多酚(海藻糖和茶多酚的终浓度分别为10g/l、5g/l)。
118.实施例13一种制备罗伊氏乳杆菌冻干的方法
119.本实施例的方法与实施例1相同,区别仅在于:37℃恒温厌氧培养12h至对数生长中期,添加海藻糖、茶多酚和二十二碳六烯酸(海藻糖、茶多酚和二十二碳六烯酸的终浓度分别为10g/l、5g/l、2g/l)。
120.实施例14一种制备罗伊氏乳杆菌冻干的方法
121.本实施例的方法与实施例1相同,区别仅在于:37℃恒温厌氧培养12h至对数生长中期,添加海藻糖、茶多酚和抗坏血酸棕榈酸酯(海藻糖、茶多酚和抗坏血酸棕榈酸酯的终浓度分别为10g/l、5g/l、1g/l)。
122.实施例15一种制备罗伊氏乳杆菌冻干的方法
123.本实施例的方法与实施例1相同,区别仅在于:37℃恒温厌氧培养12h至对数生长中期,添加海藻糖、茶多酚、二十二碳六烯酸和抗坏血酸棕榈酸酯(海藻糖、茶多酚、二十二碳六烯酸和抗坏血酸棕榈酸酯的终浓度分别为10g/l、5g/l、2g/l、1g/l)。
124.实施例16一种制备罗伊氏乳杆菌冻干的方法
125.本实施例的方法与实施例14相同,区别仅在于:在对数生长后期进行热胁迫处理(42℃应激处理30min)。
126.实施例17一种制备罗伊氏乳杆菌冻干的方法
127.本实施例的方法与实施例16相同,区别仅在于:热胁迫处理的条件为42℃应激处理45min。
128.实施例18一种制备罗伊氏乳杆菌冻干的方法
129.本实施例的方法与实施例16相同,区别仅在于:热胁迫处理的条件为42℃应激处理60min。
130.实施例19一种制备罗伊氏乳杆菌冻干的方法
131.本实施例的方法与实施例16相同,区别仅在于:热胁迫处理的条件为45℃应激处理30min。
132.实施例20一种制备罗伊氏乳杆菌冻干的方法
133.本实施例的方法与实施例16相同,区别仅在于:热胁迫处理的条件为45℃应激处理45min。
134.实施例21一种制备罗伊氏乳杆菌冻干的方法
135.本实施例的方法与实施例16相同,区别仅在于:热胁迫处理的条件为45℃应激处理60min。
136.实施例22一种制备罗伊氏乳杆菌冻干的方法
137.本实施例的方法与实施例16相同,区别仅在于:热胁迫处理的条件为48℃应激处理30min。
138.实施例23一种制备罗伊氏乳杆菌冻干的方法
139.本实施例的方法与实施例16相同,区别仅在于:热胁迫处理的条件为48℃应激处理45min。
140.实施例24一种制备罗伊氏乳杆菌冻干的方法
141.本实施例的方法与实施例16相同,区别仅在于:热胁迫处理的条件为48℃应激处理60min。
142.实施例25一种制备罗伊氏乳杆菌冻干的方法
143.本实施例的方法与实施例20相同,区别仅在于:在热胁迫处理后,还包括低温胁迫处理(15℃应激处理30min,在热胁迫后立即进行)。
144.实施例26一种制备罗伊氏乳杆菌冻干的方法
145.本实施例的方法与实施例25相同,区别仅在于:低温胁迫处理的条件为15℃应激处理45min。
146.实施例27一种制备罗伊氏乳杆菌冻干的方法
147.本实施例的方法与实施例25相同,区别仅在于:低温胁迫处理的条件为15℃应激处理60min。
148.实施例28一种制备罗伊氏乳杆菌冻干的方法
149.本实施例的方法与实施例25相同,区别仅在于:低温胁迫处理的条件为20℃应激处理30min。
150.实施例29一种制备罗伊氏乳杆菌冻干的方法
151.本实施例的方法与实施例25相同,区别仅在于:低温胁迫处理的条件为20℃应激处理45min。
152.实施例30一种制备罗伊氏乳杆菌冻干的方法
153.本实施例的方法与实施例25相同,区别仅在于:低温胁迫处理的条件为20℃应激处理60min。
154.实施例31一种制备罗伊氏乳杆菌冻干的方法
155.本实施例的方法与实施例25相同,区别仅在于:低温胁迫处理的条件为25℃应激处理30min。
156.实施例32一种制备罗伊氏乳杆菌冻干的方法
157.本实施例的方法与实施例25相同,区别仅在于:低温胁迫处理的条件为25℃应激处理45min。
158.实施例33一种制备罗伊氏乳杆菌冻干的方法
159.本实施例的方法与实施例25相同,区别仅在于:低温胁迫处理的条件为25℃应激处理60min。
160.实施例34一种制备罗伊氏乳杆菌冻干的方法
161.本实施例的方法与实施例28相同,区别仅在于:在菌泥与冻干保护剂混合后,添加菌液离心得到的上清液(添加量为菌泥重量的10%),得到乳化液。
162.实施例35一种制备罗伊氏乳杆菌冻干的方法
163.本实施例的方法与实施例34相同,区别仅在于:添加量为菌泥重量的20%。
164.实施例36一种制备罗伊氏乳杆菌冻干的方法
165.本实施例的方法与实施例34相同,区别仅在于:添加量为菌泥重量的30%。
166.实施例37一种制备罗伊氏乳杆菌冻干的方法
167.本实施例的方法与实施例34相同,区别仅在于:添加量为菌泥重量的40%。
168.实施例38一种制备罗伊氏乳杆菌冻干的方法
169.本实施例的方法与实施例34相同,区别仅在于:添加量为菌泥重量的50%。
170.对比例1一种制备罗伊氏乳杆菌冻干的方法
171.本对比例的方法与实施例1相同,区别仅在于:37℃恒温厌氧培养12h至对数生长
中期,不添加海藻糖。
172.效果实施例
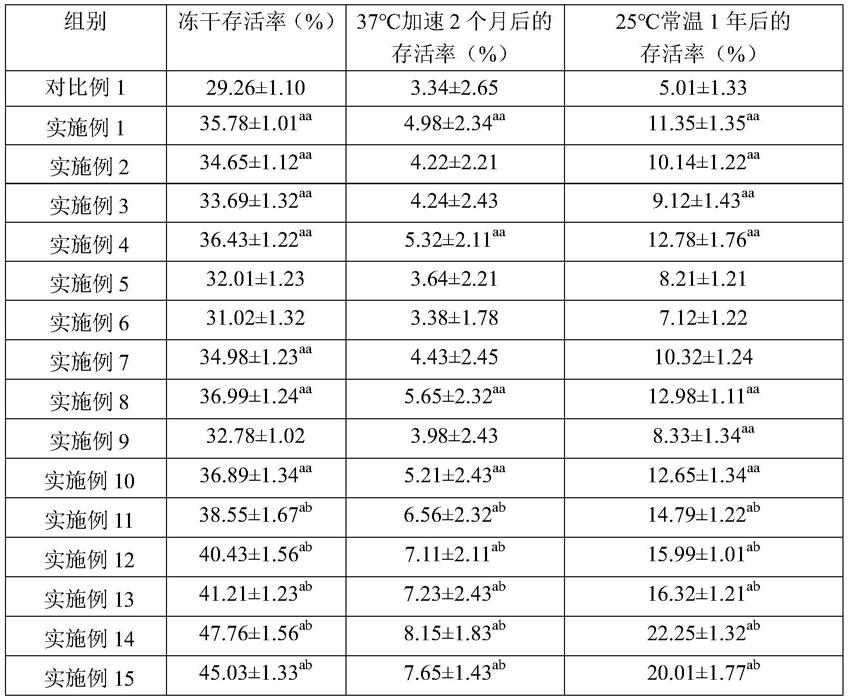
173.1.检测实施例1~15及对比例1的罗伊氏乳杆菌冻干前(乳化液)的活菌数以及得到的罗伊氏乳杆菌冻干的活菌数,计算罗伊氏乳杆菌的冻干存活率;将实施例1~15及对比例1制备得到的罗伊氏乳杆菌冻干用铝箔袋抽真空保存,置于37℃、25℃培养箱中进行储藏,在2个月、1年后取出检测活菌数,计算加速2个月和常温1年后的存活率。不同方法中罗伊氏乳杆菌的冻干存活率和储藏存活率如表1所示:在罗伊氏乳杆菌对数生长中期向培养基补加物质(物质为海藻糖、蔗糖、甘油、茶多酚、羟乙基淀粉、聚乙烯聚吡咯烷酮、二十二碳六烯酸、抗坏血酸棕榈酸酯和乳酸钠中的至少一种)可以提高罗伊氏乳杆菌的冻干存活率,相应地,该罗伊氏乳杆菌经过37℃加速2个月和25℃常温1年储藏后的存活率也高于未在对数生长中期向培养基补加物质(对比例1)得到的罗伊氏乳杆菌;尤其,在罗伊氏乳杆菌对数生长中期向培养基补加海藻糖、茶多酚和抗坏血酸棕榈酸酯后,冻干存活率高达47.76%(与未添加物质相比(对比例1)提高了18.5%),37℃加速2个月后的存活率可达8.15%(与未添加物质相比(对比例1)提高了4.81%),25℃常温1年后的存活率可达22.25%(与未添加物质相比(对比例1)提高了17.24%)。
174.表1实施例1~15及对比例1得到的罗伊氏乳杆菌的冻干存活率及储藏存活率
[0175][0176]
注:“aa”表示实施例与对比例1有显著性差异(p《0.05);“ab”表示实施例(与除标注”ab”外的实施例)之间、与对比例差异均显著(p《0.05)。
[0177]
2.检测实施例16~24的罗伊氏乳杆菌冻干前(乳化液)的活菌数以及得到的罗伊氏乳杆菌冻干的活菌数,计算罗伊氏乳杆菌的冻干存活率;将实施例14、16~24制备得到的
罗伊氏乳杆菌冻干用铝箔袋抽真空保存,置于37℃、25℃培养箱中进行储藏,在2个月、1年后取出检测活菌数,计算加速2个月和常温1年后的存活率。不同方法中罗伊氏乳杆菌的冻干存活率和储藏存活率如表2所示:在罗伊氏乳杆菌对数生长后期进行热胁迫处理可以提高罗伊氏乳杆菌的冻干存活率,相应地,该罗伊氏乳杆菌经过37℃加速2个月和25℃常温1年储藏后的存活率也可以得到提高;尤其,在罗伊氏乳杆菌对数生长后期进行45℃应激处理45min效果最佳,冻干存活率高达52.24%(与未进行热胁迫处理(实施例14)提高了4.48%),37℃加速2个月后的存活率可达12.45%(与未进行热胁迫处理(实施例14)提高了4.3%),25℃常温1年后的存活率可达27.23%(与未进行热胁迫处理(实施例14)提高了4.98%)。
[0178]
表2实施例14、16~24得到的罗伊氏乳杆菌的冻干存活率及储藏存活率
[0179][0180]
注:“aa”表示实施例(实施例16~24)与对比例(实施例14)有显著性差异(p《0.05);“ab”表示实施例(实施例16~24,与除标注”ab”外的实施例)之间、与对比例(实施例14)差异均显著(p《0.05)。
[0181]
3.检测实施例25~33的罗伊氏乳杆菌冻干前(乳化液)的活菌数以及得到的罗伊氏乳杆菌冻干的活菌数,计算罗伊氏乳杆菌的冻干存活率;将实施例25~33制备得到的罗伊氏乳杆菌冻干用铝箔袋抽真空保存,置于37℃、25℃培养箱中进行储藏,在2个月、1年后取出检测活菌数,计算加速2个月和常温1年后的存活率。不同方法中罗伊氏乳杆菌的冻干存活率和储藏存活率如表3所示:在罗伊氏乳杆菌对数生长后期进行低温胁迫处理可以提高罗伊氏乳杆菌的冻干存活率,相应地,该罗伊氏乳杆菌经过37℃加速2个月和25℃常温1年储藏后的存活率也可以得到提高;尤其,在罗伊氏乳杆菌对数生长后期进行20℃应激处理30min效果最佳,冻干存活率高达66.23%(与未进行低温胁迫处理(实施例20)提高了13.99%),37℃加速2个月后的存活率可达12.45%(与未进行低温胁迫处理(实施例20)提高了2.67%),25℃常温1年后的存活率可达27.23%(与未进行低温胁迫处理(实施例20)提高了15.21%)。
[0182]
表3实施例20、25~33得到的罗伊氏乳杆菌的冻干存活率及储藏存活率
[0183][0184]
注:“aa”表示实施例(实施例25~33)与对比例(实施例20)有显著性差异(p《0.05);“ab”表示实施例(实施例25~33,与除标注”ab”外的实施例)之间、与对比例(实施例20)差异均显著(p《0.05)。
[0185]
4.检测实施例34~38的罗伊氏乳杆菌冻干前(乳化液)的活菌数以及得到的罗伊氏乳杆菌冻干的活菌数,计算罗伊氏乳杆菌的冻干存活率;将实施例34~38制备得到的罗伊氏乳杆菌冻干用铝箔袋抽真空保存,置于37℃、25℃培养箱中进行储藏,在2个月、1年后取出检测活菌数,计算加速2个月和常温1年后的存活率。不同方法中罗伊氏乳杆菌的冻干存活率和储藏存活率如表4所示:制备乳化液过程中添加上清液可以提高罗伊氏乳杆菌的冻干存活率,相应地,该罗伊氏乳杆菌经过37℃加速2个月和25℃常温1年储藏后的存活率也可以得到提高;尤其,添加量为40%时效果最佳,冻干存活率高达90.23%(与未添加上清液(实施例28)提高了24%),37℃加速2个月后的存活率可达25.23%(与未添加上清液(实施例28)提高了10.11%),25℃常温1年后的存活率可达66.67%(与未添加上清液(实施例28)提高了24.23%)。
[0186]
表4实施例28、34~38得到的罗伊氏乳杆菌的冻干存活率及储藏存活率
[0187][0188]
注:“aa”表示实施例(实施例34~38)与对比例(实施例28)有显著性差异(p《0.05);“ab”表示实施例(实施例34~38,与除标注”ab”外的实施例)之间、与对比例(实施例28)差异均显著(p《0.05)。
[0189]
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1