幽门螺杆菌HspA的B细胞表位多肽HP11及其应用
幽门螺杆菌hspa的b细胞表位多肽hp11及其应用
技术领域
1.本发明属于生物技术领域,尤其涉及一种幽门螺杆菌hspa的b细胞表位多肽hp11及其应用。
背景技术:
2.1982年,两位澳大利亚学者robin warren和barry marshall从人胃组织中分离到了幽门螺杆菌(helicobacter pylori,h.pylori),并阐明了该菌与胃肠疾病的关系。2005年,诺贝尔生理学或医学奖授予了澳大利亚的这两位科学家,以表彰他们为此做出的贡献。
3.h.pylori是一种螺旋形、微需氧、革兰氏阴性细菌,定植于人胃中。h.pylori的发现使人们对慢性胃炎、消化性溃疡等疾病在发病学和防治学上的认识发生了颠覆性的变化。目前,h.pylori感染作为慢性胃炎、消化性溃疡的最主要病因己经得到了国际医学界的普遍认可,且已有足够证据表明该菌感染对人类具有致癌力,与胃腺癌和粘膜相关淋巴组织(malt)淋巴瘤的发生高度相关。1994年,who国际癌症研究机构(iarc)和美国nih相继通过决议,分别宣布:h.pylori为胃炎、胃和十二指肠消化性溃疡的病因,同时也是第一类致癌因子。迄今为止,h.pylori是公认的唯一与癌症发病相关联的病原细菌。
4.h.pylori感染呈全球分布,全球自然人群的感染率超过50%。在发展中国家,50%-80%以上的成年人感染本菌;在发达国家,h.pylori的感染率也达25%~50%。在我国,据流行病学调查,h.pylori感染率为40%-90%,平均为59%;最低地区是广东,为42%;最高地区是西藏,为90%。我国h.pylori的现症感染率为42-64%,平均55%;最低地区是广东,为42%;最高地区是陕西,为64%。我国儿童h.pylori感染率为25-59%,平均40%,并以平均每年0.5%-1%的速度递增。
5.h.pylori一经获得,如果不经治疗便会在人胃内持续定植与生长数年、数十年乃至一生。100%的感染者会出现无症状性胃炎,大约30%的感染者会发展为慢性胃炎,10-20%的感染者发展为胃和十二指肠消化性溃疡,约1%-2%的感染者发展为胃腺癌及胃黏膜相关的淋巴样组织淋巴瘤。临床检测表明,慢性胃炎h.pylori的检出率为54%-100%,慢性活动性胃炎h.pylori的检出率为90%以上,胃溃疡h.pylori的检出率为80%以上,十二指肠溃疡h.pylori的检出率为90%以上。h.pylori感染者胃癌发生率是非感染者的6-8倍,h.pylori感染者的年轻胃癌患者发生率是非感染者的20倍。也有研究证实,h.pylori除了可以引起上述疾病外,还涉及到与许多胃肠道外疾病相关,如与口腔、皮肤、血液、心血管及呼吸系统乃至妊娠与儿科疾病发生相关联。
6.基于人们对h.pylori感染所致疾病在认识上的统一,上述消化道常见与多发疾病采取根除h.pylori治疗的方法已成为共识。目前采用的治疗方法是基于抗生素、质子泵抑制剂和铋化合物的三联或四联组合,疗程持续10-14天。然而,近十年来,随着许多国家对克拉霉素耐药性的迅速增加,世界范围内h.pylori的根除率呈下降趋势。除了越来越多的耐药菌株报道外,治疗费用高、药物依从性差、感染复发率高也是h.pylori感染大规模控制失败的主要原因。因此,研究针对h.pylori的免疫反应和免疫保护机制,对于克服目前治疗方
法存在的问题,更有效地检测与评估,乃至预防和治疗h.pylori感染具有积极意义。
7.h.pylori热休克蛋白a(heat shock protein a,hspa)是一种细菌热休克分子伴侣,是h.pylori感染的关键毒力因子和保护性抗原之一。hspa由118个氨基酸组成,分为两个结构域:a结构域(1-90氨基酸),与groes序列具有序列相似性,以及b结构域(91-118氨基酸),这是h.pylori和helicobacter acinonuchis独有的,含有8个组氨酸和4个半胱氨酸。hspa参与细胞内镍螯合和运输,维持h.pylori的ni2
+
稳态。金属镍可影响h.pylori尿素酶和[nife]氢化酶的活性和功能,这两种酶是h.pylori在胃内存活和定植的重要毒力因子。hspa在h.pylori的诊断、治疗和预防中起着重要作用。大约40%的h.pylori感染者可以检测到hspa抗体。bi
3+
不可逆地与hspa结合并干扰其生物学功能,这种作用是铋化合物治疗效果的主要机制。hspa在小鼠模型中对h.pylori具有明显的免疫保护作用。
[0008]
众所周知,机体通过识别病原菌的表位,产生适应性免疫应答反应,来抵抗外来病原体的入侵与致病。因此,抗原表位的鉴定对于感染性疾病进行免疫诊断、免疫保护机制研究以及疫苗研发具有重要意义。
技术实现要素:
[0009]
本发明一个目的是提供一种hspa抗原表位肽。
[0010]
本发明提供的hspa抗原表位肽为如下1)或2):
[0011]
1)为序列1第2-12位所示的多肽;
[0012]
2)为在1)所示多肽的序列末端添加标签序列。
[0013]
本发明另一个目的是提供一种hspa抗原。
[0014]
本发明提供的抗原,为将上述hspa抗原表位肽与载体蛋白偶联而成。
[0015]
上述抗原中,所述载体蛋白为匙孔血蓝蛋白或者牛血清白蛋白。
[0016]
上述hspa抗原表位肽或上述hspa抗原在作为免疫原制备抗hspa的抗体中的应用也是本发明保护的范围。
[0017]
由上述hspa抗原表位肽或上述hspa抗原在作为免疫原制备的抗hspa的抗体也是本发明保护的范围。
[0018]
上述抗体在如下任一中的应用也是本发明保护的范围:
[0019]
1)检测或辅助检测hspa;
[0020]
2)检测或辅助检测h.pylori;
[0021]
3)制备用于检测或辅助检测hspa的产品;
[0022]
4)制备用于检测或辅助检测h.pylori感染引发相关疾病的产品中的应用。
[0023]
上述hspa抗原表位肽或上述的hspa抗原或上述的抗体或以上述的hspa抗原表位肽为活性成分的物质在如下(a)-(d)中任一种的应用也是本发明保护的范围:
[0024]
(a)制备用于诊断或辅助诊断hspa表达异常相关疾病的产品;
[0025]
(b)制备用于预防hspa表达异常相关疾病的产品;
[0026]
(c)制备用于诊断或辅助诊断h.pylori感染引发相关疾病的产品;
[0027]
(d)制备用于预防h.pylori感染引发相关疾病的产品。
[0028]
上述预防hspa表达异常相关疾病的产品为疫苗,具体可以为多联多聚表位疫苗制剂。
[0029]
本发明还有一个目的是提供一种产品。
[0030]
本发明提供的产品,其活性成分为上述hspa抗原表位肽或上述的hspa抗原或上述的抗体;
[0031]
所述产品具有如下功能中至少一种:
[0032]
(a)用于诊断或辅助诊断hspa表达异常相关疾病;
[0033]
(b)用于预防hspa表达异常相关疾病;
[0034]
(c)用于诊断或辅助诊断h.pylori感染引发相关疾病;
[0035]
(d)用于预防h.pylori感染引发相关疾病。
[0036]
编码上述hspa抗原表位肽的核酸分子也是本发明保护的范围。
[0037]
含有上述核酸分子的表达盒、重组载体或重组细胞系也是本发明保护的范围。
[0038]
本发明从hspa中鉴定了新的b细胞表位hp11,并检测了这些表位肽在h.pylori自然感染人群中的抗体表达谱,为进一步研究hspa在h.pylori感染免疫诊断与免疫预防中的作用提供了基础。由该表位肽制备的抗体,可以用于检测hspa或h.pylori感染。
附图说明
[0039]
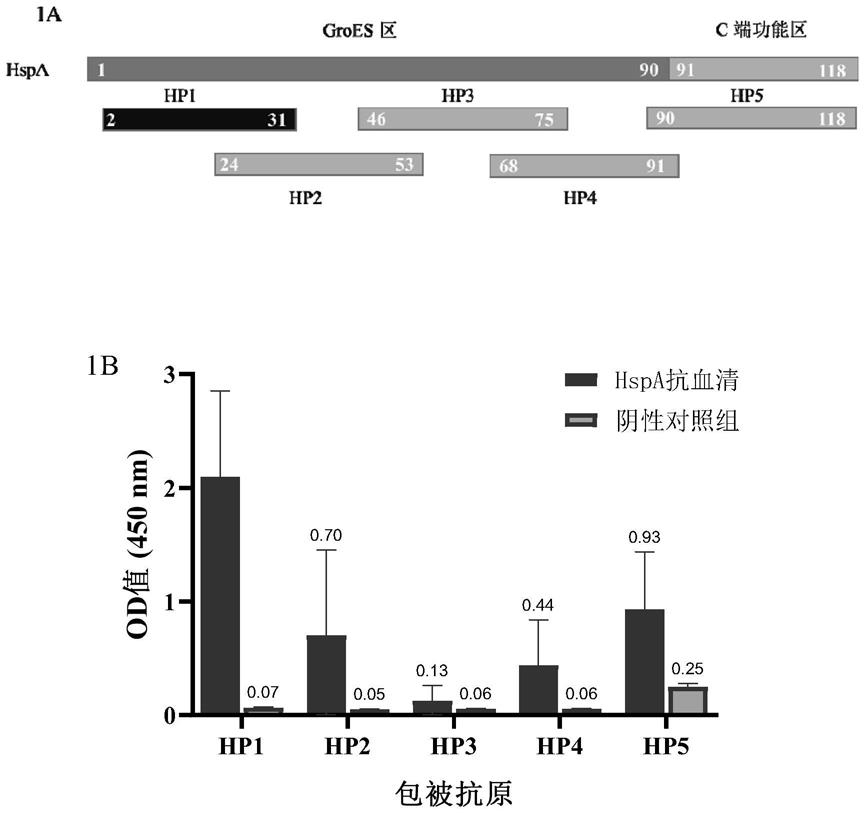
图1为hspa抗原免疫优势反应肽段的筛选。(a)来自h.pylori的hspa截短片段及其相对位置。(b)用20只小鼠抗rhspa血清通过elisa检测到的五个肽段的od值。
[0040]
图2为hspa中hp1肽段的抗原表位精细定位。(a)覆盖hp1的重叠合成肽。每个肽段包含11个氨基酸,其中9个氨基酸与相邻的肽段重叠。(b)11种多肽与小鼠抗rhspa血清的elisa检测结果。
[0041]
图3为hp11和hp19抗原表位的免疫原性和免疫反应性。(a)抗原表位-klh小鼠抗血清与合成表位肽的elisa检测结果。用合成的表位肽hp11和hp19为包被抗原,抗原表位-klh小鼠抗血清为一抗,pbs免疫小鼠血清为阴性对照。(b)hp11-klh免疫小鼠抗血清免疫印迹分析。(c)hp19-klh免疫小鼠抗血清免疫印迹分析。(d)rhspa免疫小鼠抗血清免疫印迹分析。
[0042]
图4为抗原表位特异性淋巴细胞增殖反应。抗原表位刺激相应的hp11-klh(a)和hp19-klh(b)免疫小鼠的脾淋巴细胞发生增殖反应。抗原表位刺激pbs免疫的小鼠脾淋巴细胞作为阴性对照,cona刺激作为阳性对照。脾淋巴细胞刺激指数(stimulation index,si)为刺激孔的od值除以对照孔的od值。*p《0.05,**p《0.01vs.阴性对照。
[0043]
图5为抗原表位hp11(a)和hp19(b)在自然感染者中的血清抗体谱。用来自感染h.pylori患者的42例hspa血清阳性样品,通过elisa检测针对抗原表位hp11和hp19的血清抗体od值。17例h.pylori抗体阴性血清用作阴性对照。阳性判定标准:od值》阴性对照血清平均od值*2.1。
具体实施方式
[0044]
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
[0045]
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
[0046]
下述实施例中细菌菌株和培养条件:
[0047]
下述实施例中的h.pyloriss2000超声破碎物上清液按照如下方法制备:将
h.pylori菌株sydney菌株2000(ss2000)(thompson lj,danon sj,wilson je,et al.chronic helicobacter pylori infection with sydney strain 1and a newly identified mouse-adapted strain(sydney strain 2000)in c57bl/6and balb/c mice.infection and immunity,2004,72(8):4668
–
4679)和nctc11637(美国atcc,atcc43504)在含有7%胎牛血清的h.pylori选择性琼脂平板(campylobacter agar base)上,在37℃、5%o2、10%co2和85%n2的微需氧条件下培养。培养3天后,刮取菌落并用ph7.0浓度为20mm的预冷的磷酸盐缓冲液(pbs)洗涤两次,然后在4℃下以10,000
×
g离心10分钟获得菌体沉淀。将h.pylori ss2000沉淀重悬在pbs中,通过冰浴条件下超声破碎(300w,10s,10s,20min),离心20分钟,收集h.pylori ss2000上清液,即为含有hspa的上清液,用于蛋白免疫印迹(western blotting,wb)。将h.pylori nctc11637细菌沉淀,用细菌基因组dna提取试剂盒(北京天根生化科技有限公司)提取nctc11637基因组dna。
[0048]
下述实施例中h.pylori重组hspa(rhspa)和gst融合肽的构建、表达和纯化方法如下:
[0049]
hspa的基因序列(序列2)通过pcr从幽门螺杆菌菌株nctc11637的基因组中直接扩增,并克隆到pgex-6p-1(+)(ge healthcare)表达载体中,置于bamhi和noti或xhoi酶切位点之间,得到重组质粒。重组质粒转化至大肠杆菌bl21(de3)plyss细胞(cwbio)中,用1mmiptg诱导表达重组融合蛋白gst-hspa。通过离心收集细胞并将细菌沉淀重悬于pbs中,超声破碎重悬的细胞,离心收集上清液,即含有重组表达的gst-hspa融合蛋白。
[0050]
重组gst-hspa融合蛋白,通过price glutathione superflow agarose(thermo)纯化。然后,用precision protein酶(beyotime)切除gst标签,并使用gst标签纯化树脂(beyogold)去除,根据说明书(ge healthcare,usa)进行纯化,得到重组蛋白rhspa。
[0051]
纯化后的重组蛋白rhspa用sds-page分析,纯化蛋白的浓度用bca法测定。
[0052]
gst-hp11和gst-hp19的构建、表达和纯化与gst-hspa融合蛋白相似,仅是将hspa的编码基因序列替换为hp11或hp19多肽对应的编码基因序列,且gst标签并未被移除。
[0053]
下述实施例中hp1-hp5多肽的合成,覆盖hp1全长的各重叠肽的合成,多肽hp11与hp19同钥孔血蓝蛋白(klh)的偶联(制备hp11-klh偶联肽或hp19-klh偶联肽),均由genscript(中国南京)完成。标准固相fmoc方法用于肽合成,通过高压液相色谱法评估纯度》95%,并通过激光解吸质谱法鉴定。将肽以10mg/ml的浓度溶解在dmso或超纯水中,并在-20℃下分装储存。
[0054]
下述实施例中elisa检测方法如下:
[0055]
用多肽作为抗原进行包被时,先将96孔elisa板(costar)在37℃下用150μl2.5%戊二醛预处理1小时,然后用水洗涤四次。表位肽作为包被抗原在0.1mm碳酸盐缓冲液(ph9.6)中稀释并包被elisa板(30μg/ml,100μl/孔),在37℃下孵育过夜。hspa做抗原进行包被时,抗原在0.1mm碳酸盐缓冲液(ph9.6)中稀释并包被elisa板(2μg/ml,100μl/孔),4℃孵育过夜。用pbst洗板3次。
[0056]
用封闭缓冲液(含有5%脱脂牛乳的pbst用于小鼠血清,无蛋白封闭液(thermo)用于人血清)加入elisa板,200μl/孔,37℃封闭1小时。去除封闭液,每孔加入100μl rhspa免疫血清(1:500)或klh结合肽免疫血清(1:100)或h.pylori阳性血清(1:100)并在37℃孵育1小时。pbs免疫小鼠或h.pylori感染阴性的健康人血清用作阴性对照。
[0057]
用pbst洗涤孔3次后,将hrp偶联的兔抗小鼠igg(1:5,000稀释度,abcam)或山羊抗人igg(1:20,000稀释度,abcam)二抗加入孔中(100μl/孔),37℃孵育1小时,同上洗涤elisa板。以100μl/孔加入酶底物溶液3,3,5,5-四甲基苯-联苯(tmb),反应在室温下进行15分钟。用100μl1mh2so4终止反应,用elisa酶标仪测量450nm(a450)处的吸光度。所有检测均用复孔进行,检测结果用复孔平均值。
[0058]
下述实施例中的rhspa抗血清按照如下方法制备:免疫6-8周龄雌性spf balb/c小鼠(军事医学研究院实验动物中心,每组20只),初次免疫采用50μg rhspa与完全弗氏佐剂(sigma)混合的乳剂进行皮下免疫。免后第10天和第20天使用50μg rhspa与不完全弗氏佐剂(sigma)混合的乳剂加强免疫。在第30天处死小鼠,收集血清样品即为抗rhspa血清。
[0059]
下述实施例中的统计分析,所有数据均表示为平均值
±
标准偏差(s.d.)。使用双尾t检验比较平均值,使用graphpad prism8.0.2(graphpad software)进行分析,p《0.05被认为具有统计学意义。
[0060]
实施例1、hspa抗原表位肽的鉴定与制备及免疫原性与免疫反应性检测
[0061]
一、hspa抗原免疫优势反应肽段的筛选
[0062]
将hspa(氨基酸序列为序列表中序列1)截短为五段,前4个肽段位于hspa的a结构域,每个片段重叠8个氨基酸,从n端到c端依次命名为hp1-hp4;第5个肽段位于b结构域,与hp4重叠2个氨基酸(图1a)。
[0063]
hp1肽段的氨基酸序列为序列1第2-31位;
[0064]
hp2肽段的氨基酸序列为序列1第34-53位;
[0065]
hp3肽段的氨基酸序列为序列1第46-75位;
[0066]
hp4肽段的氨基酸序列为序列1第68-91位;
[0067]
hp5肽段的氨基酸序列为序列1第90-118位;
[0068]
合成上述五段多肽作为抗原,并通过elisa用20只小鼠抗rhspa血清(hspa抗血清)检测。
[0069]
结果如图1b所示,表明hp1可与所有抗血清发生反应,免疫反应最强,hp1是hspa抗原免疫优势反应区段。
[0070]
二、hp1抗原表位的精细定位
[0071]
为了对hspa中hp1肽段的抗原表位进行精细定位,合成了一组11个氨基酸的重叠多肽,覆盖了hspa的2-31氨基酸,总共获得了11个多肽(图2a)。
[0072]
hp11多肽的氨基酸序列为序列1第2-12位;
[0073]
hp12多肽的氨基酸序列为序列1第4-14位;
[0074]
hp13多肽的氨基酸序列为序列1第6-16位;
[0075]
hp14多肽的氨基酸序列为序列1第8-18位;
[0076]
hp15多肽的氨基酸序列为序列1第10-20位;
[0077]
hp16多肽的氨基酸序列为序列1第12-22位;
[0078]
hp17多肽的氨基酸序列为序列1第14-24位;
[0079]
hp18多肽的氨基酸序列为序列1第16-26位;
[0080]
hp19多肽的氨基酸序列为序列1第18-28位;
[0081]
hp20多肽的氨基酸序列为序列1第20-30位;
[0082]
hp21多肽的氨基酸序列为序列1第21-31位;
[0083]
合成上述多肽,用合成多肽作为包被抗原进行elisa板包被,采用elisa方法检测11个多肽与20只小鼠抗rhspa血清(hspa抗血清)的反应性。
[0084]
结果如图2b所示,可以看出,hp11、hp18、hp19和hp20能够发生较强的免疫反应。其中,三种肽hp18、hp19和hp20的序列相似,且hp19(enktssgiiip)免疫反应最强,推测hp19可能是hspa的一个抗原表位。此外,hp11(kfqplgervlv)的免疫反应与hp20相当,可能是hspa的另一个表位。
[0085]
三、hp11表位肽和hp19表位肽的免疫原性和免疫反应性检测
[0086]
在初步确定了hspa中的两个b细胞表位,首先评估了这些表位是否能够诱导小鼠产生免疫反应,具体如下:
[0087]
1、hp11的klh偶联肽(hp11-klh)和hp19的klh偶联肽(hp19-klh)
[0088]
为了增强多肽的免疫原性,在hp11和hp19的c端连接了一个半胱氨酸,然后使用mbs方法将它们偶联到klh上形成klh偶联肽。
[0089]
hp11-klh偶联肽为将hp11的c端连接了一个半胱氨酸得到的多肽,再将c端连接半胱氨酸的hp11偶联到klh上,形成hp11-klh偶联肽(c端连接半胱氨酸的hp11和klh的投料质量比1:1)。
[0090]
hp19-klh偶联肽为将hp19的c端连接了一个半胱氨酸得到的多肽,再将c端连接半胱氨酸的hp19偶联到klh上,形成hp19-klh偶联肽(c端连接半胱氨酸的hp11和klh的投料质量比1:1)。
[0091]
2、小鼠免疫及样本采集
[0092]
通过免疫6-8周龄雌性spf balb/c小鼠(军事医学研究院实验动物中心,每组10-20只)来评估rhspa和hp11-klh偶联肽或hp19-klh偶联肽的免疫原性。
[0093]
初次免疫采用50μg rhspa或50μg hp11-klh偶联肽或50μg hp19-klh偶联肽分别与完全弗氏佐剂(sigma)混合的乳剂进行皮下免疫。
[0094]
初免后第10天和第20天,分别使用同初次免疫相同种类和剂量的抗原与不完全弗氏佐剂(sigma)混合制备的乳剂进行加强免疫。
[0095]
对照小鼠使用相同的免疫程序用pbs进行免疫。
[0096]
在第30天处死小鼠,收集血清样品,得到rhspa免疫血清、hp11-klh偶联肽免疫血清、hp19-klh偶联肽免疫血清,并通过elisa和蛋白免疫印迹分析;收集脾组织获得rhspa免疫小鼠脾细胞、hp11-klh偶联肽免疫小鼠脾细胞、hp19-klh偶联肽免疫小鼠脾细胞进行淋巴细胞增殖试验。
[0097]
所有动物均购自维通利华(中国北京),并在spf条件下饲养。
[0098]
3、elisa检测抗原表位的免疫原性
[0099]
按照前面所述的方法,以hp11多肽和hp19多肽作为检测抗原进行包被,将上述2采集的小鼠hp11-klh偶联肽免疫血清(1:100,又称为hp11-klh抗血清)和hp19-klh偶联肽免疫血清(1:100,又称为hp11-klh抗血清)分别作为抗体,用elisa方法检测klh偶联肽免疫小鼠获得的所有血清。以pbs免疫小鼠血清作阴性对照。
[0100]
检测结果如图3a所示,注射hp11-klh偶联肽和hp19-klh偶联肽可诱导小鼠产生强烈的免疫反应,2种表位肽特异性抗体(抗血清)滴度均超过1:1000。两个抗原表位均能够同
devices,美国)测量a450。脾淋巴细胞刺激指数(si)为刺激孔的od值除以对照孔的od值。
[0114]
结果如图4所示,cona能够刺激小鼠脾细胞发生非特异性强烈增值,抗原表位肽刺激相应的抗原表位肽-klh偶联肽免疫小鼠脾淋巴细胞增殖活性显着高于阴性对照组(p《0.01,图4)。
[0115]
四、自然感染者抗原表位的抗体检测
[0116]
用来自h.pylori自然感染者的血清,检测了hspa中鉴定的两个b细胞表位的抗体表达谱。
[0117]
本研究经解放军总医院第四医学中心伦理委员会批准,并获得患者知情同意。采集住院患者血清,采用h.pylori igg elisa试剂盒(ibl)检测是否存在抗h.pylori抗体。实验操作按照试剂盒说明书进行。当临界指数(coi)》1.2时,血清被认为是h.pylori阳性,当临界指数(coi)《0.8时,血清被认为是h.pylori阴性。
[0118]
选取85例h.pylori阳性血清(命名为p1-p85)用elisa方法检测hspa抗体和表位抗体,包被抗原分别为rhspa、表位肽hp11和hp19,17例h.pylori抗体阴性血清作为阴性对照。hspa抗体和表位抗体阳性判断限为:od值》阴性对照血清平均od值*2.1。
[0119]
结果如下:85例h.pylori感染患者中elisa检测42例hspa抗体阳性,阳性率为49.4%。17例h.pylori igg elisa试剂盒检测阴性血清(n1-n17),作为阴性对照。在42例hspa血清阳性患者中,9例检测到针对hp11抗原表位的抗体呈阳性,14例hp19抗原表位的抗体阳性,阳性率分别为21.4%和33.3%。下图为hspa血清阳性患者中两个表位的抗体反应谱(图5)。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1