一株产异黄酮类成分的黄芪内生细菌及其应用的制作方法
1.本发明涉及一株黄芪内生细菌及其应用。
背景技术:
2.黄芪为豆科植物蒙古黄芪(astragalus membranaceus(fisch.)bge.var.mongholicus(bge.)hsiao)或膜荚黄芪(astragalus membranaceus(fisch.)bge.)的干燥根,全世界共存在11亚属,其中有8亚属存在于中国,大多分布在中国的东北、西北和华北地区,具有补气升阳,固表止汗,利水消肿,生津养血,行滞通痹,托毒排脓,敛疮生肌的功效,在《神农本草经》中就已将其列为上品,且具有高效、低毒的特性,在医疗保健方面具有不可或缺的作用,具有广泛的开发前景。
3.研究表明,黄芪含有皂苷、多糖、黄酮、核黄素、叶酸、香豆素、生物碱、多种氨基酸、有机酸、微量元素等化学成分。其中皂苷类成分黄芪甲苷及黄酮类成分毛蕊异黄酮葡萄糖苷为《中国药典》2020版黄芪含量测定项下的指标成分。
4.黄芪具有广泛的药理作用,临床上用于治疗肾炎、糖尿病、蛋白尿、高血压、肝硬化和癌症等疾病。毛蕊异黄酮和芒柄花素作为黄芪的主要异黄酮类苷元,已被证实具有抗菌、抗肿瘤、抗氧化、降低血糖等作用,因此,黄芪中毛蕊异黄酮和芒柄花素的高效生产在食品和医药领域具有重要意义。
5.目前,关于毛蕊异黄酮及芒柄花素的生产,大多采用柱色谱等分离技术从药用植物中进行提取分离,但这样的分离工艺不仅浪费药用植物资源,且不利于工业化生产。
技术实现要素:
6.本发明是要解决现有从植物中提取毛蕊异黄酮及芒柄花素的方法存在浪费药用植物资源的问题,提供一株产异黄酮类成分的黄芪内生细菌及其应用。
7.本发明提供一株黄芪内生细菌,为枯草芽孢杆菌(bacillus subtilis)hhqx8,保藏于中国典型培养物保藏中心(cctcc),保藏地址是武汉市武汉大学,保藏日期为2021年11月08日,保藏编号为cctcc no:m20211384。
8.本发明枯草芽孢杆菌hhqx8的细胞形态为杆状,有鞭毛,菌落形态为圆形,菌落颜色为乳白色,革兰氏染色呈阳性,有菌膜形成。
9.本发明枯草芽孢杆菌hhqx8的淀粉水解反应、明胶液化试验、接触酶试验、油脂水解实验、g
+
/g-、甲基红试验、运动性试验、v.p试验、硝酸盐还原试验均呈阳性。
10.本发明枯草芽孢杆菌hhqx8为好氧菌,最适生长温度为37℃,最适盐浓度为4%nacl,最适生长ph值为7.0,对数生长期为10~20h。
11.本发明枯草芽孢杆菌hhqx8通过16s rdna序列比对分析,与bacillus subtilis mon6(mg833866)聚于同一分支,且两者同源性为95%。通过结合菌体形态特征、生长条件、生理生化特征和分子鉴定结果确定,本发明的菌株hhqx8属于枯草芽孢杆菌(bacillus subtilis)。
12.本发明还提供枯草芽孢杆菌hhqx8在发酵产黄芪异黄酮类化合物中的应用。
13.进一步的,所述黄芪异黄酮类化合物为毛蕊异黄酮和芒柄花素。
14.进一步的,黄芪异黄酮类化合物的提取方法为:
15.取枯草芽孢杆菌hhqx8发酵液,离心除去菌体,上清液通过d
101
大孔吸附树脂柱洗脱后,依次以不同浓度乙醇洗脱,收集70%乙醇洗脱液,回收乙醇,再通过聚酰胺柱,采用氯仿/甲醇洗脱,按10ml/瓶收集洗脱液,随行采用tlc法进行跟踪检测,合并含有黄芪异黄酮类成分的洗脱液,回收溶剂后,采用硅胶柱色谱分离,以石油醚/乙酸乙酯梯度洗脱,收集石油醚/乙酸乙酯洗脱液x,经tlc法进行跟踪检测,合并含有黄芪异黄酮类成分的洗脱液,重结晶处理,纯化得到芒柄花素;继续收集石油醚/乙酸乙酯洗脱液y,合并含有黄芪异黄酮类成分的洗脱液,多次重结晶,纯化得到毛蕊异黄酮。
16.进一步的,所述不同浓度乙醇为体积浓度依次为30%、50%、70%和90%的乙醇溶液。
17.进一步的,石油醚/乙酸乙酯洗脱液x中石油醚:乙酸乙酯为10:1。
18.进一步的,石油醚/乙酸乙酯洗脱液y中石油醚:乙酸乙酯为1:1。
19.本发明的有益效果:
20.本发明中黄芪内生细菌hhqx8的次生代谢物中含有毛蕊异黄酮及芒柄花素,具有较好的抗氧化活性。
21.本发明可以通过发酵黄芪内生细菌hhqx8来产毛蕊异黄酮和芒柄花素,纯度较高,芒柄花素的纯度可达98.63%,毛蕊异黄酮的纯度可达99.84%。本发明避免了浪费药用植物资源,且利于工业化生产。
22.本发明为采用微生物发酵法生产黄芪异黄酮类化合物提供新方法。
附图说明
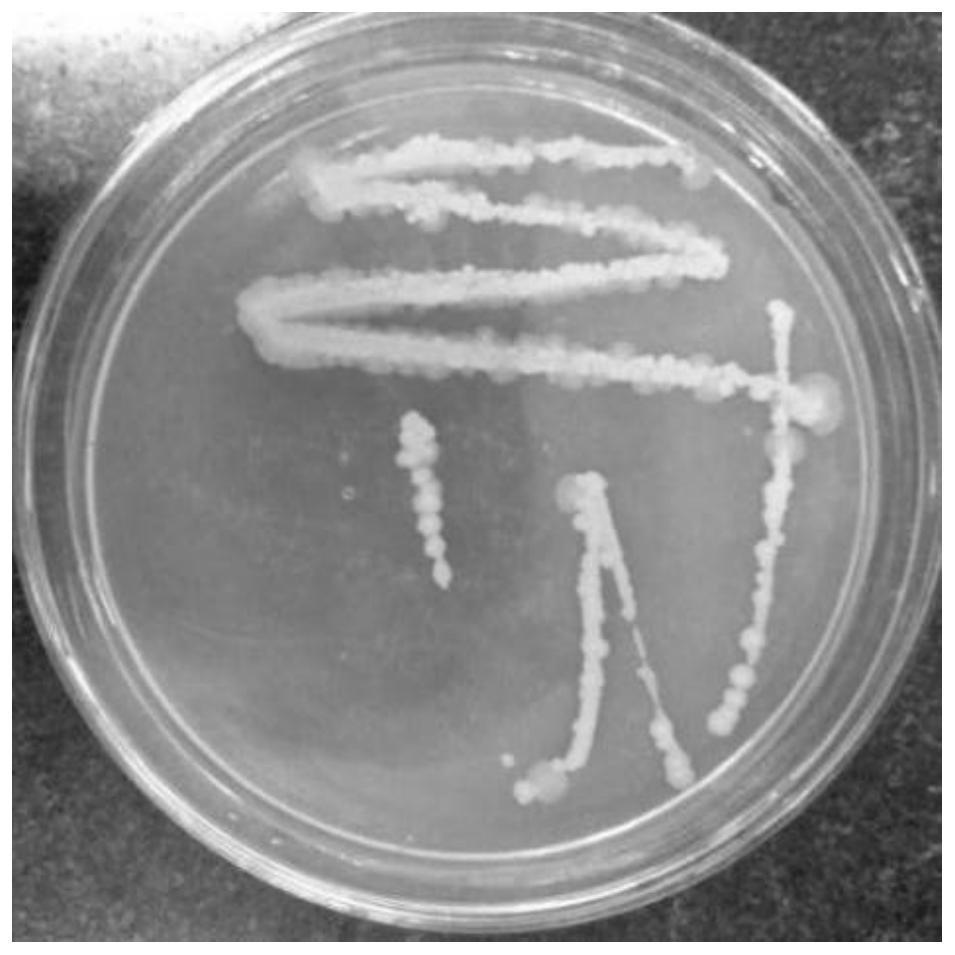
23.图1为黄芪内生细菌hhqx8的菌落形态;
24.图2为黄芪内生细菌hhqx8的显微形态;
25.图3为黄芪内生细菌hhqx8的系统发育树;
26.图4为黄芪内生细菌hhqx8对dpph自由基的清除能力;
27.图5为黄芪内生细菌hhqx8对
·
oh自由基的清除能力;
28.图6为黄芪内生细菌hhqx8发酵液次生代谢产物分析结果;
29.图7为化合物a的高效液相色谱图;
30.图8为化合物a与芒柄花素混合的高效液相色谱图;
31.图9为化合物b的高效液相色谱图;
32.图10为化合物b与毛蕊异黄酮混合的高效液相色谱图
具体实施方式
33.下面对本发明的实施例做详细说明,以下实施例在以本发明技术方案为前提下进行实施,给出了详细的实施方案和具体的操作过程,但本发明的保护范围不限于下述的实施例。
34.实施例1:
35.本实施例黄芪内生细菌,为枯草芽孢杆菌(bacillus subtilis)hhqx8,保藏于中国典型培养物保藏中心(cctcc),保藏地址是武汉市武汉大学,保藏日期为2021年11月08日,保藏编号为cctcc no:m20211384。
36.实施例2:本实施例黄芪内生细菌hhqx8的获取方法为:
37.选取健康膜荚黄芪根(膜荚黄芪选自黑龙江省林口县百里黄芪谷的健康膜荚黄芪),冲洗干净,放置阴干,切成5cm小段,置于75%酒精中浸泡1min,然后置于5%naclo中漂洗10min,接着用75%酒精浸泡1min,最后以无菌水冲洗3次后作为消毒后的实验材料;取最后一次无菌水冲洗液涂布培养平板或取适量此冲洗液倒入na培养基内作对照,另外在相同条件下,将消毒之后的实验材料于培养平板上滚动培养一周,作为对照。
38.将消毒后的实验材料两端用无菌手术刀各切1cm,使木质部与韧皮部分离,置于na培养基中,于37℃温培养箱中,培养3-5d。待实验材料周围已经长出菌体之后,挑取菌体并转入na培养基平板,多次划线后分离纯化,得到内生细菌hhqx8,将纯化后的菌株进行斜面培养,4℃条件下保存备用。
39.牛肉膏蛋白胨液体培养基(nb):取牛肉膏6g,蛋白胨20g,nacl 10g,依次加入到沸水中,定容为2l,ph值为7.0,分装完成后进行灭菌处理(121℃,30min)。
40.牛肉膏蛋白胨固体培养基(na):将nb培养基原料加入到沸水中后,少量多次加琼脂40g,定容为2l,ph值为7.0,分装完成后进行灭菌处理(121℃,30min)。
41.实施例2:内生细菌hhqx8的形态学观察及生理生化鉴定结果
42.内生细菌hhqx8的菌落形态如图1所示,内生细菌hhqx8的显微形态如图2所示。内生细菌hhqx8形态学观察及生理生化鉴定结果见表1
43.表1黄芪内生细菌hhqx88形态学观察及生理生化鉴定结果
[0044][0045]
实施例3:内生细菌hhqx8的分子鉴定
[0046]
黄芪内生细菌hhqx8的16s rdna序列扩增后获得1条1491bp的特异性条带,序列如序列表中seq id no:1所示,将测序结果利用blast分析并与genbank中的核苷酸序列进行比对,然后用mega6.0软件构建内生细菌hhqx8的系统发育树(见图3),分析结果表明,内生细菌hhqx8的16s rdna序列与bacillus subtilis mon6(mg833866)聚于同一分支,且两者
同源性为95%,综合形态学鉴定、生理生化指标的测定以及16srdna序列测定分析结果,将黄芪内生细菌hhqx8鉴定为枯草芽孢杆菌(bacillus subtilis)。
[0047]
实施例4:内生细菌hhqx8的抗氧化活性分析
[0048]
(一)内生细菌hhqx8发酵液的制备:
[0049]
将内生细菌hhqx8接种于na培养基,恒温活化培养(37℃,3d),取活化后的内生细菌hhqx8,制备1
×
107cfu
·
ml-1
的种子液(制备条件:无菌条件,挑取菌丝体接种于60mlnb培养基中,37℃,120r
·
min-1
,3d);以5%接种量将内生细菌hhqx8的种子液接种到300ml的nb培养基,恒温培养(37℃,120r
·
min-1
,5d),抽滤,收集内生细菌hhqx8发酵液,减压浓缩后,利用乙酸乙酯萃取(3
×
100ml),减压浓缩,即得内生细菌hhqx8发酵液待测样品,冻干。
[0050]
(二)dpph自由基清除能力测定:
[0051]
将5.9mg dpph溶于甲醇并定容至100ml,制备质量浓度为0.15mmol
·
l-1
的dpph溶液;将2mgvc溶于甲醇并定容至10ml,即得200μg
·
ml-1
的对照品液;取步骤(一)中内生细菌hhqx8发酵液冻干粉2mg,溶于甲醇后定容至10ml,即得200μg
·
ml-1
供试品液。
[0052]
分别将上述对照品溶液和供试品溶液依次稀释浓度至100μg
·
ml-1
、50μg
·
ml-1
、25μg
·
ml-1
、12.5μg
·
ml-1
、6.25μg
·
ml-1
,分别取上述溶液2ml置于试管中,同时以甲醇作为空白对照组。各试管中分别加入0.15mmol
·
l-1
的dpph溶液4ml,反应溶液于暗处放置30min后取出,517nm下检测各样品的吸光度值(n=3),dpph自由基清除率计算公式如下:
[0053][0054]
其中,ai表示同时加入待测样品与dpph溶液的吸光度值;aj表示同时加入待测样品与空白对照的吸光度值;a0表示同时加入空白对照与dpph溶液的吸光度值。
[0055]
dpph自由基清除能力测定结果:内生细菌hhqx8对dpph自由基的清除能力见图4,其中曲线a表示内生细菌hhqx8,b表示vc。
[0056]
(三)
·
oh自由基清除能力的测定:
[0057]
取上述不同浓度的各供试品溶液2ml置于试管中,分别依次加入2ml质量浓度为6mmol
·
l-1
的feso4、2ml质量浓度为6mmol
·
l-1
的h2o2后摇匀静置10min,加入2ml浓度为6mmol
·
l-1
的水杨酸-乙醇溶液,使反应溶液在37℃条件下静置30min,510nm下测量各样品的吸光度值(n=3),
·
oh自由基清除率计算公式如下:
[0058][0059]
其中,a1表示加入样品的吸光度值;a2表示空白对照代替水杨酸-乙醇溶液的吸光度值;a 0
表示空白对照代替样品的吸光度值。
[0060]
·
oh自由基清除能力的测定结果:内生细菌hhqx8对
·
oh自由基的清除能力见图5,其中曲线a表示内生细菌hhqx8,b表示vc。
[0061]
结论:黄芪内生细菌hhqx8发酵液在测试浓度范围内清除dpph自由基和
·
oh自由基的活性随质量浓度的增高而增强,其抗氧化能力与质量浓度具有量效关系。当浓度为100μg
·
ml-1
时,内生细菌hhqx8对dpph自由基的清除率达到85.12%,对
·
oh自由基的清除率达到80.11%,相比之下,内生细菌hhqx8对dpph自由基的清除能力更强。根据量效关系计算得
出,内生细菌hhqx8对dpph的半数清除率(ic
50
值)达到3.90
±
0.02μg
·
ml-1
,而对
·
oh自由基的ic
50
值为22.42
±
0.12μg
·
ml-1
。
[0062]
实施例5:黄芪内生细菌hhqx8次生代谢产物分析
[0063]
(一)hplc条件:
[0064]
venusil xbp-c
18
柱(4.6mm
×
250mm,5μm,usa);流动相:甲醇-水(65∶35)流速:1ml
·
min-1
;柱温:25℃;检测波长:254nm;进样量:10μl。
[0065]
(二)对照品溶液的制备:
[0066]
精密称取毛蕊异黄酮、芒柄花素对照品适量,以甲醇溶解成0.5mg/ml对照品溶液,备用。
[0067]
(三)供试品溶液的制备:
[0068]
取实施例4步骤(一)中内生细菌hhqx8发酵液冻干粉2mg,溶于甲醇后定容至10ml,即得200μg
·
ml-1
供试品液。
[0069]
内生细菌hhqx8发酵液次生代谢产物分析结果如图6所示。其中a为芒柄花素对照品,b为毛蕊异黄酮对照品,c为hhqx8发酵液,d为pdb培养基。
[0070]
由图6可知,在hhqx8发酵液中含有与宿主植物黄芪相同的异黄酮类化合物芒柄花素及毛蕊异黄酮。
[0071]
实施例6:黄芪内生细菌hhqx8发酵液中黄酮类成分的分离
[0072]
取内生细菌hhqx8发酵液15l,离心除去菌体,上清液通过d
101
大孔吸附树脂柱洗脱后,依次以不同浓度乙醇洗脱(30%,50%,70%,90%),收集70%乙醇洗脱液,回收乙醇,再通过聚酰胺柱,采用氯仿:甲醇(20:1)洗脱,收集洗脱液(10ml/瓶),随行采用tlc法进行跟踪检测,合并含有黄芪异黄酮类成分的洗脱液,回收溶剂后,采用硅胶柱色谱分离,以石油醚:乙酸乙酯梯度洗脱,收集石油醚:乙酸乙酯(10:1)洗脱液,经tlc活性跟踪检测,合并含有黄芪异黄酮类成分的洗脱液,重结晶处理,纯化得到化合物a;继续收集石油醚:乙酸乙酯(1:1)洗脱液,合并含有黄芪异黄酮类成分的洗脱液,多次重结晶,纯化得到化合物b。采用hplc及1h-nmr确定单体化合物结构。
[0073]
化合物a的高效液相色谱图如图7所示,化合物a与芒柄花素混合的高效液相色谱图如图8所示。由图7、图8的hplc分析结果可知,化合物a与混合样品均出现单一色谱峰,证明化合物a为纯度较高的单体化合物,疑似芒柄花素,其纯度为98.63%,为进一步确认该化合物的结构,采用1h-nmr进行鉴别。
[0074]
化合物a的1h-nmr鉴定结果:1h nmr(400mhz,meod)δ:8.16(1h,s,h-2),8.06(1h,d,j=8.8hz,h-5),7.47(2h,d,j=8.6hz,h-2’,6’),6.98(2h,d,j=8.6hz,h-3’,5’),6.94(1h,dd,j=8.9,2.1hz,h-6),6.86(1h,d,j=2.1hz,h-8),3.82(3h,s,-och3),c环符合黄酮类物质h谱耦合特征,在化学位移δ8.16(1h,s)处出现异黄酮2位质子信号,化合物b初步分析为异黄酮;a环存在1’,3’,3
’‑
三取代的苯环,说明化合物b是有7-oh取代的异黄酮;由δ:7.47(2h,d,j=8.6hz)和6.98(2h,d,j=8.6hz)推测b环含有一个aa’bb’耦合系统的苯环,在化学位移δ3.82(3h,s)处出现甲氧基信号,4’取代基为och3。
[0075]
综上所述,经tlc、hplc和1h-nmr鉴定,化合物a的化学式为c
16h12
o4,通过与文献中数据对比分析,将单体化合物a鉴定为7-hydroxy-4
’‑
methoxyisoflavone,即芒柄花素(formononetin),化学结构如下:
[0076][0077]
单体化合物b(6.8mg,产率为0.680mg
·
l-1
)为浅黄色结晶,易溶解于甲醇、乙酸乙酯、氯仿等有机溶剂,采用hplc,以毛蕊异黄酮作为对照品,采用标准加入法对化合物b进行hplc分析,结果如图9和图10所示。
[0078]
由图9和图10分析可得,化合物b与混合样品均出现单一吸收峰,证明化合物b为纯度较高的单体化合物,其纯度为99.84%,疑似毛蕊异黄酮,为进一步确认该化合物的结构,采用1h-nmr进行鉴别。
[0079]
化合物b的1h-nmr鉴定结果:1h nmr(400mhz,meod)δ:8.13(1h,s,h-2),8.05(1h,d,j=8.8hz,h-5),7.04(1h,s,h-2’),6.97(2h,s,h-5’,6’),6.94(1h,dd,j=8.8,2.2hz,h-6),6.85(1h,d,j=2.1hz,h-8),3.88(3h,s,-och3)。在化学位移δ8.13(1h,s)处出现异黄酮2位质子信号,说明化合物b属于异黄酮;δ:8.05(1h,d,j=8.8hz)、6.94(1h,dd,j=8.8,2.2hz)和6.85(1h,d,j=2.1hz)表明含有一个三取代的苯环,推测化合物b是a环有7-oh取代的异黄酮;化学位移δ:7.04(1h,s,h-2’)和6.97(2h,s,h-5’,6’)表示b环有一个abx耦合系统的苯环,为3’,4
’‑
二氧取代异黄酮,在δ3.88(3h,s)处出现一个甲氧基信号,4’取代基为och3。
[0080]
综上所述,经tlc、hplc和1h-nmr鉴定,化合物b的化学式为c
16h12
o5,通过与文献中数据对比分析,将单体化合物b鉴定为7,3
’‑
dihydroxy-4
’‑
methoxyisoflavone,即毛蕊异黄酮(calycosin),化学结构如下:
[0081][0082]
综上所述,黄芪内生细菌hhqx8为黄芪异黄酮类成分——毛蕊异黄酮及芒柄花素的产生菌。作为中国农业部和美国食品药物管理局(fda)认定的安全菌株,枯草芽孢杆菌常作为益生菌在药品生产、食品发酵等方面被广泛应用,产生了巨大的经济效益以及社会效益,枯草芽孢杆菌的开发与利用正在成为研究热点之一,鉴于此,黄芪内生细菌hhqx8具有广阔的应用前景。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1