一种含有五价磷中心的氮磷杂环的合成方法与流程
1.本发明涉及有机合成领域,具体讲就是涉及一种含有五价磷中心的氮磷杂环的合成方法。
背景技术:
2.有机磷化合物具有重要的学术和工业价值,在药物设计、生命科学、材料开发和合成化学中具有广泛的应用。o、s和n是杂环化合物中最常见的成员,但p也可以以这种方式发挥作用,根据价电子的数量,这些化合物可分为p(iii)和p(v)-磷杂环。由于其空间和能量分离的s和p轨道,p原子可提供独特的结构特性和电子特性。因此,环状系统的p掺杂,可以产生具有特定立体化学的手性骨架,这会对化合物结构和功能产生影响。
3.磷杂环的制备传统上依赖于多步有机合成,步骤繁琐,收率低;现有技术中钯催化下c
–
p键闭环复分解制备磷杂环的方法,虽然提高了收率,但是,p-立体杂环化合物的制备依然步骤冗长,反应收率低,手性环境难以控制。
技术实现要素:
4.本发明的技术目的,就是针对上述现有磷杂环化合物制备,步骤冗长,反应收率低,手性环境难以控制的难题,提供一种含有五价磷中心的氮磷杂环的合成方法,该方法操作简单,通用性高;在所开发的催化体系中,手性氮磷杂环可用手性p(iii)前体作原料,得到手性保持的氮磷杂环化合物。降低了生产成本的同时,得到了高价值产物。
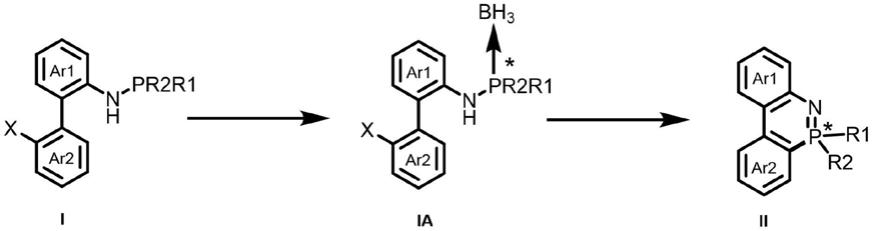
5.为了实现上述技术目的,本发明提出的一种含有五价磷中心的氮磷杂环化合物的合成方法,其特征在于,其合成路线如下
[0006][0007]
其中
[0008]
x为氟或氯或溴或碘;
[0009]
ar1为苯基或萘基或蒽基或吡啶基;
[0010]
ar2为苯基或萘基或蒽基或吡啶基;
[0011]
r1和r2能够是相同或不同的基团,所述r1和r2为c1-c10烷基或c3-c12环烷基或苯基或萘基;
[0012]
ar1和ar2分别能够被一个或多个相同或不同的r3取代;
[0013]
r3为氢或c1-c4烷基或c1-c4卤代烷基或卤素或c1-c4烷氧基或c1-c4卤代烷氧基或c1-c4氰基或c1-c4烷氧羰基或c2-c4烯基或c2-c4炔基或n,n-二(c1-c4烷基)或n,n-二
(芳基)或苯基或c2-c4烯基或c2-c4炔基或苯基;
[0014]
所述r3为c2-c4烯基或c2-c4炔基或苯基时能够被一个或多个r4取代,r4为苯基。
[0015]
进一步地,
[0016]
所述x为氯或溴;
[0017]
所述ar1为苯基或萘基或蒽基或吡啶基;
[0018]
所述ar2为苯基或萘基或蒽基或吡啶基;
[0019]
所述r1和r2能够是相同或不同的基团,所述r1和r2正丁基或叔丁基或异丙基或金刚烷基或苯基或萘基或环己基;
[0020]
所述r3为甲基或异丙基或叔丁基或氟或氯或三氟甲氧基或三氟甲基或二氟甲醚基或甲氰基或乙氧基羰基或乙烯基或乙炔基或n,n-二苯基或苯基。
[0021]
进一步地,它包括以下步骤:
[0022]
1)将化合物i、钯催化剂、碱溶于有机溶剂一中;
[0023]
2)升至100-140℃下搅拌;
[0024]
3)反应完成后,将反应液冷却至室温除去溶液;
[0025]
4)而后经快速柱层析纯化得到产物ii。
[0026]
进一步地,所述钯催化剂为摩尔分数为5-10%的pd(oac)2或pdcl2或pd(tfa)2或pd(acac)2中的一种或多种;所述碱为cs2co3或k2co3或ch3cook或na2co3或li2co3中的一种或多种;所述有机溶剂一为甲苯或1,4-二氧六环或n,n-二甲基甲酰胺或二甲苯中的一种或多种;
[0027]
进一步地,有机溶剂一与化合物(i)的比值为5-40ml/g。
[0028]
进一步地,所述化合物i与钯催化剂、碱的摩尔比为1:(0.005-0.1):(1-4)。
[0029]
进一步地,当r1和r2不同时,原料i具有手性环境,通过硼烷保护后,经过制备液相分离得到光学纯的原料ia,ia在钯催化下构建分子内c-p键,得到手性保持的产物ii,其合成路线如下,
[0030][0031]
1)在0℃下,将化合物i溶于有机溶剂二中,滴加硼烷络合物溶液,搅拌1-2小时后,将反应混合物用水淬灭,etoac萃取,经色谱纯化,得到手性化合物ia;
[0032]
2)将手性化合物ia、钯催化剂、碱溶于有机溶剂一中,升至100-140℃下搅拌,tlc监测反应完成后,将反应液冷却至室温除去溶液,而后经快速柱层析纯化得到产物ii。
[0033]
所述步骤1)中,硼烷络合物溶液为硼烷二甲硫醚络合物溶液,所述有机溶剂二为无水四氢呋喃;
[0034]
所述步骤2)中,所述钯催化剂为摩尔分数为5-10%的pd(oac)2或pdcl2或pd(tfa)2或pd(acac)2中的一种或多种;碱选自cs2co3或k2co3或ch3cook或na2co3或li2co3中的一种或
多种;所述有机溶剂一为甲苯或1,4-二氧六环或n,n-二甲基甲酰胺或二甲苯中的一种或多种;所述有机溶剂一与化合物(ia)的比值为5-40ml/g。
[0035]
所述步骤1)中,化合物i与硼烷络合物的摩尔比为1:(2-4);所述步骤2)中,所述化合物ia与钯催化剂、碱的摩尔比为1:(0.005-0.1):(1-4)。
[0036]
有益效果
[0037]
本发明提出的一种含有五价磷中心的氮磷杂环化合物的合成方法,在钯催化下构建分子内c-p键,一步合环,合成含五价磷中心的氮磷杂环化合物。该方法采用联苯型磷胺类化合物为原料,可避免竞争性buchwald-hartwig胺化;其次,p(iii)官能团在反应过程中可被氧化为p(v),简化了反应步骤;再次,反应所用钯催化剂、碱及溶剂均实现了工业化生产,市售易得,降低了制备方法的重复难度;更为重要的是,本技术所述制备方法中,可获得手性保持的氮磷杂环化合物,降低了生产成本的同时,更易得到高价值产物。整个合成过程操作简便、反应条件温和,基团耐受性强,具有高通用性。
附图说明
[0038]
附图1是本发明实施例一和实施例二中化合物ii-1b的核磁氢谱图。
[0039]
附图2是本发明实施例一和实施例二中化合物ii-1b的核磁碳谱图。
[0040]
附图3是本发明实施例一和实施例二中化合物ii-1b的核磁磷谱图。
[0041]
附图4是本发明实施例三中化合物ii-2b的核磁氢谱图。
[0042]
附图5是本发明实施例三中化合物ii-2b的核磁碳谱图。
[0043]
附图6是本发明实施例三中化合物ii-2b的核磁磷谱图。
[0044]
附图7是本发明实施例四中化合物ii-3b的核磁氢谱图。
[0045]
附图8是本发明实施例四中化合物ii-3b的核磁碳谱图。
[0046]
附图9是本发明实施例四中化合物ii-3b的核磁磷谱图。
[0047]
附图10是本发明实施例五中化合物ii-4b的核磁氢谱图。
[0048]
附图11是本发明实施例五中化合物ii-4b的核磁碳谱图。
[0049]
附图12是本发明实施例五中化合物ii-4b的核磁磷谱图。
[0050]
附图13是本发明实施例六中化合物ii-5b的核磁氢谱图。
[0051]
附图14是本发明实施例六中化合物ii-5b的核磁碳谱图。
[0052]
附图15是本发明实施例六中化合物ii-5b的核磁磷谱图。
[0053]
附图16是本发明实施例七中化合物ii-6b的核磁氢谱图。
[0054]
附图17是本发明实施例七中化合物ii-6b的核磁碳谱图。
[0055]
附图18是本发明实施例七中化合物ii-6b的核磁磷谱图。
[0056]
附图19是本发明实施例八中化合物ii-7b的核磁氢谱图。
[0057]
附图20是本发明实施例八中化合物ii-7b的核磁碳谱图。
[0058]
附图21是本发明实施例八中化合物ii-7b的核磁磷谱图。
[0059]
附图22是本发明实施例九中化合物ii-8b的核磁氢谱图。
[0060]
附图23是本发明实施例九中化合物ii-8b的核磁碳谱图。
[0061]
附图24是本发明实施例九中是化合物ii-8b的核磁磷谱图。
[0062]
附图25是本发明实施例十中化合物ii-9b的核磁氢谱图。
[0063]
附图26是本发明实施例十中化合物ii-9b的核磁碳谱图。
[0064]
附图27是本发明实施例十中化合物ii-9b的核磁磷谱图。
[0065]
附图28是本发明实施例十一中化合物ii-10b的核磁氢谱图。
[0066]
附图29是本发明实施例十一中化合物ii-10b的核磁碳谱图。
[0067]
附图30是本发明实施例十一中化合物ii-10b的核磁磷谱图。
[0068]
附图31是本发明实施例十二中化合物ii-11b的核磁氢谱图。
[0069]
附图32是本发明实施例十二中化合物ii-11b的核磁碳谱图。
[0070]
附图33是本发明实施例十二中化合物ii-11b的核磁磷谱图。
[0071]
附图34是本发明实施例十三中化合物ii-12b的核磁氢谱图。
[0072]
附图35是本发明实施例十三中化合物ii-12b的核磁碳谱图。
[0073]
附图36是本发明实施例十三中化合物ii-12b的核磁磷谱图。
[0074]
附图37是本发明实施例十四中化合物ii-13b的核磁氢谱图。
[0075]
附图38是本发明实施例十四中化合物ii-13b的核磁碳谱图。
[0076]
附图39是本发明实施例十四中化合物ii-13b的核磁磷谱图。
[0077]
附图40是本发明实施例十五中化合物ii-14b的核磁氢谱图。
[0078]
附图41是本发明实施例十五中化合物ii-14b的核磁碳谱图。
[0079]
附图42是本发明实施例十五中化合物ii-14b的核磁磷谱图。
[0080]
附图43是本发明实施例十六中化合物ii-15b的核磁氢谱图。
[0081]
附图44是本发明实施例十六中化合物ii-15b的核磁碳谱图。
[0082]
附图45是本发明实施例十六中化合物ii-15b的核磁磷谱图。
[0083]
附图46是本发明实施例十七中化合物ii-16b的核磁氢谱图。
[0084]
附图47是本发明实施例十七中化合物ii-16b的核磁碳谱图。
[0085]
附图48是本发明实施例十七中化合物ii-16b的核磁磷谱图。
[0086]
附图49是本发明实施例十八中化合物ii-17b的核磁氢谱图。
[0087]
附图50是本发明实施例十八中化合物ii-17b的核磁碳谱图。
[0088]
附图51是本发明实施例十八中化合物ii-17b的核磁磷谱图。
[0089]
附图52是本发明实施例十九中化合物ii-18b的核磁氢谱图。
[0090]
附图53是本发明实施例十九中化合物ii-18b的核磁碳谱图。
[0091]
附图54是本发明实施例十九中化合物ii-18b的核磁磷谱图。
[0092]
附图55是本发明实施例二十中化合物ii-19b的核磁磷谱图。
[0093]
附图56是本发明实施例二十中化合物ii-19b的核磁氢谱图。
[0094]
附图57是本发明实施例二十中化合物ii-19b的核磁碳谱图。
具体实施方式
[0095]
为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例的附图,对本发明实施例的技术方案进行清楚、完整地描述。显然,所描述的实施例是本发明的一部分实施例,而不是全部的实施例。基于所描述的本发明的实施例,本领域普通技术人员在无需创造性劳动的前提下所获得的所有其他实施例,都属于本发明保护的范围。除非另作定义,此处使用的技术术语或者科学术语应当为本发明所属领域内具有一般技能的
人士所理解的通常意义。
[0096]
一种含有五价磷中心的氮磷杂环的合成方法,所述含有五价磷中心的氮磷杂环的制备方法中,包括通式(i)及通式(ii)的化合物,其合成路线如下
[0097][0098]
它包含以下步骤:
[0099]
将化合物i、钯催化剂、碱溶于有机溶剂一中,升至100-140℃下搅拌,tlc监测反应完成后,将反应液冷却至室温除去溶液,而后经快速柱层析纯化得到产物ii。
[0100]
其中,化合物i的制备路线如下:
[0101][0102]
将化合物st-1、化合物st-2、钯催化剂和碱溶于有机溶剂三中,室温下搅拌5-10分钟。加入h2o,并于氩气气氛中,120℃下搅拌2-8h。冷却至室温后,用乙酸乙酯萃取,无水硫酸钠干燥并过滤,减压下脱溶,柱层析纯化得到化合物s-1。
[0103]
在0℃下,将s-1溶于无水四氢呋喃中,逐滴加入正丁基锂。搅拌(0.5-2)h小时后,滴加r2r1pcl。搅拌混合物,并在48小时内升至室温。tlc监测反应完成后,用甲醇淬灭。然后减压脱溶,柱层析纯化得到化合物s-1。
[0104]
所述步骤1)中,有机溶剂三选自甲苯或1,4-二氧六环或四氢呋喃或n,n-二甲基甲酰胺中的一种或多种;碱选自碳酸钠或碳酸钾或碳酸铯或乙酸钾或碳酸锂中的一种或多种;
[0105]
当r1,r2不同时,ia在钯催化下构建分子内c-p键,得到手性保持的产物ii,合成路线如下,包含以下步骤:
[0106][0107]
1)在0℃下,将i溶于有机溶剂二中,滴加硼烷络合物溶液。搅拌1-2小时后,将反应混合物用水淬灭,etoac萃取,经色谱纯化,得到ia。手性产物ia经lc分离获得。
[0108]
2)将化合物ia、钯催化剂、碱溶于有机溶剂一中,升至100-140℃下搅拌,tlc监测
反应完成后,将反应液冷却至室温除去溶液,而后经快速柱层析纯化得到产物ii。
[0109]
下面结合具体的基团对本合成方法进行说明。
[0110]
实施例一
[0111]
6,6-二-叔丁基-6λ
5-二苯并[c,e][1,2]氮杂膦的制备(ii-1b),包括以下几个步骤:
[0112]
步骤一
[0113][0114]
将2-碘苯胺(6mmol)、2-氯苯基硼酸(7.2mmol,1.2equiv)、pd(pph3)4(346mg,0.30mmol)和nahco3(1.51g,18mmol)溶于dme(1,2-二甲氧基乙烷)(14ml)在室温下搅拌5分钟。加入h2o(14ml),并在氩气气氛下在120℃搅拌2-8小时。冷却至室温后,混合物用etoac萃取。合并萃取液,用na2so4干燥并过滤。减压脱溶,柱层析纯化制得的2'-氯-[1,1'-联苯]-2-胺(s-1-a)。
[0115]
步骤二
[0116][0117]
在0℃下,将2'-氯-[1,1'-联苯]-2-胺s-1-1a(2mmol)溶于7ml无水thf的溶液中,逐滴加入正丁基锂(2.4mmol,2.5m inhexane)。搅拌0.5小时后,滴加t-bu2pcl(2.2mmol)。搅拌混合物并在48小时内升至室温。通过tlc测定苯胺消耗后,用2ml meoh淬灭反应。而后减压脱溶,快速柱层析进一步纯化制得1,1-二叔丁基-n-(2'-氯-[1,1'-联苯基]-2-基)膦胺(i-1a)白色固体,收率81%。
[0118]
步骤三
[0119][0120]
干燥的25ml schlenk管中,将化合物i-1a(69.4mg,0.20mmol)、pd(oac)2(4.5mg,0.02mmol)和cs2co3(195.5mg,0.60mmol)溶于干燥dmf(2.0ml)中,升至130℃下搅拌,24小时后,将反应冷却至室温。除去溶液,而后经快速柱层析纯化得到产物6,6-二-叔丁基-6λ5-二苯并[c,e][1,2]氮杂膦ii-1b,为黄色固体,52.2mg,84%产率。
[0121]1h nmr(500mhz,cdcl3)δ8.12(dd,j=7.9,4.0hz,1h),7.78(dd,j=8.1,1.7hz,1h),7.65-7.61(m,1h),7.59-7.55(m,1h),7.32-7.28(m,1h),7.15-7.11(m,1h),7.08-7.07(m,1h),6.63(ddd,j=8.1,6.7,1.5hz,1h),1.33(s,9h),1.30(s,9h).
[0122]
13
c nmr(126mhz,cdcl3)δ142.4(d,j=3.9hz),131.5(d,j=2.3hz),130.4(d,j=6.4hz),129.8(d,j=4.0hz),125.4(d,j=23.1hz),124.8(d,j=9.2hz),124.2,123.7(d,j=6.9hz),119.1(d,j=17.3hz),114.9,112.8(d,j=59.0hz),39.0(d,j=61.3hz),26.8.
[0123]
31
p nmr(202mhz,cdcl3)δ31.5.
[0124]
atr-ftir(cm-1
):3727,2361,2340,1276,1261,751,670,425.
[0125]
hrms(esi)m/z calcd for c
20h27
np(m+h)
+
:312.1876,found 312.1871.
[0126]
实施例二
[0127]
6,6-二-叔丁基-6λ
5-二苯并[c,e][1,2]氮杂膦(ii-1b)的制备,包括以下几个步骤:
[0128]
步骤一:2'-氯-[1,1'-联苯]-2-胺(s-1-a)的制备参照实施例一制备
[0129]
步骤二:1,1-二叔丁基-n-(2'-氯-[1,1'-联苯基]-2-基)膦胺(i-1a)参照实施例一制备
[0130]
步骤三:6,6-二-叔丁基-6λ
5-二苯并[c,e][1,2]氮杂膦(ii-1b)的制备(3mmol i-1a)
[0131][0132]
干燥的100ml schlenk管中,将化合物i-1a(1.04g,3.0mmol)、pd(oac)2(67.2mg,0.3mmol)和cs2co3(2.93g,9.0mmol)溶于干燥dmf(30ml)中,升至130℃下搅拌,24小时后,将反应冷却至室温。除去溶液,而后经快速柱层析纯化得到产物6,6-二-叔丁基-6λ5-二苯并[c,e][1,2]氮杂膦iib,为黄色固体,899mg,96%产率。
[0133]1h nmr(500mhz,cdcl3)δ8.12(dd,j=7.9,4.0hz,1h),7.78(dd,j=8.1,1.7hz,1h),7.65-7.61(m,1h),7.59-7.55(m,1h),7.32-7.28(m,1h),7.15-7.11(m,1h),7.08-7.07(m,1h),6.63(ddd,j=8.1,6.7,1.5hz,1h),1.33(s,9h),1.30(s,9h).
[0134]
13
c nmr(126mhz,cdcl3)δ142.4(d,j=3.9hz),131.5(d,j=2.3hz),130.4(d,j=6.4hz),129.8(d,j=4.0hz),125.4(d,j=23.1hz),124.8(d,j=9.2hz),124.2,123.7(d,j=6.9hz),119.1(d,j=17.3hz),114.9,112.8(d,j=59.0hz),39.0(d,j=61.3hz),26.8.
[0135]
31
p nmr(202mhz,cdcl3)δ31.5.
[0136]
atr-ftir(cm-1
):3727,2361,2340,1276,1261,751,670,425.
[0137]
hrms(esi)m/z calcd for c
20h27
np(m+h)
+
:312.1876,found 312.1871.
[0138]
实施例三
[0139]
6,6-二叔丁基-2-异丙基-6λ
5-二苯并[c,e][1,2]氮杂膦(ii-2b)的制备。
[0140][0141]
ii-2b参照实施例一制备,合环收率88%。
[0142]1h nmr(400mhz,cdcl3)δ8.16(dd,j=7.7,4.0hz,1h),7.65
–
7.61(m,2h),7.59
–
7.55(m,1h),7.31
–
7.27(m,1h),7.04(s,2h),2.86(p,j=7.0hz,1h),1.31(d,j=14.3hz,18h),1.27(d,j=7.0hz,6h).
[0143]
13
c nmr(101mhz,cdcl3)δ151.7,142.6(d,j=4.1hz),134.8,131.3(d,j=2.3hz),130.4(d,j=5.9hz),128.1(d,j=4.1hz),125.1(d,j=22.7hz),124.6(d,j=9.1hz),123.5(d,j=6.8hz),121.7,118.3(d,j=17.3hz),112.8(d,j=59.0hz),39.0(d,j=61.8hz),33.4,26.8,24.3.
[0144]
31
p nmr(162mhz,cdcl3)δ31.6.
[0145]
atr-ftir(cm-1
):3728,2361,2340,1276,1261,751,670.
[0146]
hrms(esi)m/z calcd for c
23h33
np(m+h)
+
:354.2345,found 354.2342.
[0147]
实施例四
[0148]
6,6-二叔丁基-9-甲氧基-6λ
5-二苯并[c,e][1,2]氮杂膦(11-3b)
[0149][0150]
ii-3b参照实施例一制备,合环收率72%。
[0151]1h nmr(500mhz,cdcl3)δ7.73(d,j=8.2hz,1h),7.59
–
7.54(m,2h),7.12(d,j=5.3hz,2h),6.91
–
6.88(m,1h),6.64
–
6.61(m,1h),3.92(s,3h),1.32(s,9h),1.29(s,9h).
[0152]
13
c nmr(126mhz,cdcl3)δ161.9(d,j=2.3hz),144.4(d,j=4.6hz),132.0(d,j=7.5hz),129.9(d,j=4.0hz),125.3(d,j=22.5hz),124.2,118.9(d,j=16.8hz),114.9,112.4(d,j=9.8hz),107.4(d,j=7.5hz),55.1,38.9(d,j=61.3hz),26.7.
[0153]
31
p nmr(202mhz,cdcl3)δ32.2.
[0154]
atr-ftir(cm-1
):2361,2340,1276,1261,750.
[0155]
hrms(esi)m/z calcd for c
21h29
nop(m+h)
+
:342.1981,found 342.1978.
[0156]
实施例五
[0157]
6,6-二叔丁基-2-氟-6λ
5-二苯并[c,e][1,2]氮杂膦(11-4b)
[0158][0159]
ii-4b参照实施例一制备,合环收率90%。
[0160]1h nmr(500mhz,cdcl3)δ7.98(dd,j=8.1,4.1hz,1h),7.64(td,j=8.9,8.4,1.5hz,1h),7.59
–
7.56(m,1h),7.44(dd,j=11.3,3.1hz,1h),7.35
–
7.31(m,1h),6.97(dd,j=8.9,5.7hz,1h),6.88
–
6.84(m,1h),1.31(s,9h),1.28(s,9h).
[0161]
13
c nmr(126mhz,cdcl3)δ154.2(d,j=230.0hz),150.1,141.6,131.6(d,j=1.7hz),130.4(d,j=5.8hz),129.9(d,j=262.4hz),126.0(dd,j=23.4,7.2hz),125.4(d,j=9.2hz),123.8(d,j=6.9hz),116.9(dd,j=22.3,3.8hz),113.1(d,j=58.4hz),109.5(d,j=23.1hz),39.1(d,j=61.3hz),26.7.
[0162]
31
p nmr(202mhz,cdcl3)δ32.0.
[0163]
19
f nmr(471mhz,cdcl3)δ-130.5.
[0164]
atr-ftir(cm-1
):2361,2340,1276,1261,750,670,446.
[0165]
hrms(esi)m/z calcd for c
20h26
fnp(m+h)
+
:330.1781,found 330.1779.
[0166]
实施例六
[0167]
5,5-二叔丁基-9,9-二氟-5λ
5-[1,3]二氧杂环[4',5':4,5]苯并[1,2-e]苯并[c][1,2]氮杂膦(ii-5b)
[0168][0169]
ii-5b参照实施例一制备,合环收率91%。
[0170]1h nmr(500mhz,cdcl3)δ7.88(dd,j=8.3,4.1hz,1h),7.62
–
7.59(m,1h),7.57
–
7.54(m,1h),7.39(s,1h),7.31
–
7.27(m,1h),6.72(s,1h),1.30(s,9h),1.27(s,9h).
[0171]
13
c nmr(126mhz,cdcl3)δ152.0,145.4(d,j=6.9hz),141.9(d,j=4.0hz),134.4(d,j=186.7hz),131.7(d,j=1.7hz),131.7,130.5(d,j=5.8hz),124.8(d,j=9.2hz),123.3(d,j=6.9hz),113.5(d,j=17.3hz),111.7(d,j=59.5hz),105.5(d,j=24.9hz),104.0,39.1(d,j=61.8hz),26.6.
[0172]
31
p nmr(202mhz,cdcl3)δ32.1.
[0173]
19
f nmr(471mhz,cdcl3)δ-51.53.
[0174]
atr-ftir(cm-1
):2361,2340,1276,1261,750,670,428.
[0175]
hrms(esi)m/z calcd for c
20h25
f2no2p(m+h)
+
:392.1585,found 392.1581.
[0176]
实施例七
[0177]
6,6-二叔丁基-8-(三氟甲基)-6λ
5-二苯并[c,e][1,2]氮杂膦(ii-6b)
[0178][0179]
ii-6b参照实施例一制备,合环收率89%。
[0180]1h nmr(500mhz,cdcl3)δ8.30
–
8.22(m,1h),7.89
–
7.79(m,3h),7.30
–
7.09(m,2h),6.70
–
6.65(m,1h),1.34(d,j=14.8hz,18h).
[0181]
13
c nmr(101mhz,cdcl3)δ154.8,145.7,130.9,127.7,127.2(d,j=4.0hz),126.1(d,j=23.1hz),124.8,123.9(d,j=6.4hz),119.3(q,j=291.1hz),117.9(d,j=17.3hz),115.2,112.7(d,j=56.6hz),108.5(d,j=4.6hz),39.1(d,j=61.8hz),26.6.
[0182]
31
p nmr(202mhz,cdcl3)δ31.5.
[0183]
19
f nmr(471mhz,cdcl3)δ-62.5.
[0184]
atr-ftir(cm-1
):2361,2340,1276,1261,750,670.
[0185]
hrms(esi)m/z calcd for c
21h26
f3np(m+h)
+
:380.1749,found 380.1745.
[0186]
实施例八
[0187]
(e)-6,6-二叔丁基-2-苯乙烯基-6λ
5-二苯并[c,e][1,2]氮杂膦(ii-7b)
[0188][0189]
ii-7b参照实施例一制备,合环收率85%。
[0190]1h nmr(500mhz,cdcl3)δ8.22(dd,j=8.0,3.6hz,1h),7.93(d,j=2.2hz,1h),7.67
–
7.60(m,2h),7.52
–
7.50(m,2h),7.45
–
7.42(m,1h),7.37
–
7.33(m,3h),7.22
–
7.18(m,1h),7.16
–
7.08(m,2h),6.94(d,j=16.3hz,1h),1.35(s,9h),1.31(s,9h).
[0191]
13
c nmr(126mhz,cdcl3)δ154.6,142.1(d,j=4.1hz),138.5,131.6(d,j=2.3hz),130.4(d,j=5.9hz),129.7,128.5,127.5(d,j=4.1hz),126.2,126.0,125.8,125.0(d,j=9.1hz),124.1,123.7,123.6(d,j=6.8hz),123.0,118.6(d,j=17.7hz),112.7(d,j=58.6hz),38.9(d,j=61.3hz),26.7.
[0192]
31
p nmr(202mhz,cdcl3)δ32.0.
[0193]
atr-ftir(cm-1
):3728,2361,2340,1276,1261,750,670,448,426.
[0194]
hrms(esi)m/z calcd for c
28h33
np(m+h)
+
:414.2345,found 414.2340.
[0195]
实施例九
[0196]
6,6-二叔丁基-2-(苯基乙炔基)-6λ
5-二苯并[c,e][1,2]氮杂膦(ii-8b)
[0197][0198]
ii-8b参照实施例一制备,合环收率89%。
[0199]1h nmr(400mhz,cdcl3)δ8.12(dd,j=8.3,4.0hz,1h),8.00(d,j=2.1hz,1h),7.62
–
7.54(m,2h),7.52
–
7.49(m,2h),7.33
–
7.23(m,5h),7.00(d,j=8.5hz,1h),1.30(s,9h),1.26(s,9h).
[0200]
13
c nmr(101mhz,cdcl3)δ141.5(d,j=4.1hz),132.8(d,j=3.6hz),131.7(d,j=1.8hz),131.1,130.3(d,j=5.9hz),128.3,128.1,127.1,125.6,125.4,125.3(d,j=9.5hz),124.4,123.7(d,j=6.8hz),118.9(d,j=17.7hz),112.6(d,j=58.6hz),108.2,91.6,86.6,38.8(d,j=61.3hz),26.6.
[0201]
31
p nmr(162mhz,cdcl3)δ32.2.
[0202]
atr-ftir(cm-1
):2361,2340,1276,1261,750,670.
[0203]
hrms(esi)m/z calcd for c
28h31
np(m+h)
+
:412.2189,found 412.2184.
[0204]
实施例十
[0205]
4-(6,6-二叔丁基-6λ
5-二苯并[c,e][1,2]氮杂膦-2-基)-n,n-二苯基苯胺(ii-9b)
[0206][0207]
ii-9b参照实施例一制备,合环收率69%。
[0208]1h nmr(500mhz,cdcl3)δ8.22(dd,j=8.5,4.0hz,1h),8.01(d,j=2.3hz,1h),7.65(t,j=8.4hz,1h),7.60(t,j=8.0hz,1h),7.49(d,j=8.6hz,2h),7.40(d,j=8.5hz,1h),7.33(t,j=8.0hz,1h),7.24(t,j=7.9hz,4h),7.12(d,j=8.4hz,7h),6.99(t,j=7.3hz,2h),1.34(d,j=14.5hz,18h).
[0209]
13
c nmr(126mhz,cdcl3)δ162.5,147.9,145.5,142.1,136.6,131.8,130.5(d,j=
6.4hz),129.9,129.3,129.1,128.9,128.5,126.8,125.1,124.7,124.1,123.8,122.5,122.4,118.9(d,j=17.9hz),39.1(d,j=60.1hz),26.8.
[0210]
31
p nmr(202mhz,cdcl3)δ31.9.
[0211]
atr-ftir(cm-1
):3728,2361,2340,1276,1261,750,670.
[0212]
hrms(esi)m/z calcd for c
38h40
n2p(m+h)
+
:555.2924,found 555.2922.
[0213]
实施例十一
[0214]
7,7-二叔丁基-7λ
5-二萘并[2,3-c:2',3'-e][1,2]氮杂膦(ii-10b)
[0215][0216]
ii-10b参照实施例一制备,合环收率76%。
[0217]1h nmr(500mhz,cdcl3)δ8.80(d,j=3.7hz,1h),8.45(s,1h),8.24(d,j=10.1hz,1h),8.03(d,j=8.2hz,1h),7.91(d,j=7.9hz,1h),7.75(d,j=7.8hz,1h),7.64
–
7.61(m,1h),7.57
–
7.53(m,2h),7.42(s,1h),7.29
–
7.26(m,1h),7.12
–
7.09(m,1h),1.41(s,9h),1.38(s,9h).
[0218]
13
c nmr(126mhz,cdcl3)δ137.6,136.1(d,j=3.5hz),134.9(d,j=1.7hz),131.1(d,j=5.8hz),130.9(d,j=3.5hz),130.6(d,j=10.4hz),128.8(d,j=4.6hz),128.4,128.09,128.06,126.6,126.5,125.98,124.9,124.4,123.6(d,j=6.9hz),120.9,118.1,117.9,116.9(d,j=59.0hz),38.9(d,j=61.8hz),27.1.
[0219]
31
p nmr(202mhz,cdcl3)δ28.6.
[0220]
atr-ftir(cm-1
):2361,2340,1276,1261,750,670.
[0221]
hrms(esi)m/z calcd for c
28h31
np(m+h)
+
:412.2189,found 412.2184.
[0222]
实施例十二
[0223]
4,4-二叔丁基-4λ
5-二萘并[2,1-c:1',2'-e][1,2]氮杂膦(ii-11b)
[0224][0225]
ii-11b参照实施例一制备,合环收率80%。
[0226]1h nmr(400mhz,cdcl3)δ8.87(ddd,j=8.3,3.6,1.7hz,1h),7.91(dd,j=4.2,1.7hz,1h),7.65
–
7.56(m,2h),7.40
–
7.35(m,1h),7.29
–
7.26(m,1h),7.01(ddd,j=8.3,4.2,2.0hz,1h),1.32(s,9h),1.28(s,9h).
[0227]
13
c nmr(101mhz,cdcl3)δ149.8,142.7(d,j=3.2hz),137.4(d,j=18.6hz),135.9,131.6(d,j=2.3hz),131.4(d,j=23.2hz),129.7(d,j=5.4hz),126.5(d,j=9.5hz),125.4(d,j=6.8hz),124.5(d,j=4.1hz),113.8(d,j=56.8hz),38.9(d,j=61.8hz),26.7.
[0228]
31
p nmr(162mhz,cdcl3)δ31.5.
[0229]
atr-ftir(cm-1
):2361,2340,1276,1261,750,670,432.
[0230]
hrms(esi)m/z calcd for c
19h26
n2p(m+h)
+
:313.1828,found 313.1824.
[0231]
实施例十三
[0232]
6-((3r,5r,7r)-金刚烷-1-基)-6-((3s,5s,7s)-金刚烷-1-基)-6λ
5-二苯并[c,e][1,2]-氮杂膦(ii-12b)
[0233][0234]
ii-12b参照实施例一制备,合环收率70%。
[0235]1h nmr(400mhz,cdcl3)δ8.13(dd,j=8.4,3.9hz,1h),7.77(dd,j=8.1,1.5hz,1h),7.58(dt,j=15.2,8.1hz,2h),7.30(d,j=7.2hz,1h),7.09(dd,j=20.8,7.1hz,2h),6.59(t,j=7.4hz,1h),2.09
–
2.08(m,12h),1.96(d,j=2.9hz,6h),1.68(s,12h).
[0236]
13
c nmr(101mhz,cdcl3)δ142.8,131.3,130.7(d,j=5.4hz),129.6(d,j=4.4hz),125.8,125.6,124.5(d,j=8.6hz),124.2,123.5(d,j=6.0hz),114.4,43.2(d,j=62.2hz),36.7(d,j=2.3hz),36.4,27.8(d,j=9.5hz).
[0237]
31
p nmr(162mhz,cdcl3)δ21.8.
[0238]
atr-ftir(cm-1
):2361,2340,1276,1261,751.
[0239]
hrms(esi)m/z calcd for c
32h39
np(m+h)
+
:468.2815,found 468.2812.
[0240]
实施例十四
[0241]
6,6-二(萘e-1-基)-6λ
5-二苯并[c,e][1,2]氮杂膦(ii-13b)
[0242][0243]
ii-13b参照实施例一制备,合环收率85%。
[0244]1h nmr(400mhz,cdcl3)δ8.86(s,2h),8.20(dd,j=8.1,4.8hz,1h),8.00(d,j=8.4hz,2h),7.95(dd,j=8.1,1.7hz,1h),7.89(d,j=8.2hz,2h),7.66
–
7.63(m,1h),7.49
(ddd,j=8.2,6.9,1.3hz,2h),7.42(ddd,j=16.9,7.2,1.4hz,4h),7.33(td,j=7.6,2.7hz,2h),7.26
–
7.15(m,3h),7.09(ddd,j=11.9,7.6,1.6hz,1h),6.78(ddd,j=8.2,6.6,1.8hz,1h).
[0245]
13
c nmr(101mhz,cdcl3)δ151.2,141.0,134.8,134.3,134.2,133.7,132.1(d,j=2.3hz),130.1,130.0,130.0,128.8,127.8,127.3,126.8,126.6,126.5,126.2(d,j=10.9hz),124.6(d,j=3.2hz),124.5,124.3,124.2,121.6(d,j=22.7hz),116.8,114.8,114.0.
[0246]
31
p nmr(162mhz,cdcl3)δ16.1.
[0247]
atr-ftir(cm-1
):2361,2340,1276,1261,750,671.
[0248]
hrms(esi)m/z calcd for c
32h23
np(m+h)
+
:452.1563,found 452.1560.
[0249]
实施例十五
[0250]
(r)-6-(叔丁基)-6-苯基-6λ
5-二苯并[c,e][1,2]氮杂膦(ii-14b)的制备包括以下几个步骤:
[0251]
步骤一
[0252][0253]
参照实施例一进行制备。
[0254]
步骤二
[0255][0256]
在0℃下,向2'-氯-[1,1'-联苯]-2-胺s-1-1a(2mmol)溶于7ml无水thf的溶液中,逐滴加入正丁基锂(2.4mmol,2.5m in hexane)。搅拌0.5小时后,滴加氯(叔丁基)苯膦(2.2mmol)。搅拌混合物并在48小时内升至室温。通过tlc测定苯胺消耗后,用2ml meoh淬灭反应。而后减压脱溶,快速柱层析进一步纯化制得1,1-二叔丁基-n-(2'-氯-[1,1'-联苯基]-2-基)膦胺(i-14a)。在0℃下,向i-14a(1mmol)溶于1ml无水thf的溶液中,滴加硼烷二甲硫醚络合物(2mmol)溶液。搅拌0.5小时后,将反应混合物在0℃下用水淬灭,并用etoac萃取,混合物经色谱纯化,得到373mg ia-14白色固体,收率98%。手性产物ia-14(》99%ee)通过lc分离获得,条件:己烷/异丙醇=99.5:0.5,流速=0.5ml/min,紫外可见光检测在λ=220nm,t
r1
=13.2min(次要),t
r2
=16.1min(主要)。
[0257]1h nmr(400mhz,cdcl3)δ7.78
–
7.57(m,3h),7.51
–
7.39(m,6h),7.13(ddt,j=6.8,5.5,1.8hz,2h),6.98
–
6.91(m,2h),4.07(s,1h),0.96(d,j=14.1hz,3h),0.90(d,j=14.1hz,6h).
[0258]
13
c nmr(101mhz,cdcl3)δ138.1(d,j=151.2hz),133.8,132.6,132.3(d,j=10.0hz),131.8,131.3(dd,j=11.8,2.7hz),130.0(d,j=33.2hz),129.7,129.6,129.6,
128.9,128.9,128.4
–
127.6(m),127.4,120.9(d,j=10.4hz),118.5(dd,j=11.1,3.4hz),30.7(dd,j=40.2,25.7hz),24.3(dd,j=7.0,3.0hz).
[0259]
31
p nmr(162mhz,cdcl3)δ68.8(d,j=75.3hz).
[0260]
11
b nmr(128mhz,cdcl3)δ-41.0.
[0261]
atr-ftir(cm-1
):2361,2340,1276,1261,750.
[0262]
hrms(esi)m/z calcd for c
22h27
bclnp(m+h)
+
382.1657,found 382.1652.
[0263]
[α]
d25
=50.0(c=0.02,chcl3).
[0264]
步骤三
[0265][0266]
干燥的25ml schlenk管中,将化合物ia-14(38.1mg,0.10mmol,》99%ee)、pd(oac)2(2.2mg,0.01mmol)和cs2co3(97.7mg,0.60mmol)溶于干燥dmf(1.0ml)中,升至130℃下搅拌,24小时后,将反应冷却至室温。除去溶液,而后经快速柱层析纯化得到28.2mg黄色固体6-(叔丁基)-6-苯基-6λ
5-二苯并[c,e][1,2]氮杂膦ii-14b,收率79%,手性纯度99%ee。
[0267]1h nmr(400mhz,cdcl3)δ8.13
–
8.09(m,1h),7.99
–
7.94(m,2h),7.84
–
7.82(m,1h),7.67(ddd,j=9.5,7.7,1.6hz,1h),7.58(ddt,j=8.4,7.2,1.3hz,1h),7.48
–
7.43(m,3h),7.34(tdd,j=7.5,2.3,1.1hz,1h),7.24
–
7.18(m,2h),6.72(ddd,j=8.2,5.9,2.5hz,1h),1.31(d,j=15.7hz,9h).
[0268]
13
c nmr(101mhz,cdcl3)δ152.8,141.6(d,j=5.0hz),132.4,132.3,131.6(d,j=1.8hz),131.3(d,j=2.7hz),129.9,129.87(d,j=2.7hz),128.4(d,j=11.4hz),126.0(d,j=23.2hz),125.6(d,j=10.0hz),124.4,124.1(d,j=7.7hz),120.6(d,j=19.1hz),115.9,113.8(d,j=69.0hz),36.6(d,j=70.8hz),25.0.
[0269]
31
p nmr(162mhz,cdcl3)δ19.6.
[0270]
atr-ftir(cm-1
):2361,2340,1276,1261,750.
[0271]
hrms(esi)m/z calcd for c
22h23
np(m+h)
+
:332.1563,found 332.1560.
[0272]
[α]
d25
=-21.6(c=0.50,chcl3).
[0273]
实施例十六
[0274]
6-(叔丁基)-2,9-二甲氧基-6-苯基-6λ
5-二苯并[c,e][1,2]氮杂膦(ii-15b)
[0275][0276]
参照实施例十五进行制备,合环收率69%,手性纯度》99%ee。
[0277]1h nmr(400mhz,cdcl3)δ7.94
–
7.89(m,2h),7.61(dd,j=9.4,8.6hz,1h),7.50
–
7.48(m,1h),7.46
–
7.41(m,3h),7.30(d,j=3.1hz,1h),7.16(d,j=8.7hz,1h),6.95
–
6.87(m,2h),3.91(s,3h),3.81(s,3h),1.28(d,j=15.5hz,9h).
[0278]
13
c nmr(101mhz,cdcl3)δ162.0,150.5,143.5,132.3,132.2,131.5(d,j=6.8hz),131.2(d,j=2.7hz),128.4,128.3,126.7,126.4,120.6(d,j=18.2hz),117.2(d,j=3.6hz),113.1(d,j=10.4hz),109.5,108.3(d,j=8.6hz),56.1,55.3,36.4(d,j=71.8hz),25.1.
[0279]
31
p nmr(162mhz,cdcl3)δ20.4.
[0280]
atr-ftir(cm-1
):2361,2340,1276,1261,750.
[0281]
hrms(esi)m/z calcd for c
24h27
no2p(m+h)
+
:392.1774,found 392.1765.
[0282]
[α]
d25
=15.0(c=0.12,chcl3).
[0283]
实施例十七
[0284]
6-环己基-6-苯基-6λ
5-二苯并[c,e][1,2]氮杂膦(ii-16b)
[0285][0286]
(ii-16b)参照实施例十五进行制备,合环收率81%,手性纯度》99%ee。
[0287]1h nmr(400mhz,cdcl3)δ8.10(dd,j=8.3,4.3hz,1h),7.85(dd,j=8.0,1.4hz,1h),7.78(ddd,j=11.2,7.3,2.1hz,2h),7.56(ddt,j=8.4,7.1,1.3hz,1h),7.48
–
7.42(m,4h),7.33(tdd,j=7.6,2.4,1.1hz,1h),7.25
–
7.19(m,2h),6.74(ddd,j=8.2,6.2,2.2hz,1h),2.48
–
2.42(m,1h),1.85
–
1.74(m,3h),1.70
–
1.61(m,3h),1.46(tdd,j=12.6,10.6,6.2hz,1h),1.32
–
1.22(m,3h).
[0288]
13
c nmr(101mhz,cdcl3)δ152.5,141.3(d,j=5.0hz),131.7(d,j=2.3hz),131.6(d,j=2.7hz),131.3(d,j=9.1hz),129.9(d,j=3.6hz),128.8,128.7,128.6,126.1(dd,j=18.2,8.1hz),125.7,124.3,123.8(d,j=7.7hz),119.9(d,j=20.0hz),119.7(d,j=102.2hz),116.2,113.8(d,j=72.7hz),110.6,37.9(d,j=75.8hz),29.7,26.3(dd,j=13.6,3.2hz),25.6(d,j=1.8hz),25.3(d,j=2.7hz),24.0(d,j=3.2hz).
[0289]
31
p nmr(162mhz,cdcl3)δ16.8.
[0290]
atr-ftir(cm-1
):2361,2340,1276,1261,750.
[0291]
hrms(esi)m/z calcd for c
24h25
np(m+h)
+
:358.1719,found 358.1712.
[0292]
[α]
d25
=-28.0(c=0.10,chcl3).
[0293]
实施例十八
[0294]
6-环戊基-6-苯基-6λ
5-二苯并[c,e][1,2]氮杂膦(ii-17b)
[0295][0296]
参照实施例十五进行制备,合环收率77%,手性纯度》99%ee。
[0297]1h nmr(400mhz,cdcl3)δ8.10(dd,j=8.3,4.3hz,1h),7.88
–
7.86(m,1h),7.84
–
7.78(m,2h),7.55(ddt,j=8.4,7.1,1.3hz,1h),7.51
–
7.42(m,3h),7.39(ddd,j=11.0,7.7,1.7hz,1h),7.32
–
7.27(m,1h),7.24
–
7.19(m,2h),6.78
–
6.72(m,1h),2.95(pd,j=8.7,4.9hz,1h),2.12
–
2.00(m,1h),1.89
–
1.52(m,7h).
[0298]
13
c nmr(101mhz,cdcl3)δ152.7,140.8(d,j=5.5hz),132.8(d,j=99.9hz),131.7,131.7(d,j=5.0hz),131.4(d,j=9.1hz),129.9(d,j=4.1hz),128.9(d,j=6.8hz),128.7(d,j=11.8hz),126.2(d,j=3.6hz),126.0(d,j=9.5hz),124.3,123.5(d,j=7.7hz),119.8(d,j=19.5hz),116.1,115.4(d,j=73.6hz),38.2(d,j=77.2hz),26.8,26.8(d,j=9.1hz),26.5(d,j=10.0hz),25.8(d,j=1.8hz).
[0299]
31
p nmr(162mhz,cdcl3)δ17.4.
[0300]
atr-ftir(cm-1
):3052,2957,2866,2162,1592,1563,1477,1423,1330,1123,1020,747,532.
[0301]
hrms(esi)m/z calcd for c
23h23
np(m+h)
+
:344.1563,found 344.1557.
[0302]
[α]
d25
=60.0(c=0.15,chcl3).
[0303]
实施例十九
[0304]
5-(叔丁基)-5-苯基-5λ
5-苯并[c]萘并[1,2-e][1,2]氮杂膦(ii-18b)
[0305][0306]
参照实施例十五进行制备,合环收率93%,手性纯度》99%ee。
[0307]1h nmr(500mhz,cdcl3)δ8.28
–
8.24(m,2h),7.87
–
7.83(m,2h),7.76(ddd,j=9.6,7.7,1.6hz,1h),7.70(dd,j=7.9,1.7hz,1h),7.64(dd,j=8.9,2.1hz,1h),7.54(ddt,j=8.4,7.2,1.2hz,1h),7.48(d,j=8.9hz,1h),7.45
–
7.36(m,4h),7.31(ddd,j=8.4,6.8,1.6hz,1h),7.17(ddd,j=7.9,6.7,1.2hz,1h),1.38(d,j=15.6hz,9h).
[0308]
13
c nmr(126mhz,cdcl3)δ152.3(d,j=6.4hz),140.5(d,j=4.6hz),132.6(d,j=8.1hz),131.9,131.6(d,j=2.9hz),130.2(d,j=2.3hz),129.8(d,j=7.5hz),129.7(d,j=3.5hz),128.5(d,j=2.3hz),128.4,128.3,128.2,125.4,125.2(d,j=10.4hz),124.2,121.2,117.2(d,j=20.2hz),115.8(d,j=72.2hz),34.4(d,j=71.7hz),25.2.
[0309]
31
p nmr(202mhz,cdcl3)δ22.3.
[0310]
atr-ftir(cm-1
):2923,2853,1610,1468,1361,1244,1107,1022,821,733.hrms(esi)m/z calcd for c
26h25
np(m+h)
+
:382.1719,found 382.1711.
[0311]
[α]
d25
=42.7(c=0.15,chcl3).
[0312]
实施例二十
[0313]
(s)-6-(叔丁基)-6-(萘-1-基)-6λ
5-二苯并[c,e][1,2]氮杂膦(ii-19b)
[0314][0315]
参照实施例十五进行制备,合环收率77%,手性纯度》99%ee。
[0316]1h nmr(500 mhz,cdcl3)δ9.03
–
9.01(m,1h),8.12
–
8.10(m,1h),7.93
–
7.86(m,2h),7.83(dd,j=8.0,1.8 hz,1h),7.77
–
7.75(m,1h),7.59(dd,j=9.5,7.6 hz,2h),7.42
–
7.40(m,3h),7.32(tdd,j=7.5,2.4,1.1 hz,1h),7.24(dd,j=8.1,1.7hz,1h),7.21
–
7.17(m,1h),6.73(ddd,j=8.2,6.8,1.7 hz,1h),1.49(d,j=15.6hz,9h).
[0317]
13
c nmr(126 mhz,cdcl3)δ152.1,141.5(d,j=5.2 hz),135.1(d,j=7.5 hz),134.3(d,j=8.7 hz),133.3,133.2,133.2,131.5(d,j=2.9 hz),130.0(d,j=3.5 hz),129.4(d,j=5.8 hz),128.5,127.8(d,j=3.5 hz),127.0,126.1,126.0(d,j=22.5hz),125.6(d,j=10.4 hz),124.7(d,j=8.1 hz),124.5,123.4(d,j=13.3 hz),121.9(d,j=20.2 hz),116.5,115.4(d,j=71.7 hz),36.3(d,j=74.0 hz),26.0.
[0318]
31
p nmr(202 mhz,cdcl3)δ24.5.
[0319]
atr-ftir(cm-1
):2361,2340,1276,1261,750.
[0320]
hrms(esi)m/z calcd for c
26h25
np(m+h)
+
:382.1719,found 382.1711.[α]
d25
=4.3(c=0.24,chcl3).
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1