一种抗破伤风单克隆抗体组合物的制备方法及应用与流程
1.本发明涉及生物免疫学技术领域,具体地说是一种抗破伤风单克隆抗体组合物的制备方法及应用。
背景技术:
2.破伤风是由破伤风杆菌入侵创伤而引起的一种特异性感染,其主要致病原是破伤风杆菌产生的破伤风类毒素。破伤风类毒素是一个由1315个氨基酸组成的分子量约为150kda蛋白。该多肽在破伤风杆菌的蛋白水解酶作用后,在456和467氨基酸残基之间裂解成为分量大约为50kd轻链(lc)和100kd重链(ln),lc和ln通过一对二硫键s439-s467连接。lc是锌依赖蛋白酶,在193-197位有一个锌指结合蛋白的功能域helih,375位的酪氨酸是一个催化活性位点。在864和863之间有一个木瓜蛋白酶(papin)切位点可以将重链进一步降解为n端(hcn)和c端(hcc或ttc)。hcn负责突触囊泡通过细胞质进入细胞质的膜,而ttc负责毒素结合神经元细胞。当ttc结合神经元上神经节苷脂受体后,在hcn协助下,lc进入神经元后被运输到神经元胞质,在那里裂解可溶性nsf黏附蛋白(solublensfattachmentprotein(snap)eceptor(snare)proteins),通过水解突触囊泡蛋白ⅱ而阻断神经抑制性介质的释放,阻断了神经元和运动神经元之间的信号传递,从而产生了破伤风特有的痉挛性瘫痪特征。表现为全身骨骼肌持续性强直和阵发性痉挛,重症患者可发生喉痉挛、窒息、肺部感染和器官功能衰竭,是一种极为严重的潜在致命性疾病。
3.目前对破伤风的认识是防重于治。破伤风在当下的预防措施包括注射破伤风类毒素主动免疫,正确处理伤口,以及在伤后采用被动免疫预防发病。最有效的方法是注射破伤风抗毒素(tat)、马破伤风免疫球蛋白f(ab’)2或人破伤风免疫球蛋白(tig)。破伤风抗毒素(tat)和马破伤风免疫球蛋白均是用破伤风类毒素免疫马匹所制得的抗毒素,其形式有所差异的,这两种形式的抗毒素来源于马匹,有一定程度过敏反应,而人破伤风免疫球蛋白(tig)是破伤风类毒素免疫人体所制得的抗毒素,虽然无过敏性但具有较昂贵、来源少、制备复杂、供应不足等等缺点。我国临床上广泛使用的仍为tat,只有在tat过敏试验阳性或者家属主动要求的情况下才会使用tig。因此,人们希望找到一种低过敏性且价格低廉的抗体,可以替代目前的抗体来源。
4.随着杂交瘤单克隆技术和噬菌体展示技术以来,人们逐渐在该领域中使用这些技术进行研究,但是这些研究仍存在的一些问题:
①
有的文章未报到筛选到单克隆抗体或者未测序;
②
筛选到的序列未进行克隆表达,仅做了序列分析;
③
克隆表达的序列仅仅进行了体外ellisa和(或)体外结合实验,未知体内的保护作用;
④
有的序列表达后进行了小鼠体内中和保护实验,但没有或者很弱的协同保护作用。一种常见的思路就是多种单抗混合类似“鸡尾酒”方式,这种思路方案有两种方案,一是分别表达单抗,再混合;一是混合表达单抗。
技术实现要素:
5.本发明为克服现有技术的不足,提供一种抗破伤风单克隆抗体组合物的制备方法及应用,利用破伤风类毒素免疫小鼠,获得了4株具有协同保护作用的单克隆抗体,并进一步对其结合片段的定位。并进行人源化且重组表达后,其协同中和保护作用的效价可达70iu/mg。
6.为实现上述目的,设计一种抗破伤风单克隆抗体组合物,其特征在于:所述的组合物包括:4株单克隆抗体,所述的4株单克隆抗体名称分别为s3a4、9-7a4、9-8c7、s1d2,并且每株克隆抗体分别由轻链及重链组合。
7.所述的s3a4单克隆抗体的轻链核苷酸序列如seq id no:1所示,s3a4单克隆抗体的轻链核苷酸编码蛋白序列如seq id no:2所示;s3a4单克隆抗体的重链核苷酸序列如seq id no:3所示,s3a4单克隆抗体的重链核苷酸编码蛋白序列如seq id no:4所示。
8.所述的s1d2单克隆抗体的轻链核苷酸序列如seq id no:5所示,s1d2单克隆抗体的轻链核苷酸编码蛋白序列如seq id no:6所示;s1d2单克隆抗体的重链核苷酸序列如seq id no:7所示,s1d2单克隆抗体的重链核苷酸编码蛋白序列如seq id no:8所示。
9.所述的9-7a4单克隆抗体的轻链核苷酸序列如seq id no:9所示,9-7a4单克隆抗体的轻链核苷酸编码蛋白序列如seq id no:10所示;9-7a4单克隆抗体的重链核苷酸序列如seq id no:11所示,9-7a4单克隆抗体的重链核苷酸编码蛋白序列如seq id no:12所示。
10.所述的9-8c7单克隆抗体的轻链核苷酸序列如seq id no:13所示,9-8c7单克隆抗体的轻链核苷酸编码蛋白序列如seq id no:14所示;9-8c7单克隆抗体的重链核苷酸序列如seq id no:15所示,9-8c7单克隆抗体的重链核苷酸编码蛋白序列如seq id no:16所示。
11.一种抗破伤风单克隆抗体组合物的制备方法,具体流程如下:
12.s1,第一次免疫:将20ug的抗原与200ul的完全弗氏佐剂混匀,配置成400ul的溶液,注射于小鼠皮下多点;
13.s2,第2~5次免疫:距上次免疫间隔两周后,将20ug的抗原与200ul的不完全弗氏佐剂混匀,配置成400ul溶液,注射于ba1b/c小鼠皮下多点;并在第4次免疫后小鼠尾静脉采血,待血清滴度》105以上;
14.s3,加强免疫:在小鼠尾静脉注射抗原20ug;
15.s4,取免疫小鼠,放血,断颈猝死,在75%的酒精中浸泡3~4min,无菌条件下取出小鼠脾脏,放入15ml的离心管中,加入少许无血清rpm 1640的培养液,用移液管轻轻吹打,碾碎,直至没有组织结块、细胞均匀为止;
16.s5,用无血清rpm 1640的培养液洗涤小鼠脾脏细胞三次;
17.s6,取对数生长期的sp2/0-ag14的小鼠骨髓瘤细胞,在无血清rpm 1640的培养液洗涤三次;
18.s7,将小鼠脾脏细胞和sp2/0-ag14的小鼠骨髓瘤细胞以10:1的比例混合,1500rpm离心7min,洗去上清液;
19.s8,在1min内缓缓加入1m1的peg,轻摇90s,再在2.5min中内加入5ml的无血清rpm 1640的培养液,最后再加入5m1的无血清培液终止反应,静置5min后,1280rpm离心8min,弃去上请,加入常规rpm 1640的培养液(含有10%胎牛血清),制备成细胞悬液;
20.s9,将上述细胞悬液以每孔2x104个细胞的密度种入96孔板,每孔200ul,置于
370c、5%co2细胞培养箱中孵育,培养24h后,更换含有hat(25x)的常规rpm 1640培养液,在370c、5%co2细胞培养箱中继续孵育,培养14d后,稀释倍数小于100倍且其od450大于1者被用于进一步筛选;
21.s10,经筛选,获得4株单克隆抗体,分别命名为s3a4、9-7a4、9-8c7和s1d2,它们的中和效价分别为52iu/ml、53iu/ml、58iu/ml和60iu/ml;
22.s11,用elisa叠加法确定4株单克隆抗体的协同性;
23.s12,从4株单克隆抗体中提取总rna,并获得4株单克隆抗体的可变区编码序列;
24.s13,将4株单克隆抗体中随机抽取2株单克隆抗体,对其轻链核苷酸序列和重链核苷酸序列分别进行人源化操作,获得轻链v区蛋白序列和重链v区蛋白序列;
25.s16,将鼠kappa链的前导肽序列氨基酸序列、人的kappa链恒定区和轻链v区蛋白序列串联、优化后,获得zumb轻链的核苷酸;
26.s17,将鼠kappa链的前导肽序列氨基酸序列、人的igg1恒定区蛋白序列和重链v区蛋白序列串联、优化后,获得zumb重链的核苷酸;
27.s18,将步骤s16及s17获得的zumb轻链的核苷酸和zumb重链的核苷酸进行基因合成,同时亚克隆到载体pcdna3.1(+)中,获得单克隆抗体组合物;
28.s19,将单克隆抗体组合物进行蛋白表达稳定株建立;
29.s20,将蛋白表达稳定株建立后的单克隆抗体组合物进行纯化处理,最终获得安全有效量的抗破伤风单克隆抗体组合物。
30.所述的抗原为宁波荣升公司的破伤风类毒素,批号为501701。
31.所述的人源化操作后的轻链v区蛋白序列为9-7a4-zumb的轻链v区蛋白序列、s3a4-zumb的轻链v区蛋白序列;所述的重链v区蛋白序列为9-7a4-zumb的重链v区蛋白序列、s3a4-zumb的重链v区蛋白序列;所述的9-7a4-zumb的轻链v区蛋白序列如seq id no:20所示,9-7a4-zumb的重链v区蛋白序列如seq id no:21所示;所述的s3a4-zumb的轻链v区蛋白序列如seq id no:22所示,所述的s3a4-zumb的重链v区蛋白序列如seq id no:23所示。
32.所述的人源化操作后的鼠kappa链的前导肽序列氨基酸序列如seq id no:17所示,人的kappa链恒定区如seq id no:18所示,人的igg1恒定区蛋白序列如seq id no:19所示。
33.一种抗破伤风单克隆抗体组合物的应用,其特征在于:
34.(1)预防破伤风的药物中应用;
35.(2)治疗破伤风的药物中应用;
36.(3)在生产破伤风类毒素抗原中,作为诊断试剂在检测产品质量中应用。
37.本发明同现有技术相比,提供一种抗破伤风单克隆抗体组合物的制备方法及应用,利用破伤风类毒素免疫小鼠,获得了4株具有协同保护作用的单克隆抗体,并进一步对其结合片段的定位。并进行人源化且重组表达后,其协同中和保护作用的效价可达70iu/mg。
38.通过小鼠杂交瘤技术获得了4株具有协同性中和作用的鼠单克隆抗体,它们分别非竞争性且特异性地结合hcc端和非hcc端。将其中两株人源化后,在cho-s细胞中重组表达,其表达产物仍具有协同性中和保护作用。本发明提供的针对破伤风毒素的抗体为人源化的单克隆抗体,低免疫原性,且特异性好、亲和力高、效价高,解决了现有技术中破伤风感
染预防和治疗药物的问题。
附图说明
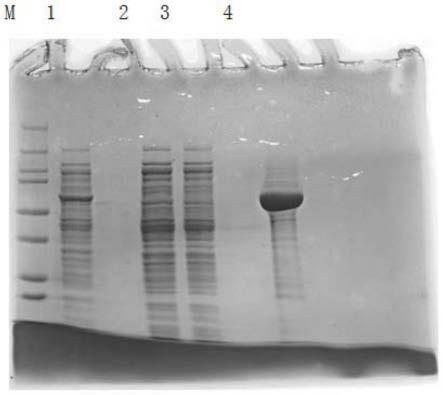
39.图1为破伤风重链c片段大肠杆菌表达图谱。其中,m:蛋白mark;1:破碎上清;2,3:平衡液;4100mm咪唑洗脱。
40.图2为1%琼脂糖电泳检测四株单抗的pcr结果。(a)重链pcr:1:s3a4;2:9-7a4;3:9-8c7;4:s1d2。(b)轻链pcr结果:5:s3a4;6:9-7a4;7:9-8c7;8:s1d2。
41.图3为抗体表达验证。1:9-7a4;2:s3a4;3:s1d2;4:9-8c7m:marker。
42.图4为抗体人源化。1:marker;2:9-7a4;3:s3a4。
具体实施方式
43.下面根据附图对本发明做进一步的说明。
44.1.4株鼠单克隆抗体的获得。
45.1.1免疫程序:
46.以宁波荣升公司的破伤风类毒素(批号:501701)为免疫原。ba1b/c小鼠购自上海生物制品所,所有免疫用ba1b/c小鼠均为3周龄、雌性、标准化无病、健康的纯种小鼠,符合美国fda标准。
47.第一次免疫:将20ug抗原(200ul)与200ul完全弗氏佐剂混匀,配置成400ul溶液,注射于ba1b/c小鼠皮下多点。第2-5次免疫:距上次免疫间隔两周后,20ug抗原(200ul)与200ul不完全弗氏佐剂混匀,配置成400ul溶液,注射于ba1b/c小鼠皮下多点。第4次免疫后小鼠尾静脉采血,采用3.2的酶联免疫吸附实验(elisa法)测定血清抗体滴度,待血清滴度》105以上时,准备做细胞融合。细胞融合前三天进行加强免疫:小鼠尾静脉注射抗原20ug(100ul)。
48.1.2细胞融合:
49.(1)sp2/0-ag14小鼠骨髓瘤细胞购自美国atcc公司。融合前一天换液,使sp2/0-ag14骨髓瘤细胞保持良好生长状态。
50.(2)脾细胞:取免疫小鼠,放血,断颈猝死,于75%酒精浸泡3-4min。无菌条件下取出小鼠脾脏,放入15m1离心管中,加入少许无血清rpm1640培养液,用移液管轻轻吹打,碾碎,直至没有组织结块、细胞均匀为止。然后,用无血清rpm1640培养液洗涤小鼠脾脏细胞三次,计数备用。
51.(3)取对数生长期的sp2/0-ag14骨髓瘤细胞,无血清rpm1640培养液洗涤三次,计数备用。
52.(4)将小鼠脾脏细胞和sp2/0-ag14骨髓瘤细胞以10:1的比例混合,1500rpm离心7min,洗去上清液,准备融合。
53.(5)1min内缓缓加入1m1peg(1450),轻摇90s;再在2.5min中内加入5ml无血清rpm1640培养液,最后再加入5m1无血清培液终止反应,静置5min后,1280rpm离心8min,弃去上请,加入常规rpm1640培养液(含有10%胎牛血清),制备成细胞悬液。
54.(6)将上述细胞悬液以每孔2x104个细胞的密度种入96孔板,每孔200ul,置于370c、5%co2细胞培养箱中孵育。培养24h后,更换含有hat(25x)的常规rpm1640培养液,于
370c、5%co2细胞培养箱中继续孵育。培养14d后,用实施例4.2elisa法检测各个克隆细胞的上清液,稀释倍数小于100倍且其od450大于1者被用于进一步筛选。
55.1.3杂交瘤表达上清中和保护实验:
56.将实施例1.2中杂交瘤上清稀释倍数小于100倍且od450大于1者,参考3.3的方法,测定杂交瘤上清的中和保护作用。
57.结果表明:经筛选,获得4株单克隆抗体,其表达上清如图3所示,分别命名为s3a4、9-7a4、9-8c7和s1d2,它们的中和效价分别为52iu/ml、53iu/ml、58iu/ml和60iu/ml。
58.1.4elisa法定位s3a4、9-7a4、9-8c7和s1d2的结合区域:
59.用elisa法定位四株单抗的结合区域,与3.2的差异在于:
60.a、包被抗原:是1中获得trx-hcc和破伤风类毒素(批号:501701)各1ug/ml。
61.b、一抗的稀释倍数:未稀释、1:10和1:100三个梯度。
62.结果表明:s3a4、9-7a4、9-8c7和s1d2的上清在以1:10稀释液中,均可以和破伤风类毒素结合,od450均大于1,而未稀释的s3a4和s1d2不能结合hcc段,od450为0.2左右。因此,9-7a4和9-8c7特异性结合hcc段,而s3a4和s1d2特异性结合非hcc段。
63.1.5elisa确定协同性:
64.用elisa叠加法鉴定;(1)9-7a4和9-8c7;(2)s3a4和s1d2的结合区域,与实施例4.2的差异在于:
65.a、抗原包被量是0.125ug,以保证加入抗体过量。
66.b、加入一抗:以9-7a4和9-8c7为一组的两孔中,都分别同时加入新鲜1:10稀释的9-7a4和9-8c7抗体0.1ml,s3a4和s1d2的一组中也做类似的处理。
67.结果判断:若9-7a4和9-8c7不存在竞争关系,则od450应为9-7a4单独加入时的1.5倍以上;若9-7a4和9-8c7存在竞争关系,则od450应与9-7a4单独加入时相当,同理也可以判断s3a4和s1d2竞争性关系。
68.结果显示:9-7a4和9-8c7不存在竞争关系。且s3a4和s1d2也不存在竞争性关系。
69.1.6单抗可变区编码序列获得:
70.参考生工生物工程(上海)股份有限公司的总rna抽提试剂盒使用说明书从s3a4、9-7a4和35c6的杂交瘤细胞株中提取总rna。
71.以总rna为模板,oligo(dt)18为引物,rt-pcr扩增抗破伤风毒素单抗cdna。反应条件:30℃10min;42℃15min;70℃15min;4℃保存。
72.已制备抗破伤风毒素单抗cdna为模板,使用表1中的引物,即pcr扩增重链h,轻链l的引物,pcr扩增抗破伤风毒素鼠源单抗可变区基因。pcr参数设置:940c,预变性,5min;30cycles:940c变性,0.5min,650c复性,o.5min,720c延伸,1.0min;720c延伸,10min。
73.表1
74.primer名称序列(5'to3')hf1aggtccagctgctcgagtctgghf2aggtccagctgctcgagtcagghf3aggtccagcttctcgagtctgghf4aggtccagcttctcgagtcagghf5aggtccaactgctcgagtctgg
hf6aggtccaactgctcgagtcagghf7aggtccaacttctcgagtctgghf8aggtccaacttctcgagtcagghrlaggcttactagtacaatccctgggcacaathr2gttctgactagtgggctctctgggctchr3gggggtactagtcttgggtattctaggctclficcagttccgagctcgttgtgactcaggaatctlf2ccagttccgagctcgtgttgacgcagccgccclf3ccagttccgagctcgtgctcacccagtctccalf4ccggttccgagctccagatgacccagtctccalf5ccggatgtgagctcgtgatgacccgagctccalf6ccagatgtgagctcgtcatgacccagtctccalf7ccagttccgagctcgtgatgacacagtctccalrgcgccgtctagaattaacactcattcctgttgaa
75.用1%琼脂糖凝胶电泳分析pcr扩增结果,并采用生工生物工程(上海)股份有限公司的胶回收试剂盒回收650bp处的单抗可变区pcr扩增片段,并连接于pmd18t克隆载体(购自takara公司)上,转入dh5α大肠杆菌感受态细胞中,进行蓝白斑筛选,将阳性克隆送生工生物工程(上海)股份有限公司测序验证。
76.结果显示:轻链混合引物扩增出轻链可变区基因,重链混合引物扩增出重链可变区基因,其大小约为650bp左右,条带单一,与预测的轻/重链基因片段的理论大小基本一致,如图2所示。
77.1.74株单克隆抗体的测序结果分析:
78.根据ncbiigblast(http://www.ncbi.nlm.nih.gov/)免疫球蛋白基因比对分析结果,筛选出功能性抗体可变区基因。
79.结果显示:测序结果seqidno:1、seqidno:3、seqidno:5、seqidno:7、seqidno:9、seqidno:11和seqidno:13,其编码蛋白的cdr见表2,即4株鼠单抗轻重链的cdr序列。
80.表2
[0081][0082]
2.人源化、重组表达、纯化及活性检测。
[0083]
2.1两株鼠单抗(s3a4和9-7a4)的人源化:
[0084]
参考文献(huwg.,etal,2012doi:10.1371/journal.pone.0045595),使用cdr移植技术进行人源化,以9-7a4的seqidno:9在ncbi(nationalcenterforbiotechnologyinformation(nih.gov))库中进行blastn比对获得seqidno:20;同理,9-7a4的重链cdr植入后得到seqidno:21;s3a4的轻链cdr植入后得到seqidno:22;s3a4的重链cdr植入后得到seqidno:23。
[0085]
依据who2011年推荐的命名原则:将来自其他物种cdr植入人的抗体链中,所获得抗体加上后缀-zumb(patrickmayrhoferandrenatekunert,humanantibodies27(2019)37
–
51),因此,本发明专利暂时将s3a4和9-7a4人源化后的单抗命名为s3a4-zumb和9-7a4-zumb。
[0086]
2.2人源化抗体的质粒构建:
[0087]
分泌信号肽选用小鼠kappa链的信号肽(其多肽序列见seqidno:17)。
[0088]
人igg1(imgt命名为ighg1)的轻链κ型的恒定区(seqidno:18)。
[0089]
人igg1(imgt命名为ighg1)的重链恒定区氨基酸(eu编码体系)包含了三个恒定区域:ch1区域、ch2区域和ch3区域(其多肽序列见seqidno:19)。
[0090]
将seqidno:17+seqidno:20+seqidno:18串联且经过序列优化后,得到编码9-7a4-zumb轻链的核苷酸seqidno:24;将seqidno:17+seqidno:21+seqidno:19串联且经过序列优化后,得到编码9-7a4-zumb重链的核苷酸seqidno:25。
[0091]
将seqidno:17+seqidno:22+seqidno:18串联且经过序列优化后,得到编码s3a4-zumb轻链的核苷酸seqidno:26;将seqidno:17+seqidno:23+seqidno:19串联且经过序列优化后,得到编码s3a4-zumb重链的核苷酸seqidno:27。
[0092]
将序列seqidno:24、seqidno:25、seqidno:26和seqidno:27送生工生物工程(上海)股份有限公司进行基因合成,同时亚克隆到载体pcdna3.1(+)中。
[0093]
2.3蛋白表达稳转株建立和纯化:
[0094]
参考质粒抽提试剂盒说明书,利用无内毒素大提试剂盒(cw2107北京康为世纪)进行质粒大提。同时,参考说明书,将cho-s细胞培养在cdcho培养基(gibco,10743-029)中,置于37℃,5%c02细胞培养箱中进行培养,准备好细胞后,使用伯乐电转仪将质粒转染到cho-s细胞中。参考说明书(freedomcho-skituserguidep32-3日,采用共转染和有限稀释法筛选稳定株,筛选8周后,获得了稳定表达株。
[0095]
将筛选得到的高表达克隆株用无血清培养基扩大培养,1000g离心收获表达上洁。表达上清用0.22um滤膜过滤后,首先,用proteina凝胶层析(ge公司,美国),其条件是:用平衡缓冲液(20mmpb,ph7.0)平衡层析柱后,表达上清过亲和层析柱,用洗脱缓冲液(20nmgly-cl,ph3.2)洗脱。其次,sp阳离子交换层析(上海博格隆公司),其条件是:平衡缓冲液a(20mm,ph6.0)平衡层析柱后,样品用双纯水稀释电导至3.0—3.5ms之问,过sp柱子结合后,用洗脱缓冲液b(20mm,1.5mnaclph6.0)线性洗脱;最后,浓缩置换缓冲液pbs。
[0096]
结果显示:sds-page显示表达正确(图4),纯化后的抗体进行hplc检测,纯度在90%以上。
[0097]
2.4抗体的效价测定:
[0098]
将实施例2.3获得的纯化产物,参考3.3的方法,测定其中和保护作用,其协同性也
被检测。
[0099]
结果表明:获得2株人源化后的单抗,分别的效价为38iu/mg和35iu/mg。它们的协同保护效价可达70iu/mg。
[0100]
3.检测方法。
[0101]
3.1蛋白浓度:参考nano(thermo公司)操作手则,测定trx-ttc、抗体等蛋白浓度。
[0102]
酶联免疫吸附实验(elisa法):
[0103]
a、包被:在每个96孔板中加含1ug/ml破伤风类毒素(宁波荣升,批号:501701)的0.1ml0.05m碳酸盐包被缓冲液(ph9.0),4℃过夜。
[0104]
b、洗板及封闭:次日,弃去孔内溶液,用洗涤缓冲液(ph7.4,20mm磷酸钠,0.15m氯化钠,0.05%吐温20)在bioten洗板机中洗板3次,最后一次拍板除去残留缓冲液。每孔加0.2ml封闭缓冲液(含5%脱脂奶粉的洗涤缓冲液),室温放置2小时封闭。
[0105]
c、加入一抗:倾去封闭缓冲液,于各反应孔中加入新鲜1:10、1:100、1:1000和1:2000稀释的鼠抗破伤风单克隆抗体0.1ml。37℃孵育1小时后,用洗涤缓冲液洗涤3次。
[0106]
d、加入二抗:加入1:2000稀释的hrp标记的羊抗鼠作为二抗(上海生工)0.1ml,37℃孵育1小时,接着用洗涤缓冲液洗涤3次。
[0107]
e、加入底物及读数:于各反应孔中加入新鲜配制的tmb底物溶液0.1ml,37℃放置30分钟后于各反应孔中加入2m硫酸0.05ml终止显色反应。在elisa检测仪上,于450nm处,以空白对照孔调零后测各孔od值。
[0108]
3.3小鼠法测定抗体中和效价:
[0109]
参考中国药典2015版通则3508,使用小鼠实验法执行。
[0110]
1、破伤风抗毒素标准品(购自中国食品药品检定研究院)配制:用硼酸盐缓冲盐水(ph7.2,50mm硼酸,0.15m氯化钠)稀释,使每ml含0.5iu,当与毒素等量混合后,每0.4ml混合溶液注射量中含0.1iu。
[0111]
2、破伤风毒素标准品(购自中国食品药品检定研究院)配制:用硼酸盐缓冲盐水稀释,使每ml含5个试验量(0.5l+,l+为破伤风毒素使小鼠100%死亡的最低致死剂量),即与抗毒素等量混合后每0.4ml注射量中含1个试验量(0.1l+)。
[0112]
将待检供试品用硼酸盐缓冲盐水稀释成数个稀释度,使每ml约含0.5iu(即0.5iu)或其上下,即与毒素等量混合后每0.4ml注射量中约含0.1iu或其上下。稀释度之间间隔约为5%。
[0113]
3、将破伤风抗毒素标准品及不同稀释度的待检供试品分别加入等量的稀释试验毒素,混合均匀,置水浴箱中于37℃结合1小时,立即注射。
[0114]
注射时,由高稀释度向低稀释度依次注射,每个稀释度各注射0.4ml于17-19g小鼠腹部或大腿根部皮下,每个稀释度各注射小鼠至少3只。
[0115]
4、结果观察,试验小鼠至少应每日上、下午各观察一次,连续5日,并记录发病及死亡情况。
[0116]
结果判定,对照小鼠应于72~120小时之内全部死亡。待检供试品之效价应为与对照小鼠同时死亡或出现破伤风神经毒症状最重者的最高稀释度。
[0117]
序列信息:
[0118]
[0119][0120]
[0121]
[0122]
[0123]
[0124]
[0125]
[0126]
[0127]
[0128]
[0129]
[0130]
[0131]
[0132]
[0133]
[0134]
[0135]
[0136]
[0137]
[0138]
[0139]
[0140]
[0141]
[0142]
[0143]
[0144]
[0145]
[0146]
[0147]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1