一种铱配合物光敏剂及其制备方法与应用
1.本发明涉及光动力治疗技术领域,尤其涉及一种铱配合物光敏剂及其制备方法与应用。
背景技术:
2.光动力治疗(pdt)因其无创、时空可控的治疗方式而受到广泛关注。在光动力治疗过程中,光敏剂(pss)在黑暗条件下具有可忽略的细胞毒性,但在光照条件下产生大量活性氧(ros),从而造成较高的细胞毒性。ros的产生机制通常可以分为两种途径:ⅰ型和ⅱ型。ⅰ型途径是由处于激发态的光敏剂向周围底物转移电子形成自由基,如o2·-和oh
·
;而在ⅱ型途径中,处于激发态的光敏剂将能量传递给三线态氧分子,形成单线态氧1o2。ⅰ型pdt对氧含量的依赖性更低,在克服肿瘤微环境中的缺氧问题时,较ⅱ型pdt具有更广阔的发展前景。
3.ros通过其强氧化作用快速破坏周围的生物分子,包括蛋白质、脂类和核酸,从而导致细胞死亡。pdt过程中产生的ros寿命短(在生命体系中为0.03~0.18ms)、扩散距离有限(在生命体系中为0.01~0.02μm),所以,ros产生的首要位置会直接影响pdt治疗效果。因此,如果将光敏剂精确地运输到重要或脆弱的细胞器中,聚集的光敏剂就可以攻击这些癌细胞的“致命部位”,就会对肿瘤组织造成更大的损伤。其中,线粒体被广泛选择为癌症治疗的有效靶点,因为它们为细胞提供能量,调节细胞的生存和死亡,对线粒体靶向的癌症治疗剂的研究具有十分重要的意义。
4.ir(ⅲ)配合物中存在的长寿命三重激发态为其向周围底物转移能量或电子提供了更大的可能,促进了活性氧及活性自由基的产生。通过配体结构的设计,不仅能够调节ir(ⅲ)配合物的激发态性质,也能够连接靶向基团以靶向重要细胞器,达到高效的pdt效果。除此之外,ir(ⅲ)配合物本身的特征磷光具有光稳定性好、stokes位移大、发射寿命长的特点,在生物成像领域也具有独特的优势。
5.因此,如何将铱配合物应用于光动力治疗中成为了本领域技术人员亟需解决的问题。
技术实现要素:
6.有鉴于此,本发明提供了一种铱配合物光敏剂及其制备方法与应用。该铱配合物光敏剂能够精确抵达线粒体,并且能够克服微环境中的缺氧问题实现ⅰ/ⅱ型光动力治疗。
7.为了达到上述目的,本发明采用如下技术方案:
8.一种铱配合物光敏剂,所述铱配合物光敏剂的结构式如下:
[0009][0010]
本发明提供了上述铱配合物光敏剂的制备方法,包括以下步骤:
[0011]
s1、将1,10-菲啰啉-5,6-二酮、对苯二甲醛、醋酸铵和醋酸进行反应,反应液与水所得混合液的ph调至中性,得到混合物,混合物顺次进行分离、溶解过滤、干燥,即得配体fmp;
[0012]
s2、在保护气体下,将2,3,3-三甲基吲哚、1,3-丙烷磺酸内酯和邻二氯苯进行反应,即得化合物1;
[0013]
s3、在保护气体下,将配体fmp、化合物1、催化剂和混合溶剂1进行反应,反应液与饱和氯化钠溶液混合后顺次进行分离、干燥,即得配体psi;
[0014]
s4、将ircl3·
3h2o、2-苯基吡啶和混合溶剂2进行反应,即得化合物2;
[0015]
s5、在保护气体下,将化合物2、配体psi和混合溶剂3进行反应后除去二氯甲烷,反应产物、nh4pf6水溶液和水混合后顺次进行分离、纯化、干燥,即得铱配合物光敏剂。
[0016]
进一步的,所述1,10-菲啰啉-5,6-二酮、对苯二甲醛、醋酸铵的摩尔比为1.8~2.2:3.8~4.2:58~65;所述醋酸铵与醋酸的摩尔体积比为58~65mmol:54~66ml;所述醋酸与水的体积比为54~66:220~280。
[0017]
进一步的,所述2,3,3-三甲基吲哚和1,3-丙烷磺酸内酯的摩尔比为2.8~3.5:3.0~4.0;所述2,3,3-三甲基吲哚和邻二氯苯的摩尔体积比为2.8~3.5mmol:2.4~4ml。
[0018]
进一步的,所述配体fmp和化合物1的摩尔比为1.0~1.5:1.8~2.4;
[0019]
所述配体fmp和混合溶剂1的摩尔体积比为1.0~1.5mmol:18~25ml;
[0020]
所述催化剂和混合溶剂1的体积比为0.8~1.2:100;
[0021]
所述饱和氯化钠溶液与混合溶剂1的体积比为180~220:18~25;
[0022]
所述催化剂为六氢吡啶,所述混合溶剂1包含乙醇和n,n-二甲基甲酰胺,所述乙醇和n,n-二甲基甲酰胺的体积比为18~22:1。
[0023]
进一步的,所述ircl3·
3h2o和2-苯基吡啶的摩尔比为1.8~2.2:4.0~6.0;
[0024]
所述ircl3·
3h2o和混合溶剂2的摩尔体积比为1.8~2.2mmol:45~60ml;
[0025]
所述混合溶剂2包含乙二醇乙醚和水,所述乙二醇乙醚和水的体积比为1~5:1。
[0026]
进一步的,所述化合物2、配体psi的摩尔比为0.1~0.2:0.3~0.4;
[0027]
所述化合物2与混合溶剂3的摩尔体积比为0.1~0.2mmol:35~45ml;
[0028]
所述nh4pf6的水溶液、水和混合溶剂3的体积比为4~8:24~35:35~45;
[0029]
所述混合溶剂3包含二氯甲烷和甲醇,所述二氯甲烷和甲醇的体积比为1~2:1~2。
[0030]
进一步的,所述步骤s2、s3和s5中的保护气体独立的为氮气、氩气、氦气、氖气或二氧化碳;
[0031]
所述步骤s1反应的温度为100~130℃,时间为25~40min;步骤s2反应的温度为100~140℃,时间为20~30h;步骤s3反应的温度为80~100℃,时间为40~55h;步骤s4反应的温度为120~150℃,时间为20~30h;步骤s5反应的时间为20~30h。
[0032]
进一步的,所述配体fmp、化合物1、配体psi和化合物2的结构式如下:
[0033][0034]
本发明还提供了上述铱配合物光敏剂在制备光动力治疗药物中的应用。
[0035]
经由上述的技术方案可知,与现有技术相比,本发明的有益效果如下:
[0036]
1、本发明所制备的铱配合物光敏剂的发光强度随光照时间的增长而增强,可以监控光动力治疗的进程。
[0037]
2、本发明所制备的铱配合物光敏剂具有低的暗细胞毒性,但在光照下,通过产生o2·-造成细胞毒性,可用于ⅰ/ⅱ型光动力治疗,能够克服微环境中的缺氧问题,同时线粒体靶向功能提高了光动力治疗效果。
[0038]
3、本发明所述的铱配合物光敏剂的制备方法简单,反应条件温和,产率较高,可实现大规模的生产。
附图说明
[0039]
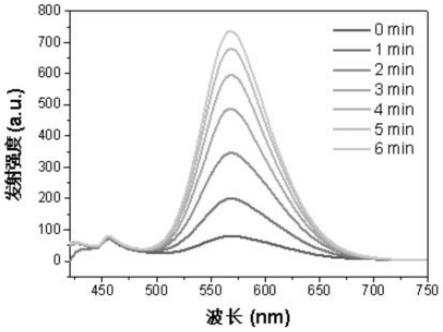
图1为实施例3所制备的铱配合物光敏剂ir-psi随光照时间发光变化的荧光发射光谱图;
[0040]
图2为实施例3所制备的铱配合物光敏剂ir-psi随光照时间吸收变化的紫外-可见
光谱图;
[0041]
图3为实施例3所制备的铱配合物光敏剂ir-psi和活性氧探针2,7-二氯二氢荧光素(dcfh)的混合溶液在光照下的荧光发射光谱;
[0042]
图4为实施例3所制备的铱配合物光敏剂ir-psi产生超氧阴离子的电子顺磁共振信号;
[0043]
图5为实施例3所制备的铱配合物光敏剂ir-psi产生单线态氧的电子顺磁共振信号图;
[0044]
图6为实施例3所制备的铱配合物光敏剂ir-psi在不同条件下对hela细胞存活率的影响;
[0045]
图7为实施例3所制备的铱配合物光敏剂ir-psi与线粒体探针的细胞共染成像图。
具体实施方式
[0046]
本发明提供了一种铱配合物光敏剂,其结构式如下:
[0047][0048]
本发明提供了上述铱配合物光敏剂的制备方法,包括以下步骤:
[0049]
s1、将1,10-菲啰啉-5,6-二酮、对苯二甲醛、醋酸铵和醋酸进行反应,反应液与水所得混合液的ph调至中性,得到混合物,混合物顺次进行分离、溶解过滤、干燥,即得配体fmp;
[0050]
s2、在保护气体下,将2,3,3-三甲基吲哚、1,3-丙烷磺酸内酯和邻二氯苯进行反应,即得化合物1;
[0051]
s3、在保护气体下,将配体fmp、化合物1、催化剂和混合溶剂1进行反应,反应液与饱和氯化钠溶液混合后顺次进行分离、干燥,即得配体psi;
[0052]
s4、将ircl3·
3h2o、2-苯基吡啶和混合溶剂2进行反应,即得化合物2;
[0053]
s5、在保护气体下,将化合物2、配体psi和混合溶剂3进行反应后除去二氯甲烷,反应产物、nh4pf6的水溶液和水混合后顺次进行分离、纯化、干燥,即得铱配合物光敏剂。
[0054]
在本发明中,所述1,10-菲啰啉-5,6-二酮、对苯二甲醛、醋酸铵的摩尔比为1.8~2.2:3.8~4.2:58~65,优选为1.9~2.1:3.9~4.1:59~64,进一步优选为2.0:4.0:60~62;所述醋酸铵与醋酸的摩尔体积比为58~65mmol:54~66ml,优选为60~64mmol:57~63ml,进一步优选为62~63mmol:60~62ml;所述醋酸与水的体积比为54~66:220~280,优选为57~63:230~260,进一步优选为60~62:240~250。
[0055]
在本发明中,所述步骤s1中的溶解过滤的具体步骤为:混合物经分离后得到的粗
产物用乙醇加热溶解;所述乙醇的体积浓度为99.7%,溶解的温度为70~90℃,优选为72~86℃,进一步优选为75~80℃;时间为20~40min,优选为22~38min,进一步优选为25~35min;所述粗产物与乙醇的质量体积比为80~120mg:180~220ml,优选为90~110mg:190~210ml,进一步优选为95~100mg:195~200ml。
[0056]
在本发明中,所述2,3,3-三甲基吲哚和1,3-丙烷磺酸内酯的摩尔比为2.8~3.5:3.0~4.0,优选为2.9~3.4:3.2~3.8,进一步优选为3.0~3.2:3.4~3.6;
[0057]
所述2,3,3-三甲基吲哚和邻二氯苯的摩尔体积比为2.8~3.5mmol:2.4~4ml,优选为2.9~3.4mmol:2.5~3.5ml,进一步优选为3.0~3.2mmol:2.8~3.2ml。
[0058]
在本发明中,所述配体fmp和化合物1的摩尔比为1.0~1.5:1.8~2.4,优选为1.1~1.4:1.9~2.3,进一步优选为1.2~1.3:2.0~2.2;
[0059]
所述配体fmp和混合溶剂1的摩尔体积比为1.0~1.5mmol:18~25ml;优选为1.1~1.4mmol:19~24ml,进一步优选为1.2~1.3mmol:20~22ml;
[0060]
所述催化剂和混合溶剂1的体积比为0.8~1.2:100,优选为0.9~1.1:100,进一步优选为1:100;
[0061]
所述饱和氯化钠溶液与混合溶剂1的体积比为180~220:18~25,优选为190~210:19~24,进一步优选为195~200:21~23;
[0062]
所述催化剂为六氢吡啶,所述混合溶剂1包含乙醇和n,n-二甲基甲酰胺,所述乙醇和n,n-二甲基甲酰胺的体积比为18~22:1,优选为19~21:1,进一步优选为20:1。
[0063]
在本发明中,所述ircl3·
3h2o和2-苯基吡啶的摩尔比为1.8~2.2:4.0~6.0,优选为1.9~2.1:4.2~5.5,进一步优选为2.0:4.5~5.0;
[0064]
所述ircl3·
3h2o和混合溶剂2的摩尔体积比为1.8~2.2mmol:45~60ml,优选为1.9~2.1mmol:48~56ml,进一步优选为2.0mmol:50~54ml;
[0065]
所述混合溶剂2包含乙二醇乙醚和水,所述乙二醇乙醚和水的体积比为1~5:1,优选为2~4:1,进一步优选为3:1。
[0066]
在本发明中,所述化合物2、配体psi的摩尔比为0.1~0.2:0.3~0.4,优选为0.12~0.18:0.32~0.38,进一步优选为0.14~0.16:0.34~0.36;
[0067]
所述化合物2与混合溶剂3的摩尔体积比为0.1~0.2mmol:35~45ml,优选为0.12~0.18mmol:38~44ml,进一步优选为0.14~0.16mmol:40~42ml;
[0068]
所述nh4pf6水溶液、水与混合溶剂3的体积比为4~8:24~35:35~45,优选为5~7:25~32:36~42,进一步优选为6:28~30:38~40;
[0069]
所述混合溶剂3包含二氯甲烷和甲醇,所述二氯甲烷和甲醇的体积比为1~2:1~2,优选为1.2~1.8:1.2~1.8,进一步优选为1.4~1.6:1.4~1.6。
[0070]
在本发明中,所述步骤s2、s3和s5中的保护气体独立的为氮气、氩气、氦气、氖气或二氧化碳,优选为氮气、氩气或二氧化碳,进一步优选为氮气;
[0071]
所述步骤s1反应的温度为100~130℃,优选为110~125℃,进一步优选为115~120℃;时间为25~40min,优选为28~36min,进一步优选为30~35min;
[0072]
步骤s2反应的温度为100~140℃,优选为110~130℃,进一步优选为115~125℃;时间为20~30h,优选为22~28h,进一步优选为24~26h;
[0073]
步骤s3反应的温度为80~100℃,优选为85~95℃,进一步优选为88~92℃;时间
为40~55h,优选为42~52h,进一步优选为45~50h;
[0074]
步骤s4反应的温度为120~150℃,优选为125~140℃,进一步优选为130~135℃;时间为20~30h,优选为22~28h,进一步优选为24~26h;
[0075]
步骤s5反应的时间为20~30h,优选为22~28h,进一步优选为24~26h。
[0076]
在本发明中,所述配体fmp、化合物1、配体psi和化合物2的结构式如下:
[0077][0078][0079]
本发明还提供了上述铱配合物光敏剂在制备光动力治疗药物中的应用。
[0080]
下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0081]
实施例1
[0082]
将1,10-菲啰啉-5,6-二酮(2mmol)、对苯二甲醛(4mmol)和醋酸铵(60mmol)溶于醋酸(60ml)中,在115℃下回流30min。冷却至室温后加入250ml蒸馏水,搅拌条件下用浓氨水(质量浓度为25%)调ph至中性,析出黄色固体。然后进行抽滤,抽滤后的粗产物用水洗涤三次,在80℃下干燥24h后得到的橙色粗产物再用乙醇在85℃下加热溶解30min,其中,橙色粗产物与乙醇的质量体积比为100mg:200ml,趁热过滤后,将滤液放入旋转干燥机中旋干即得黄色的配体fmp,产率为70.0%;
[0083]
将2,3,3-三甲基吲哚(3.14mmol)和1,3-丙烷磺酸内酯(3.48mmol)溶于3ml邻二氯苯中,氩气保护下,在120℃下回流24h。冷却后抽滤,再用乙醚洗涤三次,将所得粗产物放入真空干燥箱(70℃)中干燥24h后即得紫黑色的化合物1,产率为89.9%;
[0084]
将配体fmp(1.2mmol)和化合物1(2mmol)溶于21ml混合溶剂(乙醇和dmf的体积比
为20:1)中,并加入210μl六氢吡啶,混合溶液在氩气保护下,于90℃回流48h。冷却至室温后,将反应液加入到200ml饱和氯化钠溶液中,析出暗红色沉淀。然后进行抽滤,抽滤后的粗产物放入真空干燥箱(70℃)中干燥24h后即得黑红色的配体psi,产率为75.7%。
[0085]
对本实施例所制备得到的黑红色的配体psi的核磁共振谱图进行分析可知,本发明所述技术方案可以高效率的制备出配体psi。具体分析如下:
[0086]1hnmr(400mhz,dmso-d6)δ9.00(ddd,j=9.2,4.3,1.7hz,2h),8.91(t,j=9.5hz,2h),8.56
–
8.46(m,3h),8.42(d,j=8.2hz,2h),8.10
–
7.99(m,2h),7.85(dt,j=8.7,4.7hz,2h),7.77(dd,j=8.0,4.4hz,1h),7.68
–
7.53(m,2h),4.92(t,j=8.1hz,2h),2.70(dd,j=7.7,4.4hz,2h),2.22(d,j=8.6hz,2h),1.81(s,6h)。
[0087]
实施例2
[0088]
将ircl3·
3h2o(2mmol)和2-苯基吡啶(4.4mmol)溶于50ml的混合溶剂(乙二醇乙醚和水的体积比为3:1)中,在130℃下回流24h,冷却至室温后进行抽滤,将抽滤后的粗产物在80℃下干燥24h即得黄色的化合物2(ir2(ppy)4cl2),产率为80%;
[0089]
实施例3
[0090]
将实施例2的化合物2(0.187mmol)和实施例1的配体psi(0.374mmol)溶于40ml的混合溶剂(甲醇和二氯甲烷的体积比为1:1)中,氩气保护下,避光回流24h。停止反应后,旋掉反应液中的二氯甲烷,加入5ml的nh4pf6水溶液,搅拌30min,再补加30ml水,然后进行抽滤,抽滤后的粗产物在80℃下干燥24h。将干燥后的粗产品通过硅胶色谱柱纯化,先以体积比为60:1的二氯甲烷/甲醇淋洗掉杂质,然后再用体积比为30:1的二氯甲烷/甲醇洗涤得到橙红色组分。将橙红色组分放入旋转干燥机中旋干即得深红色的铱配合物光敏剂ir-psi,产率为62.6%。
[0091]
对本实施例所制备得到的深红色的铱配合物光敏剂ir-psi的核磁共振谱图进行分析可知,本发明所述技术方案可以高效率的制备出铱配合物光敏剂ir-psi。具体分析如下:
[0092]1h nmr(400mhz,dmso-d6)δ9.22(t,j=8.9hz,2h),8.68
–
8.48(m,5h),8.28(d,j=8.2hz,2h),8.16(d,j=14.7hz,4h),8.05(d,j=8.4hz,2h),7.97(d,j=7.8hz,2h),7.90(q,j=7.7,6.8hz,3h),7.68
–
7.60(m,2h),7.54(t,j=7.0hz,2h),7.08(t,j=7.5hz,2h),6.99(dt,j=19.1,7.0hz,4h),6.31(d,j=7.4hz,2h),4.96(t,j=8.2hz,2h),2.73(t,j=5.9hz,2h),2.26(s,2h),1.87(d,j=3.1hz,6h);
[0093]
13
cnmr(101mhz,dmso-d6)δ182.31,167.42,153.13,152.01,150.82,149.75,149.14,144.96,144.65,144.55,141.32,139.25,136.71,133.36,132.19,131.75,130.80,130.14,129.59,127.58,127.40,125.61,124.40,123.63,122.92,120.52,115.79,114.62,52.85,47.66,46.20,26.10,26.02,25.31。
[0094]
实施例4
[0095]
将实施例2的化合物2(0.19mmol)和实施例1的配体psi(0.38mmol)溶于40ml的混合溶剂(甲醇和二氯甲烷的体积比为1:1)中,氩气保护下,避光回流25h。停止反应后,旋掉反应液中的二氯甲烷,加入6ml的nh4pf6水溶液,搅拌30min,再补加30ml水,然后进行抽滤,抽滤后的粗产物在80℃下干燥24h。将干燥后的粗产品通过硅胶色谱柱纯化,先以体积比为60:1的二氯甲烷/甲醇淋洗掉杂质,然后再用体积比为30:1的二氯甲烷/甲醇洗涤得到橙红
色组分。将橙红色组分放入旋转干燥机中旋干即得深红色的铱配合物光敏剂ir-psi,产率为58.3%。
[0096]
实施例5
[0097]
将实施例2的化合物2(0.195mmol)和实施例1的配体psi(0.365mmol)溶于40ml的混合溶剂(甲醇和二氯甲烷的体积比为1:1)中,氩气保护下,避光回流25h。停止反应后,旋掉反应液中的二氯甲烷,加入7ml的nh4pf6的水溶液,搅拌30min,再补加30ml水,然后进行抽滤,抽滤后的粗产物在80℃下干燥24h。将烘干后的粗产品通过硅胶色谱柱纯化,先以体积比为60:1的二氯甲烷/甲醇淋洗掉杂质,然后再用体积比为30:1的二氯甲烷/甲醇洗涤得到橙红色组分。将橙红色组分放入旋转干燥机中旋干即得深红色的铱配合物光敏剂ir-psi,产率为56.5%。
[0098]
性能表征
[0099]
铱配合物光敏剂ir-psi的光谱测试
[0100]
具体操作步骤如下:将实施例3所制备的铱配合物光敏剂ir-psi溶解在dmso中,制成10mmol/l的储备液。除非特别指出,以下实验中所使用的样品均通过储备液稀释得到。测定铱配合物光敏剂ir-psi(10μmol/l)的吸收光谱和荧光光谱,采用365nm紫外手电筒作为外部光源,每光照1分钟采集一次紫外和荧光光谱。其中,采集荧光光谱时,激发波长为400nm。测试结果见图1和图2,由图1~2可得:随光照时间延长,铱配合物光敏剂ir-psi的发光逐渐增强,而在550nm处的吸收逐渐降低。说明在光动力治疗过程中,能够实现对治疗进程的实时监控。
[0101]
活性氧的测定
[0102]
具体操作步骤如下:用2,7-二氯二氢荧光素(dcfh)作为指标,测量ros的生成。dcfh由2,7-二氯二氢荧光素二乙酸酯(dcfh-da)活化得到。将dcfh-da(0.5ml,1mmol/l)加入naoh(2ml,10mmol/l)水溶液中,室温静置30min,充分水解。然后用pbs(10ml)缓冲液中和至ph=7.4,得到浓度为40μmol/l的储备液。将储备液置于黑暗冷冻条件下保存。
[0103]
测试时,向2ml活化的dcfh溶液中加入实施例3所制备的铱配合物光敏剂ir-psi(2μl,10-2
mol/l),每光照5s测试一次荧光光谱,激发波长为480nm。测试结果见图3,由图3可得:随光照时间增长,ir-psi和dcfh混合溶液在530nm处发光逐渐增强,说明光照过程中产生了活性氧。
[0104]
esr测定活性氧物种
[0105]
具体操作步骤如下:使用5,5-二甲基-1-吡咯啉-n-氧化物(dmpo)捕获超氧阴离子自由基(o2·-)和羟基自由基(
·
oh)。测定o2·-时,黑暗条件下向实施例3所制备的铱配合物光敏剂(100μmol/l)的甲醇溶液中加入dmpo(10mmol/l),于电子顺磁共振波谱仪测定其电子顺磁共振信号,使用365nm紫外手电照射样品1min后,再次测定其电子顺磁共振信号。测定
·
oh时,将溶剂换为体积比为1:1的水和乙腈混合液,其他测试条件相同。测试结果见图4,由图4可得:在以甲醇作溶剂时,光照下实施例3所制备的铱配合物光敏剂ir-psi的电子顺磁共振谱图显示出o2·-的信号,表明光照过程中产生了o2·-;图5为实施例3所制备的铱配合物光敏剂ir-psi产生单线态氧的电子顺磁共振信号图,选用2,2,6,6-四甲基哌啶(temp)对1o2进行捕获,由图5可得:电子顺磁共振信号图显示出1:1:1的信号峰,表明产生了1o2;
[0106]
上述结果表明ir-psi在光照过程中同时产生了o2·-和1o2,为ⅰ型和ⅱ型协同pdt治
疗机理,相比于ⅱ型光敏剂,ⅰ/ⅱ协同机理对o2的依赖性更小,更有利于应用到缺氧环境下的光动力治疗当中。
[0107]
细胞毒性测试
[0108]
具体操作步骤如下:将消化后的细胞以5
×
104/孔的密度接种入96孔细胞培养板中,设3个复孔,在温度为37℃、co2的体积浓度为5%的培养箱中培养24h。待细胞长成单层即弃去培养液,加入不同浓度梯度的实施例3所制备的铱配合物光敏剂(0μmol/l、3.125μmol/l、6.25μmol/l、12.5μmol/l、25μmol/l、50μmol/l),放入温度为37℃、co2的体积浓度为5%的培养箱孵育4h后,每孔加入20μl mtt溶液,继续培养4h。终止培养,小心吸去孔内培养液。每孔加入150μl dmso,酶标仪振荡10min,使结晶物充分溶解,酶标仪测定od值。在光毒性测试中,细胞在加入不同浓度铱配合物光敏剂孵育2h后使用氙灯进行光照后再继续孵育2h,后续处理方法与暗毒性测试一致。测试结果见图5,由图5可得:在无光照时,铱配合物光敏剂ir-psi具有可忽略的毒性。而经过光照5min(400~800nm)后,细胞存活率明显降低。延长光照时间至10min后,细胞存活率降低显著,在铱配合物光敏剂ir-psi的浓度仅为3.125μmol/l时,细胞存活率也降低至41.1%。以上结果表明,铱配合物光敏剂ir-psi在黑暗条件下的细胞毒性可忽略不计,而在光照后显示出较大的细胞毒性,当光照时间较长时,低浓度的铱配合物光敏剂ir-psi就能造成明显细胞损伤,具有优越的光动力治疗效果。
[0109]
细胞共定位
[0110]
具体操作步骤如下:hela细胞在六孔板37℃贴壁生长24h,用实施例3所制备的铱配合物光敏剂ir-psi(50μmol/l)和mito-tracker green(1μmol/l)孵育细胞20min,然后光照5min,使用共聚焦显微镜进行细胞成像。对于铱配合物光敏剂ir-psi,激发波长为405nm,发射波长为550~650nm。对于mtg,激发波长为488nm,发射波长500~530nm。测试结果见图6,由图6可得:铱配合物光敏剂ir-psi与mtg的pearson相关系数(pr)为0.93。结果表明,配合物进入细胞后主要靶向线粒体,因此,铱配合物光敏剂ir-psi在光动力治疗过程中首先破坏线粒体,而线粒体是影响细胞生命活动的重要细胞器,提高了光动力治疗的效率。
[0111]
本说明书中各个实施例采用递进的方式描述,每个实施例重点说明的都是与其他实施例的不同之处,各个实施例之间相同相似部分互相参见即可。
[0112]
对所公开的实施例的上述说明,使本领域专业技术人员能够实现或使用本发明。对这些实施例的多种修改对本领域的专业技术人员来说将是显而易见的,本文中所定义的一般原理可以在不脱离本发明的精神或范围的情况下,在其它实施例中实现。因此,本发明将不会被限制于本文所示的这些实施例,而是要符合与本文所公开的原理和新颖特点相一致的最宽的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1