AIE荧光材料的制备和应用
aie荧光材料的制备和应用
技术领域
1.本发明属于荧光小分子自组装领域,涉及三种能自组装的荧光材料合成、自组装体的制备方法及其在阳离子检测及细胞毒性方面的应用。
背景技术:
2.具有可调控发光性能的发光材料是人们关注的热点,传统的有机荧光分子由于聚集引起的猝灭(acq),只能在稀溶液中具有荧光性质,这极大地限制了其在固体发光材料中的应用。为了克服这一问题,人们做了许多努力,如在玻璃化转变温度较高的聚合物中加入支链或大环,或将其与玻璃化转变温度较高的聚合物共混,但结果都不理想。唐本忠院士等人在2001年发现的聚集诱导发光(aggregate-induced emission,aie)现象为解决这一问题提供了另一种途径。他们开发了一种新的分子,这种分子在溶液中荧光很微弱,但聚集后会发出强烈的光。这种异常的荧光行为是由于分子内旋的限制,聚集诱导的平面化,以及在某些情况下j-聚集的形成。经过多年的研究,已经设计出许多具有aie效应的神奇分子。
3.分子自组装是分子通过非共价键相互作用定向缔合成纳米或微米结构。aie分子具有固态荧光效率高、发射颜色可变等优点,是构建发光微/纳米结构的理想基石。aie分子由于其独特的性质,可以被设计为一种新型的功能材料,在生物、环境、材料、制药、农业等领域有着广泛的应用。然而,经典aie分子由于其非平面拓扑结构难以有序排列,因而难以自发组装成有序的组装体。
技术实现要素:
4.申请人课题组合成的绿色荧光蛋白发色团(hbi)衍生物同样具有aie效应,并且绿色荧光蛋白发色团衍生物在一定条件下可通过自组装形成结构均匀的纳米材料。由于hbi来自于绿色荧光蛋白的发色团,因此,其衍生物的自组装体具有较好的生物相容性和较低的细胞毒性,使其在生物医药领域具有更好的应用。此外,由于分子自组装主要通过分子间氢键,π
–
π堆叠等非共价键形成,因此一些重金属离子可通过氢键的竞争抑制分子自组装导致荧光变化或通过离子瓦解分子自组装体导致荧光淬灭,从而实现对离子的检测。可基于此原理在纯水相体系或细胞内检测重金属离子。
5.基于上述技术原理,本发明有四个目的:(1)提供几种能够通过自组装形成具有荧光性质的纳米材料的hbi衍生物;(2)提供上述能够通过自组装形成具有荧光性质的纳米材料的hbi衍生物的制备方法;(3)提供上述hbi衍生物自组装形成纳米材料的方法;(4)提供上述具有荧光性质纳米材料检测汞离子和/或铜离子的方法。
6.为了实现上述目的,本发明采取下述技术方案:
7.一、一种检测重金属离子(汞离子和/或铜离子)的分子探针
8.所述分子探针由hbi衍生物在溶剂体系中自组装形成均匀的纳米纤维状结构。所述分子探针能够识别汞离子和/或铜离子。
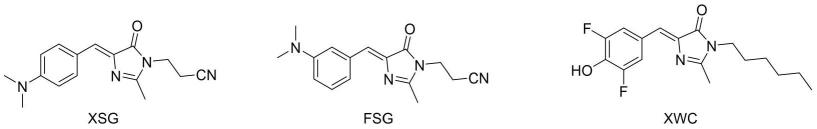
9.所述hbi衍生物的结构式如下所示:
[0010][0011]
其化学名称分别为:
[0012]
(z)-5-(4-二甲氨基苯亚甲基)-2-(2-氰基乙基)-3-甲基咪唑啉酮,标记为xsg;
[0013]
(z)-5-(3-二甲氨基苯亚甲基)-2-(2-氰基乙基)-3-甲基咪唑啉酮,标记为fsg;
[0014]
(z)-5-(4-羟基-3,5-二氟苯亚甲基)-2-正己基-3-甲基咪唑啉酮,标记为xwc。
[0015]
所述分子探针由xsg在溶剂体系中自组装形成,所述溶剂体系为纯水体系和甲醇/水体系,所述甲醇/水体系中甲醇体积比为0~20%,例如可以是甲醇体积比为20%的甲醇/水体系;优选的,所述溶剂体系为纯水相,其中不含有机溶剂。
[0016]
所述分子探针由fsg在溶剂体系中自组装形成,所述溶剂体系为甲醇/水体系、四氢呋喃/水体系、1,1,1,3,3,3-六氟-2-丙醇/水体系或二甲亚砜/水体系,其中溶剂体系中甲醇体积比为0~20%,四氢呋喃体积比为0~10%,1,1,1,3,3,3-六氟-2-丙醇体积比为0~10%,二甲亚砜体积比为0~5%;优选的,所述溶剂体系中甲醇体积比为10%~20%,四氢呋喃体积比为5%~10%,1,1,1,3,3,3-六氟-2-丙醇体积比为5%~10%,二甲亚砜体积比为1%~5%。
[0017]
所述分子探针由xwc在溶剂体系中自组装形成,所述溶剂体系为甲醇/水体系,其中溶剂体系中甲醇体积比为0~20%;优选的,所述溶剂体系中甲醇体积比为10%~20%。
[0018]
二、hbi衍生物xsg,fsg和xwc的合成方法
[0019]
hbi衍生物的合成路线如下所示:
[0020][0021][0022]
其中:路线中r.t指室温;r1为4-n,n-二甲基4-n(me)2、3-n,n-二甲基3-n(me)2或3,5-二氟-4-羟基3,5-f,4-oh;r2为丙腈或正己烷。
[0023]
三、hbi衍生物自组装形成纳米材料的方法
[0024]
将hbi衍生物溶解于溶剂体系中,混匀后,静置,获得hbi衍生物(xsg,fsg和xwc)自组装荧光材料,即获得检测重金属离子的分子探针。
[0025]
四、上述分子探针在制备检测重金属离子探针上的应用。
[0026]
所述分子探针能够识别汞离子和/或铜离子,待测溶液中铜离子浓度为0~1mmol/l,汞离子浓度为0~1mmol/l。
[0027]
一方面,所述分子探针可以通过离子抑制探针组装,导致其荧光变化检测离子。优选的,所述分子探针由xsg在溶剂体系中自组装形成。
[0028]
另一方面,所述分子探针可以通过离子瓦解组装体,导致其荧光变化(淬灭)检测离子。优选的,所述分子探针由xsg在溶剂体系中自组装形成。
[0029]
优选的,上述分子探针在制备纯水相体系中检测重金属离子探针上的应用,所述分子探针由xsg在溶剂体系中自组装形成,所述溶剂体系为纯水相,其中不含有机溶剂。
[0030]
优选的,上述分子探针在制备纯水相体系中定性和/或定量检测汞离子探针上的应用,所述分子探针由xsg在溶剂体系中自组装形成,所述溶剂体系为纯水相,其中不含有机溶剂。
[0031]
进一步,待测溶液中铜离子浓度为0.01~0.1mmol/l,汞离子浓度为0.01~0.1mmol/l。
[0032]
需要说明的是:本文所指“溶剂体系为纯水相,其中不含有机溶剂”是指该体系中有机溶剂的含量极其少量,在溶剂体系中占比低于0.1%,可忽略不计。
[0033]
与现有技术相比,本发明具有的优点及有益效果为:
[0034]
1、现有技术中利用络合的机理检测阳离子很难实现在纯水相中进行。本发明可以利用xsg分子探针实现在100%水相溶剂体系检测阳离子。
[0035]
2、汞离子可以抑制hbi衍生物(xsg、fsg、xwc)组装,可以实现裸视检测汞离子。
[0036]
3、本发明可以利用xsg分子探针实现在纯水相溶剂体系中定量检测hg
2+
。
附图说明
[0037]
图1:不同溶剂中1mg/ml的xsg自组装的荧光显微镜图(a、c、d、e)和0.17mg/ml的xsg在超纯水中自组装的荧光显微镜图;a是v/v为20%的甲醇/水、b是100%的水、c是v/v为10%的thf/水、d是v/v为10%的hfp/水、e是v/v为5%的dmso/水。
[0038]
图2:xsg在1mg/ml、20%甲醇水溶液(v/v)中自组装过程的荧光显微镜图(a-c)和扫描电镜图(d-g)。
[0039]
图3:不同溶剂中1mg/ml的fsg自组装的荧光显微镜图(a-e);a是v/v为20%的甲醇/水、b是v/v为10%的thf/水、c是v/v为10%的异丙醇/水、d是v/v为10%的hfp/水、e是v/v为5%的dmso/水。
[0040]
图4:fsg在1mg/ml、20%甲醇水溶液(v/v)中自组装过程的荧光显微镜图(a-c)和扫描电镜图(d-g)。
[0041]
图5:不同溶剂中1mg/ml的xwc自组装的荧光显微镜图(a-d):a是v/v为20%的甲醇/水、b是v/v为20%的乙腈/水、c是v/v为5%的dmso/水、d是v/v为5%的dmf/水。
[0042]
图6:xwc在1mg/ml、20%甲醇水溶液(v/v)中自组装的荧光显微镜图(a)和扫描电镜图(b、c)。
[0043]
图7:xsg、fsg、xwc在1mg/ml、20%甲醇水溶液(v/v)中分子荧光光谱图。
[0044]
图8:0.1mg/ml的xsg分别在纯水空白(a)以及1.6mmol/l的cu
2+
(b)、hg
2+
(c)、na
+
(d)、ag
+
(e)、ca
2+
(f)、k
+
(g)、mg
2+
(h)、zn
2+
(j)水溶液中自组装的荧光显微镜图(tritc模式测试)。
[0045]
图9:0.1mg/ml的xsg在纯水中形成自组装体后,测试其荧光光谱,并通过荧光显微镜观察其组装形貌;然后在组装后的溶液中分别加入10μl的汞离子和铜离子(两种离子的最终浓度均是1mmol/l),3小时后测试xsg溶液的荧光强度(激发波长是509nm,狭缝宽度是5nm-5nm),并且通过荧光显微镜(tritc模式测试)观察其组装形貌。
[0046]
图10:0.1mg/ml的xsg在汞离子浓度范围从0.01~1mmol/l时,在纯水溶液的分子荧光光谱图(10a);将图a中hg
2+
的0.01~0.1mmol/l浓度对应的曲线单独作图获得图10b,取图中533nm处的荧光数值可以获得图10b右边的折线图并获得其线性拟合图谱。
[0047]
图11:xsg、fsg、xwc在浓度分别为10-5
、10-6
、10-7
mol/l时的人神经胶质瘤细胞细胞毒性实验图。
具体实施方式
[0048]
下面结合附图和具体实施例对本发明进行详细说明。
[0049]
实施例1:hbi衍生物xsg,fsg和xwc的制备
[0050]
1.化合物2的合成
[0051]
取500ml的茄形瓶,加入200ml乙醚,32ml去离子水,10g甘氨酸甲酯盐酸盐,之后加入11g无水碳酸钾,搅拌10min,然后加入9.8g乙基乙酰亚胺盐酸盐反应10min。通过分液漏斗分离水相和有机相,水相中再次加入200ml乙醚,继续反应10min,合并有机相。向有机相中加入无水硫酸镁,干燥、过滤,旋干,得到淡黄色液体产物2。
[0052]
2.xsg的制备
[0053]
取50ml的干燥的茄形瓶,加入4-二甲氨基苯甲醛(1.49g,10mmol)和3-氨基丙腈(77mg,11mol),用20ml的无水乙醇做溶剂,氮气氛围下常温搅拌12h。旋干溶剂后得到对应的西佛碱。然后加入新制备的化合物2(1.25g,11mmol),以20ml的无水乙醇作溶剂,常温搅拌12h。反应结束后,旋干溶剂,通过柱层析分离提纯得到最终产物xsg:(z)-5-(4-二甲氨基苯亚甲基)-2-(2-氰基乙基)-3-甲基咪唑啉酮。
[0054]
hrms:calculated for[m+h]:283.15,measured:283.1551;1h nmr(400mhz,dmso,298k):δ(ppm):8.07(d,j=8.8hz,2h),6.91(s,1h),6.76(d,j=8.9hz,2h),3.85(t,j=6.5hz,2h),3.01(s,6h),2.88(t,j=6.5hz,2h),2.39(s,3h);
13
c nmr(101mhz,dmso,298k):δ(ppm):169.81,159.45,151.90,134.44,134.24,127.75,121.85,119.17,112.13,40.07,36.17,17.58,15.68.
[0055]
3.fsg的制备
[0056]
取50ml的干燥的茄形瓶,加入3-二甲氨基苯甲醛(1.49g,10mmol)和3-氨基丙腈(77mg,11mol),用20ml的无水乙醇做溶剂,氮气氛围下常温搅拌12h。旋干溶剂后得到对应的西佛碱。然后加入新制备的化合物2(1.25g,11mmol),以20ml的无水乙醇作溶剂,常温搅拌12h。反应结束后,旋干溶剂,通过柱层析分离提纯得到最终产物fsg:(z)-5-(3-二甲氨基苯亚甲基)-2-(2-氰基乙基)-3-甲基咪唑啉酮。
[0057]
hrms:calculated for[m+h]:283.15,measured:283.1547;1h nmr(400mhz,dmso,298k):δ(ppm):7.62
–
7.56(m,1h),7.25(t,j=8.0hz,1h),6.97(s,1h),6.82
–
6.78(m,1h),3.87(t,j=6.6hz,1h),2.92(s,1h),2.42(s,1h);
13
cnmr(101mhz,dmso,298k):δ(ppm):170.15,163.05,150.97,138.25,134.77,129.59,127.36,120.67,119.11,116.43,114.94,40.53,36.28,17.54,15.95.
[0058]
4.xwc的制备
[0059]
取50ml的干燥的茄形瓶,加入3,5-氟,4-羟基苯甲醛(1.58g,10mmol)和正己胺(1.45ml,11mol),用20ml的无水乙醇做溶剂,氮气氛围下常温搅拌12h。旋干溶剂后得到对应的西佛碱。然后加入新制备的化合物2(1.25g,11mmol),以20ml的无水乙醇作溶剂,常温搅拌12h。反应结束后,旋干溶剂,通过柱层析分离提纯得到最终产物xwc:(z)-5-(4-羟基-3,5-二氟苯亚甲基)-2-正己基-3-甲基咪唑啉酮。
[0060]
hrms:calculated for[m+h]:322.15,measured:322.1524;1h nmr(400mhz,dmso,298k):δ(ppm):8.05(d,j=9.0hz,2h),6.85(s,1h),6.74(d,j=9.1hz,2h),3.53(t,j=7.3hz,2h),3.01(s,6h),2.33(s,3h),1.68
–
1.43(m,2h),1.26(m,6h),0.86(t,j=6.8hz,3h);
13
c nmr(101mhz,dmso,298k):δ(ppm):170.10,164.48,153.53,151.13,138.62,136.15,125.18,123.38,115.75,40.33,31.25,28.96,26.28,22.45,15.91,14.34.
[0061]
实施例2:xsg、fsg、xwc自组装材料的制备方法
[0062]
1、xsg自组装
[0063]
(1)溶剂对xsg自组装影响
[0064]
准确称取1mg的xsg五份,其中四份分别溶解在200μl的甲醇、100μl的四氢呋喃(thf)、100μl的1,1,1,3,3,3-六氟-2-丙醇(hfp)、50μl的二甲亚砜(dmso)中,再分别对应加入800μl、900μl、900μl、950μl的超纯水,振荡器混匀后,静置2小时,获得xsg的自组装体,分别移取含自组装体的溶液至玻璃板上,待其自然晾干后,通过荧光显微镜测试xsg在不同溶剂体系中的自组装形貌,如图1(a,c-e):a甲醇/水(v/v:2/8)、c thf/水(v/v:1/9)、dhfp/水(v/v:1/9)、e dmso(v/v:0.5/9.5)。1份溶解于6ml的超纯水(水浴锅加热80摄氏度1小时),自然冷却至室温并且静置3小时,获得xsg的自组装体,荧光显微镜测试其自组装情况,如图1(b)。
[0065]
如图1所示,xsg在甲醇/水和纯水两种溶剂体系中可通过自组装形成结构均匀的纤维状纳米材料,且均表现为绿色荧光。在其它溶剂体系中自组装体结构较为复杂,无序状态较多。因此,xsg的自组装适宜的溶剂体系为甲醇/水或纯水。
[0066]
(2)xsg在甲醇和水混合溶剂中组装过程
[0067]
在室温下,准确称取1mg的xsg溶解到200μl的甲醇溶剂中,待完全溶解之后,加入800μl的超纯水,采用振荡器混合含xsg的甲醇/超纯水溶液,分别在静置0min、30min、2h后分别移取溶液至玻璃板上和硅片上,放入冷冻干燥机中冻干,通过荧光显微镜(玻璃板上的样品)和超高分辨冷场扫描电子显微镜(硅片上的样品)测试其形貌。
[0068]
如图2所示,当水加入到含xsg的甲醇溶液中时,由于xsg在水中的溶解度较差,导致xsg立即通过自组装形成细小纤维球状纳米材料(图2a,2d),随着时间的推移,这种细小的纤维球相互缠绕成更粗的棒状(图2b和图2e),最后组装形成结构均匀的纳米棒状结构(图2c和图2f),其截面图(图2g)表明它是实心棒状结构。
[0069]
2、fsg的自组装
[0070]
(1)溶剂对fsg自组装影响
[0071]
准确称取1mg的fsg五份,分别溶解在200μl的甲醇、100μl的四氢呋喃(thf)、100μl的异丙醇、100μl的1,1,1,3,3,3-六氟-2-丙醇(hfp)、50μl的二甲亚砜(dmso)中,再分别对应加入800μl、900μl、900μl、900μl、950μl的超纯水,振荡器混匀后,静置2小时,获得fsg的自组装体,分别移取含自组装体的溶液至玻璃板上,待其自然晾干后,通过荧光显微镜测试其自组装情况,如图3(a-e):a甲醇/水(v/v:2/8)、b thf/水(v/v:1/9)、c异丙醇/水(v/v:1/9)、dhfp/水(v/v:1/9)、e dmso(v/v:0.5/9.5)。
[0072]
如图3所示,fsg在异丙醇/水溶剂体系中无法通过自组装形成结构均匀的纳米材料,在其它溶剂体系中均可形成具有绿色荧光性质的纳米纤维材料,并且fsg形成的纤维较xsg形成的纤维更加细小。
[0073]
(2)fsg在甲醇和水混合溶剂中组装过程
[0074]
在室温下,准确称取1mg的fsg溶解到200μl的甲醇溶剂中,待完全溶解之后,加入800μl的超纯水,采用振荡器混合含fsg的甲醇/超纯水溶液,分别在静置0min、30min、2h后分别移取溶液至玻璃板上和硅片上,放入冷冻干燥机中冻干,通过荧光显微镜(玻璃板上的样品)和超高分辨冷场扫描电子显微镜(硅片上的样品)测试其形貌。
[0075]
如图4所示,当水加入到含fsg的甲醇溶液中时,由于fsg在水中的溶解度较差,导致fsg立即通过自组装形成比xsg更为细小纤维球状纳米材料(图4a,4d),随着时间的推移,这种细小的纤维球相互缠绕成更粗的棒状(图4b和图4e),最后组装形成结构均匀的纳米纤维状结构(图4c和图4f),其截面图(图4g)表明它是实心棒状结构。
[0076]
3、xwc的自组装
[0077]
(1)溶剂对xwc自组装影响
[0078]
准确称取1mg的xwc四份,分别溶解在200μl的甲醇、200μl的乙腈、50μl的dmso、50μl的n,n-二甲基甲酰胺(dmf)中,再分别对应加入800μl、800μl、950μl、950μl的超纯水,振荡器混匀后,静置6小时,获得xwc的自组装体,取含自组装体的溶液点到玻璃板上,待其自然晾干后,通过荧光显微镜测试xwc在不同溶剂体系中的自组装形貌,如图5(a-d):a甲醇/水(v/v:2/8)、b乙腈/水(v/v:2/8)、c dmso/水(v/v:0.9/9.5)、ddmf/水(v/v:0.5/9.5)。
[0079]
如图5所示,溶剂对xwc的组装影响较大,在甲醇和水混合体系中,xwc可形成结构均匀的纳米棒状结构,在乙腈和水混合溶剂体系中则形成宽扁的棒状结构。在极性较大的dmso和dmf体系中则形成非常细小的丝状结构。
[0080]
(2)xwc在甲醇和水混合溶剂体系中组装形貌研究
[0081]
在室温下,准确称取1mg的xwc溶解到200μl的甲醇溶剂中,待完全溶解之后,加入800μl的超纯水,振荡器混合,静置6小时后,获得xwc的自组装体,取含自组装体的溶液点到玻璃板上,放入冷冻干燥机中冻干,荧光显微镜测试其自组装情况,如图6a。取含自组装体的溶液点到硅片上,放入冷冻干燥机中冻干,通过超高分辨冷场扫描电子显微镜测试其形貌,如图6(b-c)。
[0082]
如图6a所示,xwc的自组装体也是棒状结构,其棒状结构要比xsg、fsg的更直,其截面(图6c)同样是实心棒状结构。
[0083]
4、xsg、fsg、xwc荧光性能
[0084]
分别准确称取1mg的xsg、fsg、xwc溶解到200μl的甲醇溶剂中,待完全溶解之后,再分别对应加入800μl的超纯水,振荡器混匀后,分别测试其荧光发射光谱。然后静置6小时后,待其自组装完成,再分别测试其荧光发射光谱。测试xsg的激发波长是516nm,狭缝宽度是5nm-5nm,如图7a;测试fsg的激发波长是445nm,狭缝宽度是5nm-5nm,如图7b;测试xwc的激发波长是415nm,狭缝宽度是5nm-5nm,如图7c。
[0085]
如图7a所示,xsg组装后比组装前的荧光强度增强约7.7倍,且荧光最佳发射波长发生从组装前的549nm红移至组装后的593nm;图7b显示fsg组装后比组装前的荧光强度增强约250倍,且荧光最佳发射波长发生从组装前的540nm蓝移到组装后的536nm;图7c显示xwc组装后有三个荧光发射峰出现,其中最高的荧光发射峰的强度增强约36倍,其对应的荧光发射波长发生从组装前的522nm红移到组装后549nm,此外,xwc还出现了482、518nm的荧光发射峰。
[0086]
实施例3:xsg对阳离子的检测应用
[0087]
(1)xsg对各类阳离子响应情况
[0088]
分别配制160mmol/l的cu
2+
、hg
2+
、na
+
、ag
+
、ca
2+
、k
+
、mg
2+
、zn
2+
水溶液,步骤为:分别准确称取一定量的三水合硝酸铜、三水合高氯酸汞、氯化钠、硝酸银、无水氯化钙、氯化钾、无水硫酸镁、氯化锌加入到10ml的ep管中,用移液枪取适量水溶解,超声0.5min。
[0089]
准确称取3mg的xsg两份到ep管,再加入30ml的超纯水,80℃的水浴锅加热一小时形成热溶液,移取8份3ml 0.1mg/ml的xsg水溶液到ep管,然后分别加入30μl的含cu
2+
、hg
2+
、na
+
、ag
+
、ca
2+
、k
+
、mg
2+
、zn
2+
水溶液使其最终浓度为1.6mmol/l,静置6小时,分别移取溶液至玻璃板上,利用荧光显微镜观察不同金属离子对xsg的自组装影响。图8,纯水空白(8a)、cu
2+
(8b)、hg
2+
(8c)、na
+
(8d)、ag
+
(8e)、ca
2+
(8f)、k
+
(8g)、mg
2+
(8h)、zn
2+
(8j)。
[0090]
如图8所示,cu
2+
离子和hg
2+
离子可以抑制xsg自组装,其它金属离子对xsg自组装没有影响。说明可以利用xsg自组装情况检测cu
2+
离子和hg
2+
离子。同样的,可以利用fsg、xwc在溶剂体系中自组装情况检测cu
2+
离子和hg
2+
离子。
[0091]
(2)xsg组装体分别对cu
2+
离子和hg
2+
离子响应情况
[0092]
准确称取2mg的xsg两份到ep管,再加入20ml的超纯水,80℃的水浴锅加热一小时形成热溶液,分别移取3ml 0.1mg/ml的xsg水溶液到比色皿中自组装3小时,待xsg组装完成后,测试其荧光光谱,移取部分溶液至玻璃板上,待其自然晾干后,通过荧光显微镜观察其组装形貌;然后在组装后的溶液体系中分别加入18.7μl的含hg
2+
和cu
2+
水溶液,使其最终浓度为1mmol/l。静置3小时后,测试其荧光光谱,分别移取部分溶液至玻璃板上,待其自然晾干后,通过荧光显微镜观察其组装形貌。
[0093]
如图9所示,xsg在纯水相中的自组装体在600nm左右有最大发射荧光光谱(图9d),图9a为xsg在纯水相中的自组装体形貌,图9c为加入cu
2+
的xsg的自组装体形貌,说明cu
2+
可部分瓦解xsg自组装体(图9c),导致其荧光强度降低(图9d)。图9b为加入hg
2+
的xsg的自组装体形貌,说明hg
2+
可以完全瓦解xsg自组装体(图9b),导致其荧光强度完全淬灭(图9d),因此可以利用此方法分别检测cu
2+
和hg
2+
。同样的,可以利用fsg、xwc在溶剂体系中形成组装体后检测cu
2+
离子和hg
2+
离子。
[0094]
(3)xsg对hg
2+
定量检测
[0095]
准确称取2mg的xsg两份到ep管,再加入20ml的超纯水,80℃的水浴锅加热一小时
形成热溶液,分别移取3ml 0.1mg/ml的xsg水溶液到比色皿中自组装3小时,待xsg组装完成后,测试其荧光光谱,然后分别加入10μl的不同浓度hg
2+
水溶液并确保其最终浓度为0.01~1mmol/l,静置3小时后测其荧光强度,获得图10a,从图10a中取0.01~0.1mmol/l浓度对应的荧光强度作图获得图10b。
[0096]
图10a显示hg
2+
的加入显著降低xsg自组装体的荧光强度,使其荧光最大发射峰从600nm蓝移至540nm;图10b显示随着hg
2+
浓度的增加,xsg自组装体的荧光逐渐减弱。0.01~0.1mmol/l范围内在533nm处线性拟合hg
2+
浓度和荧光值,发现二者有一定的线性关系,可通过此方法定量检测hg
2+
的浓度。同时也说明利用xsg自组装体能实现纯水相中检测cu
2+
和hg
2+
;并且能实现在纯水相中裸视检测hg
2+
以及其定量检测。
[0097]
实施例4:xsg、fsg、xwc的mtt测试
[0098]
将u87(人胶质瘤细胞系)细胞量以30000个/孔在24孔板中培养,培养基是dmem、10%的胎牛血清(fbs)、0.1%双抗(青霉素、链霉素)、5%二氧化碳,在37℃下培养24小时,然后分别加入10μl的不同浓度的xsg、fsg、xwc的dmso溶液,xsg、fsg、xwc的终浓度均分别为0.1μmol/l、1μmol/l、10μmol/l,孵育24小时,取50μl的cck-8试剂盒,加入前述u87细胞中37℃孵化2小时,多标记微孔板测试450nm的吸光度。
[0099]
图11显示,在0.1~10μmol/l浓度范围内,xsg、fsg、xwc对u87细胞的细胞毒性很低。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1