一种岩藻糖基化软骨素及其制备方法和应用
1.本发明涉及酶工程技术及合成生物学领域,特别涉及一种岩藻糖基化软骨素及其制备方法和应用。
背景技术:
2.随着人类生活水平的普遍提高和人口老龄化进程的加快,血栓性疾病日益增多,已成为一个严重影响人类生命健康的问题。肝素和低分子肝素(lmwhs)作为抗凝剂被广泛应用于血栓性疾病的治疗。肝素和低分子肝素在治疗期间有严重出血的风险,并且不能口服。因此,研究人员们一直在继续寻找更有效和更安全的抗凝药物。岩藻糖基化硫酸软骨素(fucs)是一种从海参中分离出来的结构独特的活性多糖,具有显著的抗凝和抗血栓活性,可以作为一种潜在的候选药物,其合成制备以及生物学功能研究成为了国内外科学家关注的热点。然而,由于均质寡糖的缺乏,阻碍了进一步的构效关系研究。
3.目前,fucs的获得主要有海参提取和化学法合成两种方法。提取法受海参品质和来源的限制,无法获得结构明确的fucs糖链,限制了构效关系和生物研究(如acs chem biol 2020,15(8),2232-2246.或carbohydrpolym 2017,165,7-12.或carbohydrpolym 2021,262, 117969.);化学合成fucs近年来得到了长足发展,但受糖链复杂性影响,依然存在步骤繁琐、收率低等问题,无法做到经济高效合成(如angew chem int ed engl 2018,57(39), 12880-12885.或j org chem 2020,85,24,15908
–
15919.)。
4.fucs糖链结构是由硫酸化修饰的二糖重复单元与glca o-3位分支修饰岩藻糖残基构成,其二糖重复单元主要由糖醛酸(葡萄糖醛酸glca)和n-乙酰氨基半乳糖(galnac)通过β糖苷键连接构成。不同物种来源的fucs在硫酸化位点及岩藻糖基化分支的数目上存在差异,目前现有技术中尚未有酶法合成fucs寡糖片段的相关报道,鉴于此,特提出本发明。
技术实现要素:
5.本发明克服了现有技术中存在的不足,提供了一种岩藻糖基化软骨素及其制备方法和应用。
6.本发明的第一方面提供了一种岩藻糖基化软骨素的制备方法,所述的方法包括如下步骤:
7.将l-岩藻糖基转移酶与底物gdp-l-岩藻糖和软骨素寡糖混合,酶促反应,得到岩藻糖基化软骨素。
8.进一步地,所述软骨素寡糖中可岩藻糖基化的glca与gdp-l-岩藻糖(鸟苷二磷酸岩藻糖)的摩尔比为0.5-2:1-4,优选地,所述摩尔比为0.5-1.5:1-3.5,更优选地,所述摩尔比为 1:1-3.5(如1:1、1:1.5、1:2、1:2.5、1:3、1:3.5)。
9.在本发明的一个具体实施方式中,所述软骨素寡糖中可岩藻糖基化的glca与gdp-l
‑ꢀ
岩藻糖(鸟苷二磷酸岩藻糖)的摩尔比为1:2。
10.进一步地,所述反应的ph为6.5-8.5,优选地,所述反应的ph为7-8,更优选地,所述
反应的ph为7.5。
11.进一步地,所述反应的温度为30-45℃,优选的,所述反应的温度为35-40℃,更优选的,所述反应的温度为37℃。
12.进一步地,所述反应的时间为10-30h,优选的,所述反应的时间为10-25h,更优选的,所述反应的时间为12-24h。
13.进一步地,所述l-岩藻糖基转移酶的浓度为0.1-2mg/ml,优选的,所述l-岩藻糖基转移酶的浓度为0.5-1.5mg/ml,更优选的,所述l-岩藻糖基转移酶的浓度为1mg/ml。
14.进一步地,所述的软骨素寡糖具有如下结构:
[0015][0016]
进一步地,所述n1为选自1-10的整数(如1、2、3、4、5、6、7、8、9、10)。
[0017]
优选地,所述的n1为选自1-5的整数,更优选地,所述的n1为选自1-3的整数。
[0018]
在本发明的一个具体实施方式中,所述的软骨素寡糖选自如下结构:
[0019]
[0020][0021]
进一步地,所述l-岩藻糖基转移酶的核苷酸序列如seq id no:1或seq id no:2 所示,氨基酸序列如seq id no:3或seq id no:4所示;
[0022]
进一步地,所述的l-岩藻糖基转移酶bfα1,3ft的核苷酸序列如seq id no:1所示,氨基酸序列如seq id no:3所示;
[0023]
进一步地,所述的l-岩藻糖基转移酶hpα1,3ft s45f v30g的核苷酸序列如seq id no: 2所示,氨基酸序列如seq id no:4所示。
[0024]
进一步地,所述的l-岩藻糖基转移酶选自α-1,2-岩藻糖基转移酶或α-1,3-岩藻糖基转移酶中的一种。
[0025]
优选地,所述的l-岩藻糖基转移酶为α-1,3-岩藻糖基转移酶。
[0026]
优选地,所述的l-岩藻糖基转移酶选自:seq id no:3-4中任一项所表示的多肽、seqid no3-4中任一项所表示的多肽的功能性变体、seq id no:3-4中的任一项所表示的多肽的功能性片段以及seq id no:3-4中任一项所表示的多肽的功能性片段的功能性变体。
[0027]
进一步地,所述l-岩藻糖基转移酶的来源为:脆弱拟杆菌(bacteroides fragilis)、幽门螺杆菌(helicobacter pylori)、霍乱弧菌(vibriocholera)、胆型螺杆菌(h.bilis)、朱奈德螺杆菌 (h.cinaede)、卵形拟杆菌(bacteroides ovatus)和普通拟杆菌(bacteroides vulgatus)中的一种,优选地,所述l-岩藻糖基转移酶的来源为脆弱拟杆菌(bacteroides fragilis)和/或幽门螺杆菌 (helicobacter pylori)。
[0028]
在本发明的一个具体实施方式中,所述的l-岩藻糖基转移酶为bfα1,3ft(来源于脆弱拟杆菌,bacteroides fragilis)。
[0029]
在本发明的一个具体实施方式中,所述的l-岩藻糖基转移酶为hpα1,3ft(来源于幽门螺杆菌,helicobacter pylori)。
[0030]
在本发明的一个具体实施方式中,所述的l-岩藻糖基转移酶为hpα1,3ft s45f v30g突变体,其催化活性有所提高。
[0031]
bfα1,3ft可识别寡糖内所有的d-galnac1-4-β-d-glca二糖单元并在glca o-3位进行岩藻糖基化修饰,而hpα1,3ft仅可识别非还原端为d-galnac1-4-β-d-glca结构的寡糖并且仅对其非还原端的glca o-3位进行单位点的岩藻糖基化修饰。bfα1,3ft催化识别非还原端为 d-glca1-3-β-d-galnac结构的寡糖时,非还原端大于等于两个糖未经岩藻糖基化修饰,可由软骨素合成酶催化其继续延伸,并根据需要在特定位置进一步进行岩藻糖基化修饰。
[0032]
在本发明的一个具体实施方式中,所述的hpα1,3ft s45f v30g突变体可识别的软骨素寡糖结构如式(ⅰ)所示:
[0033][0034]
在本发明的一个具体实施方式中,所述的hpα1,3ft s45f v30g突变体可识别的软骨素寡糖的结构分别如式(iv)、(vi)、(
ⅷ
)所示:
[0035][0036]
在本发明的一个具体实施方式中,所述的hpα1,3ft s45f v30g突变体催化合成的单一位点岩藻糖基化修饰的软骨素寡糖的结构分别如式(
ⅸ
)、(x)、(xi)所示:
[0037][0038]
在本发明的一个具体实施方式中,所述bfα1,3ft可识别的软骨素寡糖结构分别如式(ⅰ) 和(ⅱ)所示:
[0039][0040]
在本发明的一个具体实施方式中,所述bfα1,3ft可识别的软骨素寡糖结构分别如式(iv)、 (v)、(vi)、(vii)、(viii)所示:
[0041]
[0042][0043]
在本发明的一个具体实施方式中,所述bfα1,3ft催化合成的岩藻糖基化软骨素寡糖结构分别如式(
ⅸ
)、(
ⅻ
)、(xiii)、(xiv)、(xv)所示:
[0044]
[0045][0046]
进一步地,所述的制备方法还包括分离、纯化的步骤。
[0047]
进一步地,当岩藻糖基化软骨素寡糖的非还原端大于等于两个糖未岩藻糖基化修饰,软骨素合成酶pmcs可催化主链进一步延伸,并根据需要在特定位置由bfα1,3ft或 hpα1,3fts45f v30g催化进一步岩藻糖基化修饰,合成结构确定、岩藻糖基化程度确定的软骨素寡糖。
[0048]
进一步地,所述l-岩藻糖基转移酶hpα1,3ft s45f v30g催化非还原端结构为 d-galnac1-4-β-d-glca的glca o-3位进行单位点的岩藻糖基化修饰。
[0049]
进一步地,所述l-岩藻糖基转移酶bfα1,3ft催化结构为d-galnac1-4-β-d-glca的所有 glca o-3位进行岩藻糖基化修饰。进一步地,所述的延伸岩藻糖基化软骨素主链的步骤包括将所述主链与软骨素合成酶pmcs、糖核苷酸混合,反应。
[0050]
进一步地,所述的糖核苷酸选自:udp-galnac、udp-glca。
[0051]
在本发明的一个实施方式中,所述岩藻糖基化软骨素的制备方法包括如下步骤:首先使用软骨素合成酶延伸岩藻糖基化软骨素的主链,然后使用l-岩藻糖基转移酶hpα1,3ft s45f v30g或bfα1,3ft催化特定位点的岩藻糖基化修饰。
[0052]
在本发明的一个实施方式中,所述岩藻糖基化软骨素的制备方法包括如下步骤:首先使用软骨素合成酶延伸岩藻糖基化软骨素的主链,然后在非还原端结构为 d-galnac1-4-β-d-glca的glca o-3位使用l-岩藻糖基转移酶hpα1,3ft s45f v30g催化其进一步进行单位点的岩藻糖基化修饰。
[0053]
在本发明的一个实施方式中,所述岩藻糖基化软骨素的制备方法包括如下步骤:首先使用软骨素合成酶延伸岩藻糖基化软骨素的主链,然后在结构为d-galnac1-4-β-d-glca的所有glca o-3位使用l-岩藻糖基转移酶bfα1,3ft催化其进一步岩藻糖基化修饰。
[0054]
在本发明的一个具体实施方式中,可由软骨素合成酶pmcs进一步延伸的岩藻糖基化软骨素主链的结构分别如(
ⅻ
)、(xiv)所示:
[0055][0056]
在本发明的一个具体实施方式中,所述岩藻糖基化软骨素主链延伸后的结构分别如 (xvi)、(xvii)、(xviii)、(xix)所示:
[0057][0058][0059]
在本发明的一个具体实施方式中,使用软骨素合成酶延伸岩藻糖基化软骨素主链
的方法包括如下步骤:使用软骨素合成酶pmcs催化岩藻糖基化软骨素(
ⅻ
)进一步进行岩藻糖基化修饰,合成岩藻糖基化软骨素(xvi)。
[0060]
在本发明的一个具体实施方式中,使用软骨素合成酶延伸岩藻糖基化软骨素主链的方法包括如下步骤:使用软骨素合成酶pmcs催化岩藻糖基化软骨素(xvi)进一步进行岩藻糖基化修饰,合成岩藻糖基化软骨素(xviii)。
[0061]
在本发明的一个具体实施方式中,使用软骨素合成酶延伸岩藻糖基化软骨素主链的方法包括如下步骤:使用软骨素合成酶pmcs催化岩藻糖基化软骨素(xviii)进一步进行岩藻糖基化修饰,合成岩藻糖基化软骨素(xix)。
[0062]
在本发明的一个具体实施方式中,使用软骨素合成酶延伸岩藻糖基化软骨素主链的方法包括如下步骤:使用软骨素合成酶pmcs催化岩藻糖基化软骨素(xiv)进一步进行岩藻糖基化修饰,合成岩藻糖基化软骨素(xvii)。
[0063]
进一步地,所述的l-岩藻糖基转移酶hpα1,3fts45f v30g可识别延伸后的岩藻糖基化软骨素,催化其进一步进行岩藻糖基化修饰。
[0064]
在本发明的一个具体实施方式中,所述的岩藻糖基化软骨素的制备方法包括如下步骤:使用l-岩藻糖基转移酶hpα1,3fts45f v30g催化岩藻糖基化软骨素(xⅵ)进一步进行岩藻糖基化修饰,合成岩藻糖基化软骨素(xⅲ)。
[0065]
在本发明的一个具体实施方式中,所述的岩藻糖基化软骨素的制备方法包括如下步骤:使用l-岩藻糖基转移酶hpα1,3fts45f v30g催化岩藻糖基化软骨素(xvii)进一步进行岩藻糖基化修饰,合成岩藻糖基化软骨素(xv)。
[0066]
在本发明的一个具体实施方式中,所述的岩藻糖基化软骨素的制备方法包括如下步骤:使用l-岩藻糖基转移酶hpα1,3fts45f v30g催化岩藻糖基化软骨素(x
ⅸ
)进一步进行岩藻糖基化修饰,合成岩藻糖基化软骨素(xx)。
[0067]
进一步地,所述的l-岩藻糖基转移酶bfα1,3ft可识别延伸后的岩藻糖基化软骨素,催化其进一步进行岩藻糖基化修饰。
[0068]
在本发明的一个具体实施方式中,所述的岩藻糖基化软骨素的制备方法包括如下步骤:使用l-岩藻糖基转移酶bfα1,3ft催化岩藻糖基化软骨素(x
ⅷ
)进一步进行岩藻糖基化修饰,合成岩藻糖基化软骨素(xiv)。
[0069]
在本发明的一个具体实施方式中,所述的岩藻糖基化软骨素的制备方法包括如下步骤:使用l-岩藻糖基转移酶bfα1,3ft催化岩藻糖基化软骨素(xix)进一步进行岩藻糖基化修饰,合成岩藻糖基化软骨素(xv)。
[0070]
进一步地,所述的软骨素寡糖的制备方法包括如下步骤:将软骨素合成酶与供体底物和受体底物混合,反应,得到软骨素寡糖。
[0071]
进一步地,所述的供体底物(即糖核苷酸)选自:udp-galnac、udp-glca。
[0072]
进一步地,所述的受体底物选自:galnac。
[0073]
本发明所述的udp-galnac:中文全称为udp-n-乙酰半乳糖胺,其作用是为软骨素寡糖或软骨素多糖的合成提供活化的乙酰半乳糖胺供体(供体底物)。
[0074]
本发明所述的udp-glca:中文全称为udp-葡萄糖醛酸,其作用是为软骨素寡糖或软骨素多糖的合成提供活化的葡萄糖醛酸供体(供体底物)。
[0075]
进一步地,所述的单糖galnac与糖核苷酸的摩尔比为0.5-2:1-5,优选地,所述的
软骨素寡糖与糖核苷酸的摩尔比为0.5-1.5:1-5(如0.5:1-5、0.6:1-5、0.7:1-5、0.8:1-5、0.9:1-5、1:1-5、 1.1:1-5、1.2:1-5、1.3:1-5、1.4:1-5、1.5:1-5),更优选地,所述的软骨素寡糖与糖核苷酸的摩尔比为1:1-5(如1:1、1:1.5、1:2、1:2.5、1:3、1:3.5、1:4、1:5)。
[0076]
在本发明的一个具体实施方式中,所述的软骨素寡糖受体与糖核苷酸的摩尔比为 1:1.5-1:2。
[0077]
进一步地,所述的软骨素合成酶来源于:多杀巴斯德杆菌(pasteurellamultocida)、大肠杆菌(escherichia coli)、尿放线杆菌(actinobacillusureae)。
[0078]
进一步地,所述方法还包括分离的步骤。
[0079]
进一步地,所述的分离选自:离子交换树脂、分子筛、澄清、超滤、纳米过滤、反渗透、微滤、活性木炭或碳处理、切向流高效过滤、切向流超滤、亲和色谱、离子交换色谱、疏水相互作用色谱和/或凝胶过滤和配体交换色谱中的一种。
[0080]
进一步地,所述的分子筛选自:聚丙烯酰胺分子筛(如bio-gel p2到p300)、琼脂糖分子筛、葡聚糖分子筛。
[0081]
进一步地,所述的离子交换树脂为阴离子交换树脂,所述的阴离子交换树脂为强碱性阴离子交换树脂或弱碱性阴离子交换树脂,优选地,所述的阴离子交换树脂为强碱性阴离子交换树脂。
[0082]
进一步地,所述的强碱性阴离子交换树脂为凝胶型强碱性阴离子交换树脂。
[0083]
在本发明的一个具体实施方式中,所述的分离为阴离子交换树脂。
[0084]
在本发明的一个具体实施方式中,所述的分离为强碱性阴离子交换树脂。
[0085]
在本发明的一个具体实施方式中,所述的分离为分子筛。
[0086]
在本发明的一个具体实施方式中,所述的分离为聚丙烯酰胺分子筛。
[0087]
在本发明的一个具体实施方式中,所述的分离为bio-gel p2分子筛。
[0088]
进一步地,所述方法还包括纯化的步骤。
[0089]
进一步地,所述的纯化包括使用碱、盐、缓冲溶液或酸的适当稀释的溶液洗涤软骨素寡糖的步骤。
[0090]
进一步地,所述的纯化还包括使用活性木炭或碳,使用木炭,纳米过滤,超滤或离子交换,使用醇,使用含水醇混合物进行结晶,蒸发,浓缩、沉淀,干燥的步骤。
[0091]
进一步地,所述的浓缩选自:常压浓缩、减压浓缩、薄膜浓缩、多效浓缩,所述干燥选自:冷冻干燥、常压干燥、减压干燥、沸腾干燥、喷雾干燥、红外线干燥、微波干燥。
[0092]
在本发明的一个具体实施方式中,所述的干燥为冷冻干燥。
[0093]
进一步地,所述的岩藻糖基化软骨素,其具有如下结构:
[0094][0095]
在本发明的一个具体实施方式中,所述的岩藻糖基化软骨素具有如下结构:
[0096]
[0097]
[0098][0099]
本发明的第二方面提供了一种岩藻糖基化软骨素,其具有如下结构:
[0100][0101]
在本发明的一个具体实施方式中,所述的岩藻糖基化软骨素具有如下结构:
[0102]
[0103]
[0104][0105]
本发明的第三方面提供了两种岩藻糖基转移酶,所述岩藻糖基转移酶的核苷酸序列如seq id no:1或seq id no:2所示,氨基酸序列如seq id no:3或seq id no: 4所示。
[0106]
本发明的第四方面提供了一种重组载体,所述重组载体是由在质粒载体中插入如第三方面所述的如seq id no:1或seq id no:2所示的岩藻糖基转移酶的核苷酸序列构建得到的。
[0107]
进一步地,所述的载体为病毒载体或非病毒载体。在本发明的一个实施方式中,所述的载体为质粒载体。
[0108]
在本发明的一个实施方式中,所述的载体为pmal-c2x。
[0109]
在本发明的一个实施方式中,所述的载体为pet-41a。
[0110]
本发明的第五方面提供了一种重组细胞。
[0111]
进一步地,所述的重组细胞选自:革兰氏阳性细菌、革兰氏阴性细菌、放线菌、真菌;
[0112]
优选地,所述的革兰氏阳性细菌选自:枯草芽孢杆菌;
[0113]
优选地,所述的革兰氏阴性细菌选自:大肠杆菌;所述的放线菌为链霉菌;
[0114]
优选地,所述的真菌为酵母类、曲酶菌。
[0115]
本发明的第六方面提供了一种包含如第二方面所述的岩藻糖基化软骨素的药物组合物。
[0116]
进一步地,所述的药物组合物还包括药学上可接受的辅料。
[0117]
进一步的,所述的药学上可接受的辅料选自载体、赋形剂、稀释剂、润滑剂、润湿剂、乳化剂、防腐剂、抗氧化剂、缓冲剂、抑菌剂、使制剂与接受者的血液等渗的溶质、悬浮剂、助悬剂、增溶剂、增稠剂、稳定剂、甜味剂以及香料中的一种或两种以上的组合。
[0118]
本发明的第七方面提供了一种如第二方面所述的岩藻糖基化软骨素或如第六方面所述的药物组合物在制备抗凝血药物或岩藻糖基化硫酸软骨素中的用途。
[0119]
本发明的第八方面提供了一种如第三方面所述的岩藻糖基转移酶在合成岩藻糖基化软骨素中的应用。
[0120]
本发明的第九方面提供了如第二方面所述的一种岩藻糖基化软骨素在制备岩藻糖基化硫酸软骨素中的应用。
[0121]
本发明所述的生物酶(岩藻糖基转移酶和软骨素合成酶)来自原核生物,具有蛋白表达量高、底物适应性宽、催化效率高等优点。酶法合成过程具有高效性及高区域选择性,操作简单且安全,为岩藻糖基硫酸软骨素的工业化生产奠定了基础,解决酶法合成岩藻糖基化软骨素的瓶颈问题,提供体外多酶级联制备岩藻糖基化软骨素的方法,本发明利用酶的底物宽泛性,筛选不同来源的岩藻糖基转移酶进行底物适应性研究,开发了高效的酶法合成岩藻糖基化软骨素的方法,采用本发明的方法可对底物软骨素寡糖进行不同程度的岩藻糖基化修饰,寡糖非还原端为岩藻糖基硫酸软骨素的工业化生产奠定了基础,推动抗凝药物的开发。
附图说明
[0122]
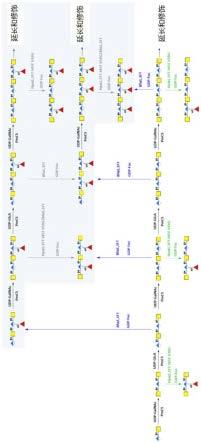
图1为岩藻糖基化软骨素的制备示意图。
具体实施方式
[0123]
为了能够更清楚地理解本发明的技术内容,特举以下实施例详细说明,其目的仅在于更好理解本发明的内容而非限制本发明的保护范围。
[0124]
本发明中所述的式(
ⅸ
)~式(xx)结构分别如下所示:
[0125]
[0126]
[0127][0128]
实施例1hpα1,3fts45fv30g催化合成单一位点岩藻糖基化修饰的软骨素寡糖
[0129]
(1)将鸟苷二磷酸岩藻糖(gdp-fuc)、软骨素三糖(iv)、mgcl2、tris-hcl配制成水溶液,反应体系中gdp-fuc、mgcl2的终浓度为20mm,软骨素三糖(iv)的终浓度为10mm,tris-hcl的终浓度为50mm,反应体系ph为7.5,然后添加l-岩藻糖基转移酶,反应12h,检测反应完成后,加入冰乙醇终止反应;将反应液离心10-20min,将上清通过bio-gelp2分子筛脱盐后,利用强碱性阴离子交换树脂介质分离纯化,再次利用bio-gelp2分子筛脱盐后,得到产物ix,转化率达到90%,其1hnmr、
13
cnmr及ms数据如下,
[0130]1hnmr(600mhz,d2o)δ5.40(d,j=4.0hz,2h,h-1
fuc
),5.22(d,j=3.8hz,1h,h-1
galnac-a
),4.69(d,j=8.5hz,1h,h-1
galnac-a
),4.57(d,j=8.0hz,1h),4.52(d,j=7.9hz,1h),4.46(dd,j=8.4,2.5hz,2h),4.29(dd,j=11.1,3.8hz,1h),4.22(d,j=3.1hz,1h),4.16-4.11(m,2h),4.02-3.89(m,11h),3.83(d,j=3.3hz,2h),3.81-3.64(m,19h),3.61-3.56(m,4h),2.05(dd,j=26.0,2.3hz,12h,cooch3,cooch3),1.25(d,j=6.6hz,6h,ch3offucose).
[0131]
13
cnmr(151mhz,d2o)δ175.42,175.40,175.06,174.92,174.62,104.01,103.85,100.00,98.31,95.17,91.19,80.77,77.73,76.73,76.67,76.62,75.22,75.18,74.95,74.91,74.22,74.19,74.16,72.06,71.54,70.25,69.25,68.42,68.13,67.71,67.53,66.66,61.50,61.26,61.05,52.24,48.83,22.47,22.22,22.01,15.37.
[0132]
esi-ms(negativemode)calcdforc
28h45
n2o
21-[m-h]-m/z745.2520,found745.2527.;
[0133]
(2)将鸟苷二磷酸岩藻糖(gdp-fuc)、软骨素五糖(vi)、mgcl2、tris-hcl配制成水溶液,反应体系中gdp-fuc、mgcl2的终浓度为20mm,软骨素五糖(vi)的终浓度为10mm,tris-hcl的终浓度为50mm,反应体系ph为7.5,然后添加l-岩藻糖基转移酶,反应12h,检测反应完成后,加入冰乙醇终止反应;将反应液离心10-20min,将上清通过bio-gelp2分子筛脱盐后,利用强碱性阴离子交换树脂介质分离纯化,再次利用bio-gelp2分子筛脱盐后,得到产物x,转化率达到86%,其1hnmr、
13
cnmr及ms数据如下,
[0134]1hnmr(600mhz,d2o)δ5.39(d,j=3.9hz,2h,h-1
fuc
),5.22(d,j=3.7hz,1h,h-1
galnac-a
),4.68(d,j=8.5hz,1h,h-1
galnac-a
),4.58-4.43(m,8h,h-1
glca-a
,h-1
galnac-b
,h-1
glca-b
,h-1
galnac-c
),4.29(dd,j=11.1,3.7hz,1h),4.20(d,j=3.1hz,1h),4.15-4.11(m,4h),4.03-3.89(m,12h),3.83-3.68(m,31h),3.67-3.54(m,9h),3.40-3.36(m,2h),2.09-2.00(m,18h,cooch3,cooch3,cooch3),1.24(d,j=6.5hz,6h,ch3offucose).
[0135]
13
cnmr(151mhz,d2o)δ175.40,175.06,174.98,174.93,174.67,174.58,104.28,104.10,104.03,100.84,99.95,98.28,95.18,91.18,80.70,80.34,79.71,77.32,76.59,76.52,76.38,75.13,74.95,74.91,74.20,73.79,73.75,72.49,72.42,72.07,71.57,
70.30,69.24,68.51,68.11,67.83, 67.60,67.53,66.62,61.50,61.26,61.08,61.04,52.31,52.24,50.88,48.91,22.48,22.45,22.22, 21.99,15.35.
[0136]
esi-ms(negative mode)calcd for c
42h66
n3o
32-[m-h]-m/z1124.3635,found 1124.3399; calcd for c
42h65
n3o
322-[m-2h]
2-m/z561.6781,found 561.6675.;
[0137]
(3)将鸟苷二磷酸岩藻糖(gdp-fuc)、软骨素七糖(viii)、mgcl2、tris-hcl配制成水溶液,反应体系中gdp-fuc、mgcl2的终浓度为20mm,软骨素七糖(viii)的终浓度为 10mm,tris-hcl的终浓度为50mm,反应体系ph为7.5,然后添加l-岩藻糖基转移酶,反应12h,检测反应完成后,加入冰乙醇终止反应;将反应液离心10-20min,将上清通过 bio-gel p2分子筛脱盐后,利用强碱性阴离子交换树脂介质分离纯化,再次利用bio-gel p2 分子筛脱盐后,得到产物xi,转化率达到90%,其1h nmr、
13
c nmr及ms数据如下,
[0138]1h nmr(600mhz,d2o)δ5.39(d,j=4.0hz,2h,h-1
fuc
),5.22(d,j=3.7hz,1h, h-1
galnac-a
),4.68(d,j=8.5hz,1h,h-1
galnac-a
),4.58-4.43(m,12h,h-1
glca-a
,h-1
galnac-b
, h-1
glca-b
,h-1
galnac-c
,h-1
glca-c
,h-1
galnac-d
),4.29(dd,j=11.1,3.8hz,1h),4.20(d,j=3.1hz, 1h),4.14-4.12(m,6h),4.02-3.88(m,13h),3.84-3.67(m,43h),3.67-3.63(m,2h),3.62-3.54(m, 8h),3.41-3.33(m,4h),2.08-2.00(m,24h,cooch3,cooch3,cooch3,cooch3),1.24(d,j= 6.5hz,6h,ch
3 of fucose).
[0139]
13
c nmr(151mhz,d2o)δ175.38,175.07,175.00,174.98,174.93,174.67,174.50,104.31, 104.29,104.11,104.04,100.87,100.81,99.94,98.28,95.18,91.18,80.72,80.32,79.75,79.66, 77.30,76.57,76.48,76.32,76.26,75.13,74.95,74.91,74.20,73.79,73.76,73.68,72.48,72.44, 72.07,72.04,71.58,70.31,69.24,68.52,68.37,68.11,67.84,67.71,67.64,67.61,67.53,66.61, 61.49,61.26,61.07,52.32,52.25,50.97,50.89,48.92,22.45,22.21,22.13,21.99,15.35.
[0140]
esi-ms(negative mode)calcd for c
56h86
n4o
432-[m-2h]
2-m/z751.2338,found 751.2213.。
[0141]
实施例2bfα1,3ft催化合成岩藻糖基化修饰的软骨素寡糖
[0142]
(1)将鸟苷二磷酸岩藻糖(gdp-fuc)、软骨素四糖(v)、mgcl2、tris-hcl配制成水溶液,反应体系中gdp-fuc、mgcl2的终浓度为20mm,软骨素四糖(v)的终浓度为10mm, tris-hcl的终浓度为50mm,反应体系ph为7.5,然后添加l-岩藻糖基转移酶bfα1,3ft,反应12h,检测反应完成后,加入冰乙醇终止反应;将反应液离心10-20min,将上清通过bio-gel p2分子筛脱盐后,利用强碱性阴离子交换树脂介质分离纯化,再次利用bio-gel p2 分子筛脱盐后,得到产物xii,其1h nmr、
13
c nmr及ms数据如下,
[0143]1h nmr(600mhz,d2o)δ5.36(d,j=3.9hz,2h,h-1
fuc
),5.17(d,j=3.7hz,1h, h-1
galnac-a
),4.63(d,j=8.5hz,1h,h-1
galnac-a
),4.53-4.41(m,6h,h-1
glca-a
,h-1
galnac-b
, h-1
glca-b
),4.24(dd,j=11.2,3.8hz,1h),4.17(d,j=3.0hz,1h),4.11-4.06(m,4h,),4.03-3.98 (m,2h),3.97-3.86(m,6h),3.79(d,j=3.3hz,2h),3.76-3.62(m,22h),3.55-3.51(m,4h), 3.47-3.41(m,4h),3.28(t,j=8.4hz,2h),1.99(dd,j=13.5,2.3hz,12h,cooch3,cooch3), 1.21(d,j=6.6hz,6h,ch
3 of fucose).
[0144]
13
c nmr(151mhz,d2o)δ175.85,175.20,175.18,174.83,174.78,174.49,103.96,103.81, 99.69,98.18,95.04,91.06,80.66,80.52,80.50,77.61,76.48,76.46,76.40,
76.08,75.14,74.84, 74.80,74.58,74.11,74.07,72.62,71.93,71.71,70.14,69.06,68.31,67.97,67.59,67.47,66.55, 61.47,61.15,60.93,59.17,52.08,50.78,48.70,22.39,22.09,21.87,15.24.
[0145]
esi-ms(negative mode)calcd for c
34h53
n2o
27-[m-h]-m/z921.2841,found 921.2821.;
[0146]
(2)将鸟苷二磷酸岩藻糖(gdp-fuc)、软骨素五糖(vi)、mgcl2、tris-hcl配制成水溶液,反应体系中gdp-fuc的终浓度为40mm,mgcl2的终浓度为20mm,软骨素五糖(vi) 的终浓度为10mm,tris-hcl的终浓度为50mm,反应体系ph为7.5,然后添加l-岩藻糖基转移酶bfα1,3ft,反应24h,检测反应完成后,加入冰乙醇终止反应;将反应液离心10-20 min,将上清通过bio-gel p2分子筛脱盐后,利用强碱性阴离子交换树脂介质分离纯化,再次利用bio-gel p2分子筛脱盐后,得到产物xiii,其1h nmr、
13
c nmr及ms数据如下,
[0147]1h nmr(600mhz,d2o)δ5.36(t,j=3.6hz,4h,,h-1
fuc-a
,h-1
fuc-b
),5.18(d,j=3.7hz, 1h,h-1
galnac-a
),4.65(d,j=8.5hz,1h,h-1
galnac-a
),4.53-4.38(m,8h,h-1
glca-a
,h-1
galnac-b
, h-1
glca-b
,h-1
galnac-c
),4.25(dd,j=11.0,3.9hz,1h),4.18(d,j=3.1hz,1h),4.12-4.04(m,4h), 4.03-3.97(m,2h),3.97-3.85(m,15h),3.8-3.78(m,4h),3.77-3.65(m,30h),3.62(dd,j=10.7, 3.2hz,2h),3.57-3.50(m,9h),2.05-1.98(m,18h,cooch3,cooch3,cooch3),1.21(dd,j= 6.6,1.9hz,12h,ch
3 of fucose-a,ch
3 of fucose-b).
[0148]
13
c nmr(151mhz,d2o)δ175.33,175.19,175.17,174.95,174.75,174.50,103.96,103.86, 103.81,99.83,99.65,98.19,98.15,95.07,91.07,81.05,80.66,77.60,76.47,76.42,75.02,74.85, 74.83,74.51,74.12,71.96,71.93,71.44,70.16,69.13,69.08,68.32,68.00,67.61,67.42,67.39, 66.56,66.52,61.49,61.41,61.17,60.94,52.13,50.66,48.72,22.39,22.35,22.11,21.88,15.25.
[0149]
esi-ms(negative mode)calcd for c
48h76
n3o
36-[m-h]-m/z 1270.4214,found 1270.3972; calcd for c
48h75
n3o
362-[m-2h]
2-m/z 634.7071,found 634.6962.;
[0150]
(3)将鸟苷二磷酸岩藻糖(gdp-fuc)、软骨素六糖(vii)、mgcl2、tris-hcl配制成水溶液,反应体系中gdp-fuc的终浓度为40mm,mgcl2的终浓度为20mm,软骨素六糖(vii) 的终浓度为10mm,tris-hcl的终浓度为50mm,反应体系ph为7.5,然后添加l-岩藻糖基转移酶bfα1,3ft,反应48h,检测反应完成后,加入冰乙醇终止反应;将反应液离心10-20min,将上清通过bio-gel p2分子筛脱盐后,利用强碱性阴离子交换树脂介质分离纯化,再次利用 bio-gel p2分子筛脱盐后,得到产物xiv,其1h nmr、ms数据如下,
[0151]1h nmr(600mhz,d2o)δ5.40(d,j=4.0hz,4h,h-1
fuc-a
,h-1
fuc-b
),5.22(d,j=3.7hz, 1h,h-1
galnac-a
),4.69(d,j=8.5hz,1h,h-1
galnac-a
),4.57-4.44(m,10h,h-1
glca-a
,h-1
galnac-b
, h-1
glca-b
,h-1
galnac-c
,h-1
glca-c
),4.29(dd,j=10.7,3.9hz,1h),4.22(d,j=2.1hz,1h), 4.16-4.12(m,4h),4.10-3.91(m,14h),3.84(s,4h),3.80-3.68(m,38h),3.60-3.56(m,8h), 3.53-3.46(m,4h),3.33(t,j=8.2hz,2h),2.07-2.01(m,18h,cooch3,cooch3,cooch3), 1.25(d,j=6.1hz,12h,ch
3 of fucose-a,ch
3 of fucose-b).
[0152]
esi-ms(negative mode)calcd for c
54h83
n3o
422-[m-2h]
2-m/z 722.7231,found 722.7092.;
[0153]
(4)将鸟苷二磷酸岩藻糖(gdp-fuc)、软骨素七糖(viii)、mgcl2、tris-hcl配制成
水溶液,反应体系中gdp-fuc的终浓度为60mm,mgcl2的终浓度为20mm,软骨素七糖 (viii)的终浓度为10mm,tris-hcl的终浓度为50mm,反应体系ph为7.5,然后添加 l-岩藻糖基转移酶bfα1,3ft,反应48h,检测反应完成后,加入冰乙醇终止反应;将反应液离心10-20min,将上清通过bio-gel p2分子筛脱盐后,利用强碱性阴离子交换树脂介质分离纯化,再次利用bio-gel p2分子筛脱盐后,得到产物xv,其1h nmr、ms数据如下,
[0154]1h nmr(600mhz,d2o)δ5.36(d,j=3.3hz,6h,h-1
fuc-a
,h-1
fuc-b
,h-1
fuc-c
),5.18(d,j= 3.5hz,1h),4.65(d,j=8.3hz,1h,h-1
galnac-a
),4.53(d,j=8.1hz,1h,h-1
galnac-a
),4.54-4.40 (m,12h,h-1
glca-a
,h-1
galnac-b
,h-1
glca-b
,h-1
galnac-c
,h-1
glca-c
,h-1
galnac-d
),4.25(d,j=11.6hz, 1h),4.18(d,j=2.7hz,1h),4.12-3.85(m,21h),3.80(m,6h),3.75-3.61(m,53h),3.55-3.52(m, 14h),2.04-1.99(m,24h,cooch3,cooch3,cooch3,cooch3),1.21(d,j=6.5hz,18h, ch
3 of fucose-a,ch
3 of fucose-b,ch
3 of fucose-c).
[0155]
esi-ms(negative mode)calcd for c
68h106
n4o
512-[m-2h]
2-m/z 897.2917,found 897.2679.。
[0156]
实施例3岩藻糖基化软骨素寡糖的主链延伸
[0157]
(1)20mm尿苷二磷酸n-乙酰氨基半乳糖(udp-galnac)、10mm岩藻糖基化软骨素寡糖受体(xii)、20mm mgcl2、50mm tris-hcl缓冲液(ph=7.5),1mg/ml软骨素合成酶的反应体系,30℃反应12h,检测反应完成后,加入冰乙醇终止反应;将反应液离心 10-20min,利用强碱性阴离子交换树脂介质分离纯化,得到产物xvi,其1h nmr、
13
c nmr 及ms数据如下,
[0158]1h nmr(600mhz,d2o)δ5.38(d,j=3.9hz,2h,h-1
fuc
),5.20(d,j=3.7hz,1h, h-1
galnac-a
),4.66(d,j=8.5hz,1h,h-1
galnac-a
),4.56-4.44(m,8h,h-1
glca-a
,h-1
galnac-b
, h-1
glca-b
,h-1
galnac-c
),4.27(dd,j=11.0,3.8hz,1h),4.20(d,j=3.1hz,1h),4.14-4.09(m,2h), 4.07-4.02(m,3h),3.98-3.85(m,10h),3.83-3.66(m,35h),3.58-3.54(m,6h),3.37-3.33(m,2h), 2.05-1.98(m,18h,cooch3,cooch3,cooch3),1.23(d,j=6.6hz,6h,ch
3 of fucose).
[0159]
13
c nmr(151mhz,d2o)δ175.21,175.19,174.97,174.87,174.81,174.63,174.52,104.16, 103.97,103.82,100.87,99.69,98.21,95.08,91.09,80.66,79.47,77.62,76.54,76.27,75.14,74.87, 74.84,74.56,74.14,74.11,73.55,72.43,71.96,71.00,70.17,69.11,68.34,68.01,67.70,67.62, 67.53,66.57,61.49,61.18,60.95,52.22,50.77,48.74,22.42,22.37,22.13,21.91,15.27.
[0160]
esi-ms(negative mode)calcd for c
42h66
n3o
32-[m-h]-m/z1124.3635,found 1124.3574; calcd for c
42h65
n3o
322-[m-2h]
2-m/z561.6781,found 561.6755.;
[0161]
(2)20mm尿苷二磷酸n-乙酰氨基半乳糖(udp-galnac)、10mm岩藻糖基化软骨素寡糖受体(xiv)、20mm mgcl2、50mm tris-hcl缓冲液(ph=7.5),1mg/ml软骨素合成酶的反应体系,30℃反应12h,检测反应完成后,加入冰乙醇终止反应;将反应液离心10-20min,利用强碱性阴离子交换树脂介质分离纯化,得到产物xvii,其1h nmr、ms数据如下,
[0162]1h nmr(600mhz,d2o)δ5.40(d,j=3.7hz,4h,h-1
fuc-a
,h-1
fuc-b
),5.22(d,j=3.7hz, 1h,h-1
galnac-a
),4.69(d,j=8.6hz,1h,h-1
galnac-a
),4.59-4.46(m,12h,h-1
glca-a
,h-1
galnac-b
, h-1
glca-b
,h-1
galnac-c
,h-1
glca-c
,h-1
galnac-d
),4.29(dd,j=11.1,3.8hz,1h),4.22(d,j=3.1hz, 1h),4.15-3.88(m,24h),3.85-3.69(m,50h),3.61-3.54(m,10h),3.37(dd,j=9.5,
7.9hz,2h),2.06-2.01(m,24h,cooch3,cooch3,cooch3,cooch3),1.25(d,j=6.6hz,12h,ch3offucose-a,ch3offucose-b).
[0163]
esi-ms(negativemode)calcdforc
62h96
n4o
472-[m-2h]
2-m/z824.2628,found824.2469.;
[0164]
(3)20mm尿苷二磷酸葡糖醛酸(udp-glca)、10mm岩藻糖基化软骨素寡糖受体(xvi)、20mmmgcl2、50mmtris-hcl缓冲液(ph=7.5),1mg/ml软骨素合成酶的反应体系,30℃反应12h,检测反应完成后,加入冰乙醇终止反应;将反应液离心10-20min,利用强碱性阴离子交换树脂介质分离纯化,得到产物xviii,其1hnmr、
13
cnmr及ms数据如下,
[0165]1hnmr(600mhz,d2o)δ5.38(d,j=4.0hz,2h,h-1
fuc
),5.19(d,j=3.8hz,1h,h-1
galnac-a
),4.66(d,j=8.5hz,1h,h-1
galnac-a
),4.54-4.44(m,10h,h-1
glca-a
,h-1
galnac-b
,h-1
glca-b
,h-1
galnac-c
,h-1
glca-c
),4.26(dd,j=11.1,3.8hz,1h),4.20-4.18(m,1h),4.15(d,j=3.1hz,2h),4.13-4.08(m,2h),4.06-4.02(m,2h),4.02-3.89(m,9h),3.82-3.65(m,37h),3.58-3.53(m,6h),3.49-3.43(m,4h),3.36-3.28(m,4h),2.03-1.99(m,18h,cooch3,cooch3,cooch3),1.23(d,j=6.6hz,6h,ch3offucose).
[0166]
13
cnmr(151mhz,d2o)δ175.79,175.14,175.13,174.87,174.85,174.80,174.50,174.46,104.16,104.05,103.97,103.82,100.73,99.68,98.19,95.07,91.06,80.65,80.21,79.59,77.61,76.49,76.44,76.18,76.17,75.99,75.17,74.88,74.83,74.55,74.12,73.55,72.60,72.37,71.94,71.69,70.16,69.08,68.33,67.99,67.58,67.51,66.57,62.36,61.48,61.17,60.98,52.11,50.91,50.76,48.72,22.39,22.11,21.88,15.25.
[0167]
esi-ms(negativemode)calcdforc
48h74
n3o
38-[m-h]-m/z1300.3956,found;calcdforc
48h73
n3o
382-[m-2h]
2-m/z649.6942,found649.6843.;
[0168]
(4)20mm尿苷二磷酸葡糖醛酸(udp-glca)、10mm岩藻糖基化软骨素寡糖受体(xviii)、20mmmgcl2、50mmtris-hcl缓冲液(ph=7.5),1mg/ml软骨素合成酶的反应体系,30℃反应12h,检测反应完成后,加入冰乙醇终止反应;将反应液离心10-20min,利用强碱性阴离子交换树脂介质分离纯化,得到产物xix,其1hnmr、
13
cnmr及ms数据如下,
[0169]1hnmr(600mhz,d2o)δ5.36(d,j=3.5hz,2h,h-1
fuc
),5.18(d,j=3.8hz,1h,h-1
galnac-a
),4.64(d,j=8.3hz,1h,h-1
galnac-a
),4.54-4.42(m,12h,h-1
glca-a
,h-1
galnac-b
,h-1
glca-b
,h-1
galnac-c
,h-1
glca-c
,h-1
galnac-d
),4.25(dd,j=11.1,3.7hz,1h),4.19-4.14(m,2h),4.12-4.08(m,4h),4.05-3.83(m,15h),3.80-3.65(m,46h),3.57-3.52(m,8h),3.35-3.31(m,4h),2.03-1.98(m,24h,cooch3,cooch3,cooch3,cooch3),1.21(d,j=6.6hz,6h,ch3offucose).
[0170]
13
cnmr(151mhz,d2o)δ174.95,174.90,174.86,174.82,174.52,174.37,174.20,104.23,104.17,100.92,100.77,99.71,98.21,95.09,91.09,80.66,80.60,80.23,79.63,79.46,77.61,76.44,76.06,75.98,75.14,74.85,74.56,74.13,74.09,73.56,72.36,71.95,70.97,70.18,69.10,68.34,68.01,67.73,67.69,67.64,67.51,66.58,62.37,61.48,61.18,60.96,60.94,52.23,52.14,50.89,50.77,48.74,45.86,22.40,22.38,22.36,22.13,21.90,15.26.
[0171]
esi-ms(negativemode)calcdforc
56h86
n4o
432-[m-2h]
2-m/z751.2338,found
751.2199.。
[0172]
实施例4岩藻糖基化软骨素寡糖主链延伸后的按需岩藻糖基化修饰
[0173]
(1)将鸟苷二磷酸岩藻糖(gdp-fuc)、岩藻糖基化软骨素寡糖受体(xvi)、mgcl2、tris-hcl配制成水溶液,反应体系中gdp-fuc的终浓度为20mm、mgcl2的终浓度为20mm,岩藻糖基化软骨素寡糖(xvi)的终浓度为10mm,tris-hcl的终浓度为50mm,反应体系ph为7.5,然后添加l-岩藻糖基转移酶hpα1,3fts45fv30g,反应12h,检测反应完成后,加入冰乙醇终止反应;将反应液离心10-20min,将上清通过bio-gelp2分子筛脱盐后,利用强碱性阴离子交换树脂介质分离纯化,再次利用bio-gelp2分子筛脱盐后,得到产物xiii;
[0174]
(2)将鸟苷二磷酸岩藻糖(gdp-fuc)、岩藻糖基化软骨素寡糖受体(xvii)、mgcl2、tris-hcl配制成水溶液,反应体系中gdp-fuc的终浓度为20mm、mgcl2的终浓度为20mm,岩藻糖基化软骨素寡糖(xvii)的终浓度为10mm,tris-hcl的终浓度为50mm,反应体系ph为7.5,然后添加l-岩藻糖基转移酶hpα1,3fts45fv30g,反应12h,检测反应完成后,加入冰乙醇终止反应;将反应液离心10-20min,将上清通过bio-gelp2分子筛脱盐后,利用强碱性阴离子交换树脂介质分离纯化,再次利用bio-gelp2分子筛脱盐后,得到产物xv;
[0175]
(3)将鸟苷二磷酸岩藻糖(gdp-fuc)、岩藻糖基化软骨素寡糖受体(xviii)、mgcl2、tris-hcl配制成水溶液,反应体系中gdp-fuc的终浓度为20mm、mgcl2的终浓度为20mm,岩藻糖基化软骨素寡糖(xviii)的终浓度为10mm,tris-hcl的终浓度为50mm,反应体系ph为7.5,然后添加l-岩藻糖基转移酶bfα1,3ft,检测反应完成后,加入冰乙醇终止反应;将反应液离心10-20min,将上清通过bio-gelp2分子筛脱盐后,利用强碱性阴离子交换树脂介质分离纯化,再次利用bio-gelp2分子筛脱盐后,得到产物xiv;
[0176]
(4)将鸟苷二磷酸岩藻糖(gdp-fuc)、岩藻糖基化软骨素寡糖受体(xix)、mgcl2、tris-hcl配制成水溶液,反应体系中gdp-fuc的终浓度为40mm、mgcl2的终浓度为20mm,岩藻糖基化软骨素寡糖(xix)的终浓度为10mm,tris-hcl的终浓度为50mm,反应体系ph为7.5,然后添加l-岩藻糖基转移酶bfα1,3ft,检测反应完成后,加入冰乙醇终止反应;将反应液离心10-20min,将上清通过bio-gelp2分子筛脱盐后,利用强碱性阴离子交换树脂介质分离纯化,再次利用bio-gelp2分子筛脱盐后,得到产物xv;
[0177]
(5)将鸟苷二磷酸岩藻糖(gdp-fuc)、岩藻糖基化软骨素寡糖受体(xix)、mgcl2、tris-hcl配制成水溶液,反应体系中gdp-fuc的终浓度为20mm、mgcl2的终浓度为20mm,岩藻糖基化软骨素寡糖(xix)的终浓度为10mm,tris-hcl的终浓度为50mm,反应体系ph为7.5,然后添加l-岩藻糖基转移酶hpα1,3fts45fv30g,反应12h,检测反应完成后,加入冰乙醇终止反应;将反应液离心10-20min,将上清通过bio-gelp2分子筛脱盐后,利用强碱性阴离子交换树脂介质分离纯化,再次利用bio-gelp2分子筛脱盐后,得到产物xx,其1hnmr和ms数据如下,
[0178]1hnmr(600mhz,d2o)δ5.40(d,j=3.7hz,4h,h-1
fuc-a
,h-1
fuc-b
),5.22(d,j=3.7hz,1h,h-1
galnac-a
),4.69(d,j=8.6hz,1h,h-1
galnac-a
),4.59-4.46(m,12h,h-1
glca-a
,h-1
galnac-b
,h-1
glca-b
,h-1
galnac-c
,h-1
glca-c
,h-1
galnac-d
),4.29(dd,j=11.1,3.8hz,1h),4.22(d,j=3.1hz,1h),4.15-3.88(m,24h),3.85-3.69(m,50h),3.61-3.54(m,10h),3.37(dd,j=9.5,7.9hz,2h),2.06-2.01(m,24h,cooch3,cooch3,cooch3,cooch3),1.25(d,j=6.6hz,12h,ch3offucose-a,ch3offucose-b).
[0179]
esi-ms(negative mode)calcd for c
62h96
n4o
472-[m-2h]
2-m/z 824.2628,found 824.2469.。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1