一种荧光金纳米簇材料的制备方法及其产品和应用
1.本发明属于酸性磷酸酶(acp)检测技术领域,涉及一种荧光金纳米簇材料的制备方法及其产品和应用。
背景技术:
2.酸性磷酸酶(acp)是在哺乳动物和植物中发现的一种常见的酶,它可以水解磷酸酯键将磷酸基团从底物中解离。血清中酸性磷酸酶(acp)的含量被认为是相关病理诊断的主要因素,它的异常表达会导致一些常见疾病,如前列腺癌、肝硬化、溶血性贫血、慢性肾炎等。由于酸性磷酸酶(acp)具有重要的临床意义,因此有必要建立一种简便、灵敏的acp检测方法。目前已报道的酸性磷酸酶(acp)的检测方法包括电化学法、荧光法、比率荧光法、比色法、色谱法等。荧光检测法由于其灵敏度高、选择性强、使用简单等优点,已被广泛应用于体内分子的检测。
3.过氧化物酶是一种氧化还原酶,分布于体液或细胞中,可催化h2o2直接氧化酚类或胺类化合物。与天然酶易受ph和温度影响而活性变化的缺点相比,模拟酶结构简单,化学性质稳定,具有酶的高效、低成本、易得等优点。随着纳米技术和生物技术的发展,各种纳米材料已被证明具有模拟过氧化物酶的活性,可用作纳米酶,如介孔氧化镍纳米花(nionfs)、c-dots/fe3o4、fes2纳米粒子、石墨烯量子点负载的cuo纳米针(gqds-cuo)等,已被证明具有类过氧化物活性。然而,这些材料中的大多数都需要复杂的合成方法和严格的实验条件。相反,具有类过氧化物酶性质和荧光特性的金纳米簇由于其合成方式简单且温和,已被广泛应用于化学物质的检测。铈(ce
3+
)是重要的稀土元素(rees)之一,它很容易从4f电离并释放出电子,具有独特的催化、磁性和电子特性。deng等将ce
3+
添加到具有过氧化物酶活性的金纳米颗粒中以增强金纳米粒子的催化活性。而ce
4+
通常用于合成具有强氧化性的纳米酶。lucaartiglia等报道了tio2@ceox可以催化h2o2将ce
3+
氧化为ce
4+
、的氧化还原机理以及不同比例的ce
3+
和ce
4+
对tio2@ceox的催化活性有不同程度的影响,甚至优于天然的过氧化物酶。
4.荧光共振能量转移(fret)作为一种灵敏的分析方法得到了广泛的应用,为分析方法的发展提供了更多的可能性。shi等合成了具有模拟过氧化物酶活性和荧光性质的fe/eu-mof材料,能够催化h2o2氧化tmb生成oxtmb,oxtmb在652nm处有较强的紫外吸收,因此以fe/eu-mof为供体,oxtmb为受体构建fret机制。ni和他的同事基于fret机制使用具有模拟过氧化物酶活性和荧光的金纳米团簇(bsa-auncs)开发了一种比色荧光双通道检测碱性磷酸酶(alp)的方法。双猝灭也是降低背景信号、提高灵敏度和选择性的好方法。zhang和他的同事开发了一种荧光双猝灭方法,用于选择性检测细胞内so2,以克服长期暴露于半胱氨酸的干扰。
5.因此,探索与荧光共振能量转移(fret)和双猝灭响应相结合的高效双“增强”检测方法在提高灵敏度和选择性方面具有很大的潜力。
技术实现要素:
6.有鉴于此,本发明的目的之一在于提供一种荧光金纳米簇材料的制备方法;本发明的目的之二在于提供一种荧光金纳米簇材料;本发明的目的之三在于提供一种荧光金纳米簇材料在酸性磷酸酶(acp)方面的应用。
7.为达到上述目的,本发明提供如下技术方案:
8.1.一种荧光金纳米簇材料的制备方法,所述制备方法包括如下步骤:
9.将三水合氯金酸(haucl
4-3h2o)水溶液加入到牛血清蛋白(bsa)水溶液中混合后,在20-50℃的水浴中搅拌,加入碱溶液调节溶液的ph为10-11,持续避光搅拌10-18h,用截流膜和超纯水透析去除未反应的原料,即可得到荧光金纳米簇材料((bsa-auncs))。
10.优选的,所述三水合氯金酸(haucl
4-3h2o)和牛血清蛋白(bsa)的摩尔质量比为1:3-8,mol:g。
11.优选的,所述三水合氯金酸(haucl
4-3h2o)通过含有浓度为8-12mm的三水合氯金酸(haucl
4-3h2o)水溶液的形式添加;
12.所述牛血清蛋白(bsa)水溶液中牛血清蛋白(bsa)的质量浓度为40-80mg/ml。
13.进一步优选的,所述碱溶液为氢氧化钠溶液。
14.优选的,所述截流膜的分子量为3kda。
15.2.根据上述制备方法制备的荧光金纳米簇材料。
16.3.上述荧光金纳米簇材料在制备酸性磷酸酶(acp)检测探针方面的应用。
17.本发明的有益效果在于:本发明公开了一种以牛血清白蛋白作为还原剂和保护剂的荧光金纳米簇材料(bsa-auncs)的制备方法,制备得到的产物具有过氧化物酶模拟活性和荧光特性,能够用于检测酸性磷酸酶(acp)的含量,首次利用荧光金纳米簇材料(bsa-auncs)建立了一种灵敏的双猝灭双增强的磷酸酶(acp)检测方法,该方法检测acp灵敏度高,线性范围为0.01~2u/l,检出限为0.003u/l,相对于其它酶(如辣根过氧化物酶、溶菌酶、葡萄糖氧化酶、酪氨酸酶)或金属离子而言,对酸性磷酸酶(acp)有较高的选择性;更重要的是,还有以下优点:首先,oxtmb作为猝灭平台,它的吸收光谱与bsa-auncs的荧光光谱重叠,bsa-auncs实现了从bsa-auncs到oxtmb的荧光共振能量转移(fret),并先进行荧光猝灭。由于酸性磷酸酶(acp)催化抗坏血酸2-磷酸(aa2p)水解为po
43-和抗坏血酸(aa),抗坏血酸(aa)可以将oxtmb还原为tmb,因此在acp存在时,可以防止fret的发生,再次“增强”荧光;其次,加入ce
3+
也使tmb氧化为oxtmb,使荧光进一步猝灭;另外,由于po
43-和ce
3+
的高配位,acp和aa2p的存在阻碍了氧化还原反应。因此,在acp存在时,荧光再次被打开,初始荧光信号的高猝灭和有效增强实现了acp的高灵敏度和选择性检测。因此,本发明制备的荧光金纳米簇材料(bsa-auncs)扩展了生物分析中敏感荧光方法的应用前景。
18.本发明的其他优点、目标和特征在某种程度上将在随后的说明书中进行阐述,并且在某种程度上,基于对下文的考察研究对本领域技术人员而言将是显而易见的,或者可以从本发明的实践中得到教导。本发明的目标和其他优点可以通过下面的说明书来实现和获得。
附图说明
19.为了使本发明的目的、技术方案和优点更加清楚,下面将结合附图对本发明作优
选的详细描述,其中:
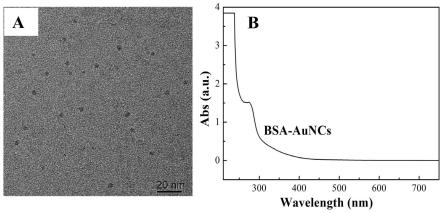
20.图1中实施例1中制备的荧光金纳米簇材料(bsa-auncs)的透射电镜(tem)图(a)和紫外吸收光谱图(b);
21.图2中浓度为5mm的荧光金纳米簇材料(bsa-auncs)溶液在可见光(a)和365nm波长处的紫外线灯(b)照射下的图;
22.图3为浓度为5mm的荧光金纳米簇材料(bsa-auncs)溶液的激发光谱、发射光谱和oxtmb吸收光谱图;
23.图4为实施例1中制备的荧光金纳米簇材料(bsa-auncs)对h2o2氧化3,3',5,5'-四甲基联苯胺(tmb)反应的影响,其中a为在可见光条件下的颜色变化、b为吸收强度的变化,其中a为向浓度为5mm的金纳米簇材料(bsa-auncs)溶液中加入0.2mm 3,3',5,5'-四甲基联苯胺(tmb)、b为向a中加入0.4mm双氧水(h2o2)、c为0.2mm的tmb和0.4mm的h2o2、d为向c中加入0.2mm的tmb和0.4mm的h2o2;
24.图5为不同溶液在可见光下的颜色变化(a)和荧光强度的变化(b),其中a为荧光金纳米簇材料(bsa-auncs)溶液、b为向a中加入0.1mm的抗坏血酸2-磷酸(aa2p)溶液、c为向a中加入1.4u/l的酸性磷酸酶(acp)、d为0.4mm的双氧水(h2o2)、0.25mm的3,3',5,5'-四甲基联苯胺(tmb)和0.1mm的抗坏血酸2-磷酸(aa2p)的混合溶液、e为向d中加入50m的ce
3+
,f为向e中加入1.4u/l的酸性磷酸酶(acp);
25.图6为不同ce
3+
浓度对不同溶液(在ph=4的hac-naac缓冲溶液中加入5mm的荧光金纳米簇材料(bsa-auncs)形成的溶液(bsa-auncs),在ph=4的hac-naac缓冲溶液中加入0.25mm的抗坏血酸2-磷酸(aa2p)、0.4mm的过氧化氢(h2o2)、0.25mm的3,3',5,5'-四甲基联苯胺(tmb)形成的溶液(无acp的对照组溶液)和在ph=4的hac-naac缓冲溶液中加入1.4u/l的酸性磷酸酶(acp)、0.25mm的抗坏血酸2-磷酸(aa2p)、0.4mm的过氧化氢(h2o2)、0.25mm的3,3',5,5'-四甲基联苯胺(tmb)形成的溶液(含acp的实验组溶液))荧光强度的影响;
26.图7为缓冲溶液中不同ph值对不同溶液(在hac-naac缓冲溶液中加入0.25mm的抗坏血酸2-磷酸(aa2p)、0.4mm的过氧化氢(h2o2)、0.25mm的3,3',5,5'-四甲基联苯胺(tmb)、50m的ce
3+
溶液形成的溶液(无acp的对照组溶液)和在hac-naac缓冲溶液中加入1.4u/l的酸性磷酸酶(acp)、0.25mm的抗坏血酸2-磷酸(aa2p)、0.4mm的过氧化氢(h2o2)、0.25mm的3,3',5,5'-四甲基联苯胺(tmb)、50m的ce
3+
溶液形成的溶液(含acp的实验组溶液))荧光强度的影响;
27.图8为不同温度对不同溶液(在ph=4的hac-naac缓冲溶液中加入0.25mm的抗坏血酸2-磷酸(aa2p)、0.4mm的过氧化氢(h2o2)、0.25mm的3,3',5,5'-四甲基联苯胺(tmb)、50m的ce
3+
溶液形成的溶液(无acp的对照组溶液)和在ph=4的hac-naac缓冲溶液中加入1.4u/l的酸性磷酸酶(acp)、0.25mm的抗坏血酸2-磷酸(aa2p)、0.4mm的过氧化氢(h2o2)、0.25mm的3,3',5,5'-四甲基联苯胺(tmb)、50m的ce
3+
溶液形成的溶液(含acp的实验组溶液))荧光强度的影响;
28.图9为不同反应时间对不同溶液(在ph=4的hac-naac缓冲溶液中加入0.25mm的抗坏血酸2-磷酸(aa2p)、0.4mm的过氧化氢(h2o2)、0.25mm的3,3',5,5'-四甲基联苯胺(tmb)、50m的ce
3+
溶液形成的溶液(无acp的对照组溶液)和在ph=4的hac-naac缓冲溶液中加入1.4u/l的酸性磷酸酶(acp)、0.25mm的抗坏血酸2-磷酸(aa2p)、0.4mm的过氧化氢(h2o2)、
0.25mm的3,3',5,5'-四甲基联苯胺(tmb)、50m的ce
3+
溶液形成的溶液(含acp的实验组溶液))荧光强度的影响;
29.图10中a为不同浓度的酸性磷酸酶(acp)溶液对浓度为5mm的荧光金纳米簇材料(bsa-auncs)的hac-naac缓冲溶液(ph=4)的荧光光谱的影响,b为添加的酸性磷酸酶(acp)溶液浓度与溶液荧光强度的关系图,c为添加的酸性磷酸酶(acp)溶液浓度与溶液荧光强度的线性拟合结果;
30.图11为荧光金纳米簇材料(bsa-auncs)对acp的选择性测试结果。向浓度为5mm的荧光金纳米簇材料(bsa-auncs)的hac-naac缓冲溶液(ph=4)中分别加入浓度为1.4u/l的空白溶液(blank)、碱性磷酸酶(alp)、辣根过氧化物酶(hrp)、溶菌酶(lys)、酪氨酸(try)、葡萄糖氧化酶(gox)、酪氨酸酶(t yr)、半胱氨酸(cys)、甘氨酸(gly)、丙氨酸(ala)、k
+
、na
+
、ca
2+
、mg
2+
、fe
2+
和acp后荧光强度变化结果;
31.图12位本发明制备的金纳米簇材料(bsa-auncs)产生过氧化物酶模拟活性和荧光特性的作用机理图。
具体实施方式
32.以下通过特定的具体实例说明本发明的实施方式,本领域技术人员可由本说明书所揭露的内容轻易地了解本发明的其他优点与功效。本发明还可以通过另外不同的具体实施方式加以实施或应用,本说明书中的各项细节也可以基于不同观点与应用,在没有背离本发明的精神下进行各种修饰或改变。需要说明的是,以下实施例中所提供的图示仅以示意方式说明本发明的基本构想,在不冲突的情况下,以下实施例及实施例中的特征可以相互组合。
33.实施例1
34.制备一种荧光金纳米簇材料(bsa-auncs),具体制备方法如下所示:
35.(1)将15ml的三水合氯金酸(haucl
4-3h2o)溶液(其中三水合氯金酸的浓度为10mm)加入到15ml的牛血清蛋白(bsa)水溶液(其中牛血清蛋白的浓度为50mg/ml)中,立即在37℃水浴中剧烈搅拌2min后,加入氢氧化钠(naoh)溶液(其中氢氧化钠的浓度为1m)调节反应体系的ph值为10,持续避光搅拌12h,以得到的浓度为5mm的金纳米簇材料(bsa-auncs)溶液,保存在4℃的冰箱中备用;
36.(2)将步骤(1)中合成的溶液使用3kda分子量的截流膜和超纯水透析24h,得到荧光金纳米簇材料(bsa-auncs)。
37.实施例2
38.制备一种荧光金纳米簇材料(bsa-auncs),具体制备方法如下所示:
39.(1)将15ml的三水合氯金酸(haucl
4-3h2o)溶液(其中三水合氯金酸的浓度为8mm)加入到9ml的牛血清蛋白(bsa)水溶液(其中牛血清蛋白的浓度为40mg/ml)中,立即在37℃水浴中剧烈搅拌2min后,加入氢氧化钠(naoh)溶液(其中氢氧化钠的浓度为1m)调节反应体系的ph值为10,持续避光搅拌12h,以得到的浓度为5mm的金纳米簇材料(bsa-auncs)溶液,保存在4℃的冰箱中备用;
40.(2)将步骤(1)中合成的溶液使用3kda分子量的截流膜和超纯水透析24h,得到荧光金纳米簇材料(bsa-auncs)。
41.实施例3
42.制备一种荧光金纳米簇材料(bsa-auncs),具体制备方法如下所示:
43.(1)将15ml的三水合氯金酸(haucl
4-3h2o)溶液(其中三水合氯金酸的浓度为12mm)加入到18ml的牛血清蛋白(bsa)水溶液(其中牛血清蛋白的浓度为80mg/ml)中,立即在37℃水浴中剧烈搅拌2min后,加入氢氧化钠(naoh)溶液(其中氢氧化钠的浓度为1m)调节反应体系的ph值为11,持续避光搅拌12h,以得到的浓度为5mm的金纳米簇材料(bsa-auncs)溶液,保存在4℃的冰箱中备用;
44.(2)将步骤(1)中合成的溶液使用3kda分子量的截流膜和超纯水透析24h,得到荧光金纳米簇材料(bsa-auncs)。
45.性能测试
46.下列性能测试过程中采用的荧光金纳米簇材料(bsa-auncs)溶液为将实施例1中制备的荧光金纳米簇材料(bsa-auncs)溶液溶于ph=4的hac-naac缓冲溶液形成的浓度为5mm的荧光纳米簇材料(bsa-auncs)溶液,荧光金纳米簇材料(bsa-auncs)为实施例1中步骤(2)中得到的产物。
47.对实施例1中制备的荧光金纳米簇材料(bsa-auncs)进行性能表征:图1中a为透射电镜(tem)对实施例1中制备的荧光金纳米簇材料(bsa-auncs)的形貌表征图,从中可以看出,通过实施例1中的制备方法,确实成功合成了荧光金纳米簇材料(bsa-auncs),其粒径在3.0-4.5nm的范围之间。此外,对实施例1中制备的荧光金纳米簇材料(bsa-auncs)进行紫外吸收检测,从紫外吸收光谱图(图1中b)可以看出,制备的荧光金纳米簇材料(bsa-auncs)无明显的等离子共振吸收峰,只有在275nm处出现了肩峰。
48.图2中浓度为5mm的荧光金纳米簇材料(bsa-auncs)溶液在可见光(a)和365nm波长处的紫外线灯(b)照射下的图片,从中可以看出,荧光金纳米簇材料(bsa-auncs)溶液在可见光下呈黄色,而在365nm波长处的紫外线照射下呈红色荧光,说明实施例1中确实成功合成了具有荧光特性的荧光金纳米簇材料(bsa-auncs)。图3为浓度为5mm的荧光金纳米簇材料(bsa-auncs)溶液的激发光谱、发射光谱以及tmb被氧化后形成的oxtmb的吸收光谱图,从中可以看出,实施例1中制备的金纳米簇材料(bsa-auncs)的发射峰波长为635nm、激发峰波长为370nm,该荧光金纳米簇材料的发射光谱与oxtmb的吸收光谱有较大重叠,符合了荧光共振能量转移(fret)原理,进一步说明实施例1中的方法确实能够制备得到荧光金纳米簇材料(bsa-auncs),并且还能用于与oxtmb一起构建fret实验体系。
49.图4为实施例1中制备的荧光金纳米簇材料(bsa-auncs)对h2o2氧化3,3',5,5'-四甲基联苯胺(tmb)反应的影响,其中a为在可见光条件下的颜色变化、b为吸收强度的变化。从图4中a可以看出,在可见光条件下,在ph=4的hac-naac缓冲溶液中,浓度为0.2mm的3,3',5,5'-四甲基联苯胺(tmb)和浓度为5mm的荧光金纳米簇材料(bsa-auncs)形成的混合溶液(a)为无色透明溶液,计入浓度为0.4mm的双氧水(h2o2)后形成的混合溶液(b)为无色透明溶液,而浓度为0.2mm的3,3',5,5'-四甲基联苯胺(tmb)和浓度为0.4mm的双氧水(h2o2)形成的混合溶液(c)由于3,3',5,5'-四甲基联苯胺(tmb)可以被h2o2氧化成蓝色的oxtmb显淡蓝色,但其蓝色不明显,但是向浓度为0.2mm的3,3',5,5'-四甲基联苯胺(tmb)和浓度为0.4mm的双氧水(h2o2)形成的混合溶液(c)中添加浓度为5mm的荧光金纳米簇材料(bsa-auncs)后形成的混合溶液(d)的蓝色加深显深蓝色,说明该混合溶液中形成的蓝色的oxtmb浓度增
大;同样的,从图4中b可以看出,a和b两种混合溶液并无明显的吸收峰出现,混合溶液c在652nm处出现明显的oxtmb吸收峰,随着混合溶液d中加入荧光金纳米簇材料(bsa-auncs),其oxtmb吸收峰的强度也明显增加。从中可以看出,本发明制备的荧光金纳米簇材料(bsa-auncs)确实能够增强双氧水(h2o2)对3,3',5,5'-四甲基联苯胺(tmb)的氧化作用,说明本发明制备的荧光金纳米簇材料(bsa-auncs)具有与过氧化物酶类似的增强过氧化氢氧化性的作用。
50.图5为不同溶液在可见光下的颜色变化(a)和荧光强度的变化(b),其中a为荧光金纳米簇材料(bsa-auncs)溶液、b为向a中加入0.1mm的抗坏血酸2-磷酸(aa2p)溶液、c为向a中加入1.4u/l的酸性磷酸酶(acp)、d为0.4mm的双氧水(h2o2)、0.25mm的3,3',5,5'-四甲基联苯胺(tmb)和0.1mm的抗坏血酸2-磷酸(aa2p)的混合溶液、e为向d中加入50m的ce
3+
,f为向e中加入1.4u/l的酸性磷酸酶(acp)。由于,酸性磷酸酶(acp)能够将底物抗坏血酸2-磷酸(aa2p)分解成抗坏血酸(aa)和磷酸根(po
43-),ce
3+
与磷酸根(po
43-)具有较高的配位性。因此,在图5的a中,混合溶液d和e中由于发生了氧化反应使得体系的颜色发生了变化,而f中由于产生磷酸根离子能够与ce
3+
发生配位作用,阻止了tmb氧化变蓝,所以蓝色变浅;而在图5的b中,在ph=4的hac-naac缓冲溶液中,在370nm的激发下,荧光金纳米簇材料(bsa-auncs)的溶液(a)以及分别向其中加入了抗坏血酸2-磷酸(aa2p)(b)和酸性磷酸酶(acp)(c)后形成的溶液的荧光强度都没有发生比较大的变化,但是在加入双氧水(h2o2)、3,3',5,5'-四甲基联苯胺(tmb)和抗坏血酸2-磷酸(aa2p)形成的溶液(d)后荧光强度大幅度降低,继续添加50m的ce
3+
形成溶液(e)的荧光强度继续降低,然后再加入1.4u/l的酸性磷酸酶(acp)形成的溶液(f)的荧光强度明显提高。由此说明,oxtmb及其他物质对荧光金纳米簇材料(bsa-auncs)在652nm处的荧光强度的影响,经研究发现仅有po
43-存在时bsa-auncs的荧光不发生变化,同时由于aa是还原剂,蓝色oxtmb被aa还原成无色的tmb溶液,使得溶液在652nm处的吸收峰消失,荧光金纳米簇材料(bsa-auncs)在652nm的荧光再次增强。更重要的是,po
43-和aa带来的这两种荧光增强效应在acp的荧光“on-on”检测中同时存在。
51.图6为不同ce
3+
浓度对不同溶液(在ph=4的hac-naac缓冲溶液中加入5mm的荧光金纳米簇材料(bsa-auncs)形成的溶液(bsa-auncs),在ph=4的hac-naac缓冲溶液中加入0.25mm的抗坏血酸2-磷酸(aa2p)、0.4mm的过氧化氢(h2o2)、0.25mm的3,3',5,5'-四甲基联苯胺(tmb)形成的溶液(无acp的对照组溶液)和在ph=4的hac-naac缓冲溶液中加入1.4u/l的酸性磷酸酶(acp)、0.25mm的抗坏血酸2-磷酸(aa2p)、0.4mm的过氧化氢(h2o2)、0.25mm的3,3',5,5'-四甲基联苯胺(tmb)形成的溶液(含acp的实验组溶液))荧光强度的影响。从图6中可以看出,无酸性磷酸酶(acp)存在时,抗坏血酸2-磷酸(aa2p)磷酸酯键不能被分解,没有抗坏血酸(aa)和磷酸根(po
43-)生成,oxtmb不能被还原,同时ce
3+
不能和磷酸根(po
43-)配位结合,oxtmb比较多,能量转移可以发生,导致了体系荧光被猝灭;当有acp时,抗坏血酸(aa)和磷酸根(po
43-),oxtmb被抗坏血酸(aa)还原,能量转移被抑制,此外,ce
3+
还可以和磷酸根(po
43-)配位结合,oxtmb的量减少,能量转移也被阻止,从而也导致了体系荧光被增强。浓度为20-60m的ce
3+
对荧光金纳米簇材料(bsa-auncs)溶液中的荧光猝灭和猝灭效果都有。
52.图7为缓冲溶液中不同ph值对不同溶液(在hac-naac缓冲溶液中加入0.25mm的抗坏血酸2-磷酸(aa2p)、0.4mm的过氧化氢(h2o2)、0.25mm的3,3',5,5'-四甲基联苯胺(tmb)、50m的ce
3+
溶液形成的溶液(无acp的对照组溶液)和在hac-naac缓冲溶液中加入1.4u/l的酸
性磷酸酶(acp)、0.25mm的抗坏血酸2-磷酸(aa2p)、0.4mm的过氧化氢(h2o2)、0.25mm的3,3',5,5'-四甲基联苯胺(tmb)、50m的ce
3+
溶液形成的溶液(含acp的实验组溶液))荧光强度的影响。实验探索和大量文献报道中显示,中性或者碱性条件下,酸性磷酸酶(acp)的激活性发挥不出来,只有在酸性条件下,其酶的活性才可以发挥出来。从图7中可以看出,加入的酸性磷酸酶(acp)能够分解抗坏血酸2-磷酸(aa2p)磷酸酯键,生成抗坏血酸(aa)和磷酸根(po
43-),在ph=3.6-5.6的酸性条件下都可以实现体系荧光的增强,说明酸性磷酸酶(acp)在ph=3.6-5.6的条件下能够发挥作用,因此可以在ph=3.6-5.6的条件下进行acp的检测。
53.图8为不同温度对不同溶液(在ph=4的hac-naac缓冲溶液中加入0.25mm的抗坏血酸2-磷酸(aa2p)、0.4mm的过氧化氢(h2o2)、0.25mm的3,3',5,5'-四甲基联苯胺(tmb)、50m的ce
3+
溶液形成的溶液(无acp的对照组溶液)和在ph=4的hac-naac缓冲溶液中加入1.4u/l的酸性磷酸酶(acp)、0.25mm的抗坏血酸2-磷酸(aa2p)、0.4mm的过氧化氢(h2o2)、0.25mm的3,3',5,5'-四甲基联苯胺(tmb)、50m的ce
3+
溶液形成的溶液(含acp的实验组溶液))荧光强度的影响。从图8中可以看出,检测温度在15-50℃之间时,加入的酸性磷酸酶(acp)都可以分解抗坏血酸2-磷酸(aa2p)磷酸酯键,生成抗坏血酸(aa)和磷酸根(po
43-)实现荧光信号的增强,说明酸性磷酸酶(acp)在15-50℃的条件下能够发挥作用,因此可以在15-50℃的条件下进行acp的检测。
54.图9为不同反应时间对不同溶液(在ph=4的hac-naac缓冲溶液中加入0.25mm的抗坏血酸2-磷酸(aa2p)、0.4mm的过氧化氢(h2o2)、0.25mm的3,3',5,5'-四甲基联苯胺(tmb)、50m的ce
3+
溶液形成的溶液(无acp的对照组溶液)和在ph=4的hac-naac缓冲溶液中加入1.4u/l的酸性磷酸酶(acp)、0.25mm的抗坏血酸2-磷酸(aa2p)、0.4mm的过氧化氢(h2o2)、0.25mm的3,3',5,5'-四甲基联苯胺(tmb)、50m的ce
3+
溶液形成的溶液(含acp的实验组溶液))荧光强度的影响。从图8中可以看出,反应时间在1-60min之间时,加入酸性磷酸酶(acp)都可以分解抗坏血酸2-磷酸(aa2p)磷酸酯键,生成抗坏血酸(aa)和磷酸根(po
43-)是一个快速的过程,基本上在1min就有荧光增强的响应。随着时间的延长,增强效果会更好,在30min之后基本上达到一个稳定的荧光增强效果,说明酸性磷酸酶(acp)已经彻底分解了抗坏血酸2-磷酸(aa2p)磷酸酯键,因此说明对acp的检测是一个快速响应的过程,作用1分钟即可实现对acp的检测。
55.图10中a为不同浓度的酸性磷酸酶(acp)溶液对浓度为5mm的荧光金纳米簇材料(bsa-auncs)的hac-naac缓冲溶液(ph=4)的荧光光谱的影响,b为添加的酸性磷酸酶(acp)溶液浓度与溶液荧光强度的关系图,c为添加的酸性磷酸酶(acp)溶液浓度与溶液荧光强度的线性拟合结果。向浓度为5mm的荧光金纳米簇材料(bsa-auncs)的hac-naac缓冲溶液(ph=4)中添加不同浓度的酸性磷酸酶(acp)溶液(添加的acp溶液浓度分别为0u/l、0.01u/l、0.03u/l、0.05u/l、0.08u/l、0.1u/l、0.25u/l、0.4u/l、0.55u/l、0.7u/l、1u/l、1.2u/l、1.4u/l、1.6u/l、1.8u/l、2u/l、3u/l、5u/l、7u/l和10u/l),荧光光谱的变化情况如图10中a所示,随着添加的acp溶液浓度增加,其荧光光谱的强度也逐渐增大,添加的acp溶液浓度与溶液荧光强度的关系图如图10中b所示。添加的acp溶液浓度从0u/l到2.0u/l,荧光金纳米簇材料(bsa-auncs)溶液的荧光强度逐渐增加,然后达到平台期,添加的acp溶液浓度从2.0u/l到10.0u/l,荧光金纳米簇材料(bsa-auncs)溶液的荧光强度不再发生变化。将acp溶液的2.0u/l-10.0u/l的浓度与相应的荧光金纳米簇材料(bsa-auncs)溶液的荧光强度进行
线性拟合,其结果如图10中c所示,得到的线性方程为i=21.18c
acp
+17.33c(u/l),相关系数(r)为0.9930,检出限(lod)为0.003u/l(3,n=11)。lod是根据响应的标准差(sd)和校准曲线的斜率计算。与其他acp检测方法相比,该双“增强”荧光结合双猝灭策略检测acp的灵敏度高,线性范围宽(如表1所示)。
56.表1不同方法检测acp线性范围和检测限
[0057][0058]
图11为荧光金纳米簇材料(bsa-auncs)对acp的选择性测试结果。向浓度为5mm的荧光金纳米簇材料(bsa-auncs)的hac-naac缓冲溶液(ph=4)中分别加入浓度为1.4u/l的空白溶液(blank)、碱性磷酸酶(alp)、辣根过氧化物酶(hrp)、溶菌酶(lys)、酪氨酸(try)、葡萄糖氧化酶(gox)、酪氨酸酶(t yr)、半胱氨酸(cys)、甘氨酸(gly)、丙氨酸(ala)、k
+
、na
+
、ca
2+
、mg
2+
、fe
2+
和acp后荧光强度变化结果,从中可以看出,本发明实施例1中制备的荧光金纳米簇材料(bsa-auncs)对acp具有良好的荧光选择性。
[0059]
同样的,将实施例2和实施例3中制备得到的荧光金纳米簇材料(bsa-auncs)用于上述性能测试,其得到的结果与实施例1中制备得到的荧光金纳米簇材料(bsa-auncs)相似。
[0060]
综上所述,本发明制备的荧光金纳米簇材料(bsa-auncs)具有过氧化物酶模拟活性和荧光特性。其作用机理如图12所示。荧光金纳米簇材料(bsa-auncs)不仅可以催化无色的tmb氧化为蓝色的oxtmb,还可以作为供体和蓝色的oxtmb建立fret从而导致荧光被猝灭,这是荧光“猝灭”的第一个关键因素;当添加ce
3+
时,荧光金纳米簇材料(bsa-auncs)催化h2o2将ce
3+
氧化为ce
4+
,而ce
4+
具有较强的氧化性,可以进一步将tmb氧化成oxtmb,增强金纳米簇材料(bsa-auncs)与蓝色的oxtmb之间建立的fret,这是荧光猝灭的第二个关键因素。由于acp能将抗坏血酸2-磷酸(aa2p)水解成磷酸根离子(po
43-)和抗坏血酸(aa),首先,po
43-和ce
3+
之间的高度配位能够阻断氧化还原反应;其次蓝色的oxtmb被aa还原导致其在652nm处的吸光度消失,这阻止了fret从金纳米簇材料(bsa-auncs)到oxtmb。基于此可以开发一种使用双猝灭和fret机制来提高检测acp的方法。
[0061]
将本发明制备的金纳米簇材料(bsa-auncs)用于实际血清样本中acp检测,具体步骤如下所示:
[0062]
(1)在室温(25℃)下,首先将20l浓度为5mm的抗坏血酸2-磷酸(aa2p)溶液与不同浓度的酸性磷酸酯(acp)在200l、浓度为0.2m、ph=4的hac-naac缓冲液中反应30min;
[0063]
(2)然后在上述样品中加入25l浓度为2mm的ce
3+
溶液、20l浓度为20mm的h2o2溶液和40l的bsa-auncs溶液;
[0064]
(3)最后,继续加入50μl浓度为5mm的tmb溶液和和适当的经过50倍稀释的血清溶液,使整个溶液的最终体积为1ml,反应30min;
[0065]
(4)添加浓度为0.2m、ph=4的hac-naac缓冲液使整个溶液的最终体积保持在1ml,充分涡旋混合后,记录荧光光谱(激发和发射的狭缝宽度分别为10nm和10nm、光电倍增管电压(pmt)保持在800v)。
[0066]
为了验证本发明制备的荧光金纳米簇材料(bsa-auncs)在实际检测acp方面的准确性,对市售山羊血清样品进行了稀释并对用该方法检测acp进行了验证。其他步骤与上述acp检测方法相同,向山羊血清样品分别添加0.5u/l、1.0u/l和1.5u/l的acp,检测得到的acp含量和加样回收率如表2所示,相对标准偏差(rsd)《5%。结果表明,本发明采用荧光金纳米簇材料(bsa-auncs)检测acp的方法具有较高的准确度,在实际acp分析领域具有广阔的应用前景。
[0067]
表2采用荧光金纳米簇材料(bsa-auncs)检测acp的测试结果
[0068][0069]
综上所述,本发明公开了一种以牛血清白蛋白作为还原剂和保护剂的荧光金纳米簇材料(bsa-auncs),具有过氧化物酶模拟活性和荧光特性,能够用于检测酸性磷酸酶(acp)的含量,首次利用荧光金纳米簇材料(bsa-auncs)建立了一种灵敏的双猝灭双增强的acp检测方法,该方法检测acp灵敏度高,线性范围为0.01~2u/l,检出限为0.003u/l,相对于其它酶(如辣根过氧化物酶、溶菌酶、葡萄糖氧化酶、酪氨酸酶)或金属离子而言,对酸性磷酸酶(acp)有较高的选择性;更重要的是,还有以下优点:首先,oxtmb作为猝灭平台,它的吸收光谱与bsa-auncs的荧光光谱重叠,bsa-auncs实现了从bsa-auncs到oxtmb的荧光共振能量转移(fret),实现了荧光的猝灭。由于酸性磷酸酶(acp)催化抗坏血酸2-磷酸(aa2p)水解为po
43-和抗坏血酸(aa),抗坏血酸(aa)可以将oxtmb还原为tmb,因此在acp存在时,可以防止fret的发生,再次“增强”荧光;其次,加入ce
3+
也使tmb氧化为oxtmb,使荧光进一步猝灭;另外,由于po
43-和ce
3+
的高配位,acp和aa2p的存在阻碍了氧化还原反应。因此,在acp存在时,荧光再次被“增强”,初始荧光信号的高猝灭和有效增强实现了acp的高灵敏度和选择性检测。因此,本发明的荧光金纳米簇材料(bsa-auncs)扩展了生物分析中敏感荧光方法的应用前景。
[0070]
最后说明的是,以上实施例仅用以说明本发明的技术方案而非限制,尽管参照较佳实施例对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本技术方案的宗旨和范围,其均应涵盖在本发明
的权利要求范围当中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1