一种低共熔溶剂辅助合成荧光探针的方法及应用与流程
1.本发明属于荧光纳米材料制备、食品、环境科学技术领域,尤其涉及一种低共熔溶剂辅助合成荧光探针的方法及应用。
背景技术:
2.亚硝酸盐俗称工业盐,广泛用作着色剂、防腐剂、抗菌剂,并广泛用作食品工业的添加剂。然而,过量摄入亚硝酸盐会损害人体健康。它在人体内可转化为多种氮氧化物,并可在酸性介质中与胺等蛋白质代谢物发生反应,形成亚硝胺,具有严重的致癌风险。除此之外,血液中过量的亚硝酸盐还会将血红蛋白转化为高铁血红蛋白,从而干扰体内的氧运输系统,导致组织缺氧和血压降低。亚硝酸盐不仅在食品工业中广泛应用,还广泛存在于化肥降解、酸雨、工业废弃物等。因此,亚硝酸盐离子含量的监测对于人们的健康越来越重要。这促使我们需要建立一种高灵敏度、高选择性的方法。此外,亚硝酸盐的加入会极大地影响ph值,检测在不同ph值下的稳定性和荧光性能尤为重要,这为其未来在水环境ph监测中的应用奠定了基础。
3.目前,亚硝酸盐的检测方法有色谱法、毛细管电泳法、电化学法和荧光光谱法等。比色法是其中最常用的方法,已经使用了几十年。该方法简单、快速、成本低、应用广泛,但仍存在灵敏度低、毒性大、易被其他基质和阴离子干扰等缺陷。色谱法和电化学法灵敏度高,选择性好,但耗时长,不适合痕量检测。
4.目前,作为荧光传感器的荧光纳米材料种类繁多,如半导体量子点、聚合物点、荧光纳米金刚石、荧光纳米团簇等。然而,合成碳点的一系列荧光材料既昂贵又有害,且大多数荧光探针检测亚硝酸盐离子时需满足酸性条件。因此,开发一种绿色的替代材料仍然是十分必要的。
5.因此,针对于亚硝酸盐的大规模生产引起的食品问题,开发绿色友好碳量子点的前驱体制备方法,实现食品内亚硝酸盐的有效检测具有重要意义。
技术实现要素:
6.鉴于现有技术所存在的问题,本发明提供一种低共熔溶剂辅助合成荧光探针的方法及应用,具有环境友好、绿色环保、低成本、荧光稳定、来源广泛、制备简单、量子产率高、水溶性好、选择性强、线性范围宽、检测灵敏度好等优点。
7.本发明解决上述技术问题的技术方案如下:
8.本发明提供一种低共熔溶剂辅助合成荧光探针的方法,包括以下步骤:
9.(1)将氢键供体与氢键受体混合,得到混合液,所述氢键受体包括金属,加热直至混合液变为均一透明的溶液,得到金属低共熔溶剂,即mdes;
10.(2)将mdes制得mdes溶液;
11.(3)将mdes溶液加热反应,冷却,得到碳点溶液;
12.(4)将碳点溶液过滤,得到含有荧光探针的溶液。
13.采用上述方案的有益效果包括:
14.本发明制备的荧光探针是基于金属型低共熔溶剂为前驱体、铁掺杂碳量子点荧光探针,低共熔溶剂具有极大的热稳定性、较高的原子经济性和生物降解性,符合“绿色化学”的概念,是有毒有机溶剂的强替代品。
15.本发明采用上述方法合成的荧光探针具有环境友好、绿色环保、低成本、荧光稳定、来源广泛、制备简单、量子产率高、水溶性好、选择性强、线性范围宽、检测灵敏度好等优点。且可实现食品与环境中亚硝酸盐检测,其在不同ph下独特的颜色变化,也可作为环境ph指示剂。
16.进一步,所述氢键供体为dl-苹果酸;所述氢键受体包括乙二醇和金属; dl-苹果酸、乙二醇、金属的摩尔比为2:8:(0.2-1.2)。
17.采用上述方案的有益效果包括:发明人在研究中意外的发现,掺杂金属所占的比例会极大影响mdes-cds荧光强度与亚硝酸盐的响应情况。采用合适的比例有利于提高荧光探针的质量。
18.进一步,所述金属选自cu、mn、fe、zn、co中的一种或几种的组合。
19.优选地,氢键供体选自dl-苹果酸,氢键受体包括乙二醇、金属fe。
20.采用上述方案的有益效果包括:dl-苹果酸-金属fe-乙二醇合成的低共熔溶剂所制备的荧光探针荧光强度高,且可实现亚硝酸盐的测定。
21.进一步,步骤(1)中,加热温度为60-80℃;步骤(3)中,加热反应的条件包括:温度为120-200℃,反应时间为2-10h;步骤(4)中,采用 0.22μm微孔滤膜过滤。
22.采用上述方案的有益效果包括:
23.加热温度为60-80℃,有利于加快反应速度,使其受热均匀,且mdes 在此温度范围内合成相对稳定。温度过低受热慢,达不到形成mdes的温度要求;温度过高容易糊底或炸裂,会出现安全性问题。
24.温度为120-200℃,反应时间为2-10h,该条件为通过研究合成温度与时间变量对荧光强度的影响获得的最优条件,进而使mdes-cds获得较高的荧光量子产率。
25.采用过滤用0.22μm微孔滤膜除去溶液中大分子杂质,可以使mdes-cds 固体具有较好的发光性质。
26.进一步,还包括过滤后透析、冷冻干燥制得mdes-cds的步骤;冷冻干燥的条件包括:真空-80℃冷冻干燥24-48h。
27.采用上述方案的有益效果包括:使得到的mdes-cds固体具有更好的发光性质。
28.进一步,还包括将mdes-cds制得mdes-cds溶液的步骤;mdes-cds溶液中,mdes-cds的浓度为10-50mg
·
ml-1
。
29.采用上述方案的有益效果包括:配制成浓度为10-50mg
·
ml-1
的 mdes-cds溶液,浓度过低荧光强度过低,用量过大;浓度过高误差变大且有可能存在自猝灭现象。
30.本发明提供一种用于检测亚硝酸盐和/或ph的试剂或试剂盒,包括上述方法合成的荧光探针。
31.采取上述技术方案的有益效果包括:本发明提供的试剂或试剂盒,具有超高的灵敏度、选择性、优异的ph依赖性发光和独特的颜色变化,具有广泛的应用前景。
32.本发明提供上述荧光探针在(1)、(2)、(3)、(4)的一种或几种中的应用,
33.(1)检测亚硝酸盐;
34.(2)检测ph;
35.(3)制作或用于检测亚硝酸盐的试剂或试剂盒;
36.(4)制作或用于检测ph的试剂或试剂盒。
37.本发明提供一种检测亚硝酸盐的方法,包括以下步骤:制作荧光强度关于亚硝酸盐浓度的标准曲线,将荧光探针与待测样品混合反应,检测荧光强度,根据标准曲线计算待测样品的亚硝酸盐浓度。
38.例如:可以根据实际需要选择是否进行预处理。然后将待测样品与 mdes-cds溶液混合,mdes-cds溶液中mdes-cds的浓度可以为10-50 mg
·
ml-1
,待测样品与mdes-cds溶液的体积可以为1:10,在ph=2的条件下,于60℃下反应20min,测试反应后的溶液的荧光强度。将该数值代入到线性回归方程中,即可计算出待测样品中亚硝酸盐的浓度。
39.采取上述技术方案的有益效果包括:本发明提供的荧光探针环境友好,对亚硝酸钠不仅具有超高的灵敏度和选择性,而且检出限可低至50nm,可以用于食品及环境中亚硝酸盐的大规模生产检测。
40.本发明提供一种检测ph的方法,包括以下步骤:制作荧光强度关于ph 的标准曲线,将荧光探针与待测样品混合反应,检测荧光强度,根据标准曲线计算待测样品的ph。
41.例如:可以根据实际需要选择是否进行预处理。然后将待测样品与 mdes-cds溶液混合,mdes-cds溶液中mdes-cds的浓度可以为10-50 mg
·
ml-1
,于60℃下反应20min,测试反应后的溶液的荧光强度。将该数值代入到线性回归方程中,即可计算出待测样品中ph。
42.采取上述技术方案的有益效果包括:本发明提供的荧光探针具有优异的 ph依赖性发光和独特的颜色变化,可以成为检测水环境的ph指示剂。并在食品与环境监测等领域具有很好的应用价值和前景。
附图说明
43.图1为本发明中一种用于亚硝酸盐,ph检测的fe掺杂碳量子点荧光探针的制备原理及检测原理示意图。
44.图2为mdes-cds的合成条件优化:金属种类(a);铁掺杂比(b);合成温度(c);时间(d)。
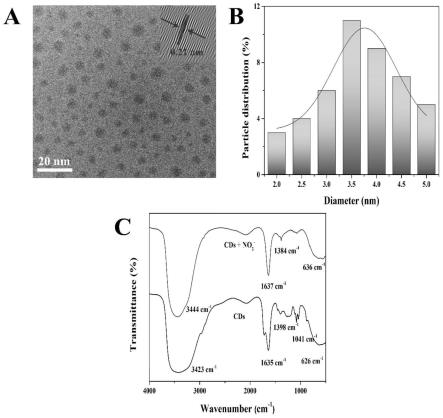
45.图3为mdes-cds的形貌、组成和表面结构研究结果;a为mdes-cds的透射电子显微镜图以及晶格分析;b为mdes-cds的粒径分布图;c为mdes-cds 的红外光谱图。
46.图4为mdes-cds的x-射线光电子能谱图:全扫光谱图(a);c 1s光谱图(b);o 1s光谱图(c);fe 2p光谱图(d)。
47.图5为通过紫外-可见吸收光谱(uv-vis)和荧光光谱验证了mdes-cds 的光学特性的结果;mdes-cds的紫外吸收光谱图以及最佳荧光激发与发射光谱图(a)(插图为mdes-cds在日光与紫外灯下的溶液颜色对比图);mdes-cds 在不同激发波长下(350-520nm)的荧光发射图(b)。
48.图6为高离子强度及辐射时间对mdes-cds荧光强度的影响结果; mdes-cds在不同浓度盐溶液(0.1-1mol
·
l-1
)的盐稳定性光谱图(a)和在最佳激发波长连续激发下(0-100min)的抗光漂白性光谱图(b)。
49.图7为mdes-cds对亚硝酸盐的检测条件优化:ph值(a);温度(b);时间(c)。
50.图8为不同亚硝酸盐浓度下mdes-cds溶液的荧光发射谱图。
51.图9为亚硝酸盐的不同浓度与mdes-cds荧光强度的线性关系图。
52.图10为不同干扰离子对mdes-cds溶液荧光强度影响的对比图。
53.图11为mdes-cds在不同ph下的荧光发射光谱图。
54.图12为mdes-cds的荧光强度与不同ph的线性关系图。
具体实施方式
55.以下结合附图对本发明的原理和特征进行描述,所举实例只用于解释本发明,并非用于限定本发明的范围。
56.如图1所示,本发明提供一种金属低共熔溶剂辅助制备荧光探针的方法及其应用,制备的荧光探针是一种金属掺杂荧光探针,该荧光探针是基于金属型低共熔溶剂为前驱体、铁掺杂碳量子点荧光探针,可以用于检测食品中亚硝酸盐及监测水环境ph。
57.本发明提供一种金属低共熔溶剂辅助制备荧光探针的方法,包括以下步骤:
58.(1)制备金属型低共熔溶剂:将氢键供体与氢键受体混合,60-80℃加热直至变为均一透明的溶液,即为金属低共熔溶剂;氢键供体包括:dl-苹果酸;氢键受体包括乙二醇和金属(选自cu,mn,fe,zn,co中的一种或几种)。优选地,dl-苹果酸作为氢键供体,乙二醇与金属fe作为氢键受体。 dl-苹果酸-金属fe-乙二醇合成的低共熔溶剂所制备的荧光探针荧光强度高,且可实现亚硝酸盐的测定。dl-苹果酸:乙二醇:金属相fe的摩尔比为 2:8:(0.2-1.2)。
59.(2)精密称取5ml mdes溶于10ml去离子水中,超声至体系混合均匀,得到mdes溶液。
60.(3)将步骤(2)中混合后的mdes溶液放置于聚四氟乙烯内胆高压反应釜中,并于烘箱120-200℃反应2-10h,待体系冷却至室温,得到碳点溶液。
61.(4)将步骤(3)中冷却至室温后的碳点溶液用0.22μm滤膜过滤,后采用透析袋(mw:500da)透析24h。
62.(5)将步骤(4)中溶液真空(-80℃)冷冻干燥24-48h,得到新型荧光探针(mdes-cds),并放置于4℃条件下低温保存备用。
63.(6)将步骤(5)中的mdes-cds固体加入超纯水配制成mdes-cds溶液 (浓度为10-50mg
·
ml-1
),放在4℃下低温保存备用。
64.通过上述制备方法可以制得金属掺杂碳量子点荧光探针(即mdes-cds 荧光探针)。
65.上述方法制备的mdes-cds荧光探针可以在亚硝酸盐检测以及环境ph检测的应用。
66.本发明提供一种检测亚硝酸盐的方法,包括以下步骤:制作荧光强度关于亚硝酸盐浓度的标准曲线,将荧光探针与待测样品混合反应,检测荧光强度,根据标准曲线计算待测样品的亚硝酸盐浓度。
67.例如:可以根据实际需要选择是否进行预处理。然后将待测样品与mdes-cds溶液混合,mdes-cds溶液中mdes-cds的浓度可以为10-50 mg
·
ml-1
,待测样品与mdes-cds溶液的体积可以为1:10,在ph=2的条件下,于60℃下反应20min,测试反应后的溶液的荧光强度。
将该数值代入到线性回归方程中,即可计算出待测样品中亚硝酸盐的浓度。
68.本发明提供一种检测ph的方法,包括以下步骤:制作荧光强度关于ph 的标准曲线,将荧光探针与待测样品混合反应,检测荧光强度,根据标准曲线计算待测样品的ph。
69.例如:可以根据实际需要选择是否进行预处理。然后将待测样品与 mdes-cds溶液混合,mdes-cds溶液中mdes-cds的浓度可以为10-50 mg
·
ml-1
,于60℃下反应20min,测试反应后的溶液的荧光强度。将该数值代入到线性回归方程中,即可计算出待测样品中ph。
70.本发明基于金属型低共熔溶剂所制备的荧光探针环境友好,低成本,荧光强度高且稳定性好。mdes-cds在水溶液中具有相对均匀的尺寸和良好的分散性,没有明显的聚集。其表面含有丰富的含氧官能团,mdes-cds可作为一种稳定优异的荧光探针用于传感测定。
71.与现有技术相比,本发明具有以下特点:
72.(1)本发明制得的荧光探针原料来源广泛,绿色。
73.(2)本发明提供的荧光探针制备简单,量子产率高,水溶性好。
74.(3)本发明提供的荧光探针具有较强的光漂白稳定性,并且在较高的盐浓度下保持基本稳定。
75.(4)本发明的荧光探针是具有蓝色荧光的mdes-cds,亚硝酸盐的加入可使得mdes-cds的荧光淬灭。并且荧光强度与亚硝酸盐浓度一定范围内具有良好的线性关系。
76.(5)荧光探针对亚硝酸盐表现出超强的选择性,线性范围宽,检测灵敏度好,并且成功用于食品与环境的样品检测。
77.(6)mdes-cds荧光探针还具有独特的ph敏感性性质,可以与ph在2-7 的范围实现优异的线性关系,mdes-cds荧光强度明显猝灭,并且日光下溶液由浅黄色-黄色-绿色的颜色转变使得该荧光探针可作为ph检测的颜色指示剂。
78.(7)基于mdes-cds对亚硝酸盐与ph的优异传感能力。使其在食品安全与环境污染等领域具有很好的应用价值。
79.下面通过具体的实施例进行介绍。
80.本发明中,荧光分光光度计的参数可以设置为:扫描速度(1000nm/min),激发带宽(10nm),发射带宽(10nm),增益(中,650v)。
81.实施例1
82.一种金属低共熔溶剂为前驱体的mdes-cds荧光探针的制备方法,包括以下步骤:
83.(1)以dl-苹果酸作为氢键供体,乙二醇及金属作为氢键受体制备金属型低共熔溶剂(mdes)。摩尔比即为dl-苹果酸:乙二醇:金属相=2:8:1。将混合物于80℃条件下磁性搅拌,30min后得到均匀透明的液相即为mdes。待自然冷却到室温后,放置封闭容器内待用。
84.(2)精密称取5ml mdes溶于10ml去离子水中,超声至体系混合均匀。将混合后的溶液在放置烘箱中并于200℃下反应6h,待体系冷却至室温,产物用0.22μm滤膜过滤。
85.对mdes-cds的合成条件进行优化,分别考察掺杂金属种类、掺杂金属比例、合成温度和时间对mdes-cds荧光性质的影响,实验结果如图2所示。
86.考察掺杂金属种类对mdes-cds荧光性质的影响。我们选取了不同金属,包括cu、mn、fe、zn及co,将其分别与dl-苹果酸、乙二醇按照与上述步骤相同的比例混合,将混合物置于80℃下磁力搅拌30min。冷却至室温后,分别取5ml并向其中加入10ml去离子水,超声使其混合均匀。然后置于聚四氟乙烯内胆高压反应釜中于烘箱200℃下反应6h,待体系冷却至
室温,用0.22μm滤膜进行过滤,然后在410nm激发波长下测试其荧光强度,发现只有fe-des制备合成的mdes-cds对亚硝酸盐具有显著的猝灭(图2a),图2a左上角的插图为日光下不同mdes-cds颜色(从左到右分别为cu、mn、 fe、zn、co制备成的金属型低共熔溶剂在相同的180℃,6h的条件下采用水热法制备出的碳点溶液在日光下的颜色),可以看出在金属fe存在的情况下,荧光强度最高,表明掺杂金属为fe时效果最好。选择掺杂金属为fe进行下面的实验。
87.考察掺杂金属比例对mdes-cds荧光性质的影响。研究了dl-苹果酸:乙二醇:掺杂fe元素摩尔比例2:8:(0.2-1.2)对mdes-cds荧光强度的影响,在相同条件下分别测试了fe元素的掺杂比例为0.2、0.4、0.6、0.8、1.0、 1.2时的荧光强度(其他步骤与上述合成mdes-cds的步骤相同),实验结果如图2b所示,结果表明当fe元素比例达到1.0时,mdes-cds荧光强度显著增强,在1.2摩尔比例时增长趋势减缓,最终将掺杂fe摩尔比定为1。
88.考察合成温度对mdes-cds荧光性质的影响。我们将其分别置于烘箱 120℃、140℃、160℃、180℃、200℃下反应6h(其他步骤与上述合成mdes-cds 的步骤相同),然后测试其荧光强度。从图2c可以看出,在120℃-180℃下mdes-cds的荧光强度增强并不明显,当反应温度达到200℃后,其荧光强度产生质的飞跃,表明200℃为其最佳反应温度。
89.考察合成时间对mdes-cds荧光性质的影响。研究了合成时间对 mdes-cds的荧光强度的影响,在200℃下分别反应2h、4h、6h、8h、10 h(其他步骤与上述合成mdes-cds的步骤相同),然后分别测试荧光强度。实验结果如图2d所示,由于6h后荧光差异并不明显,选择了6h的合成时间。
90.实施例2
91.一种金属低共熔溶剂为前驱体的mdes-cds荧光探针的制备方法,包括以下步骤:
92.(1)以dl-苹果酸作为氢键供体,乙二醇及金属(fe)作为氢键受体制备金属型低共熔溶剂(mdes)。摩尔比即为dl-苹果酸:乙二醇:金属相=2: 8:1。将混合物于80℃条件下磁性搅拌,30min后得到均匀透明的液相即为mdes。待自然冷却到室温后,放置封闭容器内待用。
93.(2)精密称取5ml mdes溶于10ml去离子水中,超声至体系混合均匀。将混合后的溶液在放置烘箱中并于200℃下反应6h,待体系冷却至室温,产物用0.22μm滤膜过滤,之后透析袋(mw:500da)透析24h,冷冻干燥得到mdes-cds。随后取适当粉末分散在超纯水中配制浓度为30μg
·
ml-1 mdes-cds溶液,保存在0-6℃低温条件下用于后续进一步表征和应用。
94.对采用上述优化方法获得的mdes-cds的形貌、组成和表面结构进行了研究,结果如图3所示。通过透射电子显微镜(tem)分析了mdes-cds形貌特征,如图3a所示,mdes-cds在水溶液中具有相对均匀的尺寸和良好的分散性,没有明显的聚集。此外,通过hr-tem图像分析其碳晶格距离为0.21nm,对应于石墨结构的晶格间距(图3a右上角的插图)。图3b表明mdes-cds 的尺寸分布主要在2-5nm范围内,且平均粒径为3.72nm。之后采用傅里叶变换红外光谱(ft-ir)鉴定了mdes-cds中的官能团。图3c中,由下至上分别是mdes-cds和mdes-cds+no
2-的红外光谱。值得注意的是,3423cm-1
处的宽而强的吸收峰是o-h的拉伸振动。此外,由于o-h的面外弯曲振动引起的mdes-cds和mdes-cds+no
2-在1398cm-1
及1384cm-1
处的吸收峰进一步证实的羟基的存在。1635cm-1
和1637cm-1
处的红外吸收峰是由羰基c=o的拉伸振动引起的,而1041cm-1
处的吸收峰可归为c-o的拉伸振动,表明结构中可能存在羧基。处在
626cm-1
的峰是c-h键的伸缩振动。根据上述表征结果,可以推导出mdes-cds的表面可能含有丰富的含氧基团,这些功能性亲水性基团大大改善了mdes-cds的水溶性和稳定性,并为亚硝酸盐的传感提供作用位点。
95.x射线光电子能谱(xps)也证实mdes-cds的元素组成和化学键合(图 4),且与ft-ir测量的元素测定结果基本一致。如图4a所示,三个大约以285,583和710ev为中心的特征峰,可分别归因于c1s,o 1s和fe 2p 的结合能,表明了fe元素的成功掺杂。图4b是c1s的高分辨率xps谱图 (从左至右分别为c=c、c-o、c=o的谱图),该图分别在284.0,285.1和 287.2ev处呈现三个拟合峰,其分别归属于c=c(sp2杂化碳),c-o和c=o。这表明制备的mdes-cds的石墨结构具有sp2杂化碳原子,以及证实了羰基官能团的存在。如图4c所示,位于530.1,531.1和532.2ev的三个拟合峰分别代表了三种类型的含氧官能团即c-o,o-h和c=o键。如图4d所示,在fe 2p的高分辨率电子能谱中,位于710.8和722.2ev处的吸收峰表明了铁以氧化态的形式的存在。这些结果进一步证实了fe元素的掺杂及含氧官能团在mdes-cds表面的形成。
96.通过紫外-可见吸收光谱(uv-vis)和荧光光谱验证了mdes-cds的光学特性(图5)。没有经任何进一步的化学改性,mdes-cds表现出优异的水溶性。如图5a所示(从左至右分别为mdes-cds、excitation、emission的结果),mdes-cds溶液在日光中是透明的淡黄色而在410nm紫外灯激发下发射处明亮的青蓝色荧光。uv-vis光谱(图5a中的黑线)显示了mdes-cds 的不同特征吸收带,包括在241和351nm处的两个紫外吸收峰,分别归因于c=c键的π-π*跃迁和c=o键的n-π*跃迁。如图5b所示,为了研究 mdes-cds的荧光发射波长是否取决于激发波长,测试其在350nm至520nm 不同激发波长下的荧光性质。结果表明mdes-cds在410nm激发下的最大发射约为473nm,且表现出明显的激发波长依赖性的特征。同时mdes-cds的绝对量子产率(abs-qy)为15.59%。
97.此外,探讨了高离子强度及辐射时间对mdes-cds荧光强度的影响(图 6)。我们将mdes-cds分别与浓度为0mol/l、0.1mol/l、0.2mol/l、0.4mol/l、 0.6mol/l、0.8mol/l、1.0mol/l的nacl溶液混合,涡旋使其混合均匀后,测试其荧光强度。图6a表明,在nacl浓度高达1m的情况下,荧光强度可以基本保持稳定。对于辐射时间,我们将其置于紫外灯410nm波长下连续照射90min,每隔5min测试其荧光强度,从图6b可以看出在410nm 紫外光辐射90min以内荧光强度可以保持在75%以上。说明mdes-cds可作为一种稳定优异的荧光探针用于传感测定。
98.实施例3
99.一种检测亚硝酸盐的方法,包括以下步骤:
100.精密称取mdes-cds 3.0mg置于100ml容量瓶中并定容,得到对应的储备液。将20μl的mdes-cds溶液(浓度为30μg
·
ml-1
)与200μl待测样品在离心管中混合,调节ph值,并加水定至1ml。反应溶液经恒温水浴震荡20min后进行荧光测试。
101.检测条件:以410nm作为激发波长,并以475nm处的荧光值作为no
2-的测定值,发射狭缝宽度设置为10nm,测试条件一式三份(即制备三份平行样品进行测定)。
102.当制作标准曲线时,待测样品可以为不同浓度的nano2溶液。采取上述的方法反应后,检测荧光强度,绘制荧光强度关于亚硝酸盐浓度的标准曲线。根据未知浓度的待测样品的荧光强度,结合标准曲线,可以计算待测样品中的亚硝酸盐浓度。
103.进行实际样品测定时,可以首先对实际样品进行适当的预处理,比如粉碎、离心、过滤和稀释等。然后将其与mdes-cds混合,在ph=2的条件下,于60℃下反应20min,测试其荧光强度。将该数值代入到线性回归方程中,即可计算出实际样品中亚硝酸盐的浓度。
104.实施例4
105.(1)制备mdes-cds探针体系用于亚硝酸盐检测条件的优化。分别考察溶液酸度、反应时间、温度等变量对mdes-cds检测亚硝酸盐性能的影响,结果如图7所示。
106.为了考察溶液酸度对检测亚硝酸盐性能的影响,我们用hcl溶液配置了 ph分别为2.08、2.59、3.15、3.64、3.93、4.26、4.66、5.40、5.90、6.50、 6.98的溶液,向其中加入mdes-cds和亚硝酸盐溶液,涡旋混合均匀,60℃下反应20min,然后用荧光分光光度计测试其荧光强度。溶液酸度(ph值) 的影响如图7a所示,mdes-cds自身的荧光强度在ph值2-7范围内迅速降低。当ph达到7时,其自身荧光消失,因为选取ph=2作为分析检测的最优条件。
107.对于反应温度的优化,我们将mdes-cds与亚硝酸盐溶液混合置于ph=2 的条件下,分别在25℃、30℃、35℃、40℃、45℃、50℃、55℃、60℃下反应20min,然后测试其荧光强度。如图7b所示,随着温度的增加,亚硝酸盐对mdes-cds的猝灭程度不断增加,在更高温度下促进了反应速度,在60℃时,荧光猝灭程度最大,因此我们最终选取60℃作为最佳反应温度。
108.图7c研究了添加亚硝酸盐后荧光强度随时间变化的趋势,我们将 mdes-cds与亚硝酸盐溶液混合,在ph=2,温度为60℃的条件下分别反应0 min、0.66min、3min、5min、10min、15min、19min、22min、25min、 27min、29min、32min,发现473nm处的荧光强度在5min内淬灭了59%, 20min后高达96%,表明反应在20min内完成。因此,选择20min作为最佳反应时间。
109.(2)在mdes-cds最佳合成条件下(200℃,6h,摩尔比dl-苹果酸:乙二醇:fe=2:8:1),研究了mdes-cds对亚硝酸盐的响应能力。将mdes-cds 在ph=2的条件下分别与不同浓度的亚硝酸盐混合,在60℃下反应20min,然后测试其荧光强度。图8表明了在不同浓度亚硝酸盐存在下的荧光光谱,由上至下分别为kb(空白)、0.2μm、1μm、5μm、10μm、20μm、30μm、 40μm、50μm、60μm、80μm、100μm、150μm、300μm的曲线,从图8 中可以看出,随着亚硝酸盐浓度(0-300μm)的增加,mdes-cds的荧光强度逐渐下降。
110.(3)如图9所示,我们将荧光强度数值对亚硝酸盐浓度做点线图,发现荧光强度跟随亚硝酸盐浓度在0.2-80μm范围内呈现线性响应(0.2μm、 3μm、7μm、15μm、20μm、30μm、40μm、50μm、60μm、70μm、80μm),得到的回归方程为y=-39.62[no
2-]+4212,线性系数r2为0.9932。检测限(lod, s/n=3)。
[0111]
通过平行测定11组空白溶液,计算出他们3倍的标准方差再比上线性方程斜率而计算得出亚硝酸盐浓度的检测限为50nm。
[0112]
进行实际样品检测时,例如香肠,先对其进行适当的预处理,然后将其加入亚硝酸盐和mdes-cds的混合溶液中,在与步骤(2)相同的条件下进行反应,测试其荧光值,将其代回线性方程,即可得知香肠中含有亚硝酸盐的浓度。这使得我们能够准确定量实际样品中的亚硝酸盐。
[0113]
(4)不同干扰离子对mdes-cds溶液荧光强度影响的对比图如图10所示。
[0114]
考察了mdes-cds传感平台在亚硝酸盐检测中的选择性,取多个1ml的离心管,分别
在1ml的离心管中加入实施例2中的mdes-cds溶液20μl和 200μl五倍浓度的干扰物质,干扰物质包括阴离子、金属离子以及一些添加剂,阴离子例如:no
2-、f-、cl-、br-、i-、oh-、no
3-、so
42-、so
32-、co
3-、ch3coo-、 hco
3-等,金属离子例如:fe
3+
、mg2、k
+
、na
+
、cu
2+
、zn
2+
、ca
2+
、fe
2+
等,添加剂例如:dl-苹果酸、l-半胱氨酸、乳酸、抗坏血酸、柠檬酸、葡萄糖、谷氨酸、谷胱甘肽等,测量并记录荧光强度。
[0115]
实验结果如图10a所示,可以观察到只有亚硝酸盐可以引起荧光强度的急剧下降,而在其他阴离子的存在下没有观察到明显的荧光变化。
[0116]
此外,在mdes-cds和亚硝酸盐共存的条件下,向其中分别加入200μl 五倍浓度上述的干扰物质,干扰物质包括阴离子、金属离子、添加剂,阴离子、金属离子、添加剂的种类同上,测量并记录荧光强度,可以观察到猝灭程度与只有亚硝酸盐存在时无太大差别,如图10b所示,表明在亚硝酸盐与干扰离子共存条件下进行干扰实验,mdes-cds的荧光强度受到的影响微乎其微。这表明该所制备的mdes-cds对亚硝酸盐的检测具有高选择性。
[0117]
实施例5
[0118]
一种检测ph的方法,包括以下步骤:
[0119]
精密称取mdes-cds 3.0mg置于100ml容量瓶中并定容,得到对应的储备液。该实验将20μl的mdes-cds溶液(浓度为30μg
·
ml-1
)置于盛有待测样品的离心管中,定容至1ml。检测条件:以410nm作为激发波长,并以475nm处的荧光值作为ph的测定值,发射狭缝宽度设置为10nm,测试条件一式三份(即制备三份平行样品进行测定)。
[0120]
当制作标准曲线时,待测样品为不同ph的溶液。采取上述的方法反应后测定荧光强度,绘制荧光强度关于ph的标准曲线。根据未知ph的待测样品的荧光强度,结合标准曲线,可以计算待测样品的ph。
[0121]
当进行实际样品检测时,可以首先对实际样品(如水)进行适当的预处理(离心、过滤、稀释等),然后将其与mdes-cds混合,与60℃下反应20 min,测试其荧光强度。将该数值带入到线性回归方程中,即得得知实际样品的ph值。
[0122]
实施例6
[0123]
制备mdes-cds探针体系用于ph的优化及检测。
[0124]
1)精密称取mdes-cds 3.0mg置于100ml容量瓶中并定容,得到对应的储备液。该实验将20μl的mdes-cds溶液(浓度为30μg
·
ml-1
)置于盛有不同ph溶液的离心管中,定容至1ml。检测条件:以410nm作为激发波长,并以475nm处的荧光值作为ph的测定值,发射狭缝宽度设置为10nm,测试条件一式三份(即制备三份平行样品进行测定)。
[0125]
2)在mdes-cds最佳合成条件下(200℃,6h,dl-苹果酸:乙二醇: fe=2:8:1,在此条件下合成的mdes-cds荧光效果最好),研究了mdes-cds 对ph的响应能力。荧光光谱图如图11所示,从上至下分别为ph为2.08、 2.59、3.64、3.96、4.26、4.66、5.30、5.91、6.50、6.98的曲线,从图 11中可以看出,随着ph值从2增加到7,mdes-cds荧光强度明显猝灭,且溶液由浅黄色-黄色-绿色的颜色转变为该样品提供了优异的特性,可作为ph 检测的颜色指示剂。
[0126]
3)如图12所示,mdes-cds的荧光强度随ph值在2-7之间呈线性减弱 (ph为2.08、2.59、3.15、3.64、3.93、4.26、4.66、5.40、5.90、6.50、 6.98,可以用hcl和naoh调节获得不同的ph溶液),线性方程为y=-923.2 [ph]+6660,r2=0.9931。
[0127]
对于待测样品,采用上述同样的操作,并检测荧光强度,通过上述的线性方程可以
获得ph。上述方法为我们对于实际样品如各种水环境的ph检测奠定了基础。
[0128]
以上实施例仅用以说明本发明的技术方案,仅为便于该技术领域的普通技术人员能理解和使用发明而非对其进行限制;熟悉本领域技术的人员依然可以对本发明的具体实施方式进行修改或者对部分技术特征进行等同替换;并把在此说明的一般原理应用到其他实施例中而不必经过创造性的劳动。因此,本发明不限于上述实施例,本领域技术人员根据本发明的揭示,不脱离本发明范畴所做出的改进和修改都应该在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1