通过嗜盐古菌生物降解有机污染物的制作方法
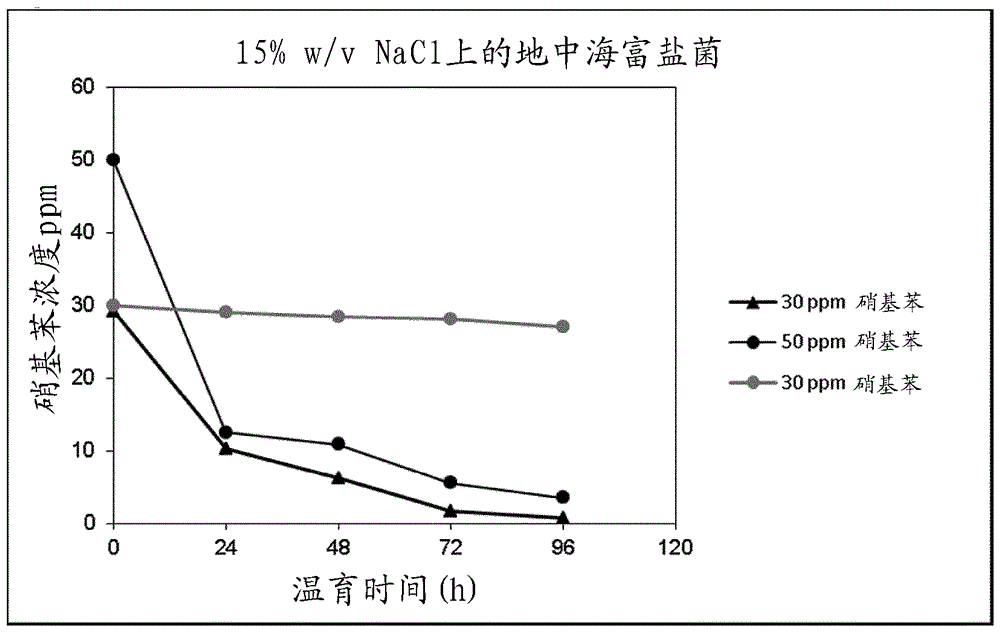
本发明涉及减少高盐废水中至少一种选自硝基苯、甲酸盐/甲酸根、苯酚、4,4'-亚甲基二苯胺(mda)和苯胺的污染物的含量的方法,所述方法包括以下步骤:(a)提供包含高盐废水和所述至少一种污染物的组合物a,和(b)使组合物a与地中海富盐菌(haloferaxmediterranei)细胞接触,由此生成包含所述组合物a和地中海富盐菌细胞的组合物b。本发明进一步涉及生产氯气和氢氧化钠的方法。本发明进一步涵盖了包含高盐废水、所述至少一种污染物和地中海富盐菌细胞的组合物。工业过程产生数百万升高盐残余水。据估计,全球流出物中的5%是高盐的。例如,二苯基甲烷系列的二胺和多胺(其为用于生产聚氨酯的主要中间体)的生产伴随着大量高盐废水的产生(参见us2009240076)。二苯基甲烷系列的二胺和多胺通常通过在酸催化剂(如盐酸)的存在下使苯胺与甲醛反应来生产。在产生二苯基甲烷系列的二胺和多胺后,通过添加碱(通常为氢氧化钠水溶液)来中和酸催化剂。通常,添加中和剂,以使所得中和混合物可以分离为含有二苯基甲烷系列的多胺及过量苯胺的有机相和含有氯化钠与残余有机成分的水相(即高盐废水)。过去,高盐废水通常在通过物理和/或化学方法(例如吸附、臭氧化和电化学处理)除去有机成分后弃置,参见us2009240076。但是,用于处理含有有机化合物的残余水的物理和/或化学方法通常不能将含盐残余物流中的总有机碳含量减少至所要求的最高水平以下。残余水(如生产二苯基甲烷系列的二胺和多胺所产生的废水)常常包含有机污染物如甲酸盐/甲酸根、苯酚、苯胺、硝基苯和4,4'-亚甲基二苯胺(mda),并在用淡水大量稀释后排入环境中或通过物理-化学方法处理它们。因此,需要高盐废水的替代处理方案。通过好氧和厌氧生物处理来处理有机物的替代系统目前是主要研究焦点。常规的非嗜极微生物不能在高盐浓度下进行有机污染物的去除。当盐胁迫与污染胁迫相叠加时,嗜盐菌在高盐浓度的存在下降解或转化不同有机污染物的能力非常重要。因此,非常需要能够在高盐浓度下生长或能够降解或转化高盐废水中的不同有机污染物的微生物。高盐废水中存在的典型有机污染物是甲酸盐/甲酸根、苯酚、苯胺、硝基苯和4,4'-亚甲基二苯胺(mda)。这些化学中间体通常用于制造除草剂、显影剂、香水、药物、橡胶和染料。由于它们在工业中的广泛使用,越来越大量的这些化合物被释放到土壤和水体中,这对活生物体构成了环境威胁和健康风险。此外,高盐溶液是氯碱工艺的重要材料,氯碱工艺是电解氯化钠(nacl)的工业方法。它是用于生产氯气和氢氧化钠的技术。但是,需要非常纯的高盐溶液。因此,难以将再循环的高盐废水用于氯碱工艺。例如,来自亚甲基二胺生产的高盐废水含有有机污染物如甲酸盐/甲酸根、苯酚、苯胺、硝基苯和4,4'-亚甲基二苯胺(mda),其应当在对废水施以氯碱工艺之前除去。例如,必须除去甲酸盐/甲酸根,否则氯气将被co2污染。先前对有机化合物(如甲酸盐/甲酸根或苯胺)的生物降解的研究集中于单一化合物在温和条件下的降解或转化。但是,在高盐浓度(例如高达2000mg/lnacl)的存在下能够同时降解多种有机化合物(如甲酸盐/甲酸根、苯酚、苯胺、mda和硝基苯)的微生物目前还未知。例如,苯胺和/或甲酸盐/甲酸根的生物降解先前已经报道为在温和条件下被假单胞菌属(pseudomonas)、毛单胞菌属(comamonas)、不动杆菌属(acinetobacter)、红球菌属(rhodococcus)、弗拉特氏菌属(frateuria)、莫拉菌属(moraxella)、代尔夫特菌属(delftia)、诺卡菌属(nocardia)和迪茨氏菌属(dietzia)的多种细菌物种降解。但是,含有苯胺和/或甲酸盐/甲酸根和潜在的其它有机污染物如硝基苯、苯酚和/或mda的残余物流常常具有提高的盐度,并且由于高盐浓度破坏普通生物处理系统中存在的细菌代谢,因此高盐残余物流的处理是一项挑战。而且,将普通细菌用于高盐残余物流需要用淡水(如果有的话)预先稀释以降低盐度。wo2013/124375公开了通过某些嗜盐和/或嗜盐嗜碱微生物减少总有机碳。woolard和irvine(1995)公开了在序批式反应器中处理高盐废水(woolard和irvine.treatmentofhypersalinewastewaterinthesequencingbatchreactor.waterresearch29.4(1995):1159-1168)。rodriguez-valeria等人(1983)报道了地中海盐杆菌(halobacteriummediterranei)的鉴定,这是一种利用碳水化合物的极端嗜盐菌的新物种。已经显示地中海盐杆菌能够使用许多不同的化合物作为唯一的碳和能量来源,并且不产生h2s。campo等人(2011)涉及来自被芳族化合物污染的土壤的活性污泥。观察到高达5mg/l苯胺的胺类(如苯胺和mda)的好氧生物降解(campo,p等人,aerobicbiodegradationofaminesinindustrialsalinewastewaters.chemosphere85.7(2011):1199-1203)。antón等人(1988)报道了通过地中海富盐菌生产细胞外多糖。作者表明,地中海富盐菌能够产生胞外聚合物质,特别是含有甘露糖作为主要组分的杂多糖,这使菌落具有典型的黏液特性。该物质在所检测的几种条件和底物下产生,尽管用糖类(特别是葡萄糖)作为碳和能量来源获得最高产率(antón,j等人,productionofanextracellularpolysaccharidebyhaloferaxmediterranei.appliedandenvironmentalmicrobiology54.10(1988):2381-2386)。oren(2000)研究了嗜盐菌。作者提到富盐菌属(haloferax)物种用于生产聚β羟基链烷酸酯或细胞外多糖的潜在用途。特别地,据报道,可以由嗜盐古细菌地中海富盐菌以高产率获得作为生物可降解塑料材料的来源的β-羟基链烷酸酯。此外,地中海富盐菌可以积聚与罗尔斯顿氏菌属一样多的β-羟基链烷酸酯,并可以使用淀粉作为廉价的碳和能量来源(oren,a.diversityofhalophilicmicroorganisms:environments,phylogeny,physiology,andapplications.journalofindustrialmicrobiologyandbiotechnology28.1(2002):56-63)。oren等人(2014)进一步报道了地中海富盐菌在代谢上非常多样,并具有广泛的耐盐性。根据作者的说法,地中海富盐菌是一种古细菌,其比任何其它可比较的极端嗜盐菌生长更快,具有宽的耐盐性窗口,可以在简单和复杂的底物上生长,并降解聚合物质,具有不同的厌氧生长模式,可以积聚储存聚合物,产生气体囊泡,并分泌能够杀死其它古菌的嗜盐菌素(oren,a等人,microbialweedsinhypersalinehabitats:theenigmaoftheweed-likehaloferaxmediterranei.femsmicrobiologyletters359.2(2014):134-142)。尽管存在许多涉及芳族化合物的微生物降解的报道,但是在高盐浓度下有机污染物的降解仍然受到限制。因此,当盐胁迫叠加污染胁迫时,在高盐浓度存在下降解或转化有机污染物的微生物至关重要。特别地,非常需要减少高盐废水中硝基苯、甲酸盐/甲酸根、苯酚、4,4'-亚甲基二苯胺(mda)和/或苯胺的含量的手段和方法。据报道,古菌菌株地中海富盐菌dsm.1411具有代谢多样性,可能使用大范围的单一碳源。已报道,地中海富盐菌dsm.1411可以使用广泛的糖类、有机酸和甘油以及某些氨基酸作为底物,当它们作为唯一碳源存在时促进生物量增长。对于水的生物修复过程,该菌株还用于除去硝酸盐和亚硝酸盐。但是,不存在一个关于该菌株在高盐废水中生长的报道,也没有一个关于底物甲酸盐/甲酸根、苯酚、苯胺、硝基苯和/或4,4'-亚甲基二苯胺(mda)在高盐条件下降解的报道。作为本发明基础的技术问题可以视为提供符合前述需求的方法。该技术问题通过权利要求和下文中表征的实施方案来解决。有利地,在本发明的研究中已发现,地中海富盐菌dsm.1411在高盐度条件下有效地降解不同污染物。特别地,已经显示可以通过地中海富盐菌dsm.1411降解污染物,如甲酸盐/甲酸根、苯酚、硝基苯、苯胺和4,4'-亚甲基二苯胺(mda)。本发明的发现是令人惊讶的。例如,迄今为止尚没有关于在盐度下硝基苯的生物降解的报道。因此,这是首次显示该组分在盐的存在下是可生物降解的。此外,显示了地中海富盐菌dsm.1411的细胞可以同时降解来自其高盐环境的所有前述化合物。本发明的这些发现可以应用于自然和工业残余物流。因此,本发明涉及减少废水中至少一种选自硝基苯、甲酸盐/甲酸根、苯酚、亚甲基二苯胺(mda),特别是4,4'-亚甲基二苯胺(mda)、和苯胺的污染物的含量的方法,所述方法包括以下步骤:(a)提供包含废水和所述至少一种污染物的组合物a,和(b)使组合物a与地中海富盐菌细胞接触,由此生成包含所述组合物a和地中海富盐菌细胞的组合物b。根据本发明的方法的步骤(a),将提供包含废水的组合物a。所述组合物a是包含所述废水和所述至少一种选自硝基苯、甲酸盐/甲酸根、苯酚、4,4'-亚甲基二苯胺(mda)和苯胺的污染物的溶液。该废水将为高盐废水,即如下文中定义的具有高nacl浓度的废水。特别地,该废水将为包含所述至少一种污染物的工业废水,如工业盐水。根据本发明的方法的步骤(b),使组合物a与地中海富盐菌细胞接触。由此,生成包含组合物a(并由此包含废水和所述至少一种污染物)和地中海富盐菌细胞(即该菌株的细胞)的组合物b。在本发明的方法的一个实施方案中,通过将组合物a与细胞混合以使组合物a与该细胞接触。地中海富盐菌菌株是嗜盐菌株,由此需要高nacl浓度以便生长。因此,组合物b将以高浓度包含nacl。这使得能够在不稀释废水的情况下处理高盐废水(即使得能够如本文中所述那样减少污染物)。因此,组合物b,以及由此的高盐废水,将以高浓度包含nacl。本文中所述的高nacl浓度是基于废水或组合物的总体积计至少6%(w/v)的浓度。废水、组合物a或b可以以高达nacl的饱和浓度的浓度包含nacl,因为在作为本发明基础的研究中已经显示,即使在20.0%(w/v)的nacl浓度下也可以减少例如苯胺含量。因此,该浓度的上限在原则上是nacl的饱和浓度。因此,高nacl浓度是基于废水或组合物的总体积计至少6%(w/v)至最高25%(w/v)的浓度。因此,该废水不是半咸水或海水,这二者均具有较低的nacl浓度。优选地,高nacl浓度为基于组合物或废水(例如组合物b)的总体积计至少7%(w/v)、更优选至少10%(w/v)、甚至更优选至少12%(w/v)、和最优选至少15%(w/v)的nacl浓度。尽管高nacl浓度的上限在原则上是nacl的饱和浓度,但设想废水、组合物a或b以小于饱和浓度的浓度包含nacl。优选地,废水、组合物a或组合物b中的nacl浓度为基于组合物或废水的总体积计小于23%(w/v)、更优选小于22%(w/v)、甚至更优选小于20%(w/v)。在作为本发明基础的研究中,已经显示,在大约17%(w/v)的nacl浓度下实现了最佳处理。因此,同样基于组合物或废水的总体积计,废水、组合物a、或b优选以12%至22%(w/v)的浓度、更优选以12%至20%(w/v)的浓度、甚至更优选以15%至20%(w/v)的浓度、和最优选以16%至18%(w/v)的浓度包含nacl。最佳nacl浓度可以取决于污染物。例如,相对于苯胺,废水、组合物a或b优选以基于组合物或废水的总体积计12%至最高25%(w/v)的浓度包含nacl。此外,最佳nacl浓度可能取决于废水/组合物中污染物的浓度。例如,在作为本发明基础的研究中,观察到如果苯胺浓度高(例如大于20mg/l)的话,更高浓度的nacl使得能够促进苯胺的减少。可以在各种工业废水中发现高nacl浓度。在一个优选实施方案中,从亚甲基二胺生产(作为聚氨酯的预产物)中分离出高盐废水。因此,本发明的方法的步骤a)可以包括从亚甲基二胺生产中分离高盐废水。特别地,该废水来自于,即分离自二苯基甲烷系列的二胺和多胺的生产。术语“二苯基甲烷系列的二胺和多胺”是指以下类型的胺和胺的混合物:其中n是2或大于2的整数。如本文中其它地方所述,二苯基甲烷系列的二胺和多胺是聚氨酯的预产物,并可以通过公知的方法来生产。生产所述二苯基甲烷系列的二胺和多胺的优选方法例如公开在ep1813598a1中,其经此引用以其全文并入本文。在一个实施方案中,通过在酸催化剂的存在下使苯胺与甲醛反应来生产二苯基甲烷系列的二胺和多胺。在一个实施方案中,将盐酸用作酸催化剂。在生产二苯基甲烷系列的二胺和多胺后,通过添加氢氧化钠来中和该酸催化剂。优选地,添加中和剂,以使所得中和混合物可以分离为含有二苯基甲烷系列的二胺和特别是多胺以及过量的苯胺的有机相和水相。该水相是如本文中所述的含有至少一种污染物的高盐废水。在本发明的另一实施方案中,高盐废水分离自,即来自于碳酸二芳酯的生产。碳酸二芳酯(更特别为碳酸二苯酯)的生产通常通过连续法,通过光气的生产或引入以及在惰性溶剂中在碱和氮催化剂的存在下在反应界面处单酚与光气的后续反应来进行。碳酸二芳酯的生产在本领域中是公知的。优选的生产方法描述在us2008053836中,其全部内容经此引用并入本文。在本发明的另一实施方案中,高盐废水分离自,即来自于聚碳酸酯的生产。在进行步骤a)之前,可能已经对高盐废水施以一个或多个纯化步骤。所述一个或多个纯化步骤将能够减少废水中溶剂残余物的量。这例如可以通过用蒸汽汽提溶液和/或用吸附剂(特别是用活性炭)处理来实现。此外,该废水可能已经过滤。此外,该高盐废水可能已经通过用臭氧处理废水(臭氧化)来纯化。臭氧化(也称为臭氧处理)是基于将臭氧注入水中的化学水处理技术(参见例如wo2000078682)。此外,设想在实施本发明的方法的步骤a)之前浓缩废水的nacl浓度,例如通过膜蒸馏法、渗透蒸馏或反渗透,此外,在本文中其它地方描述了浓缩包含nacl的组合物的优选方法。有利地,在本发明的上下文中已经表明,地中海富盐菌菌株的细胞能够减少高盐盐水中的本文中所述的至少一种污染物(至少一种选自硝基苯、甲酸盐/甲酸根、苯酚、亚甲基二苯胺,特别是4,4'-亚甲基二苯胺(iupac名称:双(4-氨基苯基)甲烷)和苯胺的污染物)的含量。因此,设想高盐废水、组合物a和组合物b包含所述至少一种污染物。根据本发明,至少一种选自硝基苯、甲酸盐/甲酸根、苯酚、亚甲基二苯胺,特别是4,4'-亚甲基二苯胺(mda)和苯胺的污染物的含量将减少,即在高盐废水中并由此在组合物a和b中的所述至少一种污染物的含量将减少。本文中所用的术语“至少一种污染物”是指一种或多于一种。因此,可以减少一种、两种、三种、四种或五种污染物的含量。在一个优选实施方案中,减少一种污染物的含量。在一个优选实施方案中,通过本发明的方法减少四种污染物的含量:根据本发明的方法所述的甲酸盐/甲酸根、苯酚、亚甲基二苯胺,特别是4,4'-亚甲基二苯胺(mda)和苯胺。在另一优选实施方案中,通过本发明的方法减少根据本发明的方法所述的所有五种污染物的含量。特别地,所述含量同时减少。因此,高盐废水、组合物a和b将包含所述至少一种污染物,优选至少0.5mg/l的甲酸盐/甲酸根、0.5mg/l的苯酚、0.5mg/l的硝基苯、0.5mg/l的4,4'-亚甲基二苯胺(mda)和/或0.5mg/l的苯胺,更优选3mg/l的甲酸盐/甲酸根、3mg/l的苯酚、3mg/l的硝基苯、3mg/l的4,4'-亚甲基二苯胺(mda)和/或3mg/l的苯胺。以下应用于污染物苯胺:优选地,高盐废水、组合物a和/或组合物b以至少0.5mg/l的量、更优选以至少2mg/l的量、和最优选以至少5mg/l的量包含苯胺。此外,设想组合物a(或b)以至少10mg/l的量、特别是以至少20ml/l的量包含苯胺。同样优选地,高盐废水、组合物a和/或组合物b以1至100mg/l的量、更优选以2至50mg/l的量、和最优选以2至20mg/l的量包含苯胺。此外,设想其以2至12mg/l的量包含苯胺。以下应用于污染物甲酸盐/甲酸根:优选地,高盐废水、组合物a和/或组合物b以至少10mg/l的量、更优选以至少30mg/l的量、和最优选以至少100mg/l的量包含甲酸盐/甲酸根。同样优选地,高盐废水、组合物a和/或组合物b以10mg/l至10g/l的量、更优选以30mg/l至1g/l的量、和最优选以50至500mg/l的量包含甲酸盐/甲酸根。以下应用于污染物硝基苯:优选地,高盐废水、组合物a和/或组合物b以至少1mg/l的量、更优选以至少5mg/l的量、和最优选以至少10mg/l的量包含硝基苯。同样优选地,高盐废水、组合物a和/或组合物b以1至100mg/l的量、更优选以2至50mg/l的量、和最优选以2至20mg/l的量包含硝基苯。以下应用于污染物4,4'-亚甲基二苯胺:优选地,高盐废水、组合物a和/或组合物b以至少0.25mg/l的量、更优选以至少0.5mg/l的量、和最优选以至少1mg/l的量包含4,4'-亚甲基二苯胺。此外,设想其以至少3mg/l的量包含4,4'-亚甲基二苯胺。同样优选地,高盐废水、组合物a和/或组合物b以0.25至30mg/l的量、更优选以1至10mg/l的量、和最优选以2至7mg/l的量包含4,4'-亚甲基二苯胺。此外,设想其以0.5至20mg/l的量包含4,4'-亚甲基二苯胺。以下应用于污染物苯酚:优选地,高盐废水、组合物a和/或组合物b以至少1mg/l的量、更优选以至少5mg/l的量、和最优选以至少10mg/l的量包含苯酚。此外,设想其以至少20mg/l的量包含苯酚。同样优选地,高盐废水、组合物a和/或组合物b以1至500mg/l的量、更优选以5至100mg/l的量、和最优选以5至50mg/l的量包含苯酚。此外,设想其以5至20mg/l的量包含苯酚。优选地,组合物a具有大于50mg/l、更优选大于60mg/l、甚至更优选大于60mg/l、和最优选大于65mg/l的总有机碳(“toc”)含量。此外,设想组合物a具有大于70mg/l、特别是大于70mg/l的toc(总有机碳)含量。优选地,组合物a具有高达1000mg/l和更高的总有机碳(“toc”)含量。根据本发明,高盐废水的至少一种污染物的含量和由此组合物a和组合物b各自的所述至少一种污染物的含量将减少(术语“含量”、“量”和“浓度”在本文中可互换使用)。所述至少一种污染物选自硝基苯、甲酸盐/甲酸根、苯酚、亚甲基二苯胺,特别是4,4'-亚甲基二苯胺(mda)和苯胺。本文中所用的术语“减少”指的是高盐废水的污染物(即至少一种污染物)含量的显著减少。优选地,该术语表示减少高盐废水、组合物a和组合物b中分别存在的所述污染物的总含量的至少30%、至少50%、至少70%或特别是至少90%或至少95%的所述污染物。因此,组合物b(或组合物a)中的如本文中所述的污染物的总含量将减少至少30%、至少50%、至少70%或特别是至少90%、或至少95%。所得组合物c,即经处理的废水,优选以小于5mg/l的量包含苯胺。更优选地,其以小于1mg/l和最优选小于0.2mg/l的量包含苯胺。同样优选地,在实施本发明的方法后,经处理的废水以小于15mg/l、更优选小于10mg/l和最优选小于5mg/l的量包含甲酸盐/甲酸根。同样优选地,在实施本发明的方法后,经处理的废水以小于15mg/l、更优选小于10mg/l和最优选小于5mg/l的量包含硝基苯。同样优选地,在实施本发明的方法后,经处理的废水以小于15mg/l、更优选小于10mg/l和最优选小于5mg/l的量包含4,4'-亚甲基二苯胺。同样优选地,在实施本发明的方法后,经处理的废水以小于15mg/l、更优选小于10mg/l和最优选小于5mg/l的量包含苯酚。此外,设想完全消除所述至少一种污染物。通过实施本发明的方法,toc含量也将减少(即除了所述至少一种污染物的含量之外)。优选地,经处理的废水具有小于40mg/l、更优选小于30mg/l和最优选小于20mg/l的toc含量(特别是在将细胞与组合物b分离后,如本文中其它地方所述)。优选地,本文中所述的至少一种污染物的含量通过本文中所述的地中海富盐菌细胞的存在和由此通过其活动而减少。优选地,通过经由所述细胞降解污染物来减少所述含量。通过稀释废水、或组合物a或b降低至少一种污染物的浓度不被视为减少所述至少一种污染物的含量。因此,术语“减少至少一种污染物的含量……”不包括通过稀释作用(例如通过稀释高盐废水或组合物a或b)降低所述至少一种污染物的浓度。根据本发明要使用的细胞是地中海富盐菌细胞。优选地,所述细胞是来自已经以dsm编号1411保藏在dsm(deutschesammlungvonmikroorganismenundzellkulturen,braunschweig,germany)的地中海富盐菌菌株的细胞。因此,预期使用来自地中海富盐菌dsm1411菌株的细胞(在本文中缩写为hfx)。该菌株已经由rodriguez-valera,f.,juez,g.,kushner,d.j.(1983).halobacteriummediterraneisp.nov.,anewcarbohydrate-utilizingextremehalophile.syst.appl.microbiol.4:369-381进行了描述。该文献经此引用以其全文并入本文。如何培养该菌株在本领域中是公知的。例如,对于该菌株,可以例如从dsmz数据库评估合适的培养条件。适于该菌株的培养基组成描述在实施例部分的实施例1中。要在步骤b)中与组合物a接触(即与组合物a混合)的细胞应当是活的,即活细胞。如何评估细胞是否存活可以通过公知的方法来评估。当然,一定百分比的要与组合物a混合的细胞可能不是活的。但是,本领域技术人员考虑到了这一点。在一个实施方案中,将地中海富盐菌的细胞悬浮液与组合物a混合。该细胞优选源自相应菌株的细胞的预培养物。该悬浮液应包含合适的底物(即碳源)。尽管并非必需,细胞的预培养可以在本文中所述的至少一种污染物的存在下进行。要与组合物a混合(即与组合物a接触)的本文中所述的地中海富盐菌的细胞的量可以由本领域技术人员确定。要混合的细胞量将允许充分地减少在高盐废水中和由此在组合物a和b(其包含高盐废水)中的本文中所述的至少一种污染物。该量例如取决于要通过本发明的方法处理的组合物a的体积。通常,要处理的组合物a的体积越大,要使用的细胞的量也将越大。本领域技术人员将考虑到这一点。该混合可以在合适的容器中进行。在一个实施方案中,该混合在生物反应器中进行。本文中所用的术语“生物反应器”是指其中严密控制条件以允许减少本文中所述的至少一种污染物的含量的系统。在一个实施方案中,所述生物反应器是搅拌釜反应器。优选地,该生物反应器由非腐蚀性材料如不锈钢制成。该生物反应器可以具有任何尺寸,只要其可用于组合物b的温育。优选地,该生物反应器允许大幅度减少所述至少一种污染物的含量。因此,设想该生物反应器具有至少1、10、100、500、1000、2500或5000升的体积或任何中间体积。但是,还设想以小规模(如采用5至100毫升的组合物b)实施本发明的方法。组合物b可以进一步包含使得能够通过地中海富盐菌细胞减少所述至少一种污染物的含量的培养基组分。此类培养基组分在本领域中是公知的,并包括例如nh4cl、kh2po4、na2so4、mgcl2(例如mgcl2•6h2o)、fecl3、mgso4、cacl2(例如cacl2•2h2o)、kbr和kcl。在一个实施方案中,组合物b包含磷源、氮源、硫源、钾源和/或镁源(作为培养基组分)。组合物b可以进一步包含微量元素如铁、铜、锌和钴。在一个实施方案中,在组合物a与细胞接触后,即该组合物与细胞混合(如步骤(b)中所述)后,将培养基组分添加到组合物b中。可以由本领域技术人员毫不费力地选择合适的培养基组分。此外,本领域技术人员可以毫不费力地确定合适的培养基组分浓度。例如,以下培养基组分的以下浓度范围和浓度被认为是合适的。但是,本发明不限于上文提及的培养基组分和以下浓度范围。组合物b中的浓度:•nh4cl:0.5至3g/l,例如1.5g/l•kh2po4:0.05至0.5g/l,例如0.15g/l•mgcl2*6h2o:0.5至3g/l,例如1.3g/l•cacl2*2h2o:0.1至2g/l,例如0.55g/l•kcl:0.5至3g/l,例如1.66g/l•mgso4.7h2o:0.5至3g/l,例如1.15g/l•fecl3:0.001至0.1g/l,例如0.005g/l•kbr:0.1至2g/l,例如0.5g/l•mncl2.4h2o:0.001至0.1g/l,例如0.003g/l。在实施例部分的表1中规定了培养基组分的其它优选浓度。此外,该组合物可以包含微量元素。在本发明的一个优选实施方案中,组合物b进一步包含底物。所述底物将允许地中海富盐菌细胞生长。底物是否允许菌株生长可以由本领域技术人员毫不费力地评估。在一个实施方案中,除了至少一种选自硝基苯、甲酸盐/甲酸根、苯酚、亚甲基二苯胺,特别是4,4'-亚甲基二苯胺(mda)和苯胺的污染物之外,所述底物也将存在,因为污染物仅被降解而不用作底物。因此,预期的是,该底物不是所述至少一种污染物,即不是硝基苯、甲酸盐/甲酸根、苯酚、亚甲基二苯胺,特别是4,4'-亚甲基二苯胺(mda)和苯胺。因此,该底物在本文中也被称为辅底物。优选地,所述底物的存在使得能够促进例如苯胺和甲酸盐/甲酸根的含量的减少(参见实施例部分)。例如,添加甘油显著提高了所有污染物(甲酸盐/甲酸根、苯胺、mda、硝基苯和苯酚)的降解率,同样参见实施例和图1。优选将底物添加到组合物b中。因此,设想底物在组合物a中不存在或基本不存在。所述底物优选是碳水化合物(其使得地中海富盐菌细胞能够生长),所述底物更优选是甘油、有机酸或糖(其使得地中海富盐菌细胞能够生长),该底物更优选选自甘油、乙酸盐/乙酸根、葡萄糖、蔗糖、乳酸盐/乳酸根、苹果酸盐/苹果酸根、琥珀酸盐/琥珀酸根和柠檬酸盐/柠檬酸根。在一个特别优选的实施方案中,该底物是甘油。优选地,如果温育以连续过程的方式进行,则组合物b包含底物。底物将允许生物量以缓慢速率增长以实现连续模式下降解的稳定性。有利地,观察到例如将另外的底物(甘油)连续添加到组合物b(即含有组合物b的反应器)中时,一旦细胞以其最大生长速率生长,苯胺的含量就可以连续下降。本领域技术人员可以毫不费力地确定适于底物的浓度或浓度范围。减少废水(组合物a)中的本文中所述至少一种污染物的含量和由此本文中所述的温育优选在碳限制下进行。因此,设想底物的浓度(如生长)允许生物量以缓慢速率生长。由此产生新鲜的生物量,这使得能够以连续方式减少所述至少一种污染物的含量。优选地,以完全被细胞吸收的量将该底物添加到组合物b中。因此,设想通过添加底物将不会增加toc含量。例如,设想组合物b中的底物浓度,特别是上面提及的底物的浓度为0.5g/l至10g/l、特别是0.5g/l至5g/l。在本发明的一个实施方案中,特别是在将组合物a与地中海富盐菌细胞混合之后,将另外的培养基组分和/或合适的底物添加到组合物b中。例如,另外的培养基组分和/或合适的底物可以在组合物b的温育开始时或在组合物b的温育期间添加(例如连续或以脉冲形式)。当然,底物的浓度在温育过程中将改变,因为底物将以一定速率被组合物b所包含的细胞代谢。因此,底物浓度可能并不恒定。然而,在温育过程中可能添加附加的底物以补偿底物含量的减少。根据本发明的方法,设想在步骤(b)中使组合物a与细胞接触不会显著提高所得组合物b的体积(与组合物a的体积相比)。因此,组合物b的主要组分将是组合物a。因此,步骤(b)不会显著稀释组合物a。稀释因子优选低于1.2、更优选低于1.1、和最优选低于1.05。此外,设想稀释因子低于1.03或1.02。本文中所用的术语“稀释因子”优选是指组合物b的体积与组合物a的体积之比。换句话说,组合物b包含(特别是由其组成)基于组合物b的总重量计至少80重量%、更优选至少90重量%、和最优选至少95重量%的组合物a。此外,设想组合物b包含(特别是由其组成)基于组合物b的总重量计至少97重量%或98重量%的组合物a。由于稀释因子可忽略不计,设想组合物a包含与组合物b相同或基本相同含量的所述至少一种污染物和nacl。因此,对组合物a或高盐废水提供的nacl和至少一种污染物的浓度优选也是组合物b中的nacl和至少一种污染物的浓度。当然,组合物b中的所述至少一种污染物的浓度由于地中海富盐菌细胞的活动将会随时间降低。在使组合物a与细胞接触后,将所得的组合物b温育以便能够通过地中海富盐菌来减少所述至少一种污染物。因此,本发明的方法优选包括温育组合物b的另一步骤(c)。在该温育步骤中,减少了所述至少一种污染物的含量。因此,本发明特别设想了一种减少高盐废水(即包含高盐废水的组合物)的至少一种选自硝基苯、甲酸盐/甲酸根、苯酚、亚甲基二苯胺,特别是4,4'-亚甲基二苯胺(mda)和苯胺的污染物的含量的方法,所述方法包括以下步骤:(a)提供包含高盐废水和所述至少一种污染物的组合物a,(b)使组合物a与地中海富盐菌细胞接触,由此生成包含所述组合物a和所述地中海富盐菌微生物菌株的细胞的组合物b,和(c)温育组合物b,由此减少所述组合物的所述至少一种污染物的含量。组合物b的温育将在合适的条件下进行,即在使得能够如本文中所述通过所述地中海富盐菌的细胞减少所述至少一种污染物的含量的条件下。优选地,温育在生物反应器中进行。优选地,组合物b的温育(和由此减少所述至少一种污染物的含量)在6.0至8.2、更优选6.2至7.6、最优选6.8至7.4的组合物b的ph值下进行。最佳ph值为7.2。此外,设想温育优选在18℃至55℃的温度下、更优选在25℃至45℃的温度下、甚至更优选在30℃至40℃的温度下、最优选在35℃至40℃的温度下进行。最佳温度为37℃。设想在恒温下进行所述减少。但是,还预期温度可能在温育过程中改变。在本发明的一个优选实施方案中,在温育过程中监测组合物b的温度。在本发明的方法的一个优选实施方案中,搅拌组合物b(在温育过程中)。温育在好氧条件下进行。优选地,通过向组合物b连续添加空气或纯化氧气来维持好氧条件。优选地,组合物b具有5.8至8.5、更优选6.0至8.0、和最优选6.2至7.5的ph值。因此,温育优选在5.8至8.5、优选6.2至7.5的ph值下进行。在一个优选实施方案中,在温育过程中监测组合物b的ph值。设想在培养过程中使ph值保持恒定。这可以例如通过添加hcl来实现。在温育步骤中,细胞的生物量的浓度可以是使得能够降低所述至少一种污染物的含量的任何浓度。例如,生物量浓度可以为0.2至10g/l,特别是0.5至4.5g/l。例如,对于250mg/l苯胺的最佳生物量浓度为1.6g/l。因此,还设想生物量浓度为1.3至1.9g/l。如上所述,本发明的方法优选大规模进行。因此,组合物b优选具有至少1、10、100、500、1000、2500或5000升的体积或任何中间体积。但是,本发明也设想较小的体积,如至少5毫升或100毫升的体积(例如用于试验)。本发明的方法,特别是在本发明的方法的步骤(c)中的如本文中所述的温育,优选以分批法、补料分批法或连续法的形式进行,特别是以伴随着细胞保留的分批法、补料分批法或连续法进行(优选在生物反应器中)。因此,组合物b在分批条件、补料分批条件或连续条件下温育。术语“分批法”优选是指温育细胞的方法,其中在温育过程开始时提供最终用于温育细胞的所有组分(包括底物和另外的培养基成分、组合物a以及细胞本身)。分批法优选在某一点停止,并分离经处理的高盐废水。本文中所用的术语“补料分批法”是指温育细胞的方法,其中在培养过程开始后的某个时间向培养物提供附加组分(如附加的培养基组分和/或底物)。补料分批培养优选在某一点停止,收获培养基中的细胞和/或组分并分离经处理的高盐废水。在一个特别优选的实施方案中,本发明的方法以及由此的本文中所述的温育采用使用如上所述的底物(如甘油或乙酸盐/乙酸根)的混合进料系统在连续培养中进行。在本发明的前述方法的一个优选实施方案中,该方法进一步包括将地中海富盐菌细胞与组合物b分离,由此提供组合物c的步骤。作为步骤(d),将细胞与组合物b分离将在组合物b的温育之后,即在减少所述至少一种污染物的含量之后进行。所得组合物c(其在本文中也被称为“经处理的废水”)将基本不含地中海富盐菌细胞。换句话说,组合物c将不包含细胞。细胞与组合物b的分离可以通过所有被认为合适的细胞保留手段来实现。例如,细胞的分离可以通过离心、过滤、或通过倾析来实现。优选地,通过过滤将细胞与组合物b分离。此外,可以将细胞固定在珠粒或固体载体上,由此使细胞与组合物b分离。如果进行连续法,则预期将分离的细胞进料回到废水中。因此,分离的细胞与组合物a接触,或特别与组合物b接触。如果该方法在生物反应器中进行,则生物反应器优选包括用于细胞保留的装置。优选地,生物反应器包括适于通过过滤将细胞与组合物b分离的膜。组合物c优选具有小于40mg/l、更优选小于30mg/l和最优选小于20mg/l的toc含量。在本发明的一个优选实施方案中,该方法进一步包括浓缩组合物c,由此得到组合物c*。该步骤将提高经处理的废水的nacl浓度,即nacl在组合物中浓缩(up-concentrated)。优选地,浓缩的组合物c*以基于组合物a的总体积计大于20.0%(w/v)、特别是以大于22%(w/v)的浓度包含nacl。当用于氯碱工艺的进料物流时,这些nacl浓度是理想浓度。根据本发明,组合物c的浓缩可以是通过任何认为合适的方法进行的浓缩。优选的方法是反渗透、超滤和纳滤。在这些方法中,向过滤膜的一侧施加正渗透压。此外,可以通过蒸发实现浓缩。如上所述,组合物a和b可以以基于所述组合物的总体积计大于20%(w/v)的浓度包含nacl。如果使用这些浓度,则在对经处理的废水施以氯碱工艺时,原则上可以省略浓缩步骤。但是,可以对组合物c和c*施以进一步的纯化步骤。在本发明的方法的一个实施方案中,该方法进一步包括从所述组合物中去除无机组分。所述无机组分优选是培养基组分的微量元素和/或盐。在对组合物c或c*施以氯化钠电解之前将进行所述去除。上文中给出的定义和解释在必要修改后适用于本发明的以下主题,特别适用于本发明的用于生产氯气和/或氢氧化钠的以下方法、适用于本发明的组合物、适用于本发明的生物反应器、和本发明的用途。本发明还涉及生产氯气和氢氧化钠的方法,包括以下步骤:(i)提供根据本发明的方法的组合物c或根据本发明的方法的组合物c*,和(ii)对根据(a)的组合物施以氯化钠电解,由此产生氯气和氢氧化钠。前述方法的步骤(i),即提供根据本发明的方法的组合物c或根据本发明的方法的组合物c*,优选包括用于减少高盐溶液的至少一种选自硝基苯、甲酸盐/甲酸根、苯酚、4,4'-亚甲基二苯胺(mda)和苯胺的污染物的含量的方法的步骤。在一个实施方案中,通过以下步骤提供组合物c:(a)提供包含高盐废水和所述至少一种污染物的组合物a,和(b)使组合物a与地中海富盐菌细胞接触,由此产生包含所述组合物a和所述细胞的组合物b,(c)温育组合物b,由此减少该组合物的所述至少一种污染物的含量,和(d)将地中海富盐菌细胞与组合物b分离,由此提供组合物c。如果提供组合物c*的话,则步骤ii)优选包括进一步的步骤(e):浓缩组合物c,由此提供组合物c*。氯化钠的电解可以通过本领域中公知的方法进行。膜电解法通常用于,例如,含有氯化钠的溶液的电解(关于这一主题,参见peterschmittinger,chlorine,wiley-vchverlag,2000)。这里,使用一分为二的电解池,该电解池包括具有阳极的阳极空间和具有阴极的阴极空间,阳极空间和阴极空间由离子交换膜隔开。将含有氯化钠且氯化钠浓度通常大于300g/l的溶液引入到阳极空间中。在阳极处,氯离子被氧化成氯气,氯气与贫化的氯化钠溶液(大约200g/l)一起从电解池中排放出。钠离子在电场的作用下通过离子交换膜迁移到阴极空间中。在该迁移的过程中,取决于膜,每摩尔钠随其携带3.5至4.5摩尔的水。这导致阳极电解液的水耗尽。与阳极电解液不同,通过电解水形成氢氧根离子和氢气,水在阴极侧被消耗。在30%的入口浓度和4ka/m2的电流密度下,随钠离子携带到阴极电解液中的水足以将输出中的氢氧化钠浓度保持在31-32重量%。在阴极空间中,水被电化学还原以形成氢氧根离子和氢气。作为一个替代方案,可以使用气体扩散电极作为阴极,在该电极处氧气与电子反应形成氢氧根离子并且不形成氢气。氢氧根离子与已经经由离子交换膜迁移到阴极空间中的钠离子一起形成氢氧化钠。通常将浓度为30重量%的氢氧化钠溶液进料到阴极室中,并排放出浓度为31-32重量%的氢氧化钠溶液。目的是获得非常高浓度的氢氧化钠,因为氢氧化钠通常以50%强度的溶液形式储存或运输。但是,商业膜目前不耐受浓度大于32重量%的碱溶液,因此氢氧化钠溶液必须通过热蒸发来浓缩。在电解氯化钠的情况下,经由含有氯化钠的这种溶液将附加的水引入到阳极电解液中,但是水仅经由膜排放到阴极电解液中。如果经由含有氯化钠的溶液引入的水多于可以输送至阴极电解液的水,则阳极电解液会耗尽氯化钠,且电解不能连续进行。在氯化钠浓度非常低的情况下,将会发生形成氧的次级反应。在本发明的方法的一个优选实施方案中,电解是氯化钠的膜电解池电解,特别是使用耗氧电极的膜电解、氯化钠的隔膜电解池电解或氯化钠的汞电解池电解。本发明进一步涉及如上文结合本发明的方法所定义的组合物b。因此,本发明涉及组合物b,其包含高盐废水、至少一种选自硝基苯、甲酸盐/甲酸根、苯酚、4,4'-亚甲基二苯胺(mda)和苯胺的污染物、以及地中海富盐菌细胞。结合本发明的用于减少苯胺和/或甲酸盐/甲酸根含量的方法,公开了所述至少一种污染物的优选含量/浓度和/或进一步优选的nacl浓度。此外,该组合物可以包含如上所述的组分(如其它培养基组分和/或合适的底物等等)。此外,本发明涉及包含至少1升的本发明的组合物b的生物反应器。此外,本发明涉及地中海富盐菌细胞用于减少高盐废水的至少一种选自硝基苯、甲酸盐/甲酸根、苯酚、4,4'-亚甲基二苯胺(mda)和苯胺的污染物的含量的用途。特别地,本发明涉及所述细胞用于减少组合物b的所述至少一种污染物的含量的用途。结合本发明的减少所述至少一种污染物的含量的方法在上文中给出的定义和解释相应地适用于前述用途。因此,根据前述用途,优选结合本发明的方法如上文所述那样减少所述至少一种污染物的含量。附图显示了:图1.该图示出了在加入1.4g/l甘油作为辅底物后的真实盐水(15%w/vnacl)中使用嗜盐菌地中海富盐菌的细胞降解甲酸盐/甲酸根。甲酸盐/甲酸根与甘油同时降解(用三角形表示)。在对照实验(用星号表示)不含细胞的摇瓶中,甘油和甲酸盐/甲酸根都不降解。图2.图表示在含有15%w/vnacl的模型培养基中使用地中海富盐菌细胞降解苯胺(5和10mg/l)。在温育并监测240小时后,在作为唯一底物的苯胺上没有观察到生物量生长。在第二底物(50mg/l苯酚)的存在下,显示生物量浓度随苯胺和苯酚的减少而增加。苯胺降解的速率取决于初始苯胺浓度。在没有细菌细胞的对照实验中,没有检测到苯胺或苯酚浓度的明显变化。图3.系数图显示了两个因素——初始苯胺浓度和ph——对地中海富盐菌菌株降解苯胺的显著影响。nacl浓度似乎对苯胺去除没有显著影响,在所有nacl浓度下,hfx均会降解苯胺。图4.响应等值线图(counterplot)显示,对于地中海富盐菌菌株,在较低的初始苯胺浓度下可能发生最佳的苯胺降解。图5.该图示出了使用嗜盐菌地中海富盐菌细胞在各种盐浓度(0至20%w/vnacl)下的苯胺降解。盐浓度越高,苯胺的降解速率越高。图6.该图示出了使用嗜盐古菌地中海富盐菌的细胞在15%w/v盐浓度下降解硝基苯。在温育的前24小时中,总硝基苯含量中的80%降解。在使用30ppm硝基苯的对照实验中,没有观察到硝基苯含量的显著减少。图7.使用5g/l地中海富盐菌生物量连续处理含0.3g/l甲酸盐/甲酸根的工业盐水。甲酸盐/甲酸根被降解。残余甲酸盐/甲酸根浓度的量取决于稀释率。辅底物甘油对于生物量增长是必需的,并且在稳态条件下被完全吸收。本说明书中引用的所有参考文献在其全部公开内容和本说明书中具体提及的公开内容方面经此引用并入本文。通过以下实施例仅说明本发明。所述实施例无论如何不应解释为限制本发明的范围。实施例实施例1:摇瓶中的降解实验菌株和培养基地中海富盐菌(dsm1411)(在本研究中为hfx)野生型菌株购自dsmz-德国微生物和细胞培养物保藏中心。用于接种制剂的摇瓶培养物在180rpm和37℃下在实验室温育箱(infors,switzerland)中生长,dsmz建议的第97号培养基略有改变,具有以下组成(g/l):nacl250、mgso4.7h2o20.0、kcl2.0、柠檬酸钠3.0、feso4.7h2o0.05、mnso4.h2o、酵母提取物10.0和葡萄糖5.0;ph7.0。总是对500毫升锥形瓶和培养基进行灭菌。分析使用shimadzuuv/vis分光光度计在600nm下在各种时间间隔内测量浊度作为细胞生长的指标。使用hplc测量培养基上清液中的残余甲酸盐/甲酸根、乙酸盐/乙酸根和甘油浓度。在30℃下用来自bio-rad的aminexhpx-87h柱进行hplc(thermo-fisher)方法,等度洗脱液为mq水中的0.1%tfa,流量为0.5ml/min,随后在210nm下进行uv检测。在20µl的进样体积下对于甲酸盐/甲酸根和乙酸盐/乙酸根的定量限为5mg/l。用于定量的标样在与样品相同的含盐基质中制备。使用hplc测量培养物上清液中的残余苯胺、苯酚、硝基苯和mda浓度。使用acclaimpac-163µm柱(thermo-fisher)进行hplc(thermo-fisher)方法。乙腈、25mmkh2po4ph3.5缓冲液和mq用作流动相,并用190nm下的uv进行检测。在5µl的进样体积下,对于苯胺的定量限为1ppm,对于苯酚的定量限为0.5mg/l,对于硝基苯的定量限为1ppm,对于4,4'-mda的定量限为0.1mg/l。也可检测到更低的浓度。摇瓶实验中的甲酸盐/甲酸根降解地中海富盐菌(dsm1411)是一种极端嗜盐古细菌,其需要至少10%(w/v)的nacl才能生长。对于20-25%nacl(w/v)的浓度报道了最佳生长。对于甲酸盐/甲酸根研究,在含有0.37g/l甲酸盐/甲酸根和15%(w/v)nacl的真实工业盐水中培养细胞。将盐水的ph调节至7.0后,根据表1补充培养基组分。发酵前没有对培养基进行灭菌。培养基d是具有表2中所示组成的合成培养基。表1.添加到用于培养基a、b和c的ph7.0的盐水中的培养基组分。摇瓶用不含有任何复合碳或氮源的预培养物接种。接种物不含任何残余碳源。接种摇瓶以便在200毫升的总体积中实现0.25的起始od。使用500毫升摇瓶以180rpm和37℃在实验室温育箱(infors,switzerland)中生长细胞。一式两份地进行实验,并且在仅有培养基且没有细胞的情况下进行对照实验。组成量g/lnacl150甲酸盐/甲酸根6.0g/lnh4cl1.50kh2po40.15fecl30.005mgcl2.6h2o1.30mgso4.7h2o1.10cacl2.2h2o0.55kcl1.66kbr0.50mncl2.4h2o0.003微量元素(表3)1ml表2.用于合成培养基d的培养基组分(ph7.0)。组成量mg/100mlfeso4.7h2o139cuso4.5h2o100mncl2.4h2o78cocl2.2h2o62znso4.7h2o86表3.微量元素储备溶液的组成。在摇瓶实验中研究了hfx降解甲酸盐/甲酸根的能力。添加a)甘油、b)乙酸盐/乙酸根和c)甲酸盐/甲酸根来制备三种不同的培养基。在a和b应显示hfx是否可以在辅底物的存在下吸收甲酸盐/甲酸根的同时,试验c应显示甲酸盐/甲酸根是否支持hfx的生长。通过大量采样监测细胞生长和甲酸盐/甲酸根降解。当存在第二底物(例如甘油或乙酸盐/乙酸根)时,可以检测到甲酸盐/甲酸根迅速降解。在那些实验中,甲酸盐/甲酸根和辅底物被同时吸收。通过向工业盐水(培养基c)中补充附加的甲酸盐/甲酸根,研究了甲酸盐/甲酸根是否可以被吸收并转化为生物量。结果显示,甲酸盐/甲酸根被降解,但是没有可检测到的生长,表明甲酸盐/甲酸根被hfx用作能量源但并非用于生物量生产。进一步的实验显示,hfx需要第二碳源来降解甲酸盐/甲酸根。与培养基c(其是一种已知含有有机污染物如苯胺、mda和硝基苯的工业废物流)不同,培养基d仅含有甲酸盐/甲酸根作为碳源。对于这种培养基,既没有检测到生长,也没有检测到甲酸盐/甲酸根的降解。实施例2:摇瓶中的苯胺和苯酚吸收研究为苯胺吸收研究制备了合成限定培养基。下面列出了培养基组成:组成量g/lnacl150nh4cl1.50kh2po40.15fecl30.005mgcl2.6h2o1.30mgso4.7h2o1.10cacl2.2h2o0.55kcl1.66nahco30.20kbr0.50mncl2.4h2o0.003微量元素1ml苯胺99%5-100mg苯酚50至100mg微量元素组成量mg/100mlfeso4.7h2o136cuso4.5h2o100mncl2.4h2o50cocl2.2h2o44znso4.7h2o86表4.用于研究苯酚和苯胺被地中海富盐菌吸收的合成限定培养基和微量元素组成。研究了该菌株的苯胺吸收。通过在3000rpm下离心5分钟来收获先前在复合培养基上生长的细胞。将细胞洗涤并溶解在摇瓶中,摇瓶含有100毫升相应的合成限定培养基和15%w/vnacl,苯胺作为唯一碳源,并将其在37℃的温度下温育并搅拌。在零小时处,测量od600,并储存一毫升样品用于hplc分析作为参照。监测在苯胺上的生长和残余苯胺浓度。地中海富盐菌菌株并未使用苯胺作为用于生长的源,但是取决于初始苯胺浓度,随时间推移的残余苯胺浓度表明在合成培养基上和在实际盐水上苯胺均已完全从培养基中去除。在第二底物(在这种情况下为苯酚50至100mg/l)的存在下,检测到生物量浓度提高和更好的苯胺降解。在不存在苯胺的情况下也检测到苯酚的增长。为了能够控制其它过程参数,在摇瓶以及生物反应器中的更多实验中,对苯胺和苯酚的降解进行了更详细的研究。实施例3:苯胺降解的最佳培养条件使用多变量实验设计的苯胺研究为了找到hfx降解苯胺的最佳条件,使用了多变量实验设计。进行了部分析因实验设计以评价三个因素(ph、苯胺浓度和nacl浓度)对三个参数(δ生物量、残余苯胺浓度和ph)的影响。在该实验中研究的因素以及相应的范围在(表5)中给出。因素名称范围ph6.2至8.2苯胺浓度15至50mg/lnacl12至18%w/v表5.对于hfx降解苯胺所研究的因素和响应。对于该研究,统计工具modde建议进行11项实验。在摇瓶中在37℃和170rpm搅拌(strokes)下在合成限定培养基上进行实验。在24小时间隔处测定生物量浓度、ph变化和残余苯胺浓度。在144小时后获得的测量值通过modde来分析。获得了δ苯胺的有效模型。在所有实验中苯胺均被降解。系数曲线显示了初始苯胺浓度和ph对苯胺降解的显著影响。hfx细胞对苯胺的最佳降解发生在ph6.2、12%w/vnacl和15mg/l苯胺下,其中在144小时后,94%的苯胺被降解。在各种盐浓度下的苯胺降解在摇瓶实验中在含有30mg/l苯胺作为碳源的合成培养基中在0至20%w/v的各种盐浓度下研究了苯胺的降解。在24小时间隔处通过hplc测定残余苯胺浓度。对于hfx菌株,在高于14%w/v的较高nacl浓度下,发生更好的苯胺降解,其中在20%w/vnacl下降解最好。实施例4:通过地中海富盐菌降解硝基苯对硝基苯的初步摇瓶实验为硝基苯吸收研究制备了合成限定培养基。在(表1)中给出了所用的培养基组成,其中使用30和50ppm的硝基苯作为唯一底物替代苯胺。通过在3000rpm下离心5分钟来收获先前在复合培养基上生长的细胞。将细胞洗涤并溶解在摇瓶中,摇瓶含有100毫升相应的合成限定培养基和15%w/vnacl,硝基苯作为唯一碳源,并将其在37℃的温度和170rpm的搅拌下温育。在零小时处,测量od600,并储存一毫升样品用于hplc分析作为参照。监测在硝基苯上的生长和残余硝基苯浓度。地中海富盐菌菌株并未使用硝基苯作为用于生长的源,但是随时间推移的残余硝基苯浓度表明在合成培养基上和在实际盐水上硝基苯均已完全从培养基中去除。在前24小时过程中观察到最高降解率。为了能够控制其它过程参数,在摇瓶以及生物反应器中的更多实验中,对硝基苯的降解进行了更详细的研究。使用多变量实验设计的硝基苯研究为了找到hfx降解硝基苯的最佳条件,使用了多变量实验设计进行了研究。进行了部分析因实验设计以评价三个因素(ph、硝基苯浓度和nacl浓度)对三个参数(δ生物量、残余硝基苯浓度和δph)的影响。在该实验中研究的因素以及相应的范围在(表6)中给出。因素名称范围ph6至8硝基苯浓度5至25mg/lnacl15至20%w/v表6.对于hfx降解硝基苯所研究的因素和响应。对于该研究,统计工具modde建议进行11项实验。在摇瓶中在37℃和170rpm搅拌(strokes)下在合成限定培养基上进行实验。在24小时间隔处测定生物量浓度、ph变化和残余硝基苯浓度。在72小时后获得的测量值通过modde来分析,显示在表7中。实验ph硝基苯nacl%w/v∆od600降解%n16515-0.09960.1n28515-0.09880n362515-0.09381n482515-0.0864.5n56520-0.11780.4n68520-0.13680.4n762520-0.12489.3n882520-0.12887.7n971517.5-0.106100n1071517.5-0.094100n1171517.5-0.108100对照71517.50.0113表7.显示通过hfx对硝基苯降解获得的结果。表7显示了实验矩阵和所获得的结果。在几乎所有实验中,硝基苯均被降解。在所有实验中均观察到生物量浓度的降低。与实验n9至11中的100%去除相比,在没有细胞的对照实验中发生13%的硝基苯氧化,实验n9至11显示出在hfx细胞的存在下87%的较高降解。hfx细胞对硝基苯的最佳降解发生在centerpoint实验,ph7.0、17.5%w/vnacl和15mg/l硝基苯的情况下,其中在72小时后100%的硝基苯被降解。实施例5:以分批模式降解实际盐水中的苯胺、苯酚、硝基苯和4,4'-mda为了检查降解菌株在实际过程中在工业残余水上的适用性,在生物反应器中进行了培养。对于本实验,hfx细胞用于使用含有15%w/vnacl的实际盐水的过程。在这种情况下,控制过程参数和培养条件,并在适于在高盐环境下培养的特种耐腐蚀生物反应器设备中进行实验。使用特种非腐蚀性labforspeek(infors,ag,switzerland)反应器,其规格如下:硼硅酸盐玻璃培养容器:1l容量硼硅酸盐玻璃排气冷却特种耐腐蚀聚合物(peek)生物反应器顶盖特种耐腐蚀聚合物(peek)温度计支架硼硅酸盐玻璃采样管和进气管特种耐腐蚀搅拌器反应器容器上的硼硅酸盐玻璃夹套。在线分析:排气co2排气o2玻璃ph探头hastelloyclarkpo2和空气热质量流量控制器。将以下培养基组分添加到盐水中:kcl0.66g/l,nh4cl1.5g/l,kh2po40.15g/l,mgcl2.6h2o1.3g/l,mgso4.7h2o1.1g/l,fecl30.005g/l,cacl2.2h2o0.55g/l,kbr0.5g/l,mn储备液3ml和微量元素1ml。温度:37℃ph:7.2(0.5mhcl和0.5mnaoh用于ph控制)。由于该研究中的芳族化合物大多数被降解且不用作促进生物量增长以提高生物反应器中生物量浓度的底物,因此在盐水上进行了分批培养,其中添加了培养基组分和甘油作为生长底物(表1)。一旦获得足够的生物量(大约3g/l),将含有苯胺5mg/l、苯酚5mg/l和4,4'-mda3mg/l的预混物以脉冲形式添加到反应器中。在分批培养过程中,芳族化合物的完全降解花费长达96小时。实施例6:在使用细胞保留系统的连续生物处理中,实际残余水中甲酸盐/甲酸根、mda、硝基苯、苯胺和苯酚的降解具有细胞保留的生物反应器设置使用细胞保留系统进行实际盐水中污染物的连续降解。工业盐水补充有表1中给出的培养基组分和作为辅底物的甘油。以使得实现0.026h-1的比生长速率的方式调节培养基中甘油的量。如对于摇瓶实验所述的那样,在生物反应器中进行培养。在450rpm搅拌和37℃下进行生物反应器中的发酵。将使用面积为420cm2且孔尺寸为0.2μm的聚砜(psu)中空纤维微滤膜滤筒的细胞保留系统设置在生物反应器中。130至610g/h的进料流量导致0.1至0.6h-1的稀释率。通过调节与含细胞的排出流(bleedflow)和不含细胞的收获物相关的进料流量,可以在发酵器中实现恒定生物量。在整个方法过程中测量作为细胞密度指标的浊度和残余甲酸盐/甲酸根、乙酸盐/乙酸根和甘油的hplc分析。残余mda、硝基苯、苯胺和苯酚也通过hplc测量。发酵在1升生物反应器中培养hfx,以便在具有大约0.3克/升甲酸盐/甲酸根的连续流的盐水中降解污染物。对于该实验,两个参数——生物量浓度(g/l)和稀释率(h-1)分别在2-5g/l和0.1-0.6h-1的范围内变化。对于所有的连续培养均观察到明显的甲酸盐/甲酸根降解。具有较高生物量浓度的实验导致较低的残余甲酸盐/甲酸根浓度。在具有较高流量的实验中可以测得较高的残余甲酸盐/甲酸根浓度。对从反应器中采样的培养物上清液的分析表明,在生物处理过程中也可以减少mda和苯胺的量。苯酚和硝基苯被降解至低于检出限的浓度。hfx可以以分批以及连续的方式降解甲酸盐/甲酸根、mda、苯胺、苯酚和硝基苯。所提及的污染物的降解速率取决于生物量浓度、稀释率和盐水中污染物的浓度。小结-结论:高盐废水通常包含有机污染物如甲酸盐/甲酸根、苯胺、苯酚、硝基苯和4,4'-亚甲基二苯胺。几种物理和化学方法,例如吸附、臭氧化和电化学处理,用于处理含有有机化合物的残余水。但是,大多数所提及的处理方法不能将含盐残余物流中的总有机碳含量降低至所要求的最大水平以下。在本发明中,发现地中海富盐菌dsm.1411可以主动降解来自有机污染物的高达200g/l盐度的高盐环境中的有毒的有机污染物。此外,发现地中海富盐菌dsm.1411可以降解来自高盐环境中的甲酸盐/甲酸根、苯胺、苯酚、硝基苯和4,4'-亚甲基二苯胺。本发明可涉及对含有以下任何组分或其组合的任何高盐水的最佳和有效的处理:甲酸盐/甲酸根、苯酚、硝基苯、4,4'-亚甲基二苯胺(mda)和苯胺,意在降低总有机碳含量。当前本发明的另一方面包括残余物转变为价值的概念。一方面,富含大量不期望的有机污染物的高盐残余物流造成的环境问题,和另一方面,对高品质盐水作为用于其它工业过程(如膜电解)的前体的需求,使得这些高盐残余物流的预处理绝对至关重要。本发明有助于实现这种便宜、快速且有效的预处理,以满足膜电解由经处理的盐水产生氯气和/或氢氧化钠的要求。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1