一种壳-核结构磁性微球及其对羊肉中瘦肉精的萃取方法与流程
本发明属于食品检测技术领域,特别涉及一种壳-核结构磁性微球及其对羊肉中瘦肉精的萃取方法。
背景技术
最近几年,在一些猪、羊、牛等肉类中检查出瘦肉精的报道时常发生,老百姓们越来越关注一些肉类及其肉制品的卫生制作条件。瘦肉精是一种可对人体造成严重的不良反应的饲料添加剂,人们如果大量食用超标的肉制品后会产生中毒乃至死亡现象。如何快速、有效的检测肉类中瘦肉精的含量成为人们普遍关注的问题。
由于肉类基质复杂,而瘦肉精的含量通常是痕量级,因此需要对样品进行前处理。由于传统的固相萃取小柱存在有机溶剂消耗量大、特异性不强、价格贵、且只能使用一次的问题,需要开发对瘦肉精富集能力强、制备方法简单、价格低廉、具有选择性的新型萃取材料。所以,一种高效、快速、便捷的新型样品前处理技术-磁固相萃取技术,越来越引起人们的关注。
技术实现要素:
本发明的目的是提供一种壳-核结构的磁性纳米微球及其对羊肉中瘦肉精的萃取方法。利用所述壳-核结构磁性纳米微球可实现羊肉样品中瘦肉精的萃取,配合色谱分析实现羊肉中痕量瘦肉精的快速、灵敏检测。
本发明的目的是通过以下技术方案实现的:
称取修饰碳壳的磁性纳米微球(fe3o4@c),加入超纯水、无水乙醇、丁醇、硝酸钴、柠檬酸钠和尿素,超声至混合均匀后,将混合物转入50ml的水热合成釜中,置于烘箱中加热至120℃。待反应结束后,磁性分离黑色固体,即为磁性fe3o4@c@co3o4。
进一步的,所述制备方法还包括以下步骤:将制备得到的fe3o4@c@co3o4,依次用水、无水乙醇充分洗涤后,再进行真空干燥处理。
本发明的另一目的是通过以下技术方案实现的:
一种利用上述磁性纳米微球萃取羊肉中瘦肉精的方法,包括以下步骤:
使用无水乙醇超声提取羊肉中的瘦肉精,得到含有瘦肉精的样品溶液,氮气吹干,超纯水定容,再用盐酸或氢氧化钠溶液调ph至9,得到提取液;
取上述提取液10ml,再加入权利要求1所述的壳-核结构磁性吸附剂fe3o4@c@co3o4,涡旋萃取、磁性分离负载了瘦肉精的吸附剂,弃去上清液;加入洗脱液再次涡旋洗脱、磁性分离,移取上清液在水浴下氮气吹干,即完成瘦肉精的萃取,用超纯水定容至一定体积后进行色谱分析。
进一步的,所述磁性微球fe3o4@c@co3o4的添加量为0.5-3mg//ml。优选的,添加量为1.5mg/ml。
进一步的,用盐酸或氢氧化钠溶液调ph至9。
进一步的,每次涡旋萃取的时间为5-30min。优选的,每次涡旋萃取20min。
进一步的,所述洗脱液为醋酸:甲醇=15%:85%,涡旋洗脱时间为5-20min,优选的涡旋洗脱10min。
本发明相比现有技术的有益效果为:
1、本发明所述的磁性纳米微球fe3o4@c@co3o4呈壳-核结构,粒径为100-150nm,c@co3o4被成功包裹到了fe3o4表面,均匀分布约为5nm的介孔,中心包裹着fe3o4;
2、将fe3o4@c@co3o4与不修饰co3o4的磁性微球fe3o4@c对瘦肉精的回收率进行了对比,本发明所述的壳-核结构磁性纳米微球fe3o4@c@co3o4对提取液中瘦肉精的萃取性能最佳;
3、将本发明所述的壳-核结构磁性纳米微球fe3o4@c@co3o4作为吸附剂,优化萃取时间、体系ph值、洗脱液体积、洗脱时间等条件,萃取羊肉中的瘦肉精,实现了对羊肉中瘦肉精的选择性萃取,从而提高液相色谱对瘦肉精检测的灵敏度;
4、虽然碳材料对瘦肉精也具有一定的萃取能力,但是其萃取不具有选择性,而修饰了co3o4外壳的磁性纳米微球,通过金属与瘦肉精分子间的配位作用,使其萃取具有一定的选择性,降低了背景的干扰,色谱峰更清晰、干扰少,利用fe3o4@c@co3o4磁性分散萃取样品溶液中的瘦肉精,有利于吸附剂与目标分子的充分作用,也不存在固相萃取(spe)小柱容易发生柱堵塞的问题,具有明显的优势。
附图说明
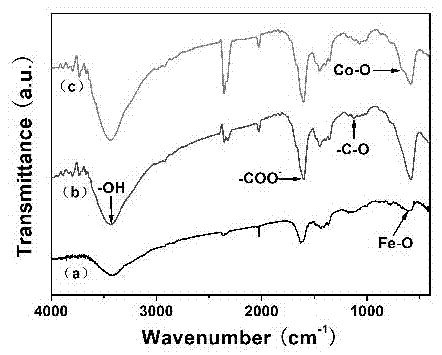
图1为所述磁性微球的红外光谱结果示意图;
其中,a-fe3o4,b-fe3o4@c,c-fe3o4@c@co3o4;
图2为所述磁性微球的xrd结果示意图;
图3为所述磁性微球的不同放大倍数下的tem结果示意图;
其中,a-0.2μm,b-20nm;
图4为吸附剂质量对萃取效率的影响示意图;
图5为吸附时间对萃取效率的影响示意图;
图6为不同ph对萃取效率的影响示意图;
图7为不同洗脱时间对萃取效率的影响示意图;
图8为不同洗脱液体积对萃取效率的影响示意图;
图9为不同磁性微球对瘦肉精萃取效率的示意图;
其中,1-fe3o4@c,2-fe3o4@c@co3o4。
具体实施方式
使用的主要试剂与仪器:
超高效液相色谱仪uplc(h-class,美国waters仪器公司);微型涡旋混合仪(上海沪西分析仪器厂有限公司);盐酸克伦特罗分析标准品(德国dr);莱克多巴胺、沙丁醇胺分析标准品(sigmaaldrich)。
实施例1
本实施例提供了一种壳-核结构磁性纳米微球及其制备方法,称取0.2g的磁性fe3o4@c,加入11.6ml超纯水、8.3ml无水乙醇、0.1ml丁醇、0.291g的硝酸钴(1mmol)、0.1g的柠檬酸钠(na3cit)和0.16g的尿素,超声至混合均匀后,将混合物转入50ml的水热合成釜中,置于烘箱中加热至120℃。待反应8h后,将磁性fe3o4@c@co3o4通过磁铁分离,经超纯水和无水乙醇充分洗涤后,置于60℃的真空干燥箱干燥。
以下,通过红外光谱、x-射线衍射(xrd),透射电镜(tem)等方法表征磁性fe3o4@c@co3o4的物化性能。
由图1可知,如a所示,可以观察到fe3o4晶体中的fe-o键在591cm-1处存在较强的特征吸收峰;b为fe3o4@c红外光谱图,可以观察到在3450cm-1处有一强烈吸收峰,归属为羟基的特征吸收,在1600cm-1处出现的强吸收峰归属于羧基的伸缩振动,这说明碳壳被成功地修饰于fe3o4磁性微球的表面,c为fe3o4@c@co3o4的红外光谱图,在665cm-1处有一吸收峰,归属于co-o键的吸收峰。
由图2中可知,xrd结果表明产物同时具有fe3o4和co3o4的特征衍射峰。
由图3中a可知,fe3o4@c@co3o4分散性较好,呈球形,壳-核结构,直径为100-150nm。由图2中b可知,fe3o4@c@co3o4表面存在均一的纳米孔道。
实施例2
本实施例利用实施例1制备得到的壳-核结构磁性纳米微球fe3o4@c@co3o4萃取羊肉中瘦肉精的方法,包括以下步骤:
使用30ml无水乙醇超声提取10g羊肉中的瘦肉精,得到含有瘦肉精的样品溶液,氮气吹干,超纯水定容至50ml,再用盐酸或氢氧化钠溶液调ph至9,得到提取液;
取上述提取液10ml,再加入权利要求1所述的磁性吸附剂fe3o4@c@co3o420mg,涡旋萃取20min、磁性分离负载了瘦肉精的吸附剂,弃去上清液;加入洗脱液醋酸:甲醇=15%:85%洗脱液3ml,再次涡旋洗脱10min、磁性分离,移取上清液在水浴下氮气吹干,用超纯水定容至1ml后进行色谱分析。
实施例3
考察磁性微球fe3o4@c@co3o4用量对羊肉中瘦肉精萃取效率的影响。
按照实施例2所述方法萃取羊肉中的瘦肉精,区别在于,磁性微球fe3o4@c@co3o4的添加量分别为5、10、15、20、30mg。如图4所示,在磁性微球fe3o4@c@co3o4质量为20mg时,对三者具有较好的萃取效率,因此,本发明选择的最佳吸附剂质量为20mg。
实施例4
考察不同吸附时间对萃取羊肉中瘦肉精萃取效率的影响。
按照实施例2所述方法萃取羊肉中的瘦肉精,区别在于,吸附时间分别为5、10、15、20、25、30min。由图5可知,当吸附时间达到20min时,三者的萃取效率均达到最大,因此本发明选择的吸附时间为20min。
实施例5
考察不同体系ph对磁性微球fe3o4@c@co3o4萃取羊肉中瘦肉精萃取效率的影响。
按照实施例2所述方法萃取羊肉中的瘦肉精,区别在于,样品溶液ph值分别调节至3、5、7、9、11。如图6所示,当ph为9时,磁性微球对三种瘦肉精的萃取效率最大,本发明选择的体系ph=9。
实施例6
考察不同洗脱时间对萃取羊肉中瘦肉精萃取效率的影响。
按照实施例2所述方法萃取羊肉中的瘦肉精,区别在于,洗脱时间分别为2、5、10、20min。由图7可知,三种目标分析物的洗脱时间在10min时萃取效率已经达到了最大值,本发明选择洗脱10min。
实施例7
考察不同洗脱液体积对萃取羊肉中瘦肉精萃取效率的影响。
按照实施例2所述方法萃取羊肉中的瘦肉精,区别在于,洗脱液的体积分别为1、2、3、4ml。由图8可知,在洗脱液体积为3ml时,萃取效率达到最大。因此,本发明洗脱过程加入的洗脱液体积为3ml。
对比例
为了证明,co3o4在吸附剂制备中的作用,制备了fe3o4@c磁性微球,称取0.23g的磁性fe3o4,加入1.8g的葡萄糖和40ml的超纯水,超声至混合均匀后,将混合物转入50ml的水热合成釜中,置于烘箱中加热至180℃。待反应8h后,即可得到磁性fe3o4@c,将磁性fe3o4@c通过磁分离,用超纯水和无水乙醇充分洗涤后,置于60℃的真空干燥箱干燥,即得到黑色的磁性fe3o4@c。
为了确保所制备的fe3o4@c@co3o4确实对瘦肉精的富集与萃取有效且与中间产物的相比最好,采用了将fe3o4@c与实施例1所述的磁性纳米微球fe3o4@c@co3o4的萃取效率进行了对比。两种磁性纳米材料的实验条件相同的情况下,数据情况如图9所示,fe3o4@c@co3o4显示了更强的萃取能力。
证实经过本发明所述的壳-核结构的fe3o4@c@co3o4能够对羊肉中的瘦肉精进行有效的、选择性的富集,并且瘦肉精被吸附于磁性材料上,之后又被转移到了较小的溶液环境当中,证实本发明在选择性富集并检测羊肉中瘦肉精含量方面获得理想效果。
- 还没有人留言评论。精彩留言会获得点赞!