用于抗微生物剂敏感性测试的测定和试剂的制作方法
相关申请的交叉引用
本申请要求2018年7月11日提交的题为“assaysandreagentsforantimicrobialsusceptibilitytesting”的美国临时申请号62/696,732的优先权。前述申请通过引用以其整体并入本文并用于所有目的。
领域
本公开涉及用于抗微生物剂敏感性测试的方法。
背景
抗微生物剂抗性微生物感染与差的临床结果相关,包括在感染的患者中增加的发病率、死亡率和医疗保健成本。在过去的30年中,这些生物体在美国这样的设施中的流行稳步增加。微生物的表型抗微生物剂敏感性测试(ast)对于告知医师适当的治疗方案是关键的。使用目前的方法,ast确定通常需要最少八小时,由于在许多临床微生物学实验室中的轮班工作,使得它成为过夜过程。在等待来自目前的ast方法的确定的同时,通常给予患者广谱抗微生物剂,其通常对患者健康具有显著的有害作用和/或促成增长的抗微生物剂抗性流行。此外,获得准确的抗微生物剂治疗信息的该时间延迟增加患者在医院的停留时间,从而增加患者的成本和不便。
针对该背景,政府和行业利益相关者已经提出促进医院中的抗微生物剂管理工作的规则。然而,抗微生物剂管理工作的努力可能由于目前的ast方法和抗微生物剂处方实践的限制而复杂化。发明人以前已经公开了一种快速ast的方法,其可以减少ast确定所需的时间并促进抗微生物剂管理工作。例如,利用结合微生物表面的荧光探针的ast系统和方法在共同拥有的美国专利号9,834,808中描述。这些系统和方法的优点在于,它们以成本有效的方式解决该需求,并且可以与现有的测定硬件部件兼容。
概述
本公开提供了改进的快速ast系统和方法,其对于例如由于获得抗微生物剂抗性而引起的微生物表面电荷的变化是稳健的。在一个方面,本公开涉及用于进行多测定快速抗微生物剂敏感性测试(ast)序列的方法。该方法可以包括将包含衍生自临床样品的微生物的样品接种到测试面板的多个孔中,所述多个孔中的至少一个包含浓度高于流行病学截断值的阳离子抗微生物剂,并且所述多个孔中的至少一个不包含抗微生物剂;将所述测试面板孵育一段时间;确定包含所述阳离子抗微生物剂的所述测试面板的所述至少一个孔中的所述微生物的生长相对于所述微生物的生长的比率,并且如果所述比率高于预定阈值,使所述测试面板的所述剩余的多个孔中的至少一个与表面活性剂接触;和对所述测试面板的所述剩余的多个孔中的至少一个中的所述样品进行至少一种基于表面积的测量。
在各种实施方案中,所述表面活性剂可以选自十六烷基-三甲基溴化铵(ctab)、奥替尼啶二盐酸盐、十六烷基氯化吡啶、苯扎氯铵、二甲基二(十八烷基)氯化铵、甲基三烷基(c8-c10)氯化铵(adogen464)、苄索氯铵、西曲溴铵和二(十八烷基)二甲基溴化铵。所述方法可以进一步包括在进行所述至少一种基于表面积的测量之前从所述剩余的多个孔中的至少一个去除所述表面活性剂的步骤。进行所述至少一种基于表面积的测量可以包括使所述至少一个剩余的孔与阳离子信号传导剂接触。所述阳离子信号传导剂可以是镧系元素穴状化合物,并且进行所述至少一种基于表面积的测量包括检测所述镧系元素穴状化合物与所述样品中的所述微生物的表面之间的缔合。所述方法可以进一步包括如果所述比率低于预定阈值,使所述测试面板的所述剩余的多个孔中的至少一个与表面活性剂接触的步骤,所述表面活性剂选自脂肪醇乙氧基化物、壬苯醇醚、辛基酚乙氧基化物(tritonx-100)、乙氧基化的胺、泊洛沙姆、单硬脂酸甘油酯、单月桂酸甘油酯、司盘、吐温、烷基多糖苷、氧化胺、亚砜和氧化膦。所述预定比率可以是0.1、0.2、0.3、0.4、0.5或0.6。所述预定比率可以是0.2-0.4。所述方法可以进一步包括在将所述测试面板孵育一段时间后评估所述测试面板的所述多个孔中的至少一个中的生长水平的步骤,并且如果所述生长水平未达到预定生长阈值,任选地将所述测试面板孵育另外的一段时间。
在另一方面,本公开涉及用于进行多测定快速抗微生物剂敏感性测试(ast)序列的方法。该方法可以包括将包含微生物的样品接种到测试面板的多个孔中,所述多个孔中的至少一个包含浓度高于流行病学截断值的多阳离子抗微生物剂,并且所述多个孔中的至少一个不包含抗微生物剂;将所述测试面板孵育一段时间;确定包含所述阳离子抗微生物剂的所述测试面板的所述至少一个孔中的所述微生物的生长相对于不包含抗微生物剂的所述至少一个孔中的所述微生物的生长的比率;如果所述比率高于预定阈值,增加所述微生物的细胞膜的阴离子电荷密度;和测量阳离子信号传导剂与所述测试面板的所述剩余的多个孔中的至少一个中的所述微生物的细胞壁的缔合。
在各种实施方案中,增加所述微生物的所述细胞膜的所述阴离子电荷密度的步骤可以包括使所述剩余的多个孔中的至少一个与表面活性剂接触。所述表面活性剂可以选自十六烷基-三甲基溴化铵(ctab)、奥替尼啶二盐酸盐、十六烷基氯化吡啶、苯扎氯铵、二甲基二(十八烷基)氯化铵、甲基三烷基(c8-c10)氯化铵(adogen464)、苄索氯铵、西曲溴铵和二(十八烷基)二甲基溴化铵。所述方法可以进一步包括如果所述比率低于所述预定阈值,使所述测试面板的所述剩余的多个孔中的至少一个与表面活性剂接触的步骤,所述表面活性剂选自脂肪醇乙氧基化物、壬苯醇醚、辛基酚乙氧基化物(tritonx-100)、乙氧基化的胺、泊洛沙姆、单硬脂酸甘油酯、单月桂酸甘油酯、司盘、吐温、烷基多糖苷、氧化胺、亚砜和氧化膦。
在另一方面,本公开涉及用于抗微生物剂敏感性测试的测试面板。所述测试面板可以包含96-384之间个储器,每个储器配置成容纳75-200μl的流体体积,所述储器中的至少一个包含(a)至少0.05、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1.0、1.1、1.2、1.3、1.4、1.5、2、2.5或3μg的多阳离子抗微生物剂,或(b)至少5、10、15、20、25、30、35或40μg的多阳离子抗微生物剂。所述多阳离子抗微生物剂可以是粘菌素。所述多个储器可以包含选自抗微生物剂组的抗微生物剂,并且所述多个储器可以限定所述抗微生物剂组中的每一种的稀释系列。至少一个储器可以不包括抗微生物剂。
在另一方面,本公开涉及用于进行多测定快速抗微生物剂敏感性测试序列的方法。该方法可以包括将包含衍生自临床样品的微生物的样品接种到测试面板的多个孔中,所述测试面板包含至少一个缺乏抗微生物剂的生长对照孔、至少一个包含多阳离子抗微生物剂的阴离子测试孔和多个限定用于多个抗微生物剂的多个稀释系列的孔,所述多阳离子抗微生物剂的量足以导致在接种后浓度超过流行病学截断值;将所述测试面板负载到自动化的快速抗微生物剂敏感性测试系统中用于进行多测定测试序列;和操作所述测试系统以:在所述孵育组件中孵育并搅动所述接种的样品;在预定间隔之后,或响应于所述生长对照孔中的所述样品的参数,停止孵育;确定所述阴离子测试孔与生长对照孔中微生物生长的比率,并且如果所述比率超过预定阈值,使所述测试面板的所述剩余的孔中的至少一个与表面活性剂接触,所述表面活性剂的浓度足以破坏所述微生物的膜而不使所述微生物大量裂解;和对在所述测试面板中的孵育的样品进行一种或多种端点细胞表面测定;测量来自所述测试面板的所述多个孔中的所述样品的光学输出,所述光学输出对应于所述多个孔中的每一个中剩余的所述微生物的量;和报告以下中的至少一个:对所述多个孔中的每一个中剩余的所述微生物和所述多个抗微生物剂的最小抑制浓度和/或定性敏感性解释。
在另一方面,本公开涉及用于进行多测定快速抗微生物剂敏感性测试序列的方法。该方法可以包括将含有微生物的患者材料的样品或子样品接种到测试面板的多个孔中,至少一个测试孔包含阳离子调节的muellerhinton肉汤(mhb),至少一个测试孔包含粘菌素,并且多个孔限定抗微生物剂稀释系列;向含有阳离子调节的mhb和粘菌素的孔中加入代谢指示剂,并在适于微生物生长的条件下孵育所述测试面板;读取所述代谢指示剂作为荧光信号ex560/em590,以确定背景调节的荧光信号;由在粘菌素中生长的样品的所述背景扣除荧光信号除以在mhb中生长的样品的所述背景扣除荧光信号来计算阴离子比;预处理限定所述测试面板的所述抗微生物剂稀释系列的所述孔,其中如果所述阴离子比大于预定阈值,所述预处理步骤包括用十六烷基三甲基溴化铵处理,而如果所述阴离子比小于所述预定阈值,所述预处理步骤包括用具有1%tween的磷酸盐缓冲的盐水(pbst)处理;施加表面结合试剂;读取所述抗微生物剂稀释系列的所述多个孔中的每一个中的时间分辨荧光信号;和基于所述时间分辨荧光信号,确定存在于所述测试面板中的抗微生物剂的最小抑制浓度(mic)。
在各种实施方案中,所述预定阈值可以在0.05-0.3之间。所述预定阈值可以是0.05、0.1、0.15、0.2和0.25。
在另一方面,本公开涉及用于进行多测定快速抗微生物剂敏感性测试(ast)序列的方法。该方法可以包括将包含衍生自临床样品的微生物的样品接种到包含离子特征测定的测试面板的多个孔中,所述离子特征测定包含一个或多个包含阳离子抗微生物剂的孔和一个或多个不包含抗微生物剂的孔,所述阳离子抗微生物剂的浓度等于或高于流行病学截断值或抗性断点,将所述测试面板孵育一段时间,和确定包含所述阳离子抗微生物剂的所述测试面板的所述至少一个孔中的微生物生长相对于不包含抗微生物剂的孔中的所述微生物生长的离子特征比率。如果所述离子特征测定比高于预定阈值,可以使所述测试面板的所述剩余的多个孔中的至少一个与表面活性剂接触,和可以对所述测试面板的所述剩余的多个孔中的至少一个中的所述样品进行至少一种基于表面积的测量。
在另一方面,本公开涉及用于进行多测定快速抗微生物剂敏感性测试序列的方法。该方法可以包括将包含衍生自临床样品的微生物的样品接种到包含离子特征测定的测试面板的多个孔中,所述离子特征测定包含一个或多个包含阳离子抗微生物剂的孔和一个或多个不包含抗微生物剂的孔,所述阳离子抗微生物剂的浓度等于或高于流行病学截断值或抗性断点,将所述测试面板孵育一段时间,确定包含所述阳离子抗微生物剂的所述测试面板的所述至少一个孔中的微生物生长相对于不包含抗微生物剂的孔中的所述微生物生长的离子特征比率,和如果所述离子特征测定比高于预定阈值,增加所述微生物的细胞膜的阴离子电荷密度,和测量阳离子信号传导剂与所述测试面板的所述剩余的多个孔中的至少一个中的所述微生物的细胞壁的缔合。
在各种实施方案中,增加所述微生物的所述细胞膜的所述阴离子电荷密度的步骤可以包括使所述剩余的多个孔中的至少一个与表面活性剂接触。在所述离子特征测定中的所述阳离子抗微生物剂可以是多阳离子的。所述阳离子抗微生物剂可以包括但不限于多粘菌素a-e中的一种或多种。所述阳离子抗微生物剂可以是粘菌素(多粘菌素e)或多粘菌素b中的一种或多种。所述离子特征测定的最低阳离子抗微生物剂浓度可以等于或高于2μg/ml。所述离子特征测定的最低阳离子抗微生物剂浓度可以等于或低于36μg/ml。所述离子特征测定可以包含具有不同阳离子抗微生物剂浓度的两个孔。所述离子特征测定可以包含8μg/ml和16μg/ml的粘菌素。可以通过吸光度和/或代谢指示剂确定所述离子特征测定中的微生物生长。所述代谢指示剂可以包含刃天青。所述刃天青浓度可以在10μm至100mm之间。所述代谢指示剂可以进一步包含代谢探针制剂,所述制剂进一步包含浓度在50μm至1m之间的1-甲氧基-5-甲基吩嗪鎓甲基硫酸盐(1-甲氧基pms);浓度在100nm至5μm之间的亚甲蓝;和浓度在0.0001%至0.1%(w/v)之间的亚铁氰化物和铁氰化物中的每一种。在将所述代谢指示剂加入到多个所述离子特征测定孔之后可以进行30分钟至6小时的孵育。
在各种实施方案中,所述方法可以进一步包括进行充分生长测定,其包含一个或多个包含培养基但不包含抗微生物剂且不包含微生物的对照孔,和一个或多个包含培养基和微生物但不包含微生物的测定孔,其中在面板孵育开始的2小时内可以将代谢指示剂加入到多个所述充分生长测定孔中,并将所述测定孔与对照孔中的吸光度和/或荧光的比率与预定阈值进行比较,使得如果实现所述阈值,确定已经实现充分生长,而如果未实现所述阈值,在再次进行所述吸光度和/或荧光测量之前将所述样品孵育30分钟至4小时的时间段,并重复该过程,直到实现所述充分生长阈值或已经逝去12小时。所述充分生长测定阈值可以是1、1.05、1.11、1.15、1.2。所述代谢指示剂可以包含刃天青。所述刃天青浓度可以在10μm至100mm之间。所述代谢指示剂可以进一步包含代谢探针制剂,所述制剂进一步包含浓度在50μm至1m之间的1-甲氧基-5-甲基吩嗪鎓甲基硫酸盐(1-甲氧基pms);浓度在100nm至5μm之间的亚甲蓝;和浓度在0.0001%至0.1%(w/v)之间的亚铁氰化物和铁氰化物中的每一种。用于所述离子特征测定的所述代谢指示剂的所述制剂可以与用于所述充分生长测定的所述代谢指示剂的所述制剂大致相同。所述离子特征测定可以平行进行并且使用与在所述板中包含不同抗微生物剂的稀释系列的多个孔上进行的活力测定大致相同的代谢指示剂。如果所述离子特征测定比等于或大于所述预定阈值,加入的所述表面活性剂可以选自十六烷基-三甲基溴化铵(ctab)、奥替尼啶二盐酸盐、十六烷基氯化吡啶、苯扎氯铵、二甲基二(十八烷基)氯化铵、甲基三烷基(c8-c10)氯化铵(adogen464)、苄索氯铵、西曲溴铵和二(十八烷基)二甲基溴化铵。所述表面活性剂可以是ctab。所述ctab浓度可以在0.001%至1%之间,例如在0.01%至0.1%之间。包含所述表面活性剂的制剂可以进一步包含金属离子螯合剂。所述金属离子螯合剂可以是乙二胺四乙酸(edta)。所述edta浓度可以在0.001-1m之间、在0.01-0.5m之间。
在各种实施方案中,所述方法可以进一步包括如果所述离子特征测定比低于所述预定阈值,使所述测试面板的所述剩余的多个孔中的至少一个与表面活性剂接触的步骤,所述表面活性剂选自脂肪醇乙氧基化物、壬苯醇醚、辛基酚乙氧基化物(tritonx-100)、乙氧基化的胺、泊洛沙姆、单硬脂酸甘油酯、单月桂酸甘油酯、司盘、吐温、烷基多糖苷、氧化胺、亚砜和氧化膦。所述表面活性剂可以是吐温-20(聚山梨醇酯20)。所述吐温浓度可以在0.001-1%之间。所述离子特征测定的所述预定阈值比可以是0.01、0.05、0.1、0.2、0.3、0.4、0.5或0.6。所述预定阈值比可以是0.1-0.3。所述方法可以进一步包括在进行所述至少一种基于表面积的测量之前从所述剩余的多个孔中的至少一个去除所述表面活性剂的步骤。进行所述至少一种基于表面积的测量可以包括使所述至少一个剩余的孔与阳离子信号传导剂接触。所述阳离子信号传导剂可以是镧系元素穴状化合物,并且进行所述至少一种基于表面积的测量可以包括检测所述镧系元素穴状化合物与所述样品中的所述微生物的表面之间的缔合。所述微生物可以是革兰氏阴性的。
在另一方面,本公开涉及用于抗微生物剂敏感性测试的测试面板。该测试面板可以包含:96-384之间个储器,每个储器配置成容纳75-250μl的流体体积,所述储器中的至少一个包含(a)至少0.05、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1.0、1.1、1.2、1.3、1.4、1.5、2、2.5或3μg的多阳离子抗微生物剂,或(b)至少5、10、15、20、25、30、35或40μg的多阳离子抗微生物剂。所述多阳离子抗微生物剂为多粘菌素。所述多阳离子抗微生物剂可以是粘菌素和/或多粘菌素b。多个储器可以包含选自抗微生物剂组的抗微生物剂,并且所述多个储器可以限定所述抗微生物剂组中的每一种的稀释系列。至少一个测试面板可以不包括抗微生物剂。
在另一方面,本公开涉及用于进行多测定快速抗微生物剂敏感性测试序列的方法。该方法可以包括将包含衍生自临床样品的微生物的样品接种到测试面板的多个孔中,除了一个或多个包含生长培养基但不包含微生物的阴性对照孔之外,所述测试面板包含至少两个缺乏抗微生物剂的阳性生长孔、至少一个包含多阳离子抗微生物剂的离子特征孔和多个限定用于多个抗微生物剂的多个稀释系列的孔,所述多阳离子抗微生物剂的量足以导致在接种后浓度超过流行病学截断值或抗性断点。所述方法可以进一步包括将所述测试面板负载到自动化的快速抗微生物剂敏感性测试系统中用于进行多测定测试序列,和操作所述测试系统以:将代谢指示剂加入到所述阴性对照孔和阳性生长孔中,所述代谢指示剂包含浓度在10μm至100mm之间的刃天青,浓度在50μm至1m之间的1-甲氧基-5-甲基吩嗪鎓甲基硫酸盐(1-甲氧基pms),浓度在100nm至5μm之间的亚甲蓝,和浓度在0.0001%至0.1%(w/v)之间的亚铁氰化物和铁氰化物中的每一种;在所述孵育组件中孵育并任选地搅动所述接种的样品;在预定间隔之后或在实现或超过以所述阳性生长对照孔与阴性对照孔的吸光度和/或荧光确定的充分生长测定的1.0、1.05、1.1、1.15、1.2的比率之后,将代谢指示剂加入到多个孔中,所述多个孔包括所述离子特征测定孔和未用于所述充分生长测定的阳性生长对照孔,并进行30分钟或更长时间的孵育,所述代谢指示剂包含与用于所述充分生长测定的制剂大致等同的制剂;确定多个孔的所述吸光度和/或荧光,并计算离子特征测定比,所述离子特征测定比限定为所述一个或多个离子特征测定孔与一个或多个生长对照孔中的微生物生长的比率,并且如果所述比率等于或超过预定阈值,使所述测试面板的所述剩余的孔中的至少一个与表面活性剂接触,所述表面活性剂的浓度足以破坏所述微生物的膜而不使所述微生物大量裂解,而如果所述阴离子特征测定比小于所述预定阈值,使所述测试面板的所述剩余的孔中的至少一个与不同的表面活性剂接触;和对在所述测试面板中的孵育的样品进行一种或多种端点细胞表面测定;测量来自所述测试面板的所述多个孔中的所述样品的光学输出,所述光学输出对应于所述多个孔中的每一个中剩余的所述微生物的量;和报告以下中的至少一个:对所述多个孔中的每一个中剩余的所述微生物和所述多个抗微生物剂的最小抑制浓度和/或定性敏感性解释。
在另一方面,本公开涉及用于进行多测定快速抗微生物剂敏感性测试序列的方法。该方法可以包括将含有微生物的患者材料的样品或培养的样品接种到测试面板的多个孔中,除了一个或多个包含阳离子调节的muellerhinton肉汤(mhb)但不包含抗微生物剂的阴性对照孔以外,所述接种的孔中至少两个孔限定离子特征测定,其中至少一个测试孔包含mhb和粘菌素并且至少一个测试孔包含mhb并且不包含抗微生物剂,并且多个孔限定不同抗微生物剂的多个抗微生物剂稀释系列;在所述孵育组件中孵育并任选地搅动所述接种的样品;在预定间隔之后或在实现或超过以所述阳性生长对照孔与阴性对照孔的吸光度和/或荧光确定的充分生长测定的1.0、1.05、1.1、1.15、1.2的比率之后,将代谢指示剂加入到多个孔中,所述多个孔包括所述离子特征测定孔和未用于所述充分生长测定的阳性生长对照孔,并进行30分钟或更长时间的孵育,所述代谢指示剂包含与用于所述充分生长测定的制剂大致等同的制剂,并且包含:浓度在10μm至100mm之间的刃天青;浓度在50μm至1m之间的1-甲氧基-5-甲基吩嗪鎓甲基硫酸盐(1-甲氧基pms);浓度在100nm至5μm之间的亚甲蓝;和浓度在0.0001%至0.1%(w/v)之间的亚铁氰化物和铁氰化物中的每一种。所述方法可以进一步包括在550-650nm处读取吸光度以确定所述吸光度信号和/或所述代谢指示剂作为所述荧光信号ex560/em590,以确定多个孔中的背景调节的荧光信号,在实现所述充分生长测定阈值后向所述多个孔中加入所述代谢指示剂;由在粘菌素中生长的样品的所述背景扣除荧光信号除以在mhb中生长的样品的所述背景扣除荧光信号或粘菌素中样品生长的所述吸光度信号除以mhb中样品生长的所述信号来计算离子特征测定比;在开始表面结合测定之前预处理限定所述测试面板的所述抗微生物剂稀释系列的所述孔,其中如果所述离子特征测定比大于预定阈值,预处理步骤包括用ctab处理,而如果所述离子比小于所述预定阈值,所述预处理步骤包括用具有吐温-20的磷酸盐缓冲的盐水处理;施加表面结合试剂;读取所述抗微生物剂稀释系列的所述多个孔中的每一个中的时间分辨荧光信号;和基于所述时间分辨荧光信号,确定存在于所述测试面板中的抗微生物剂的最小抑制浓度(mic)。
在各种实施方案中,所述预定阈值可以在0.1-0.3之间。所述预定阈值可以是0.05、0.1、0.15、0.2和0.25。
附图说明
图1描述铕-穴状化合物二胺探针。
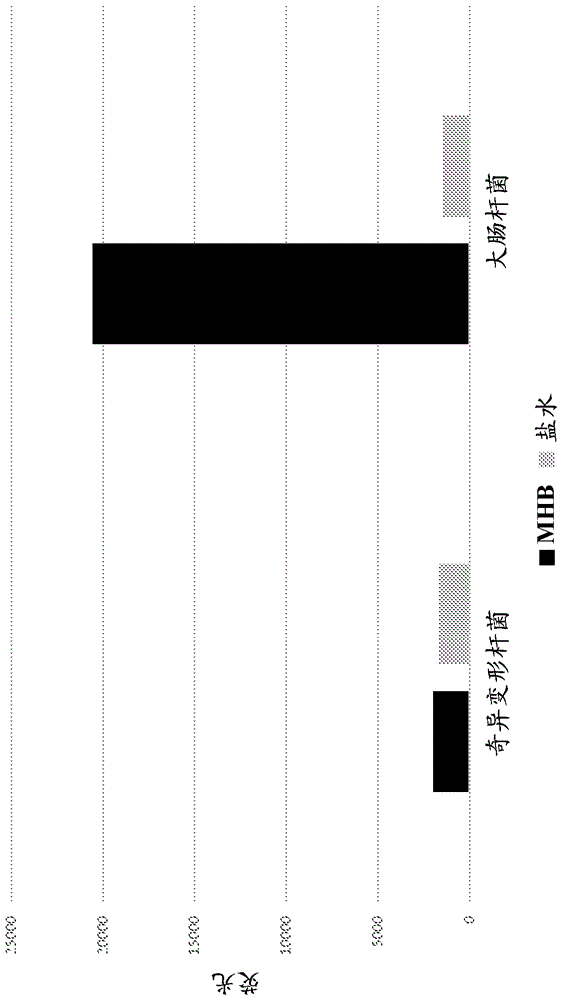
图2显示在330/615nm处具有标准表面阴离子电荷的微生物大肠杆菌(ecoli)和具有低阴离子电荷的微生物奇异变形杆菌(p.mirabilis)的时间分辨荧光(trf)信号,每种微生物在muellerhinton肉汤(mhb)或盐水中孵育。大肠杆菌被铕探针良好结合,并因此在细菌生长的条件(mhb)对比没有发生生长的条件(盐水)下显示高信号。然而,低阴离子电荷的生物体奇异变形杆菌在mhb和盐水条件两者下都证明低trf信号,指示铕探针的结合差。
图3显示在应用铕-穴状化合物探针之前,在mhb或盐水中孵育并用十六烷基-三甲基溴化铵(ctab)预处理的奇异变形杆菌样品的trf信号。如该图指示,ctab处理揭示在mhb条件下的生长,指示铕穴状化合物探针的结合。
图4显示ctap处理的金黄色葡萄球菌(s.aureus)万古霉素(van)稀释系列的trf信号。在一种条件下,在应用铕穴状化合物探针之前去除ctab;在另一种条件下,不去除ctab。当用van处理时,金黄色葡萄球菌的最小抑制浓度(mic)为2μg/ml。在ctab去除条件下,如右图所示,观察到信号剂量依赖性降低,并且在2μg/ml和更低浓度下观察到最小信号。在不去除ctab的条件下没有观察到相同的关系,指示残留的ctab可能干扰铕穴状化合物探针的结合或信号传导。
图5显示哌拉西林-三唑巴坦(tzp)和阿奇霉素(atm)的大肠杆菌稀释系列的trf信号。每个稀释系列包括mhb(无抗微生物剂)和盐水条件,并且对于每种抗微生物剂,评价两种条件:用ctab预处理和用磷酸盐缓冲的盐水(pbst)预处理。对于测试的大肠杆菌菌株,tzp的mic值通常在1-4μg/ml之间,而atmmic值通常小于或等于0.25μg/ml。对于用pbst预处理的tzp稀释系列,观察到铕穴状化合物探针信号的剂量依赖性降低;当用ctab预处理稀释系列时,该效果变得模糊。在atm稀释系列中,最低atm浓度等于或高于mic值,但在pbst预处理条件下在所有浓度下观察到类似的铕穴状化合物探针信号;ctab条件下的信号变化更大,没有可辨别的剂量关系。
图6描述本公开的示例性ast方法,其包括以下步骤:确定样品中微生物的相对阴离子电荷(例如“阴离子比”),并且基于该确定,在使用阳离子探针(例如铕穴状化合物二胺)的表面积测定之前选择ctab或其它预处理。
图7显示庆大霉素(gen)和环丙沙星(ciproflaxin)(cip)稀释系列在奇异变形杆菌和克雷白氏肺炎杆菌(k.pneumonia)中的trf信号。基于阴离子比选择每种微生物的预处理条件,所述阴离子比由在4μg/ml粘菌素中生长的样品的背景扣除荧光信号(ex560/em590)除以在mhb中生长的细菌的背景扣除荧光信号来计算。奇异变形杆菌的阴离子比为0.96,指示低粘菌素敏感性并且表明低表面阴离子电荷。克雷白氏肺炎杆菌的阴离子比为-0.08,表明较高的阴离子电荷。基于这些比率,用ctab预处理奇异变形杆菌样品,而不预处理克雷白氏肺炎杆菌样品。稀释系列显示与每种抗微生物剂的已知mic值一致的剂量关系,指示在每种情况下,预处理条件适于探针的结合和检测。
图8描述在用所指示的ctab或pbst处理后,在与铕-穴状化合物表面结合后,来自含有所指示的生物体的孔的信号与来自阴性对照未接种的孔的信号的比率。
描述
综述
发明人先前已经描述了用于快速ast的系统和方法,其利用阳离子表面结合信号传导剂,例如图1中所示的铕-穴状化合物二胺。不希望受任何理论的束缚,这些信号传导剂可以在合适的条件下与微生物细胞膜化学计量地缔合,允许以足够的精确度测量微生物生长,以在不同的生长模式之间区分,例如细胞分裂相对于细丝形成或膨胀。
本领域技术人员将理解,某些微生物(例如奇异变形杆菌)相对于例如大肠杆菌表现出相对较低的表面阴离子电荷。另外,某些突变,例如赋予阳离子抗微生物剂(如粘菌素)抗性的那些突变可以减少表面阴离子电荷。在这些设置中的每一种中,微生物细胞膜的阴离子电荷的变化将导致阳离子信号传导剂的结合水平的变化,并因此导致与这样的结合相关的信号的变化,这可能使利用阳离子信号传导剂的ast方法复杂化。
同样,不希望受任何理论的束缚,发明人已经发现某些阳离子表面活性剂可以增加微生物细胞膜的阴离子电荷,以促进用于快速ast的阳离子信号传导剂的结合。然而,不是所有的阳离子表面活性剂都与快速ast相容,并且在一些情况下,使用阳离子表面活性剂可能干扰阳离子信号传导剂的结合。还应注意到,阳离子表面活性剂在全文中用作示例性,但也可以利用非离子和/或阴离子表面活性剂。
根据本公开的某些实施方案的快速ast方法涉及以下步骤,在图6中示意性地说明:首先,将含有微生物的样品接种到包括多个储器的ast测试面板上,所述储器包括(a)至少一个不包括抗微生物剂的储器,或生长对照储器,和(b)至少一个包括试剂的测试储器,根据微生物的阴离子表面电荷,所述试剂有差别地影响微生物的生长,例如,相对于具有较低阴离子表面电荷的微生物,减少具有较高阴离子电荷的微生物的生长的试剂。
该测试面板通常还包括多个储器,所述储器限定多个抗微生物剂的稀释系列,并且本公开的ast方法通常涉及评估跨稀释系列的每种抗微生物剂中的微生物生长,以确定每种抗微生物剂的最小抑制浓度和任选的断点浓度。在评估抗微生物剂稀释系列的微生物生长之前,将测试面板在适合于微生物生长的条件(例如在25℃、30℃、35℃、37℃等的温度(以摄氏度计))下孵育一段时间,任选地在孵育期的至少一部分期间搅动。孵育后,在至少一个生长对照储器中评估微生物生长。如果生长满足或超过预定最低水平,进行微生物的阴离子电荷的评估,例如通过比较在测试储器中的生长水平与在生长对照储器中的生长水平。基于该比较,选择样品制备程序;对于确定具有低阴离子电荷的样品,样品制备程序包括用阳离子表面活性剂处理测试面板的剩余的储器以使表面活性剂与储器中的微生物细胞膜缔合,以及在用阳离子检测试剂处理储器之前去除过量的阳离子表面活性剂的步骤。
根据微生物的阴离子表面电荷而有差别地影响微生物的生长的试剂可以包括例如阳离子抗微生物剂,如粘菌素。某些形式的粘菌素抗性导致细胞膜的阴离子电荷的减少,降低粘菌素的效力,并允许微生物在暴露于高于为同一菌株的粘菌素易感微生物限定的粘菌素的临床断点浓度的浓度时存活。在本公开的一些实施方案中,当患者样品中的微生物已知时,测试孔包括高于已知微生物的断点浓度的量的粘菌素。在微生物未知的实施方案中,测试孔包括高于例如最高已知或最高可接受的断点浓度和/或最低已知或最低可接受断点浓度的量的粘菌素。或者,所述测试面板包括多个测试孔,所述测试孔限定跨越已知或可接受的断点浓度范围延伸的粘菌素的稀释系列。基于阴离子表面电荷可以有差别地影响微生物生长的其它试剂包括多粘菌素b、多粘菌素e、阳离子抗微生物剂肽、防卫素和/或cathelicidin。
在一些情况下,不是基于响应于试剂的微生物生长差异来评估阴离子电荷,而是从微生物的另一已知特性推断阴离子电荷。例如,某些革兰氏阴性微生物可能比革兰氏阳性微生物更容易产生粘菌素抗性,因此在本公开的一些实施方案中,为了ctab预处理确定的目的,已知革兰氏染色阴性的微生物可以假定为低阴离子电荷微生物。在其它实施方案中,微生物的阴离子电荷从atp、nad、nadh、遗传材料和/或酶活性的测定或对其的测定推断。
用于本公开的方法的阳离子表面活性剂可以是十六烷基-三甲基溴化铵(ctab)、奥替尼啶二盐酸盐、十六烷基氯化吡啶、苯扎氯铵、二甲基二(十八烷基)氯化铵、甲基三烷基(c8-c10)氯化铵(adogen464)、苄索氯铵、西曲溴铵或二(十八烷基)二甲基溴化铵。在一些情况下,暴露于高浓度的这些表面活性剂可以导致细胞裂解,并且游离的表面活性剂可以与阳离子信号传导剂缔合。因此,在本公开的一些实施方案中,将阳离子表面活性剂施用于ast测试面板有限的时间段,和/或以低于观察到显著的细胞裂解的浓度施用。本公开的方法可以包括在去除阳离子表面活性剂之后和在将阳离子信号传导剂施用于测试面板的贮器之前的一次或多次漂洗。
微生物
感染可以包括微生物来源的任何感染试剂,例如细菌、真菌细胞、古细菌和原生动物。在一些实例中,所述感染剂是细菌,例如革兰氏阳性细菌、革兰氏阴性细菌和非典型细菌。抗微生物剂抗性微生物可以是对于抗微生物剂(即抗菌药物、抗真菌药物、抗古细菌药物和抗原生动物药物)具有抗性的微生物。
微生物(例如,微生物的液体悬浮液)可以包括微生物的一种菌株。微生物可以包括微生物的一种物种。微生物可以包括多于一种微生物的菌株。微生物可以包括微生物的一种顺序。微生物可以包括一种微生物的类别。微生物可以包括微生物的一种家族。微生物可以包括微生物的一种界。
微生物(例如,微生物的液体悬浮液)可以包括多于一种微生物的菌株。微生物可以包括多于一种微生物的物种。微生物可以包括多于一种微生物的属。微生物可以包括多于一种微生物的顺序。微生物可以包括多于一种微生物的类别。微生物可以包括多于一种微生物的家族。微生物可以包括多于一种微生物的界。
微生物可以是细菌。细菌的实例包括但不限于橙黄色醋杆菌、沥青不动杆菌、不动杆菌属某些种、衣氏放线菌、放线菌属某些种、气球菌属某些种、放射形土壤杆菌、根瘤农杆菌土壤杆菌(agrobacteriumtumefaciens)、红孢子虫属、嗜吞噬细胞无形体、固氮根瘤菌、棕色固氮菌(azotobactervinelandii)、芽孢杆菌、炭疽芽孢杆菌、短芽孢杆菌、仙人掌芽孢杆菌、梭杆菌芽孢杆菌、地衣芽孢杆菌、巨大芽胞杆菌、丝状亚种芽孢杆菌、芽孢杆菌属某些种、嗜热脂肪芽孢杆菌、枯草芽孢杆菌、苏云金芽胞杆菌、拟杆菌、脆弱拟杆菌、牙龈拟杆菌、产黑色素拟杆菌(也称为产黑色普雷沃菌)、巴尔通氏体、汉氏巴尔通氏体、五日热巴尔通氏体、巴尔通氏体属属某些种、博德特菌、支气管炎博德特菌、百日咳博德特菌、博德特菌属某些种、伯氏疏螺旋体(borreliaburgdorferi)、布鲁菌、流产布鲁菌、羊布鲁菌、布鲁菌属某些种、猪布鲁菌、伯克霍尔德菌、洋葱伯克霍尔德菌、鼻疽伯克霍尔德菌、类鼻疽伯克霍尔德菌、肉芽肿鞘杆菌、弯曲杆菌、大肠弯曲杆菌、胚胎弯曲杆菌、空肠弯曲杆菌、幽门弯曲杆菌、弯曲杆菌属某些种、衣原体、衣原体属某些种、沙眼衣原体、衣原体、肺炎衣原体(chlamydophilapneumoniae)(以前称为肺炎衣原体(chlamydiapneumonia))、鹦鹉热衣原体(chlamydophilapsittaci)(以前称为鹦鹉热衣原体(chlamydiapsittaci))、衣原体属某些种、梭菌、肉毒梭菌、艰难梭菌、产气荚膜梭菌(以前称为魏氏梭菌)、梭菌属某些种、破伤风梭菌、棒杆菌、白喉棒杆菌、梭形棒杆菌、棒杆菌属某些种、伯纳特氏立克次氏体、ehrlichiachaffeensis、埃立克体属某些种、阴沟肠杆菌、肠杆菌属某些种、肠球菌、鸟肠球菌、耐久肠球菌、粪肠球菌、屎肠球菌、鹑鸡肠球菌、enterococcusmaloratus、肠球菌属某些种、大肠埃希菌、弗朗西斯氏菌属某些种、土拉弗朗西斯病、具核梭杆菌、加德纳氏菌属某些种、阴道加德纳氏菌、嗜血杆菌属某些种、嗜血杆菌、杜克雷嗜血杆菌、流感嗜血杆菌、副流感嗜血杆菌、百日咳嗜血杆菌、嗜血杆菌鞘突、幽门螺杆菌、螺杆菌属某些种、克雷白氏肺炎杆菌、克雷伯菌属某些种、乳杆菌、嗜酸乳杆菌、保加利亚乳杆菌、干酪乳杆菌、乳杆菌属某些种、乳酸乳球菌、嗜肺军团菌、军团菌属某些种、细螺旋体属某些种、单核细胞增生利斯特菌、利斯特菌属某些种、methanobacteriumextroquens、多形性小细菌属、滕黄微球菌、卡他莫拉菌、分枝杆菌、鸟分枝杆菌、牛结核分枝杆菌、白喉分枝杆菌、mycobacteriumintracellulare、麻风分枝杆菌、鼠麻风分枝杆菌、草分枝杆菌、包皮垢分枝杆菌、分枝杆菌属某些种、结核分枝杆菌、支原体、mycoplasmafermentans、生殖支原体、人支原体、穿透支原体、肺炎支原体、支原体属某些种、奈瑟球菌、淋病奈瑟球菌、脑膜炎奈瑟球菌、奈瑟球菌属某些种、奴卡菌属某些种、巴斯德菌、多杀巴斯德菌、巴斯德菌属某些种、土拉巴斯德菌、消化链球菌、牙龈卟啉单胞菌、产黑色普雷沃菌(以前称为产黑色拟杆菌)、变形杆菌属某些种、铜绿假单胞菌、假单胞菌属某些种、放射型根瘤菌、立克次氏体、普氏立克次氏体、鹦鹉热衣原体立克次氏体、五日热立克次氏体、立氏立克次氏体、立克次氏体属某些种、沙眼立克次氏体、罗卡利马体、rochalimaeahenselae、五日热罗卡利马体、龋齿罗菌、沙门菌、肠炎沙门菌、沙门菌属某些种、伤寒沙门菌、鼠伤寒沙门菌、粘质沙雷菌、痢疾志贺菌、志贺菌属某些种、迂回螺菌、葡萄球菌、金黄色葡萄球菌、表皮色葡萄球菌、葡萄球菌属某些种、嗜麦芽寡养单胞菌、寡养单胞菌属某些种、链球菌、无乳链球菌、鸟链球菌、牛链球菌、仓鼠链球菌、屎肠链球菌、粪链球菌、野生鼠链球菌、鹑鸡链球菌、乳酸链球菌、轻型链球菌、缓症链球菌、变异链球菌、口腔链球菌、肺炎链球菌、化脓链球菌、鼠链球菌、唾液链球菌、血链球菌、表兄链球菌、链球菌属某些种、螺旋体、齿垢密螺旋菌、梅毒螺旋体、螺旋体属某些种、尿素原体属某些种、弧菌、霍乱弧菌、逗号弧菌、副溶血弧菌、弧菌属某些种、创伤弧菌、绿色链球菌、沃尔巴克氏体、耶尔森菌、小肠结肠炎耶尔森菌、鼠疫耶尔森菌、假结核耶尔森菌和耶尔森菌属某些种。
微生物可以是真菌。真菌的实例包括但不限于曲霉属真菌属某些种、芽生菌属某些种、假丝酵母属某些种、枝孢属、球孢子菌属某些种、隐球酵母属某些种、突脐蠕孢属、镰刀菌属、组织胞浆菌属某些种、伊萨酵母属某些种、mucormycetes、肺囊虫属某些种、癣、丝孢菌属、孢子丝菌和葡萄穗霉属某些种。微生物可以是原生动物。原生动物的实例包括但不限于痢疾变形虫、疟原虫属某些种、肠兰伯氏鞭毛虫和布氏锥虫。
抗微生物剂
当微生物为细菌时,示例性抗微生物剂包括阿米卡星、氨基糖苷、氨基糖苷阿莫西林、氨基糖苷类、阿莫西林、阿莫西林/克拉维酸盐、氨苄西林、氨苄西林/舒巴坦、抗毒素、砷凡纳明、阿奇霉素、阿洛西林、氨曲南、β-内酰胺、杆菌肽、卷曲霉素、卡巴培南、羧苄西林、头孢克洛、头孢羟氨苄、头孢氨苄、cefalothin、头孢噻吩、头孢孟多、头孢唑林、头孢地尼、头孢托仑、头孢吡肟、头孢克肟、头孢哌酮、头孢噻肟、头孢西丁、头孢泊肟、头孢丙烯、头孢洛林(ceftaroline),ceftarolinefosamil、头孢他啶、头孢布烯、头孢唑肟、头孢吡普(ceftobiprole)、头孢曲松、头孢呋辛、头孢菌素类、氯霉素、氯霉素(bs)、环丙沙星、克拉霉素、克林霉素、氯法齐明、氯唑西林、粘菌素、复方新诺明、环丝氨酸、达巴万星(dalbavancin)、氨苯砜、达托霉素、地美环素、双氯西林、地红霉素、多利培南、多西环素、依诺沙星、厄他培南(ertapenem)、红霉素、乙胺丁醇、乙胺丁醇(bs)、乙硫异烟胺、氟氯西林、氟喹诺酮、氟喹诺酮类、磷霉素、呋喃唑酮、夫西地酸、加替沙星、格尔德霉素、吉米沙星、庆大霉素、格帕沙星、除莠霉素(herbimycin)、亚胺培南/西司他丁、异烟肼、卡那霉素、左氧氟沙星、林可霉素、利奈唑胺、洛美沙星、氯碳头孢、大环内酯类、磺胺米隆、美罗培南、甲氧西林、甲硝唑、美洛西林、二甲胺四环素、莫西沙星、莫匹罗星、萘夫西林、萘夫西林、萘啶酸、新霉素、萘替米星、呋喃妥因(bs)、诺氟沙星、氧氟沙星、奥利万星、苯唑西林、土霉素、巴龙霉素、青霉素、青霉素g、青霉素v、哌拉西林、哌拉西林/三唑巴坦、平板霉素(platensimycin)、多粘菌素b、泼斯唑来(posizolid)、吡嗪酰胺、奎奴普丁/达福普汀、雷德唑来(radezolid)、瑞西巴库(raxibacumab)、利福布汀、利福平(rifampicin)、利福平(rifampin)、利福喷汀、利福昔明、罗红霉素、磺胺嘧啶银、司帕沙星、大观霉素、大观霉素(bs)、螺旋霉素、链阳性菌素类、链霉素、舒巴坦、磺胺醋酰、磺胺嘧啶、磺胺地索辛、磺胺甲二唑、磺胺甲噁唑、磺胺二甲异噁唑(sulfanilimide)、柳氮磺吡啶、磺胺异噁唑、sulfonamidochrysoidine、特地唑胺(tedizolid)、替考拉宁、teixobactin、telavancin、泰利霉素、替马沙星、替莫西林、四环素、甲砜霉素、替卡西林、替卡西林/克拉维酸盐、替卡西林/克拉维酸、替加环素(tigecycline)、替加环素(bs)、替硝唑、tmp/smx、妥布霉素、特地佐利(torezolid)、甲氧苄啶(bs)、甲氧苄啶-磺胺甲噁唑、醋竹桃霉素、曲伐沙星、万古霉素及其属或其变体。
与微生物的相互作用影响并且受微生物表面上的负电荷影响的抗微生物剂可以包括:多阳离子氨基糖苷,其在结合细胞表面后替代桥接脂质膜组分的mg2+离子,从而破坏外部膜并增强药物摄取;阳离子多粘菌素(粘菌素和多粘菌素b),其与微生物细胞的结合也依赖于膜的负电荷,并且通过减少膜负电荷发生突变和质粒介导的抗性;和达托霉素,类似于宿主先天免疫反应阳离子抗微生物剂肽的脂肽,并且其膜破坏作用机制需要ca2+和磷脂酰甘油,并且其抗性也可以涉及细胞表面电荷的改变。
当微生物为真菌时,示例性抗微生物剂包括5-氟胞嘧啶、阿巴芬净(abafungin)、阿巴康唑(albaconazole)、烯丙胺、两性霉素b、氟胞嘧啶、阿尼芬净、唑、秘鲁香脂、苯甲酸、联苯苄唑、布康唑、克念菌素、卡泊芬净、环吡酮、克霉唑、克立米巴(cresemba)、结晶紫、大扶康、棘球白素类、益康唑、艾氟康唑(efinaconazole)、氟环唑(epoxiconazole)、芬替康唑、非律平、氟康唑、氟胞嘧啶、微粉化灰黄霉素制剂、灰黄霉素、超微粉化灰黄霉素制剂、卤普罗近、哈霉素、咪唑、isavuconazole、isavuconazonium、异康唑、伊曲康唑、酮康唑、兰美抒、卢立康唑(luliconazole)、米卡芬净(micafungin)、咪康唑、那他霉素、泊沙康唑(noxafil)、制霉菌素、奥美康唑、onmel、oravig、奥昔康唑、泊沙康唑、丙环唑(propiconazole)、雷夫康唑、龟裂杀菌素、舍他康唑、斯皮仁诺、硫康唑、特比萘芬、特康唑、噻唑、硫代氨基甲酸酯抗真菌剂、噻康唑、托萘酯、三唑、十一烯酸、含伏立康唑(vfend)、伏立康唑及其属或其变体。
当微生物为原生动物时,示例性抗微生物剂包括8-氨基喹啉、乙酰胂胺、抗变形虫的药剂、臭椿苦酮、阿莫地喹、两性霉素b、安普罗铵、抗毛滴虫药、除虐霉素(aplasmomycin)、胂噻醇、artelinicacid、、蒿甲醚、蒿甲醚/本芴醇、青蒿素、蒿乙醚、青蒿氧烷(arterolane)、青蒿琥酯、蒿甲醚/阿莫地喹、阿托伐醌、阿托伐醌/氯胍、阿扎硝唑、阿奇霉素、苄硝唑、溴羟喹啉、布帕伐醌、卡巴胂、卡硝唑、喹碘方、氯喹、氯丙胍、氯丙胍/氨苯砜、氯丙胍/氨苯砜/青蒿琥酯、氯喹那多、囊泡藻界(chromalveolate)杀寄生虫药、金鸡纳皮、cipargamin、克拉珠剂、克立法胺、氯碘羟喹、抗球虫药、codinaeopsin、cotrifazid、白叶藤素、环氯胍、去氢依米丁、双苯他胂、二氢青蒿素、二氯尼特、二脒那秦、戒酒硫、多西环素、依氟鸟氨酸、elq-300、依米丁、依托法胺、excavata杀寄生虫药、夫马洁林、呋喃唑酮、甘铋胂、gnf6702、卤泛群、羟氯喹、咪多卡、异丙硝唑、jesuit树皮、本芴醇、马度米星、甲氟喹、megazol、锑酸葡胺、美拉胂醇、米帕林、甲硝唑、米替福新、neuroleninb、硝卡巴嗪、硝呋替莫、尼莫唑、硝苯胂酸、两面针碱、呋喃西林、olivacine、奥硝唑、oroidin、帕马喹、巴龙霉素、喷他脒、五价含胂药剂、泛喹酮、氧二苯脒、哌喹、伯氨喹、氯呱、project523、普罗硝唑、乙胺嘧啶、咯萘啶、喹法米特、奎宁、罗硝唑、schedularomana、scyx-7158、塞克硝唑、塞马莫德(semapimod)、葡萄糖酸锑钠、螺吲哚酮、磺胺多辛、磺胺多辛-乙胺嘧啶、磺胺林、苏拉明、他非诺奎、替克洛占、替诺尼唑、甲溴羟喹、替硝唑、三甲曲沙、杀锥虫药、瓦勃氏酊剂及其属或其变体。
抗微生物剂可以是通过类似于本文所述的药物的机制操作的药物。本领域已知的其它抗微生物剂药物可以用于本文所述的方法中。
液体悬浮液
液体可以包括生长培养基,例如阳离子调节的muellerhinton肉汤。该培养基可以包含本领域技术人员已知的添加剂以促进微生物生长和稳定性。除了不同的抗微生物剂之外,不同的测试孔可以包含已知改进特定抗微生物剂的ast准确度的添加剂。例如,可以向包含苯唑西林的测试中加入另外的氯化钠,并向包含达托霉素的测试中加入另外的钙。
生物样品
本文所述的微生物可以衍生自生物样品。在一些实施方案中,生物样品是包含微生物(例如细菌和真菌细胞)的任何样品。生物样品可以衍生自临床样品。
示例性生物样品可以包括但不限于全血、血浆、血清、痰、尿、粪便、白细胞、红细胞、血沉棕黄层、泪液、粘液、唾液、精液、阴道液、淋巴液、羊水、脊髓液或脑脊液、腹膜渗出液、胸腔积液、渗出液、点状渗出液、上皮涂片、活检、骨髓样品、来自囊肿或脓肿的液体、滑液、玻璃体液或房水、洗眼液或抽吸液、支气管肺泡灌洗液、支气管灌洗液或肺灌洗液、肺抽吸液,以及器官和组织,包括但不限于肝、脾、肾、肺、肠、脑、心脏、肌肉、胰腺等,拭子(包括但不限于伤口拭子、颊拭子、喉拭子、鼻拭子、阴道拭子、尿道拭子、宫颈拭子、直肠拭子、病变拭子、脓肿拭子、鼻咽拭子等),及其任何组合。还包括细菌培养物或细菌分离物、真菌培养物或真菌分离物。普通技术人员也可以理解,从任何上述示例性生物样品获得的分离物、提取物或材料也在本发明的范围内。
从生物样品获得的微生物可以如本领域常规进行的那样进行培养或以其它方式处理。
用于ast方法的对照
对照可以包括微生物不易感的抗微生物剂。作为实例,如果该测定用于确定革兰氏阳性细菌的敏感性,则对照(和测试孵育)可以包括一种或多种靶向革兰氏阴性细菌的抗微生物剂,而如果该测定用于确定真核微生物的敏感性,对照(和测试孵育养)可以包括一种或多种抗菌抗微生物剂。
在一些实施方案中,对照是在其它方面相同条件但无抗微生物剂或具有一种或多种微生物不易感的抗微生物剂下从微生物测量的阳性对照。在一些实施方案中,对照在其它方面相同条件但无营养物下从微生物测量。在一些实施方案中,对照在其它方面相同条件具有一种或多种已知抑制微生物生长的毒素下从微生物测量。
对照可以是历史对照。在一些实施方案中,在已经进行对照孵育之后进行测试孵育。在一些实施方案中,对照在与包含测试孵育的盒不同的盒中进行。
盒
盒可以是能够容纳微生物的液体悬浮液并允许其生长的容器。盒的非限制性实例可以包括培养瓶、培养皿(culturedish)、培养皿(petridish)、生物测定皿、培养管、测试管、微量离心管、瓶、微室板、多室板、微量滴定板、微孔板。所述盒可以包含一个室。所述盒可以包括多个室,每个室是能够容纳与另一空间物理隔离的液体悬浮液的空间;室的一个实例是多层板中的室。所述盒可以包含1、2、3、4、5、6、7、8、9、10、11、12、24、48、96、192、384、1536个或更多个室,以及其间的任何数量的室。盒室的底部可以是平的、圆的或v形的。
存在于盒上的多个室内的抗微生物剂可以悬浮于介质中。在一些实施方案中,抗微生物剂以抗微生物剂膜的形式存在。在某些实施方案中,抗微生物剂为固体形式。在一些实施方案中,固体抗微生物剂为冻干和/或干燥的。某些实施方案提供了一种或多种抗微生物剂,其作为抗微生物剂膜以固体形式、在引入微生物的悬浮液之前冻干形式或干燥形式存在于一个或多个盒室中。
在用样品接种板之前,抗微生物剂稀释系列可以是冷冻的、冻干的或新鲜制备的。在一些情况下,可以手工或使用自动化系统进行盒的接种。在一些实例中,例如在新鲜抗微生物剂板的情况下,自动化的液体处理系统可以用于制备具有抗微生物剂稀释系列的盒。接种方法可以包括可能是本领域已知的各种方法中的任一种。
如本文所述,盒可以用于容纳流体的各种组合,以进行多个测试序列,例如检查点测定和多个不同的生长测定。在一些实施方案中,盒具有用于促进一种或多种检验点测定的一组室和用于促进一种或多种生长测定的一组室。通过实例的方式,盒可以包括以行和列布置的室的阵列。所述盒可以包括对照室组和抗微生物剂测试室组。对照室组可以包括两个室,而测试室组可以包括沿板的剩余的室。在一些实施方案中,对照室组包括至少两个室,其中一个室是生长室,而另一个室是非生长室。在一些实施方案中,生长室包括或被接种以包括肉汤和患者样品的组合,使得患者样品中的微生物可以在孵育期期间在肉汤内生长。在某些实施方案中,不向检查点测定室中加入抗微生物剂。而在一些实施方案中,非生长室可以包括或被接种以包括不含患者样品的肉汤(即,不存在来自患者样品的微生物的肉汤)。在一些实施方案中,也不向非生长室中加入抗微生物剂。因此,在孵育期期间,与微生物可以在其中生长的生长室相比,非生长室可以用作基线。
在一些实施方案中,每个盒包括“测试面板”,以每个抗微生物剂的限定的稀释系列(例如,2倍稀释系列、10倍稀释系列等)跨多个孔分布的多个抗微生物剂。此外,每个盒或测试面板可以含有对照室,例如生长对照室、非生长(污染)对照室和/或盐水对照室。盐水对照室可以代表fit对照,其大约等于接种物中微生物的初始浓度。所述盒可以包括多个室(例如96室盒或384室盒),所述室具有盖(例如可去除的盖)和唯一地限定抗生素配置的标识符(例如条形码)和唯一代码,所述唯一代码限定板并且可以与符合hipaa的唯一患者样品缔合。
测试室可以包括患者样品和各种类型和浓度的抗微生物剂的各种组合中的任一种,其中可以分析敏感性。室的行可以专用于特定的抗微生物剂,并且该抗微生物剂的浓度可以在同一行的列之间变化。例如,盒可具有一排含有青霉素的室,其中从左到右的每个室含有浓度渐增的青霉素。
当然,其它实例也是可能的。例如,不同的室和不同组的室可以沿着盒定位在各种位置中的任何位置处。另外,不同组的室(例如,对照室和测试室)可以包括沿着盒的更多或更少的单独的室。另外,在一些情况下,在测试期间不是所有室都被使用/占用。
自动化的ast方法
本文所述的方法可以使用市售可得的设备、定制设备或其组合以自动化的方式进行。所述方法的自动化允许进行更多数量的测定以及增加测定之间的一致性。自动化也可以提高这些方法的速度和分辨率。
表面结合探针测定
表面结合测定(也称为表面结合探针测定)可以利用信号传导剂。信号传导剂通常包含能够结合到微生物的部分(例如,结合到微生物表面的抗体和/或凝集素、非特异性结合到微生物表面的带电荷的部分和/或功能部分)和能够提供信号或有助于产生信号的化学部分(例如,酶化学发光体和镧系元素螯合物)。示例性酶包括辣根过氧化物酶、碱性磷酸酶、乙酰胆碱酯酶、葡萄糖氧化酶、β-d-半乳糖苷酶、β-内酰胺酶及其组合。
信号发生剂可以包括与一种或多种微生物受体缀合的一种或多种化学部分。信号发生剂包括但不限于一种或多种催化剂(包括酶、金属氧化物纳米颗粒、有机金属催化剂、设计用于信号放大的纳米颗粒(例如在本申请要求优先权并通过引用以其整体并入本文的美国临时申请中描述的那些)、包含信号发生元件的噬菌体、荧光团(包括有机荧光团、铕或钌(ii)、铼(i)、钯(ii)、含铂(ii)的有机金属)和/或比色染料(包括有机染色剂)。可以使用上述的组合,例如纳米颗粒、树状分子和/或具有酶、荧光团和/或有机金属分子的其它纳米规格结构。
在信号传导剂与微生物接触之前,在信号传导剂最初与微生物接触的同时,或在信号传导剂已经与微生物接触之后,可以将化学部分与信号传导剂缀合。
当将信号传导剂加入到含有微生物的ast稀释物中时,信号传导剂受体(例如,可以特异性或非特异性结合到微生物的部分)可以与微生物表面缔合。因此,例如,在溶液中存在的完整微生物越多,则与这些细菌缔合的信号传导剂的数量就越多。因此,完整细菌的数目与溶液中游离的信号传导剂的数目之间存在相反的关系,如由未结合到完整细菌的那些信号传导剂所限定。注意到,如果例如微生物响应于抗微生物剂处理而裂解,游离信号传导剂可以结合到可溶性微生物组分。
与微生物表面缔合和/或插入微生物表面的信号传导剂的数量与微生物表面积成比例。微生物表面积与真正抗性的微生物强烈相关。特别地,在微生物响应mic浓度和亚mic浓度的抗微生物剂(例如,细丝形成细菌)而膨胀或伸长的情况下,已知代谢和/或体积鉴定对于快速ast时间点给出假的敏感性分布,限定为少于六小时的那些。为了克服该限制,本发明将微生物表面积(而不是体积)转化为可测量的信号,例如光学信号。本文所述的方法能够在少于六小时内准确地确定微生物抗性分布。
为了将与微生物缔合和/或插入微生物中的信号传导剂与游离的信号传导剂分离,可能需要进行一个或多个分离和/或竞争性结合步骤。这样的步骤包括但不限于离心(例如,用>500×g的g-力)、过滤(例如,通过具有小于或等于0.45微米、或小于或等于0.2微米的孔的过滤器)、电泳和/或磁性捕获;这样的步骤是本领域技术人员公知的。
为了促进信号传导剂结合和/或降低背景,在加入信号传导剂之前,从孵育期间微生物悬浮在其中的液体中分离微生物可能是进一步有利的。这样的分离可以包括但不限于离心、过滤、电泳和/或磁性捕获。
信号传导剂可以与微生物和/或抗微生物剂一起加入,使得它们在整个ast孵育阶段存在。该总时间段可以长达24小时,或在8小时内,或在5小时内。或者,在规定的孵育期之后,可以将信号传导剂加入到微生物和抗微生物剂中。该时间段可以长达24小时,或在8小时内,或在4小时内。
信号传导剂设计成与微生物表面(包括壁和/或膜)缔合和/或插入微生物表面(包括壁和/或膜)。设计用于缔合的信号传导剂包含结合部分,包括但不限于一种或多种抗体、凝集素、其它蛋白质、具有一个或多个带电荷的化学基团的小分子、具有一个或多个功能性化学基团的小分子、噬菌体、糖蛋白、肽、适配体、带电荷的小分子、具有固定电荷的小分子、带电荷的聚合物、具有固定电荷的带电荷的聚合物、疏水性小分子、带电荷的肽、具有固定电荷的带电荷的肽、具有交替的亲水性和疏水性区域的肽、和/或小分子配体(其可以是或可以不是有机金属络合物)。设计用于微生物缔合的分子是本领域技术人员公知的。信号传导剂可以保持结合到微生物和/或可以被内在化,因此包括所有的缔合。设计用于插入的信号传导剂可以包括但不限于小的疏水性分子、疏水性肽和/或具有交替的疏水性和亲水性区域的肽。设计用于微生物插入的分子是本领域技术人员公知的。信号传导剂可以进一步对一种或多种类型的微生物为特异性的。信号传导剂可以具有多种受体。这些可以增强结合和/或使得能够同时结合到两种或更多种微生物,其可以进一步用于凝集细菌。在加入信号传导剂之前或同时,调节溶液ph可能是有利的。这对于增强微生物和信号传导剂之间的电荷-电荷相互作用可能是有益的。微生物的阴离子电荷可以通过滴定溶液ph值超过中性(碱性更强)来增加。因此,利用具有一个或多个固定的阳离子电荷的部分可能是有益的。
值得注意的是,信号传导剂可以特异性地结合到微生物(例如,特异性地结合到微生物物种或微生物的菌株的抗体)或可以非特异性地结合到微生物(例如,通过本领域已知的一般共价或非共价键形成和另一种非特异性化学缔合)。
或者,可以将能够与信号传导剂缔合的化学品和/或生物化学品加入到微生物在生长期间悬浮于其中的液体中,使得化学品和/或生物化学品在孵育期间掺入微生物中。这可以用于增强信号传导剂与微生物的缔合。在替代实施方案中,信号传导剂本身可以存在于微生物在孵育期间悬浮于其中的液体中,并且可在生长期间掺入微生物中。
信号传导剂可以包含放大剂信号发生剂(放大剂组),使得来自每个完整微生物的信号可以被放大超过与每个微生物缔合的信号传导剂的数目。例如,已知酶辣根过氧化物酶(hrp)能够放大信号>1×104倍。因此,如果100个hrp分子结合到每个微生物表面,可以实现106的放大。这可以通过区分微生物浓度来提高ast确定的速度,否则所述微生物浓度不能被区分。铕制剂的使用类似地提供信号放大。
或者,信号传导剂可以包含本领域技术人员已知的光学染料前体,如膜染料,其设计成在插入疏水区域(如细胞膜)后大大增加荧光发射。用这些信号传导剂设计的测定可能需要将微生物集中到更小的体积中,接近平面,以产生足够的信号,以容易地光学测量。干扰物质可能需要使用近红外荧光团。
示例性放大剂组包括在例如国际公开号wo2016/015027和国际申请号pct/us16/42589中描述的那些,各自通过引用以其整体并入本文。放大剂组可以包含催化剂、荧光团、比色染料、酶、催化剂或纳米颗粒。示例性荧光团包括在国际申请号pct/us16/42589的图1,表1中描述的那些,其通过引用以其整体并入本文。放大剂组可以包含镧系元素。镧系元素包括但不限于铕、锶、铽、钐或镝。
放大剂组可以包含有机荧光团,例如配位络合物。所述配位络合物可以是铕配位络合物、钌配位络合物、铼配位络合物、钯配位络合物、铂配位络合物。放大剂可以包含化学发光体、量子点、酶、铁配位催化剂、铕配位络合物、钌配位络合物、铼配位络合物、钯配位络合物、铂配位络合物、钐配位络合物、铽配位络合物或镝配位络合物。
在一些实施方案中,放大剂组包含如下部分:
在一些实施方案中,放大剂组包含如下部分:
放大剂组可以包含荧光团或比色染料。合适的荧光团和比色染料是本领域技术人员公知的,并且描述于themolecularprobes®handbook:aguidetofluorescentprobesandlabelingtechnologies,第11版(2010)以及gomes,fernandes和limaj.biochem.biophys.methods65(2005)第45-80页,其通过引用以其整体并入本文。示例性荧光团还包括例如在国际公开号wo2016/015027和国际申请号pct/us16/42589中描述的那些,各自通过引用以其整体并入本文。
合适的荧光团或比色染料的实例包括但不限于溴乙啡啶、碘化丙锭、sytox绿、菲啶、吖啶、吲哚、咪唑、花青、toto、to-pro、syto、5-羧基-2,7-二氯荧光素、5-羧基荧光素(5-fam)、5-羧基萘荧光素、5-羧基四甲基罗丹明(5-tamra)、5-fam(5-羧基荧光素)、5-hat(羟基色胺)、5-rox(羧基-x-罗丹明)、6-羧基罗丹明6g、7-氨基-4-甲基香豆素、7-氨基放线菌素d(7-aad)、7-羟基-4-甲基香豆素、9-氨基-6-氯-2-甲氧基吖啶、acma(9-氨基-6-氯-2-甲氧基吖啶)、吖啶、alexafluoros、茜素、别藻蓝素(apc)、amca(氨基甲基香豆素)、bodipy、羧基-x-罗丹明、儿茶酚胺、荧光素(fitc)、羟基香豆素、丽丝胺罗丹明、monobromobimane、oregongreen、藻红素、syto、硫二碳菁染料(disc3)、硫磺素、x-罗丹明、c或四甲基罗丹明异硫氰酸酯。
放大剂组可以包含有机金属化合物、过渡金属络合物或配位络合物。这样的放大剂组的实例包括但不限于在ep0180492、ep0321353、ep0539435、ep0539477、ep0569496、ep139675、ep64484、us4,283,382、us4,565,790、us4,719,182、us4,735,907、us4,808,541、us4,927,923、us5,162,508、us5,220,012、us5,324,825、us5,346,996、us5,373,093、us5,432,101、us5,457,185、us5,512,493、us5,527,684、us5,534,622、us5,627,074、us5,696,240、us6,100,394、us6,340,744、us6,524,727、us6,717,354、us7,067,320、us7,364,597、us7,393,599、us7,456,023、us7,465,747、us7,625,930、us7,854,919、us7,910,088、us7,955,859、us7,968,904、us8,007,926、us8,012,609、us8,017,254、us8,018,145、us8,048,659、us8,067,100、us8,129,897、us8,174,001、us8,183,586、us8,193,174、us8,221,719、us8,288,763、us8,362,691、us8,383,249、us8,492,783、us8,632,753、us8,663,603、us8,722,881、us8,754,206、us8,890,402、us8,969,862、us9,012,034、us9,056,138、us9,118,028、us9,133,205、us9,187,690、us9,193,746、us9,312,496、us9,337,432、us9,343,685、us9,391,288和us9,537,107中所述的那些,其通过引用以其整体并入本文。示例性有机金属化合物、过渡金属络合物或配位络合物还包括例如在国际公开号wo2016/015027和国际申请号pct/us16/42589中描述的那些,各自通过引用以其整体并入本文。
在一些实施方案中,放大剂组是镧系元素配位络合物,例如镧系元素(例如eu或tb)和四齿配体之间的络合物或镧系元素(例如eu或tb)和穴状化合物配体之间的络合物。在一些实施方案中,放大剂组是镧(la)、铈(ce)、镨(pr)、钕(pm)、钐(sm)、铕(eu)、钆(gd)、铽(tb)、镝(dy)、钬(ho)、铒(er)、铥(tm)、镱(yb)、镥(lu)、钌(ru)、铑(rh)、钯(pd)、锇(os)、铱(ir)或铂(pt)的配位络合物。在一些实施方案中,放大剂组是稀土金属的配位络合物,稀土金属总体上是指17种元素,其由从原子序数为57的镧到原子序数为71的镥的15种元素(镧系元素)以及由原子序数为21的钪和原子序数为39的钇的两种另外的元素组成。稀土金属的具体实例包括铕、铽、镧、铈、镨、钕、钷、钐、钆、镝、钬、铒、铥、镱、镥、钪和钇。在一些实施方案中,放大剂组是镧系元素(例如铕或铽)与二亚乙基三胺四乙酸或穴状化合物配体的配位络合物。
信号传导剂的具体实例包括但不限于包含以下的部分:
信号传导剂可以包含发光体(供体),其特征在于高发光量子效率和长的发光衰减时间(>100ns)。示例性发光体是钯、铑、铂、钌、锇、稀土元素(特别是铕和镧)的阳离子金属有机络合物。这些金属有机络合物的有机部分可以由例如卟啉、联吡啶、菲咯啉或其它杂环化合物的配体组成。
在一些实施方案中,能够结合微生物表面的信号传导剂包含抗体(例如单克隆或多克隆的)、修饰的抗体(例如生物素化的单克隆抗体、生物素化的多克隆抗体、铕螯合物-抗体、辣根过氧化物酶缀合的抗体)、抗体变体(例如fab:片段、抗原结合(一个臂);f(ab')2:片段、抗原结合,包括铰链区域(两个臂);fab':片段、抗原结合,包括铰链区域(一个臂);scfv:单链可变片段;二-scfv:二聚单链可变片段;sdab:单结构域抗体;双特异性单克隆抗体;三功能抗体;和bite:双特异性t细胞接合物)、wga-生物素、多粘菌素b-生物素、凝集素、天然肽、合成肽、合成和/或天然配体、合成和/或天然聚合物、合成和/或天然糖聚合物、碳水化合物结合蛋白和/或聚合物、糖蛋白结合蛋白和/或聚合物、带电荷的小分子、其它蛋白质、噬菌体和/或适配体。
在一些实施方案中,能够结合微生物表面的信号传导剂包含或由包含抗体、凝集素、天然肽、合成肽、合成和/或天然配体、合成和/或天然聚合物、合成和/或天然糖聚合物、碳水化合物结合蛋白和/或聚合物、糖蛋白结合蛋白和/或聚合物、带电荷的小分子、其它蛋白质、噬菌体和/或适配体的结构形成。
在一些实施方案中,能够结合微生物表面的信号传导剂包含放大剂组,所述放大剂组包含镧系元素配位络合物和/或酶和链霉亲和素和/或抗体和/或适配体。在一些实施方案中,能够结合微生物表面的信号传导剂包含结合部分,所述结合部分包含多克隆和/或单克隆抗体。
在一些实施方案中,能够结合微生物表面的信号传导剂包含结合部分,所述结合部分包含修饰的抗体。示例性修饰的抗体包括生物素化的单克隆抗体、生物素化的多克隆抗体、铕螯合物-抗体和辣根过氧化物酶缀合的抗体。在一些实施方案中,能够结合微生物表面的信号传导剂包含结合部分,所述结合部分包含抗体变体。示例性抗体变体包括fab:片段、抗原结合(一个臂);f(ab')2:片段、抗原结合,包括铰链区域(两个臂);fab':片段、抗原结合,包括铰链区域(一个臂);scfv:单链可变片段;二-scfv:二聚单链可变片段;sdab:单结构域抗体;双特异性单克隆抗体;三功能抗体;和bite:双特异性t细胞接合物。
在一些实施方案中,能够结合微生物表面的信号传导剂包含wga-生物素或多粘菌素b-生物素。在一些实施方案中,能够结合微生物表面的信号传导剂包含结合部分,所述结合部分包含合成和/或天然配体和/或肽。在一些实施方案中,配体和/或肽选自双(锌-二甲基吡啶基胺)、tat肽、丝氨酸蛋白酶、cathelicidins、阳离子糊精、阳离子环糊精、水杨酸、赖氨酸及其组合。在一些实施方案中,能够结合微生物表面的信号传导剂包含结合部分,所述结合部分包含合成和/或天然聚合物和/或糖聚合物。在实施方案中,天然和/或合成聚合物是线性或支化的,并且选自支链淀粉、聚(n-[3-(二甲基氨基)丙基]甲基丙烯酰胺)、聚(乙烯亚胺)、聚-l-赖氨酸、聚[甲基丙烯酸2-(n,n-二甲基氨基)乙酯]及其组合。在一些实施方案中,天然和/或合成聚合物和/或糖基聚合物包含结合部分,所述部分包括但不限于壳聚糖、明胶、葡聚糖、海藻糖、纤维素、甘露糖、阳离子葡聚糖和环葡聚糖、季胺、三溴吡啶鎓、组氨酸、赖氨酸、半胱氨酸、精氨酸、锍、鏻或其组合,包括但不限于共嵌段、接枝和交替聚合物。在一些实施方案中,能够结合微生物表面的信号传导剂包含结合部分,所述结合部分包含选自甘露糖结合凝集素、其它凝集素、膜联蛋白及其组合的糖蛋白。
在一些实施方案中,能够结合微生物表面的信号传导剂包含:抗体;和铕配位络合物。在一些实施方案中,能够结合微生物表面的信号传导剂包含连接基团l,其包含nh2-peg-生物素(2k)、nh2-peg-生物素(4k)、硫代-nhs-生物素、wga-生物素或多粘菌素b-生物素。在一些实施方案中,能够结合微生物表面的信号传导剂包含铕络合物,所述铕络合物包含:
在一些实施方案中,能够结合微生物表面的信号传导剂包含铕络合物,所述铕络合物包含:
或者,信号传导剂可以是一对的一部分,如fret/tr-fret供体和受体或由光敏剂和检测剂组成的单线态氧对。用这些信号传导剂设计的测定可能需要将微生物与初始生长培养基分离,随后在加入信号传导剂之前重悬浮于所需的反应缓冲液中。相反,由于产生信号所需的相对距离,用这些信号传导剂设计的测定可能不需要分离步骤。
fret/tr-fret供体的实例包括但不限于含有镧系元素(eu、sm、dy或tb)的穴状化合物有机金属(cisbio)、lanceeu-w1024(perkinelmer)、lanceeu-w8044(perkinelmer),以及任何有机荧光对供体。
fret/tr-fret受体的实例包括但不限于匹配的有机染料,例如ulight染料(perkinelmer)、surelightapc(perkinelmer)、别藻蓝素、cy5、d2染料(cisbio),以及任何有机荧光对受体。
单线态氧光敏剂的实例包括但不限于methuselahgreencarboxy(ursabio)、sensitizerblue(ursabio)、孟加拉玫瑰红、赤藓红b、亚甲蓝、叶绿素、alphabead供体(perkinelmer)。
单线态氧检测剂的实例包括但不限于单线态氧检测剂绿(thermofisher)、反式-1-(2’-甲氧基乙烯基)芘、si-dma(dojindo)、alphabead受体(perkinelmer)。
掺入剂的实例包括但不限于乙炔基-d-丙氨酸(eda)、叠氮基-d-丙氨酸(ada)、在angewchemintedengl.2012年12月7日;51(50):12519-12523中所述的荧光d-丙氨酸。
实施例
实施例1:低阴离子电荷生物体不被铕-穴状化合物-二胺探针结合。
细菌(大肠杆菌和奇异变形杆菌)在营养肉汤(mhb)或盐水(阴性对照)中生长并与铕探针结合。通过将菌落稀释到盐水中以达到mcfarland值为0.5(其使用分光光度计验证)来制备细菌,将其稀释并接种到含有阳离子调节的muellerhinton肉汤或盐水的96孔板中。将板在35℃下孵育,在150rpm下振荡3小时,之后将10μl的alamarblue加入到每个孔中,并将板再孵育1小时。在此孵育后,将100μl具有1%tween-20的磷酸盐缓冲的盐水(pbs)加入到每个孔中。将板放置在450rpm的振荡器上10分钟,然后在2500×g下离心2.5分钟。抽吸孔,并将100μl具有0.05%tween-20的pbs(pbst)添加回孔中。将10微升eu-穴状化合物-二胺(5ng/孔)加入到每个孔中,并将板振荡10分钟。然后将板进行离心,抽吸孔,并将200μl1×pbst加入到每个孔中。将这些步骤重复两次。在最后的洗涤后,在330/615nm下读取所有孔的时间分辨荧光。
如图2所示,大肠杆菌被铕探针良好结合,并因此在细菌生长的条件(mhb)中相对于在没有发生生长的条件(盐水)中显示高信号。然而,低阴离子电荷生物体奇异变形杆菌在mhb和盐水条件两者下都证明低trf信号,指示铕探针的结合差。
实施例2:阳离子表面活性剂ctab使低阴离子电荷生物体能够被铕-穴状化合物-二胺结合
通过将菌落稀释到盐水中以达到mcfarland值为0.5(其使用分光光度计进行验证)来制备奇异变形杆菌,将其稀释并接种到含有阳离子调节的muellerhinton肉汤或盐水的96孔板中。将板在35℃下孵育,在150rpm下振荡3小时,之后将10μl的alamarblue加入到每个孔中,并将板再孵育1小时。在此孵育后,将100μl的0.03%十六烷基三甲基溴化铵和0.1medta溶液加入到每个孔中。将板放置在450rpm的振荡器上10分钟,然后在2500×g下离心2.5分钟。抽吸孔,并将100μl具有0.05%tween-20的pbs(pbst)添加回孔中。将10微升eu-穴状化合物-二胺(5ng/孔)加入到每个孔中,并将板振荡10分钟。然后将板进行离心,抽吸孔,并将200μl1×pbst加入到每个孔中。将这些步骤重复两次。在最后的洗涤后,在330/615nm下读取所有孔的时间分辨荧光。
图3显示在盐水条件下trf信号如预期的那样低,而在mhb条件下信号增加,指示ctab预处理后铕穴状化合物探针的结合。
实施例3:去除阳离子表面活性剂ctab改进铕-穴状化合物-二胺结合
通过将菌落稀释到盐水中以达到mcfarland值为0.5(其使用分光光度计验证该值)来制备金黄色葡萄球菌,将其稀释并接种到含有阳离子调节的muellerhinton肉汤和万古霉素的两倍稀释的96孔板中。将板在35℃下孵育,在150rpm下振荡3小时,之后将10μl的alamarblue加入到每个孔中,并将板再孵育1小时。在此孵育后,将100μl具有0.1medta溶液的0.03%十六烷基三甲基溴化铵加入到每个孔中。将板放置在450rpm的振荡器上10分钟,然后在2500×g下离心2.5分钟。抽吸孔,并将100μl具有0.05%tween-20的pbs(pbst)或100μl具有0.1medta溶液的0.03%十六烷基三甲基溴化铵添加回孔中。将10微升eu-穴状化合物-二胺(5ng/孔)加入到每个孔中,并将板振荡10分钟。然后将板进行离心,抽吸孔,并将200μl1×pbst加入到每个孔中。将这些步骤重复两次。在最后的洗涤后,在330/615nm下读取所有孔的时间分辨荧光(trf)。
如图4所示,在没有添加回ctab的条件下,观察到对van的剂量依赖性反应,而van处理的金黄色葡萄球菌样品似乎具有2μg/ml的mic。然而,当添加回ctab时,没有观察到剂量关系,这指示ctab可能干扰eu-穴状化合物-二胺探针的结合或信号传导。
实施例4:用标准阴离子电荷ctab预处理生物体降低铕-穴状化合物-二胺结合。
通过将菌落稀释到盐水中以达到mcfarland值为0.5(其使用分光光度计验证)来制备大肠杆菌,将其稀释并接种到含有阳离子调节的muellerhinton肉汤和两种抗生素(哌拉西林-三唑巴坦(tzp)和阿兹色霉素(atm))的两倍稀释的96孔板中。将板在35℃下孵育,在150rpm下振荡3小时,之后将10μl的alamarblue加入到每个孔中,并将板再孵育1小时。在此孵育后,将100μl去污剂溶液(具有1%tween-20的磷酸盐缓冲的盐水或具有0.1medta的0.03%十六烷基三甲基溴化铵)加入到每个孔中。将板放置在450rpm的振荡器上10分钟,然后在2500×g下离心2.5分钟。抽吸孔,并将100μl具有0.05%tween-20的pbs(pbst)添加回孔中。将10微升eu-穴状化合物-二胺(5ng/孔)加入到每个孔中,并将板振荡10分钟。然后将板进行离心,抽吸孔,并将200μl1×pbst加入到每个孔中。将这些步骤重复两次。在最后的洗涤后,在330/615nm下读取所有孔的时间分辨荧光。
实施例5:阴离子比预测合适的表面活性剂处理条件
通过将菌落稀释到盐水中以达到mcfarland值为0.5(其使用分光光度计验证)来制备奇异变形杆菌和克雷白氏肺炎杆菌,将其稀释并接种到含有阳离子调节的muellerhinton肉汤和庆大霉素(gen)和环丙沙星(cip)的两倍稀释的96孔板中。将板在35℃下孵育,在150rpm下振荡3小时,之后将10μl的alamarblue加入到每个孔中,并将板再孵育1小时。在此孵育后,以荧光信号ex560/em590读取alamarblue信号。然后,将100μl去污剂溶液(具有1%tween-20的磷酸盐缓冲的盐水或具有0.1medta的0.03%十六烷基三甲基溴化铵)加入到每个孔中。将板放置在450rpm的振荡器上10分钟,然后在2500×g下离心2.5分钟。抽吸孔,并将100μl具有0.05%tween-20的pbs(pbst)添加回孔中。将10微升eu-穴状化合物-二胺(5ng/孔)加入到每个孔中,并将板振荡10分钟。然后将板进行离心,抽吸孔,并将200μl1×pbst加入到每个孔中。将这些步骤重复两次。在最后的洗涤后,在330/615nm下读取所有孔的时间分辨荧光。
从在4μg/ml粘菌素中生长的细菌的背景扣除荧光信号(ex560/em590)除以在mhb中生长的细菌的背景扣除荧光信号计算阴离子比。奇异变形杆菌的阴离子比为0.96,表明受粘菌素的抑制很小或没有抑制,并且具有减少的阴离子电荷,而克雷白氏肺炎杆菌的阴离子比为-.08,表明高度的生长抑制和标准阴离子电荷。因此,奇异变形杆菌样品用ctab预处理,而克雷白氏肺炎杆菌样品接受pbst。trf信号如图7所示,并显示与每种生物体中的每种抗微生物剂的已知mic值一致的剂量关系,指示基于阴离子比选择正确的预处理条件。
- 还没有人留言评论。精彩留言会获得点赞!