用于高压应用的用于将酸性气体从工艺气体物流移除的非水性溶剂的制作方法
用于高压应用的用于将酸性气体从工艺气体物流移除的非水性溶剂
1.相关申请的交叉引用
2.本技术要求于2019年12月11日提交的美国临时专利申请no.62/946,737的权益,所述专利的全部内容以引用的方式并入本文。
技术领域
3.本发明涉及用于将酸性气体从气体物流移除的溶剂体系,以及使用这样的体系的装置和方法。例如,所述溶剂体系可在高压应用中提供酸性气体(诸如二氧化碳(co2)、羰基硫化物(cos)、二硫化碳(cs2)、硫氧化物(so
x
)或其组合)的移除。
背景技术:
4.将酸性气体从气体物流分离或移除是各种工业工艺中的重要步骤。例如,将酸性气体从合成气以及天然气生产中的工艺物流移除。这些气体通常含有一定水平的酸气体污染物,无论其来自天然气源还是合成气体生产中上游化学反应的副产物。将这些酸气体(诸如co2、cos、cs2、h2s、so
x
、no
x
、hcl,等等)从产物气体移除,以满足所要求的管线规范、下游气体纯度需求,或者防止下游工艺中的催化剂中毒。
5.在典型的基于溶剂的工艺中,使待处理的工艺气体物流通过与气体物流中的酸性化合物(例如co2和so2)反应并将其与非酸性组分分离的液体溶剂。所述溶剂变得富含酸气体组分,随后将所述酸气体组分在不同组操作条件下移除,使得可将所述溶剂再循环,以用于另外的酸气体移除。
6.一般而言,分离工艺包括吸收器和解吸器,伴随着溶剂循环,以将酸气体移除。存在若干用于这样的应用的可商购获得的溶剂,其可归类为水性(富水)和非水性(贫水)体系。典型地,水性体系使用水作为稀释剂,且同时含有20-50重量%的反应物以将酸气体从工艺气体物流移除,而非水性溶剂含有最小量的水以及10至60重量%的活性反应物以将酸气体从工艺气体物流移除。
7.溶剂体系的基本移除机理可归类为物理或化学吸收。物理吸收利用压力以使酸气体分子溶解到液体溶剂中。溶解在物理溶剂中的酸气体的量随着压力增加而成比例地增加。当降低压力时,所述酸气体从富气体的物理溶剂释放。即,酸气体可通过在较低压下将气体从富气体的溶剂闪蒸而释放。将酸气体从物理溶剂释放并回收所述溶剂以再利用所需的能量相对低。然而,对于深度移除(即,移除高浓度的酸气体,例如大于90重量%或大于95重量%)或在低浓度酸气体的情况下(由于在低分压下的溶解性限制),物理溶剂典型地性能不佳。
8.化学吸收涉及酸气体物种与化学吸收溶剂的反应以在所述酸气体和溶剂之间形成化学键。吸收(其性质为放热的)非常快速地发生,并且能够对酸气体进行深度移除,只要所述溶剂含有足够的反应物来与酸气体反应直至其反应极限。反应极限通常是由化学吸收溶剂和酸气体物种的化学计量比确定的。此化学计量比还可用来确定将每单位体积的酸气
体污染物移除需要多少化学吸收溶剂。
9.一般而言,化学吸收反应的逆转(reversal)要求至少将正反应所产生的量的能量添加回到富溶剂,更不用说为了使富气体的化学吸收剂溶剂达到逆转可观的温度以及为了维持条件以使逆反应完成到可观的程度所需要的能量。因此,化学吸收溶剂要求相对高量的能量,以使溶剂和酸性气体之间的化学键解离。在水性溶剂体系中的化学吸收的能量使用增加得甚至更多,因为更多能量用于将水性体系中的过量水加热和蒸发。
10.大部分可商购获得的溶剂或是物理水性溶剂或是化学水性溶剂。水性溶剂广泛用于多种酸气体移除应用。然而,使用水性溶剂具有包括但不限于以下的缺点:腐蚀速率高,为使溶剂再生而能量要求高,以及过程足迹大,所有这些均导致高资本成本。
11.鉴于上述内容,期望提供用于酸气体移除应用的溶剂体系,所述溶剂体系可降低资本成本以及操作成本。
技术实现要素:
12.在本发明的第一方面中,配置成将酸性气体从气体物流移除的非水性溶剂体系包括:由包括含氮碱的化学吸收组分形成的溶液,其中所述含氮碱具有使得其与所述酸性气体的一部分反应的结构;以及包括有机稀释剂的物理吸收组分,其不与酸性气体反应,并且具有使得其在高于大气压的压力下吸收所述酸性气体的一部分的结构。所述溶剂体系具有小于约10g溶剂/100ml水的与水的溶解性。
13.在所述第一方面的特征中,所述含氮碱可包含:1,4-二氮杂双环-十一碳-7-烯("dbu");1,4-二氮杂双环-2,2,2-辛烷;哌嗪("pz");三乙基胺("tea");1,1,3,3-四甲基胍("tmg");1,8-二氮杂双环十一碳-7-烯;单乙醇胺("mea");二乙基胺("dea");乙二胺("eda");1,3-二氨基丙烷;1,4-二氨基丁烷;六亚甲基二胺;1,7-二氨基庚烷;二乙醇胺;二异丙基胺("dipa");4-氨基吡啶;戊基胺;己基胺;庚基胺;辛基胺;壬基胺;癸基胺;叔辛基胺;二辛基胺;二己基胺;2-乙基-1-己基胺;2-氟苯乙基胺;3-氟苯乙基胺;3,5-二氟苄基胺;n-甲基苄基胺;3-氟-n-甲基苄基胺;4-氟-n-甲基苄基胺;咪唑;苯并咪唑;n-甲基咪唑;1-三氟乙酰基咪唑;1,2,3-三唑;1,2,4-三唑;或其混合物。所述有机稀释剂可选自:醇、酮、脂族烃、芳族烃、氮杂环、氧杂环、脂族醚、环状醚、酯、和酰胺,及其混合物。
14.在所述第一方面的另一特征中,所述化学吸收组分可以范围为1至50重量%的浓度存在,相对于总体系计。此外,所述物理吸收组分可以范围为40至95重量%的浓度存在,相对于总体系计。所述体系可进一步包含水。
15.在本发明的第二方面中,将酸性气体从气体物流移除的方法包括:将包含物理吸收组分和化学吸收组分的非水性溶剂体系引入至吸收器器皿,所述吸收器器皿在高于大气压的压力下操作,以及向所述吸收器器皿引入包含酸性气体的气体物流,使得所述气体物流与所述非水性溶剂体系流体接触并且通过所述非水性溶剂体系,由此通过所述溶剂体系将酸性气体从气体物流移除。
16.在本发明的第三方面中,相对于常规水性溶剂的溶剂再生所要求的能量的量而言降低酸性气体洗涤工艺中非水性溶剂体系(nass)的溶剂再生所要求的能量的量的方法包括:使用如上文所描述的nass在吸收器器皿中将酸性气体从工艺物流移除,所述吸收器器皿在高于大气压并在60巴或低于60巴的压力下操作,由此形成含有酸气体的nass。所述方
法还包括:将所述含有酸气体的nass引入至泄压器皿,其中所述泄压器皿在一定温度和压力下操作,并且其中所述泄压器皿操作压力小于所述吸收器器皿操作压力,由此一旦引入至泄压器皿,则由nass的物理吸收组分所吸收的酸性气体就从含有酸性气体的nass释放,以及由此所述泄压器皿操作温度使得由含有酸性气体的nass的化学吸收组分所吸收的酸性气体从含有酸性气体的nass释放,由此提供经再生的nass,所述经再生的nass基本上不含酸性气体,并且可在气体洗涤工艺中再利用。藉由所描述的方法,在酸性气体洗涤工艺中,用以提供经再生的nass的能量相对于用以提供经再生形式的水性溶剂的能量而言降低。
17.将理解,上述本发明的一般描述以及以下详细描述两者均为示例性的,而非对本发明限制性的。
附图说明
18.通过参考以下详细描述,当与附图联系起来考虑时,将更完整地理解本发明以及其众多随之产生的优点,因其变得更好理解,其中:
19.图1为示例性溶剂体系的组分的示意图。
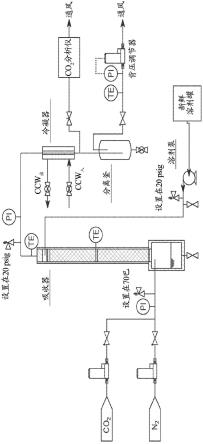
20.图2为用于从气体物流移除co2的示例性系统的示意性流程图。
21.图3为用以确定对于溶剂体系的化学吸收组分而言的再沸器热负荷的示例性计算的图示。
22.图4为用于测试的吸收器塔(absorber column)的示意性流程图。
23.图5a-5c为显示在实施例1中使用示例性溶剂体系(图5a)、amdea替代物(图5b)和水(图5c)的co2浓度随时间变化的线图。
24.图6为显示实施例2的实验设置的示意图,其包括反应器和间歇式器皿。
25.图7为显示所述溶剂体系的示例性实施方式、环丁砜和depg的气液平衡曲线的线图。
26.图8为显示对于所述溶剂体系的示例性实施方式和amdea而言,在不同压力下的预计再生能的线图。
27.图9为显示对于不同合成气进料压力而言计算得的能量节省的柱形图。
具体实施方式
28.本文中所描述的是配置成将酸性气体从气体物流移除的非水溶剂体系。术语“酸气体(acid gas)”或“酸性气体(acidic gas)”旨在指当与水混合时可导致形成酸的任何气体组分。本发明所涵盖的酸气体的非限制性实例包括:co2、so2、cos、cs2和no
x
。出于简易起见,以下以具体关于co2的方式描述本发明。然而理解,本发明涵盖用于将任何酸气体组分从气体物流移除的方法和体系(系统)。
29.在某些实施方式中,所述溶剂体系是可再生的,因为酸性气体可从所述溶剂释放,并且所述溶剂可再利用以将另外的酸性气体从另外的气体混合物分离。
30.所述溶剂体系包括由化学吸收组分和物理吸收组分形成的溶液。所述化学吸收组分包含含氮碱,并且所述含氮碱具有使得其与所述酸性气体的一部分反应的结构。所述物理吸收组分包含有机稀释剂,所述有机稀释剂不与所述酸性气体反应,并且具有使得其在
高于大气压的压力下吸收所述酸性气体的一部分的结构。
31.所述有机稀释剂可为,但是不必然为,相对酸性的组分。本文中所使用的术语“相对酸性的组分”可与术语“酸性组分”互换,并且理解为意指具有大于水的酸性、优选地显著地大于水的酸性的酸性的材料。例如,在一些实施方式中,所述稀释剂可具有小于约15、小于约14、小于约13、小于约12、小于约11、或小于约10的pka。在其它实施方式中,所述有机稀释剂不是相对酸性的组分,并且不具有落入上文所述范围内的pka。例如,在某些实施方式中,所述有机稀释剂可具有大于约15的pka。
32.在某些实施方式中,所述溶剂体系中使用的有机稀释剂可一般选自:醇、酮、脂族烃、芳族烃、氮杂环、氧杂环、脂族醚、环状醚、酯和酰胺,及其混合物。在更具体实施方式中,所述稀释剂可选自聚乙二醇二烷基醚。例如,所述稀释剂可选自聚二醇二甲基醚和聚二醇二丁基醚,例如:一缩二乙二醇二丁基醚、二缩三乙二醇二丁基醚、三缩四乙二醇二丁基醚,或其组合。在实施方式中,所述稀释剂一般具有低蒸气压和低粘度。使用所述稀释剂或物理吸收组分将酸气体移除是通过所述酸气体和所述稀释剂之间的直接接触实现的。
33.所述含氮碱特征可为具有可从氮贡献的质子的任何含氮碱,所述含氮碱经由氨基甲酸酯路径与酸气体反应,并且避免与酸气体反应形成碳酸酯。在某些实施方式中,所述含氮碱组分可为满足此要求的几乎任何含氮碱,包括但是不限于:伯胺、仲胺、二胺、三胺、四胺、五胺、环状胺、环状二胺、胺低聚物、多元胺、醇胺、胍、脒,等等。在一些实施方式中,所述含氮碱可具有约8至约15、约8至约14、约8至约13、约8至约12、约8至约11、或约8至约10的pka。在某些实施方式中,所述含氮碱组分具有小于约11的pka。
34.伯胺理解为是具有式nh2r的化合物,其中r可为含碳基团,包括但是不限于c
1-c
20
烷基。仲胺理解为是具有式nhr1r2的化合物,其中r1和r2独立地为含碳基团,包括但是不限于c
1-c
20
烷基,其中r、r1和r2独立地为含碳基团,包括但是不限于c
1-c
20
烷基。r、r1和r2上的氢中的一个或多个可任选地被一个或多个取代基替代。例如,r、r1和r2上的氢中的一个或多个可被以下替代:任选地取代的c
1-c6烷基,任选地取代的c
1-c6烷氧基,任选地取代的c
2-c
10
烯基;任选地取代的c
2-c
10
炔基;任选地取代的烷芳基;任选地取代的芳基烷基;任选地取代的芳氧基;任选地取代的杂芳基;任选地取代的杂环;卤素(例如cl、f,br和i);羟基;卤代烷基(例如cf3、2-br-乙基、ch2f、ch2cf3和cf2cf3);任选地取代的氨基;任选地取代的烷基氨基;任选地取代的芳基氨基;任选地取代的酰基;cn;no2;n3;ch2oh;conh2;c
1-c3烷硫基;硫酸酯(硫酸根);磺酸;磺酸酯(例如甲磺酸基);膦酸;磷酸酯(磷酸根);膦酸酯(膦酸根);单-、二-或三磷酸酯;三苯甲基或单甲氧基三苯甲基;cf3s;cf3so2;或者硅烷基(例如,三甲基硅烷基,二甲基-叔丁基硅烷基,以及二苯基甲基硅烷基)。环状胺是其中单原子形成环结构的一部分的胺,并且可包括但是不限于:氮丙啶、氮杂环丁烷、吡咯烷、哌啶、哌嗪、吡啶、嘧啶、脒、吡唑和咪唑。环状胺可包含一个或多个环,并且可任选地被一个或多个上文所列举的取代基取代。在一些实施方式中,所述含氮碱具有胍结构,其任选地被一个或多个上文所提及的取代基取代。在一些实施方式中,所述含氮碱具有脒结构,其任选地被上文所提及的一个或多个取代基取代。在一些实施方式中,所述含氮碱可为二胺。在一些实施方式中,所述含氮碱可为伯或仲醇胺。醇胺亦称为氨基醇,并且既含有醇基团又含有胺基团。醇胺的胺基团可为本文中所公开的任何类型的胺。在一些实施方式中,所述醇胺为伯、仲或叔醇胺。
35.在某些实施方式中,所述伯或仲胺可选自被含氟烷基芳族基团官能化的胺。在具
体实施方式中,所述胺可选自2-氟苯乙基胺、3-氟苯乙基胺、4-氟苯乙基胺、2-氟-n-甲基苄基胺、3-氟-n-甲基苄基胺、和4-氟-n-甲基苄基胺、3,5-二-氟苄基胺、d-4-氟-α-甲基苄基胺、以及l-4-氟-α-甲基苄基胺。
36.在某些实施方式中,所述含氮碱可选自:1,4-二氮杂双环-十一碳-7-烯("dbu");1,4-二氮杂双环-2,2,2-辛烷;哌嗪("pz");三乙基胺("tea");1,1,3,3-四甲基胍("tmg");1,8-二氮杂双环十一碳-7-烯;单乙醇胺("mea");二乙基胺("dea");乙二胺("eda");1,3-二氨基丙烷;1,4-二氨基丁烷;六亚甲基二胺;1,7-二氨基庚烷;二乙醇胺;二异丙基胺("dipa");4-氨基吡啶;戊基胺;己基胺;庚基胺;辛基胺;壬基胺;癸基胺;叔辛基胺;二辛基胺;二己基胺;2-乙基-1-己基胺;2-氟苯乙基胺;3-氟苯乙基胺;3,5-二氟苄基胺;n-甲基苄基胺;3-氟-n-甲基苄基胺;4-氟-n-甲基苄基胺;咪唑;苯并咪唑;n-甲基咪唑;1-三氟乙酰基咪唑;1,2,3-三唑;1,2,4-三唑;及其混合物。在某些实施方式中,所述含氮碱可为胍或脒。在实施方式中,所述含氮碱可为n-甲基苄基胺。
37.图1中说明了某些具体溶剂体系。如图1中所示,在溶剂体系中,含氮碱可为n-甲基苄基胺,并且有机稀释剂可为一缩二乙二醇二丁基醚、二缩三乙二醇二丁基醚或三缩四乙二醇二丁基醚之一或其组合。
38.在一些实施方式中,所述溶剂体系可包括包含含氮碱和稀释剂的混合物,其组分可以按摩尔计大致等比例存在(即以等摩尔量存在)。在某些实施方式中,所述稀释剂以过量方式存在。例如,稀释剂对含氮碱的摩尔比可为约1:1至约100:1,例如约1.1:1至约20:1、1.1:1至约15:1、1.1:1至约10:1、1.1:1至约5:1、1.1:1至约3:1、约2:1至约20:1、约2:1至约15:1、2:1至约10:1、2:1至约5:1、约3:1至约20:1、约3:1至约15:1、约3:1至约10:1、约4:1至约20:1、约4:1至约15:1、约4:1至约10:1、约5:1至约20:1、约5:1至约15:1、或约5:1至约10:1。
39.在实施方式中,所述溶剂体系可包括包含化学吸收组分和物理吸收组分的混合物,其组分可以重量百分数计大致等比例存在。在某些实施方式中,所述物理吸收组分以过量方式存在。例如,所述化学吸收组分可以范围为约1至约50重量%的浓度存在,相对于总体系重量计,例如总体系的约5至约30重量%,约10至约20重量%,或总体系的约10至约15重量%。在实施方式中,所述物理吸收组分可以范围为约40至约95重量%的浓度存在,相对于总体系计,例如,总体系的约50至约90重量%,总体系的约70至约90重量%。在实施方式中,所述溶剂体系可进一步包括水。水可以范围为总体系的约1至约10重量%的浓度存在。在示例性实施方式中,所述组分可以以下浓度存在:约1至20重量%化学吸收组分,约70至98重量%物理吸收组分,以及约1至10重量%水。
40.在实施方式中,溶剂体系可由疏水胺物种(其以化学方式与co2反应)以及疏水有机溶剂(其以物理方式吸收co2)的组合配制。所述溶剂体系可以相似或更佳容量工作,并且可与可商购获得的酸气体洗涤溶剂竞争。在实施方式中,所述溶剂体系可用于将co2从合成气体物流移除。所述溶剂体系可为替代可商购获得的基于水性胺的酸移除溶剂(例如活化的甲基二乙醇胺(amdea))的良好候选物。
41.如想在以下实施例部分中描述的,所述溶剂体系的示例性实施方式能够进行与可商购获得的amdea相似的深度co2移除,而同时降低溶剂再生所需要的能量的量。在示例性实施方式中,可使用n-甲基苄基胺(nmba)作为含氮碱来以化学方式结合co2,并且可使用包
含聚乙二醇二丁基醚的有机稀释剂以在升高压力下以物理方式吸收co2。为了释放经物理吸附的co2部分,简单的闪蒸罐是足够的,其要求很少的能量。
42.虽然不希望受理论制约,据信使用另外的组分可用以降低或防止所述溶剂体系中的固体沉淀。在一些实施方式中,所述溶剂体系可进一步包含一种或多种另外的组分。可添加所述另外的组分,例如以增加溶剂体系中捕集的co2产物的溶解性,并从而避免形成沉淀。然而,在其它实施方式中,可期望形成固体,并且这样的形成可通过改变一个或多个溶剂体系组分的浓度而增强。
43.在一些实施方式中,所述溶剂体系可用于从气体物流捕集co2。在另外的实施方式中,所述溶剂体系可用于在高于大气压的压力下从气体物流捕集co2。例如,所述吸收器器皿的操作压力可为约2巴至约60巴。
44.气体物流可为混合气体物流,其除了co2以外还具有一种或多种其它组分。当溶剂体系与含有co2的气体混合物接触时,所述溶剂体系的化学吸收组分经历与co2的化学反应,将co2结合于溶液中。所述溶剂体系的物理吸收组分利用压力以将co2溶解。溶解在物理吸收溶剂中的酸气体的量随着压力增加而成比例地增加。
45.在一些实施方式中,所述溶剂体系具有高co2移除。例如,所述溶剂体系可用于捕集或移除存在于工艺气体物流中的co2的大于约80重量%。例如,所述溶剂体系可捕集或移除存在于工艺气体物流中的co2的大于约85重量%、86重量%、87重量%、88重量%、89重量%、90重量%、91重量%、92重量%、93重量%、94重量%、95重量%、96重量%、97重量%、98重量%、99重量%、或最高达100重量%。如本文中所使用的,术语“深度移除”意指存在于工艺气体物流中的co2的大于约90重量%、91重量%、92重量%、93重量%、94重量%、95重量%、96重量%、97重量%、98重量%、99重量%、或最高达100重量%的co2的捕集或移除。术语深度移除还对不同于co2的酸气体适用。在实施方式中,所述溶剂体系可同于捕集或移除近于全部或基本上全部存在于工艺气体物流中的co2。例如,在接触溶剂体系后,已从其捕集或移除co2的气体物流(“贫气体物流”)可具有以小于或等于约1500ppm的量存在的co2。例如,co2可以约500ppm至约1500ppm的量存在于所述贫气体物流中。在实施方式中,co2可以小于或等于约500ppm、600ppm、700ppm、800ppm、900ppm、1000ppm、1100ppm、1200ppm、1300ppm、1400ppm、或1500ppm的量存在于所述贫气体物流中。
46.在一些实施方式中,所述溶剂体系可用于部分co2移除。例如,所述溶剂体系可用于捕集或移除存在于工艺气体物流中的co2的约30重量%至约70重量%。例如,所述溶剂体系可捕集或移除存在于工艺气体物流中的co2的约30重量%、35重量%、40重量%、45重量%、50重量%、55重量%、60重量%、65重量%、或70重量%。
47.在某些实施方式中,选择稀释剂(即物理吸收组分)使得其具有低的与水混溶性。例如,在一些实施方式中,所述稀释剂具有在25℃下在水中小于或等于约10g/100ml的溶解性(即,10g溶剂/100ml水)。在其它实施方式中,所述稀释剂具有在25℃下在水中小于或等于约0.01g/100ml、小于或等于约0.1g/100ml、小于或等于约0.5g/100ml、小于或等于约1g/100ml、小于或等于约1.5g/100ml、小于或等于约2g/100ml、小于或等于约2.5g/100ml、小于或等于约3g/100ml、小于或等于约4g/100ml、小于或等于约5g/100ml、小于或等于约6g/100ml、小于或等于约7g/100ml、小于或等于约8g/100ml、或小于或等于约9g/100ml的在水中的溶解性。在一些实施方式中,所述稀释剂与水完全不混溶。使用具有低水溶解性的稀释
剂可导致溶剂体系展现以下特性的一个或多个:其可要求更少能量用于再生;可具有更高co2移除容量;可能够耐受气体物流中的水;和/或可能够在不具有大能量不利(penalty)的情况下从水分离。
48.在另外的实施方式中,类似地选择溶剂体系的含氮碱化的(nitrogenous based)组分(即化学吸收组分)使得其具有低的与水混溶性。在优选实施方式中,所述含氮碱和与水混溶性相比具有更高的与稀释剂混溶性。在一些实施方式中,所述含氮碱具有更高的在稀释剂中的溶解性。这样的含氮碱的实例包括但是不限于:具有包含三个或更多个碳的一个或多个烃链的脂族胺,以及具有包含三个或更多个碳的一个或多个烃链的其中一个或多个氟原子取代所述烃链中的氢的脂族胺。注意,虽然优选的是具有低的与水混溶性的稀释剂和/或含氮碱,但是本发明还涵盖如下溶剂体系:其中所述稀释剂、含氮碱和/或其组合是与水至少部分混溶的。
49.在实施方式中,所述溶剂体系具有在10至60℃的温度下范围为1mpas至20mpas的动态粘度。例如,所述动态粘度可为约1mpas至约10mpa、约1mpas至约8mpa、或约1mpas至约4mpas。在实施方式中,所述溶剂体系具有在20℃下范围为约0.02mbar至约0.03mbar的蒸气压。
50.在一些实施方式中,所述溶剂体系是对水的存在耐受的。在某些实施方式中,所述溶剂体系以按体积计最高达或等于约30%水的方式耐受水。例如,在一些实施方式中,所述溶剂体系耐受按体积计最高达或等于约25%水,按体积计最高达或等于约20%、最高达或等于约15%、最高达或等于约10%、最高达或等于约5%、最高达或等于约2%、或最高达或等于约1%水。在一些实施方式中,对水的存在的耐受意味着直至所述体积的水时都存在很少或者不存在溶剂体系性能的劣化。在一些实施方式中,所述溶剂体系直至所述体积的水时都维持在或近于co2移除的起始容量。
51.在实施方式中,可将使用本发明的溶剂体系所捕集的co2释放以使溶剂体系再生以再利用。期望所述溶剂体系是在温和条件下(例如,在相对低的温度和压力下)可再生的。在一些实施方式中,释放co2以及相应的所述溶剂体系的再生是通过降低溶液的压力以及加热所述溶液来实现的。当降低压力时,经物理吸收的co2从所述溶剂体系的物理吸收组分释放。当加热含有以化学方式结合的co2的溶液时,与所述化学吸收组分的化学反应被逆转,并且释放以化学方式结合的co2。经释放的co2提供浓缩的co2物流。
52.在一些实施方式中,本技术涉及用于将co2从气体物流移除的溶剂体系和工艺。所述工艺对含有co2的任何气体物流均适用。例如,在特定实施方式中,所述工艺涉及将co2从化石燃料燃烧烟道气、天然气混合物、或者含有co2的来自封闭环境的呼吸气体的混合物移除。所述工艺涉及使混合气体物流通过包含稀释剂和含氮碱组分的溶剂体系。在一些实施方式中,所述工艺进一步涉及所述溶剂体系的再生,其释放co2。在一些实施方式中,溶剂体系的再生涉及在足以释放co2的温度下加热所述溶剂体系。在一些实施方式中,所述工艺涉及在如下温度下加热所述溶剂体系:在约200℃或低于约200℃,例如在约185℃或低于约185℃,在约150℃或低于约150℃,或者在约125℃或低于约125℃。在优选实施方式中,所述工艺涉及在约100℃或低于约100℃的温度下加热所述溶剂体系,例如在如下温度下:在约95℃或低于约95℃,在约90℃或低于约90℃,在约85℃或低于约85℃,在约80℃或低于约80℃,在约75℃或低于约75℃,或者在约70℃或低于约70℃。在一些实施方式中,co2可在环境
温度下释放。
53.在一些实施方式中,溶剂体系的再生涉及降低所述溶剂体系的压力以释放在相对较高的压力下吸收的co2。在一些实施方式中,所述工艺涉及降低所述溶剂体系的压力,在约60巴或低于约60巴,例如在约40巴或低于约40巴,在约20巴或低于约20巴,或者在约5巴或低于约5巴。在某些实施方式中,降低压力至大气压。在某些实施方式中,在水作为单独的、较低密度相积聚的条件下,将co2捕集于非水性相中。可将此相与富、非水性相送至再生器(regenerator),以在与单独的对应的富水性相相比更低的温度下再生。这可随后继以从贫、再生的溶剂相分离,之后送回到吸收器。
54.在一些实施方式中,本技术涉及将酸性气体从气体物流深度移除的方法。所述方法包括将包含物理吸收组分和化学吸收组分的非水性溶剂体系引入至吸收器器皿,所述吸收器器皿在高于大气压的压力下操作。所述方法进一步包括向所述吸收器器皿引入包含酸性气体的气体物流,使得所述气体物流与所述非水性溶剂体系流体接触并通过所述非水性溶剂体系,由此,通过所述溶剂体系将所述酸性气体的至少90重量%从所述气体物流移除。在实施方式中,所述吸收器器皿是在约2至60巴的压力下操作的。例如,该压力可为约10至30巴。在实施方式中,酸性气体的至少95重量%从所述气体物流移除。例如,所述酸性气体的至少97重量%、至少98重量%、或至少99重量%从气体物流移除。在一些实施方式中,当将气体物流引入至吸收器器皿时,所述气体物流具有起始酸性气体浓度,并且在通过所述吸收器器皿之后具有经降低的酸性气体浓度,并且所述经降低的酸性气体浓度为约750ppm至1500ppm。所述经降低的酸性气体浓度可小于或等于1500ppm。
55.在某些实施方式中,当使所述溶剂体系再生时,在或约100%的co2从富co2的溶剂体系移除。然而,在其它实施方式中,小于100%的co2从富co2的溶剂体系移除。在实施方式中,所捕集的co2的约50至100%从富co2的溶剂体系移除,例如约75%至100%、约80%至100%、约90%至100%、约95%至约100%、或约98%至100%。例如,在一些实施方式中,所捕集的co2的至少约98%、95%、90%、85%、80%、75%、70%、60%、或50%从富co2的溶剂体系移除。
56.在一些实施方式中,提供了用于将co2从气体物流移除的系统。图2中描绘了本发明的示例性系统的示意图。co2移除系统10包括吸收器12,吸收器12配置有入口,以接收气体物流。所述气体物流可例如直接来自发电长的沸腾器系统(锅炉系统,boiler system)的燃烧室。所述气体物流可或可不在进入所述co2移除系统之前通过其它清洁系统。所述吸收器可为其中含有用于移除co2的溶剂体系的任何腔室,其具有气体物流的入口和出口,并且其中可使所述气体物流与所述溶剂体系接触。在吸收器内,co2可根据本文中讨论的原理从气相传递至液相。所述吸收器可为任意类型;例如,所述吸收器可包含喷淋塔吸收器、填料床吸收器(包括逆流流动塔或错流塔),塔盘塔吸收器(其具有各种塔盘类型,包括泡罩塔盘、筛孔塔盘、撞击式塔盘、和/或浮阀塔盘),风险(通风式,venture)吸收器,或者喷射器吸收器。
57.可控制所述吸收器内的温度和压力。例如,在一个实施方式中,所述吸收器的温度可维持在或近于-10℃至约60℃。例如,所述吸收器的温度可为约0℃至约60℃、约30℃至约60℃、或约50℃至约60℃。在实施方式中,所述吸收器的压力维持在高于大气压的压力下。例如,所述吸收器的压力可维持在如下的压力下:约5巴至约60巴,约10巴至约60巴,约30巴
至约60巴,约10巴至约30巴,约5巴至约20巴,或者约10巴至约20巴。在实施方式中,所述吸收器可维持在或近于大气压。因而,所述吸收器可装配有加热/冷却系统和/或压力/真空系统。
58.在所述吸收器内,使所述气体物流与包含稀释剂和含氮碱组分的溶剂体系流体接触并且通过所述溶剂体系。所述溶剂体系通过化学和物理吸收与存在于所述气体物流中的co2反应,将其从气体的剩余组分捕集。所得的不含co2的气体物流通过出口从吸收器释放。随着使混合气体物流通过,所述溶剂体系继续与进入吸收器的co2反应,直至其变得“富”有co2。任选地,所述吸收器连接至一个或多个操作单元。例如,所述吸收器可配置有用于将所述溶剂体系引导至如下单元的手段:在该单元中可将水倾析、离心或以其它方式从系统移除。在实施方式中,所述溶剂体系可吸收来自气体物流的多于一种类型的酸气体。例如,所述溶剂体系可吸收co2和硫物种酸气体。在此示例性实施方式中,所述吸收器可连接至一个或多个如下操作单元:所述操作单元可将co2和硫物种酸气体分离成两股物流,以实现高纯度(≥90重量%)co2物流和具有大于50%纯度的硫物种的物流。
59.在co2捕集工艺中的任何阶段,可使所述溶剂体系再生。因此,系统包括任选的再生系统14,以经由单独的co2气体物流将捕集的co2释放,并从而使所述溶剂体系再生。将所述再生系统配置成接收来自吸收器的“富”溶剂的进料,并且一旦已将co2从所述“富”溶剂分离就使经再生的溶剂返回到吸收器。所述再生系统可简单地包含如下腔室:其在比吸收器更低的压力下操作,并且具有加热单元,以将所述溶剂体系加热至足以释放co2气体的温度,以及释放阀,以允许将co2从所述再生系统移除。其还可为如下的蒸馏塔:其在比吸收器更低的压力下操作,并且具有基本上与如上文对于吸收塔所描述的相同的设计。所述再生器可任选地连接至一个或多个单元。例如,所述再生器可配置有用于将溶剂引导至如下单元的手段:在该单元中可将水倾析、离心或以其它方式从所述系统移除。
60.经释放的co2可输出至存储,或用于其它预定用途。经再生的溶剂再一次准备好吸收来自气体物流的co2,并且可引导回到吸收器中。
61.在一些实施方式中,本技术涉及用于降低酸性气体洗涤工艺中非水性溶剂体系(nass)的溶剂再生所要求的能量的量的方法。再生能量节省是相对于常规的水性的基于胺的溶剂的溶剂再生所要求的能量的量而言的。本文中所描述的溶剂体系可用以在吸收器器皿中将酸性气体从气体物流移除,所述吸收器器皿在高于大气压并且在60巴或低于60巴的压力下运行,由此形成含有酸性气体的nass。可将含有酸气体的nass引入至泄压器皿,所述泄压器皿在小于所述吸收器器皿操作压力的压力下操作。降低压力导致通过nass的物理吸收组分所吸收的酸性气体从所述含有酸性气体的nass释放。将所述泄压器皿加热至使得通过所述含有酸性气体的nass的化学吸收组分所吸收的酸性气体释放的温度,由此提供经再生的nass,经再生的nass可在气体洗涤工艺中再利用。在酸性气体洗涤工艺中,相对于提供经再生形式水性溶剂所使用的能量而言,提供经再生的nass所使用的能量降低。在实施方式中,通过nass的物理吸收组分所吸收的酸气体的百分数大于通过所述nass的化学吸收组分所吸收的酸气体的百分数。例如,通过物理吸收组分所吸收的酸气体相对于通过化学吸收组分所吸收的酸气体的比率在1.5:1至30:1的范围中。例如,此比率可为2:1、3:1、4:1、5:1、6:1、7:1、8:1、9:1、或10:1。
62.可进行计算,以估计与可商购获得的水性的基于胺的体系相比,通过使用本文中
所描述的溶剂体系,在溶剂再生期间可实现的能量节省的量。图3提供了用于确定溶剂体系的化学吸收组分的再沸器热负荷的示例性计算的说明。所述计算包括将溶剂加热至再生温度所要求的显热,将所吸收的酸气体从物理吸收组分移除所要求的气化热,以及将所吸收的酸气体从化学吸收组分移除所要求的吸收热。如将在以下实施例部分中解释的,化学吸收组分的吸收热显著影响再沸器热负荷。
63.文本中所描述的溶剂体系提供了相对于现有酸气体洗涤溶剂的优点。在实施方式中,相对于可商购获得的水性吸收溶剂而言,释放所捕集的co2所需要的再生能降低。此外,在实施方式中,与可商购获得的较高粘度溶剂(例如amdea)相比,所述溶剂体系的相对低的粘度使得能够实现泵送成本的节省。进一步地,在实施方式中,所述溶剂体系在相对低温度下具有高工作容量,从而使得能够实现工艺足迹降低、操作成本降低以及溶剂排放最小化。
64.受益于以上描述和附图中所呈现的教导,本发明所属领域中的技术人员将想到本文中所阐述的本发明的多种修改和其它实施方式。因此,将理解,本发明将不限于所公开的具体实施方式,以及修改和其它实施方式旨在被包括在所附权利要求的范围内。虽然本文中采用了特定术语,但是它们仅仅以一般和描述性含义使用的,并且并非出于限制目的。
65.实施例
66.实施例1——评估co2移除效率
67.使用单程、气-液接触高压吸收器塔,将所述溶剂体系的示例性实施方式的co2移除效率与具有与可商购获得的(碱性胺水溶液,由basf(路德维希港,德国)生产并市售)相似组成的溶剂的co2移除效率进行比较。图4提供了用于测试的吸收器塔的示意图。n2和co2质量流量控制器用以控制进入吸收器塔底部的气体组成。所述吸收器塔如下构建:使用1英寸od ss管,附接有4l ss集液池(sump),所述集液池位于塔的底部并且用陶瓷纤维绝缘物绝缘。吸收塔填充有大约300克的0.16英寸突出无规金属填料,其中填料高度为3.5m。对溶剂进行计量,并通过膜式泵在吸收器顶部递送。溶剂和含有co2的气体在吸收器塔中彼此接触,并且富co2液体收集于吸收器集液池中,而不含co2的气体从塔的顶部离开。吸收器的尾气使用冷凝器冷却,以将带出的溶剂移除,其中所述溶剂通过分离釜(knock-out pot)收集。在分离釜之前,提取干燥、不含溶剂的气体物流的滑流(slipstream),并将其进料至co2分析仪,以降低由器皿产生的相应迟滞时间。剩余气体通过位于分离釜出口处的背压调节器离开系统,以维持塔中压力恒定。在气体进料位置处始终(throughout,整个)安装泄压阀,以防止系统过度加压。分别经由温度探头(te)和压力指示器(pi)来监测不同位置处的温度和压力。
68.测试中所使用的示例性溶剂体系为n-甲基苄基胺(nmba)与聚二醇二丁基醚和水的共混物,其具有以下浓度:约10.5重量%nmba、约5.2重量%水和余量的聚二醇二丁基醚。由于的组分是专有而非公共可得的,因此制造62.6重量%mdea、5.37%哌嗪和余量的水的共混物,并充当的替代配混物。
69.co2移除效率实验是通过使用20体积%co2在n2中的混合物将系统加压至20巴(a)(300psia)来进行的。一旦达到目标压力并且co2分析仪读取到位于吸收器出口的co2浓度处在约20%的恒定数值,就将气体流速调整至200sccm。向塔以受控速率进料新鲜溶剂,以捕集来自混合气体的co2。co2吸收是在室温下进行的。
70.受评估的不同溶剂以及其co2移除性能的汇总列举于表1中。水(运行a1)用来确定
在高压条件下co2在水中物理吸收的性能。结果表明,使用水的情况下仅30%的co2被吸收,这与所要求的大于99%的co2的深度移除相比是极小的。使用2.4和3.3克/分钟的液体流速(分别为运行a2和a3)测试amdea替代物,得到大于99%的深度co2捕集。将amdea替代物液体流速减少至2.4克/分钟产生具有1100ppm的更高co2浓度(与3.3克/分钟的更高流速下的800ppm相比)的经处理的气体物流。示例性溶剂体系(运行a4)显示出与在相似液体流速下对于amdea替代物所报道的相当的移除效率。注意到,由于溶剂泵的控制问题,示例性溶剂体系实验在实现稳定co2测线之前终止。图5a-5c为显示使用示例性溶剂体系(图5a)、amdea替代物(图5b)以及水(图5c)的co2浓度随时间变化的线图。基于结果,预期使用示例性溶剂体系可在稳态下实现750-800ppm的低co2水平。
71.表1.在高压吸收器中测试的溶剂及其co2移除性能的汇总
[0072][0073]
实施例2——co2气液平衡研究
[0074]
在电脑控制、搅拌着的反应器器皿(由chemisens供应,用自动化的气体操作系统进行改变)中测量溶剂体系的示例性实施方式的co2气液平衡。图6是显示实验设置的示意图,所述实验设置包括反应器和间歇式器皿。所述反应器为260ml圆柱状不锈钢器皿,其具有推进器搅拌器和四个桨叶,以将液相和气相两者混合。可将搅拌速度改变成期望数值,精度为
±
1rpm。通过丙二醇浴将反应器的温度维持在所需的等温条件下。反应器的压力通过压力传感器(pi-301)监测,精度
±
0.03%fso。反应器连接至电磁调节阀(hv-305),以在等温条件下从178ml间歇式器皿向反应器中供应所需气体。在阀(hv-305)和所述间歇式器皿之间,安装了质量流量控制器、电磁调节阀(hv-250)以及压力传感器(pi-302),以控制流速并监测反应器入口段中的压力。间歇式器皿中的压力通过压力传感器(pi-221)测量。使用流量控制阀(fcv-230),以通过打开电磁调节阀(hv-211)控制从间歇式器皿去往歧管和反应器的流。去往间歇式器皿的气体通过阀(hv-210)由所需气体的柱桶(cylinder,缸)供应。此外,电磁调节阀的组(hv-225、hv-331、hv-334、hv-332和hv-333)用以使用氮气(n2)吹扫
系统,以及抽真空以在实验之前对溶剂进行脱气并对系统进行通风。反应器设置放置在培育器内,所述培育器维持在30℃的恒定温度下,以避免温度涨落。
[0075]
为了测量co2等温线,向ss反应器中加载100ml的溶剂,并使该溶剂经受脱气。所述脱气通过如下进行:重复7至8次使用n2吹扫单元(cell)、继以真空条件的循环。在脱气之后,向反应器中注射co2,并允许达到气液平衡,所述气液平衡通过反应器单元中的恒定压力读数指示。伴随着后续注射使实验继续,直至反应器的总体压力达到大致300psia。
[0076]
图7中测量并绘制了溶剂体系的示例性实施方式的co2气液平衡(vle)。图7还包括了环丁砜(其为环状砜,具有式(ch2)4so2)以及depg(其为聚乙烯的二甲基醚的混合物),它们并非测得的而是在文献来源中找到的。amdea为化学吸收溶剂,而环丁砜和depg为物理吸收溶剂。溶剂体系的示例性实施方式为杂合溶剂,其可通过化学吸收模式和物理吸收模式两者吸收co2。
[0077]
虽然化学吸收溶剂可在低co2浓度下实现co2的深度洗涤,但是其吸收容量限制于在溶剂中可用的与co2以化学方式反应的胺。化学吸收是独立于系统压力的。在测试中,amdea展现了在600kpa下约0.2摩尔co2/摩尔溶剂的饱和容量。由于co2在水中的物理溶解性的限制,增加压力未使co2加载量改进超过饱和点。
[0078]
一般而言,物理溶剂在将co2从稀释的气体物流移除方面性能差。然而,吸收容量随着系统压力增加而线性增加。即便当co2的浓度相对低时,溶剂体系的示例性实施方式也能够进行深度co2捕集。其还能够在压力增加时增加co2移除容量。
[0079]
能够在宽压力范围中进行co2吸收是本文中所描述的溶剂体系相对于amdea和其他水性的基于胺的溶剂的优点。此优点对于将co2从高压气体(例如,充满co2的合成气物流)移除而言是特别相关的。因为所述溶剂体系在增加的压力下具有更高的co2移除容量(即,能够由气体物流吸收更多co2),移除相同量的co2需要更少溶剂。因此,可降低洗涤工艺的足迹,因为可使用较小溶液存量。进一步,由于本文中所描述的溶剂体系的再生能力,填料塔再生器可被装配有加热线圈的更小的闪蒸器皿替代,以使所述溶剂体系再生。此替代导致设备成本更低以及操作简化。
[0080]
通过本文中所描述的溶剂体系,化学吸收组分维持了通过化学吸收剂实现的深度洗涤能力,但再生能显著小于仅通过化学吸收工作的水性的基于胺的溶剂(例如amdea)的再生能。通过所描述的溶剂体系,大部分co2被所述溶剂体系的物理吸收组分(与化学吸收组分相反)捕集,并从而通过闪蒸而非加热移除。计算表明,对于使用闪蒸罐而非amdea再生工艺使溶剂再生而言,每kg从富溶剂移除的co2能量节省30%。
[0081]
进行计算,以评估目标co2产物压力对用于溶剂再生的能量的影响。图8是显示对于溶剂体系的示例性实施方式和amdea而言,在不同压力下产生co2的预计的再生能。对于计算,使用将100摩尔co2从溶剂移除的基础。对于溶剂体系而言,假设:co2的一部分将通过闪蒸(对于物理吸收组分)移除,以及剩余部分将通过供热移除用于再生(对于化学吸收组分)。经由闪蒸移除的co2的量是通过确定在10巴(a)的起始压力下的co2加载量(x
co2
)和在给定闪蒸压力下的co2加载量的差异确定的。假设,通过闪蒸将co2移除不需要能量。将剩余co2移除所要求的能量是通过将co2的吸收热(对于溶剂体系,dh
abs,nas
=80kj/摩尔co2,以及对于amdea,dh
abs,amdea
=60kj/摩尔co2)乘以co2的剩余量确定的。使用量热计,对配制物中的胺测量组分的吸收热。基于计算,若将在大气压下产生纯co2,则通过使用溶剂体系可实现最
高达40%的再生能的降低。随着目标co2产物压力增加并达到与amdea在5巴(a)处的平衡点(break-even),溶剂体系的能量节省益处开始消减。此结果是由于在较高再生压力下经物理结合的co2被移除的部分较小,以及使经化学结合的co2再生要求的能量更多。将注意,这些预计仅考虑了吸收热,而将溶剂加热至再生温度所要求的显热未被包括,因为估计显热的贡献对总体能量要求相对小(《20%),并且对于不同溶剂而言是相似的。
[0082]
还检验了合成气进料压力对用于再生的能量使用的影响。图9是显示对于不同合成气进料压力而言计算的能量节省的柱形图。对于所述计算,进料气体压力以10巴增量由30至100巴,a变化。对于再生的co2而言,目标压力固定在1巴,a。计算显示,随着进料气体压力增加,本文中所描述的溶剂体系比amdea要求更少再生能。对于所述计算,使用上文所描述的相同方法确定溶剂再生所要求的能量。如上文所描述的,所述计算确定使经化学吸收的co2再生所要求的能量的量。所述计算假设,对于所有合成气压力而言,co2的浓度均在20体积%。对于所述溶剂体系,随着合成气压力增高,co2的更大部分通过物理吸收而被吸收,从而导致可将经吸收的co2的更大部分通过闪蒸而移除。与之相比,amdea具有0.2mol-co2/摩尔-溶剂的co2饱和限制,而不管压力如何。因此,大部分经吸收的co2必须以热方式移除(即,起始和最终压力的x
co2
之间差异小)。
[0083]
对于本文中所描述的溶剂体系,所述化学吸收组分允许所述溶剂体系实现与amdea相似的深度co2洗涤。此外,所述物理吸收组分在升高压力下提供了另外的co2移除容量,在升高的压力下化学吸收溶剂,包括amdea,在其移除容量方面限制于co
2-胺化学计量。为了使溶剂体系再生,可通过简单地将溶剂闪蒸将大部分co2移除,而仅小部分的经化学结合的co2需要以热方式移除。对于amdea而言,状况反转,因为大部分co2是通过热再生(thermal regeneration)移除的。从而,使用所述溶剂体系提供来自对于如此应用的降低的能量使用的潜在节省。
[0084]
鉴于上述教导,可对本发明进行多种改变和变化。因此,将理解,在所附权利要求的范围内,本发明除了如上文所具体描述的之外,还可以其它方式实践。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1