一种超支化抗菌型聚氨酯反渗透膜及其制备方法与流程
1.本发明属于高分子合成技术领域,具体来说,涉及一种超支化抗菌型聚氨酯反渗透膜及其制备方法。
背景技术:
2.近年来,全球水资源短缺已经成为制约社会和经济发展的重要因素。反渗透膜分离技术作为一种先进的膜分离技术,广泛应用于海水、苦咸水淡化,废水资源化和物质分离浓缩等领域。膜污染现象的产生,导致了反渗透系统运行过程中需要频繁的对膜进行化学清洗,而频繁的清洗会造成反渗透膜元件使用寿命降低,增加反渗透系统的运行成本。开发具有抗生物污染性能的反渗透膜,可以有效解决反渗透膜的生物污染问题。
3.胍基聚合物是一类高效、广谱、无毒的阳离子杀菌剂。其杀菌机理如下:胍类聚合物的抗菌剂通常都显碱性,当阳离子型胍类衍生物与细菌接触时,胍类化合物携带的阳离子与带负电荷的细菌相互吸引,从而限制了细菌的正常活动,损坏细菌呼吸系统,导致“接触死亡”。另外,由于阳离子与负电荷相互吸引,导致细菌表面的负电荷分布不均匀而变形,使得细胞膜破裂,致使细胞内部的蛋白质等物质溢出,发生“细菌溶体”现象而死亡。
4.目前国内外许有多学者将胍盐引入到高聚物中,对高聚物进行胍基化改性。反渗透膜表面引入胍基用于抗菌的研究目前还较少,已有的报道主要是将商品聚合物胍材料通过物理涂覆的方法引入到反渗透膜表面。如nikkola等将聚乙烯醇(pva)和聚六亚甲基盐酸胍(phmg)的混合溶液涂覆在商品芳香聚酰胺反渗透膜表面。周艺璇等通过对聚乙烯胺(pvam)进行胍基化修饰,再将合成的双胍基化聚乙烯胺(pvamg)通过二次界面聚合引入到反渗透膜表面,制备出具有抗生物污染性能的pvamg改性反渗透膜。专利cn108786498.7将初生反渗透膜表面浸没在含有双胍基化壳寡糖水溶液中反应,利用芳香聚酰胺复合反渗透膜表面剩余的酰氯与双胍基化壳寡糖连接,构成抗粘附抗生物污染反渗透膜。专利cn107303470.6将凹凸棒土/二氧化硅—纳米银复合无机粉末与亲水性高分子材料混合后,涂覆在反渗透膜功能层的表面,经过热处理,得到具有交联结构涂层的抗菌反渗透复合膜。尽管如此,但上述抗污染反渗透膜的研究还存在着诸多问题:第一,对膜材料进行表面接枝改性时,往往会造成膜孔堵塞,渗透性能下降;第二,改性材料在膜表面的稳定性不好,长期使用会逐渐丧失抗污染能力;第三,大多数膜改性方法过程繁杂,生产成本高,难以实现规模化制备。
技术实现要素:
5.为了解决现有的技术问题,本发明提供一种超支化抗菌型聚氨酯反渗透膜及其制备方法,与现有方法相比,既可以规避无机抗菌剂带来的分散和脱落问题,又可以避免常规有机抗菌剂因热稳定性不好而分解,还可以避免因改性材料在膜表面的稳定性不好,发生相分离,造成长期使用会逐渐丧失抗污染能力。
6.为解决上述技术问题,本发明采用以下技术方案:
7.一种超支化抗菌型聚氨酯反渗透膜,该反渗透膜为孔隙率可控的超支化聚氨酯纳米纤维膜,其拉伸强度为5~6mpa。断裂伸长率为70~85%。
8.所述的一种超支化抗菌型聚氨酯反渗透膜的制备方法,包括以下步骤,
9.步骤1)将合成原料二异氰酸酯和聚二醇置于电热真空干燥箱中干燥;
10.步骤2)将步骤1)干燥处理后的二异氰酸酯与聚二醇在n2保护下搅拌混合均匀,升温至80~90℃,加入催化剂二月桂酸二丁基锡(dbtdl)反应0.5~1h后,降温至60~70℃,加入1,4—丁二醇扩链反应0.5~1h,再加入三羟甲基丙烷交联反应0.5~1h,加入适量有机溶剂降低体系黏度,保温反应2~3h,得到异氰酸酯基封端的聚氨酯预聚体;步骤3)升温至80~90℃,将预先溶于有机溶剂的端羟基或端胺基超支化聚合物缓慢滴加入步骤2)得到的异氰酸酯基封端的聚氨酯预聚体中,控制滴速为0.05~0.1ml/s,滴加完成后保温2~3h,得到异氰酸酯基封端的超支化聚氨酯;
11.步骤4)采用逐滴滴加的方式,控制滴速为0.05~0.1ml/s,将预先溶于有机溶剂的抗菌小分子双胍基盐酸盐滴入到步骤3)得到的异氰酸酯基封端的超支化聚氨酯中,接枝反应2~4h后,降温至30~45℃,得到超支化抗菌型聚氨酯溶液;
12.将得到的超支化抗菌型聚氨酯溶液用有机溶剂稀释,室温25℃下磁力搅拌4~6h,得到质量分数为5~8wt%的纺丝溶液,将纺丝溶液注入注射泵,控制接收板与平头针的距离为12~15cm,外加电压为16~20kv,灌注速率为0.8~1.5ml/h,环境湿度为45~60%,采用内径为0.25~0.35mm平头针进行静电纺丝,将得到的膜进行真空干燥,制备得到超支化抗菌型聚氨酯反渗透膜。
13.步骤1)所述聚二醇为聚氧化丙烯二元醇、聚四氢呋喃醚二元醇、聚己内酯二元醇、聚碳酸酯二元醇和聚己二酸丁二醇酯二元醇中的一种,其相对分子质量为1000。
14.步骤1)所述二异氰酸酯为异佛尔酮二异氰酸酯(ipdi)、甲苯二异氰酸酯(tdi)、六亚甲基二异氰酸酯(hdi)和二苯基甲烷二异氰酸酯(mdi)中的一种。
15.步骤2)中所述的有机溶剂为n,n—二甲基甲酰胺(dmf)、二甲基亚砜(dmso)、四氢呋喃(thf)、n—甲基吡咯烷酮(nmp)、甲苯中的一种。
16.步骤2)所述二异氰酸酯、聚二醇、二月桂酸二丁基锡dbtdl、1,4—丁二醇(bdo)和三羟甲基丙烷(tmp)的质量比为13~38:20~60:0.05~0.1:0.8~1.1:1.4~2.0,所述有机溶剂与反应单体总量的质量比为1~2:1。
17.步骤3)所述端羟基或端胺基超支化聚合物为端羟基聚酰胺胺零代(cyd—100h)、端氨基聚酰胺胺零代(cyd—100a)和聚醚胺(t403)中的一种。
18.步骤3)所述有机溶剂与端羟基或端胺基超支化聚合物质量比为10:1,端羟基或端胺基超支化聚合物与异氰酸酯基封端的聚氨酯预聚体质量比为1.5~3.2:35~105。
19.步骤4)所述抗菌小分子双胍基盐酸盐为1,1—二甲基双胍盐酸盐、盐酸缩二胍、聚六亚甲基双胍盐酸盐和1—苯基双胍盐酸盐中的一种。
20.步骤4)所述有机溶剂与抗菌小分子双胍基盐酸盐的质量比为5:1,抗菌小分子双胍基盐酸盐与异氰酸酯基封端的超支化聚氨酯质量比为2.0~4.0:35~105。
21.步骤5)所述真空干燥温度为60~80℃。
22.本发明的有益效果是:
23.与现有技术相比,本发明首先采用超支化的方式对聚氨酯骨架进行了改善,提高
了反渗透膜的拉伸强度和韧性,膜的抗冲击性得到提升;其次,通过静电纺丝法制备得到的反渗透膜,可以获得微观纤维结构匀称,孔隙率可控的纤维膜,有助于提高膜的通透性,且单一组分的膜不易发生相分离,结构稳定;另外本发明的反渗透膜定量引入抗菌活性基团,抗菌性能和抗污染性能好,可以有效控制膜污染,不仅可以延长膜的使用寿命,还能降低能耗和处理成本,在海水、苦咸水淡化,废水资源化和物质分离浓缩等领域有着潜在应用价值。
24.以下通过附图说明和实施例对本发明的超支化抗菌型聚氨酯反渗透膜及其制备方法做进一步描述。
附图说明
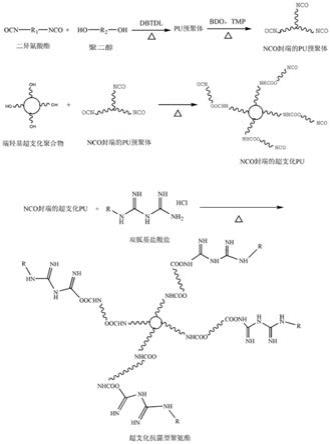
25.图1为本发明制备超支化抗菌型聚氨酯的合成原理图;
26.图2为本发明实施例1制备得到的超支化抗菌型聚氨酯反渗透膜的微观结构图;
27.图3为本发明实施例2制备得到的超支化抗菌型聚氨酯反渗透膜的微观结构图;
28.图4为本发明实施例3制备得到的超支化抗菌型聚氨酯反渗透膜的微观结构图。
具体实施方式
29.实施例1
30.如图1所示,将原料异佛尔酮二异氰酸酯(ipdi)和聚氧化丙烯二元醇置于电热真空干燥箱中干燥。称取25.3g干燥处理后的异佛尔酮二异氰酸酯和42.8g聚氧化丙烯二元醇(m
w
=1000)在n2保护下搅拌混合均匀,升温至80℃,加入0.1g催化剂二月桂酸二丁基锡(dbtdl)反应0.5h后,降温至60℃,加入0.82g 1,4—丁二醇(bdo)扩链反应0.5h,再加入1.52g三羟甲基丙烷(tmp)交联反应0.5h,加入70.5g n,n—二甲基甲酰胺(dmf)降低体系黏度,保温反应2h,得到异氰酸酯基封端的聚氨酯预聚体。
31.升温至85℃,将2.0g端羟基聚酰胺胺零代(cyd—100h)预先溶于20g n,n—二甲基甲酰胺(dmf)的缓慢滴加到异氰酸酯基封端的聚氨酯预聚体中,控制滴速为0.06ml/s,滴加完成后保温2h,得到异氰酸酯基封端的超支化聚氨酯。
32.将2.5g 1,1—二甲基双胍盐酸盐预先溶于12.5g n,n—二甲基甲酰胺(dmf)中,控制滴速为0.05ml/s,逐滴滴加到异氰酸酯基封端的超支化聚氨酯溶液中,接枝反应3h后,降温至45℃,得到超支化抗菌型聚氨酯溶液。
33.称取5g超支化抗菌型聚氨酯溶液,用n,n—二甲基甲酰胺(dmf)稀释至6wt%,室温25℃下磁力搅拌5h,取5ml纺丝溶液注入注射泵,控制接收板与平头针的距离为12cm,外加电压为16kv,灌注速率为0.8ml/h,环境湿度为45%,采用内径为0.33mm平头针进行静电纺丝,将得到的膜在60℃下进行真空干燥,制备得到超支化抗菌型聚氨酯反渗透膜,膜的微观形貌结构如图2所示,可见该反渗透膜为超支化聚氨酯纳米纤维膜。所制备的超支化抗菌型聚氨酯反渗透膜的测试结果列于表1。
34.实施例2
35.如图1所示,将原料甲苯二异氰酸酯(tdi)和聚己内酯二元醇置于电热真空干燥箱中干燥。称取15.4g干燥处理后的甲苯二异氰酸酯和22.5g聚己内酯二元醇(m
w
=1000)在n2保护下搅拌混合均匀,升温至85℃,加入0.05g催化剂二月桂酸二丁基锡(dbtdl)反应0.7h
后,降温至65℃,加入0.83g 1,4—丁二醇(bdo)扩链反应0.5h,再加入1.42g三羟甲基丙烷(tmp)交联反应1.0h,加入64g n—甲基吡咯烷酮(nmp)降低体系黏度,保温反应2.5h,得到异氰酸酯基封端的聚氨酯预聚体。
36.升温至85℃,将1.6g端氨基聚酰胺胺零代(cyd—100a)预先溶于16.0g n—甲基吡咯烷酮(nmp)的缓慢滴加到异氰酸酯基封端的聚氨酯预聚体中,控制滴速为0.06ml/s,滴加完成后保温2.5h,得到异氰酸酯基封端的超支化聚氨酯。
37.将3.0g盐酸缩二胍预先溶于15.0g n—甲基吡咯烷酮(nmp)中,控制滴速为0.08ml/s,逐滴滴加到异氰酸酯基封端的超支化聚氨酯溶液中,接枝反应4h后,降温至40℃,得到超支化抗菌型聚氨酯溶液。
38.称取5g超支化抗菌型聚氨酯溶液,用n—甲基吡咯烷酮(nmp)稀释至5wt%,室温25℃下磁力搅拌4h,取5ml纺丝溶液注入注射泵,控制接收板与平头针的距离为13cm,外加电压为20kv,灌注速率为1.2ml/h,环境湿度为50%,采用内径为0.25mm平头针进行静电纺丝,将得到的膜在70℃下进行真空干燥,制备得到超支化抗菌型聚氨酯反渗透膜,膜的微观形貌结构如图3所示,可见该反渗透膜为超支化聚氨酯纳米纤维膜。所制备的超支化抗菌型聚氨酯反渗透膜的测试结果列于表1。
39.实施例3
40.如图1所示,将原料六亚甲基二异氰酸酯(hdi)和聚四氢呋喃醚二元醇置于电热真空干燥箱中干燥。称取36.8g六亚甲基二异氰酸酯干燥处理后的和56.4g聚四氢呋喃醚二元醇(m
w
=1000)在n2保护下搅拌混合均匀,升温至90℃,加入0.08g催化剂二月桂酸二丁基锡(dbtdl)反应0.7h后,降温至70℃,加入1.1g 1,4—丁二醇(bdo)扩链反应1.0h,再加入1.9g三羟甲基丙烷(tmp)交联反应1.0h,加入190.8g二甲基亚砜(dmso)降低体系黏度,保温反应2.5h,得到异氰酸酯基封端的聚氨酯预聚体。
41.升温至90℃,将3.1g聚醚胺(t403)预先溶于31.0g二甲基亚砜(dmso)的缓慢滴加到异氰酸酯基封端的聚氨酯预聚体中,控制滴速为0.1ml/s,滴加完成后保温2.5h,得到异氰酸酯基封端的超支化聚氨酯。
42.将4.0g聚六亚甲基双胍盐酸盐预先溶于20.0g二甲基亚砜(dmso)中,控制滴速为0.1ml/s,逐滴滴加到异氰酸酯基封端的超支化聚氨酯溶液中,接枝反应4h后,降温至30℃,得到超支化抗菌型聚氨酯溶液。
43.称取5g超支化抗菌型聚氨酯溶液,用二甲基亚砜(dmso)稀释至7.5wt%,室温25℃下磁力搅拌5h,取5ml纺丝溶液注入注射泵,控制接收板与平头针的距离为15cm,外加电压为18kv,灌注速率为1.5ml/h,环境湿度为60%,采用内径为0.35mm平头针进行静电纺丝,将得到的膜在80℃下进行真空干燥,制备得到超支化抗菌型聚氨酯反渗透膜,膜的微观形貌结构如图4所示,可见该反渗透膜为超支化聚氨酯纳米纤维膜。所制备的超支化抗菌型聚氨酯反渗透膜的测试结果列于表1。
44.对比例1
45.将原料异佛尔酮二异氰酸酯(ipdi)和聚氧化丙烯二元醇置于电热真空干燥箱中干燥。称取25.3g干燥处理后的异佛尔酮二异氰酸酯和42.8g聚氧化丙烯二元醇(m
w
=1000)在n2保护下搅拌混合均匀,升温至80℃,加入0.1g催化剂二月桂酸二丁基锡(dbtdl)反应0.5h后,降温至60℃,加入0.82g 1,4—丁二醇(bdo)扩链反应0.5h,再加入1.52g三羟甲基
丙烷(tmp)交联反应0.5h,加入70.5g n,n—二甲基甲酰胺(dmf)降低体系黏度,保温反应2h,得到异氰酸酯基封端的聚氨酯预聚体。
46.将3.2g 1,1—二甲基双胍盐酸盐预先溶于16.0g n,n—二甲基甲酰胺(dmf)中,控制滴速为0.1ml/s,逐滴滴加到异氰酸酯基封端的聚氨酯溶液中,接枝反应3h后,降温至45℃,得到抗菌型聚氨酯溶液。
47.称取5g抗菌型聚氨酯溶液,用n,n—二甲基甲酰胺(dmf)稀释至6wt%,室温25℃下磁力搅拌5h,取5ml纺丝溶液注入注射泵,控制接收板与平头针的距离为12cm,外加电压为17kv,灌注速率为1.0ml/h,环境湿度为45%,采用内径为0.33mm平头针进行静电纺丝,将得到的膜在60℃下进行真空干燥,制备得到抗菌型聚氨酯反渗透膜。所制备的抗菌型聚氨酯反渗透膜的测试结果列于表1。
48.对比例2
49.将原料异佛尔酮二异氰酸酯(ipdi)和聚氧化丙烯二元醇置于电热真空干燥箱中干燥。称取25.3g干燥处理后的异佛尔酮二异氰酸酯和42.8g聚氧化丙烯二元醇(m
w
=1000)在n2保护下搅拌混合均匀,升温至80℃,加入0.1g催化剂二月桂酸二丁基锡(dbtdl)反应0.5h后,降温至60℃,加入0.82g 1,4—丁二醇(bdo)扩链反应0.5h,再加入1.52g三羟甲基丙烷(tmp)交联反应0.5h,加入70.5g n,n—二甲基甲酰胺(dmf)降低体系黏度,保温反应2h,得到异氰酸酯基封端的聚氨酯预聚体。
50.升温至85℃,将2.0g端羟基聚酰胺胺零代(cyd—100h)预先溶于20g n,n—二甲基甲酰胺(dmf)的缓慢滴加到异氰酸酯基封端的聚氨酯预聚体中,控制滴速为0.2ml/s,滴加完成后保温2h,得到超支化聚氨酯溶液。
51.称取5g超支化聚氨酯溶液,用n,n—二甲基甲酰胺(dmf)稀释至6wt%,室温25℃下磁力搅拌5h,取5ml纺丝溶液注入注射泵,控制接收板与平头针的距离为12cm,外加电压为17kv,灌注速率为1.0ml/h,环境湿度为45%,采用内径为0.33mm平头针进行静电纺丝,将得到的膜在60℃下进行真空干燥,制备得到超支化聚氨酯反渗透膜。所制备的超支化聚氨酯反渗透膜的测试结果列于表1。
52.本发明实施例和对比例测试的项目有:力学性能测试、透过性测试和抗菌性测试。(1)力学性能测试参照gb/t 1040—1992执行;(2)透过性测试:a、在2.0mpa、25℃错流流量1.5l/min下,使用2500mg/l的氯化钠水溶液测试初生反渗透膜的初始渗透通量和截盐率。b、将反渗透膜膜片置于1000μg/l牛血清蛋白和溶菌酶溶液中(ph=7.0)连续运行24h,然后测试污染后膜的水通量和截盐率。c、保持反渗透膜膜片不取出,将测试系统中的污染液排放干净,在0.7mpa、25℃错流流量4.0l/min下,利用2500mg/l的氯化钠水溶液冲洗反渗透膜1h,在2.0mpa、25℃错流流量1.5l/min下,测试清洗后膜的水通量和截盐率,通过得到的数据,计算水通量衰减率和恢复率。(3)将500μl大肠杆菌和金黄色葡萄球菌混合悬液(菌体浓度ca.2
×
106cfu/ml))均匀涂敷在5cm
×
5cm反渗透膜表面,按照现行gb/t31402检测标准检测抗菌率。
53.实施例1~3所制备的反渗透膜和对比例1~2制备的反渗透膜经测试后得到的拉伸应力、断裂伸长率、渗透通量、截盐率、抗菌性能均列于表1中。
54.表1实施例和对比例的测试结果:
[0055][0056]
由实施例1~3的性能测试结果可知,实施例1~3制备得到的反渗透膜具有良好的力学性能、初始渗透通量和截盐率,并且具有优异的抗菌性能和抗污染性能。通过实施例1~3和对比例1可以看出,本发明的反渗透膜中引入端羟基或端胺基超支化聚合物,可以有效提升反渗透膜的力学强度和柔韧性,通过实施例1~3和对比例2可以看出,胍基的引入可以有效提升反渗透膜的抗菌性和抗污染性能。
[0057]
综上,尽管以具体实施例对本发明作出了详细描述,但是,这些描述是示例性的,本领域技术人员能够在其基础上进行各种修改和变更,只要不脱离本发明原理,这些修改和变更均落入本发明的范畴中,本发明的保护范围由所附权利要求限定。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1