一种双环氧基修饰的生物芯片基片的制备方法与流程
1.本发明涉及生物领域,尤其涉及一种双环氧基修饰的生物芯片基片的制备方法。
背景技术:
2.生物芯片技术作为一种可以进行高通量多样品平行分析的重要工具,已经开始广泛应用于基因组学研究、单核苷酸多态性分析、临床医学检验等方面。它将大量的生物大分子探针、基因片段、寡聚核苷酸或蛋白质等按特定方式排列在特殊载体的固定位置上,在特定条件下与待检样品进行作用,通过精密的扫描仪器进行记录、检测、分析,具有自动化程度高、检测目的分子数量较多、高通量等优点。
3.生物芯片一般来说选择经过相应处理的硅片、玻璃片、金属片、塑料片或聚丙烯膜、硝酸纤维素膜等作为载体。以玻璃片为载体的二维表面修饰有氨基修饰、醛基修饰、巯基修饰及聚赖氨酸修饰等,这类载体大部分通过一些分子间亲和力或共价键把基因或蛋白探针固定在其表面,这种方法成本较低、便于制备、重复性好、荧光背景相对较低。但是仍存在一定缺陷,如探针固定量较小、表面均一性差、点样点不够规整以及表面官能团与探针之间发生非特异性交互作用使玻璃片背景增高等问题。三维表面修饰是在玻璃片表面包一层凝胶或树突状多聚物,然后再引入活性基团,从而在玻璃片表面形成三维立体结构。由于三维多孔结构,载体表面与探针接触面积大大增加,从而固定量也增加,提高了固定效率;另外,凝胶内湿润微环境使固定在上面的蛋白质溶液不易蒸发,从而保持了蛋白的活性。但是由于这些纳米级的多孔材料结构较为复杂,使得微阵列上的各种生物大分子探针间的距离控制较为困难,探针及多孔材料之间的交互作用因此增强,导致检测时的背景增高;此外,这些大分子多孔材料的使用给微阵列的后续洗脱也带来了问题。因此有良好的生物分子结合能力和表面质量高、背景低、信号强度高的生物芯片基片的发明势在必行。
4.为解决上述问题,本技术中提出一种双环氧基修饰的生物芯片基片的制备方法。
技术实现要素:
5.(一)发明目的
6.为解决背景技术中存在的技术问题,本发明提出一种双环氧基修饰的生物芯片基片的制备方法,本发明解决了氨基片接点作用力小,点样不匀,与醛基修饰相比很大程度上提升了芯片的信号强度,可广泛应用在各类生物芯片上。
7.(二)技术方案
8.为解决上述问题,本发明提供了一种双环氧基修饰的生物芯片基片的制备方法,包括以下步骤:
9.s1、将基片清洗干净后,将处理好的基底放入等离子体真空设备中,等离子体处理2-5min;
10.s2、加入装有氨基硅烷的25ml的烧瓶中,缓慢搅拌加入稳定剂n-羟基琥珀酰亚胺0.5ml,再加入对苯二甲醛4ml,充分反应0.5-1h得到环氧基硅烷试剂,取出合成好的环氧基
硅烷试剂;
11.s3、将等离子体处理好的基片放入环氧基硅烷的真空氛围中,通过真空缓慢挥发来修饰基片得到环氧基硅烷芯片;
12.s4、取出基片,将适宜浓度的寡核苷酸探针或pcr产物,抗原抗体,室温下,将配置好的点样液直接通过移液枪或者点样机点在芯片功能位点处,对于免疫体系,芯片点完液之后放置在湿度20-30%的条件下并且温度控制在37℃孵育四个小时;温度控制在25℃室温,湿度控制在70%左右;
13.s5、探针与环氧基的结合点样后,将芯片放入芯片盒中;
14.s6、洗片:制备洗涤液1,漂洗两遍最后氮气烘干测试其荧光强度。
15.优选的,在s1中,基片可选用玻璃或者塑料基片。
16.优选的,玻璃基片通过浓硫酸和双氧水3:1煮沸清洗;塑料基片通过氮气枪吹。
17.优选的,在s2中,环氧基硅烷合成方案取试剂4ml为刚性分子不可以任意扭曲,其分子式中的两个环氧基只有一个与基片上的氨基反应并开环,另一个则暴露在基片表面上。
18.优选的,在s4中,基因芯片稀释液可选用pbs或者tween、肌氨酸、sds柠檬酸钠标准液浓度都在0.05-0.1%左右;crp蛋白质浓度在1-2000ng/ml;一些细胞类点样的稀释液为50%的dmso作为点样液。
19.优选的,在s1中,等离子体工艺氧气进气量控制在50-200sccm,等离子体功率在100-500w,辅助氩气进气量50-100sccm。
20.优选的,在s5中,在37℃恒温恒湿箱中静止4-24小时。
21.本发明的上述技术方案具有如下有益的技术效果:
22.利用气相接枝法一步修饰改性微流控与生物芯片基片表面,在缩小试剂的消耗以及低成本的同时,能够实现芯片的批量化量产的功能。此项涂层加工工艺技术大大缩减了微流控相关企业在成品研发环节中的各项研发成本,大力促进终端产品的上市进程。
23.本发明开发出的生物塑料材料表面涂层加工技术与传统的涂层加工技术相比具有显著的特点:价格低廉、高质量、普适性广、可量产化、满足实际应用要求等,尤其在解决长期制约微流控与生物塑料芯片微通道结构表面改性,以提供合适的物理、化学或生物功能等关键应用技术难题上具有显著特色,打破了相关国外企业在材料表界面修饰领域的技术垄断,以突破了生产工艺中的量产化技术局限。
附图说明
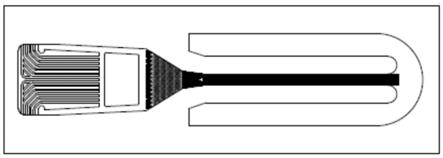
24.图1为本发明提出的一种双环氧基修饰的生物芯片基片的制备方法中芯片的结构示意图。
25.图2为本发明提出的一种双环氧基修饰的生物芯片基片的制备方法中盖板的结构示意图。
26.图3为本发明提出的一种双环氧基修饰的生物芯片基片的制备方法中测试crp数据之一图。
27.图4为本发明提出的一种双环氧基修饰的生物芯片基片的制备方法中测试crp数据其一图。
具体实施方式
28.为使本发明的目的、技术方案和优点更加清楚明了,下面结合具体实施方式并参照附图1-4,对本发明进一步详细说明。应该理解,这些描述只是示例性的,而并非要限制本发明的范围。此外,在以下说明中,省略了对公知结构和技术的描述,以避免不必要地混淆本发明的概念。
29.本发明提出的一种双环氧基修饰的生物芯片基片的制备方法,包括以下步骤:
30.s1、将基片清洗干净后,将处理好的基底放入等离子体真空设备中,等离子体处理2-5min;
31.s2、加入装有氨基硅烷的25ml的烧瓶中,缓慢搅拌加入稳定剂n-羟基琥珀酰亚胺0.5ml,充分反应0.5-1h得到环氧基硅烷试剂,取出修饰好的环氧基芯片;
32.s3、将等离子体处理好的基片放入环氧基硅烷的真空氛围中,通过真空缓慢挥发来修饰基片得到环氧基硅烷芯片;
33.s4、取出基片,将适宜浓度的寡核苷酸探针或pcr产物,抗原抗体,室温下,将配置好的点样液直接通过移液枪或者点样机(加入适量甘油)点在芯片功能位点处,对于免疫体系,芯片点完液之后放置在湿度20-30%的条件下并且温度控制在37℃孵育四个小时;温度控制在25℃室温,湿度控制在70%左右;
34.s5、探针与环氧基的结合点样后,将芯片放入芯片盒中;
35.s6、洗片:制备洗涤液1(2xssc/0.2%sds),漂洗两遍最后氮气烘干测试其荧光强度。
36.在一个可选的实施例中,在s1中,基片可选用玻璃或者塑料基片。
37.在一个可选的实施例中,玻璃基片通过浓硫酸和双氧水3:1煮沸清洗;塑料基片通过氮气枪吹。
38.在一个可选的实施例中,在s2中,环氧基硅烷合成方案取试剂4ml(1,4-丁二醇二缩水甘油醚)为刚性分子不可以任意扭曲,其分子式中的两个环氧基只有一个与基片上的氨基反应并开环,另一个则暴露在基片表面上。
39.在一个可选的实施例中,在s4中,基因芯片稀释液可选用pbs或者tween、肌氨酸、sds柠檬酸钠标准液浓度都在0.05-0.1%左右;crp蛋白质浓度在1-2000ng/ml;一些细胞类点样的稀释液为50%的dmso作为点样液。
40.在一个可选的实施例中,在s1中,等离子体工艺氧气进气量控制在50-200sccm,等离子体功率在100-500w,辅助氩气进气量50-100sccm。
41.在一个可选的实施例中,在s5中,在37℃恒温恒湿箱中静止4-24小时。
42.crp实验流程
43.1.样片的准备:
44.取免疫荧光芯片-pmma(白)15片用作孵育c反应蛋白孵育一抗的基底,备用的芯片保持表面的干净且无任何颗粒物的粘附,因为任何杂质的存在都会影响最后的检测结果。
45.2.crp一抗的孵育:
46.取浓度为2mg/ml的c反应蛋白,试剂先经过顺时离心机离心再分别点样在pmma(白)表面,每片点样0.5ul。分为五组,用作二抗梯度孵育。点样完成的芯片需放置于37℃烘箱中,孵育时间为4h。
47.3.梯度质控的制备:
48.1)准备离心管,标记命名;
49.母液瞬离;
50.100ug/ml—1000ng/ml—500ng/ml—50ng/ml—5ng/ml—0
51.a:先加pbs稀释液;
52.b:后加ab,涡旋混合。
53.2)加荧光抗体标记,90ul+3ul,涡旋混匀。荧光抗体标记是经过pbs稀释40倍,涡旋混匀备用。
54.3)质控浓度分为五组,分别为:1000ng/ml,500ng/ml,50ng/ml,5ng/ml,0(阴性对照)。其浓度的配比都是通过质控浓度为100ug/ml的试剂等比例稀释制备。梯度稀释得到的质控液再分别滴加浓度稀释40倍的荧光标记物,混匀备用。
55.4.梯度质控进液:
56.孵育一抗的样片,会首先经过贴膜处理。膜均采用亲水薄膜,膜的形状会提前通过激光切割匹配芯片。每个质控浓度下芯片的进液量控制为30ul的量,进液时间控制在20min。进液结束后,撕膜并进行清洗,最后经过甩片离心机清理表面多余的废水。
57.5.测试芯片表面荧光信号:
58.处理完的芯片会被密封且避光,荧光芯片通过博奥luxscan 10k测试,表征其芯片表面荧光强度。
59.测试crp数据如下:
[0060][0061][0062]
应当理解的是,本发明的上述具体实施方式仅仅用于示例性说明或解释本发明的原理,而不构成对本发明的限制。因此,在不偏离本发明的精神和范围的情况下所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。此外,本发明所附权利要求旨在涵盖落入所附权利要求范围和边界、或者这种范围和边界的等同形式内的全部变化和修改例。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1