聚合物介导高性能琼脂糖整体柱及其制备方法
:
1.本发明属于生物工程技术领域,具体涉及聚合物介导高性能琼脂糖整体柱及其制备方法。
背景技术:
2.生物技术的迅速发展不仅为新型产品的拓展打开了思路,更为下游产品纯化技术提出了更高的要求。为了更好的适应新生物产品的分离纯化需求,下游设计生物纯化制备领域的各个环节均需要获得有效的纯化,其中设计到生物物质纯化关键的核心色谱介质仍旧是重点改进目标之一。目前色谱介质仍旧占据下游生物产品纯化的核心,其中以琼脂糖为基质的色谱凝胶仍在生物纯化领域占据不可取代的地位;其在亲和、疏水、排阻色谱等领域均占据广阔的市场。琼脂糖层析介质具有开放性的网络结构,作为色谱介质在生化领域中具有异质性影响低、生物相容性高、易于操作等优势。其中ni亲和柱是生物下游应用最广泛的填料之一,在生物产品的制备过程具有至关重要的作用。目前市场应用的琼脂糖介质均以琼脂糖微球的形式存在,但现有的琼脂糖微球在分离效率等方面难以满足生物分离领域对高效率分离介质的需求。尤其现有琼脂糖微球较小的孔隙结构导致极大的传质阻力,同时对于复杂生物基质的耐受性会进一步下降,这一点在生物纯化领域尤其大规模制备领域会带来较大的负面影响。因此如何基于琼脂糖介质开发新型的色谱层析材料是解决现有生物技术下游制备领域关键平静性技术的最佳方案。
3.与传统颗粒层析介质相比,整体柱因为具有处理时间短、流量大、柱压低的优势已经引起人们的广泛关注。早期整体柱固定相利用自由基聚合反应形成整体凝胶,但是因为其内部不具备大孔结构导致扩散性能较差;聚氨酯泡沫作为整体柱的另一种尝试被应用与气相色谱分离;但是这些整体凝胶均具有制备方法复杂、渗透率低、凝胶过软等的劣势;大孔化学凝胶在很大程度上解决了整体柱结构强度及渗透性的问题,但其化学基团往往带来非特异性吸附的问题。以琼脂糖构建大孔凝胶整体柱不仅可以避免基质的非特异性吸附,更可以发挥琼脂糖温度可控固相转变的优势,简化制备过程;且琼脂糖易于修饰特点可以从分发挥其多功能性的优势,构建新型的色谱层析介质。
4.大孔凝胶高通透性的优势在提高基质耐受性的同时也导致其吸附量不足。大孔凝胶体系之下,样品溶液通过凝胶层析介质的速度会增大,因此仅凝胶表面的亲核基团可以有效发挥亲和识别功能;琼脂糖介质虽然可以通过调节其浓度进而调节整体柱的孔隙比例,但增大浓度会进一步降低其通透性。功能化聚合物通过提供中间桥架构建多位点亲和识别体系,在溶液体系中通过扩散的三维结构实现对目标物的高容量富集;因此将功能化聚合物与大孔琼脂糖整体柱结合开发一种高性能、方法简单并具备良好机械强度的大孔琼脂糖整体柱艺并应用于生物分离下游体系具有重要的意义。
技术实现要素:
5.本发明要解决的技术问题是琼脂糖介质应用在大孔凝胶时可以通过调节其浓度
进而调节整体柱的空袭比例,但增大浓度会进一步降低其通透性。
6.为解决上述问题,本发明将功能化聚合物与大孔琼脂糖整体柱结合,得到了一种高性能、方法简单并具备良好机械强度的大孔琼脂糖整体柱。
7.为达到上述目的,本发明通过以下技术方案实现,聚合物介导高性能琼脂糖整体柱的制备方法,包括以下步骤:
8.(1)制备功能性聚合物;
9.(2)制备叠氮化琼脂糖整体柱;
10.(3)制备聚合物功能化琼脂糖整体柱。
11.进一步的,在步骤(3)的聚合物功能化琼脂糖整体柱复合材料表面引入ida或nta基团。具体为将步骤(3)获得的聚合物功能化琼脂糖整体柱分散在10%nicl2水溶液中(w/v),随后室温下振荡摇晃6h;获得的样品用去离子水充分清洗之后保存在20%乙醇水溶液中备用,命名为ag@poly(nipam-co-gma)@ida(nta)-ni。
12.进一步的,步骤(1)为将甲基丙烯酸缩水甘油酯、共聚物、偶氮二异丁腈、2-苯基-2-丙基苯并二硫溶解在甲醇中,在冰浴条件下去除空气;然后样品封闭并于70℃条件下反应24h;去除杂质后40℃旋转蒸发干燥得到聚合物poly(nipam-co-gma);甲基丙烯酸缩水甘油酯、共聚物为单体用于构建聚合物,偶氮二异丁腈为引发剂、2-苯基-2-丙基苯并二硫为raft试剂,用于聚合物的眼神;在体系中在aibn的初始催化下,聚合物单体以raft试剂为引导合成结构及分子量可控聚合物。
13.将亚氨基二乙酸或nα,nα-二(羧甲基)-l-赖氨酸,与炔丙氨溶解于碳酸盐缓冲液中,调节 ph至11.0,得到混合液;将poly(nipam-co-gma)溶解与甲醇中,随后与上述混合液混合并在80℃下搅拌反应12h,去除杂质后旋转蒸发干燥得到功能性聚合物 poly(nipam-co-gma)@ida@alkyne。其中,亚氨基二乙酸或nα,nα-二(羧甲基)-l-赖氨酸用于偶联ni2+,cu2+,co2+等离子;炔丙氨用于实现聚合物在琼脂糖凝胶整体柱表面经点击化学反应聚合。期间,三种试剂的氨基与环氧基发生反应,实现修饰。
14.进一步的,所述共聚物为n-异丙基丙烯酰胺、甲基丙烯酸,甲基丙烯酸羟乙酯,甲基乙烯酸,甲基丙烯酸二甲氨基乙酯中的一种或一种以上的混合物,形成具有不同结构及基团的聚合物。
15.进一步的,步骤(2)为将琼脂糖溶液利用微波加热方法至溶液透明,待温度下降至与有机体系的沸点一致与油相溶液混合搅拌形成均一的乳液;乳液随后转移到4℃条件下冷却,去除杂质后命名为ag;琼脂糖在水中加热到90℃以上溶解,并在温度下降到35-40℃时可以形成良好的半固体状凝胶;将琼脂糖溶液与油相溶液混合时,油相中乳化剂分子的一端亲水,另一端亲油。经过搅拌后,油相与琼脂糖溶液被分散成小颗粒,并在乳化剂的作用下混合。整个体系的形态是水以小液滴的形式分散于油中。
16.将上述琼脂糖整体柱ag分散在1.0m naoh溶液中,随后在溶液中加入环氧氯丙烷,二甲基亚砜及硼氢化钠;随后获得的样品体系在40℃条件下振荡反应6h;随后将获得的凝胶清洗干净,命名为ag@epoxy。1)环氧氯丙烷将活泼的环氧基团引入ag上,以利于ag 与亲和配基在常温或低温下反应制备亲和吸附介质。环氧氯丙烷在活化的同时,又使ag达到一定程度的交联,不仅改进了ag的机械性能,且对强碱和热的耐受性能大大增加。2)二甲基亚砜可消除琼脂糖凝胶与环氧氯丙烷之间的相界面,促进活化试剂的溶解,提高了琼脂糖色
谱介质中环氧基的修饰密度,并通过对环氧氯丙烷浓度及反应时间的优化,得出最大环氧基修饰密度下的最佳活化反应条件。3)硼氢化钠可以防止环氧基被氧化。
17.将ag@epxoy凝胶浸没在n,n-二甲基甲酰胺或水或水与n,n-二甲基甲酰胺混合溶液中,随后于体系中加入叠氮化钠及氯化铵;超声后样品于60℃条件下振荡24h;反应完毕后的凝胶冲洗干净得到叠氮化琼脂糖整体柱,命名为ag@n3。n,n-二甲基甲酰胺为溶剂,叠氮化钠可以与环氧基反应为叠氮基,氯化铵为催化试剂;期间叠氮化钠与环氧基反应将环氧基转换为叠氮基。
18.进一步的,油相为含tween 80的液体石蜡,有机体系的沸点为85℃。
19.进一步的,油相为含tween 80的环己烷,有机体系的沸点为75℃。
20.进一步的,步骤(2)得到ag的反应条件为100ml琼脂糖溶液,50ml油相溶液,3-6 ml tween 80,混合后在1000rpm转速条件下搅拌1h。琼脂糖浓度、油相体积、tween 80 的量、转速决定了最终琼脂糖整体柱的空隙大小,其中,转速过快会导致ag颗粒偏小,转速过慢会导致ag颗粒偏大;琼脂糖浓度相对低会导致ag颗粒过于松散,易破碎,琼脂糖浓度相对高会导致ag颗粒偏硬,通透性降低。
21.进一步的,步骤(3)为将ag@n3与poly(nipam-co-gma)@ida@alkyne分散在甲醇水溶液中,随后样品体系去除空气并加入硫酸铜水溶液及抗坏血酸钠;样品随后封闭并在 37℃~60℃条件下反应24h;反应完毕之后,获得的样品用清洗,得到聚合物功能化琼脂糖整体柱,命名为ag@poly(nipam-co-gma)@ida。其中,硫酸铜水与抗坏血酸钠反应形成一价铜,进而催化聚合物炔基与琼脂糖整体柱的叠氮基反应实现聚合物固定化。
22.本发明的有益效果在于:
23.1)琼脂糖溶液与油相在搅拌下形成乳液,去除杂质后得到的ag内部充满孔隙,首先可以解决琼脂糖微球在分离纯化样品过程中,由于其细小孔隙所造成的较大传质阻力问题,提高微球使用寿命;其次,微球内具备较大的孔隙,可以在后续反应过程中为反应物提供更多的结合位点,这进一步在分离纯化过程中提高了微球的工作效率。
24.2)本发明中,琼脂糖微球虽然具有较大的孔隙,但是空隙内结合特异性亲和吸附基团,避免了由于大孔隙造成的非特异性吸附情况出现,提高了纯化后样品的纯度。
25.3)本发明中,琼脂糖溶液与油相的配比组成使得ag结构稳定,避免了由于微球结构强度不够而导致的破碎现象,以及强度过硬而出现的纯化效率下降。
26.4)本发明中,poly(nipam-co-gma)@ida的应用,提高了微球表面功能基团的密度以及与待纯化样品的接触面积,在一定程度上提高了纯化效率。
27.5)本发明中,微球的制备方法简便,降低生产成本,提高生产效率。综上,相较于目前市场应用的琼脂糖微球吸附材料,该发明具备生产工艺简便、产品结构强度稳固、渗透率高、扩散性好、特异性吸附,分离纯化效率高等优点。
附图说明
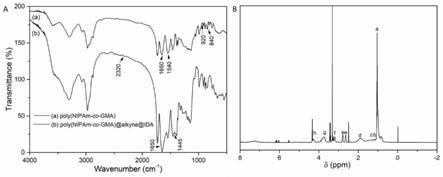
28.图1(a)功能化聚合物poly(nipam-co-gma)及poly(nipam-co-gma)@ida@alkyne ftir表征图,(b)poly(nipam-co-gma)聚合物1hnmr谱图。
29.图2复合材料ag(a),ag@epoxy(b),ag@n3(c),ag@ida(d)及ag@ poly(nipam-co-gma)@ida(e)ft ir红外图谱。
30.图3ag(a,b)及ag@poly(nipam-co-gma)@ida sem图。比例尺分别为200μm(a, c)及50μm(b,d)。
31.图4ag@poly(nipam-co-gma)@ida-ni亲和凝胶处理样品sds page分析结果图。 lane m:蛋白标准样品;lane a1:尾丝蛋白lys360大肠杆菌表达液;lane a2:亲和凝胶处理后上清液;lane(a3,a4,a5,a6)分别为20mm,50mm,100mm,200mm咪唑磷酸盐缓冲液洗脱液。lane b1:壳寡糖酶大肠杆菌表达液;lane b2:亲和凝胶处理后上清液;lane(b3, b4,b5,b6,b7)分别为20mm,40mm,60mm,80mm,100mm咪唑磷酸盐缓冲液洗脱液。
具体实施方式:
32.为使本发明实施例的目的、技术方案和优点更加清楚,下面对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
33.实施例1:
34.聚合物介导高性能琼脂糖整体柱的制备方法,包括以下步骤:
35.(1)制备功能性聚合物:
36.n-异丙基丙烯酰胺(nipam,2.567g)及甲基丙烯酸缩水甘油酯(gma,1.619g)(gma 是必选试剂,nipam为共聚物,可以用其他物质代替),偶氮二异丁腈(aibn,12.4mg),2
‑ꢀ
苯基-2-丙基苯并二硫(cdb,65.2mg)溶解在50ml甲醇中,随后样品转移到100ml圆底烧瓶并在冰浴条件下氮气鼓吹15min完全去除空气。随后样品瓶封闭并于70℃条件下反应 24h,反应完毕后的功能化聚合物通过透析方式去除杂质;随后40℃旋转蒸发干燥并命名为 poly(nipam-co-gma)。
37.亚氨基二乙酸(200mg)(或nα,nα-二(羧甲基)-l-赖氨酸)及炔丙氨(200μl)溶解于10ml碳酸盐缓冲液(0.1m),随后溶液用naoh调节ph至11.0。聚合物poly(nipam-co-gma) (120mg)溶解于30ml甲醇,随后于上述溶液混合并在80℃下搅拌反应12h。反应完毕后获得的复合物通过透析去除杂质并旋转蒸发干燥后命名为 poly(nipam-co-gma)@ida@alkyne。
38.(2)制备叠氮化琼脂糖整体柱
39.100ml 2~8%的琼脂糖溶液利用微波加热方法至溶液透明,待温度下降至85℃或75℃ (与有机体系的沸点一致)时与50ml油相溶液(液体石蜡、环己烷等油相,含3-6mltween 80)混合后,于85℃(液体石蜡)或75℃(环己烷)条件下搅拌1h(1000rpm转速)形成均一的乳液(琼脂糖浓度、油相体积、tween 80的量、转速决定了最终琼脂糖整体柱的空隙大小)。2ml乳液随后转移到6ml spe管中随后于4℃条件下冷却至。冷却后的整体柱用去离子水充分冲洗去除杂质,并命名为ag。
40.5块制备的琼脂糖整体柱分散待50ml 1.0m naoh溶液中,随后在溶液中加入50ml环氧氯丙烷,32ml二甲基亚砜及75mg硼氢化钠;随后获得的样品体系在40℃条件下振荡反应6h;随后获得的凝胶用80%的乙醇水溶液及去离子水充分清洗干净,并命名为ag@epoxy。
41.2块ag@epxoy凝胶浸没在15mln,n-二甲基甲酰胺(或水或水与n,n-二甲基甲酰胺混合溶液)中,随后于体系中加入156mg叠氮化钠及129mg氯化铵;超声15min后样品与 60℃条件下振荡24h;反应完毕后凝胶用去离子水冲洗干净并命名为ag@n3。
42.(3)制备聚合物功能化琼脂糖整体柱
43.ag@n3(3块)与150mg poly(nipam-co-gma)@ida@alkyne分散在24ml甲醇水溶液中(3:1,v/v),随后样品体系用氮气鼓泡15min去除空气并随后加入100μl 0.5m硫酸铜水溶液及50mg抗坏血酸钠。样品继续氮气鼓泡15min随后封闭并在45℃(37℃~60℃之间)反应24h。反应完毕之后,获得的样品用5%edta溶液充分冲洗后用乙醇及去离子水梯度清洗,随后命名为ag@poly(nipam-co-gma)@ida。
44.实施例2:
45.在复合材料表面引入ida或nta基团:
46.将实施例1获得的ag@poly(nipam-co-gma)@ida(nta)分散在10%nicl2水溶液中(w/v),随后室温下振荡摇晃6h。获得的样品用去离子水充分清洗之后保存在20%乙醇水溶液中备用,命名为ag@poly(nipam-co-gma)@ida(nta)-ni。
47.蛋白吸附验证:
48.将琼脂糖整体柱ag@poly(nipam-co-gma)@ida-ni 1ml装柱到6ml spe固相萃取管中,随后用磷酸盐缓冲液(ph 8.0,50mm磷酸氢二钠,300mm氯化钠及1%甘油)活化,蛋白样品缓慢通过凝胶柱,以重力柱方式流过。随后用磷酸盐缓冲液冲洗去除残留蛋白及杂质,并用梯度浓度咪唑缓冲液洗脱,收集洗脱液sds page验证。
49.实验结果
50.(1)功能化聚合物表征:
51.图1(a)为poly(nipam-co-gma)及经过炔丙氨及ida反应的poly(nipam-co-gma) 的ft ir图;红外结果显示,840及920cm-1
处吸收信号表明聚合物含有环氧基,表明gma 在聚合物中聚合成功;1540及1650cm-1处吸收信号为酰胺基-c=o及-n-h的震动信号;引入炔丙氨及ida之后,1445及1650cm-1处增强的信号验证聚合物表面引入羰基,同时2230 cm-1处微弱的吸收峰表明聚合物含有炔基,该结果表明聚合物ida及炔基化修饰成功。图1 (b)为poly(nipam-co-gma)1hnmr图,在图1(b)所示的1hnmr谱图中,1.04ppm(a) 及3.73ppm(g)处为pnipam中异丙基吸收信号;此外ch-ch
2-o(2.65ppm(e)及2.80ppm(e)) 及ch-ch
2-o(3.22ppm(f))信号来自于gma片段。4.28ppm(h)处信号为gma片段中链接酯基的亚甲基信号;根据nipam异丙基(a)及gma酯基(e)信号面积对比,聚合物中nipam与gma的比为2.45:1,表明聚合物poly(nipam-co-gma)制备成功。
52.(2)ag@poly(nipam-co-gma)@ida亲和材料表征
53.由图2红外结果显示,经过环氧氯丙烷修饰之后,860cm-1处信号表明琼脂糖整体柱表面环氧基团修饰成功(curve b);经过叠氮化钠修饰之后整体柱ft ir出现很强烈的叠氮基信号(2100cm-1,curve c),不仅表明琼脂糖表面含有环氧基并且表明叠氮基修饰成功。经过 poly(nipam-co-gma)@ida@alkyne以点击反应修饰到ag@n3表面之后,叠氮基信号消失表明聚合物制备修饰成功(curve e);对于ag@ida,ft ir结果表明1460与1620处信号可以归因于羟基面内震动及羰基的伸缩振动(curve d),表明ida在亲和凝胶整体柱表面修饰成功。
54.由图3的sem图显示,ag整体柱呈现连续圆润的内部结构,其内部孔径大于50μm;代表面修饰功能化聚合物之后,表面出现粗糙的聚合物层(图3.c,d),表明聚合物在整体柱表面修饰成功。
55.(3)ag@poly(nipam-co-gma)@ida净化蛋白效果
56.以含组氨酸标签尾丝蛋白lys360,壳寡糖酶大肠杆菌表达液为样品,验证亲和凝胶纯化效果,结果如图4所示,制备的亲和凝胶对四种样品体系中目标蛋白均有良好的纯化效果,灰度分析目标物纯度均》90%。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1