生产金属铅的方法与流程
本发明涉及金属提炼技术领域,具体而言,涉及一种生产金属铅的方法。
背景技术:
铅是一种对人体健康有害的重金属,近几十年来,防控铅冶炼对环境造成污染的要求逐渐严格,以致于铅冶炼的环境成本逐年增高。
火法炼铅工艺已有新技术取得产业化应用:如德国鲁奇的qsl法、意大利的kivcet法以及澳大利亚的isa法。我国同期展开了底吹炼铅半工业试验,并于本世纪初在国内广为应用。虽然较传统鼓风炉方法进步很大,但仍存在问题,达不到≤50ug/m3pb的排放标准。另外,铅与其他金属的不同,硫酸铅不溶于水,因此铅的浸出不能用铜、镍、钴、锌等常用成熟的硫酸体系进行浸出,虽然可以用现行湿法工艺中基于氯化物水溶液,采用锌置换的方式,或采用硅氟酸体系进行电解湿法炼铅,从而减少铅尘及铅蒸汽对大气的污染程度,但是湿法电解回收铅效率较低。
技术实现要素:
本发明旨在提供一种生产金属铅的方法,以解决现有技术中生产金属铅造成空气污染或铅回收效率低的技术问题。
为了实现上述目的,根据本发明的一个方面,提供了一种生产金属铅的方法。该方法包括:采用氯化物处理硫化铅获得氯化铅;对结晶干燥后的氯化铅进行熔盐电解生产得到金属铅。
进一步地,采用氯化物处理硫化铅包括:将硫化铅原料采用氯化铁体系进行氧化浸出处理,处理过程中通入氧气,控制反应温度为20~150℃,反应时间为0.5~5h,氯化铁用量系数为1~1.8。
进一步地,将硫化铅原料采用氯化铁体系进行氧化浸出处理后还包括对氧化浸出反应液进行浮选或过滤,得到滤液和滤渣。
进一步地,将滤液降温冷却,析出氯化铅固体,过滤洗涤、干燥得到氯化铅,剩余液体为氯化亚铁溶液。
进一步地,熔盐电解的熔盐电解体系包括选自由licl、nacl、kcl、cscl、mgcl2和cacl2组成的组中的一种或多种。
进一步地,熔盐电解的阴极和阳极通入直流电,阴极为熔点高于铅的金属,阳极为石墨。
进一步地,阴极为钨或钼。
进一步地,熔盐电解的温度为400~900℃,阴极的电流密度控制在0.1~10a/cm2。
进一步地,该生产金属铅的方法还包括:将氯化亚铁溶液进行氧化处理,采用盐酸控制盐酸浓度为10-50g/l,控制反应温度为20~180℃,加入氧化剂,氧分压控制在2~10bar,将二价铁全部氧化成三价铁,返回采用氯化物处理硫化铅的步骤中使用。
进一步地,氧化剂为双氧水、氧气或氯气;优选的,氯气为电解产生的氯气;优选的,电解产生的氯气用于硫化铅的氧化浸出。
应用本发明的技术方案,先采用湿法处理硫化铅,获得中间产品氯化铅,再采用熔盐电解的方式进行处理,由于熔盐体系是一种离子导体,扩散速度快,浓差极化程度小,可以提高电流密度,从而提高电解过程效率,并提高产品纯度。
附图说明
构成本申请的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。在附图中:
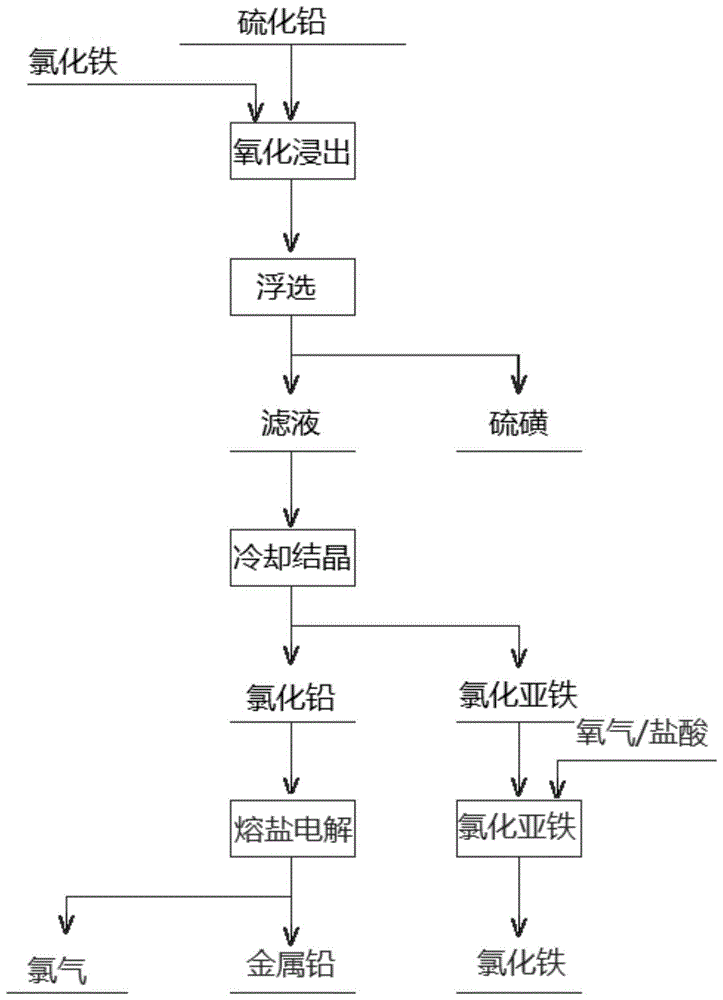
图1示出了根据本发明一实施方式的生产金属铅的流程示意图。
具体实施方式
需要说明的是,在不冲突的情况下,本申请中的实施例及实施例中的特征可以相互组合。下面将参考附图并结合实施例来详细说明本发明。
针对现有技术中生产金属铅造成空气污染或铅回收效率低的技术问题,本发明提出了以下列技术方案。
根据本发明一种典型的实施方式,提供一种生产金属铅的方法。该方法包括采用氯化物处理硫化铅获得氯化铅;对结晶干燥后的氯化铅进行熔盐电解生产得到金属铅。
应用本发明的技术方案,先采用湿法处理硫化铅,获得中间产品氯化铅,再采用熔盐电解的方式进行处理,由于熔盐体系是一种离子导体,扩散速度快,浓差极化程度小,可以提高电流密度,从而提高电解过程效率,并提高产品纯度。
优选的,采用氯化物处理硫化铅包括:将硫化铅原料采用氯化铁体系进行氧化浸出处理,处理过程中通入氧气,控制反应温度为20~150℃,反应时间为0.5~5h,氯化铁用量系数为1~1.8,其中,当用量系数是1时候,用量是与化学反应方程式摩尔比一致,当为1.8时是过量了80%。采用此种处理方法浸出效率高,浸出率高,将铅转化到氯化物体系中,为氯化物熔盐电解体系准备原料。另外,电解产生的氯气也可以用于硫化铅的氧化浸出,能够实现物质的循环利用,降低生产成本。
在本发明一典型的实施方式中,将硫化铅原料采用氯化铁体系进行氧化浸出处理后还包括对氧化浸出反应液进行浮选或过滤,得到滤液和滤渣,其中,滤渣为硫磺,将滤液降温冷却,析出氯化铅固体,过滤洗涤、干燥得到氯化铅,剩余液体为氯化亚铁溶液。优选的,熔盐电解的熔盐电解体系包括选自由licl、nacl、kcl、cscl、mgcl2和cacl2组成的组中的一种或多种。熔盐电解的阴极和阳极通入直流电,阴极为熔点高于铅的金属,例如钨或钼;阳极为石墨。
优选的,熔盐电解的温度为400~900℃,在此温度范围内可以让铅熔化形成液态铅,熔盐体系为液态,若温度高于900℃,则能耗较高,氯化物挥发多,不利于工业化生产。阴极的电流密度控制在0.1~10a/cm2,在此电流密度范围内,不会因电流过高导致阴极极化严重,氯化物体系中碱金属离子放电形成金属,污染铅,又能保证较高的生产效率。
优选的,方法还包括:将氯化亚铁溶液进行氧化处理,采用盐酸控制盐酸浓度为10-50g/l,控制反应温度为20~180℃,例如30℃、40℃、50℃、60℃、70℃、80℃、90℃、100℃、110℃、120℃、130℃、140℃、150℃、160℃或170℃,加入氧化剂,氧分压控制在2~10bar,将二价铁全部氧化成三价铁,返回采用氯化物处理硫化铅的步骤中使用,降低生产成本。其中,氧化剂为双氧水或氧气氧化剂为双氧水、氧气或氯气;优选的,所述氯气为电解产生的氯气;这些氧化剂的使用不会引入其他的杂质,简化生产流程,提高生产效率,降低生产成本。
在本发明一典型的实施方式中,相关反应方程式如下:
pbs+2fecl3→pbcl2+2fecl2+s
4fecl2+o2(g)+4hcl=4fecl3+2h2o
下面将结合实施例进一步说明本发明的有益效果。
实施例1
参见图1所示的流程,将硫化铅进行加压氧化浸出,加入三氯化铁溶液,三氯化铁用量系数为1.1,控制反应温度为120℃,时间为2h。
反应后液进行浮选或过滤,滤渣为硫磺。
反应后液降温冷却,析出氯化铅固体,过滤洗涤并干燥。
氯化铅去熔盐电解,熔盐体系是nacl-kcl,阴极阳极通入直流电,阴极为钼,阳极为石墨棒,阴极析出液态铅,阳极析出氯气,氯气进行尾气收集,电解温度控制在700℃,阴极电流密度控制在3a/cm2。
过滤后获得氯化亚铁溶液,采用氧化处理,采用盐酸控制盐酸浓度为50g/l,控制反应温度为150℃,加入氧化剂氧气,氧分压控制在4bar,将二价铁全部氧化成三价铁,返回硫化铅加压氧化浸出步骤循环使用。
在本实施例中,铅总回收率为98.5%,电流效率为93%,金属铅纯度为99.9%。
实施例2
参见图1所示的流程,将硫化铅进行加压氧化浸出,加入三氯化铁溶液,三氯化铁用量系数为1.8,控制反应温度为120℃,时间为2h。
反应后液进行浮选或过滤,滤渣为硫磺。
反应后液降温冷却,析出氯化铅固体,过滤洗涤并干燥。
氯化铅去熔盐电解,熔盐体系是nacl-kcl,阴极阳极通入直流电,阴极为钼,阳极为石墨棒,阴极析出液态铅,阳极析出氯气,氯气进行尾气收集,电解温度控制在900℃,阴极电流密度控制在8a/cm2。
过滤后获得氯化亚铁溶液,采用氧化处理,采用盐酸控制盐酸浓度为50g/l,控制反应温度为150℃,加入氧化剂氧气,氧分压控制在4bar,将二价铁全部氧化成三价铁,返回硫化铅加压氧化浸出步骤循环使用。
在本实施例中,铅总回收率为95.1%,电流效率为85%,
金属铅纯度为99.1%。
实施例3
与实施例1基本相同,唯一不同之处是采用氯化物处理硫化铅的反应温度为20℃。
在本实施例中,铅总回收率为87.2%,电流效率为91.1%,金属铅纯度为95.2%。
实施例4
与实施例1基本相同,唯一不同之处是采用氯化物处理硫化铅的反应时间为0.5h。
在本实施例中,铅总回收率为90.5%,电流效率为90.8%,金属铅纯度为96.3%。
实施例5
与实施例1基本相同,唯一不同之处是采用氯化物处理硫化铅的反应时间为5h。
在本实施例中,铅总回收率为99.0%,电流效率为94.6%,金属铅纯度为99.9%。
实施例6
与实施例1基本相同,唯一不同之处是熔盐体系是为nacl-kcl-cscl。
在本实施例中,铅总回收率为98.3%,电流效率为92%,金属铅纯度为99.9%。
实施例7
与实施例1基本相同,唯一不同之处是熔盐电解的温度为400℃,licl-nacl-kcl-cscl熔盐体系。
在本实施例中,铅总回收率为99.0%,电流效率为95%,金属铅纯度为99.0%。
实施例8
与实施例2基本相同,唯一不同之处是氧化处理反应温度为180℃。
在本实施例中,铅总回收率为96.5%,电流效率为88%,金属铅纯度为99.4%。
实施例9
与实施例2基本相同,唯一不同之处是氧化处理反应温度为20℃。
在本实施例中,铅总回收率为90.8%,电流效率为80.5%,金属铅纯度为98.2%。
实施例10
与实施例2基本相同,唯一不同之处是氧化处理的氧分压控制为2bar。
在本实施例中,铅总回收率为89.4%,电流效率为82.5%,金属铅纯度为96.6%。
实施例11
与实施例2基本相同,唯一不同之处是氧化处理的氧分压控制为10bar。
在本实施例中,铅总回收率为98.9%,电流效率为88.9%,金属铅纯度为99.9%。
对比例1
关于浸出条件
参见图1所示的流程,将硫化铅进行加压氧化浸出,加入三氯化铁溶液,三氯化铁用量系数为1~1.8,控制反应温度为20~150℃,反应时间为0.5~5h。
在本对比例中,分别进行了三氯化铁用量系数、反应温度及反应时间为上述数值范围端点值及端点值以外的实验,实验结果表明,浸出超过边界条件上限后,硫会被氧化成硫酸根,造成体系中硫酸根超标,铅会形成硫酸铅,造成损失。若低于下限时,反应率会不足,也就是硫化铅转变率不够,造成整体铅回收率不足。
对比例2
关于熔盐体系
在本对比例中,分别进行了不同熔盐体系的实验,包括licl-nacl、kcl-cscl-mgcl2和licl-nacl-cacl2等二元体系、三元体系,其对工艺过程影响甚微。
对比例3
基本与实施例1相同,不同之处在于,过滤后获得氯化亚铁溶液,采用氧化处理,采用盐酸控制盐酸浓度为50g/l,控制反应温度为150℃,加入氧化剂氧气,氧分压控制在4bar,将二价铁全部氧化成三价铁,返回硫化铅加压氧化浸出步骤循环使用。
基于上述条件,进一步研究以下问题:
(1)盐酸浓度不足问题
该反应为4fecl2+o2+4hcl=4fecl3+2h2o,可以看出,盐酸是消耗的,要参与氧化反应,盐酸不足(低于10g/l),则会造成二价铁直接被氧化为铁红(赤铁矿法除铁),造成铁损失。
(2)温度和氧气分压边界条件
温度和氧分压对于这个反应来讲,是越高越好,高的时候,各项工艺指标都要,但是过高主要考虑能耗问题。
若较低,反应率较低。如温度低于100℃,反应几乎发生很慢,80℃下采用氧气,铁氧化率仅仅有60%,采用空气(氧分压降低至1/5),铁氧化率不足30%。
从以上的描述中,可以看出,本发明上述的实施例实现了如下技术效果:
1)避免了火法造成的铅对空气的污染;
2)湿法处理硫化铅+氯化铅熔盐电解的组合工艺,提高了生产效率。
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!