海鲜产品检测试剂盒、其制备方法及应用与流程
本发明涉及一种试剂盒,特别涉及一种可应用于检测海鲜产品中食源性致病菌,例如副溶血性弧菌的试剂盒、其制备方法和应用,属于微生物检测领域。
背景技术:
副溶血性弧菌是常见的食源性致病菌之一,该菌主要来源于虾、鱼和贝类等海产品。据国家食源性疾病监测网报告,至1998年以来我国由副溶血性弧菌引起的食物中毒呈上升趋势,且超过沙门菌食物中毒而跃居首位,成为最严重的食源性病原菌。人类食用该菌感染的海产品可引发肠胃炎和败血症等肠胃疾病,是我国部分沿海地区的食物中毒案例中的首要病原菌。自1950年发现副溶血性弧菌至今,国内外检测该菌的方法仍以常规分离培养法为主。该法操作复杂、检测周期长(4-7d),已不能适应卫生应急检测的需要。因此它是必须的建立快速、灵敏的检测方法。
近年来,胶体金免疫层析技术以其操作简单、快速、准确、廉价等特点而得到迅速推广,成为基层快速筛查的重要手段。但胶体金试纸条的检测灵敏度相对不高(通常高于104CFU/mL),在检测低灵敏度要求的物质(欧盟规定副溶血性性弧菌不得检出)时,该方法的应用就受到限制。
技术实现要素:
鉴于现有技术的不足,本发明的主要目的在于提供一种具有灵敏度高、稳定性好的海鲜产品检测试剂盒、其制备方法及应用。
为实现前述发明目的,本发明采用的技术方案包括:
在本发明的一个实施方案之中提供了一种海鲜产品检测试剂盒,其包括:
试纸条,包括过滤垫、样本垫和检测垫,所述样本垫的边缘部分别与过滤垫和检测垫相互接触或重合,所述检测垫上分布有彼此不重合的检测线和质控线,所述检测线和质控线分别包含有第一抗体和第二抗体;
以及,免疫纳米银金核壳颗粒,包含接枝功能性高分子的纳米银金核壳纳米颗粒以及与所述功能性高分子共价结合的第三抗体,所述纳米银金核壳纳米颗粒包含纳米银核和包裹纳米银核的纳米金壳层;
其中,所述第一抗体仅在有目标物存在的情况下才能与目标物及第三抗体以夹心方式特异性结合,而所述第二抗体无论在有或无目标物存在的情况下均能与第三抗体特异性结合。
进一步的,所述目标物至少选自食源性致病菌,所述食源性致病菌包括副溶血性弧菌。
相应的,在一较为具体的实施方案之中提供了一种副溶血性弧菌检测试剂盒,其包括:
试纸条,包括过滤垫、样本垫和检测垫等,所述检测垫上分布有彼此不重合的检测线和质控线;
以及,免疫纳米银金核壳颗粒;
其中,所述检测线含有目标物免疫获得的捕获抗体,其仅在有目标物存在的情况下才能与目标物及免疫纳米银金核壳颗粒所含的目标物免疫的单抗以夹心方式特异性结合,而所述质控线含有无论在有或无目标物存在的情况下均能与所述目标物免疫的单抗特异性结合的二抗。
在一更为具体的实施案例之中,所述第一抗体为副溶血性弧菌免疫得到的兔多抗,所述第二抗体为驴抗鼠二抗,所述第三抗体为副溶血性弧菌免疫得到的鼠单抗。
在一些实施方案之中,所述试纸条包括依次设置的过滤垫、样本垫、检测垫和吸水垫,所述检测垫与吸水垫的边缘部相互接触或重合。
在一些实施方案之中,所述试纸条可基于PVC底板而形成,即,所述试纸条包含依次分布于PVC底板上的过滤垫、样本垫、检测垫和吸水垫(亦可称为吸水纸)。
其中,所述过滤垫用于过滤样品基质,消除基质干扰对实验结果的影响。
其中,所述样本垫用于对待检测样品和免疫银金核壳颗粒的传输以及对样品pH环境的调节。
其中,所述吸水纸用于吸收多余的免疫银金核壳颗粒以及未参加反应的液体样品。
其中,所述过滤垫、样本垫、检测垫和吸水垫可采用任何合适的材料。例如,所述过滤垫可采用聚酯膜,所述样品垫可采用玻璃纤维膜,而所述检测垫可采用硝酸纤维膜。
在一些实施方案之中,所述功能性高分子可选自一端具有巯基,另一端具有羧基的高分子,例如巯基化的PAA(聚丙烯酸)。
在一些尤为优选的实施案例之中,所述纳米银金核壳颗粒的粒径为15-200nm,其中Ag与Au的摩尔比为1-100:1。
在本发明的一个实施方案之中还提供了一种制备所述试剂盒的方法,其包括:
提供试纸条,包括:
至少取样本垫、检测垫、吸水垫依次设置,并使样本垫的边缘部与过滤垫及检测垫相互接触或重合,
将第一抗体和第二抗体分别施加至检测垫上,形成彼此不重合的检测线和质控线;
以及,提供免疫纳米银金核壳颗粒,包括:
制备银纳米粒子,
取所述银纳米粒子、柠檬酸钠及HAuCl4水溶液均匀混合反应,获得纳米银金核壳纳米颗粒,
以功能性高分子修饰所述纳米银金核壳纳米颗粒后,再与第三抗体充分混合反应,并以BSA或者酪蛋白封闭,之后除去未标记的第三抗体。
在一些更为具体的实施方案之中,所述制备方法可以包括:取HAuCl4水溶液在120-130℃恒温回流加热,待温度恒定后,加入银纳米粒子和柠檬酸钠溶液进行反应,获得纳米银金核壳颗粒。其中,通过调节HAuCl4和柠檬酸钠的添加量等可以得到不同粒径、不同金银含量的纳米银金核壳纳米颗粒。
在一实施案例中,可以取0.1w/v%HAuCl4水溶液在120-130℃恒温回流加热,待温度恒定后,加入银纳米粒子分散液和1w/v%柠檬酸钠溶液,其中HAuCl4水溶液、银纳米粒子分散液和柠檬酸钠溶液的体积比为25:10:1,反应30min,获得纳米银金核壳颗粒。
前述银纳米粒子可采用业界所知的任何合适方式制备。例如,在一实施案例之中,银纳米粒子的制备工艺可以包括:取柠檬酸三钠溶液和单宁酸溶液在240-250℃恒温回流加热,沸腾后加入AgNO3水溶液,当溶液颜色稳定后,停止加热,获得银纳米粒子。其中,通过调控单宁酸溶液的浓度等,可以调控所获银纳米粒子的粒径等。
在一些实施例之中,可以将所获纳米银金核壳纳米颗粒接枝功能性高分子并与副溶血性弧菌鼠单抗混合搅拌,用BSA或者酪蛋白封闭,离心除去未结合的抗体,用复溶液复溶,备用。
而对于前述试纸条,其也可以采用业界所知的任何合适方式制备,例如,可以将过滤垫、样本垫、检测垫、吸水垫依次粘贴在PVC底板上,并将第一抗体和第二抗体分别喷加到检测 垫上,形成检测线和和质控线。
在本发明的一个实施方案之中还提供了一种检测系统,其包括:
前述的任一种试剂盒,
以及,检测设备,用以监测在所述试纸条上施加待检样品与免疫纳米银金核壳颗粒的混合物前后,于所述试纸条的质控线和检测线处的信号变化情况,从而实现对待检样品中目标物的定性和/或定量判断。
其中,所述检测设备包括试纸条读取仪。
在一些实施方案之中,本发明提供了一种副溶血性弧菌检测系统,包括前述的副溶血性弧菌检测试剂盒以及试纸条读取仪。
在本发明的一个实施方案之中还提供了一种检测方法,其包括:
提供前述的任一种试剂盒,
将液态的待检样品与免疫纳米银金核壳颗粒混合后,再施加至所述试纸条上,
以及,以裸眼判读和/或试纸条读取仪检测作为检测手段,对样品内的目标物进行定性和/或定量判断。
在一些实施案例之中,所述检测方法具体可包括:将免疫纳米银金核壳颗粒与液态的待检样品充分混合后,再滴加到试纸条的样本垫上,经设定时间后,通过裸眼观察试纸条上检测线和质控线的颜色变化,定性分析待检样品中是否存在目标物,或者以试纸条读取仪记录T、C值和T/C值,并与预先建立的标准曲线对照,从而定量检测待检样品中目标物的含量。
显然的,前述标准曲线可通过业界悉知的方式建立,例如,可以通过下列方法获得,即:制备一系列不同浓度的目标物,例如食源性致病菌的标准样品,依照前述检测方法,分别获得和记录与不同浓度标准样品对应的T、C值和T/C值,并探知检测结果与样品浓度存在的数学关系,从而建立标准曲线。其中,T、C值分别为试纸条读取仪测得的检测线(T线)和和质控线(C线)的检测值,例如吸光度值等,这应是本领域技术人员依据常识及本说明书可很容易且明确的知悉的。
在一些实施案例之中,本发明提供了一种副溶血性弧菌检测方法,其包括:
提供前述任一种副溶血性弧菌检测试剂盒:
将所述免疫纳米银金核壳颗粒与待检样品混合,待反应完全后,将混合物加入试纸条加样孔,待混合物在试纸条上充分扩散后,则:
通过肉眼观察T、C线的颜色强度,从而实现对样品中是否存在副溶血性弧菌定性判断。
或者,通过试纸条读取仪记录T、C值和T/C值,并与标准曲线对照,定量判断待检测样品中副溶血性弧菌的含量。
在前述检测方法中,较为优选的,可以将免疫纳米银金核壳颗粒与待检物预先充分反应3-5min,而非将免疫纳米银金核壳颗粒喷在结合垫上与待检物瞬时反应,如此可有效提高试纸条的稳定性。
进一步的,该方法对副溶血性弧菌检测限为10CFU/mL。
需要说明的是,本发明的试剂盒、检测系统及检测方法所适用的检测对象还可包含大部分大分子物质,例如:细菌、毒素、病毒等。
与现有技术相比,本发明有益效果至少在于:
(1)本发明制备的试剂盒具有操作简单、检测时间短(10-15min)、适用于现场检测的优点;
(2)本发明为副溶血性弧菌高灵敏、快速检测提供了新的途径;
(3)本发明采用具有优异光学性质的纳米银金核壳颗粒作为标记物替代传统的胶体金制备试纸条,可大幅度提高试纸条的灵敏度(检测限可低至10CFU/mL);
(4)制备过程,本发明通过在标记物银金核壳纳米颗粒表面接枝功能化高分子,使抗体和标记物通过化学作用结合,可极大提高免疫标记物的稳定性,较之传统的免疫层析试纸条(标记物和抗体的主要是通过物理作用如静电吸附、疏水作用结合),其稳定保存时间从3天提高到2周以上,同时还可有效提高银金核壳纳米粒子上的抗体标记量(至少提高约20%);
(5)非常令人惊奇的是,本发明的试剂盒及检测方法在应用于检测海鲜产品时,表现出的检测效果(检测限约10CFU/mL)远远优于应用于检测传统食品(肉、蛋、蔬菜等)的效果(检测限约104CFU/mL)。
附图说明
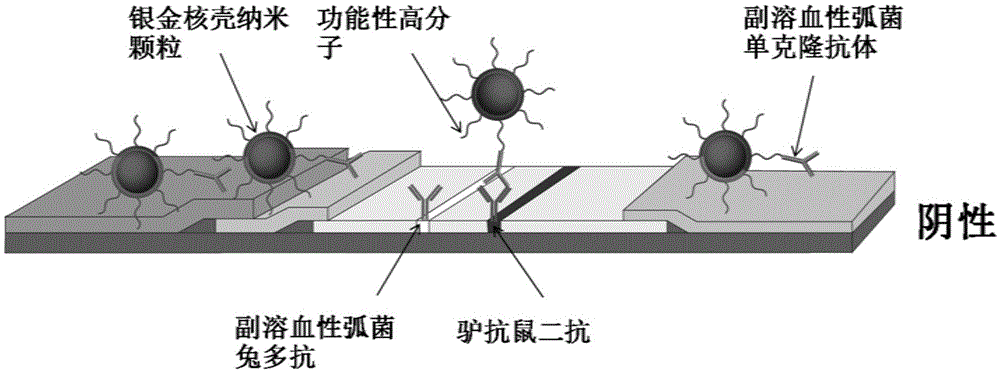
图1是本发明一典型实施方案之中使用纳米银金核壳颗粒免疫层析试纸条检测阴性样本的示意图;
图2是本发明一典型实施方案之中使用纳米银金核壳颗粒免疫层析试纸条检测阳性样本的示意图。
图3是本发明一典型实施例之中制备的纳米银金核壳颗粒的透射电镜图。
具体实施方式
如前所述,鉴于现有技术的诸多缺陷,本案发明人经大量研究和实践,发现采用银金核壳纳米粒子作为标记物,特别是采用枝接有功能性高分子的银金核壳纳米粒子共价标记抗体而与免疫层析试纸条构建检测试剂盒,可有效提高检测灵敏度和稳定性。尤其出乎意料的是,若由此构建应用于检测海鲜产品的试剂盒,特别是对于海鲜产品中食源性致病菌(尤其是副溶血性弧菌),其检测的效果还更为显著。
基于前述发现,本案发明人得以提出本发明的技术方案,其如前文所述,此处不再赘述。
例如,在本发明的一典型实施案例中,本发明可通过如下技术方案实现:
(1)制备具有不同金银含量的纳米银金核壳颗粒:该实验主要有2个步骤:
第一,银纳米粒子的合成:取合适浓度的,例如100mL 5mM柠檬酸三钠溶液和0.1mM单宁酸溶液在240-250℃恒温回流加热,沸腾后加入合适浓度的,例如1mL 25mM AgNO3水溶液,当溶液颜色稳定后,继续搅拌2-3min,停止加热,避光冷却至室温。
第二,纳米银金核壳颗粒的合成:取合适浓度的,例如100mL 10mg的HAuCl4水溶液在120-130℃恒温回流加热,一定时间后,例如10-15min,加入一定量的,例如4mL制备好的银纳米粒子和400uL 1%(w/v)柠檬酸钠溶液,一定时间后,例如30min停止加热,冷却至室温。调控单宁酸溶液的浓度以及HAuCl4和柠檬酸钠的添加量的可以得到不同金银含量的纳米银金核壳颗粒。
(2)纳米银金核壳颗粒的标记
取一定量的,例如5mL纳米银金核壳颗粒溶液,离心2次,加入等体积超纯水复溶,加入一定量的功能性高分子溶液,例如:2mL巯基化PAA对纳米银金核壳表面进行羧基化,调节pH值,加入一定量的,例如0.5mL副溶血性弧菌免疫的鼠单抗,搅拌30min,加入0.5mL 5%-10%BSA或者酪蛋白封闭30min,8000rpm离心30min,去上清,加入一定量的,例如0.5mL复溶液复溶,得到免疫银金核壳纳米颗粒,4℃保存备用。
(3)免疫层析试纸条的制备:将样本垫以一定的处理液,例如pH 8.50.1M PBS缓冲液(0.5%BSA,0.5%Tween-20)处理,置于60℃鼓风干燥箱,3h后取出置于干燥缸中备用;将副溶血性弧菌免疫的兔多抗和驴抗鼠二抗按一定的浓度和喷量,例如浓度均为1.0-1.5mg/mL,喷量均为0.75uL/cm喷到检测垫(一般为硝酸纤维膜)上分别作为检测线(T线)和质控线(C线),30℃真空干燥过夜。按一定顺序将样品垫、结合垫、NC膜、吸水纸组装好后切成4mm宽带条,置于锡箔袋中加干燥剂并密封,置于干燥皿中保存备用。
(4)试纸条对样品的检测:取一定量的,例如4-6uL制备好的免疫银金核壳纳米颗粒滴加到ELISA板孔中,将一定量的,例如100μL稀释好的不同浓度梯度的副溶血性弧菌菌液加入含有免疫银金核壳纳米颗粒的ELISA板孔,孵育一定的时间,例如3-5min后,取出混合物滴加到试纸条的样品孔中,反应一定时间,例如10-15min后用肉眼观察试纸条T、C线的颜色变化,并用试纸条读取仪记录T、C值和T/C的值。
(5)检测结果的判定:本研究以纳米银金核壳颗粒为标记,结合免疫层析技术,建立纳米银金核壳免疫层析试纸条。在该试纸条检测垫分别喷有副溶血性弧菌免疫的兔多抗和驴抗鼠二抗作为检测线和质控线,由于检测对象为大分子,该研究检测原理以双抗夹心为模型,如果样品中含有一定浓度的目标物时,该目标物就会首先与免疫纳米银金核壳颗粒结合形成纳米银金核壳颗粒-抗体-抗原复合物,该复合物流经NC膜会被检测线处喷的兔多抗捕获,形成一条肉眼可见的条带或者试纸条读取仪可以检测的信号,判断其为阳性(参阅图1),如果样品中不含待检物,免疫纳米银金核壳颗粒就不与检测线处喷的兔多抗结合,检测线不显色,判断其为阴性(参阅图2)。无论目标物存在与否,免疫纳米银金核壳颗粒都与试纸条质控线处喷的驴抗鼠二抗结合,并在该区域形成一条肉眼可见的条带。
以下结合若干较佳实施例对本发明的技术方案作进一步的解释说明,但其中的实验条件和设定参数不应视为对本发明基本技术方案的局限。并且本发明的保护范围不限于下述的实施例。
实施例1:纳米银金核壳颗粒免疫层析系统对虾肉中副溶血性弧菌的检测
(1)纳米银金核壳颗粒的制备:该实验主要有2个步骤,第一,银纳米粒子的合成:取100mL 5mM柠檬酸三钠溶液和0.1mM单宁酸溶液在240-250℃恒温回流加热,沸腾后加入1mL 25mM AgNO3水溶液,当溶液颜色稳定后,继续搅拌3min,停止加热,避光冷却至室温。第二,纳米银金核壳颗粒的合成:取100mL 10mg的HAuCl4水溶液在120-130℃恒温回流加热,10min后,加入4mL制备好的银纳米粒子和400uL 1%(w/v)柠檬酸钠溶液,反应30min后停止加热,冷却至室温,如图3所示。
(2)纳米银金核壳颗粒的标记:取5mL纳米银金核壳颗粒溶液,离心2次,加入等体积超纯水复溶,加入一定量的功能性高分子溶液,例如:2mL巯基化PAA对纳米银金核壳表面进行羧基化,调节pH到7-8,加入0.5mL副溶血性弧菌免疫的鼠单抗,搅拌30min,加入0.5mL 10%BSA封闭30min,8000rpm离心30min,去上清,加入0.5mL复溶液复溶,得到免疫银金核壳纳米颗粒,4℃保存备用。
(3)取50g副溶血性弧菌阴性虾肉,以无菌操作剪碎并匀浆,加入50mL灭菌的6%氯化钠蛋白胨水稀释作为样本基质,接种一定量的副溶血性弧菌(105、104、103、102、101CFU/mL)到该基质中。
(4)免疫层析试纸条的制备:将样本垫用pH 8.50.1M PBS缓冲液(0.5%BSA,0.5%Tween-20)处理,置于60℃鼓风干燥箱,3h后取出置于干燥缸中备用;将副溶血性弧菌兔多抗和驴抗鼠二抗喷到硝酸纤维膜上分别作为检测线和质控线,浓度均为1.0-1.5mg/mL,喷量均为0.75uL/cm,30℃真空干燥过夜取出置于干燥缸中备用;将过滤垫、样本垫、检测垫、吸水纸依次粘贴在PVC底板上,贴好后将其切成4mm宽的试纸条,装卡。将制备好的试纸条装入铝箔袋中,加干燥剂密封,置于干燥缸中保存备用。
(5)试纸条对样本检测:取4uL制备好的免疫银金核壳纳米颗粒滴加到ELISA板孔中,将100μL浓度为105、104、103、102、101CFU/mL的副溶血性弧菌样液加入含有免疫银金核壳纳米颗粒的ELISA板孔,孵育3min后,取出混合物滴加到试纸条的样品孔中,反应10min后,用肉眼观察试纸条T、C线的颜色变化,并用试纸条读取仪记录T、C值和T/C的值,以副溶血性弧菌的浓度为横坐标,以T/C值为纵坐标绘制标准曲线。
(6)参考所做的标准曲线图,对虾肉样品中副溶血性弧菌的含量进行确证。定量检验副溶血性弧菌的浓度范围在101~105CFU/mL。
实施例2:纳米银金核壳颗粒免疫层析系统对鱼中副溶血性弧菌的检测
(1)纳米银金核壳颗粒的制备:该实验主要有2个步骤,第一,银纳米粒子的合成:取100mL 5mM柠檬酸三钠溶液和0.1mM单宁酸溶液在240-250℃恒温回流加热,沸腾后加入1mL 25mM AgNO3水溶液,当溶液颜色稳定后,继续搅拌3min,停止加热,避光冷却至室温。第二,第二,纳米银金核壳颗粒的合成:取100mL 10mg的HAuCl4水溶液在120-130℃恒温回流加热,10min后,加入4mL制备好的银纳米粒子和400uL 1%(w/v)柠檬酸钠溶液,反应30min后停止加热,冷却至室温。
(2)纳米银金核壳颗粒的标记:取5mL纳米银金核壳颗粒溶液,离心2次,加入等体积超纯水复溶,加入一定量的功能性高分子溶液,例如:2mL巯基化PAA对纳米银金核壳表面进行羧基化,调节pH到7-8,加入0.5mL副溶血性弧菌免疫的鼠单抗,搅拌30min,加入0.5mL 10%BSA封闭30min,8000rpm离心30min,去上清,加入0.5mL复溶液复溶,得到免疫银金核壳纳米颗粒,4℃保存备用。
(3)取50g副溶血性弧菌阴性鱼表皮肤、腮、内脏等,以无菌操作剪碎并匀浆,加入 50mL灭菌的6%氯化钠蛋白胨水稀释作为样本基质,接种一定量的副溶血性弧菌(105、104、103、102、101CFU/mL)到该基质中。
(4)免疫层析试纸条的制备:将样本垫用pH 8.50.1M PBS缓冲液(0.5%BSA,0.5%Tween-20)处理,置于60℃鼓风干燥箱,3h后取出置于干燥缸中备用;将副溶血性弧菌兔多抗和驴抗鼠二抗喷到硝酸纤维膜上分别作为检测线和质控线,浓度均为1.0-1.5mg/mL,喷量均为0.75uL/cm,30℃真空干燥过夜取出置于干燥缸中备用;将过滤垫、样本垫、检测垫、吸水纸依次粘贴在PVC底板上,贴好后将其切成4mm宽的试纸条,装卡。将制备好的试纸条装入铝箔袋中,加干燥剂密封,置于干燥缸中保存备用。
(5)试纸条对样本检测:取4uL制备好的免疫银金核壳纳米颗粒滴加到ELISA板孔中,将100μL浓度为105、104、103、102、101CFU/mL的副溶血性弧菌样液加入含有免疫银金核壳纳米颗粒的ELISA板孔,孵育3min后,取出混合物滴加到试纸条的样品孔中,反应10min后,用肉眼观察试纸条T、C线的颜色变化,并用试纸条读取仪记录T、C值和T/C的值,以副溶血性弧菌的浓度为横坐标,以T/C值为纵坐标绘制标准曲线。
(6)参考所做的标准曲线图,对鱼样品中副溶血性弧菌的含量进行确证。定量检验副溶血性弧菌的浓度范围在101~105CFU/mL。
很显然,利用本发明的检测试剂盒,可大幅度的提高海鲜产品中食源性致病菌,特别是副溶血性弧菌的检测限,增加检测范围(101~105CFU/mL),实现高灵敏度的定量检测,且操作简单、检测时间短、适宜于现场检测。
应当指出,以上所述本发明的具体实施方式,并不构成对本发明保护范围的限定。任何根据本发明的技术构思所作出的各种其他相应的改变与变形,均应包含在本发明权利要求的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!