一种抗干扰能力强的肌酐苦味酸法检测试剂盒的制作方法
本发明涉及肌酐检测技术领域,特别涉及一种抗干扰能力强的肌酐检测试剂盒。
背景技术:
肌酐是肌肉中的磷酸肌酸发生不可逆转化而形成。血清肌酐(CREA)是临床中常用的检测项目,也是急诊肾功能检测项目之一。血清肌酐值是评价肾小球滤过率(GFR)及诊断急性、慢性肾功能衰竭的有效指标。肌酐易溶于水(80.1g/L,16℃)。正常情况下,人体内肌酐的含量基本稳定,一般维持在3~14mg/L。当肌酐含量高于正常范围时,通过肾小球滤过,随尿液排出体外,不被肾小球重吸收。当肾脏机能受损时,肌酐的正常排泄受到阻碍,致使血清中肌酐含量增加,血清中肌酐含量升高意味着肾功能受到损害,因此血清肌酐是肾脏功能的重要指标。肾病在我国乃至世界上的发病率居于前10位。调查数据显示,我国隐形肾病患者约占人口的25%,因此肌酐水平的测定对肾脏疾病具有重要的临床意义。
肌酐常用的检测方法有Jaffé反应法、酶法、毛细管电泳法、高效液相色谱法等。
1.Jaffé反应
Jaffé在1886年发现肌酐和苦味酸在碱性环境中反应时,可生成一种红色物质。Greenwald第一个系统地研究了Jaffé反应的化学过程,认为Jaffé反应的红色产物是肌酐与苦味酸之间生成1∶1和1∶2的络合物。一些肌酐的同系物或衍生物如胍基乙酸内酰胺(glycocyamidine),5-甲基胍基乙酸内酰胺以及乙酰乙酸、丙酮酸、胆红素、乙内酰脲等物质均能和苦味酸发生反应,这些物质称为“假肌酐”,可导致肌酐测定结果不准确。
2.酶法
酶法测定肌酐主要是利用肌酐酶催化肌酐水解生成肌酸及其逆反应。肌氨酸氧化酶法灵敏度高,线性范围宽,试剂稳定性好。对多种可能的干扰物的实验表明,胆红素、乳糜、抗坏血酸、溶血以及常用药物均不干扰此方法,且其线性范围上限达1760μmol/L,但该法的主要缺点是试剂不够稳定,且肌酐酶不易得到,使得试剂盒价格昂贵。
3.毛细管电泳法
毛细管电泳法具有以下特点:分离效率高,分析速度快,样品用量少,自动化程度高。缺点:残留的少量蛋白质会吸附在毛细管内壁上导致检测结果的重复性差。
4.高效液相色谱法
高效液相色谱法与传统方法相比,准确度高,因为样品经过除蛋白处理,同时由于液相色谱柱的高分离性能,使得肌酐测定中的干扰大大减少。缺点:分析成本高,液相色谱仪价格及日常维护费用贵,分析时间长。
技术实现要素:
针对于现有技术存在的问题,本发明在苦味酸法的基础上,优化反应体系,添加多种抗干扰物质和稳定剂,显著改善了试剂的抗干扰能力。提供了一种抗干扰能力强的肌酐(CREA)苦味酸法检测试剂盒。
本发明一种抗干扰能力强的肌酐苦味酸法检测试剂盒,包括试剂R1和试剂R2,所述试剂R1和试剂R2的组成如下:
R1:
R2:
苦味酸 17.2mmol/L
曲拉通-100 2ml/L。
一种抗干扰能力强的肌酐苦味酸法检测试剂盒,其特征在于,所述试剂R1和试剂R2在使用时的比例为R1:R2=200:100。
种抗干扰能力强的肌酐苦味酸法检测试剂盒,其特征在于所述防腐剂为NaN3和二乙胺。
所述的肌酐检测试剂来检测肌酐的检测方法,其特征在于使用全自动生化分析仪利用速率法进行测定,检测主波长为505nm。
本发明的基本原理如下:
肌酐和苦味酸在碱性环境中反应时,可生成一种红色物质,红色产物是肌酐与苦味酸之间生成1∶1和1∶2的络合物。该方法容易受高胆红素负干扰而致结果明显偏低,甚至出现负值,先通过高铁氰化钾和次氯酸钠对胆红素进行氧化,并通过2,4-二硝基苯肼消除α-酮戊二酸干扰,然后加入苦味酸试剂,碱性条件下,苦味酸与肌酐形成络合物而显红色。
本发明的有益效果是:
(1)本发明选择使用了铁氰化钾和次氯酸钠作为氧化剂,使胆红素对肌酐检测的影响降到最低;
(2)本发明使用了2,4-二硝基苯肼,2,4-二硝基苯肼在碱性条件下能够结合α-酮戊二酸和丙酮酸,降低其对肌酐检测的正干扰;
(3)本发明使用了二乙胺和叠氮钠作为稳定剂,提高了试剂的稳定性。
附图说明
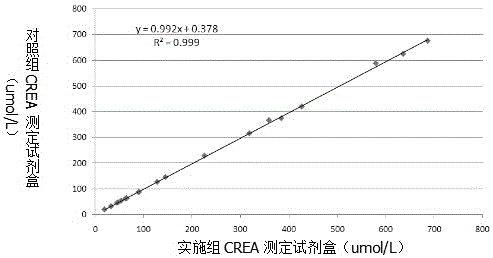
图1为两种试剂的相关性曲线图;
图2为两种试剂有效期稳定性曲线图。
具体实施方式
下面结合具体实施例对本发明进行进一步说明:
实施例1
一种抗干扰能力强的肌酐苦味酸法检测试剂盒,包括试剂R1和试剂R2:
1)其R1的组成为:
2)试剂R2的组分为:
苦味酸 17.2mmol/L
曲拉通-100 2ml/L。
3)本实施例试剂的使用方法:
本实施例描述的肌酐检测试剂,在使用时采用具有双试剂功能的全自动生化分析仪,如日立7180全自动分析仪等,利用终点法进行测定。将R1和R2按照3:1的比例放置到对应的试剂位上,在样品盘的对应位置放置好蒸馏水、标准品和样本,操作如表1。
表1实施例1试剂检测方法
肌酐的含量(μmol/L)=(ΔA测定/min÷ΔA标准/min)×C标准。
实施例2
干扰性试验:取新鲜混合血清,分成2等份,然后将每等份再分成5等份,加入不同的干扰物质,使其在血清中的浓度达到表2的要求。然后分别用实施例1所得试剂,与市场常见并认可的肌酐检测试剂同时对比测定血清中肌酐的含量,对照组测定结果与加入不同干扰物质后各组的测定结果见表2。相对偏差(%)=(干扰样本的测定均值-对照样本的测定均值)/对照样本的测定均值×100%。
表2实施例试剂抗干扰性能比较
由表2可以看出,实施例1试剂在抗坏血酸≤1704μmol/L、α酮戊二酸20mmol/L、胆红素≤684μmol/L、血红蛋白≤10g/L、甘油三酯≤22.6mmol/L对测试结果没有明显干扰。而对照组试剂在上述浓度干扰物质存在时,受到明显干扰,这说明实施例1试剂的抗干扰性能远远优于对比试剂。
实施例3
相关性实验
利用实施例1配方配制试剂,与市场常见的国家食品药品监督管理局认可的某公司的肌酐试剂盒进行对照检测,同时检测了20个临床血清样本,检测结果如表3所示。并获得了两种试剂的相关性曲线(如图1所示),通过检测结果显示,两个试剂盒的相关系数为0.999,说明了两者有极大的相关性。
表3实施例1试剂与市场常见并得到认可的肌酐测定试剂盒对比检测结果
试验所用校准品和质控品分别为:
校准品:朗道复合标准(926UN),其中CREA的含量为133μmol/L。
质控品:朗道复合质控(952UN)其中CREA的靶值为121μmol/L,靶
值范围:96.7-145μmol/L。
实施例4
试剂稳定性验证试验的具体操作方法:
将本发明实施例1-3中所得检测试剂作为试验组,取一种市售肌酐苦味酸法检测试剂盒(品牌:武汉利弘,产品批号:20150415)作为对照组,试验组与对照组试剂每组各自取相同的两份,一份做15天开瓶稳定性试验,将试剂开瓶放置在仪器的2-8℃冷藏箱中(15天不取出),作为15天开瓶稳定性检测;另一份做37℃热稳定性检测试验,封闭放置在37℃恒温水浴锅中(每天仅在检测的时候取出,检测完毕后,依然封口放回37℃水浴锅中,连续7天),作为7天37℃热稳定性验证。将试剂同时在日立7180全自动生化分析仪器上,按照如下表1方法进行检测,并在仪器上建立标准曲线。取朗道的冻干粉质控品,溶解均匀后,各自平均分成15份,-20℃储存,每天取值质控各取一个,并且跟踪检测结果,其跟踪监测趋势如图2。
- 还没有人留言评论。精彩留言会获得点赞!