一种基于抑制COX-2活性的中药组合物检测方法与流程
本发明涉及中药组合物的生物检测方法,属于医药领域。
背景技术:
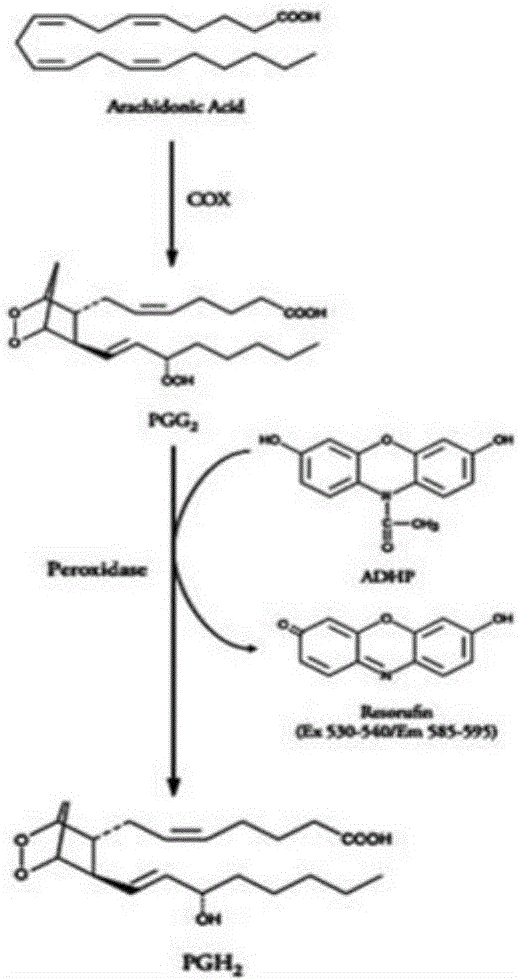
:目前,中药复方的质量评价仅通过测定单一化学成分来进行,首先,该化学成分是否是复方发挥药效的物质,第二,控制该化学成分的最低含量是否能有效控制其质量的有效性和一致性?从目前的研究来看,仅通过测定单一化学成分对中药复方进行质量评价显然是不行的。因此,如何根据中药复方的具体情况,结合现代科学技术,探索能够符合中医药特点,在一定程度上既关联临床疗效又关联作用机制,具有可操作性的中药复方制剂质量评控方法,保证中药复方临床疗效的一致性和稳定性,是中药研究领域中最重要的课题之一。生物活性测定指导原则已被《中国药典》收录,并在水蛭等药材的质量控制中采用了生物评价的方法;美国fda在《植物药研发行业指南》中也明确提出生物评价将作为植物药注册评审的主要内容。可见,生物评价已成为中药及中药复方制剂品质评价的发展方向。对于中药而言,临床应用绝大多数为中药复方,很少存在单一药味使用的情况,其复杂的成分以及多样的药理作用都决定了检测一种或几种活性成分并不能体现其整体药效,仅通过这一标准评价中药是行不通的。将生物评价方法引入中药质量控制体系不仅仅可以鉴定品种,评价质量,还可以与其药效相挂钩,并且观察其毒副作用。在某种程度上来说,利用生物评价方法检测中药的质量较传统化学方法存在着明显的优越性。其中对于中药大复方的分析更能体现其优势。技术实现要素:针对现有技术存在的不足,本发明提供一种中药组合物的生物检测方法,相对于现有技术仅检测一种或几种活性成分的检测方法,本发明的生物检测方法能更全面的表征中药组合物的整体药效,从而控制其质量。一种中药组合物的检测方法,该方法包括:将中药组合物制备为可检测的样品,与环氧化酶(cox)接触,测定样品对环氧化酶(cox)的抑制率。在具体的实施方式中,所述检测方法包括如下步骤:a)制备中药组合物样品溶液和/或对照品溶液;b)测定样品溶液和对照品溶液对cox-2酶活力的抑制率;c)以cox-2酶活力抑制率为指标,计算效价和可信限率;其中,步骤b测定样品溶液和对照品溶液对cox-2酶活力的抑制率可采用酶免疫法等进行测定。作为优选的实施方式,可按如下方法测定抑制率:a)向待测溶液中加入cox-2酶,培养一定时间;b)向待测溶液中加入adhp和aa;c)显色,检测荧光强度;d)按如下公式计算抑制率,抑制率%=(初始活性样品的荧光强度-待测样品的荧光强度)/初始活性样品的荧光强度×100%。优选的,步骤a中cox-2酶用量为500u/ml~1000u/ml;优选的,步骤b中aa经过纯化;优选的,步骤c中荧光强度在激发光波长530-540nm,发射波长585-595nm下检测。在具体的实施方式中,步骤a中所述对照品选自常规抗炎药物,如塞来昔布、罗非昔布(refocoxib),或可用于作为对照品的本发明中药组合物。所述对照品溶液的制备方法包括:取对照品,加有机溶剂提取,提取液即为对照品溶液;优选的,所述对照品溶液浓度为1×105u/ml~2×105u/ml;更优选的,所述对照品溶液浓度为1.2×105u/ml。步骤a中所述中药组合物样品溶液的制备方法包括:取中药组合物,加有机溶剂提取,提取液即为对照品溶液;优选的,所述样品溶液浓度为1×105u/ml~2×105u/ml;更优选的,所述样品溶液浓度为1.2×105u/ml。其中,所述有机溶剂选自二甲基亚砜(dmso)、甲醇、乙醇等;所述提取方法选自超声提取、回流提取、微波提取中的任意一种。步骤c所述“效价”和“可信限率”按《药品生物检定》(周海钧主编)中“质反应平行线法”计算;抑制cox-2酶活力的效价不得低于500u·μg-1,平均可信限率小于25%。本发明所述中药组合物由如下原料药组成:连翘200-300重量份、金银花200-300重量份、炙麻黄50-100重量份、炒苦杏仁50-100重量份、石膏200-300重量份、板蓝根200-300重量份、绵马贯众200-300重量份、鱼腥草200-300重量份、广藿香50-100重量份、大黄30-80重量份、红景天50-100重量份、薄荷脑5-10重量份、甘草50-100重量份。优选的,所述中药组合物由如下原料药组成:连翘210-270重量份、金银花210-270重量份、炙麻黄60-90重量份、炒苦杏仁60-90重量份、石膏210-270重量份、板蓝根210-270重量份、绵马贯众210-270重量份、鱼腥草210-270重量份、广藿香60-90重量份、大黄40-60重量份、红景天60-90重量份、薄荷脑6-8重量份、甘草60-90重量份。更有选的,所述中药组合物由如下原料药组成:连翘255重量份、金银花255重量份、炙麻黄85重量份、炒苦杏仁85重量份、石膏255重量份、板蓝根255重量份、绵马贯众255重量份、鱼腥草255重量份、广藿香85重量份、大黄51重量份、红景天85重量份、薄荷脑7.5重量份、甘草85重量份。所述中药组合物的制备方法:以上十三味,广藿香加水蒸馏提取物挥发油,收集挥发油,水提取液滤过,备用;连翘、炙麻黄、鱼腥草、大黄用70%乙醇提取二次,第一次2小时,第二次1.5小时,提取液滤过,合并,回收乙醇,备用;金银花、石膏、板蓝根、绵马贯众、甘草、红景天加水煎煮至沸,加入炒苦杏仁,煎煮二次,第一次1.5小时,第二次1小时,煎液滤过,滤液合并,加入广藿香提油后备用的水溶液,浓缩至相对浓度为1.10~1.15(60℃),加乙醇使含醇量达70%,在4℃冷藏24小时,滤过,滤液回收乙醇,与上述连翘等四味的备用醇提取液合并,浓缩至相对密度为1.10~1.15(60℃),喷雾干燥,与适量淀粉混匀,制成颗粒,干燥,过筛,筛出适量细粉,将薄荷脑、广藿香挥发油用适量乙醇溶解,喷入细粉中,混匀,与上述颗粒混匀,密闭30分钟,装入胶囊,制成1000粒,即得。本发明检测方法的原理是基于荧光法,在cox-2作用下,花生四烯酸(aa)转变为前列腺素环内过氧化物(pgg2),催化产生的pgg2和adhp(10-acetyl-3,7-dihydroxyphenoxazine)之间发生反应生成荧光物质试卤灵。在特定波长下产生荧光,通过检测试卤灵的荧光强度,即可体现cox-2酶活力的大小,进而评价待测药物抑制cox-2的活性(见图1)。本发明的有益效果:1、本发明基于网络药理学的预测、转录组学的验证和整体动物代谢组学的分析,确立了cox-2为抗炎生物活性指标建立中药组合物的质量生物活性评价方法;2、本发明以cox-2酶活力为指标,评价了中药组合物对cox-2酶活力的抑制作用,建立了一种结合临床适应症的酶水平的抗炎生物评价方法,经过方法学考察,该生物评价方法精密度较高,重复性较好,rsd值控制在10%以内,较细胞水平的抗炎生物效价方法更稳定;3、应用该方法对中药组合物进行生物活性评价,发现其批次间抑制cox-2的生物效价也存在一定的差异,从40个批次市售样品来看,其生物效价范围在510u/μg~1413u/μg之间,平均生物效价为856u/μg。实验室自制的破坏性样品抑制cox-2酶活力的生物效价较正常合格样品明显降低,提示该方法也可以区分不同质量的样品;4、本发明方法弥补化学单一指标质量评价方法的不足,为该中药组合物制剂提供更有证据力的检测方法;5、本发明方法不仅可以应用于本发明所述中药组合物的质量评价,也可以用于其他具有抗炎活性的中药及中药复方的质量评价,具有普适性。附图说明图1为cox-2活性检测原理;图2为不同浓度中药组合物对cox-2酶活力的抑制作用实验例1中药组合物对h1n1流感病毒感染小鼠的保护作用及生物评价指标的验证1.实验材料1.1实验仪器leicadm3000倒置显微镜(德国leica公司);d3024r台式高速冷冻型微量离心机(dragonlab);sigmaj-26冷冻离心机(德国sigma公司);al201电子天平(梅特勒-托利多仪器(上海)有限公司);rm2245电控进样的手动轮转切片机、eg1150h分体式石蜡包埋机(德国leica公司);s1000thermalcyclerpcr仪(bio-rad公司);jy-1000m型电热恒温鼓风干燥箱(吴江市志胜烘箱设备厂);steponeplus荧光定量pcr仪(美国abi公司);sw-cj-1fd超净工作台(苏净安泰公司);nanodrop2000超微量分光光度计(美国thermo公司)。1.2药物与试剂中药组合物胶囊剂(实施例1制备);pbs购于gibco公司;4%多聚甲醛溶液购于gbcbio公司;二甲苯购于广州化学试剂厂;苏木素染料、伊红染料购于珠海贝索生物技术有限公司;il-6、cox-2、gapdh引物购于美国life公司;trizolreagent购于life公司(批号15596-026),depc处理水购于solarbio(批号r1600);cdnasynthesissupermix购于novoprotein公司(批号e044-01b);三氯甲烷、异丙醇、无水乙醇购于国药集团化学试剂有限公司(批号10006818、80109218、10009218);第一链cdna合成试剂盒购于美国thermo公司(批号#k1622);faststartuniversalsybrgreenmaster(rox)购于美国roche公司(批号04913914001)。1.3动物balb/c小鼠,雌性,6-8周龄,清洁级,体重18-20g,广东省实验动物中心,合格证号:[scxk(粤)2003-0002]。ivc笼具饲养,自由饮水取食,室温25±2℃,湿度60-70%,设置12小时的室内明/暗循环,以标准食物和水饲养,保持笼具、餐具及环境的清洁卫生,保持室内安静。所有动物在实验前预先适应性饲养7天,实验中所有小鼠都受到精心照顾。获得动物实验伦理委员会批准。1.4病毒与细胞株甲1型流感病毒pr8株(a/pr/8/34,h1n1),购自美国经典培养物收藏中心(atcc)。使用时接种9-11日龄鸡胚尿囊腔,37℃培养3天,收集尿囊液备用(血凝测效价)。按照reed-muench的方法在小鼠测定ld50(50%致死剂量)。mdck(madindarbycaninekidney,狗肾细胞)细胞购自中国科学院协和细胞库。2.实验方法2.1测定小鼠感染病毒的半数致死量(ld50)balb/c小鼠50只,6-8周龄,雌性,随机平均分成5组,用灭菌pbs进行10倍系列稀释病毒(a/pr/8/34,h1n1)为10-2,10-3,10-4,10-5,10-6共5个稀释度。小鼠经乙醚轻度麻醉后,以滴鼻途径感染小鼠,每只小鼠感染50μl,观察15天,记录不同稀释度的病毒液感染小鼠的存活及死亡情况。按照reed-muench的方法计算病毒对小鼠的半数致死量ld50。2.2动物实验分组及给药将小鼠随机分成5组,每组15只。分别为正常组(normal),模型组(model),奥司他韦组(oseltamivir)(60mg/kg/day),中药组合物给药高剂量组(1300mg/kg/day)、低剂量组(650mg/kg/day)。小鼠浅度呼吸麻醉,模型组用2个ld50的h1n1病毒稀释液,以滴鼻途径感染,每只小鼠50μl;空白组同法滴入无菌pbs。感染当天于感染前2小时给药,连续给药5天。奥司他韦组和中药组合物高、低剂量组每只灌胃给药0.2ml,每天2次,间隔8小时给药,空白组和模型组同法服用生理盐水。2.3肺组织中il-6和cox-2mrna表达的测定2.3.1肺组织中总rna的提取称取各组小鼠肺组织100mg,加入trizol1ml,15000rpm,每次10s进行三次匀浆。匀浆完成按trizol法提取rna。rna纯度od260/od280在1.8~2.0之间。用于后续实验。2.3.2pcr反应体系和程序pcr反应体系:primer1μl,10×dntp2μl,ri1μl,rt1μl,reactionbuffer4μl;调整至相同浓度的templaterna和depc水共11μl。total20μl。逆转录成cdna,反应条件:25℃5min,42℃60min,70℃5min。pcr反应程序:逆转录完成后,用depc水稀释5倍。每孔加入样本1μl,预混液9μl(sybrgreen4μl,f1μl,r1μl,depc水3μl),覆膜,离心后上机检测。检测程序:预变性95℃10min,循环40次95℃15s→60℃60s,溶解曲线75℃→95℃,每20s升温1℃。pcr引物序列见表1。表1pcr引物序列genefril-6gctaccaaactggatataatcaggaccaggtagctatggtactccagaacox-2ccctgctggtggaaaagcctggtcctactgtagggttaatgtcatctaggapdhgtcctcagtgtagcccaagatcaatgtgtccgtcgtggatct2.4统计学分析graphpadprism6.0和originpro9.2软件处理,t检验进行统计学分析,p<0.05为有统计学意义。以gapdh为内参,采用2-△△ct法进行相对基因表达分析。3.实验结果实验于各感染给药后第5天收集各组小鼠肺组织样本,提取肺组织中il-6、cox-2rna后进行实时定量pcr检测。结果如表2所示,中药组合物高、低剂量组对il-6和cox-2mrna的表达有显著的抑制作用(p<0.01,p<0.05),且具有量-效关系。表2中药组合物对小鼠肺组织中il-6、cox-2mrna表达的影响*p<0.05,**p<0.01与model比较以上结果表明,正常组小鼠精神状态良好,行动较敏捷,毛发较光泽,呼吸较均匀,体重增长。模型组小鼠于感染第二天后,呼吸不均匀,蜷缩,毛耸无光泽,饮食明显减少,消瘦。说明该h1n1流感病毒小鼠模型是成功的。病毒感染后,小鼠体重开始下降,给予奥司他韦阳性药和中药组合物均可减轻小鼠体重降低的幅度。小鼠肺脏病毒载量、肺指数数据及肺组织病理切片也表明,中药组合物可有效的抑制流感病毒在小鼠体内的复制,具有明显的抵抗流感病毒致肺炎的作用。采用实时定量pcr技术,测定了小鼠肺组织中il-6和cox-2的mrna表达,发现中药组合物可显著降低肺组织中两种基因的表达,并具有剂量依赖关系,从整体动物水平验证了中药组合物抗炎生物评价指标选择il-6和cox-2的可靠性。实验例2基于抑制cox-2活性的中药组合物生物检测方法基于实验例1的研究结果,确定cox-2与中药组合物的抗炎作用机制密切相关,因此将其作为中药组合物生物评价的指标,建立中药组合物生物评价方法。1.实验材料1.1仪器与材料synergyh2全功能微孔板检测仪(美国biotek公司);台式高速离心机(美国thermo公司);微量移液器、多道移液器(德国eppendorf公司);万分之一电子分析天平(梅特勒-托利多仪器上海有限公司);dk-600s三用恒温水箱(上海精宏实验设备有限公司);vortex-2涡旋仪(深圳市安必胜科技有限公司);离心管(美国康宁公司)。1.2药物与试剂dmso购于美国amresco公司(批号3304c252);k547-100cox-2inhibitorscreeningkit(f)购于美国biovision公司(批号2f280547);中药组合物按实施例1制备,共40个批次(编号s01-s40);胶囊内容物分别于高温(60℃)、高湿(rh95%)、光照(4500lx)条件下放置20d的样品a1、a2、a3(编号s41-s43);塞来昔布购于aladdin公司(批号#e1528116)。2.实验方法2.1检测步骤步骤1:在96孔板中,加入待测药物;加入cox-2并孵育一定时间,使药物与cox-2发生抑制反应;步骤2:分别加入adhp和aa,利用催化产生的pgg2结合adhp,产生试卤灵;步骤3:对酶标孔进行显色,激发光波长530-540nm,发射波长585-595nm下检测荧光强度,与空白和100%有活性孔比较,按公式计算药物对cox-2的抑制率;步骤4:将药物对cox-2的抑制率进行坐标转换后,计算效价和可信限率。2.2药液的制备用无菌超纯水将assaybufferr(10×)稀释10倍,作为稀释后的缓冲液;用稀释后的缓冲液按1∶10稀释血红素(heme)、cox-2(冰上操作)、adhp(用前配制);用koh按1∶1稀释aa,涡旋后再用无菌超纯水按1∶5稀释为2mm。精密称取塞来昔布一定量,加dmso溶解超声提取10min,0.45μm滤膜过滤,加dmso稀释成0.45μg/ml的母液,置4℃冰箱中保存备用,用时稀释至所需浓度。精密称取中药组合物一定量,加dmso溶解配成1mg/ml的母液,超声提取10min,12000rpm/min离心10min,取上清备用。用时稀释至所需浓度。2.3cox-2抑制率的测定实验设置背景组(background)、cox-2100%初始活性组(100%initialactivity)、药物抑制剂组(inhibitor)。96孔板中,在100%initialactivity孔加入150μl反应缓冲液、10μl血红素、10μlcox-2和10μl溶剂;在background孔加入160μl反应缓冲液、10μl血红素和10μl溶剂;在inhibitor中加入150μl反应缓冲液、10μl血红素、10μlcox-2和10μl不同浓度的抑制剂。室温孵育10min;各孔加入10μl的adph;各孔迅速加入花生四烯酸10μl以开始反应,室温孵育5分钟。放入酶标仪,激发光波长530-540nm,发射波长585-595nm下检测荧光强度。100%初始活性样品和抑制剂样品的荧光强度需要扣除背景的荧光强度。以扣除背景的100%初始活性样品的荧光强度(initialactivity)减去各抑制剂样品的荧光强度(sampleactivity),再除以initialactivity,乘以100,得到样品对cox-2的抑制率(inhibition%),计算公式如下。抑制率%=(initialactivity-sampleactivity)/initialactivity×100%2.4中药组合物生物效价测定以塞来昔布为标准对照物质和中药组合物参照物(s40)按1∶0.5倍比稀释4个浓度,复3孔分别测定对cox-2的抑制率,定义中药组合物参照物(s40)原始效价赋值为1000u/μg。其他不同批次的样品为供试品组,根据简单概率单位法的原理计算抑制cox-2活性的效价(pt)及可信限率(fl%)。3.实验结果3.1试剂aa纯化前后对药物抑制cox-2活性的影响按照上述实验方法,测定各浓度塞来昔布孔的荧光强度,考察aa纯化前后对测定结果的影响。结果表明,aa纯化前,检测到的荧光背景值为317,并且有抑制率超过100%的现象;而纯化后(纯度>95%)背景值显著下降为50以下。纯化后塞来昔布的ic50为2.5μm。因此,实验过程中需选择纯化后的aa作为检测试剂。3.2cox-2酶用量对药物抑制cox-2活性的影响按照上述实验方法,选择500u/ml和1000u/ml的cox-2酶量用于反应,测定中药组合物对cox-2抑制活性的生物效价。结果表明,不同酶量对药物抑制cox-2活性的生物效价影响较小,从成本角度考虑,酶用量选择为500u/ml。3.3中药组合物对cox-2酶活力的抑制作用将配制的中药组合物供试品溶液,按2.2.4方法测定各组的荧光强度,考察中药组合物对cox-2酶活力的抑制作用,结果见图2。结果表明,中药组合物各给药组比100%初始活性组的荧光强度显著下降(p<0.01),表明中药组合物对cox-2酶活力具有显著的抑制作用,且具有浓度依赖关系。3.4方法学考察结果3.4.1精密度考察取同一份相同浓度(60μg·ml-1)的中药组合物溶液,按上述方法测定,测定6次其对cox-2的抑制作用,计算中药组合物cox-2活力平均抑制率为67.23%,rsd为5.14%,方法日内精密度良好。取同一批号相同浓度的中药组合物溶液,共6份,于第1天至第6天,按上述方法测定其对cox-2的抑制作用,计算中药组合物cox-2活力平均抑制率为64.73%,rsd为8.56%,方法日间精密度良好。3.4.2重复性考察取同一批号中药组合物样品(s40)6份,制成供试品溶液,按上述方法测定,计算中药组合物cox-2活力平均抑制率为70.48%,rsd为9.32%。综上,精密度高,重复性好,满足生物评价方法的要求,可以用于生物评价。3.5中药组合物参照物的生物效价标化采用上述建立的方法,以塞来昔布为对照物质,按照“质反应平行线法”对中药组合物参照物的抑制cox-2酶活性的效价值进行标化。定义中药组合物参照物的生物效价为1000u·μg-1,检测塞来昔布的效价。结果见表3。表3中药组合物参照物与塞来昔布的效价转换将抑制率和相应给药浓度进行坐标转换后,输入效价计算软件计算效价,计算结果为1u中药组合物参照物的作用相当于3.805ng的塞来昔布。3.6中药组合物抑制cox-2活性的生物效价测定根据上述检测方法对中药组合物供试品抑制cox-2酶活力值进行测定,计算得到各批次中药组合物对cox-2酶活力的抑制率,以s40为标准参照物,将抑制率和相应给药浓度进行坐标转换后,输入效价计算软件得到各个批次中药组合物抑制cox-2酶活力的效价,测定结果见表4。表4中药组合物抑制cox-2效价测定结果测定结果显示,不同批次的中药组合物抑制cox-2活性效价为510u/μg~1413u/μg,平均生物效价为856u/μg。中药组合物不同批次的抑制cox-2效价存在一定差异,s26号样品的效价最高,s05号样品的效价最低,非正常供试品测定结果与正常样品之间比较效价下降,具有明显差异,其中抑制cox-2活性效价下降的顺序为高湿>高温>光照。实验例3中药组合物质量化学评价与生物评价相关性分析以中药组合物中9种化学成分(绿原酸、芦丁、连翘酯苷a、连翘酯苷、异绿原酸c、异绿原酸b、咖啡酸、薄荷脑、百秋李醇)含量指标为自变量,生物效价为应变量,对40批次中药组合物为统计分析样品,考察抑制cox-2生物效价、抑制巨噬细胞分泌il-6生物效价与9种化学成分含量测定结果的相关性分析,采用多元统计spss统计软件计算。结果见表5。表5生物活性与化学成分含量的相关性分析从抑制cox-2活性的抗炎生物效价来看,存在相关性的成分为绿原酸、异绿原酸b、异绿原酸c等酸类成分,且为正相关(p<0.05),提示这3种成分的含量越高,其抑制cox-2酶活力的水平也有增高的趋势。因此,在化学成分指控时应考虑增加这类关联活性的指标成分的检测,在一定程度上提高中药组合物质量的一致性的评控能力。从抑制巨噬细胞分泌il-6活性的抗炎生物效价来看,存在相关性的成分为连翘苷,且为正相关(p<0.05),提示连翘苷成分的含量越高,其抑制细胞分泌il-6的水平也有增高的趋势。提示,连翘苷是发挥抗炎作用的有效成分,其含量对中药组合物质量具有一定的影响。具体实施方式实施例1组方:连翘255g、金银花255g、炙麻黄85g、炒苦杏仁85g、石膏255g、板蓝根255g、绵马贯众255g、鱼腥草255g、广藿香85g、大黄51g、红景天85g、薄荷脑7.5g、甘草85g;制备方法:以上十三味,广藿香加水蒸馏提取挥发油,收集挥发油,水提取液滤过,备用;连翘、炙麻黄、鱼腥草、大黄用70%乙醇提取二次,第一次2小时,第二次1.5小时,提取液滤过,合并,回收乙醇、备用;金银花、石膏、板蓝根、绵马贯众、甘草、红景天加水煎煮至沸,加入炒苦杏仁,煎煮二次,第一次1.5小时,第二次1小时,煎液滤过,滤液合并,加入广藿香提油后备用的水溶液,浓缩至相对密度为1.10~1.15(60℃),加乙醇使含醇量70%,在4℃冷藏24小时,滤过,滤液回收乙醇,与上述连翘等四味的备用醇提取液合并,浓缩至相对密为1.15~1.20(60℃),喷雾干燥,与适量淀粉混匀,制成颗粒,干燥,过筛,筛出适量细粉,将薄荷脑、广藿香挥发油用适量乙醇溶解,喷入细粉中,混匀,与上述颗粒混匀,密闭30分钟,装入胶囊,制成1000粒,即得。生物检测方法:对照品的制备:精密称取中药组合物工作参照物(以塞来昔布化学纯品标化效价1000u·μg-1),研细,加dmso超声提取30min,10000r/min离心10min,取上清液制成每1ml含1.2×105u的溶液,即得。供试品的制备:取中药组合物内容物适量,研细,加dmso超声提取30min,10000r/min离心10min,取上清,临用按估计效价制成每1ml含1.2×105u的溶液,即得。测定法:取对照品溶液和供试品溶液按稀释比在1:0.8~1:0.5之间,按实验例2“2.1检测步骤”项下测定抑制率,以cox-2酶活力的抑制率作为指标,按《药品生物检定》(周海钧主编)中“质反应平行线法”计算效价和可信限率。抑制cox-2酶活力的效价不得低于500u·μg-1,平均可信限率小于25%。实施例2生物检测方法:对照品的制备:精密称取中药组合物工作参照物(罗非昔布化学纯品标化效价1000u·μg-1),研细,加甲醇溶液超声提取30min,10000r/min离心10min,取上清液制成每1ml含1.2×105u的溶液,即得。供试品的制备:取中药组合物内容物适量,研细,加dmso超声提取30min,10000r/min离心10min,取上清,临用按估计效价制成每1ml含1.2×105u的溶液,即得。测定法:取对照品溶液和供试品溶液按稀释比在1:0.8~1:0.5之间,按市售cox-2荧光检测试剂盒(上海碧云天生物技术有限公司)说明书操作,测定抑制率,以cox-2酶活力的抑制率作为指标,按《药品生物检定》(周海钧主编)中“质反应平行线法”计算效价和可信限率。抑制cox-2酶活力的效价不得低于500u·μg-1,平均可信限率小于25%。实施例3生物检测方法:对照品的制备:精密称取中药组合物工作参照物(塞来昔布化学纯品标化效价1000u·μg-1),研细,加乙醇溶液超声提取30min,10000r/min离心10min,取上清液制成每1ml含1.2×105u的溶液,即得。供试品的制备:取中药组合物内容物适量,研细,加dmso超声提取30min,10000r/min离心10min,取上清,临用按估计效价制成每1ml含1.2×105u的溶液,即得。测定法:取对照品溶液和供试品溶液按稀释比在1:0.8~1:0.5之间,按实验例2“2.1检测步骤”项下测定抑制率,以cox-2酶活力的抑制率作为指标,按《药品生物检定》(周海钧主编)中“质反应平行线法”计算效价和可信限率。抑制cox-2酶活力的效价不得低于500u·μg-1,平均可信限率小于25%。实施例4生物检测方法:对照品的制备:精密称取中药组合物工作参照物(罗非昔布化学纯品标化效价1000u·μg-1),研细,加dmso超声提取30min,10000r/min离心10min,取上清液制成每1ml含1.2×105u的溶液,即得。供试品的制备:取中药组合物内容物适量,研细,加dmso超声提取30min,10000r/min离心10min,取上清,临用按估计效价制成每1ml含1.2×105u的溶液,即得。测定法:取对照品溶液和供试品溶液按稀释比在1:0.8~1:0.5之间,按“放射酶免疫法”定抑制率,以cox-2酶活力的抑制率作为指标,按2015年版《中国药典》(三部)生物检定统计法项下质反应平行线法计算效价和可信限率。抑制cox-2酶活力的效价不得低于500u·μg-1,平均可信限率小于25%。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1