一种研究口用型无烟气烟草制品烟草特有的亚硝胺口腔释放情况的方法与流程
本发明属于口用型无烟气烟草制品分析技术领域,具体涉及一种研究口用型无烟气烟草制品烟草特有的亚硝胺口腔释放情况的方法,通过该方法可以研究分析口用型无烟气烟草制品烟草特有的亚硝胺溶出情况。
背景技术:
无烟气烟草制品(smokelesstobaccoproducts,简称stps)是指不经燃烧,直接通过口腔或鼻腔吸食的烟草制品,与传统卷烟相比其有害成分少,危害性较小;同时它不产生二手烟气,能在一定程度上缓解公共场所禁烟和吸烟的矛盾,并在一定程度上满足烟民的生理需要。
无烟气烟草制品有袋装口含烟、鼻烟和嚼烟等多种多样的形式,其中消费主体是口用型无烟气烟草制品,主要包括袋装口含烟、胶基型嚼烟和含化烟。袋装口含烟是具有一定颗粒度的烟草粉末混合适量的烟草特有的亚硝胺、矫味剂、水、保润剂和酸碱调节剂经热处理加工制成的,用无纺布小袋包装,置于唇齿之间消费。胶基型无烟气烟草制品(tobaccochewinggum)由瑞典火柴公司(swedishmatch)于2003年首先研发成功并试投放市场。它又称为新型嚼烟、胶基型无烟气烟草、烟草口香糖、胶基烟,是一种以烟草和/或烟草提取物为效用组分,可食用胶基为载体,通过咀嚼方式向人体递送烟草特有的亚硝胺的新型烟草制品。
2016年,全球stps销售额为120亿美元,其中袋装口含烟销售额增加40%以上,嚼烟增加10%左右。stps覆盖全球70个国家,占总人口的73%。通过stps形式进行消费时,烟草不经燃烧,不会产生卷烟烟气中特有的一些有害成分,更重要的是不会产生令人讨厌的“二手烟”,是禁烟环境下烟草消费的重要补充形式。受到当前世界控烟运动的影响,这一类的烟草制品正成为国际烟草领域的重要发展趋势。
目前世界上已发现有300多种n-亚硝胺对40多种动物有致癌性,但烟草制品和烟气中已经知道的只有以下八种:n-亚硝基降盐烟碱(n-nitrosonornicotine,nnn);4-(甲基亚硝胺)-1-(3-吡啶基)-1-丁酮(4-(n-methyl-n-nitrosamino)-1-(3-pyridyl)-1-butanone,nnk);n-亚硝基新烟碱(n-nitrosoanatabine,nat);n-亚硝基新烟草碱(n-nitrosoanabasine,nab);4-(甲基亚硝胺)-4-(3-吡啶基)-丁醛(4-(n-methyl-n-nitrosamino)-4-(3-pyridyl)-butanal,nna);4-(甲基亚硝胺)-1-(3-吡啶基)-1-丁醇(4-(n-methyl-n-nitrosamino)-1-(3-pyridyl)-1-butanol,nnal);4-(甲基亚硝胺)-4-(3-吡啶基)-丁醇(4-(n-methyl-n-nitrosamino)-4-(3-pyridyl)-1-butanol,iso-nnal)。其中nnn、nnk和nat的含量高于其它几种。目前普遍认为tsnas会使人患肺癌,特别是nnn和nnk。用啮齿动物研究表明,无论是喂食还是注射,nnk均会导致肺部肿瘤——表皮细胞良性肿瘤,以及肺腺癌——恶性上皮瘤。另外,美国国家科学院估计,每天抽一盒烟的吸烟者对tsnas的接触量是17毫克。普遍认为烟草制品中tsnas产生的机理是烟草生物碱的自然亚硝化作用。新鲜烟草中tsnas和亚硝酸盐含量极微,一般认为tsnas的形成和积累是发生在采摘之后和调制处理阶段。无烟气烟草制品的制作工艺包括发酵,因此极容易产生大量的烟草特有的亚硝胺(tsnas),其安全性还受到科学界和公共健康团体的质疑。消费者从无烟气烟草制品中吸食的tsnas除了与该产品本身的性质有关外,还与消费者的消费习惯有密切联系。目前关于口用型无烟气烟草制品烟草特有的亚硝胺口腔释放情况还未见报道,消费者使用该类产品时对tsnas的释放吸收情况尚不清楚。因此如何克服现有技术的不足是目前口用型无烟气烟草制品分析技术领域亟需解决的问题。
技术实现要素:
本发明针对口用型无烟气烟草制品中烟草特有的亚硝胺体外释放情况尚未研究,提供了一种研究口用型无烟气烟草制品烟草特有的亚硝胺口腔释放情况的方法,该方法是一种更为接近人体口腔条件的试验方法,利用该方法可以更加准确的研究口用型无烟气烟草制品在人体口腔的释放情况,为该类产品的加工制作、质量控制及安全性评价提供技术支撑和理论依据。
为实现上述目的,本发明采用的技术方案如下:
一种研究口用型无烟气烟草制品烟草特有的亚硝胺口腔释放情况的方法,包括如下步骤:
步骤(1),口用型无烟气烟草制品的筛选:对待研究的某种口用型无烟气烟草制品选取多颗进行重量检测,计算该制品单颗重量平均值和方差;之后,选择重量范围在平均值±(1-3)倍方差范围内的制品作为试样进行后续测定;
步骤(2),模拟溶出参数的确定:选择多位身体健康的自愿者在自然状态下吸食步骤(1)筛选出的试样,并在事先确定的时间点收集残留样品和各自愿者唾液,每个时间点使用一颗样品;
步骤(3),体内实验烟草特有的亚硝胺口腔释放情况的测定:利用液相色谱质谱分别对待研究口用型无烟气烟草制品、残留样品和自愿者唾液进行测试,以确定各时间段自愿者吸食样品的烟草特有的亚硝胺溶出量;
步骤(4),体外试验模拟:采用全仿真模拟咀嚼机模拟吸食该待研究口用型无烟气烟草制品,并根据步骤(3)得到的自愿者吸食样品的烟草特有的亚硝胺溶出量和步骤(2)得到的唾液量,设置全仿真模拟咀嚼机的压合力、唾液流速、唾液量和口腔温度参数;
步骤(5),液相色谱质谱分析:利用液相色谱质谱分别对待研究口用型无烟气烟草制品、残留样品和全仿真模拟咀嚼机中的人工唾液进行测试,用此测试结果来表征待研究口用型无烟气烟草制品的烟草特有的亚硝胺口腔释放情况;
步骤(6),烟草特有的亚硝胺口腔释放规律研究:采用上述全仿真模拟咀嚼机及设定的参数对同种口用型无烟气烟草制品整个咀嚼过程中的不同时间点进行测试,绘制烟草特有的亚硝胺释放曲线,进行烟草特有的亚硝胺口腔释放规律研究。
进一步,优选的是,步骤(1)中,选择至少50颗待研究的某种口用型无烟气烟草制品进行重量检测。
进一步,优选的是,步骤(1)中,所述的口用型无烟气烟草制品的种类包括口含烟、嚼烟、含化烟、膏状含烟、牙粉和可溶解烟草,其中,所述的口含烟的种类包括袋装口含烟、烟草口香糖、含片和硬质糖。
进一步,优选的是,步骤(2)中,所述自愿者为年龄为18-55周岁;所述残留样品和自愿者唾液的收集时间点为实验开始后0-60min内任意一点。
进一步,优选的是,步骤(4)体外试验模拟时,所采用的人工唾液为无机盐类人工唾液或蛋白酶类人工唾液。
进一步,优选的是,步骤(5)利用液相色谱质谱进行测试时,采用内标法定量。
进一步,优选的是,对口用型无烟气烟草制品、残留样品采用液相色谱质谱进行测试时,做如下处理:测试时取1颗制品或残留样品,加入0.01~0.1mol/l盐酸水溶液1~5ml和100ng/ml的混合内标溶液100μl,涡旋混匀,超声提取,离心,上清液全部上样到活化后的oasishlb固相萃取柱上,加3ml体积浓度为2%甲醇水溶液淋洗,最后用3ml甲醇洗脱,收集洗脱液氮气吹干,加入1.0~5.0ml甲醇超声溶解,经0.2μm滤膜过滤至进样瓶中,之后使用液相色谱质谱定量分析;
所述的混合内标溶液中的内标物为烟草特有的亚硝胺的氘代物,各个内标物的浓度均为100ng/ml。
进一步,优选的是,超声提取时间为30~120min;离心时间为5~30min,转速为≧10000r/min;oasishlb固相萃取柱的活化方式为:依次经1~5ml甲醇、2~10ml超纯水淋洗进行活化。
进一步,优选的是,液相色谱为高效液相色谱,参数如下:
色谱柱:watersacquitybehc18柱(1.7μm,2.1mm×100mm);
流速:0.3ml/min;
柱温:40℃;
进样量:5μl;
流动相a:甲醇,流动相b:质量浓度为0.1%的乙酸水溶液;
测试时,采用梯度洗脱,梯度洗脱条件见表1;
表1
进一步,优选的是,质谱条件如下:
离子源:电喷雾电离源;
扫描方式:正离子扫描;
检测方式:多反应监测;
电喷雾电压:5000v;
烟草特有的亚硝胺质谱检测参数见表2;
表2
目前,人工唾液大体分为两类,一类为无机盐类人工唾液,另一类为蛋白酶类人工唾液;蛋白酶类人工唾液处理包括无机盐外,还包括蛋白、酶。
无机盐类人工唾液可如表3和表4所示,但不限于此。
蛋白酶类人工唾液可如表5所示,但不限于此。
表3人工唾液配方一
表4人工唾液配方二
表5人工唾液配方三
注:*单位为units/ml
本发明中测试过程中:烟草特有的亚硝胺溶出量=总烟草特有的亚硝胺含量-残留样品烟草特有的亚硝胺含量。
本发明采用的全仿真模拟咀嚼机可以为zl201610554134.7所示产品,但不限于此。全仿真模拟咀嚼机中所采用的部件可以如zl201610555175.8、zl201610555228.6、zl201620743278.2和zl201620742852.2所示,但不限于此。
本发明设计了一种研究口用型无烟气烟草制品烟草特有的亚硝胺口腔释放情况的方法:通过自愿者体内实验对口用型无烟气烟草制品烟草特有的亚硝胺口腔释放的体外研究参数进行确定;确定压合力、唾液流速、唾液量和口腔温度等模拟溶出参数;利用全仿真模拟咀嚼机对口用型无烟气烟草制品的烟草特有的亚硝胺释放率、释放量等释放规律进行研究。本发明方法可控性强稳定性高,操作简单,可以很好的避免传统人工品尝带来的主观和客观因素的影响,避免了大量人群实验的伦理道德制约,同时节约实验费用的同时还减少了因人体实验对健康带来的危害,适用于样品的批量研究。
同时,第一,本发明采用重量检测的方法对样品进行筛选,优化了筛选范围,超过本发明的筛选范围会使得结果产生较大的偏差,降低了定量的准确性;
第二,本发明基于筛选出来的样品,以体内试验参数为基准来设置体外实验参数,避免了现有技术中体外试验参数设置问题而导致的研究偏差。
第三,本发明通过对同一种类制品的体内试验设置的体外试验参数,在后续过程中,同种类制品无需重复体内实验,可直接采用已经设置好的体外试验参数进行测试,对烟草特有的亚硝胺口腔释放规律进行研究,准确性优异。
第四,本发明优化了烟草特有的亚硝胺含量分析方法,使烟草特有的亚硝胺尽可能的萃取出,避免了因分析方法上的不足而导致的研究上出现的偏差;
第五,本发明在设置体外试验参数时,研究人体的吸食情况,设置不同的压合力、咀嚼频率,并针对不同的时间点设置不同的唾液加入量和唾液流速,更真实的模拟制品在口腔中的消费条件,大大提高了结果的准确性;
第六,在色谱分析时,优化了色谱参数,使得烟草特有的亚硝胺峰分离情况更好,且避免了其它物质对烟草特有的亚硝胺峰的干扰,提高了结果的准确性。
本发明与现有技术相比,其有益效果为:
(1)本发明利用体内实验进行体外研究参数确定,体外采用全仿真模拟咀嚼机对样品进行测试,所用装置能完全模拟人体口腔吸食无烟气烟草制品的状态,对口用型无烟气烟草制品中的tsnas进行体外释放情况研究,在压合力、唾液流速、唾液量和口腔温度参数上均可调控,且可控性强稳定性高,操作简单,能为产品配方设计和安全性评价提供借鉴参考;
(2)本发明口用型无烟气烟草制品烟草特有的亚硝胺口腔释放的研究方法可以很好的避免传统人工品尝带来的主观和客观因素的影响,避免了大量人群实验的伦理道德制约,同时节约实验费用的同时还减少了因人体实验对健康带来的危害,适用于样品的批量研究,为该类产品的配方开发、加工制作及质量控制提供技术支撑和理论依据。
附图说明
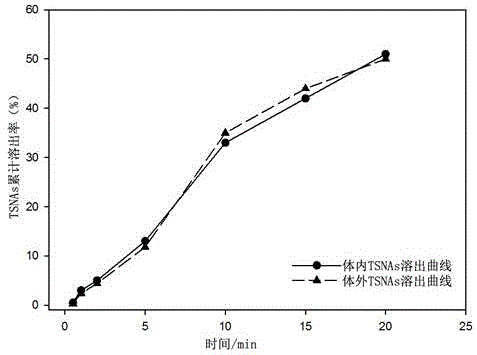
图1为胶基型嚼烟的烟草特有的亚硝胺体内和体外溶出趋势图;
图2为应用实例1种5种胶基型嚼烟外模拟溶出趋势图;其中,产品1购于美国(表6样品1),产品2购于加拿大(表6样品13),产品3、4、5均为云南中烟自制样品(表6样品21、24、25)。
其中,累计溶出率=nnn、nnk、nat、nab四个物质总的溶出量/四个物质总的含量。
具体实施方式
下面结合实施例对本发明作进一步的详细描述。
本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限定本发明的范围。实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。所用材料或设备未注明生产厂商者,均为可以通过购买获得的常规产品。
实施例1
一种研究口用型无烟气烟草制品烟草特有的亚硝胺口腔释放情况的方法,包括如下步骤:
步骤(1),口用型无烟气烟草制品的筛选:对待研究的某种口用型无烟气烟草制品选取100颗进行重量检测,计算该制品单颗重量平均值和方差;之后,选择重量范围在平均值±3倍方差范围内的制品作为试样进行后续测定;
步骤(2),模拟溶出参数的确定:选择多位身体健康的自愿者在自然状态下吸食步骤(1)筛选出的试样,并在事先确定的时间点收集残留样品和各自愿者唾液,每个时间点使用一颗样品;
步骤(3),体内实验烟草特有的亚硝胺口腔释放情况的测定:利用液相色谱质谱分别对待研究口用型无烟气烟草制品、残留样品和自愿者唾液进行测试,以确定各时间段自愿者吸食样品的烟草特有的亚硝胺溶出量;
步骤(4),体外试验模拟:采用全仿真模拟咀嚼机模拟吸食该待研究口用型无烟气烟草制品,并根据步骤(3)得到的自愿者吸食样品的烟草特有的亚硝胺溶出量和步骤(2)得到的唾液量,设置全仿真模拟咀嚼机的压合力、唾液流速、唾液量和口腔温度参数;
步骤(5),液相色谱质谱分析:利用液相色谱质谱分别对待研究口用型无烟气烟草制品、残留样品和全仿真模拟咀嚼机中的人工唾液进行测试,用此测试结果来表征待研究口用型无烟气烟草制品的烟草特有的亚硝胺口腔释放情况;
步骤(6),烟草特有的亚硝胺口腔释放规律研究:采用上述全仿真模拟咀嚼机及设定的参数对同种口用型无烟气烟草制品整个咀嚼过程中的不同时间点进行测试,绘制烟草特有的亚硝胺释放曲线,进行烟草特有的亚硝胺口腔释放规律研究。
所述的口用型无烟气烟草制品的种类为口含烟。
步骤(4)体外试验模拟时,所采用的人工唾液为无机盐类人工唾液,如表3所示。
实施例2
一种研究口用型无烟气烟草制品烟草特有的亚硝胺口腔释放情况的方法,包括如下步骤:
步骤(1),口用型无烟气烟草制品的筛选:对待研究的某种口用型无烟气烟草制品选取50颗进行重量检测,计算该制品单颗重量平均值和方差;之后,选择重量范围在平均值±1倍方差范围内的制品作为试样进行后续测定;
步骤(2),模拟溶出参数的确定:选择多位身体健康的自愿者在自然状态下吸食步骤(1)筛选出的试样,并在事先确定的时间点收集残留样品和各自愿者唾液,每个时间点使用一颗样品;
步骤(3),体内实验烟草特有的亚硝胺口腔释放情况的测定:利用液相色谱质谱分别对待研究口用型无烟气烟草制品、残留样品和自愿者唾液进行测试,以确定各时间段自愿者吸食样品的烟草特有的亚硝胺溶出量;
步骤(4),体外试验模拟:采用全仿真模拟咀嚼机模拟吸食该待研究口用型无烟气烟草制品,并根据步骤(3)得到的自愿者吸食样品的烟草特有的亚硝胺溶出量和步骤(2)得到的唾液量,设置全仿真模拟咀嚼机的压合力、唾液流速、唾液量和口腔温度参数;
步骤(5),液相色谱质谱分析:利用液相色谱质谱分别对待研究口用型无烟气烟草制品、残留样品和全仿真模拟咀嚼机中的人工唾液进行测试,用此测试结果来表征待研究口用型无烟气烟草制品的烟草特有的亚硝胺口腔释放情况;
步骤(6),烟草特有的亚硝胺口腔释放规律研究:采用上述全仿真模拟咀嚼机及设定的参数对同种口用型无烟气烟草制品整个咀嚼过程中的不同时间点进行测试,绘制烟草特有的亚硝胺释放曲线,进行烟草特有的亚硝胺口腔释放规律研究。
所述的口用型无烟气烟草制品的种类为含化烟。
步骤(2)中,所述自愿者为年龄为18-55周岁;所述残留样品和自愿者唾液的收集时间点为实验开始后0-60min内任意一点。
步骤(4)体外试验模拟时,所采用的人工唾液为无机盐类人工唾液,如表4所示。
步骤(5)利用液相色谱质谱进行测试时,采用内标法定量。
实施例3
一种研究口用型无烟气烟草制品烟草特有的亚硝胺口腔释放情况的方法,包括如下步骤:
步骤(1),口用型无烟气烟草制品的筛选:对待研究的某种口用型无烟气烟草制品选取150颗进行重量检测,计算该制品单颗重量平均值和方差;之后,选择重量范围在平均值±2倍方差范围内的制品作为试样进行后续测定;
步骤(2),模拟溶出参数的确定:选择多位身体健康的自愿者在自然状态下吸食步骤(1)筛选出的试样,并在事先确定的时间点收集残留样品和各自愿者唾液,每个时间点使用一颗样品;
步骤(3),体内实验烟草特有的亚硝胺口腔释放情况的测定:利用液相色谱质谱分别对待研究口用型无烟气烟草制品、残留样品和自愿者唾液进行测试,以确定各时间段自愿者吸食样品的烟草特有的亚硝胺溶出量;
步骤(4),体外试验模拟:采用全仿真模拟咀嚼机模拟吸食该待研究口用型无烟气烟草制品,并根据步骤(3)得到的自愿者吸食样品的烟草特有的亚硝胺溶出量和步骤(2)得到的唾液量,设置全仿真模拟咀嚼机的压合力、唾液流速、唾液量和口腔温度参数;
步骤(5),液相色谱质谱分析:利用液相色谱质谱分别对待研究口用型无烟气烟草制品、残留样品和全仿真模拟咀嚼机中的人工唾液进行测试,用此测试结果来表征待研究口用型无烟气烟草制品的烟草特有的亚硝胺口腔释放情况;
步骤(6),烟草特有的亚硝胺口腔释放规律研究:采用上述全仿真模拟咀嚼机及设定的参数对同种口用型无烟气烟草制品整个咀嚼过程中的不同时间点进行测试,绘制烟草特有的亚硝胺释放曲线,进行烟草特有的亚硝胺口腔释放规律研究。
所述的口用型无烟气烟草制品的种类为可溶解烟草。
步骤(2)中,所述自愿者为年龄为18-55周岁;所述残留样品和自愿者唾液的收集时间点为实验开始后0-60min内任意一点。
步骤(4)体外试验模拟时,所采用的人工唾液为蛋白酶类人工唾液,如表5所示。
对口用型无烟气烟草制品、残留样品采用液相色谱质谱进行测试时,做如下处理:测试时取1颗制品或残留样品,加入0.01mol/l盐酸水溶液1ml和100ng/ml的混合内标溶液100μl,涡旋混匀,超声提取30min,离心5min,离心转速为≧10000r/min,上清液全部上样到活化后的oasishlb固相萃取柱上,加3ml体积浓度为2%甲醇水溶液淋洗,最后用3ml甲醇洗脱,收集洗脱液氮气吹干,加入1.0ml甲醇超声溶解,经0.2μm滤膜过滤至进样瓶中,之后使用液相色谱质谱定量分析;
其中,oasishlb固相萃取柱的活化方式为:依次经1ml甲醇、2ml超纯水淋洗进行活化。
所述的混合内标溶液中的内标物为烟草特有的亚硝胺的氘代物,各个内标物的浓度均为100ng/ml。
实施例4
一种研究口用型无烟气烟草制品烟草特有的亚硝胺口腔释放情况的方法,包括如下步骤:
步骤(1),口用型无烟气烟草制品的筛选:对待研究的某种口用型无烟气烟草制品选取200颗进行重量检测,计算该制品单颗重量平均值和方差;之后,选择重量范围在平均值±1.5倍方差范围内的制品作为试样进行后续测定;
步骤(2),模拟溶出参数的确定:选择多位身体健康的自愿者在自然状态下吸食步骤(1)筛选出的试样,并在事先确定的时间点收集残留样品和各自愿者唾液,每个时间点使用一颗样品;
步骤(3),体内实验烟草特有的亚硝胺口腔释放情况的测定:利用液相色谱质谱分别对待研究口用型无烟气烟草制品、残留样品和自愿者唾液进行测试,以确定各时间段自愿者吸食样品的烟草特有的亚硝胺溶出量;
步骤(4),体外试验模拟:采用全仿真模拟咀嚼机模拟吸食该待研究口用型无烟气烟草制品,并根据步骤(3)得到的自愿者吸食样品的烟草特有的亚硝胺溶出量和步骤(2)得到的唾液量,设置全仿真模拟咀嚼机的压合力、唾液流速、唾液量和口腔温度参数;
步骤(5),液相色谱质谱分析:利用液相色谱质谱分别对待研究口用型无烟气烟草制品、残留样品和全仿真模拟咀嚼机中的人工唾液进行测试,用此测试结果来表征待研究口用型无烟气烟草制品的烟草特有的亚硝胺口腔释放情况;
步骤(6),烟草特有的亚硝胺口腔释放规律研究:采用上述全仿真模拟咀嚼机及设定的参数对同种口用型无烟气烟草制品整个咀嚼过程中的不同时间点进行测试,绘制烟草特有的亚硝胺释放曲线,进行烟草特有的亚硝胺口腔释放规律研究。
所述的口用型无烟气烟草制品的种类为牙粉。
步骤(4)体外试验模拟时,所采用的人工唾液为蛋白酶类人工唾液,如表5所示。
对口用型无烟气烟草制品、残留样品采用液相色谱质谱进行测试时,做如下处理:测试时取1颗制品或残留样品,加入0.1mol/l盐酸水溶液5ml和100ng/ml的混合内标溶液100μl,涡旋混匀,超声提取120min,离心30min,离心转速为≧10000r/min,上清液全部上样到活化后的oasishlb固相萃取柱上,加3ml体积浓度为2%甲醇水溶液淋洗,最后用3ml甲醇洗脱,收集洗脱液氮气吹干,加入5.0ml甲醇超声溶解,经0.2μm滤膜过滤至进样瓶中,之后使用液相色谱质谱定量分析;
其中,oasishlb固相萃取柱的活化方式为:依次经5ml甲醇、10ml超纯水淋洗进行活化。
所述的混合内标溶液中的内标物为烟草特有的亚硝胺的氘代物,各个内标物的浓度均为100ng/ml。
液相色谱为高效液相色谱,参数如下:
色谱柱:watersacquitybehc18柱(1.7μm,2.1mm×100mm);
流速:0.3ml/min;
柱温:40℃;
进样量:5μl;
流动相a:甲醇,流动相b:质量浓度为0.1%的乙酸水溶液;
测试时,采用梯度洗脱,梯度洗脱条件见表1。
质谱条件如下:
离子源:电喷雾电离源;
扫描方式:正离子扫描;
检测方式:多反应监测;
电喷雾电压:5000v;
烟草特有的亚硝胺质谱检测参数见表2。
实施例5
一种研究口用型无烟气烟草制品烟草特有的亚硝胺口腔释放情况的方法,包括如下步骤:
步骤(1),口用型无烟气烟草制品的筛选:对待研究的某种口用型无烟气烟草制品选取120颗进行重量检测,计算该制品单颗重量平均值和方差;之后,选择重量范围在平均值±2倍方差范围内的制品作为试样进行后续测定;
步骤(2),模拟溶出参数的确定:选择多位身体健康的自愿者在自然状态下吸食步骤(1)筛选出的试样,并在事先确定的时间点收集残留样品和各自愿者唾液,每个时间点使用一颗样品;
步骤(3),体内实验烟草特有的亚硝胺口腔释放情况的测定:利用液相色谱质谱分别对待研究口用型无烟气烟草制品、残留样品和自愿者唾液进行测试,以确定各时间段自愿者吸食样品的烟草特有的亚硝胺溶出量;
步骤(4),体外试验模拟:采用全仿真模拟咀嚼机模拟吸食该待研究口用型无烟气烟草制品,并根据步骤(3)得到的自愿者吸食样品的烟草特有的亚硝胺溶出量和步骤(2)得到的唾液量,设置全仿真模拟咀嚼机的压合力、唾液流速、唾液量和口腔温度参数;
步骤(5),液相色谱质谱分析:利用液相色谱质谱分别对待研究口用型无烟气烟草制品、残留样品和全仿真模拟咀嚼机中的人工唾液进行测试,用此测试结果来表征待研究口用型无烟气烟草制品的烟草特有的亚硝胺口腔释放情况;
步骤(6),烟草特有的亚硝胺口腔释放规律研究:采用上述全仿真模拟咀嚼机及设定的参数对同种口用型无烟气烟草制品整个咀嚼过程中的不同时间点进行测试,绘制烟草特有的亚硝胺释放曲线,进行烟草特有的亚硝胺口腔释放规律研究。
所述的口用型无烟气烟草制品的种类为牙粉。
步骤(2)中,所述自愿者为年龄为18-55周岁;所述残留样品和自愿者唾液的收集时间点为实验开始后0-60min内任意一点。
步骤(4)体外试验模拟时,所采用的人工唾液为蛋白酶类人工唾液,如表5所示。
对口用型无烟气烟草制品、残留样品采用液相色谱质谱进行测试时,做如下处理:测试时取1颗制品或残留样品,加入0.05mol/l盐酸水溶液3ml和100ng/ml的混合内标溶液100μl,涡旋混匀,超声提取80min,离心15min,离心转速为≧10000r/min,上清液全部上样到活化后的oasishlb固相萃取柱上,加3ml体积浓度为2%甲醇水溶液淋洗,最后用3ml甲醇洗脱,收集洗脱液氮气吹干,加入3.0ml甲醇超声溶解,经0.2μm滤膜过滤至进样瓶中,之后使用液相色谱质谱定量分析;
其中,oasishlb固相萃取柱的活化方式为:依次经3ml甲醇、7ml超纯水淋洗进行活化。
所述的混合内标溶液中的内标物为烟草特有的亚硝胺的氘代物,各个内标物的浓度均为100ng/ml。
液相色谱为高效液相色谱,参数如下:
色谱柱:watersacquitybehc18柱(1.7μm,2.1mm×100mm);
流速:0.3ml/min;
柱温:40℃;
进样量:5μl;
流动相a:甲醇,流动相b:质量浓度为0.1%的乙酸水溶液;
测试时,采用梯度洗脱,梯度洗脱条件见表1。
质谱条件如下:
离子源:电喷雾电离源;
扫描方式:正离子扫描;
检测方式:多反应监测;
电喷雾电压:5000v;
烟草特有的亚硝胺质谱检测参数见表2。
对比试验1
考察萃取方式,萃取方式选择浸提、超声、振荡,其余都与实施例5相同相同。结果与实施例5相比,显示出浸提、振荡萃取,色谱上烟草特有的亚硝胺峰均很小,应该是萃取不充分。
对比试验2
考察超声时间,超声时间分别为5min、100min,其余都与实施例5相同相同。结果与实施例6相比,显示出超声时间为5min时,色谱上烟草特有的亚硝胺峰很小,应该是萃取不充分;当超声时间为100min时,检测结果与实施例5无明显差异。
对比试验3
考察萃取溶剂,与采用含0.5%醋酸的甲醇溶液、乙酸铵相比,本发明萃取效果远远优于现有技术中的效果;采用含0.5%醋酸的甲醇溶液、乙酸铵的色谱上,烟草特有的亚硝胺的色谱峰偏小,不易分离。
对比试验4
考察提取后进样前的处理方式,处理方式包括(1)实施例6处理方式、(2)提取液直接氮气吹干、(3)与实施例6处理方式的区别在于不离心。结果发现,处理方式(2)和(3)杂峰均较多,很难对烟草特有的亚硝胺的含量进行精确的定量分析,以处理方式(2)的杂峰最多。
应用实例1
一种研究口用型无烟气烟草制品烟草特有的亚硝胺口腔释放情况的方法,包括如下步骤:
步骤(1),口用型无烟气烟草制品的筛选:对待研究的某种口用型无烟气烟草制品选取100颗进行重量检测,计算该制品单颗重量平均值和方差;之后,选择重量范围在平均值±2倍方差范围内的制品作为试样进行后续测定;
所述的口用型无烟气烟草制品的种类为嚼烟;所选择得到的试样信息如表6;
表6
注:序号21-25产品为云南中烟工业责任有限公司产品。
步骤(2),模拟溶出参数的确定:选择10位年龄为~55周岁身体健康的自愿者在自然状态下吸食步骤(1)筛选出的试样,并在事先确定的时间点收集残留样品和各自愿者唾液,每个时间点使用一颗样品;
所述残留样品和自愿者唾液的收集时间点为实验开始后0.5、1、2、5、10、15、20min;
步骤(3),体内实验烟草特有的亚硝胺口腔释放情况的测定:样品经过前处理,利用液相色谱质谱分别对待研究口用型无烟气烟草制品、残留样品和自愿者唾液进行测试,以确定各时间段自愿者吸食样品的烟草特有的亚硝胺溶出量;
a仪器与试剂
1)仪器
液相色谱串联质谱仪:1290高效液相色谱仪(美国agilent公司),agilent6460三重四级杆液相色谱-串联质谱仪,配有电喷雾离子源(美国agilent公司);分析天平(瑞士梅特勒;型号:ab204-s;感量0.1mg)。
)试剂与材料
甲醇(色谱纯,dikma);乙腈(色谱纯,dikma);乙酸(分析纯);甲酸(分析纯);超纯水(电阻率≥18.2mω·cm);乙酸铵(分析纯);氘代-4-(甲基亚硝胺基)-1-(3-吡啶基)-1-丁酮,4-(methylnitrosoamino)-1-(3-pyridyl-d4)-1-butanone(nnk-d4),纯度≥99%;氘代-n-亚硝基降烟碱,racn′-nitrosonornicotine-d4(nnn-d4),纯度≥99%;n-亚硝基假木贼碱,(r,s)-n-nitrosoanabasine(nab),纯度≥98%;n-亚硝基新烟碱,(r,s)-n-nitrosoanatabine(nat),纯度≥98%;4-(甲基亚硝胺基)-1-(3-吡啶基)-1-丁酮,4-(methylnitrosoamino)-1-(3-pyridyl)-1-butanone(nnk),纯度≥98%;n-亚硝基降烟碱,racn′-nitrosonornicotine(nnn),纯度≥98%。
材料:色谱柱:watersacquitybehc18柱(1.7μm,2.1mm×100mm);oasishlb固相萃取小柱(60mg/3ml,美国waters公司);针筒和滤头;高纯氮气(纯度大于99.999%)。
溶液配制
1)内标储备液
各称取10.0mg的nnk-d4和nnn-d4,用甲醇完全溶解后,分别转移至2个10ml棕色容量瓶中,用甲醇定容至刻度,配制成浓度均为1.0mg/ml的内标储备液。该内标储备溶液于-18℃条件下避光保存,有效期为6个月。
分别移取1.0mlnnk-d4和nnn-d4的1.0mg/ml内标储备液至100ml棕色容量瓶中,用甲醇定容至刻度,配制成nnk-d4和nnn-d4浓度均为10.0μg/ml的一级混合内标溶液。该溶液于-18℃条件下避光保存,有效期为6个月。使用时,稀释成浓度均为100ng/ml的混合内标溶液。
)标准溶液
各称取10.0mg的nab、nat、nnk和nnn,用甲醇完全溶解后,分别转移至4个10ml棕色容量瓶中,用甲醇定容至刻度,配制成浓度均为1.0mg/ml的标准储备液。该储备液于-18℃条件下避光保存,有效期为6个月。
样品处理方法
将样品剪碎,准确称取1粒样品,置于10ml离心管中,加入0.05mol/l盐酸水溶液5ml及100ng/ml的内标溶液100μl,涡旋混匀,超声提取60min,再于10000r/min离心10min,上清液全部上样到活化后的oasishlb固相萃取柱上(依次经3ml甲醇、5ml超纯水预活化),加3ml体积浓度为2%甲醇水溶液淋洗,最后用3ml甲醇洗脱,收集洗脱液氮气吹干,加入1.0ml流动相超声溶解,经0.2μm滤膜过滤至进样瓶中,待测定。
分析
高效液相色谱参考条件
——色谱柱:watersacquitybehc18柱(1.7μm,2.1mm×100mm);
——流速:0.3ml/min;
——柱温:40℃;
——进样量:5μl;
——流动相a:甲醇(4.2),流动相b:0.1%的乙酸溶液;
——梯度洗脱条件见表7。
表7
质谱参考条件
——离子源:电喷雾电离源(esi);
——扫描方式:正离子扫描;
——检测方式:多反应监测(mrm);
——电喷雾电压:5000v;
——各分析物质谱检测参数见表8。
表8
e结果的计算与表述
1)定性结果
在相同实验条件先测定标准溶液和样品溶液,如果样品溶液中检出的色谱峰的保留时间与标准溶液中的某种组分峰的保留时间一致,并且所选择的至少两对离子的质荷比一致,在对标准混合工作溶液的测定后得到tsnas的离子相对丰度比见表9,样品定性离子相对丰度与浓度相当标准工作溶液的定性离子的相对丰度进行比较时,相对偏差不超过表9规定的范围,则可判定样品中存在该组分。其中,标准混合工作溶液为浓度为0.20ng/ml~50ng/ml系列浓度的tsnas标准混合工作溶液。
表9定性确定时相对离子丰度的最大允许偏差
2)定量结果
嚼烟中tsnas含量由式(1)计算得出:
式中:
x——每克样品中tsnas的含量,单位为纳克每克(ng/g);
c——萃取溶液中tsnas的浓度,单位为纳克每毫升(ng/ml);
v——萃取溶液的体积,单位为毫升(ml);
m——称取样品量,单位为克(g)。
其中萃取溶液是样品处理方法中的盐酸水溶液。
取两次平行测定结果的平均值为最终测试结果,精确至0.01ng/g,平行测定结果其相对平均偏差应小于10%。
结果分析
1)线性关系
配制浓度为0.20ng/ml~50ng/ml系列浓度的tsnas标准混合工作溶液(nnn、nnk、nat、nab的浓度均为0.20ng/ml~50ng/ml),用液相色谱串联质谱测定,得到tsnas积分峰面积,以峰面积作为纵坐标,用于制作标准曲线,对校正数据进行线性回归,回归方程和相关系数见表10。
表10tsnas的线性关系
*线性方程中a为峰面积;c为各组分的浓度,单位为ng/ml。
从表10可以看出,tsnas的相关系数大于0.999,表明在一定浓度范围内线性关系良好,满足检测要求。
)重现性
选取样品称取6次,样本进行前处理,测定tsnas含量,在相同条件下进行6次测定,其rsd%见表11。
表11胶基烟tsnas的重现性结果rsd%(ng/ml)
由表可知,连续6次测定tsnas的rsd在3.80%~5.69%,rsd≤5.69%,说明该方法对tsnas的重现性较好。
)检测限
检测器产生的响应信号为噪声值3倍时的量为检出限,检测器产生的响应信号为噪声值10倍时的量为定量限,用3倍和10倍噪音计算该方法的检出浓度和定量浓度,并通过定容体积和样品量换算得到样品的检出限和定量限,见表12。
表12tsnas的检出浓度、定量浓度、检出限和定量限
由表12可知,该方法的检出限和定量限较低,本发明建立的tsnas检测方法的检出限和定量限低于文献报道的。说明该方法有较好的灵敏度、较低的检测限,能够很好的满足检测要求。
)回收率
选取了样品,采用加入tsnas标准物质后,选取低、中、高三个梯度的tsnas溶液进行加标实验,每个浓度平行进行实验3次,分别得到了tsnas的回收率,见表13。
表13胶基烟tsnas的加标回收率
由表13可知,胶基烟回收率在88.47%~111.33%。说明建立的分析方法回收率较好,满足胶基烟中tsnas含量的检测要求。
步骤(4),体外试验模拟:采用全仿真模拟咀嚼机模拟吸食该待研究口用型无烟气烟草制品,并根据步骤(3)得到的自愿者吸食样品的烟草特有的亚硝胺溶出量和唾液量,设置全仿真模拟咀嚼机的压合力、咀嚼频率、唾液量和口腔温度参数;所采用的人工唾液为表1所示的无机盐类人工唾液;
其中,设置全仿真模拟咀嚼机的压合力、唾液流速、唾液量和口腔温度的具体参数如表14。
表14仪器参数
步骤(5),液相色谱质谱分析:利用液相色谱质谱分别对待研究口用型无烟气烟草制品、残留样品和全仿真模拟咀嚼机中的人工唾液进行测试,用此测试结果来表征待研究口用型无烟气烟草制品的烟草特有的亚硝胺口腔释放情况;
步骤(6),烟草特有的亚硝胺口腔释放规律研究:采用上述全仿真模拟咀嚼机及设定的参数对同种口用型无烟气烟草制品整个咀嚼过程中的不同时间点进行测试,绘制烟草特有的亚硝胺释放曲线,进行烟草特有的亚硝胺口腔释放规律研究。
由图1可以看出,模拟口腔体外实验数据与人群体内实验数据吻合度较高,烟草特有的亚硝胺的体内体外溶出曲线趋势基本一致,说明该方法能较好地模拟胶基型嚼烟中烟草特有的亚硝胺的体内溶出行为。利用该发明方法对云南中烟自制的口用型无烟气烟草制品中的烟草特有的亚硝胺口腔溶出情况与国外产品进行对比,结果如表2,从表2中可以看出,由于云南中烟自制的产品中有烟草原料的直接引入,因此能看出亚硝胺的溶出规律曲线。而国外产品由于烟碱的引入形式是直接添加烟碱,因此产品中未能检测出烟草特有的亚硝胺,所以两种产品的折线图是完全重合的。总之,本发明口用型无烟气烟草制品烟草特有的亚硝胺口腔释放的研究方法可以很好的避免传统人工品尝带来的主观和客观因素的影响,避免了大量人群实验的伦理道德制约,同时节约实验费用的同时还减少了因人体实验对健康带来的危害,适用于样品的批量研究,为该类产品的配方开发、加工制作及质量控制提供技术支撑和理论依据。
以上显示和描述了本发明的基本原理、主要特征和本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,这些变化和改进都落入要求保护的本发明范围内。本发明要求保护范围由所附的权利要求书及其等效物界定。
- 还没有人留言评论。精彩留言会获得点赞!