一种检测维生素C药物中降解杂质含量的方法与流程
本发明涉及药物分析
技术领域:
,尤其涉及一种采用高效液相色谱法检测维生素c药物中降解杂质含量的方法,该方法用于检测维生素c原料药及制剂中降解杂质l-苏糖酸、脱氢vc和l-木糖的含量。
背景技术:
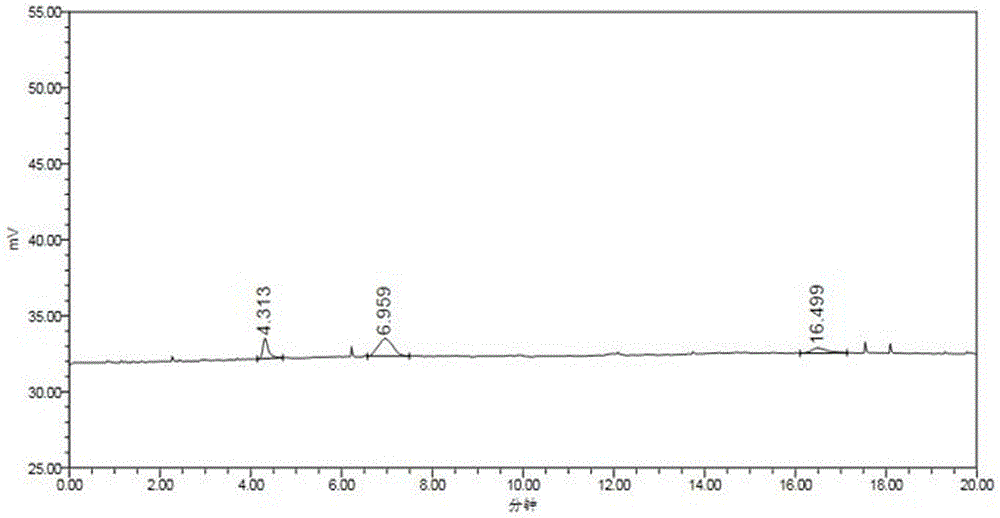
:维生素c药物中的主药为维生素c,维生素c的化学名称为l-坏血酸,分子式为c6h8o6,分子量为176.13,结构式为:维生素c参与氨基酸代谢、神经递质的合成、胶原蛋白和组织细胞间质的合成,可降低毛细血管的通透性,加速血液的凝固,刺激凝血功能,促进铁在肠内的吸收,促使血脂下降,增加对感染的抵抗力,参与解毒功能,且有抗组胺的作用及阻止致癌物质(亚硝胺)生成的作用。维生素c是一种具有还原性的化合物,易被氧化,因此在接触到氧的环境里,维生素c可降解产生l-苏糖酸和脱氢vc,同时在无氧环境下,维生素c也可发生无氧降解产生l-木糖,l-苏糖酸的结构式为:脱氢vc的结构式为:l-木糖的结构式为:根据国家食品药品监督管理局的要求,应对药品的相关杂质进行控制,但上述降解杂质l-苏糖酸和l-木糖均是基本无紫外吸收的小分子极性化合物,不适合采用普通的紫外检测器进行检测,亦不适合采用气相色谱法检测,而薄层色谱法又无法达到相应的检测灵敏度。因此,有必要研发一种能够同时准确检测维生素c原料药及制剂中降解杂质l-苏糖酸、脱氢vc和l-木糖含量的方法。技术实现要素:本发明的目的在于解决现有技术中存在的上述问题,提供一种检测维生素c药物中降解杂质含量的方法,本发明能够同时检测出维生素c药物中降解杂质l-木糖、l-苏糖酸和脱氢vc的含量,灵敏度高,专属性强,保证了维生素c药物的质量控制。为实现上述目的,本发明采用的技术方案如下:一种检测维生素c药物中降解杂质含量的方法,其特征在于:采用高效液相色谱法进行检测,检测条件如下:色谱柱:hilic色谱柱,规格为4.6×250mm,5μm;流动相:缓冲盐溶液和乙腈的混合液,等度洗脱;检测器:蒸发光散射检测器;所述缓冲盐溶液为甲酸铵溶液、乙酸铵溶液中的一种或按任意比例混合的两种。所述混合液中缓冲盐溶液与乙腈的质量比为15—20:80—85。所述缓冲盐溶液的浓度为0.05—0.2mol/l。所述流动相的流速为0.8—1.2ml/min。所述色谱柱的柱温为25—40℃。所述检测器的漂移管温度为80—100℃。所述检测器的气体流速为1.5—3.0l/min。所述的检测方法包括如下步骤:取系统适用性试验溶液、供试品溶液和多组浓度不同的线性对照品溶液各10μl,分别进样,记录色谱图;根据线性对照品溶液的浓度和峰面积,计算线性对照品溶液中各组分浓度的对数值与相应的峰面积对数值的线性回归方程,并用回归方程计算出供试品中各杂质的含量;其中,所述供试品溶液由维生素c药物经稀释剂稀释而成,供试品溶液中维生素c含量为40mg/ml;所述线性对照品溶液由取相同量的脱氢vc对照品储备液、l-木糖对照品储备液和l-苏糖酸钙对照品储备液在10ml量瓶中经稀释剂均匀稀释至刻度而成,多组浓度不同的线性对照品溶液是指各组线性对照品溶液中对照品储备液的取样量不同;所述系统适用性试验溶液由脱氢vc对照品储备液、l-木糖对照品储备液和l-苏糖酸钙对照品储备液混合并经稀释剂稀释而成,系统适用性试验溶液中脱氢vc、l-木糖和l-苏糖酸钙的含量均为60μg/ml。所述脱氢vc对照品储备液由脱氢vc经稀释剂稀释而成,脱氢vc对照品储备液中脱氢vc的含量为1mg/ml;所述l-木糖对照品储备液由l-木糖经稀释剂稀释而成,l-木糖对照品储备液中l-木糖的含量为1mg/ml;所述l-苏糖酸钙对照品储备液由l-苏糖酸钙经水溶解而成,l-苏糖酸钙对照品储备液中l-苏糖酸钙的含量为1mg/ml。所述稀释剂为水与乙腈的混合溶液,且水与乙腈的质量比为40—80:20—60。采用本发明的优点在于:1、本发明提供了一种维生素c药物中小分子极性化合物杂质含量的新检测方法,各色谱峰之间分离度高,相互之间无干扰,可以同时实现对脱氢vc、l-木糖、l-苏糖酸的准确检测,而且操作简便,容易控制,检测成本低,并具有良好的线性关系,专属性、精密度、灵敏度、耐用性,检测结果准确可靠,为监控维生素c药物中杂质的含量提供了一种行之有效的检测方法,进一步保证了维生素c产品的质量和患者的用药安全。2、本发明中所述维生素c药物中还包括其它杂质,如杂质c、杂质d、5-羟甲糠醛、糠醛、异维生素c,其中,杂质c的结构式为:杂质d的结构式为5-羟甲糠醛的结构式为糠醛的结构式为:异维生素c的结构式为但这些杂质均不会影响脱氢vc、l-木糖、l-苏糖酸的准确检测(详见实施例部分的专属性试验),从而保证了检测结构的准确性。3、本发明检测的l-木糖、l-苏糖酸是一类没有紫外吸收的化合物,不适用普通的紫外检测器,因此本发明采用蒸发光散射检测器(elsd),蒸发光散射检测器是一种通用型质量检测器,可以检测没有紫外吸收的有机物质,消除了常见于传统hplc检测方法的难点,不同于紫外和荧光检测器,蒸发光散射检测器的响应不依赖于样品的光学特性,任何挥发性低于流动相的样品均能被检测,不受其官能团的影响。4、本发明检测的l-木糖、l-苏糖酸是一类极性较强的化合物,在普通反相柱上几乎无保留,因此本发明采用亲水性的hilic色谱柱,hilic色谱柱是近年来色谱领域研究的热点之一,此类色谱柱对极性化合物有较高的选择性,且性能更优于传统的氨基柱、氰基柱。附图说明图1为实施例1中检测系统适用性试验溶液的色谱图;图2为实施例2中检测系统适用性试验溶液的色谱图;图3为实施例3中检测系统适用性试验溶液的色谱图;具体实施方式本发明公开了一种检测维生素c药物中降解杂质含量的方法,采用高效液相色谱法进行检测,检测条件如下:高效液相色谱仪:沃特世e2695;色谱柱:hilic色谱柱,规格为4.6×250mm,5μm;柱温:25—40℃;流动相:缓冲盐溶液和乙腈的混合液,等度洗脱;流速:0.8—1.2ml/min;检测器:蒸发光散射检测器;检测器的漂移管温度:80—100℃;检测器的气体流速:1.5—3.0l/min;进样量:10μl。其中,所述混合液中缓冲盐溶液与乙腈的质量比为15—20:80—85,所述缓冲盐溶液的浓度为0.05—0.2mol/l,所述缓冲盐溶液为甲酸铵溶液、乙酸铵溶液中的一种或按任意比例混合的两种。所述的检测方法包括如下步骤:1,先制备系统适用性试验溶液、供试品溶液和线性对照品溶液,具体的:所述供试品溶液由维生素c药物经稀释剂稀释而成,供试品溶液中维生素c含量为40mg/ml。所述线性对照品溶液由取相同量的脱氢vc对照品储备液、l-木糖对照品储备液和l-苏糖酸钙对照品储备液在10ml量瓶中经稀释剂均匀稀释至刻度而成,所述脱氢vc对照品储备液由脱氢vc经稀释剂稀释而成,脱氢vc对照品储备液中脱氢vc的含量为1mg/ml;所述l-木糖对照品储备液由l-木糖经稀释剂稀释而成,l-木糖对照品储备液中l-木糖的含量为1mg/ml;所述l-苏糖酸钙对照品储备液由l-苏糖酸钙经水溶解而成,l-苏糖酸钙对照品储备液中l-苏糖酸钙的含量为1mg/ml。所述系统适用性试验溶液由脱氢vc对照品储备液、l-木糖对照品储备液和l-苏糖酸钙对照品储备液混合并经稀释剂稀释而成,系统适用性试验溶液中脱氢vc、l-木糖和l-苏糖酸钙的含量均为60μg/ml。其中,制备系统适用性试验溶液、供试品溶液和线性对照品溶液所使用的稀释剂为水与乙腈的混合溶液,水与乙腈的质量比为40—80:20—60。2,精密量取系统适用性试验溶液、供试品溶液和多组浓度不同的线性对照品溶液各10μl,分别进样,记录色谱图;根据线性对照品溶液的浓度和峰面积,计算线性对照品溶液中各组分浓度的对数值与相应的峰面积对数值的线性回归方程,并用回归方程计算出供试品中各杂质的含量。其中,多组浓度不同的线性对照品溶液是指各组线性对照品溶液中对照品储备液的取样量不同,多组浓度不同的线性对照品溶液的组数至少为3组,优选为5组。例如,5组线性对照品溶液中的组分可分别取0.4ml、0.6ml、0.8ml、1.2ml、2.0ml,这样,第1组线性对照品溶液就由0.4ml的脱氢vc对照品储备液、0.4ml的l-木糖对照品储备液和0.4ml的l-苏糖酸钙对照品储备液在10ml量瓶中经稀释剂均匀稀释至刻度而成,第2组线性对照品溶液就由0.6ml的脱氢vc对照品储备液、0.6ml的l-木糖对照品储备液和0.6ml的l-苏糖酸钙对照品储备液在10ml量瓶中经稀释剂均匀稀释至刻度而成,第3组线性对照品溶液就由0.8ml的脱氢vc对照品储备液、0.8ml的l-木糖对照品储备液和0.8ml的l-苏糖酸钙对照品储备液在10ml量瓶中经稀释剂均匀稀释至刻度而成,第4组线性对照品溶液就由1.2ml的脱氢vc对照品储备液、1.2ml的l-木糖对照品储备液和1.2ml的l-苏糖酸钙对照品储备液在10ml量瓶中经稀释剂均匀稀释至刻度而成,第5组线性对照品溶液就由2.0ml的脱氢vc对照品储备液、2.0ml的l-木糖对照品储备液和2.0ml的l-苏糖酸钙对照品储备液在10ml量瓶中经稀释剂均匀稀释至刻度而成。下面结合具体实施例对本发明进行说明。实施例1一种检测维生素c药物中降解杂质含量的方法,采用高效液相色谱法进行检测,检测条件如下:高效液相色谱仪:沃特世e2695;色谱柱:hilic色谱柱,规格为4.6×250mm,5μm;柱温:30℃;流动相:缓冲盐溶液和乙腈的混合液,等度洗脱;流速:1ml/min;检测器:蒸发光散射检测器;检测器的漂移管温度:90℃;检测器的气体流速:2.5l/min;进样量:10μl。其中,所述混合液中缓冲盐溶液与乙腈的质量比为15:85,所述缓冲盐溶液的浓度为0.1mol/l,所述缓冲盐溶液为乙酸铵溶液。在上述检测条件下进行系统适用性试验:先分别精密量取脱氢vc对照品储备液、l-木糖对照品储备液和l-苏糖酸钙对照品储备液适量,用稀释剂稀释成每1ml中脱氢vc、l-木糖、l-苏糖酸各60μg的混合溶液,作为系统适用性试验溶液。稀释剂为水与乙腈的混合溶液,水与乙腈的质量比为50:50。然后将系统适用性试验溶液注入到高效液相色谱仪进行高效液相分析记录色谱图,结果见图1和下表1。表1、系统适用性试验结果结合杂质定位保留时间,图1保留时间为6.129分钟的色谱峰是脱氢vc的色谱峰,保留时间为11.866分钟的色谱峰是l-木糖的色谱峰,保留时间为35.780的色谱峰是l-苏糖酸的色谱峰。在上述色谱条件下,杂质与杂质之间分离度好,且峰形良好,分析时间短,满足中国药典的要求。实施例2一种检测维生素c药物中降解杂质含量的方法,采用高效液相色谱法进行检测,检测条件如下:高效液相色谱仪:沃特世e2695;色谱柱:hilic色谱柱,规格为4.6×250mm,5μm;柱温:25℃;流动相:缓冲盐溶液和乙腈的混合液,等度洗脱;流速:0.8ml/min;检测器:蒸发光散射检测器;检测器的漂移管温度:80℃;检测器的气体流速:1.5l/min;进样量:10μl。其中,所述混合液中缓冲盐溶液与乙腈的质量比为15:85,所述缓冲盐溶液的浓度为0.05mol/l,所述缓冲盐溶液为乙酸铵溶液。在上述检测条件下进行系统适用性试验:先分别精密量取脱氢vc对照品储备液、l-木糖对照品储备液和l-苏糖酸钙对照品储备液适量,用稀释剂稀释成每1ml中脱氢vc、l-木糖、l-苏糖酸各60μg的混合溶液,作为系统适用性试验溶液。稀释剂为水与乙腈的混合溶液,水与乙腈的质量比为40:60。然后将系统适用性试验溶液注入到高效液相色谱仪进行高效液相分析记录色谱图,结果见图2和下表2。表2、系统适用性试验结果峰#保留时间分离度理论塔板数高度(mau)对称因子17.278——809132751.66213.7145.617745920.89335.05413.65147633731.44结合杂质定位保留时间,图2保留时间为7.278分钟的色谱峰是脱氢vc的色谱峰,保留时间为13.714分钟的色谱峰是l-木糖的色谱峰,保留时间为35.054分钟的色谱峰是l-苏糖酸的色谱峰。在上述色谱条件下,杂质与杂质之间分离度好,且峰形良好,分析时间短,满足中国药典的要求。实施例3一种检测维生素c药物中降解杂质含量的方法,采用高效液相色谱法进行检测,检测条件如下:高效液相色谱仪:沃特世e2695;色谱柱:hilic色谱柱,规格为4.6×250mm,5μm;柱温:40℃;流动相:缓冲盐溶液和乙腈的混合液,等度洗脱;流速:1.2ml/min;检测器:蒸发光散射检测器;检测器的漂移管温度:100℃;检测器的气体流速:3.0l/min;进样量:10μl。其中,所述混合液中缓冲盐溶液与乙腈的质量比为20:80,所述缓冲盐溶液的浓度为0.2mol/l,所述缓冲盐溶液为甲酸铵溶液。在上述检测条件下进行系统适用性试验:先分别精密量取脱氢vc对照品储备液、l-木糖对照品储备液和l-苏糖酸钙对照品储备液适量,用稀释剂稀释成每1ml中脱氢vc、l-木糖、l-苏糖酸各60μg的混合溶液,作为系统适用性试验溶液。稀释剂为水与乙腈的混合溶液,水与乙腈的质量比为80:20。然后将系统适用性试验溶液注入到高效液相色谱仪进行高效液相分析记录色谱图,结果见图3和下表3。表3、系统适用性试验结果峰#保留时间分离度理论塔板数高度(mau)对称因子14.313——731813091.5226.9596.15176111531.09316.49916.0887423281.26结合杂质定位保留时间,图3保留时间为4.313分钟的色谱峰是脱氢vc的色谱峰,保留时间为6.959分钟的色谱峰是l-木糖的色谱峰,保留时间为16.499分钟的色谱峰是l-苏糖酸的色谱峰。在上述色谱条件下,杂质与杂质之间分离度好,且峰形良好,分析时间短,满足中国药典的要求。下面在实施例1的检测条件下通过试验对本发明的检测效果进行说明。1,专属性试验专属性试验1:取脱氢vc、l-木糖、l-苏糖酸、维生素c及维生素c的其它杂质(杂质c、杂质d、5-羟甲糠醛、异维生素c)对照品适量,用稀释剂制备成一定浓度的定位溶液,精密量取空白溶剂及各定位溶液10μl,分别注入高效液相色谱仪,按所述的色谱条件测定,记录色谱图。结果为上述维生素c及其它杂质均不干扰脱氢vc、l-木糖、l-苏糖酸的检测,专属性良好。结果见下表4。表4、专属性试验结果成分保留时间(min)空白溶剂未出峰脱氢vc6.3l-木糖12.4l-苏糖酸38.4杂质c未出峰杂质d6.8异维生素c25.35-羟甲糠醛未出峰糠醛未出峰维生素c33.2结果表明,在拟定的色谱条件下,空白无干扰,维生素c主峰及维生素c的其它降解杂质或工艺杂质(杂质c、杂质d、维生素c、糠醛、5-羟甲基糖醛)均不干扰目标峰检测。专属性试验2:强制降解试验精密取本品适量,用水-乙腈(50:50)定量稀释制成每1ml中含维生素40mg的溶液,作为未破坏供试品溶液。取在高温60℃下破坏一段时间后的样品适量,用水-乙腈(50:50)定量稀释制成每1ml中含维生素40mg的溶液,作为高温破坏供试品溶液。取在强光(5000lx)照射下放置3天后的样品适量,用水-乙腈(50:50)定量稀释制成每1ml中含维生素40mg的溶液,作为光照破坏供试品溶液。精密量取上述各溶液10μl,分别注入高效液相色谱仪,记录色谱图,试验结果见下表5。表5、强制降解试验结果条件脱氢vc峰面积l-木糖峰面积l-苏糖酸峰面积其它杂质峰面积未破坏样品8805未检出未检出3678光照破坏样品31432未检出4710未检出高温破坏样品22679未检出未检出未检出未破坏空白辅料未检出未检出未检出未检出本品在光照、高温条件下降解产生脱氢vc,在光照条件下降解产生l-苏糖酸,无降解杂质峰干扰目标峰检测。说明该色谱条件能有效检测本品的l-木糖、l-苏糖酸、脱氢vc,方法专属性良好。2、线性考察取脱氢vc、l-木糖、l-苏糖酸钙适量,l-苏糖酸钙用水适量溶解并制成含l-苏糖酸1mg/ml的储备液,脱氢vc、l-木糖用稀释剂溶解并稀释成1mg/ml的储备液。分别精密量取各杂质对照品储备液0.4ml、0.6ml、0.8ml、1.2ml、2.0ml至10ml量瓶中,用稀释剂稀释至刻度,摇匀,作为线性试验系列溶液。精密量取线性试验系列溶液各10μl,分别注入高效液相色谱仪,按所述的色谱条件测定,记录色谱图。以样品溶液浓度(μg/ml)的对数为横坐标、峰面积对数为纵坐标计算各杂质的线性回归方程。结果见下表6。表6、线性考察结果成分浓度范围回归方程r脱氢vc39.6~198.0y=1.847x+1.1800.999l-木糖41.5~207.4y=1.534x+1.5150.998l-苏糖酸41.7~208.4y=1.777x+1.1680.999试验结果表明,各杂质在约40μg~200μg范围内,即在主成分浓度(40mg/ml)的0.1%~0.5%范围内浓度与峰面积的对数呈线性关系。3、检测限、定量限考察取脱氢vc、l-木糖、l-苏糖酸钙适量,l-苏糖酸钙用水适量溶解并制成含l-苏糖酸1mg/ml的储备液,脱氢vc和l-木糖分别用稀释剂溶解并稀释成1mg/ml的储备液。分别取各储备液用稀释液稀释制成检测限溶液,取检测限溶液注入高效液相色谱仪,记录色谱图。以信噪比为3:1时的进样量作为其检测限,以信噪比为10:1时的进样量作为其定量限。结果见下表7。表7、检测限、定量限结果成分检测限浓度(μg/ml)检出量(ng)定量限浓度(μg/ml)定量限(ng)脱氢vc6.7679.999l-木糖29.729739.6396l-苏糖酸20.820831.9319结论:各杂质的检测限浓度均低于30μg/ml,即当样品浓度为40mg/ml时,含有0.08%以上的杂质即可被检出,各杂质的定量限浓度均低于40μg/ml,即当样品浓度为40mg/ml时,含有0.1%以上的杂质即可定量测定,检测灵敏度满足要求。4、进样精密度试验取脱氢vc、l-木糖、l-苏糖酸钙适量,l-苏糖酸钙用水适量溶解并制成含l-苏糖酸1mg/ml的储备液,脱氢vc和l-木糖分别用稀释剂溶解并稀释成1mg/ml的储备液。分别精密量取各杂质对照品储备液0.6ml至10ml量瓶中,用稀释剂稀释至刻度,摇匀,作为对照品溶液。照拟定的色谱条件进样6次,考察进样精密度,结果见下表8、表9。表8、进样精密度结果(峰面积)序号脱氢vc峰面积l-木糖峰面积l-苏糖酸峰面积132041200232540623281219963260153317081985025264432923201452540853254319510253946328282042925738rsd%1.5%1.5%1.1%表9、进样精密度结果(保留时间)序号脱氢vcl-木糖l-苏糖酸16.12911.96736.69226.1311.93336.74536.12912.02636.70246.1312.03236.76156.12512.02336.78666.12911.97936.787平均值6.12911.99336.746rsd%0.030.330.11结果表明,同一溶液多次进样的结果没有明显差异,各成分峰面积rsd均小于2.0%,各成分峰保留时间rsd均小于1.0%,系统精密度良好。5、重复性试验取脱氢vc、l-木糖、l-苏糖酸钙适量,l-苏糖酸钙用水适量溶解并制成含l-苏糖酸1mg/ml的储备液,脱氢vc和l-木糖分别用稀释剂溶解并稀释成1mg/ml的储备液。分别精密量取各杂质对照品储备液0.4ml、0.6ml、0.8ml、1.2ml、2.0ml至10ml量瓶中,用稀释剂稀释至刻度,摇匀,作为线性对照系列溶液。精密取本品适量,用水-乙腈(50:50)定量稀释制成每1ml中含维生素40mg的溶液,作为供试品溶液。平行制备6份。分别取线性对照系列溶液与准确度试验溶液进样分析,记录色谱图。根据线性对照溶液的浓度和峰面积,以对照品溶液浓度的对数值为横坐标,以相应的峰面积对数值为纵坐标,进行线性回归,计算回归方程。以回归方程计算供试品溶液中的杂质含量,结果见下表10。表10、重复性结果结论:由上述结果可知,本发明检测方法的重复性良好。6、中间精密度试验更换试验人员,在不同日期,精密量取“重复性”项下各杂质对照品储备液0.4ml、0.6ml、0.8ml、1.2ml至10ml量瓶中,用稀释剂稀释至刻度,摇匀,作为线性对照系列溶液。精密取本品适量,用水-乙腈(50:50)定量稀释制成每1ml中含维生素40mg的溶液,作为供试品溶液。平行制备6份。分别取线性对照系列溶液与供试品溶液进样,记录色谱图。根据线性对照溶液的浓度和峰面积,以对照品溶液浓度的对数值为横坐标,以相应的峰面积对数值为纵坐标,进行线性回归,计算回归方程。以回归方程计算供试品溶液中的杂质含量。并结合“重复性”试验项下结果,统计12份结果,考察方法中间精密度,结果见下表11。表11、中间精密度试验结果表上述结果表明,不同实验员在不同日期分别测定的共12份样品中检出已知杂质个数一致,检出杂质含量基本一致,rsd为7.0%,说明本方法中间精密度良好。7、溶液稳定性取脱氢vc、l-木糖、l-苏糖酸钙适量,l-苏糖酸钙用水适量溶解并制成含l-苏糖酸1mg/ml的储备液,脱氢vc和l-木糖分别用稀释剂溶解并稀释成1mg/ml的储备液。分别精密量取各杂质对照品储备液0.6ml至10ml量瓶中,用稀释剂稀释至刻度,摇匀,作为混合对照品溶液。取混合对照品溶液在室温下放置0、2、4、6、8小时后分别进样,考察溶液稳定性。结果见表12。表12、混合对照品溶液稳定性结果表时间0小时2小时4小时6小时8小时rsd%脱氢vc峰面积34138340113311332730329521.9l-木糖峰面积12109117891241711914122842.1l-苏糖酸峰面积72702737797366472583741790.96结果表明,混合对照品溶液各杂质的峰面积的rsd均小于2.1%,对照溶液在室温下放置8小时内稳定。8、准确度试验取脱氢vc、l-木糖、l-苏糖酸钙适量,l-苏糖酸钙用水适量溶解并制成含l-苏糖酸1mg/ml的储备液,脱氢vc和l-木糖分别用稀释剂溶解并稀释成1mg/ml的储备液。分别精密量取各杂质对照品储备液0.4ml、0.6ml、0.8ml、1.2ml、2.0ml至10ml量瓶中,用稀释剂稀释至刻度,摇匀,作为线性对照系列溶液。分别精密量取各杂质对照品储备液4.8ml、6ml、7.2ml至10ml量瓶中,用稀释剂稀释至刻度,摇匀,作为准确度贮备液1、2、3。表13、准确度试验溶液的配制按上表13分别准确移取贮备液1、2、3各1ml分别置10ml量瓶中,在相应量瓶中各加入维生素c400mg,加稀释剂溶解并稀释至刻度,摇匀,即得准确度试验溶液,每个浓度水平平行配制3份准确度试验溶液。分别取线性对照系列溶液与准确度试验溶液进样,按上述条件进行高效液相分析,记录色谱图。根据线性对照溶液的浓度和峰面积,以对照品溶液浓度的对数值为横坐标,以相应的峰面积对数值为纵坐标,进行线性回归,计算回归方程。以回归方程计算各杂质的测得量。结果见表14~16。表14、脱氢vc准确度试验结果表15、l-木糖准确度试验结果表16、l-苏糖酸准确度试验结果结论:杂质脱氢vc准确度试验溶液r1~r3平均回收率为97.5%,杂质l-木糖准确度试验溶液r1~r3平均回收率为95.1%,杂质l-苏糖酸准确度试验溶液r1~r3平均回收率为100.4%,符合要求(80.0%~120%)。各杂质9个回收率数据的rsd值分别为5.7%、4.3%、2.5%,均符合要求(rsd不得超过10.0%)。最后,本发明还进行了耐用性试验,具体如下:精密取本品适量,用水-乙腈(50:50)定量稀释制成每1ml中含维生素40mg的溶液,作为供试品溶液。精密量取各杂质对照品储备液0.4ml、0.6ml、0.8ml、1.2ml至10ml量瓶中,用稀释剂稀释至刻度,摇匀,作为线性对照品溶液。在原始色谱条件下同时改变柱温、流速及检测器漂移管的温度,分别进样对照品系列溶液与供试品溶液,考察方法耐用性。以“重复性”试验作为原始条件,考察结果见表17。表17、耐用性考察结果类别原始条件耐用性条件1耐用性条件2柱温30℃28℃32℃流速1ml/min0.9ml/min1.1ml/min漂移管温度90℃88℃92℃线性2#溶液中脱氢vc保留时间6.163min6.875min5.467min线性2#溶液中l-木糖保留时间12.007min13.741min10.509min线性2#溶液中l-苏糖酸保留时间37.080min42.035min31.606min样品中脱氢vc含量0.10%0.12%0.11%样品中l-木糖含量未检出未检出未检出样品中l--苏糖酸含量未检出未检出未检出上述结果表明,在同时改变柱温、流速及检测器漂移管的温度的情况下,混合对照品溶液中各杂质分离良好,检出杂质个数一致,检出杂质含量基本一致,方法耐用性良好。综上所述,本发明提供了一种维生素c药物中小分子极性化合物杂质的含量的新检测方法,各色谱峰之间分离度高,相互之间无干扰,可以同时实现对脱氢vc、l-木糖、l-苏糖酸的准确检测,而且操作简便,容易控制,检测成本低,并具有良好的线性关系,专属性、精密度、灵敏度、耐用性,检测结果准确可靠。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1