一种流式细胞分析装置的制作方法
本实用新型涉及医疗器械领域,尤其涉及一种流式细胞分析装置。
背景技术:
在血液细胞/细胞分析领域一般使用光散射原理或阻抗法(库尔特原理),对溶液中悬浮的细胞进行计数、体积(大小)、形态检测。
使用光散射原理检测细胞时,流式细胞术是核心技术难点,其基本方法是使用鞘液将样本细胞约束为单细胞流,经过传感器,由确定光斑尺寸的激光照射细胞探测散射光变化,产生不同幅值和数量的脉冲,从而对细胞进行计数和大小等信息的分析。使用阻抗法(库尔特原理)检测细胞时,经典的方法是样本由一个细小的微孔(几十微米)隔离,同时小孔两端设有正负电极,使小孔置于一定的电场中;在小孔的另一端通入负压吸取样本液,样本通过小孔时呈层流状态,细胞位置确定,每个细胞经过小孔时,瞬时小孔内电阻率上升,在电极上便会产生脉冲,记录脉冲数量、幅值,从而对细胞进行分析。
现有流式细胞装置存在以下问题:(1)不能在一个流路同时进行阻抗、光学两种方法学检测,因此无法实时校验计数结果,如果结果错误,只能再次检测。(2)两套模块需要两套配套液路结构支持功能,结构复杂,故障率高,使用成本高。
技术实现要素:
本实用新型的目的在于,解决现有技术中存在的上述不足之处。
为实现上述目的,第一方面,本实用新型提供一种流式细胞分析装置,包括流动室整流室,阻抗整流室,阻抗小孔,阻抗正电极,样本针,流动室,激光光源模块和散射光收集模块;样本针位于阻抗整流室内部,阻抗小孔位于阻抗整流室的后端,阻抗小孔的出口端连接阻抗正电极,样本针连接负极;阻抗整流室的后端位于流动室整流室的内部,流动室位于阻抗小孔的后端。
优选地,流动室包含边长为200为微米的正方形微流道。
优选地,流式细胞分析装置还包括激光光源模块和散射光收集模块,激光光源模块和散射光收集模块分别位于流动室的相对的两侧。
优选地,流动室包含边长为200为微米的正方形微流道。
第二方面,本实用新型提供一种流式细胞分析装置的补偿方法,应用于第一方面的流式细胞分析装置,包括以下步骤:
步骤一:使用存储器对阻抗信号进行缓存,其中,缓存深度为D=(L/v)*S;
步骤二:检测光学通道上升沿,得到光学通道上升沿触发时刻Ts和光学通道上升沿消抖时刻Tse;
步骤三:检测光学通道下降沿及峰值,得到光学通道下降沿触发时刻Tes和光学通道下降沿消抖时刻Te;
步骤四:设置光学通道脉冲前后扩展窗:根据光学通道上升沿触发时刻Ts得到扩展窗第一时刻Ts_ex,根据光学通道下降沿消抖时刻Te得到扩展窗第二时刻Te_ex;
步骤五:设置阻抗有效脉冲区间:阻抗有效脉冲区间的开始时刻为Ts_ex+D,结束时刻为Te_ex+D;
步骤六:检测阻抗通道上升沿,得到阻抗通道上升沿触发时刻Ts_i和阻抗通道上升沿消抖时刻Tse_i;
步骤七:检测阻抗通道下降沿及峰值,得到阻抗通道下降沿触发时刻Tes_i、阻抗通道下降沿消抖时刻Te_i和阻抗通道峰值时刻Tmax_i;
步骤八:光学通道与阻抗通道同一细胞信号特征同步:读取Tmax_i,当Tmax_i在Ts_ex+D至Te_ex+D时间段出现时,表示识别到同一细胞产生的光学通道信号及阻抗信号;
其中,S为模数转换器ADC的采样率,v为细胞从宝石孔中心流至光学检测中心平均流速,L为宝石孔中心至光学检测中心的距离。
优选地,在步骤八之后还包括:
步骤九:系统稳定性判断:当脉冲延时特征Pdl小于报警区间下限或者大于报警区间上限,其中,Pdl=Ts_rs/(Ts_ex-Te_ex),Ts_rs=(Tmax_i Ts_ex-D)。
本实用新型公开的流式细胞分析装置及补偿方法,具有以下效果:(1)结构清晰,组装简单,维护和制造成本低,可靠性高;(2)光学与阻抗检测集成一体,样本测试效率高;(3)二次鞘流保护样本不会污染传感器,同时信号质量好;(4)可靠的补偿算法,使流路结构复杂度减小。
附图说明
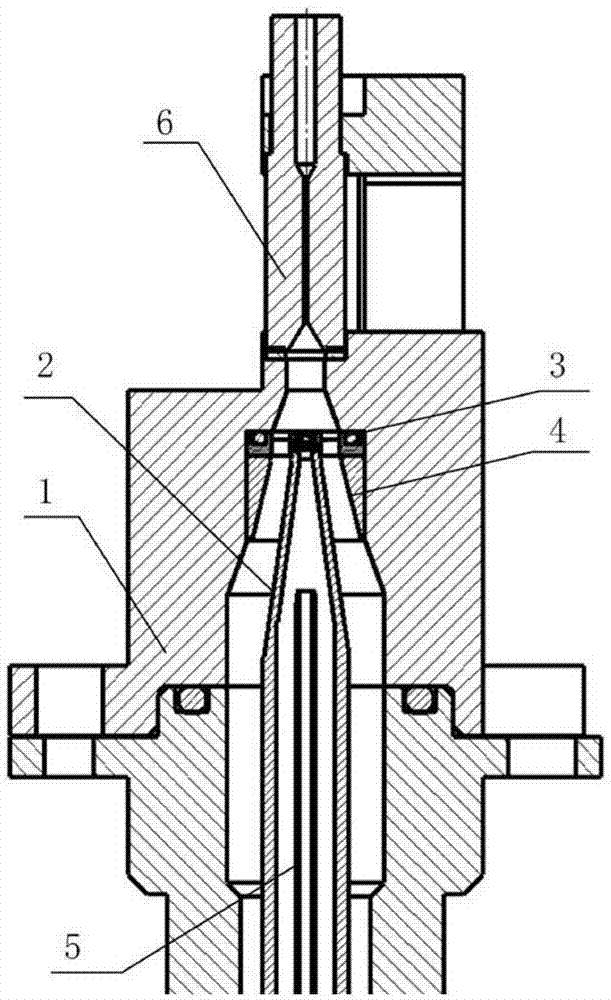
图1为本实用新型提供的一种流式细胞分析装置的结构示意图;
图2为本实用新型提供的一种流式细胞分析装置的工作原理示意图;
图3为本实用新型实施例提供的一种扩展窗中的有效脉冲示意图;
图4为本实用新型实施例提供的一种扩展窗中抛弃的异常脉冲图;
图5为本实用新型实施例提供的一种散射光脉冲信号识别图;
图6为本实用新型实施例提供的一种根据散射光脉冲信号生成扩展窗的示意图;
图7为本实用新型实施例提供的一种寻找阻抗脉冲信号区间的示意图;
图8为本实用新型实施例提供的一种识别阻抗脉冲信号峰值的示意图;
图9为本实用新型实施例提供的一种阻抗脉冲信号识别方法的示意图;
图10为本实用新型实施例提供的一种阻抗信号扩展窗内的有效脉冲的示意图;
图11为本实用新型实施例提供的一种方法稳定性判断的示意图。
具体实施方式
下面结合附图和实施例,对本实用新型的技术方案做进一步的详细描述。
如图1-2,本实用新型实施例提供的流式细胞分析装置,包括流动室整流室1,阻抗整流室2,阻抗小孔3,阻抗正电极4,样本针5,流动室6,激光光源模块7和散射光收集模块8;样本针5位于阻抗整流室2内部,阻抗小孔3位于阻抗整流室2的后端,阻抗小孔3的出口端连接阻抗正电极4,提供正向电压,样本针5连接负极,提供负向电压;阻抗整流室2的后端位于流动室整流室1的内部,流动室6位于阻抗小孔3的后端,激光光源模块7和散射光收集模块8分别位于流动室6的相对的两侧。具体工作过程如下:
细胞悬浊液由样本针5连接的管路进入,同时,阻抗整流室2内通入鞘液,当细胞流出样本针5时,由阻抗整流室2内鞘液包裹流向阻抗小孔3,其中,阻抗小孔3出口端连接阻抗正电极4,样本针5连接负极,并在阻抗小孔3的小孔中产生恒流检测电场。细胞经过阻抗小孔3时,置换掉阻抗小孔3中的鞘液,导致阻抗小孔3内电导率下降,电阻上升,同时产生细胞脉冲,其中,细胞大小不同,电阻也不同,因此脉冲幅度和宽度也不同,通过计数脉冲数量、幅值来区分细胞数量和大小。当细胞流出阻抗小孔3时,被流动室整流室1内的二次鞘流包裹形成单细胞流流向流动室6,激光光源模块7在流动室6的确定位置形成一定大小的光斑,并由散射光收集模块8接收。当细胞经过光斑时,不同大小的细胞遮挡光斑面积不同,散射光收集模块8收集的散射光也不同,每个细胞经过光斑都会触发产生一个散射光,并被散射光收集模块8收集,散射光收集模块8经过光电转换将收集的散射光转换成脉冲信号,通过分析脉冲数量、幅值来区分细胞数量和大小。
在一个示例中,流动室6包含边长为200为微米的正方形微流道9。
本实用新型实施例还提供一种上述装置的补偿方法,定义模数转换器(analog to digital converter,ADC)的可测量信号范围为0V~+4V,有效脉冲信号宽度为0.5uS~2uS,记作(wmin,wmax),ADC的采样率为40MHz,记作S;细胞从宝石孔中心10流至光学检测中心11平均流速为v,宝石孔中心10至光学检测中心11距离为L。该补偿方法包括以下步骤:
步骤一:使用可编程存储深度的FIFO存储器对阻抗信号进行缓存,其中,缓存深度为D=(L/v)*S;
步骤二:检测光学通道上升沿:设置光学通道上升沿触发电平Vsp为0.01V至0.3V之间,设置光学通道上升沿消抖电平Vsn为0.02V至0.45V之间;
a)如图5,当散射光检测通道电平大于Vsp时,记录该时刻为光学通道上升沿触发时刻Ts,第一计数累加器∑T1设置为1。
b)继续下一采集点Ts+n电平判断,n为第n次电平判断,检测的电平当小于Vsn时,对第一计数累加器∑T1加1。当∑T1大于最大有效脉冲宽度Wmax=(wmax*S)/2时,标记此脉冲为异常脉冲,并对第一异常脉冲计数器∑Cerror_o进行累加,结束本脉冲上升沿检测。当∑T1小于等于Wmax时,重复b)执行;当采集点Ts+n的电平大于电平Vsn时,标记此采集时刻为光学通道上升沿消抖时刻Tse,上升沿检测成功,记录采集点Ts+n电平至随机存取存储器(random access memory,RAM)中,记作Vmax。
步骤三:如图5,检测光学通道下降沿及峰值,光学通道下降沿及峰值检测。设置光学通道下降沿触发电平Vep为0.015V至0.4V之间,设置光学通道下降沿消抖电平Ven为0.01V至0.3V之间;通常设置Vep电平小于Vsn。
a)当散射光检测通道电平小于Vep时,记作该时刻为光学通道下降沿触发时刻Tes,第二计数累加器∑T2设置为1。
b)继续下一采集点Tes+m电平判断,m为第m次电平判断,当检测到的电平大于电平Ven时,对第二计数累加器∑T2加1。当∑T2大于最大有效脉冲宽度Wmax=(wmax*S)/2时,标记此脉冲为异常脉冲,并对第一异常脉冲计数器∑Cerror_o进行累加,结束本脉冲下降沿检测,当∑T2小于等于Wmax时,重复b)执行;当采集点Tes+m的电平小于电平Ven时,对计数累加器∑T2清零,标记该采集时刻为光学通道下降沿消抖时刻Te,下降沿检测成功。
在执行b阶段时,对每一次采集点电平与RAM中的Vmax进行比较,当此采集点电平大于RAM中的Vmax时,将此采集点电平记录至RAM中的Vmax,同时记录此采集时刻为光学通道峰值时刻Tmax_o。
步骤四:如图6,设置光学通道脉冲前后扩展窗:设置脉冲上升沿扩展窗Wnd_s为1uS,下降沿扩展窗Wnd_e为1uS。上升沿扩展窗采样点为S*Wnd_s,下降沿扩展窗采样点为S*Wnd_e。以采集时刻Ts向前推Wnd_s记录为扩展窗第一时刻Ts_ex;以采集时刻Te向后推Wnd_e记录为扩展窗第二时刻Te_ex。
步骤五:如图7,设置阻抗有效脉冲区间:以Ts_ex+D时刻开始至Te_ex+D时刻结束作为光学通道有效脉冲在阻抗通道的阻抗特性识别时间区间。
步骤六:如图9,检测阻抗通道上升沿,设置阻抗通道上升沿触发电平Vsp_i为0.01V至0.3V之间,设置阻抗通道上升沿消抖电平Vsn_i为0.02V至0.45V之间;
得到阻抗通道上升沿触发时刻Ts_i和阻抗通道上升沿消抖时刻Tse_i;
a)如图4,当阻抗检测通道电平大于Vsn_i取值范围时,对第二异常脉冲计数器∑Cerror_i进行累加,结束本脉冲上升沿检测。当阻抗检测通道电平大于Vsp_i时,标记该时刻为阻抗通道上升沿触发时刻Ts_i,第三计数累加器∑T3_i设置为1。
b)继续下一采集点Ts_i+n电平判断,n为第n次,当检测的电平小于电平Vsn_i时,对第三计数累加器∑T3_i加1。当∑T3_i大于最大有效脉冲宽度Wmax=(wmax*S)/2时,标记此脉冲为异常脉冲,并对第二异常脉冲计数器∑Cerror_i进行累加,结束本脉冲上升沿检测。当∑T3_i小于等于Wmax时,重复b)执行;当采集点Ts_i+n的电平大于电平Vsn_i时,标记此采集时刻为阻抗通道上升沿消抖时刻Tse_i,上升沿检测成功,记录采集点Ts_i+n电平至RAM中的Vmax_i。
步骤七:检测阻抗通道下降沿及峰值,设置触发电平Vep_i为0.015V至0.4V之间,设置消抖电平Ven_i为0.01V至0.3之间;通常设置Vep_i电平小于Vsn_i。
a)当阻抗检测通道电平小于Vep_i时,标记该时刻为阻抗通道下降沿触发时刻Tes_i,第四计数累加器∑T4_i设置为1。
b)继续下一采集点Tes_i+m电平判断,m为第m次电平判断,当检测到的电平大于电平Ven_i时,对第四计数累加器∑T4_i加1。当∑T4_i大于最大有效脉冲宽度Wmax=(wmax*S)/2时,标记此脉冲为异常脉冲,并对第二异常脉冲计数器∑Cerror_i进行累加,结束本脉冲上升沿检测,当∑T4_i小于等于Wmax_i时,重复b)执行;当采集点Tes_i+m电平小于电平Ven_i时,对第四计数累加器∑T4_i清零,标记此采集时刻为阻抗通道下降沿消抖时刻Te_i,下降沿检测成功,如图3。
如图8,在执行b阶段时,对每一次采集点电平与RAM中的Vmax_i进行比较,当此采集点电平大于RAM中的Vmax_i时,将此采集点电平记录至RAM中的Vmax_i,同时记录此采集时刻为阻抗通道峰值时刻Tmax_i。如图9中所标识。
步骤八:如图10所示,光学通道与阻抗通道同一细胞信号特征同步:读取Tmax_i,当Tmax_i在Ts_ex+D至Te_ex+D时间段出现时,表示识别到同一细胞产生的光学通道信号及阻抗信号。
在一个示例中,在所述步骤八之后还包括步骤九:系统稳定性判断:设置对步骤八识别到的信号时间进行判读,标记(Ts_ex+D-Tmax_i)为Ts_rs,记录此脉冲延时特征Pdl=Ts_rs/(Ts_ex-Te_ex)。对于每次样本测量,统计所有脉冲的延时特征,计算其均值A,当均值大于0.5时,表示细胞从阻抗通道至光学通道流经时间变短,当均值小于0.5时,表示细胞从阻抗通道至光学通道流经时间变长。设置时间报警区间下限为0.4,设置上限为0.6,如图11。当测试样本均值A未在报警区间内时,对仪器进行报警。应当理解,根据设计需求,报警区间下限和上限是可以改变的。
以上的具体实施方式,对本实用新型的目的、技术方案和有益效果进行了进一步详细说明,所应理解的是,以上仅为本实用新型的具体实施方式而已,并不用于限定本实用新型的保护范围,凡在本实用新型的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本实用新型的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!