乌美溴铵维兰特罗吸入粉雾剂微细粒子剂量的检测方法与流程
1.本发明涉及分析化学技术领域,尤其是涉及一种乌美溴铵维兰特罗吸入粉雾剂微细粒子剂量的检测方法。
背景技术:
2.呼吸系统疾病是常见病、高发病,致死率仅次于肿瘤和心血管病,哮喘和慢性阻塞性肺病(copd)是世界公认的医学难题。我国有哮喘患者超过3000万,copd患者超过8000万,吸入制剂是国际公认治疗哮喘和copd的首选药物,但目前有70%的患者从未使用吸入疗法,农村地区长期使用吸入药物治疗者仅占4.46%,大部分的患者都通过打针吃药治疗哮喘,从而导致心血管副作用频现。
3.吸入制剂主要分为气雾剂和粉雾剂,吸入粉雾剂相较气雾剂具有易于使用,患者主动吸入药粉;无抛射剂氟利昂,避免对大气环境污染;计量准确,无超剂量给药的危险;不含防腐剂和乙醇等溶剂,对病变黏膜无刺激性;药物呈干粉状,稳定性好,干扰因素少等优点。
4.乌美溴铵维兰特罗吸入粉雾剂是我公司开发的4类仿制药。具有长效支气管扩张作用,适用于慢性阻塞性肺病(copd)的长期维持治疗,一日一次用于缓解copd患者的症状。乌美溴铵是长效毒蕈碱受体拮抗剂,主要通过竞争性抑制乙酰胆碱与呼吸道平滑肌上m3型毒蕈碱受体的结合而发挥支气管扩张作用。维兰特罗是选择性长效β2肾上腺素受体激动剂,对细胞内腺苷酸环化酶有活化作用,该酶可催化atp转化为环状-3’,5
’-
磷酸腺苷camp水平,松弛支气管平滑肌并抑制细胞(尤其是肥大细胞)释放速发型超敏反应介质。与单独给药相比,乌美溴铵和三苯乙酸维兰特罗联合吸入给药的单药全身暴露量(auc和cmax)相似或较低,复方中单药对其他成分暴露量没有增加效应。联合给药在起效时能够通过双重作用通路实现机制互补,达到优化气道舒化的效果,起效比较快,而且能够达到24小时长效绩效的特点,可让患者不适的情况快速得到改善,并且能够稳定提高肺功能,缓解慢性阻塞性肺炎所带来的一系列不适症状。
5.三苯乙酸维兰特罗的分子式为c
24
h
33
cl2no5·
c
20
h
16
o2,结构式(i)如下:
[0006][0007]
乌美溴铵的分子式为c
29
h
34
brno2,结构式(ii)如下:
[0008]
[0009]
经文献调研,未查询到任何文献及药典同时对乌美溴铵维兰特罗吸入粉雾剂中有效成分乌美溴铵和三苯乙酸维兰特罗的微细粒子剂量进行测定的方法。
[0010]
有鉴于此,特提出本发明。
技术实现要素:
[0011]
本发明的主要目的在于提供一种乌美溴铵维兰特罗吸入粉雾剂微细粒子剂量的检测方法,以期至少部分地解决上述技术问题中的至少之一。
[0012]
本发明提供了一种乌美溴铵维兰特罗吸入粉雾剂微细粒子剂量的检测方法,采用高效液相色谱法,色谱条件包括:采用十八烷基硅烷键合硅胶填充剂的色谱柱;检测器:维兰特罗使用荧光检测器,乌美溴铵使用紫外检测器;流动相由流动相a和流动相b组成,流动相a:三氟乙酸溶液,流动相b:含有三氟乙酸的乙腈溶液,按照下表进行梯度洗脱:
[0013]
时间(min)流动相a(%)流动相b(%)0a1b13.5-4.0a2b2
[0014]
其中,a1=63-67%,a2=28-32;b1=33-37%,b2=68-72。
[0015]
进一步的,采用高效液相色谱法,色谱条件包括:采用十八烷基硅烷键合硅胶填充剂的色谱柱;检测器:维兰特罗使用荧光检测器,,乌美溴铵使用紫外检测器;流动相由流动相a和流动相b组成,流动相a:三氟乙酸溶液,流动相b:含有三氟乙酸的乙腈溶液,按照下表进行梯度洗脱:
[0016]
时间(min)流动相a(%)流动相b(%)0a1b13.5-4.0a2b24.1-4.6a1b15.5-6.0a1b1
[0017]
其中,a1=63-67%,a2=28-32;b1=33-37%,b2=68-72。
[0018]
进一步的,所述流动相a为0.05-0.15vol%的三氟乙酸溶液。
[0019]
进一步的,所述流动相a为0.1vol%的三氟乙酸溶液。
[0020]
进一步的,所述流动相b为含有0.05-0.15vol%的三氟乙酸的乙腈溶液。
[0021]
进一步的,所述流动相b为含有0.1vol%的三氟乙酸的乙腈溶液。
[0022]
进一步的,所述维兰特罗使用荧光检测器,激发波长为220-230nm,检测波长为310-320nm。
[0023]
进一步的,所述维兰特罗使用荧光检测器,激发波长为225nm,检测波长为315nm。
[0024]
进一步的,所述乌美溴铵使用紫外检测器,检测波长为210-230nm。
[0025]
进一步的,所述乌美溴铵使用紫外检测器,检测波长为220nm。
[0026]
进一步的,所用柱温为28-32℃。
[0027]
进一步的,所用柱温为30℃。
[0028]
进一步的,待测样品采用甲醇和水的混合液溶解。
[0029]
进一步的,所述甲醇和水的体积比为60:40。
[0030]
进一步的,所用流速为0.8-1.2ml/min。
[0031]
进一步的,所用流速为0.9-1.1ml/min。
[0032]
进一步的,所用流速为1.0ml/min。
[0033]
进一步的,所用进样量为90-110μl。
[0034]
进一步的,所用进样量为100μl。
[0035]
进一步的,采用高效液相色谱法,色谱条件包括:采用十八烷基硅烷键合硅胶填充剂的色谱柱;检测器:维兰特罗使用荧光检测器,激发波长为220-230nm,检测波长为310-320nm,乌美溴铵使用紫外检测器,检测波长为210-230nm;流动相由流动相a和流动相b组成,流动相a:三氟乙酸溶液,流动相b:含有三氟乙酸的乙腈溶液,按照下表进行梯度洗脱:
[0036]
时间(min)流动相a(%)流动相b(%)065354.03070。
[0037]
进一步的,采用高效液相色谱法,色谱条件包括:采用十八烷基硅烷键合硅胶填充剂的色谱柱;检测器:维兰特罗使用荧光检测器,激发波长为220-230nm,检测波长为310-320nm,乌美溴铵使用紫外检测器,检测波长为210-230nm;流动相由流动相a和流动相b组成,流动相a:三氟乙酸溶液,流动相b:含有三氟乙酸的乙腈溶液,按照下表进行梯度洗脱:
[0038]
时间(min)流动相a(%)流动相b(%)065354.030704.165356.06535。
[0039]
进一步的,采用高效液相色谱法,色谱条件包括:采用十八烷基硅烷键合硅胶填充剂的色谱柱;检测器:维兰特罗使用荧光检测器,激发波长为225nm,检测波长为315nm,乌美溴铵使用紫外检测器,检测波长为220nm;流动相由流动相a和流动相b组成,流动相a:0.1vol%的三氟乙酸溶液,流动相b:含有0.1vol%的三氟乙酸的乙腈溶液,按照下表进行梯度洗脱:
[0040]
时间(min)流动相a(%)流动相b(%)065354.030704.165356.06535。
[0041]
与现有技术相比,本发明具有以下有益效果:
[0042]
本发明提供的乌美溴铵维兰特罗吸入粉雾剂微细粒子剂量的检测方法,根据乌美溴铵和三苯乙酸维兰特罗的理化性质,通过优选检测器、流动相和洗脱梯度,开发了一套液相色谱体系,使用一种流动相条件可快速准确检测乌美溴铵维兰特罗吸入粉雾剂中乌美溴铵和三苯乙酸维兰特罗两种成分的微细粒子剂量;该检测方法的优点是:操作简便,测定结
果准确可靠,专属性强,耐用性好,灵敏度高,检测时间较短。
附图说明
[0043]
为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
[0044]
图1为荧光通道三苯乙酸维兰特罗空白辅料的hplc色谱图;
[0045]
图2为紫外通道乌美溴铵空白辅料的hplc色谱图;
[0046]
图3为荧光通道三苯乙酸维兰特罗空白溶剂的hplc色谱图;
[0047]
图4紫外通道乌美溴铵空白溶剂的hplc色谱图;
[0048]
图5为荧光通道三苯乙酸维兰特罗对照品溶液的hplc色谱图;
[0049]
图6为紫外通道乌美溴铵对照品溶液的hplc色谱图;
[0050]
图7为荧光通道三苯乙酸维兰特罗ngi测试的hplc色谱图;
[0051]
图8为紫外通道乌美溴铵ngi测试的hplc色谱图;
[0052]
图9为乌美溴铵的系统适用性试验的hplc色谱图;
[0053]
图10为三苯乙酸维兰特罗的系统适用性试验的hplc谱图。
具体实施方式
[0054]
下面将结合实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限制本发明的范围。实施例中未注明具体条件者,按照常规条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
[0055]
水,来自屈臣氏;
[0056]
乙腈(色谱纯),来自tedia;
[0057]
三氟乙酸(分析纯),来自天津市科密欧化学试剂有限公司;
[0058]
乌美溴铵工作对照品(纯度99.63%),来自天津药业研究院有限公司;
[0059]
三苯乙酸维兰特罗工作对照品(纯度99.11%),来自天津药业研究院有限公司;
[0060]
乌美溴铵维兰特罗吸入粉雾剂,来自天津药业研究院有限公司。
[0061]
实施例1专属性试验
[0062]
供试品溶液:依法连接装置(中国药典2015年版四部通则0951装置3*),使用前,收集杯1中加19.25%(w/v)聚乙二醇200丙酮溶液4ml,其余收集杯中加19.25%(w/v)聚乙二醇200丙酮溶液2ml,放置待丙酮挥干,预分离器中加入甲醇-水(60:40)15ml,外部过滤器放置专用滤纸,调节流速至60l/min,检查控制阀的压降比,p3/p2应不大于0.5。取本品1盒,拉动开关,插入适配器,开启真空泵,抽气4s,重复吸出第1、8、16、23和30吸的剂量(其余各吸在专用装置中弃去,流速调节至(60
±
2)l/min),每吸之间至少等待30s,关闭泵,取下吸入装置,称量,记录读数,共测试5吸。照下表分別用相应体积的甲醇-水(60:40)洗涤各部件提取样品,振摇使溶解,滤过,取续滤液作为ngi供试品溶液。
[0063][0064][0065]
混合对照品溶液:取乌美溴铵与三苯乙酸维兰特罗对照品适量,精密称定,加甲醇-水(60:40)溶解并定量稀释制成每1ml中分别含乌美溴铵与维兰特罗约1.1μg和0.25μg的混合对照品溶液;
[0066]
再取乌美溴铵对照品适量,同法制成每1ml中含乌美溴铵约1.1μg的乌美溴铵对照品溶液;
[0067]
再取三苯乙酸维兰特罗对照品适量,同法制成每1ml中含维兰特罗约0.25μg的三苯乙酸维兰特罗对照品溶液。
[0068]
空白辅料溶液:同法配制和上述主药量成处方比例的辅料溶液,作为空白辅料溶液。
[0069]
空白溶剂:甲醇-水(60:40)。
[0070]
实施例1-1
[0071]
色谱条件:
[0072]
色谱柱:安捷伦zorbax sb-c18(50
×
4.6mm,1.8μm);
[0073]
流动相:流动相a:0.1vol%三氟乙酸溶液,流动相b:含有0.1vol%的三氟乙酸的乙腈溶液;
[0074]
检测波长:维兰特罗使用荧光检测器,激发波长为225nm,检测波长为315nm,乌美溴铵用紫外检测器,为220nm;
[0075]
柱温:30℃;
[0076]
流速:1.0ml/min;
[0077]
进样量:100μl;
[0078]
按照下表进行梯度洗脱:
[0079]
时间(min)流动相a(%)流动相b(%)065354.030704.165356.06535。
[0080]
分别精密量取上述各溶液100μl,注入液相色谱仪,记录色谱图。荧光通道三苯乙酸维兰特罗空白辅料的hplc色谱图如图1所示,紫外通道乌美溴铵空白辅料的hplc色谱图如图2所示,荧光通道三苯乙酸维兰特罗空白溶剂的hplc色谱图如图3所示,紫外通道乌美溴铵空白溶剂的hplc色谱图如图4所示,荧光通道三苯乙酸维兰特罗对照品溶液的hplc色谱图如图5所示,紫外通道乌美溴铵对照品溶液的hplc色谱图如图6所示,荧光通道三苯乙酸维兰特罗ngi测试的hplc色谱图如图7所示,紫外通道乌美溴铵ngi测试的hplc色谱图如图8所示。
[0081]
按外标法以乌美溴铵和维兰特罗的峰面积分别计算ngi各级乌美溴铵和维兰特罗的质量,再根据每级乌美溴铵和维兰特罗的质量,用“copley inhaler testing dataanalysis software”软件计算小于5.0μm的微细粒子药物量,结果如表1所示。
[0082]
表1微细粒子剂量测定结果
[0083][0084]
由图1-8可知,本实施例检测方法下的色谱条件,空白辅料和溶剂对主药无干扰,乌美溴铵和维兰特罗分离度良好,且均无相邻杂质峰。
[0085]
实施例1-2
[0086]
色谱条件:
[0087]
色谱柱:安捷伦zorbax sb-c18(50
×
4.6mm,1.8μm);
[0088]
流动相:流动相a:0.05vol%三氟乙酸溶液,流动相b:含有0.15vol%的三氟乙酸的乙腈溶液;
[0089]
检测波长:维兰特罗使用荧光检测器,激发波长为220nm,检测波长为320nm,乌美溴铵用紫外检测器,为210nm;
[0090]
柱温:31℃;
[0091]
流速:0.9ml/min;
[0092]
进样量:110μl;
[0093]
按照下表进行梯度洗脱:
[0094]
时间(min)流动相a(%)流动相b(%)063373.532684.663375.56337。
[0095]
分别精密量取上述各溶液100μl,注入液相色谱仪,记录色谱图。由于本实施例的色谱图与实施例1-1的色谱图差别不大,在此未提供。
[0096]
按外标法以乌美溴铵和维兰特罗的峰面积分别计算ngi各级乌美溴铵和维兰特罗的质量,再根据每级乌美溴铵和维兰特罗的质量,用“copley inhaler testing dataanalysis software”软件计算小于5.0μm的微细粒子药物量,结果如表2所示。
[0097]
表2微细粒子剂量测定结果
[0098][0099]
本实施例检测方法下的色谱条件,空白辅料和溶剂对主药无干扰,乌美溴铵和维兰特罗分离度良好,且均无相邻杂质峰。
[0100]
实施例1-3
[0101]
色谱条件:
[0102]
色谱柱:安捷伦zorbax sb-c18(50
×
4.6mm,1.8μm);
[0103]
流动相:流动相a:0.15vol%三氟乙酸溶液,流动相b:含有0.05vol%的三氟乙酸的乙腈溶液;
[0104]
检测波长:维兰特罗使用荧光检测器,激发波长为230nm,检测波长为310nm,乌美溴铵用紫外检测器,为230nm;
[0105]
柱温:29℃;
[0106]
流速:1.1ml/min;
[0107]
进样量:90μl;
[0108]
按照下表进行梯度洗脱:
[0109]
时间(min)流动相a(%)流动相b(%)067333.828724.467335.86733。
[0110]
分别精密量取上述各溶液100μl,注入液相色谱仪,记录色谱图。由于本实施例的色谱图与实施例1-1的色谱图差别不大,在此未提供。
[0111]
按外标法以乌美溴铵和维兰特罗的峰面积分别计算ngi各级乌美溴铵和维兰特罗的质量,再根据每级乌美溴铵和维兰特罗的质量,用“copley inhaler testing dataanalysis software”软件计算小于5.0μm的微细粒子药物量,结果如表3所示。
[0112]
表3微细粒子剂量测定结果
[0113][0114]
本实施例检测方法下的色谱条件,空白辅料和溶剂对主药无干扰,乌美溴铵和维兰特罗分离度良好,且均无相邻杂质峰。
[0115]
实施例1-4
[0116]
色谱条件:
[0117]
色谱柱:安捷伦zorbax sb-c18(50
×
4.6mm,1.8μm);
[0118]
流动相:流动相a:0.08vol%三氟乙酸溶液,流动相b:含有0.12vol%的三氟乙酸
的乙腈溶液;
[0119]
检测波长:维兰特罗使用荧光检测器,激发波长为223nm,检测波长为317nm,乌美溴铵用紫外检测器,为218nm;
[0120]
柱温:28℃;
[0121]
流速:0.8ml/min;
[0122]
进样量:95μl;
[0123]
按照下表进行梯度洗脱:
[0124]
时间(min)流动相a(%)流动相b(%)066344.02971。
[0125]
分别精密量取上述各溶液100μl,注入液相色谱仪,记录色谱图。由于本实施例的色谱图与实施例1-1的色谱图差别不大,在此未提供。
[0126]
按外标法以乌美溴铵和维兰特罗的峰面积分别计算ngi各级乌美溴铵和维兰特罗的质量,再根据每级乌美溴铵和维兰特罗的质量,用“copley inhaler testing data analysis software”软件计算小于5.0μm的微细粒子药物量,结果如表4所示。
[0127]
表4微细粒子剂量测定结果
[0128][0129]
本实施例检测方法下的色谱条件,空白辅料和溶剂对主药无干扰,乌美溴铵和维兰特罗分离度良好,且均无相邻杂质峰。
[0130]
实施例1-5
[0131]
色谱条件:
[0132]
色谱柱:安捷伦zorbax sb-c18(50
×
4.6mm,1.8μm);
[0133]
流动相:流动相a:0.12vol%三氟乙酸溶液,流动相b:含有0.08vol%的三氟乙酸的乙腈溶液;
[0134]
检测波长:维兰特罗使用荧光检测器,激发波长为227nm,检测波长为312nm,乌美溴铵用紫外检测器,为222nm;
[0135]
柱温:32℃;
[0136]
流速:1.2ml/min;
[0137]
进样量:105μl;
[0138]
按照下表进行梯度洗脱:
[0139]
时间(min)流动相a(%)流动相b(%)064364.03169。
[0140]
分别精密量取上述各溶液100μl,注入液相色谱仪,记录色谱图。由于本实施例的
色谱图与实施例1-1的色谱图差别不大,在此未提供。
[0141]
按外标法以乌美溴铵和维兰特罗的峰面积分别计算ngi各级乌美溴铵和维兰特罗的质量,再根据每级乌美溴铵和维兰特罗的质量,用“copley inhaler testing data analysis software”软件计算小于5.0μm的微细粒子药物量,结果如表5所示。
[0142]
表5微细粒子剂量测定结果
[0143][0144]
本实施例检测方法下的色谱条件,空白辅料和溶剂对主药无干扰,乌美溴铵和维兰特罗分离度良好,且均无相邻杂质峰。
[0145]
实施例2系统适用性试验
[0146]
对照品溶液:精密称取乌美溴铵对照品15mg置于100ml量瓶中,用甲醇-水(60:40)溶解并稀释至刻度,摇匀,作为乌美溴铵贮备液,精密量取乌美溴铵贮备液1ml置于25ml量瓶中,用甲醇-水(60:40)溶解并稀释至刻度,摇匀,作为贮备液a;
[0147]
精密称取三苯乙酸维兰特罗对照品20mg置于100ml量瓶中,用甲醇-水(60:40)溶解并稀释至刻度,摇匀,作为三苯乙酸维兰特罗贮备液,精密量取三苯乙酸维兰特罗贮备液1ml置于50ml量瓶中,用甲醇-水(60:40)溶解并稀释至刻度,摇匀,作为贮备液b;
[0148]
分别精密量取贮备液a和b各1ml,置于10ml量瓶中,用甲醇-水(60:40)溶解并稀释至刻度,摇匀,作为系统适用性溶液。
[0149]
色谱条件:
[0150]
色谱柱:安捷伦zorbax sb-c18(50
×
4.6mm,1.8μm);
[0151]
流动相:流动相a:0.1vol%三氟乙酸溶液,流动相b:含有0.1vol%的三氟乙酸的乙腈溶液;
[0152]
检测波长:维兰特罗使用荧光检测器,激发波长为225nm,检测波长为315nm,乌美溴铵用紫外检测器,为220nm;
[0153]
柱温:30℃;
[0154]
流速:1.0ml/min;
[0155]
进样量:100μl;
[0156]
按照下表进行梯度洗脱:
[0157]
时间(min)流动相a(%)流动相b(%)065354.030704.165356.06535。
[0158]
取对系统适用性溶液,连续进样6针,考察色谱条件的系统适用性。乌美溴铵的系统适用性试验的hplc色谱图如图9所示,检测数据如表6所示。
[0159]
表6乌美溴铵的系统适用性结果
[0160][0161]
三苯乙酸维兰特罗的系统适用性试验的hplc色谱图如图10所示,检测数据如表7所示。
[0162]
表7三苯乙酸维兰特罗的系统适用性结果
[0163][0164]
由表6-7可知,6针重复进样,乌美溴铵峰面积的rsd值为0.23%<2.0%;乌美溴铵保留时间的rsd为0.51%<1.0%;维兰特罗峰面积的rsd值为0.60%<2.0%;维兰特罗保留时间的rsd为0.20%<1.0%;乌美溴铵和维兰特罗峰的理论塔板数均>3000,说明此微细粒子剂量测定方法具有较好的系统适用性。
[0165]
实施例3耐用性试验
[0166]
供试品溶液:依法连接装置(中国药典2015年版四部通则0951装置3*),使用前,收集杯1中加19.25%(w/v)聚乙二醇200丙酮溶液4ml,其余收集杯中加19.25%(w/v)聚乙二醇200丙酮溶液2ml,放置待丙酮挥干,预分离器中加入甲醇-水(60:40)15ml,外部过滤器放置专用滤纸,调节流速至60l/min,检查控制阀的压降比,p3/p2应不大于0.5。取本品1盒,拉动开关,插入适配器,开启真空泵,抽气4s,重复吸出第1、8、16、23和30吸的剂量(其余各吸在专用装置中弃去,流速调节至(60
±
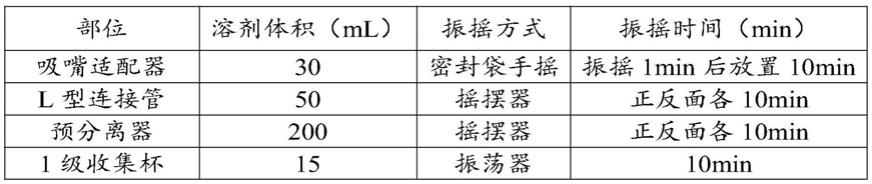
2)l/min),每吸之间至少等待30s,关闭泵,取下吸入装置,称量,记录读数,共测试5吸。照下表分別用相应体积的甲醇-水(60:40)洗涤各部件提取样品,振摇使溶解,滤过,取续滤液作为ngi供试品溶液。
[0167]
部位溶剂体积(ml)振摇方式振摇时间(min)吸嘴适配器30密封袋手摇振摇1min后放置10minl型连接管50摇摆器正反面各10min预分离器200摇摆器正反面各10min1级收集杯15振荡器10min2级收集杯15振荡器10min3级收集杯15振荡器10min4级收集杯15振荡器10min5级收集杯15振荡器10min6级收集杯15振荡器10min7级收集杯15振荡器10minmoc级收集杯100振荡器10min
[0168]
对照品溶液:精密称取乌美溴铵对照品15mg置于100ml量瓶中,用甲醇-水(60:40)溶解并稀释至刻度,摇匀,作为乌美溴铵贮备液,精密量取乌美溴铵贮备液1ml置于25ml量瓶中,用甲醇-水(60:40)溶解并稀释至刻度,摇匀,作为贮备液a;
[0169]
精密称取三苯乙酸维兰特罗对照品20mg置于100ml量瓶中,用甲醇-水(60:40)溶解并稀释至刻度,摇匀,作为三苯乙酸维兰特罗贮备液,精密量取三苯乙酸维兰特罗贮备液1ml置于50ml量瓶中,用甲醇-水(60:40)溶解并稀释至刻度,摇匀,作为贮备液b;
[0170]
分别精密量取贮备液a和b各1ml,置于10ml量瓶中,用甲醇-水(60:40)溶解并稀释至刻度,摇匀,作为对照品溶液。
[0171]
原色谱条件:
[0172]
色谱柱:安捷伦zorbax sb-c18(50
×
4.6mm,1.8μm);
[0173]
流动相:流动相a:0.1vol%三氟乙酸溶液,流动相b:含有0.1vol%的三氟乙酸的乙腈溶液;
[0174]
检测波长:维兰特罗使用荧光检测器,激发波长为225nm,检测波长为315nm,乌美溴铵用紫外检测器,为220nm;
[0175]
柱温:30℃;
[0176]
流速:1.0ml/min;
[0177]
进样量:100μl;
[0178]
梯度洗脱程序:
[0179]
时间(min)流动相a(%)流动相b(%)065354.030704.165356.06535。
[0180]
对检测波长、柱温、流速和流动相初始比例做微小变动,检测波长、柱温、流速和流动相初始比例变化条件如下:
[0181][0182]
分别精密量取上述各溶液100μl,在各变化的色谱条件下进行检测。按外标法以乌美溴铵和维兰特罗的峰面积分别计算ngi各级乌美溴铵和维兰特罗的质量,再根据每级乌美溴铵和维兰特罗的质量,用“copley inhaler testing data analysis software”软件计算小于5.0μm的微细粒子药物量。观察原色谱条件做微小变动前后测定结果的一致性,结果如表8-11所示。
[0183]
表8流速变化微细粒子剂量测定结果
[0184][0185]
表9柱温变化微细粒子剂量测定结果
[0186][0187]
表10检测波长变化微细粒子剂量测定结果
[0188][0189]
表11流动相比例变化微细粒子剂量测定结果
[0190][0191]
由表8-11可知,当流速、柱温、检测波长和流动初始相比例发生微小变化时,测定供试品溶液中乌美溴铵及维兰特罗的微细粒子剂量均无明显差异,rsd值均<2.0%,说明本研究提供的测定方法耐用性良好,可以满足微细粒子剂量测定的要求。
[0192]
实施例4灵敏度试验
[0193]
乌美溴铵和维兰特罗检出限:取含乌美溴铵和维兰特罗浓度分别为为0.511μg/ml和0.049μg/ml的对照品溶液,进行逐级稀释,依次进样,记录色谱图,取色谱图中乌美溴铵和维兰特罗信噪比在2-4时的进样浓度记为检测限,经考察,乌美溴铵主峰信噪比为4.12,维兰特罗主峰信噪比为3.86,因此乌美溴铵和维兰特罗微的最小检出限分别为0.0025μg/ml和0.00024μg/ml。
[0194]
乌美溴铵和维兰特罗定量限:取含乌美溴铵和维兰特罗浓度分别为为0.511μg/ml和0.049μg/ml的对照品溶液,进行逐级稀释,依次进样,记录色谱图,取色谱图中乌美溴铵
和维兰特罗信噪比在9-11时的进样浓度记为检测限,经考察,乌美溴铵主峰信噪比为11.98,维兰特罗主峰信噪比为11.42,因此乌美溴铵和维兰特罗微的定量限分别为0.0511μg/ml和0.0049μg/ml。
[0195]
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1