用于检测NTRK融合蛋白的组织化学和细胞化学方法与流程
用于检测ntrk融合蛋白的组织化学和细胞化学方法
1.相关专利申请的交叉引用
2.本申请要求于2018年9月13日提交的题为histochemical and cytochemical methods for detecting ntrk fusion proteins的美国临时专利申请号62/731,032的权益,其内容通过引用整体并入本文。
3.通过引用并入序列表
4.本申请在此通过引用并入以计算机可读格式随本文提交的序列表,该序列表具有文件名“p35023
‑
wo pct fling sequence listing”,创建于2019年9月9日,大小为21,260字节。
技术领域
5.除其他外,本公开涉及用于融合蛋白的组织化学和细胞化学检测的方法,该融合蛋白涉及ntrk基因产物;可用于此类方法中的材料、试剂盒和系统;以及执行此类方法所产生的产品。
背景技术:
6.神经营养酪氨酸受体激酶(ntrk1、ntrk2和ntrk3)为编码受体酪氨酸激酶蛋白(trka、trkb和trkc)的基因家族,其在中枢和外周神经系统的发育和成熟过程中发挥作用(barbacid i、barbacid ii、lemmon&schlessinger和klein)。在癌症中,三种ntrk基因中的一种的完整激酶结构域可以与各种上游配偶体(例如etv6、lmna、tpm3)融合,其使用促进二聚化的结构基序取代trk蛋白的配体结合结构域(eide,luberg,&vaishnavi)。这导致trk信号传导的组成性激活和不受检查的增殖,从而引发融合蛋白的表达。
7.ntrk基因融合在某些罕见肿瘤中具有特殊病征,诸如婴儿纤维肉瘤、先天性中胚叶肾瘤、分泌性乳腺癌和唾液腺分泌性癌(masc)(argani,bishop,bourgeois,rubin,&tognon)。相反地,ntrk基因融合很少发生在各种成人和儿童实体瘤中,该实体瘤包括但不限于:阑尾癌、乳腺癌、胆管癌、结直肠癌(crc)、gist、肺癌、黑素瘤、胰腺癌、甲状腺癌和多种肉瘤(debraud,brzezianska,fernandez
‑
cuesta,leeman
‑
neill,&ross)。鉴定ntrk基因融合具有重要的临床意义,因为当前正在开发的小分子抑制剂可用于治疗具有ntrk基因融合的实体瘤(vaishnavi&de braud)。
8.迄今为止,由于不同方法的特异性和敏感性不一致,对于肿瘤中ntrk融合的检测没有黄金标准。当前的检测方法包括荧光原位杂交(fish)、原位杂交(ish)、下一代测序(ngs)和免疫组织化学(ihc)。fish和ish测定的优化和枚举/解释可能是困难的。ngs具有高度特异性,但缺乏敏感性。相反,ihc可具有高度敏感性,但其检测蛋白质表达而非检测实际融合的存在。另外,由于一些肿瘤(即神经内分泌肿瘤和gist)中的野生型trk蛋白的内源性存在,对融合产物的ihc测定进行优化,继而开发特定的评定算法以选择此融合产物,可能具有挑战性。
技术实现要素:
9.本公开涉及用于鉴定由trk融合蛋白驱动的非神经内分泌肿瘤的方法。
10.在一个实施例中,提供了一种检测非神经内分泌肿瘤样品中的trka、trkb或trkc融合蛋白的方法,该方法包括:用生物标志物特异性试剂对样品进行亲和组织化学染色,该生物标志物特异性试剂与以下项中的一项或多项特异性地结合:包含seq id no:1的残基363
‑
760、基本上由其组成或由其组成的氨基酸序列;包含seq id no:2的残基646
‑
838、基本上由其组成或由其组成的氨基酸序列;或者包含seq id no:3的残基718
‑
839、基本上由其组成或由其组成的氨基酸序列;检测样品中的染色模式;以及如果出现以下情况,则评定样品对涉及trka、trkb或trkc的融合蛋白呈阳性:样品具有细胞质染色模式和/或膜染色模式并且具有大于或等于染色高于预定特异性染色强度的肿瘤细胞的第一阈值百分比;或者样品具有核染色模式并且大于或等于在阈值肿瘤细胞区域内以任何强度特异性地染色的细胞的第二阈值百分比。
11.在一个实施例中,提供了一种检测非神经内分泌肿瘤样品中的trka、trkb或trkc融合蛋白的方法,该方法包括:用生物标志物特异性试剂对样品进行亲和组织化学染色,该生物标志物特异性试剂与以下项特异性地结合:包含seq id no:1的残基363
‑
760、基本上由其组成或由其组成的氨基酸序列;包含seq id no:2的残基646
‑
838、基本上由其组成或由其组成的氨基酸序列;以及包含seq id no:3的残基718
‑
839、基本上由其组成或由其组成的氨基酸序列;检测样品中的染色模式;以及如果出现以下情况,则评定所述样品对涉及trka、trkb或trkc的融合蛋白呈阳性:样品具有细胞质染色模式和/或膜染色模式并且具有大于或等于染色高于预定特异性染色强度的肿瘤细胞的第一阈值百分比;或者样品具有核染色模式并且大于或等于在阈值肿瘤细胞区域内以任何强度特异性地染色的细胞的第二阈值百分比。
12.在一个实施例中,提供了一种检测非神经内分泌肿瘤样品中的trka、trkb或trkc融合蛋白的方法,该方法包括:用生物标志物特异性试剂对样品进行亲和组织化学染色,该生物标志物特异性试剂与由seq id no:2的残基816
‑
838组成的氨基酸序列特异性地结合;检测样品中的染色模式;以及如果出现以下情况,则评定所述样品对涉及trka、trkb或trkc的融合蛋白呈阳性:样品具有细胞质染色模式和/或膜染色模式并且具有大于或等于染色高于预定特异性染色强度的肿瘤细胞的第一阈值百分比;或者样品具有核染色模式并且大于或等于在阈值肿瘤细胞区域内以任何强度特异性地染色的细胞的第二阈值百分比。
13.在一个实施例中,提供了一种检测非神经内分泌肿瘤样品中ntrk重排的方法,该方法包括根据本文所述的方法检测样品中trk融合蛋白的存在状况,以及如果样品经评定为对涉及trka、trkb或trkc的融合蛋白呈阳性,则通过测序、逆转录酶聚合酶链式反应或原位杂交筛选样品来确认ntrk重排的存在。
14.在一个实施例中,提供了一种选择患者以接受trk导向疗法的方法,该方法包括根据本文所述的方法检测非神经内分泌肿瘤样品中trk融合蛋白的存在状况或ntrk重排情况,以及如果样品经评定为对涉及trka、trkb或trkc的融合蛋白呈阳性或者检测到ntrk重排,则选择患者以接受疗法。
15.在一个实施例中,还提供了针对trka、trkb或trkc以及涉及其激酶结构域的融合蛋白的存在或不存在对样品进行染色的方法,该方法包括:(a)对样品进行热诱导表位修复
过程;以及(b)使样品与生物标志物特异性试剂和一组检测试剂接触,以在与样品结合的任何生物标志物特异性试剂附近沉积明场染料,其中生物标志物特异性试剂与以下项中的一项或多项特异性地结合:包含seq id no:1的残基363
‑
760、基本上由其组成或由其组成的氨基酸序列;包含seq id no:2的残基646
‑
838、基本上由其组成或由其组成的氨基酸序列;或者包含seq id no:3的残基718
‑
839、基本上由其组成或由其组成的氨基酸序列。
16.在一个实施例中,还提供了针对trka、trkb或trkc以及涉及其激酶结构域的融合蛋白的存在或不存在对样品进行染色的方法,该方法包括:(a)对样品进行热诱导表位修复过程;以及(b)使样品与生物标志物特异性试剂和一组检测试剂接触,以在与样品结合的任何生物标志物特异性试剂附近沉积明场染料,其中生物标志物特异性试剂为与以下项中的一项或多项特异性地结合的一级抗体:包含seq id no:1的残基363
‑
760、基本上由其组成或由其组成的氨基酸序列;包含seq id no:2的残基646
‑
838、基本上由其组成或由其组成的氨基酸序列;或者包含seq id no:3的残基718
‑
839、基本上由其组成或由其组成的氨基酸序列;并且其中该组检测试剂包括:二级抗体,其与一级抗体有免疫反应性;三级抗体,其与二级抗体有免疫反应性,该二级抗体与酶缀合;以及一组试剂,其与酶有反应性,以实现明场染料在样品上的沉积。
17.在一个实施例中,还提供了针对trka、trkb或trkc以及涉及其激酶结构域的融合蛋白的存在或不存在对样品进行染色的方法,该方法包括:(a)对样品进行热诱导表位修复过程;以及(b)使样品与生物标志物特异性试剂和一组检测试剂接触,以在与样品结合的任何生物标志物特异性试剂附近沉积明场染料,其中生物标志物特异性试剂为与以下项中每项特异性地结合的一级抗体:包含seq id no:1的残基363
‑
760、基本上由其组成或由其组成的氨基酸序列;包含seq id no:2的残基646
‑
838、基本上由其组成或由其组成的氨基酸序列;或者包含seq id no:3的残基718
‑
839、基本上由其组成或由其组成的氨基酸序列;并且其中该组检测试剂包括:二级抗体,其与一级抗体有免疫反应性;三级抗体,其与二级抗体有免疫反应性,该二级抗体与酶缀合;以及一组试剂,其与酶有反应性,以实现明场染料在样品上的沉积。
18.根据以下公开内容,其他实施例将变得显而易见。
附图说明
19.图1 trka(seq id no:1的氨基酸残基363
‑
760)、trkb(seq id no:2的氨基酸残基646
‑
838)和trkc(seq id no:3的氨基酸残基718
‑
839)的示例性保留部分之间的序列比对。使用来自embl
‑
ebi的kalign多序列比对工具(https://www.ebi.ac.uk/tools/msa/kalign/)来生成序列比对。使用默认设置,该默认设置包括clustalw输出格式,间隙打开罚分11,间隙延伸罚分0.85,末端间隙罚分0.45,并且奖励评分0。
20.图2a用于多种肿瘤类型中的trk融合的ihc结果。正交测试法用于评估trk融合的存在。
21.图2b用于多种肿瘤类型中的trk融合的ihc结果。正交测试法用于评估trk融合的不存在。
22.图3a在数据集中的具有ish确认的的融合阳性案例的肿瘤类型按肿瘤细胞染色百分比(0
‑
100%)和染色强度(0
‑
3+)的染色分布。圆表示融合阴性案例,而三角形代表融合阳
性案例。菱形指示通过ish检测到融合的案例,但观察到固定梯度。模式代表各种肿瘤组织学。图5a和图5b示出了没有检测到融合阳性案例的神经内分泌肿瘤的染色分布。
23.图3b在数据集中的具有ish确认的的融合阴性案例的肿瘤类型按肿瘤细胞染色百分比(0
‑
100%)和染色强度(0
‑
3+)的染色分布。
24.图4基于ihc和ish测试的实体瘤的子分类。
25.图5用本文所述的染色方法获得的染色模式定位差异的实例。(a)通过断裂原位杂交测定来确定为具有ntrk1重排、通过下一代测序来确认为ntrk1
‑
tpm3融合的结直肠肿瘤中的细胞质染色模式/膜染色模式。(b)通过断裂原位杂交测定来确定为具有ntrk1重排、通过下一代测序来确认为ntrk1
‑
eml4融合的结直肠肿瘤中的细胞质染色模式。(c)通过断裂原位杂交测定来确定为具有ntrk3重排、通过下一代测序来确认为ntrk3
‑
etv6融合的乳腺样分泌性癌(masc)中的核染色模式/细胞质染色模式。
26.图6组织中固定梯度的实例,以及表现出核定位似乎比细胞质定位/膜定位更受梯度的影响。底行示出低倍率图像分段,并且顶行示出紧随其下图像分段的高倍率。
具体实施方式
27.i.定义
28.除非另外定义,否则本文所用的科学技术术语具有如本领域的普通技术人员通常理解的相同意义。参见例如,lackie,dictionary of cell and molecular biology,elsevier(第4版.2007);sambrook等人,molecular cloning,a laboratory manual,cold springs harbor press(cold springs harbor,n.y.1989)。术语“一个”或“一种”旨在表示“一个或多个/一种或多种。”在列举步骤或要素之前,术语“包括”、“包含”和“含有”旨在表示添加进一步的步骤或要素是任选的,而非排除性的。
29.抗体:本文的术语“抗体”以最广泛的含义使用,并且包括各种抗体结构,包括但不限于单克隆抗体、多克隆抗体、多特异性抗体(例如,双特异性抗体)和抗体片段,只要它们表现出所需的抗原结合活性即可。
30.抗体片段:“抗体片段”是指除了完整抗体以外的分子,其包含完整抗体的一部分且结合完整抗体结合的抗原。抗体片段的实例包括但不限于fv、fab、fab'、fab'
‑
sh、f(ab')2;双体抗体;线性抗体;单链抗体分子(例如,scfv);以及由抗体片段形成的多特异性抗体。
31.生物标志物:如本文所用,术语“生物标志物”应指在生物样品中发现的任何分子或分子组,所述任何分子或分子组可用于表征生物样品或从中获得生物样品的受试者。例如,生物标志物可为一个分子或一组分子,该一个分子或一组分子的存在、不存在或相对丰度为:
32.·
特定细胞或组织类型或状态的特征;
33.·
特定病理状况或状态的特征;或
34.·
指示病理状况的严重性、病理状况进展或消退的可能性,和/或病理状况对特定治疗作出应答的可能性。
35.作为另一个实例,生物标志物可为细胞类型或微生物(诸如细菌、分枝杆菌、真菌、病毒等),或者取代基分子或其分子的基团。
36.生物标志物特异性试剂:一种能够直接与细胞样品中的一种或多种生物标志物特
异性地结合的特异性检测试剂,诸如一级抗体。
37.细胞样品:如本文所用,术语“细胞样品”是指任何含有完整细胞的样品,诸如细胞培养物、体液样品或手术样品,采集该细胞样品以用于病理、组织学或细胞学解释。
38.细胞化学检测:涉及用生物标志物特异性试剂和检测试剂标记细胞学样品中的生物标志物或其他结构的过程,该过程以如下方式进行:允许在完整细胞的背景下对生物标志物或其他结构进行显微检测。
39.细胞学样品:如本文所用,术语“细胞学样品”应指体内没有横截面空间关系的细胞样品(诸如衍生自血液样品、尿液样品、痰液等的细胞样品),或其中横截面空间关系已至少部分受到破坏的细胞样品(诸如组织涂片、液基细胞学样品、细针抽吸物等)。
40.检测试剂:“检测试剂”为用于在细胞样品中的生物标志物特异性试剂附近沉积染色剂的任何试剂。非限制性实例包括生物标志物特异性试剂(诸如一级抗体)、二级检测试剂(诸如能够与一级抗体结合的二级抗体)、三级检测试剂(诸如能够与二级抗体结合的三级抗体)、与生物标志物特异性试剂直接或间接相关联的酶、与此类酶反应以影响荧光或显色染色剂的沉积的化学物质、在染色步骤之间使用的洗涤试剂等。
41.可检测部分:可产生可检测信号(诸如视觉、电子或其他方式)的分子或材料,该可检测信号指示沉积在样品上的可检测部分的存在(即定性分析)和/或浓度(即定量分析)。可检测信号可由任何已知或尚未发现的机制生成,该机制包括光子(包括射频、微波频率、红外频率、可见频率和紫外频率光子)的吸收、发射和/或散射。术语“可检测部分”包括显色、荧光、磷光和发光分子和材料,将一种物质转化为另一种物质以提供可检测差异(诸如通过将无色物质转化为有色物质,反之亦然,或者通过产生沉淀或增加样品浊度)的催化剂(诸如酶)。在一些实例中,可检测部分为荧光团,该荧光团属于若干常见化学类别,其包括香豆素、荧光素(或荧光素衍生物和类似物)、罗丹明、试卤灵、发光团和花菁。荧光分子的额外实例可参见molecular probes handbook—a guide to fluorescent probes and labeling technologies,molecular probes,eugene,or,thermofisher scientific,第11版。在其他实施例中,可检测部分为可经由明场显微术检测的分子,诸如包括二氨基联苯胺(dab)、4
‑
(二甲基氨基)偶氮苯
‑
4'
‑
磺酰胺(dabsyl)、四甲基罗丹明(discovery purple)、n,n'
‑
双羧基戊基
‑
5,5'
‑
二磺酸根基
‑
吲哚二碳菁(cy5)和罗丹明110(rhodamine)的染料。
42.组织化学检测:涉及用生物标志物特异性试剂和检测试剂标记组织样品中的生物标志物或其他结构的过程,该过程以如下方式进行:允许在组织样品结构之间的横截面关系的背景下对生物标志物或其他结构进行显微检测。
43.单克隆抗体:从基本上同质的抗体群体获得的抗体,即,除了可能的变异抗体(例如,包含天然存在的突变或在单克隆抗体制剂的生产过程中产生,此类变体通常以微量存在)之外,包括该群体的各个抗体是相同的和/或结合相同的表位。与通常包括针对不同决定簇(表位)的不同抗体的多克隆抗体制剂相反,单克隆抗体制剂的每种单克隆抗体针对抗原上的单一决定簇。因此,修饰语“单克隆”表示抗体的特征是从基本上同质的抗体群体获得的,并且不应解释为需要通过任何特定方法产生抗体。例如,根据本发明使用的单克隆抗体可通过多种技术制备,包括但不限于杂交瘤方法、重组dna方法、噬菌体展示方法,以及利用包含全部或部分人免疫球蛋白基因座的转基因动物的方法或它们的组合。
[0044]“保留部分”应表示保持在致癌融合蛋白中的致癌融合蛋白野生型对应物的任何
部分。
[0045]
特异性结合:如本文所用,术语“特异性结合”、“特异性地结合”或“具有特异性”或其他类似迭代是指介于靶标与特异性检测试剂之间的可测量和可再现的相互作用,在存在分子(包括生物分子)的异质群体的存在下,其确定靶标的存在。例如,与靶标特异性地结合的抗体为与其结合至其他靶标相比具有更大亲和力、亲合力、更容易和/或持续时间更长的结合该靶标的抗体。在一个实施例中,特异性检测试剂与无关靶标的结合程度小于所测得的抗体与靶标的结合(例如通过放射性免疫测定(ria))的约10%。在某些实施例中,与靶标特异性地结合的生物标志物特异性试剂的解离常数(kd)≤1μm、≤100nm、≤10nm、≤1nm或≤0.1nm。在另一实施例中,特异性结合可以包括但不要求排他结合。
[0046]
特异性检测试剂:任何能够与在细胞样品的背景下的靶标化学结构特异性地结合的物质组合物。
[0047]
染色/染色剂(stain):当用作名词时,术语“染色剂(stain)”应指可用于使细胞样品中的特定分子或结构可视化以用于显微分析的任何物质,该显微分析包括明场显微术、荧光显微术、电子显微术等。当用作动词时,术语“染色(stain)”应指导致染色剂在细胞样品上沉积的任何过程。
[0048]
受试者:如本文所用,术语“受试者”或“个体”为哺乳动物。哺乳动物包括但不限于驯养的动物(例如牛、绵羊、猫、犬和马)、灵长类动物(例如人和非人灵长类动物,诸如猴)、兔以及啮齿类动物(例如小鼠和大鼠)。在某些实施例中,该个体或受试者为人。
[0049]
测试样品:从受试者获取的肿瘤样品,该肿瘤样品在获取样品时具有未知结果。
[0050]
组织样品:如本文所用,术语“组织样品”应指保持细胞之间的横截面空间关系的细胞样品,因为它们存在于从中获得样品的受试者体内。
[0051]
肿瘤样品:从肿瘤获得的组织样品。
[0052]
ii.染色方法
[0053]
本公开基于使用第一生物标志物特异性试剂的非神经内分泌ntrk融合蛋白的亲和组织化学或细胞化学染色样品,该第一生物标志物特异性试剂靶向trka、trkb和trkc中的一个或多个的保留部分。通过鉴定产生融合蛋白的野生型蛋白的断点,并靶向保留在融合蛋白中的断点的一侧上的野生型蛋白的一部分来选择生物标志物特异性试剂。许多资源可用于通过基因组位置并且通过在所得融合蛋白中表达的第一外显子来鉴定融合蛋白断点,该资源包括例如包含断点的记号的cosmic数据库。表1中列示了示例性野生型蛋白序列:
[0054]
表1
[0055]
野生型蛋白示例性氨基酸序列背景参考文献trkauniprot p04629
‑
3(seq id no:1)amatu等人;stransky等人trkbuniprot q16620
‑
4(seq id no:2)amatu等人;stransky等人trkcuniprot q16288
‑
1(seq id no:3)amatu等人;stransky等人
[0056]
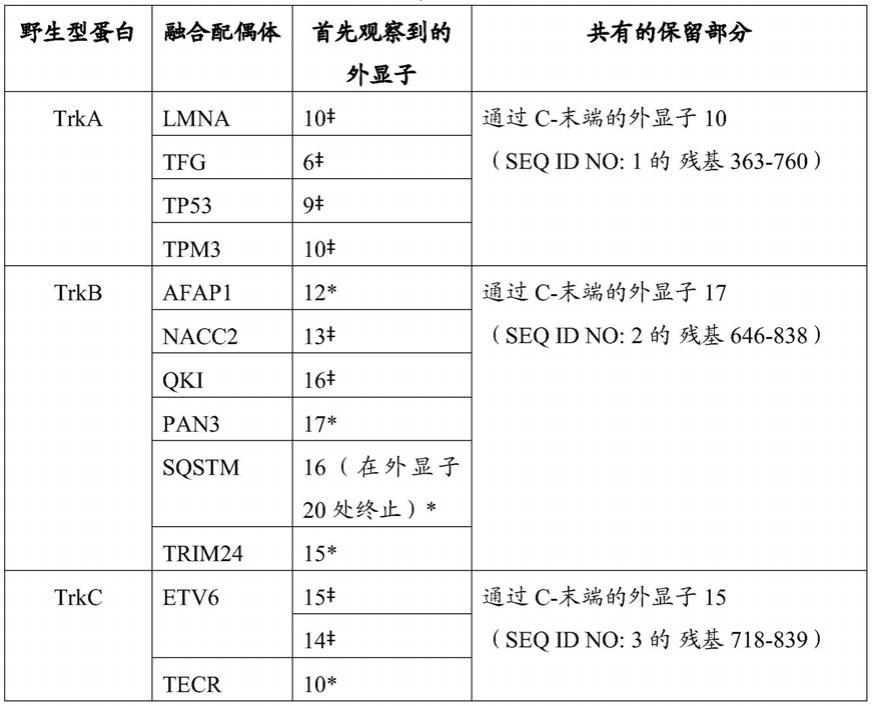
表2中示出了用于保留trka、trkb或trkc的c
‑
末端的融合蛋白的示例性断点和共有的保留部分:
[0057]
表2
inc.,new york,ny)、smip(emergent biosolutions,inc.,rockville,md)和tetranectin(基于c型凝集素结构域(ctld)的支架,四连接素;borean pharma a/s,aarhus,dk)。由wurch等人,development of novel protein scaffolds as alternatives to whole antibodies for imaging and therapy:status on discovery research and clinical validation,current pharmaceutical biotechnology,第9卷,第502
‑
509页(2008)对此类工程化特异性结合结构的描述进行综述,其内容通过引用并入。
[0061]
在一个特定实施例中,生物标志物特异性试剂为抗体。在另一个特定实施例中,抗体为单克隆抗体(诸如小鼠单克隆或兔单克隆抗体)。在另一个特定实施例中,抗体与trka、trkb或trkc中的一个或多个的保留部分特异性地结合。在另一个特定实施例中,抗体与以下项中的一项或多项所包含的表位特异性地结合:(a)包含seq id no:1的残基363
‑
760、基本上由其组成或由其组成的氨基酸序列;(b)包含seq id no:2的残基646
‑
838、基本上由其组成或由其组成的氨基酸序列;或者(c)包含seq id no:3的残基718
‑
839、基本上由其组成或由其组成的氨基酸序列。在另一个特定实施例中,抗体与以下项特异性地结合:(a)包含seq id no:1的残基363
‑
760、基本上由其组成或由其组成的氨基酸序列;(b)包含seq id no:2的残基646
‑
838、基本上由其组成或由其组成的氨基酸序列;以及(c)包含seq id no:3的残基718
‑
839、基本上由其组成或由其组成的氨基酸序列。在一个实施例中,抗体为根据表3的可商购获得的抗体:
[0062]
表3
[0063][0064]
在一个特定实施例中,抗体为epr17341。
[0065]
生物标志物特异性试剂用于对疑似携带ntrk融合蛋白的样品进行亲和组织化学或亲和细胞化学染色。亲和组织化学和细胞化学染色技术通常涉及在足以允许生物标志物特异性试剂与目标生物标志物之间进行特异性结合的条件下,使沉积在载玻片或其他固体支撑物上的样品与生物标志物特异性试剂接触。生物标志物特异性试剂与生物标志物的结合有助于在包含生物标志物的位置附近、在样品上沉积可检测部分。可检测部分可用于定位和/或定量生物标志物特异性试剂所涉及的生物标志物。由此,可通过检测由可检测部分产生的信号来检测样品中靶标的存在和/或相对量。
[0066]
染色过程可以是手动的、自动化的、或手动步骤与自动化步骤的组合。在一个实施例中,可在自动化高级染色平台上进行染色过程。自动化高级染色平台通常包括至少:用于染色方案中的各种试剂的储存器、与储存器进行流体通信以用于将试剂分配至载玻片上的试剂分配单元、用于从载玻片上移除使用过的试剂和其他废料的废料移除系统、以及协调试剂分配单元和废料移除系统的动作的控制系统。除了执行染色步骤外,许多自动化载玻片染色仪还可执行对染色进行辅助的步骤(或与执行此类辅助步骤的单独系统相容),该步骤包括:载玻片烘烤(用于将样品粘附至载玻片)、除蜡(也称为脱蜡)、表位修复、复染色、脱水和清洁以及盖玻片。prichard描述了自动化ihc/ish载玻片染色仪的若干具体实例及其
各种特征,其包括intellipath(biocare medical)、wave(celerus diagnostics)、dako omnis和dako autostainer link 48(agilent technologies)、benchmark(ventana medical systems,inc.)、leica bond以及lab vision autostainer(thermo scientific)自动化载玻片染色仪。另外,ventana medical systems,inc.为多项美国专利的受让人,这些专利公开了用于执行自动化分析的系统和方法,其包括美国专利号5,650,327、5,654,200、6,296,809、6,352,861、6,827,901和6,943,029,以及美国已公布的专利申请号20030211630和20040052685,所述专利中的每项均通过引用整体并入本文。可商购获得的染色单元通常按以下原理中的一个进行操作:(1)开放式单个载玻片染色,其中载玻片水平定位,并且试剂作为水坑分配在包含组织样品的载玻片表面(诸如在dako autostainer link 48(agilent technologies)和intellipath(biocare medical)染色仪上实施);(2)液体覆盖技术,其中试剂受到沉积在样品上方的惰性流体层覆盖或通过沉积在样品上方的惰性流体层进行分配(诸如ventana benchmark和discovery染色仪上实施);(3)毛细管间隙染色,其中将载玻片表面放置在另一表面(可为另一载玻片或盖板)附近以创建狭窄间隙,毛细力通过该间隙使液体试剂与样品接触并加以保持(诸如由dako techmate、leica bond和dako omnis染色仪使用的染色原理)。一些毛细管间隙染色的迭代不混合间隙中的流体(诸如在dako techmate和leica bond上)。在称为动态间隙染色的毛细管间隙染色的变体中,毛细力用于将样品应用到载玻片上,然后在孵育过程中,平行表面相对于另一个表面进行平移以搅动试剂,以实现试剂混合(诸如在dako omnis载玻片染色仪(agilent)上实施的染色原理)。在平移间隙染色中,一个可平移的头部定位在载玻片上方。头部的下表面与载玻片间隔足够小的第一间隙,以允许在载玻片的平移过程中从载玻片上的液体形成液体弯月面。具有小于载玻片宽度的横向尺寸的混合延伸部从可平移的头部的下表面延伸,以限定小于混合延伸部与载玻片之间的第一间隙的第二间隙。在头部的平移过程中,混合延伸部的横向尺寸足以在载玻片上的液体中生成在通常从第二间隙延伸至第一间隙的方向上的横向运动。参见wo 2011
‑
139978 a1。近来有人提出使用喷墨技术在载玻片上沉积试剂。参见wo 2016
‑
170008 a1。此染色技术列表并不旨在具有全面性,并且任何用于执行生物标志物染色的全自动化或半自动化系统均可使用。
[0067]
在疑似组织的细胞样品上实践染色方法,该细胞样品包括组织样品和细胞学样品。在一些实施例中,从患有或疑似患有肿瘤的受试者中获得细胞样品。在一些实施例中,直接从肿瘤获得样品。在一些实施例中,肿瘤为实体瘤,诸如癌、淋巴瘤或肉瘤。在一个实施例中,肿瘤为非神经内分泌肿瘤。在一个实施例中,非神经内分泌肿瘤为唾液腺、甲状腺、皮肤、乳房、头部和/或颈部、肺、上消化道(包括食道和胃)、女性生殖系统(包括子宫、输卵管和卵巢肿瘤)、下消化道(包括结肠、直肠和肛门肿瘤)、泌尿生殖道、外分泌、内分泌、肾脏的实体瘤,或淋巴细胞来源的实体瘤。在一个实施例中,受试者患有黑素瘤、唾液腺癌、甲状腺癌、乳腺癌、卵巢癌、胰腺癌、头颈癌、肺癌、食道癌、胃癌(不包括胃肠道间质瘤(gist))、结直肠癌(包括结肠、直肠和肛门的癌)、前列腺癌、尿路上皮癌或淋巴瘤。
[0068]
在使用组织样品的情况下,以与组织化学染色相容的方式处理组织样品,该方式包括例如固定、包埋在蜡基质(例如石蜡)中以及切片(诸如用切片机)。本公开不需要特定的处理步骤,只要所获得的样品与用该组生物标志物特异性试剂对样品进行组织化学染色相容即可。在一个特定实施例中,在染色过程中使用福尔马林固定、石蜡包埋(ffpe)样品的
超薄切片。在使用细胞学样品的情况下,将样品固定在福尔马林中。
[0069]
取决于所使用的生物标志物特异性试剂和所使用的样品,在应用生物标志物特异性试剂之前,可对样品进行表位修复过程(也称为抗原修复)。示例性的表位修复过程包括:热诱导表位修复(hier),其涉及在不同ph水平的各种缓冲液中加热样品;基于蛋白酶的表位修复(pber),其中在染色之前由蛋白水解酶消化样品;以及hier和pber的组合。由shi等人、d'amico等人、yamashita等人、vinod等人和warford等人对各种特异性表位修复过程进行了综述,尽管这并不详尽。是否执行待使用的表位修复以及特定形式的表位修复取决于所选择的特定生物标志物特异性试剂,并且可能需要对所使用的每种生物标志物特异性试剂进行经验性确定。
[0070]
取决于所使用的试剂和样品,在添加生物标志物特异性试剂和/或检测试剂之前,还可能需要阻断内源性蛋白的活性。例如,在检测试剂取决于生物素和生物素结合蛋白的情况下,可能有必要使用例如游离的、未标记的生物素结合蛋白来阻断内源性生物素。同样,许多检测方案依赖于酶的活性,该酶包括磷酸酶和过氧化物酶,这需要中和具有类似活性的内源性酶。可商购获得的试剂盒可用于此类阻断过程,例如,内源性生物素阻断试剂盒(目录号e21390,thermofisher scientific)、内源性亲和素/生物素阻断试剂盒(目录号ab64212,abcam,plc.)、内源性生物素阻断试剂盒目录号760
‑
050,ventana medical systems,inc.)、过氧化氢阻断试剂(目录号ab64218,abcam plc.)、过氧化物酶和碱性磷酸酶阻断试剂(代码s2003,agilent technologies)等。
[0071]
在将生物标志物特异性试剂应用于样品之前,阻断生物标志物特异性试剂可与之非特异性结合的样品上的位点也可能是有用的。常见的阻断剂包括正常血清、脱脂奶粉、bsa(牛血清白蛋白)和明胶的缓冲溶液,以及可商购获得的阻断剂,诸如ebioscience
tm
ihc/icc阻断缓冲液
‑
高蛋白(目录号00
‑
4952
‑
54,thermofisher scientific)、ebioscience
tm
ihc/icc阻断缓冲液
‑
低蛋白(目录号00
‑
4953
‑
54,thermofisher scientific)、discovery抗体阻断剂(目录号760
‑
4204,ventana medical systems,inc.)等。
[0072]
在这些预处理步骤中的每一项之后,可通过应用洗涤缓冲液洗涤一遍或多遍来执行洗涤步骤。洗涤缓冲液通常为中性缓冲生理盐溶液,其还可包含少量的洗涤剂。示例性洗涤缓冲液包括例如磷酸盐缓冲盐水(pbs)、pbs
‑
tween20、tris缓冲盐水(tbs)、tbs
‑
tween20(聚山梨醇酯20)、tris
‑
hcl、tris
‑
hc
‑
tween20、磷酸盐缓冲液(pb)、ap缓冲液等。
[0073]
一旦样品已准备用于染色,便将生物标志物特异性试剂应用于样品,并在足够的时间段和条件下孵育,以促进生物标志物与生物标志物特异性试剂之间的特异性结合。在用生物标志物特异性试剂孵育样品之后,可通过应用洗涤缓冲液洗涤一遍或多遍来执行洗涤步骤。这会从样品中移除未结合或非特异性结合的生物标志物特异性试剂,以减轻脱靶和/或背景染色。
[0074]
通过在紧邻与样品结合的生物标志物特异性试剂的位置处沉积可检测部分,实现对样品中生物标志物的检测。在一些实施例中,可检测部分与生物标志物特异性试剂直接缀合,因此在生物标志物特异性试剂与其靶标结合时沉积在样品上(通常称为直接标记方法)。在其他实施例中,通过在施用生物标志物特异性试剂后将一组检测试剂施用于样品来实现可检测部分的沉积,其中检测试剂以影响可检测部分沉积的方式(通常称为间接标记
法)与生物标志物特异性试剂结合或以其他方式与生物标志物特异性试剂反应。
[0075]
在使用间接方法的一些实施例中,可检测部分经由定位至生物标志物特异性试剂的酶促反应进行沉积。用于此类反应的合适的酶是众所周知的,并且包括但不限于氧化还原酶、水解酶和过氧化物酶。明确包括的特定酶为辣根过氧化物酶(hrp)、碱性磷酸酶(ap)、酸性磷酸酶、葡萄糖氧化酶、β
‑
半乳糖苷酶、β
‑
葡萄糖醛酸酶和β
‑
内酰胺酶。酶可直接与生物标志物特异性试剂缀合,或者可经由标记缀合物间接与生物标志物特异性试剂相关联。如本文所用,“标记缀合物”包括:
[0076]
(a)特异性检测试剂;以及
[0077]
(b)与特异性检测试剂缀合的酶,其中酶在适当的反应条件下与显色底物、信号传导缀合物和/或酶反应性染料反应,以实现染料的原位生成和/或染料在组织样品上的沉积。
[0078]
在非限制性实例中,标记缀合物的特异性检测试剂可为二级检测试剂(诸如与一级抗体结合的物类特异性二级抗体、与半抗原缀合性一级抗体结合的抗半抗原抗体、或与生物素化一级抗体结合的生物素结合蛋白)、三级检测试剂(诸如与二级抗体结合的物类特异性三级抗体、与半抗原缀合性二级抗体结合的抗半抗原抗体、或与生物素化二级抗体结合的生物素结合蛋白)或其他此类布置。由此,定位至样品结合的生物标志物特异性试剂的酶然后可用于多个方案中以沉积可检测部分。
[0079]
在一些情况下,该酶与显色化合物/底物反应。显色化合物/底物的特定非限制性实例包括4
‑
硝基苯磷酸盐(pnpp)、固红、溴氯吲哚磷酸酯(bcip)、硝基四氮唑兰(nbt)、bcip/nbt、固红、ap橙、ap蓝、四甲基联苯胺(tmb)、2,2'
‑
联氮
‑
双
‑
[3
‑
乙基苯并噻唑啉磺酸盐](abts)、邻联茴香胺、4
‑
氯萘酚(4
‑
cn)、硝基苯基
‑
β
‑
d
‑
吡喃半乳糖苷(onpg)、邻苯二胺(opd)、5
‑
溴
‑4‑
氯
‑3‑
吲哚基
‑
β
‑
吡喃半乳糖苷(x
‑
gal)、甲基伞形酮酰
‑
β
‑
d
‑
吡喃半乳糖苷(mu
‑
gal)、对硝基苯基
‑
α
‑
d
‑
吡喃半乳糖苷(pnp)、5
‑
溴
‑4‑
氯
‑3‑
吲哚基
‑
β
‑
d
‑
葡糖苷酸(x
‑
gluc)、3
‑
氨基
‑9‑
乙基卡咔唑(aec)、品红、碘硝基氯化四氮唑蓝(int)、四唑蓝或四唑紫。
[0080]
在一些实施例中,酶可用于金相检测方案。金相检测方法包括使用酶(诸如碱性磷酸酶)与水溶性金属离子和酶的氧化还原失活底物组合。在一些实施例中,底物由酶转化为氧化还原活性剂,并且氧化还原活性剂还原金属离子,使其形成可检测沉淀。(参见例如2004年12月20日提交的美国专利申请号11/015,646,pct公开号2005/003777和美国专利申请公开号2004/0265922;所述专利中的每一项均通过引用整体并入本文)。金相检测方法包括与水溶性金属离子、氧化剂和还原剂一起使用氧化还原酶(诸如辣根过氧化物酶),再次用于形成可检测沉淀。(例如,参见美国专利号6,670,113,其通过引用整体并入本文)。
[0081]
在一些实施例中,酶促作用发生在酶与染料本身之间,其中反应将染料从非结合物类转化为沉积在样品上的物类。例如,dab与过氧化物酶(诸如辣根过氧化物酶)的反应使dab氧化,使其沉淀。
[0082]
在其他实施例中,可检测部分经由包含潜伏反应性部分的信号传导缀合物加以沉积,该潜伏反应性部分配置为与酶反应以形成可与样品或与其他检测成分结合的反应性物类。这些反应性物类能够在其生成物的近端,即在酶附近与样品反应,但迅速转化为非反应性物类,使得信号传导缀合物并不沉积在远离酶沉积位点的位点处。潜伏反应性部分的实例包括:醌甲基化物(qm)类似物,诸如在wo2015124703a1描述的那些醌甲基化物类似物;以
及酪酰胺缀合物,诸如在wo2012003476a2描述的那些酪酰胺缀合物,所述专利中的每一项均在此通过引用整体并入本文。在一些实例中,潜伏反应性部分直接与染料(诸如n,n'
‑
双羧基戊基
‑
5,5'
‑
二磺酸根基
‑
吲哚二碳菁(cy5)、4
‑
(二甲基氨基)偶氮苯
‑
4'
‑
磺酰胺(dabsyl)、四甲基罗丹明(disco purple)和罗丹明110(rhodamine))缀合。在其他实例中,潜伏反应性部分与特异性结合对的一个成员缀合,并且染料连接至特异性结合对的另一个成员。在其他实例中,潜伏反应性部分连接至特异性结合对的一个成员,并且酶连接至特异性结合对的另一个成员,其中酶(a)与显色底物反应以实现染料的生成,或(b)与染料反应以实现染料的沉积(诸如dab)。特异性结合对的实例包括:
[0083]
(1)连接至潜伏反应性部分的生物素或生物素衍生物(诸如脱硫生物素),以及连接至染料或连接至酶的生物素结合实体(诸如亲和素、链霉亲和素、脱糖基化亲和素(诸如neutravidin)、或在其生物素结合位点上具有硝化酪氨酸的生物素结合蛋白(诸如captavidin)),该酶与显色底物反应或与染料反应(例如,当染料为dab时,连接至生物素结合蛋白的过氧化物酶);以及
[0084]
(2)连接至潜伏反应性部分的半抗原,以及连接至染料或连接至酶的抗半抗原抗体,该酶与显色底物反应或与染料反应(例如,当染料为dab时,连接至生物素结合蛋白的过氧化物酶)。
[0085]
特定地包括表4中列示的生物标志物特异性试剂与检测试剂组合的非限制性实例。
[0086]
表4
[0087]
[0088]
[0089]
[0090]
[0091]
[0092]
[0093]
[0094]
[0095]
[0096][0097]
在一个特定实施例中,表4中列示的生物标志物特异性试剂和特异性检测试剂为抗体。如本领域的普通技术人将认识到的,用于生物标志物特异性试剂中的每种的检测方案可为相同的,或可为不同的。
[0098]
适用于本方法的可商购获得的检测试剂或包含检测试剂的试剂盒的非限制性实例包括:ventana ultraview检测系统(与酶缀合的二级抗体,所述酶包括hrp和ap);
ventana iview检测系统(生物素化的抗物类二级抗体和链霉亲和素缀合的酶);ventana optiview检测系统(optiview)(与半抗原缀合的抗物类二级抗体和与酶多聚体缀合的抗半抗原三级抗体);ventana扩增试剂盒(未缀合的二级抗体,该未缀合的二级抗体可与前述ventana检测系统中的任何一种一起使用,以扩增沉积在一级抗体结合位点处的酶的数量);ventana optiview扩增系统(与半抗原缀合的抗物类二级抗体、与酶多聚体缀合的抗半抗原三级抗体以及与相同半抗原缀合的酪酰胺。在使用中,使二级抗体与样品接触,以实现与一级抗体的结合。然后使用抗半抗原抗体孵育样品,以实现酶与二级抗体的联合。然后使用酪酰胺孵育样品,以实现额外的半抗原分子的沉积。然后使用抗半抗原抗体再次孵育样品,以实现额外的酶分子的沉积。然后使用可检测部分孵育样品以实现染料沉积);ventana discovery、discovery omnimap、discovery ultramap抗半抗原抗体、二级抗体、生色团、荧光团和染料试剂盒,上述产品中的每种均可从ventana medical systems,inc.(tucson,arizona)获得;powervision和powervision+ihc检测系统(直接与hrp或ap聚合成携带高比例的酶比抗体的紧凑型聚合物的二级抗体);以及dako envision
tm
+系统(与二级抗体缀合的酶标记聚合物)。
[0099]
如果需要,可对生物标志物染色的载玻片进行复染色,以辅助鉴定形态学相关区域。复染剂的实例包括显色核复染剂,诸如苏木精(染色为蓝色至紫色)、亚甲基蓝(染色为蓝色)、甲苯胺蓝(染色为细胞核深蓝色和多糖粉红色至多糖红色)、核固红(也称为kernechtrot染料,染色为红色)和甲基绿(染色为绿色);非核显色染色剂,诸如曙红(染色为粉红色);荧光核染色剂,其包括4',6
‑
二氨基
‑2‑
苯基吲哚(dapi,染色为蓝色)、碘化丙啶(染色为红色)、hoechst染色剂(染色为蓝色)、核绿dcs1(染色为绿色)、核黄(hoechst s769121,在中性ph值下染色为黄色,并且在酸性ph值下染色为蓝色)、draq5(染色为红色)、draq7(染色为红色);荧光非核染色剂,诸如荧光团标记鬼笔环肽,(对丝状肌动蛋白进行染色,颜色取决于缀合荧光团)。
[0100]
iii.染色评估
[0101]
在一个实施例中,由当前公开的方法生成的一组染色样品用于确定存在或不存在患者样品中融合蛋白。在通常情况下,如上所述,样品从患者处获得并进行制备以用于分析。制备样品的一部分(例如,肿瘤切除样品的活检的第一组织切片,或从肿瘤细胞的细胞学样品(诸如细胞涂片(诸如宫颈涂片)、细针抽吸物、分离的循环肿瘤细胞等)制备的第一载玻片,并且用生物标志物特异性试剂对其进行染色。然后针对细胞染色百分比和/或等于或高于预定阈值水平的细胞染色百分比,来对染色的样品进行评定。优选地,将样品固定在福尔马林溶液中。在一个实施例中,阈值染色强度为至少1.5+,并且具有阈值染色强度的肿瘤细胞的阈值水平在25%至75%的范围内。在一个实施例中,阈值染色强度为至少1.5+,并且具有阈值染色强度的肿瘤细胞的阈值水平为50%。在一个实施例中,阈值染色强度为至少1.5+,并且具有阈值染色强度的肿瘤细胞的阈值水平为60%。在一个实施例中,阈值染色强度为至少1.5+,并且具有阈值染色强度的肿瘤细胞的阈值水平为75%。在一个实施例中,阈值染色强度为至少2+,并且具有阈值染色强度的肿瘤细胞的阈值水平在25%至75%的范围内。在一个实施例中,阈值染色强度为至少2+,并且具有阈值染色强度的肿瘤细胞的阈值水平为50%。在一个实施例中,阈值染色强度为至少2+,并且具有阈值染色强度的肿瘤细胞的阈值水平为60%。在一个实施例中,阈值染色强度为至少2+,并且具有阈值染色强度的肿
瘤细胞的阈值水平为75%。
[0102]
在一些情况下,基于表达模式对染色样品进行分层,然后用针对染色模式的评定方法进行评定。例如,在观察到固定梯度的情况下,第一评定方法应用于具有细胞质表达模式和/或膜表达模式的样品,而第二评定方法应用于具有核细胞定位的样品。例如,具有细胞质染色模式和/或膜染色模式的样品可通过确定样品是否满足或超过肿瘤细胞的阈值水平来进行评定(该肿瘤细胞等于或高于阈值染色强度),这被视为trk融合蛋白阳性。在一个实施例中,阈值染色强度为至少1.5+,并且具有阈值染色强度的肿瘤细胞的阈值水平在25%至75%的范围内。在一个实施例中,阈值染色强度为至少1.5+,并且具有阈值染色强度的肿瘤细胞的阈值水平为50%。在一个实施例中,阈值染色强度为至少1.5+,并且具有阈值染色强度的肿瘤细胞的阈值水平为60%。在一个实施例中,阈值染色强度为至少1.5+,并且具有阈值染色强度的肿瘤细胞的阈值水平为75%。在一个实施例中,阈值染色强度为至少2+,并且具有阈值染色强度的肿瘤细胞的阈值水平在25%至75%的范围内。在一个实施例中,阈值染色强度为至少2+,并且具有阈值染色强度的肿瘤细胞的阈值水平为50%。在一个实施例中,阈值染色强度为至少2+,并且具有阈值染色强度的肿瘤细胞的阈值水平为60%。在一个实施例中,阈值染色强度为至少2+,并且具有阈值染色强度的肿瘤细胞的阈值水平为75%。
[0103]
作为另一个实例,具有核染色模式的样品可通过确定样品的最小邻接肿瘤细胞区域是否具有等于或高于阈值表达水平染色的肿瘤细胞浓度来进行评定。在一个实施例中,阈值邻接肿瘤细胞区域为至少20个细胞,阈值染色强度为高于背景的任何特异性染色,并且细胞的阈值百分比在25%至75%或25%至80%的范围内。在另一个实施例中,阈值邻接肿瘤细胞区域为至少20个细胞,阈值染色强度为高于背景的任何特异性染色,并且细胞的阈值百分比为至少75%。在另一个实施例中,阈值邻接肿瘤细胞区域为至少20个细胞,阈值染色强度为高于背景的任何特异性染色,并且细胞的阈值百分比为至少80%。在一个实施例中,阈值邻接肿瘤细胞区域为至少20个细胞,阈值染色强度≥0.5+,并且细胞的阈值百分比在25%至75%或25%至80%的范围内。在另一个实施例中,阈值邻接肿瘤细胞区域为至少20个细胞,阈值染色强度≥0.5+,并且细胞的阈值百分比为至少75%。在另一个实施例中,阈值邻接肿瘤细胞区域为至少20个细胞,阈值染色强度≥0.5+,并且细胞的阈值百分比为至少80%。在一个实施例中,阈值邻接肿瘤细胞区域为至少50个细胞,阈值染色强度为高于背景的任何特异性染色,并且细胞的阈值百分比在25%至75%或25%至80%的范围内。在另一个实施例中,阈值邻接肿瘤细胞区域为至少50个细胞,阈值染色强度为高于背景的任何特异性染色,并且细胞的阈值百分比为至少75%。在另一个实施例中,阈值邻接肿瘤细胞区域为至少50个细胞,阈值染色强度为高于背景的任何特异性染色,并且细胞的阈值百分比为至少80%。在一个实施例中,阈值邻接肿瘤细胞区域为至少50个细胞,阈值染色强度≥0.5+,并且细胞的阈值百分比在25%至75%或25%至80%的范围内。在另一个实施例中,阈值邻接肿瘤细胞区域为至少50个细胞,阈值染色强度≥0.5+,并且细胞的阈值百分比为至少75%。在另一个实施例中,阈值邻接肿瘤细胞区域为至少50个细胞,阈值染色强度≥0.5+,并且细胞的阈值百分比为至少80%。
[0104]
vi.临床应用
[0105]
在一个实施例中,本文所述的测定用于表征来自患者的肿瘤样品。例如,获得活检
切片或切除样品,对其固定、包埋在石蜡中、切片并染色。如上所述,对染色切片进行评定。在一些实施例中,具有指示存在融合蛋白的评定的肿瘤表征为“融合阳性”,而具有未指示存在融合蛋白的评定的肿瘤表征为“融合阴性”。在其他实施例中,介于“融合阳性”与“融合阴性”之间的中间类别细胞表征为“性质不明”。例如,其中评定方法基于染色等于或高于阈值水平的细胞的阈值百分比,低于阈值百分比的百分比范围可定义为“性质不明”,并且将具有低于性质不明范围的细胞的百分比的所有其他样品视为“融合阴性”。作为另一个实例,其中评定方法基于在阈值肿瘤细胞区域内染色等于或高于阈值水平的细胞的阈值百分比,低于阈值肿瘤细胞区域的百分比范围可定义为“性质不明”,并且将具有低于性质不明范围的细胞的百分比的所有其他样品视为“融合阴性”。
[0106]
在一些实施例中,该测定用作筛选测试,以便鉴定有资格进行基于核酸的测定以确认融合蛋白存在的患者。例如,可使用该测定针对存在或不存在融合蛋白筛选样品,并且仅对那些表征为融合阳性的样品进行基于测序或基于pcr的测定,以确认在该测定中检测到的融合的存在和/或同一性。在其他实施例中,该测定为反射性测试,以确认由基于核酸的测定来鉴定的融合蛋白的存在和表达。例如,可使用基于测序或基于pcr的测定来针对存在或不存在ntrk基因重排情况筛选样品,并且仅有那些通过基于测序或基于pcr的测定表征为重排阳性的样品通过本文所述的测定进行筛选,以确认由核酸测定检测的融合的存在和/或表达。在其他实施例中,仅基于测定对融合蛋白的存在或不存在进行表征。在其他实施例中,可通过基于测序或基于pcr的测定来针对ntrk基因重排的存在情况筛选表征为“融合阴性”或“性质不明”的样品,而表征为“融合阳性”的细胞则不进行。
[0107]
在一些实施例中,该测定用于为患者选择疗法。例如,具有表征为“融合阳性”的肿瘤或样品的患者接受针对野生型对应物的靶向疗法,任选地与用于肿瘤的标准治疗过程组合。示例性靶向疗法包括表5中列举的那些:
[0108]
表5
[0109][0110]
具有表征为融合阴性的肿瘤或样品的患者接受标准疗法,而不包括针对野生型对应物的靶向治疗。
[0111]
viii.实例
[0112]
为了评估是否可开发一种可预测不同肿瘤类型的trk融合的存在的评定算法,对超过3000个组织在多个指示项方面进行ihc染色和分析。
[0113]
可商购获得的福尔马林固定、石蜡包埋(ffpe)的正常组织和肿瘤组织。以使用泛trk抗体克隆epr17341的原型ihc测定来筛选组织,其包括热诱导表位修复,然后在benchmark ultra自动化载玻片染色仪(rtd,tucson,arizona)上使用optiview dab detection(rtd,tucson arizona)进行抗体孵育和色度发展。
[0114]
以原位杂交(ish,其使用用于ntrk1、ntrk2和ntrk3的断裂探针)来进一步评估案例的子集,该案例的子集大多数具有由泛trk(epr17341)测定进行的特异性染色。ntrk 1、2
和3断裂oligo探针各自由靶向基因组区域的两个寡核苷酸(oligo)池组成,该基因组区域横跨ntrk1、ntrk2和ntrk3基因的5'和3'末端。在合成过程中,使用dnp
‑
teg亚磷酰胺(link technologies ltd,bellshill,lanarkshire)和6
‑
荧光素亚磷酰胺(link technologies ltd,bellshill,lanarkshire)将dnp和荧光素半抗原以基本插入构型附接至oligo。使用反相色谱柱纯化合成的oligo,并且执行质谱分析以验证截短的oligo的移除情况。
[0115]
基于对正常组织中和没有泛trk ihc表达的肿瘤中的平均断裂率的评估来确定用于定义ish测定的断裂状态的标准。其中断裂率高出平均值大于5个标准偏差的肿瘤被视为代表真正的ntrk基因融合。
[0116]
图2a
‑
2b中示出了具有各种基因分型的不同肿瘤类型的泛trk染色的代表性图像。当定义为>0%的肿瘤细胞染色时,9%(n=324)的肿瘤表现出特异性泛trk ihc染色(对应地,在胃癌和唾液腺癌中范围为0%
‑
54%)。当仅考虑分别≥10%和≥25%的肿瘤细胞中的具有ihc特异性染色的标本时,具有特异性染色的案例的总体百分比下降至5%(n=191)和4%(n=133)。
[0117]
164个案例表现出任何由ihc进行的染色可用于ish测试。其中发现12例携带ntrk融合(5例crc、2例黑素瘤、2例乳头状甲状腺癌、2例唾液腺癌和1例胰腺癌)。在表6中示出了不同类型的肿瘤在各个肿瘤细胞染色百分比下的泛trk阳性案例率(包括由ish进行的确认测试结果):
[0118]
表6
[0119][0120]
染色强度和肿瘤细胞染色百分比随组织类型的不同而不同,但发现携带融合的案例倾向于具有较高的染色强度和较大的肿瘤细胞染色百分比(参见图3a&3b)。图3a和3b示出了ish确认的样品按肿瘤细胞染色百分比(0
‑
100%)和染色强度(0
‑
3+)的分布。圆表示融合阴性案例,而三角形代表融合阳性案例。颜色代表各种肿瘤组织学。图3a示出了在数据集中的具有ish确认融合阳性案例的肿瘤类型的染色分布,并且图3b示出了没有检测到融合阳性案例的神经内分泌肿瘤的染色分布。
[0121]
在表7示出了在数据集中的所有肿瘤中由ihc进行肿瘤细胞染色百分比的结果:
[0122]
表7
[0123][0124]
12/164(7%)的案例,其中ihc特异性染色大于肿瘤细胞的0%,这表现出存在由ish检测的ntrk融合。10/88(11%)的案例,其中ihc特异性染色大于肿瘤细胞的25%,这表现出存在由ish检测的融合(表6)。与非融合肿瘤相比,示出由ish检测的融合的肿瘤倾向于以更高的强度和更高的肿瘤百分比由泛trk ihc进行染色(右上方象限;图3a),但神经内分泌肿瘤除外(图3b)。使用更高的ihc特异性阳性染色的定义(>25%)将导致两种融合阳性黑素瘤排除在ish测试之外(表6)。这两个组织样品未由ihc充分染色,这表现出固定梯度的证据。重要的是,这些组织的确在未由固定相关伪影影响的区域中、在高百分比(>90%)的邻接细胞中表现出高强度的核染色。
[0125]
图4示出了基于ihc和ish测试的实体瘤的子分类。
[0126]
图5和图6示出了观察到的染色模式的实例。如图5所示,染色模式可包括膜染色(a)、细胞质染色(a
‑
c)和核染色(c)的方面。图7示出了一些样品经历固定梯度,这可能会影响一些细胞的染色水平。应当注意,具有核定位的样品比具有细胞质定位/膜定位的样品对固定梯度更敏感。
[0127]
总之,泛trk ihc染色在不同肿瘤类型的肿瘤细胞染色的强度和百分比上均有差异。与具有野生型trk蛋白表达的肿瘤相比,基于ish的携带融合的实体瘤示出了强度更高且在更大百分比的肿瘤细胞中的ihc染色,但神经内分泌和梭形细胞肿瘤除外。在野生型trk蛋白表达率较低的肿瘤类型(例如crc和乳头状甲状腺癌)中,泛trk ihc染色可用于帮助鉴定携带融合的肿瘤。相比之下,在野生型trk蛋白表达率较高的肿瘤(例如神经内分泌肿瘤、gist)中,ihc染色百分比和强度的分布不支持野生型表达与融合之间的明确区分。根据表6,随着使用泛trk ihc的肿瘤细胞染色百分比的增加,进行ish的标本数量(在总共164个案例中)逐渐下降;然而,此下降并不影响在保持完好的组织中通过ish鉴定具有ntrk基因融合的肿瘤。结合ihc染色强度的增加,此度量似乎通过ish测试进一步突出了那些具有ntrk基因融合的肿瘤。
[0128]
两种黑素瘤和一种胰腺导管腺癌并未遵循上述观察结果。观察到的较低百分比的肿瘤细胞染色可能与固定伪影有关。然而有趣的是,在高强度下,小面积的邻接存活肿瘤的确表现出高百分比的核染色。
[0129]
vi.参考文献
[0130]
以下参考文献通过引用整体并入本文:
[0131]
amatu等人,ntrk gene fusions as novel targets of cancer therapy across multiple tumour types,esmo open,第1卷,第2期,e000023 doi:10.1136/esmoopen
‑
2015
‑
000023(2016)。
[0132]
bailey等人,tropomyosin receptor kinase inhibitors:an updated patent review for 2010
‑
2016
–
part ii,expert opinion on therapetuic patents,第27卷,第7期,第831
–
49页(mar.2017)。
[0133]
d’amico等人,state of the art in antigen retrieval for immunohistochemistry,j immunol methods.第341(1
‑
2)卷,第1
‑
18页(feb.28,2009)。
[0134]
hechtman等人,pan
‑
trk immunohistochemistry is an efficient and reliable screen for the detection of ntrk fusions,am.j.surg.path.,第41卷,第11期,第1547
–
51页(nov.2017)。
[0135]
prichard,overview of automated immunohistochemistry,arch pathol lab med.,第138卷,第1578
–
1582页(2014)
[0136]
shi等人,antigen retrieval immunohistochemistry:review and future prospects in research and diagnosis over two decades,j histochem cytochem,第59卷,第1期,第13
‑
32页(jan.2011)。
[0137]
stransky等人,the landscape of kinase fusions in cancer,nature communications,第5卷,article no.4846(2014)doi:10.1038/ncomms5846。
[0138]
vinod等人,a simple and effective heat induced antigen retrieval method,methodsx,第3卷,第315
–
19页(在线发表于apr.8,2016)。
[0139]
warford等人,antigen retrieval,blocking,detection and visualisation systems in immunohistochemistry:a review and practical evaluation of tyramide and rolling circle amplification systems,methods,第70卷,第1期,第28
–
33页(nov.2014)。
[0140]
wellcome sanger institute,cosmic
–
the catalogue of somatic mutations in cancer(cosmic数据库),可在http://cancer.sanger.ac.uk/cosmic/fusion获得(上次于13
‑
sep
‑
2018访问)。
[0141]
yamashita等人,mechanisms of heat
‑
induced antigen retrieval:analyses in vitro employing sds
‑
page and immunohistochemistry,j.histochemistry and cytochemistry,第53卷,第1期,第13
–
21页(2005)。
[0142]
barbacid m.等人biochim.biophys.acta rev.cancer 1991。
[0143]
barbacid m.annals new york academy of sciences.1995:442
‑
458。
[0144]
lemmon ma和schlessinger j.cell 2010;141:1117
‑
1134。
[0145]
klein r等人cell 1991;85:189
‑
197。
[0146]
eide f等人j.neurosci.1996;16(10):3123
‑
3129。
[0147]
luberg k等人bmc neurosci.2015:16:78 doi 10.1186/s12868
‑
015
‑
0215
‑
x。
[0148]
vaishnavi a,等人nature medicine.2013;19(11):1469
‑
1472。
[0149]
de braud fg等人2014 asco annual meeting;abstract 2502。
[0150]
argani pm,等人mod pathol.2000;13(1):29
‑
36。
[0151]
bishop ja等人hum pathol.2013;44(10):1982
‑
1988。
[0152]
bourgeois jm等人am j surg pathol.2000;24(7):937
‑
946。
[0153]
rubin bp等人am j pathol.1998;153(5):1451
‑
1458。
[0154]
tognon c等人cancer cell.2002;2:367
‑
376。
[0155]
brzezianska e等人mutat res.2006;599(1
‑
2):26
‑
35。
[0156]
fernandez
‑
cuesta l等人105th annual meeting of the american association for cancer research,2014,san diego,california,aacr。
[0157]
leeman
‑
neill rj等人cancer.2014;120(6):799
‑
807。
[0158]
ross j.s等人oncologist.2014;19(3):235
‑
242。
[0159]
farago等人jco precision oncology.在线发表于july 23,2018。
[0160]
gatalica z等人mod pathol.在线发表于23 august 2018。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1