一种快速联合检测卡及其制备方法和应用与流程
本发明属于体外诊断领域,涉及一种可同时检测新型冠状病毒n蛋白、甲型流感病毒和乙型流感病毒的快速联合检测卡及其制备方法和应用。
背景技术:
2019新型冠状病毒(novelcoronaviruspneumonia,ncp),即“covid-19”,国际病毒分类委员会冠状病毒研究小组(csg)建议,在对相关冠状病毒进行系统分析的基础上,将2019-ncov命名为“严重急性呼吸综合征冠状病毒2”,即“sars-cov-2”。
新冠病毒感染的肺炎疫情暴发以来,市面上出现大量的pcr核酸、igm/igg检测试剂,针对抗原的检测几乎没有。单个样品采用核酸荧光pcr法需要3个小时才能给出检测结果,采用核酸测序法需要6个小时才能给出检测结果,更重要的是由于基因扩增对实验室环境要求极高导致检测通量成为最大制约因素,其极大制约了新型冠状病毒快速检测服务的供给能力,不足以全面满足疫情的防控需要。igm/igg在人体内出现的时间较抗原相对滞后。并且目前大部分的研究主要是单一性的针对新冠病毒引起的肺炎检测的研究。而其他常见呼吸道病毒例如甲型流感病毒、乙型流感病毒等引起的患者症状与新冠病毒肺炎患者症状相似,因此在早期联合多种呼吸道病毒检测试剂对疑似病例进行筛查,快速进行患者疾病分型,对于做到快速隔离、有针对性的治疗具有非常重要的意义。
技术实现要素:
有鉴于此,本发明的主要目的在于提供一种可同时检测新型冠状病毒n蛋白、甲型流感病毒和乙型流感病毒的快速联合检测卡及其制备方法和应用。
为了实现上述目的,本发明提供了如下技术方案:
一种快速联合检测卡,包括用于检测样本的新冠/甲流/乙流检测试纸条和卡壳;所述卡壳包括相互卡合的底槽和上盖,所述新冠/甲流/乙流检测试纸条设置在卡壳底槽上。
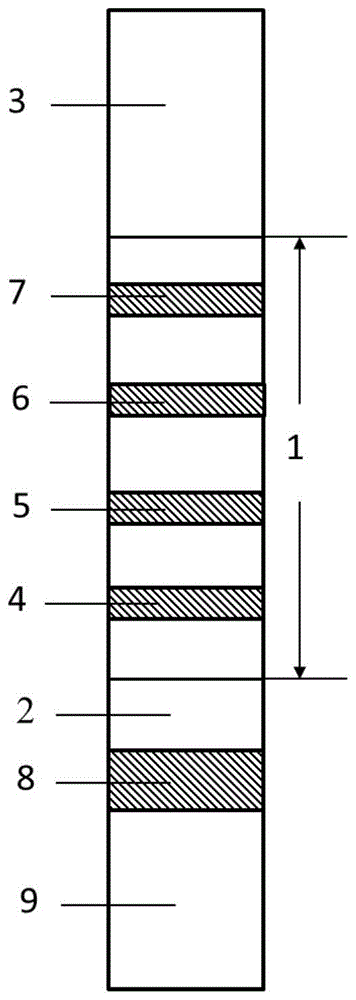
在本发明的一个具体方案中,其中所述新冠/甲流/乙流检测试纸条包括底板,所述底板上固定有依次连接的样品垫、标记物垫、包被垫及吸水垫;所述包被垫靠近检测线的一端连接有标记物垫,靠近质控线的一端连接有吸水垫;所述包被垫上依次设有第一检测线、第二检测线、第三检测线及质控线,所述样品垫和标记物垫连接为一体。
在本发明的一个具体方案中,其中所述上盖对应新冠/甲流/乙流检测试纸条样品垫的位置分别设置有加样孔。
在本发明的一个具体方案中,其中所述上盖对应新冠/甲流/乙流检测试纸条的第一检测线、第二检测线、第三检测线和质控线的位置分别设置有用于检测线和质控线的数据采集的观察窗。
在本发明的一个具体方案中,其中所述新冠/甲流/乙流检测试纸条中,所述第一检测线、第二检测线或第三检测线上分别包被有一株抗新型冠状病毒n蛋白单克隆抗体、一株抗甲型流感病毒单克隆抗体、一株抗乙型流感病毒单克隆抗体中的一种且三个检测线上包被的物质各不相同;所述质控线上包被有羊抗兔多克隆抗体。
在本发明的一个具体方案中,其中所述标记物垫上包被有标记物标记的另一株抗新型冠状病毒n蛋白单克隆抗体、标记物标记的另一株抗甲型流感病毒单克隆抗体、标记物标记的另一株抗乙型流感病毒单克隆抗体和标记物标记的兔igg。
在本发明的一个具体方案中,其中所述标记物标记的另一株抗新型冠状病毒n蛋白单克隆抗体、标记物标记的另一株抗甲型流感病毒单克隆抗体、标记物标记的另一株抗乙型流感病毒单克隆抗体和标记物标记的兔igg的摩尔比为1:1:1:(0.1~4)。
在本发明的一个具体方案中,所述标记物选自荧光微球、胶体金、胶体硒、彩色乳胶或磁性微球。
在本发明的一个具体方案中,所述样本选自鼻拭子、咽拭子、空腔拭子、痰液、唾液、肺泡灌洗液或血液。
一种快速联合检测卡的制备方法,包括以下步骤:
1)将标记物标记的另一株抗新型冠状病毒n蛋白单克隆抗体、标记物标记的另一株抗甲型流感病毒单克隆抗体、标记物标记的另一株抗乙型流感病毒单克隆抗体和标记物标记的兔igg混合均匀,之后将得到的混合物包被在玻璃纤维素膜上制成标记物垫;
2)将一株抗新型冠状病毒n蛋白单克隆抗体、一株抗甲型流感病毒单克隆抗体、一株抗乙型流感病毒单克隆抗体分别任意地包被在第一检测线、第二检测线和第三检测线上且三个检测线上所包被的物质各不相同,将羊抗兔多克隆抗体包被在质控线上,制成包被垫;
3)在底板上粘接包被垫,然后在靠近包被垫上质控线的一端搭接吸水垫,在靠近包被垫上检测线的一端搭接记物垫及与其连接的样品垫,用切条机切成试纸条,将试纸条放入卡壳中制成新冠/甲流/乙流快速联合检测卡。
一种快速联合检测卡的的应用方法,包括以下步骤:
将采集的样本经样本保存液处理获得待测样本,取30~200μl的待测样本加入到新冠/甲流/乙流快速联合检测卡的加样孔处,静置5~30min,
将新冠/甲流/乙流快速联合检测卡插入到荧光免疫层析分析仪中进行检测,仪器自动计算出各检测线与质控线对应的t/c值,将各自的t/c值与对应的新型冠状病毒n蛋白、甲型流感病毒和乙型流感病毒正常值范围进行比较以判断阴阳性;
或者通过肉眼直接观察或在紫外光下肉眼观察,在质控线出现带颜色的条带或荧光条带的前提下,任意检测线出现带颜色的条带或荧光条带时,该检测线对应的检测物质即为阳性。
本发明的有益效果为:
1、本发明所提供的快速联合检测卡,其能够同时对具有联合检测价值的新型冠状病毒n蛋白、甲型流感病毒、乙型流感病毒进行检测,以做到在早期对疑似病例进行筛查,快速进行患者疾病分型,从而对做到快速隔离、有针对性的治疗具有非常重要的意义。
2、本发明所提供的快速联合检测卡,其能够对鼻咽拭子、口咽拭子、肺泡灌洗液、口腔拭子、唾液等样本进行检测,检测速度快,15min出检测结果,配合荧光免疫层析仪使用,并支持肉眼判读或紫外光下肉眼判读,操作简单,适用于基层医疗机构。
3、本发明所提供的快速联合检测卡,其能够改善pcr对仪器操作、人员、环境等的专业性要求限制,以及检测抗体无法在早期进行筛查的缺陷,能够加速疫情一线疑似病例筛查,从而快速进行确诊人员隔离,有效降低社会恐慌情绪。
附图说明
图1为本发明所提供的新冠/甲流/乙流检测试纸条的结构示意图;
图2a为本发明所提供的快速联合检测卡中一种卡壳上盖的内部结构示意图;
图2b为本发明所提供的快速联合检测卡中一种卡壳底槽的内部结构示意图;
其中,1-包被垫,2-标记物垫,3-吸水垫,4-第一检测线,5-第二检测线,6-第三检测线,7-质控线,8-标记物结合处,9-样品垫,10-底槽,11-上盖,12-新冠/甲流/乙流检测试纸条放置区域,13-第一限定部,14-第二限定部,15-第三限定部,16-加样孔,17-观察窗,18-定位柱,19-定位孔。
具体实施方式
为了进一步理解本发明,下面结合实施例对本发明优选实施方案进行描述,但是应当理解,这些描述只是为进一步说明本发明的特征和优点,而不是对本发明权利要求的限制。
以下材料或试剂,如非特别说明,均为市购。
实施例1新冠/甲流/乙流检测试纸条的制备
1、采用胶体金标记另一株鼠抗冠状病毒n蛋白单克隆抗体
取0.5ml胶体金溶液,用0.2mol/l碳酸钾调节ph至8.5,静置10min,取100μl另一株鼠抗冠状病毒n蛋白单克隆抗体,在120r/min的磁力搅拌下在1min内滴加到上述胶体金溶液中,继续搅拌30min,加入0.5mlbsa,混匀后静置30min,按照12000r/min的转速离心10min,去除上清液。最后,将离心后获得的固体沉淀物复溶至1ml,再加入1μl的proclin300在4℃下保存待用。
2、采用胶体金标记另一株鼠抗甲型流感病毒单克隆抗体
取0.5ml胶体金溶液,用0.2mol/l碳酸钾调节ph至8.5,静置10min,取100μl另一株鼠抗甲型流感病毒单克隆抗体,在120r/min的磁力搅拌下1min滴加到上述胶体金溶液中,继续搅拌30min,加入0.5mlbsa,混匀后静置30min,按照12000r/min的转速离心10min,去除上清液。最后,将离心后获得的固体沉淀物复溶至1ml,再加入1μl的proclin300在4℃下保存待用。
3、采用胶体金标记另一株鼠抗乙型流感病毒单克隆抗体
取0.5ml胶体金溶液,用0.2mol/l碳酸钾调节ph至8.5,静置10min,取100μl另一株鼠抗乙型流感病毒单克隆抗体,在120r/min的磁力搅拌下1min滴加到上述胶体金溶液中,继续搅拌30min,加入0.5mlbsa,混匀后静置30min,按照12000r/min的转速离心10min,去除上清液。最后,将离心后获得的固体沉淀物复溶至1ml,再加入1μl的proclin300在4℃下保存待用。
4、采用胶体金标记羊抗兔igg多克隆抗体
取0.5ml胶体金溶液,用0.2mol/l碳酸钾调节ph至8.5,静置10min,取100μl羊抗兔igg多克隆抗体,在120r/min的磁力搅拌下1min滴加到上述胶体金溶液中,继续搅拌30min,加入0.5mlbsa,混匀后静置30min,按照12000r/min的转速离心10min,去除上清液。最后,将离心后获得的固体沉淀物复溶至1ml,再加入1μl的proclin300在4℃下保存待用。
5、包被垫的制备
将一株鼠抗新型冠状病毒n蛋白单克隆抗体、一株甲型流感病毒单克隆单体、一株乙型流感病毒单克隆抗体和羊抗兔多克隆抗体分别用0.2m的磷酸盐缓冲液(ph=7.4)稀释成1mg/ml,用划膜喷金仪在硝酸纤维素膜(nc膜)上进行划膜。含有一株鼠抗冠状病毒n蛋白单克隆抗体的作为第一检测线(t1线)4,含有一株甲型流感病毒单克隆单体的作为第二检测线(t2线)5,含有一株乙型流感病毒单克隆抗体的作为第三检测线(t3线)6,含有羊抗兔多克隆抗体的作为质控线(c线)7,然后在37℃,湿度<30%的环境下干燥4h制成包被垫1。
6、标记物垫的制备
①将玻璃纤维素膜在0.2m的磷酸盐缓冲液(ph=7.4)中浸泡6h,然后在35℃下干燥8h,备用。
②将摩尔比为1:1:1:1的胶体金标记的另一株鼠抗冠状病毒n蛋白单克隆抗体、胶体金标记的另一株甲型流感病毒单克隆单体、胶体金标记的就另一株乙型流感病毒单克隆单体和胶体金标记的兔igg混合均匀后,按照10μl/cm的速度喷涂在玻璃纤维素膜上,然后放置在45℃下干燥2h制成标记物垫2。标记物垫2上包被有胶体金标记的另一株鼠抗冠状病毒n蛋白单克隆抗体、胶体金标记的另一株甲型流感病毒单克隆单体、胶体金标记的就另一株乙型流感病毒单克隆单体和胶体金标记的兔igg的地方叫做标记物结合处8。
设置标记物结合处8的目的在于:
当待测样本中含有新型冠状病毒n蛋白时,将待测样本滴加到样品垫9上,在吸水垫3的作用下,待测样本向前层析,在标记物结合处8待测样本中的新型冠状病毒n蛋白与标记物结合处包被的胶体金标记的另一株鼠抗新型冠状病毒n蛋白单克隆抗体反应,反应后的物质记作第一免疫复合物,随后反应后的第一免疫复合物、胶体金标记的兔igg随着样本继续层析,在第一检测线处反应后的第一免疫复合物与检测线上包被的一株鼠抗新型冠状病毒n蛋白单克隆抗体反应而停留在第一检测线处,在质控线处荧光微球标记的兔igg与质控线包被的羊抗兔多克隆抗体反应而停留在质控线,其他物质继续层析,最后直接用肉眼进行结果判读,在质控线显示色带的前提下,当第一检测线显示色带时,表明样本中新型冠状病毒n蛋白的检测结果为阳性,当第一检测线不显示色带时,表明新型冠状病毒n蛋白的检测结果为阴性;
当待测样本中含有甲型流感病毒时,将待测样本滴加到样品垫9上,在吸水垫3的作用下,待测样本向前层析,在标记物结合处8待测样本中的甲型流感病毒与标记物结合处包被的胶体金标记的另一株甲型流感病毒单克隆抗体反应,反应后的物质记作第二免疫复合物,随后反应后的第二免疫复合物、胶体金标记的兔igg随着样本继续层析,在第二检测线处反应后的第二免疫复合物与检测线上包被的一株鼠抗甲型流感病毒单克隆抗体反应而停留在第二检测线处,在质控线处荧光微球标记的兔igg与质控线包被的羊抗兔多克隆抗体反应而停留在质控线,其他物质继续层析,最后直接用肉眼进行结果判读,在质控线显示色带的前提下,当第二检测线显示色带时,表明样本中甲型流感病毒的检测结果为阳性,当第二检测线不显示色带时,表明甲型流感病毒的检测结果为阴性;
当待测样本中含有乙型流感病毒时,将待测样本滴加到样品垫9上,在吸水垫3的作用下,待测样本向前层析,在标记物结合处8待测样本中的乙型流感病毒与标记物结合处包被的胶体金标记的另一株乙型流感病毒单克隆抗体反应,反应后的物质记作第三免疫复合物,随后反应后的第三免疫复合物、胶体金标记的兔igg随着样本继续层析,在第三检测线处反应后的第三免疫复合物与检测线上包被的一株鼠抗乙型流感病毒单克隆抗体反应而停留在第三检测线处,在质控线处荧光微球标记的兔igg与质控线包被的羊抗兔多克隆抗体反应而停留在质控线,其他物质继续层析,最后直接用肉眼进行结果判读,在质控线显示色带的前提下,当第三检测线显示色带时,表明样本中乙型流感病毒的检测结果为阳性,当第三检测线不显示色带时,表明乙型流感病毒的检测结果为阴性。
在某些实施例中,采用荧光微球作为标记物,可以将加入样本后的检测卡通过荧光免疫层析仪分别采集第一检测线的荧光信号(记作ta)、第二检测线的荧光信号(记作tb)、第三检测线的荧光信号(tc)和质控线的荧光的信号(记作c),计算ta/c、tb/c、tc/c值,将ta/c与新型冠状病毒n蛋白的正常值范围进行比较以判断阴阳性,将tb/c与甲型流感病毒的正常值范围进行比较以判断阴阳性,将tc/c与乙型流感病毒的正常值范围进行比较以判断阴阳性。同时也可以在紫外光下进行结果判读,在质控线显示荧光条带的前提下,第一检测线显示荧光条带时,表明样本中新型冠状病毒n蛋白的检测结果为阳性,当第一检测线不显示荧光条带时,表明新型冠状病毒n蛋白的检测结果为阴性;在质控线显示荧光条带的前提下,当第二检测线显示荧光条带时,表明样本中甲型流感病毒的检测结果为阳性,当第二检测线不显示荧光条带时,表明甲型流感病毒的检测结果为阴性;在质控线显示荧光条带的前提下,当第三检测线显示荧光条带时,表明样本中乙型流感病毒的检测结果为阳性,当第三检测线不显示荧光条带时,表明乙型流感病毒的检测结果为阴性。
7、试纸条的制备
首先在pvc板(图中未示出)上粘接包被垫1,然后在靠近包被垫1上的质控线7的一端搭接吸水垫3,在靠近包被垫1的第一检测线4的一端搭接标记物垫2及与其连接的样品垫7,用切条机切成4mm±0.1mm的试纸条(见图1),备用。
实施例2快速联合检测卡的组装
将实施例1中制备的新冠/甲流/乙流检测试纸条插入到卡壳中制备成快速联合检测卡。
所述卡壳(如图2所示)可以包括:底槽10,其连接于所述底板(具体为pvc板)上;上盖11,其连接于所述底槽10,
如图2b所示,所述底槽10包括:位于其内表面的对称分布的多个定位孔19,多个所述定位孔19之间设有多个用于限定新冠/甲流/乙流检测试纸条横向移动的第一限定部13以及用于限定试纸条纵向移动的第二限定部14;对称设置的所述第一限定部13与所述第二限定部14围设成新冠/甲流/乙流检测试纸条放置区域12(虚线区域),用于放置新冠/甲流/乙流检测试纸条;
如图2a所示,所述上盖11包括:与多个所述定位孔19相配合的多个定位柱18,这样配合使用以将上盖11和底槽10固定在一起;所述上盖11还包括用于限定新冠/甲流/乙流检测试纸条上下移动的第三限定部15。
所述上盖11上设置有用于向所述新冠/甲流/乙流检测试纸条的样品垫9上加样的加样孔16;
观察窗17,其设置于上盖11上,用于新冠/甲流/乙流检测试纸条的包被垫1上的第一检测线4、第二检测线5、第三检测线6和质控线7的数据采集;
所述观察窗17开设于所述上盖11上与新冠/甲流/乙流检测试纸条放置区域12的中部相对应的位置;
所述上盖11在与所述新冠/甲流/乙流检测试纸条的样品垫9相对应的位置处开设有加样孔16以用于向新冠/甲流/乙流检测试纸条的样品垫9上滴加待测样本。所述检测线距离加样孔15-25mm。
在其他实施例中,样品垫9可以省略,加样孔16直接对应到标记物垫2的标记物结合处8,从加样孔16直接滴加待测样本到标记物结合处,直接进行反应。
实施例3检测
采用实施例1和2制备的快速联合检测卡对待测样本进行检测,能够进行鼻拭子、咽拭子、空腔拭子、痰液、唾液、肺泡灌洗液或血液的检测。
以咽拭子样本的检测为例。
将采集的咽拭子样本经样本保存液进行样本前处理,处理方式:在塑料软管中加入0.5ml样本保存液,随后将采集样本后的棉棒浸在样本保存液中并搅拌。用手指挤压塑料软管外侧数次,使样本保存液充分浸透棉棒,然后拔出棉棒,绞出(即将棉棒上采集的样本混合到样本保存液中)的液体即为待测样本。随后取60μl处理好的待测样本分别滴加到新冠/甲流/乙流检测试纸条的样品垫9对应的加样孔16处,静置15min,最后直接用肉眼进行结果判读,在质控线显示色带(酒红色或紫红色)的前提下,当第一检测线显示色带(酒红色或紫红色)时,表明样本中新型冠状病毒n蛋白的检测结果为阳性,当第一检测线不显示色带时,表明新型冠状病毒n蛋白的检测结果为阴性;当第二检测线显示色带(酒红色或紫红色)时,表明样本中甲型流感病毒的检测结果为阳性,当第二检测线不显示色带时,表明样本中甲型流感病毒的检测结果为阴性;当第三检测线显示色带(酒红色或紫红色)时,表明样本中乙型流感病毒的检测结果为阳性,当第三检测线不显示色带时,表明样本中乙型流感病毒的检测结果为阴性。
实施例4性能评价
采用实施例1和实施例2制备的联合检测卡进行如下的性能评价实验。
1、灵敏度
(1)新型冠状病毒n蛋白检测结果的灵敏度
以新型冠状病毒n蛋白合成的多肽片段分别配制浓度为50ng/ml(l1)、100ng/ml(l2)、200ng/ml(l3)的标准品,检测结果如下表1所示。
表1
(2)甲型流感病毒检测结果的灵敏度
用p.b缓冲溶液分别配制浓度为200ng/ml(n1)、400ng/ml(n2)、800ng/ml(n3)的甲型流感病毒抗原标准液,检测结果如下表2所示。
表2
(3)乙型流感病毒检测结果的灵敏度
用p.b缓冲溶液分别配制浓度为100ng/ml(p1)、150ng/ml(p2)、300ng/ml(p3)的甲型流感病毒抗原标准液,检测结果如下表3所示。
表3
从上述表1、表2、表3的检测结果中可以看出,本发明的快速联合检测卡能够检测出新型冠状病毒n蛋白、甲型流感病毒和乙型型流感病毒,符合灵敏度的检测要求。
2、特异性
利用腺病毒、合胞病毒、肺炎支原体、肺炎衣原体的标准液作为干扰物质分别滴加500μl到实施例1和实施例2中制备的快速联合检测卡中进行检测,15分钟后用肉眼观察检测结果,检测结果表4所示。
表4
从表4的检测结果中说明,本发明的快速联合检测卡具有很强的特异性,与其他腺病毒、合胞病毒、肺炎支原体、肺炎衣原体等呼吸道病毒无交叉反应。
实施例5新冠/甲流/乙流检测试纸条的制备
1、“采用胶体金标记另一株鼠抗冠状病毒n蛋白单克隆抗体”与实施例1中的制备方式相同;
2、“采用胶体金标记另一株鼠抗甲型流感病毒单克隆抗体”与实施例1中的制备方式相同;
3、“采用胶体金标记另一株鼠抗乙型流感病毒单克隆抗体”与实施例1中的制备方式相同;
4、“采用胶体金标记羊抗兔igg多克隆抗体”与实施例1中的制备方式相同;
5、“包被垫的制备”与实施例1中的制备方式相同;
6、标记物垫按照以下方式制备:
①将玻璃纤维素膜在0.2m的磷酸盐缓冲液(ph=7.4)中浸泡6h,然后在35℃下干燥8h,备用。
②将摩尔比为1:1:1:4的胶体金标记的另一株鼠抗冠状病毒n蛋白单克隆抗体、胶体金标记的另一株甲型流感病毒单克隆单体、胶体金标记的就另一株乙型流感病毒单克隆单体和胶体金标记的兔igg混合均匀后,按照10μl/cm的速度喷涂在玻璃纤维素膜上,然后放置在45℃下干燥2h制成标记物垫2。标记物垫2上包被有胶体金标记的另一株鼠抗冠状病毒n蛋白单克隆抗体、胶体金标记的另一株甲型流感病毒单克隆单体、胶体金标记的另一株乙型流感病毒单克隆单体和胶体金标记的兔igg的地方叫做标记物结合处8。
7、“试纸条的制备”与实施例1中的制备方式相同;
8、“快速联合检测卡的组装”与实施例2中的制备方式相同;
9、“检测”过程与实施例3中的检测过程相同;
实施例6性能评价
采用实施例5制备的联合检测卡进行如下的性能评价实验。
1、灵敏度
(1)新型冠状病毒n蛋白检测结果的灵敏度
以新型冠状病毒n蛋白合成的多肽片段分别配制浓度为50ng/ml(l1)、100ng/ml(l2)、200ng/ml(l3)的标准品,检测结果如下表5所示。
表5
(2)甲型流感病毒检测结果的灵敏度
用pbs分别配制浓度为200ng/ml(n1)、400ng/ml(n2)、800ng/ml(n3)的甲型流感病毒抗原标准液,检测结果如下表6所示。
表6
(3)乙型流感病毒检测结果的灵敏度
用p.b缓冲溶液分别配制浓度为100ng/ml(p1)、150ng/ml(p2)、300ng/ml(p3)的甲型流感病毒抗原标准液,检测结果如下表7所示。
表7
从上述表5、表6、表7的检测结果中可以看出,本发明的快速联合检测卡能够检测出新型冠状病毒n蛋白、甲型流感病毒和乙型型流感病毒,符合灵敏度的检测要求。
2、特异性
利用腺病毒、合胞病毒、肺炎支原体、肺炎衣原体的标准液作为干扰物质分别滴加500μl到实施例5中制备的快速联合检测卡中进行检测,15分钟后用肉眼观察检测结果,检测结果表8所示。
表8
从表8的检测结果中说明,本发明的快速联合检测卡具有很强的特异性,与其他腺病毒、合胞病毒、肺炎支原体、肺炎衣原体等呼吸道病毒无交叉反应。
附:所需溶液配置
(1)样本保存液
纯化水定容至1000ml;
(2)p.b缓冲溶液
磷酸氢二钠51.68g
磷酸二氢钠9.92g
纯化水定容至1000ml。
以上所述实施例仅是为充分说明本发明而所举的实施例,本发明的保护范围不限于此。本技术领域的技术人员在本发明基础上所作的等同替代或变换,均在本发明的保护范围之内。本发明的保护范围以权利要求书为准。
- 还没有人留言评论。精彩留言会获得点赞!