一种更昔洛韦有关物质的检测方法与流程
1.本发明涉及药物分析领域,具体而言,涉及一种更昔洛韦有关物质的检测方法。
背景技术:
2.更昔洛韦(ganciclovir),化学名称为:9-(1,3-二羟基-2-丙氧甲基)-鸟嘌呤,是一种高效、低毒、选择性强的抗病毒药物,对人体6种疱疹病毒染均有很强的抑制作用,用于治疗和预防免疫缺陷患者、器官移植者巨细胞病毒感染。
3.药物在生产和/或储存过程中会引入有关物质,这些有关物质都会不同程度地影响药物的稳定性、安全性,因此药物有关物质的检查也是控制药物纯度,提高药品质量的一个非常重要的环节。中国药典2015版中用高效液相色谱法(hplc)测定更昔洛韦中的有关物质,具体色谱条件为:以十八烷基硅烷键合硅胶为填充剂,以甲醇-水(5:95)为流动相,检测波长为252nm。进口注册标准(jx20110078)中用高效液相色谱法(hplc)测定更昔洛韦中的有关物质,具体色谱条件为:以十八烷基硅烷键合硅胶为填充剂,以磷酸二氢铵溶液(取磷酸二氢铵约1.38g,加水500ml,然后加磷酸1.2ml溶解,用水稀释至100ml)为流动相,检测波长为254nm。然而,本发明人用该两种方法检测更昔洛韦中的有关物质,发现其分离效果并不理想,无法有效分离更昔洛韦中存在的多种有关物质,不能满足工业上日益提升的质控要求。
4.随着药品质量控制要求地日益严格,为进一步提高药品质量,保证用药安全,急需开发出一种能有效、快速检测出更昔洛韦中更多的有关物质的方法。
技术实现要素:
5.本发明的发明目的在于:针对上述存在的问题,提供一种新的更昔洛韦有关物质的检测方法。
6.本发明采用的技术方案如下:
7.一种更昔洛韦有关物质的检测方法,用十八烷基硅烷键合硅胶色谱柱,以0.012mol/l磷酸二氢铵溶液-甲醇(98-95:2-5,v/v)为流动相a,以甲醇为流动相b,进行梯度洗脱,检测更昔洛韦中的有关物质;其中,磷酸二氢铵溶液用磷酸溶液调节ph值至2.5-3.5。洗脱程序为如表1所示。
8.表1本发明的洗脱程序
[0009][0010][0011]
进一步地,流动相a中磷酸二氢铵溶液与甲醇的比例为97:3(v/v)。
[0012]
进一步地,流动相a中,磷酸二氢铵溶液用磷酸溶液调节ph值至3.0。
[0013]
进一步地,柱温为25-35℃,优选地,柱温为30℃。
[0014]
进一步地,检测波长为250-255nm,优选地,检测波长为252nm。
[0015]
进一步地,流动相的流速为0.8-1.2ml/min,优选地,流速为1.0ml/min。
[0016]
综上所述,由于采用了上述技术方案,本发明的有益效果是:
[0017]
本发明的检测方法可以快速有效的分离更昔洛韦原料药中潜在的多种微量有关物质,基线平稳、峰形美观,同时还具有主峰与相邻杂质以及相邻杂质之间分离度好、耐用性高等优点,能够高效的实现更昔洛韦中多种有关物质的定性和定量,适于工业大生产上对更昔洛韦料的快速质量监测,对于产品质量控制有着重要意义。
附图说明
[0018]
本发明将通过例子并参照附图的方式说明,其中:
[0019]
图1是对比例1中色谱条件下的hplc色谱图;
[0020]
图2是对比例2中色谱条件下的hplc色谱图;
[0021]
图3是对比例3中色谱条件下的hplc色谱图;
[0022]
图4是对比例4中色谱条件下的hplc色谱图;
[0023]
图5是对比例5中色谱条件下的hplc色谱图;
[0024]
图6是对比例6中色谱条件下的hplc色谱图;
[0025]
图7是实施例1中色谱条件下的hplc色谱图;
[0026]
图8是用实施例1的色谱条件检测实施例2中供试品溶液得到的hplc色谱图;
[0027]
图9是对比例7中色谱条件下的hplc色谱图
[0028]
图10是对比例8中色谱条件下的hplc色谱图。
具体实施方式
[0029]
对比例1
[0030]
色谱柱:t3柱(t3,4.6*250mm 5μm)
[0031]
波长:252nm;柱温:30℃,流速:1.0ml/min;流动相:5%甲醇。
[0032]
更昔洛韦样品:参照朱忠华等(朱忠华,朱世龙,朱世仁,et al.更昔洛韦的合成研究[j].广东化工,2010,37(4):113-114.)提供的工艺合成。
[0033]
样品溶液:取上述更昔洛韦样品适量,用水配制成1ml中约含更昔洛韦0.3mg的溶液即得。精密量取该样品溶液20μl,注入液相色谱仪进行分析,记录检测结果。检测结果如图1所示。图1中,2号峰为主峰,1号以及3-5号峰均为有关物质峰。100min内共检测出4种有关物质,2号主峰与3号有关物质峰之间未实现基线分离。
[0034]
对比例2
[0035]
色谱柱:t3柱(t3,4.6*250mm 5μm)
[0036]
波长:254nm;柱温:30℃,流速:1.0ml/min;流动相:磷酸二氢铵溶液(取磷酸二氢铵约1.38g,加水500ml,然后加磷酸1.2ml溶解,用水稀释至1000ml)。
[0037]
样品溶液:同对比例1。精密量取样品溶液20μl,注入液相色谱仪进行分析,记录检测结果。检测结果如图2所示。图2中,3号峰为主峰,1、2、4号峰为有关物质峰。100min内仅检
测出3种有关物质。
[0038]
对比例3
[0039]
色谱柱:t3柱(t3,4.6*250mm 5μm);
[0040]
波长:252nm;柱温:35℃,流速:1.0ml/min;
[0041]
流动相:流动相a为:水-甲醇(97:3),流动相b为:甲醇。
[0042]
样品溶液:同对比例1。精密量取样品溶液20μl,注入液相色谱仪进行分析,记录检测结果。洗脱程序如表2所示。检测结果如图3所示。图3中,2号峰为主峰,1、3-7号峰为有关物质峰。52min内共检测出6种有关物质,1号主峰与2号有关物质峰之间未能实现基线分离,基线波动不稳定。
[0043]
表2对比例3的洗脱程序
[0044][0045][0046]
对比例4
[0047]
色谱柱:t3柱(t3,4.6*250mm 5μm);
[0048]
波长:252nm;柱温:30℃,流速:1.0ml/min;
[0049]
流动相:流动相a为:0.012mol/l磷酸二氢铵溶液(用磷酸调节ph值至3.0)-甲醇(97:3),流动相b为:甲醇。
[0050]
样品溶液:同对比例1。精密量取样品溶液20μl,注入液相色谱仪进行分析,记录检测结果。洗脱程序如表2所示。检测结果如图4所示。图4中,2号峰为主峰,1号、3-7号峰为有关物质峰,52min内共检测出6种有关物质,2号主峰与3号有关物质峰之间未能实现基线分离。
[0051]
对比例5
[0052]
色谱柱:t3柱(t3,4.6*250mm 5μm);
[0053]
波长:252nm;柱温:30℃,流速:1.0ml/min;
[0054]
流动相:流动相a为:0.012mol/l磷酸二氢铵溶液(用磷酸调节ph值至3.0)-甲醇(97:3),流动相b为:甲醇。
[0055]
样品溶液:同对比例1。精密量取样品溶液20μl,注入液相色谱仪进行分析,记录检测结果。洗脱程序如表3所示。检测结果如图5所示。图5中,2号峰为主峰,1号、3-8号峰为有关物质峰。60min内共检测出7种有关物质,2号主峰与3号有关物质峰之间未能实现基线分离。
[0056]
表3对比例5的洗脱程序
[0057]
时间/min流动相a(v%)流动相b(v%)0100015964454060
501000601000
[0058]
对比例6
[0059]
色谱柱:t3柱(t3,4.6*250mm 5μm);
[0060]
波长:252nm;柱温:35℃,流速:1.0ml/min;
[0061]
流动相:流动相a为:水-甲醇(97:3),流动相b为:甲醇。
[0062]
样品溶液:同对比例1。精密量取样品溶液20μl,注入液相色谱仪进行分析,记录检测结果。洗脱程序如表4所示。检测结果如图6所示。图6中,2号峰为主峰,1号、3-7号峰为有关物质峰。60min内共检测出6种有关物质。
[0063]
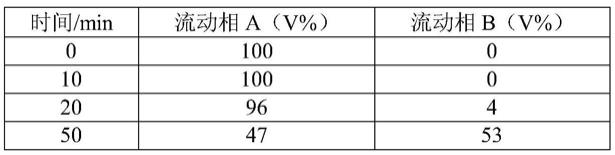
表4对比例6的洗脱程序
[0064]
时间/min流动相a(v%)流动相b(v%)0100010100020964504753511000601000
[0065]
实施例1
[0066]
色谱柱:t3柱(t3,4.6*250mm 5μm);
[0067]
波长:252nm;柱温:30℃,流速:1.0ml/min;
[0068]
流动相:流动相a为:0.012mol/l磷酸二氢铵溶液(用磷酸调节ph值至3.0)-甲醇(97:3),流动相b为:甲醇;
[0069]
样品溶液:同对比例1。精密量取样品溶液20μl,注入液相色谱仪进行分析,记录检测结果。洗脱程序如表4所示。检测结果如图7所示。图7中,3号峰为主峰,1-2号、4-11号峰为有关物质峰。采用本发明的检测方法,60min内可同时检测出10种有关物质,并且3号主峰与4号有关物质峰实现基线分离,整体基线平稳,峰形良好,无明显拖尾,可满足对有关物质准确定性和定量的需求。
[0070]
实施例2
[0071]
耐用性测试条件如下:
[0072]
柱温变化:在实施例1中提供的色谱条件柱温25℃基础上变更
±
5℃,即25℃和35℃。
[0073]
流速变化:在实施例1中提供的色谱条件流速1.0ml/min基础上变更
±
0.1ml/min,即0.9ml/min和1.1ml/min。
[0074]
流动相ph变化:在实施例1中提供的色谱条件ph3.0基础上变更
±
0.2,即ph2.8和ph3.2
[0075]
供试品溶液:精密称定更昔洛韦(湖北葛店人福药业有限公司,批号:f-gxl190101)150mg于50ml量瓶中,加0.6mol/l氢氧化钠溶液1ml使溶解,用水稀释至刻度,摇匀,精密量取适量,用水稀释制成每1ml中约含0.3mg的溶液。
[0076]
对照溶液:精密移取供试品溶液1ml于1000ml量瓶中,用水稀释并定容至刻度,摇
匀,即得。
[0077]
本发明中,杂质含量采用自身对照法进行计算,计算公式如下:
[0078]
单杂%=ax/as/1000*100%;
[0079][0080]
式中,ax为各杂质对应峰面积,as为自身对照峰面积,a总为总峰峰面积,1000为稀释倍数。
[0081]
本实施例中,在上述各个色谱条件下变化时,各耐用性样品溶液与初始条件中各有关物质含量差值均小于
±
0.03%,总杂含量rsd均小于10%。具体结果如表5所示,用实施例1中的色谱条件分析供试品溶液,结果如图8所示。图8中,2号峰为主峰,1号、3-4号峰为有关物质峰。
[0082]
表5更昔洛韦检测方法耐用性考察结果表
[0083][0084]
注:表5中杂质1和杂质2分别指按照实施例1提供的检测方法检测供试品溶液,如图8所示出峰顺序分别为第1和第4的物质,出峰顺序为第3的峰,峰面积占比低于0.03%,忽略不计。
[0085]
由表5可知,本发明提供的更昔洛韦有关物质的检测方法的耐用性高。
[0086]
对比例7
[0087]
色谱柱:t3柱(t3,4.6*250mm 5μm);
[0088]
波长:252nm;柱温:30℃,流速:1.0ml/min;
[0089]
流动相:流动相a为:0.012mol/l磷酸二氢铵溶液(用0.01mol/ml磷酸氢二铵溶液调节ph值至5.0)-甲醇(97:3),流动相b为:甲醇。
[0090]
样品溶液:同对比例1。精密量取样品溶液20μl,注入液相色谱仪进行分析,记录检测结果。洗脱程序同表4所示。检测结果如图9所示。图9中,2号峰为主峰,1号、3-7号峰为有关物质峰。62min内共检测出6种有关物质,2号主峰与3号有关物质峰之间未能实现基线分离。
[0091]
对比例8
[0092]
色谱柱:t3柱(t3,4.6*250mm 5μm);
[0093]
波长:252nm;柱温:30℃,流速:1.0ml/min;
[0094]
流动相:流动相a为:0.012mol/l磷酸二氢铵溶液(用磷酸调节ph值至2.0)-甲醇(97:3),流动相b为:甲醇。
[0095]
样品溶液:同对比例1。精密量取样品溶液20μl,注入液相色谱仪进行分析,记录检测结果。洗脱程序同表4所示。检测结果如图10所示。图10中,3号峰为主峰,1-2号、4-9号峰为有关物质峰。60min内共检测出8种有关物质,3号主峰与4号有关物质峰之间未能实现基线分离。
[0096]
由对比例7和对比例8的检测结果可知,流动相ph值对更昔洛韦有关物质分离效果影响较为明显,当流动相ph为5.0或2.0时,会出现主峰与其相邻的杂质峰不能基线分离,目标杂质峰数目减少等问题,不利于生产上对产品有关物质的准确定性和定量。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1