分离测定倍他米松的方法与流程
1.本发明涉及药物分析技术领域,特别是涉及一种利用高效液相色谱法分析二丙酸倍他米松起始物料中倍他米松的含量的方法。
背景技术:
2.倍他米松是一种药品,倍他米松的糖代谢及抗炎作用较氢化可的松强,为氢化可的松的15倍,但钠潴留作用为氢化可的松的百倍以上,在原发性肾上腺皮质功能减退症中,可与糖皮质类固醇一起用于替代治疗。也适用于低肾素低醛固酮综合征和植物神经病变所致体位性低血压等。
3.二丙酸倍他米松可用于治疗皮肤炎症和瘙痒症,如神经性皮炎、接触性皮炎、脂溢性皮炎、湿疹、局限性瘙痒症、盘状红斑狼疮等。而倍他米松作为二丙酸倍他米松的起始物质,研究倍他米松含量分析方法,可有效减少检测过程中的误差以及时间成本等。
4.本发明在中国药典基础方法上,提供了一种更加优化的分析方法。该方法专属性、精密度、准确度和耐受性较好,并与中国药典2015版各论中倍他米松质量标准中倍他米松含量测定进行了对比,结果基本一致,但分析时间大大减少。
技术实现要素:
5.本发明的目的之一是提供一种分离倍他米松的方法。通过该方法可以有效的减少分离时间。
6.为了实现上述目的,本发明提供的方案为:
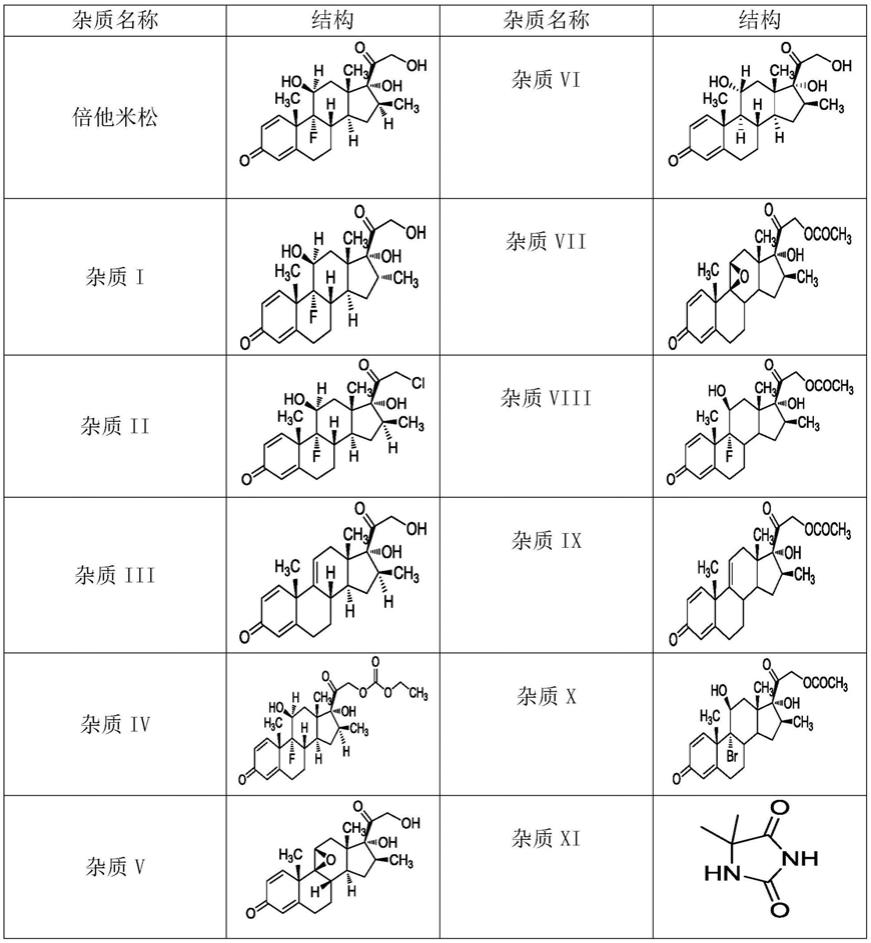
7.分离倍他米松的方法,其特征在于,用填充有十八烷基硅烷键合硅胶的色谱柱作为固定相,以四氢呋喃、异丙醇和水为流动相进行梯度洗脱,将所述倍他米松进行分离,其中所述倍他米松结构式及其相关杂质如下:
[0008][0009]
进一步,所述流动相四氢呋喃:异丙醇体积比为:85~90:10~15,四氢呋喃、异丙醇与水的体积比为20~40:60~80。
[0010]
具体的,所述四氢呋喃-异丙醇(体积比为88:12):水的体积比为20:80。
[0011]
进一步,所述流动相流速为0.5ml~1.0ml/min。
[0012]
具体的,所述流动相流速每分钟0.9ml。
[0013]
进一步,所述色谱柱为ods hypersil 100
×
4mm,3μm。
[0014]
进一步,所述色谱柱柱温为23℃~27℃。
[0015]
具体的,所述柱温为25℃。
[0016]
进一步,所述梯度洗脱程序为:
[0017]
时间/min流速/ml/min四氢呋喃/异丙醇/%水/%00.92080150.9208015.50.654060
23.00.65406026.00.9208032.00.92080。
[0018]
本发明的目的之二是提供一种检测倍他米松的方法。通过该方法可以有效的鉴别出组合物中是否存在倍他米松。
[0019]
为了实现上述目的,本发明提供的方案为:
[0020]
检测倍他米松的方法,其特征在于,将高效液相检测器波长设定为230~250nm,利用目的一中的方法,将倍他米松进行分离,通入检测器进行检测;将供试品色谱图与已知对照品色谱图进行对比,判定检测物中是否含有所述倍他米松。
[0021]
本发明的目的之三是提供一种测定倍他米松含量的方法。通过该方法可以简单快速的测定出其含量。
[0022]
为了实现上述目的,本发明提供的方案为:
[0023]
测定二丙酸倍他米松起始物料中倍他米松含量的方法,其特征在于,具体包含以下步骤:
[0024]
1)试剂配制
[0025]
取供试样品溶于溶解剂中,加稀释剂,得供试品溶液;取倍他米松对照品溶于溶解剂中,加稀释剂,得对照品溶液;
[0026]
2)分离
[0027]
利用目的一中所述方法,用填充有十八烷基硅烷键合硅胶的色谱柱作为固定相,以四氢呋喃、异丙醇和水为流动相将所述倍他米松分离;
[0028]
3)检测
[0029]
利用目的二中所述方法,将检测器波长设定为230~250nm进行检测,将供试品色谱图与已知对照品色谱图进行对比,判定检测物中是否含有所述倍他米松;
[0030]
4)含量计算
[0031]
根据测量得到的峰面积,使用外标法测量检测物中倍他米松的含量。
[0032]
进一步,所述步骤1)中溶解剂为乙腈:甲醇:水体积比为1:1:2。
[0033]
进一步,所述步骤1)中稀释剂为乙腈:水体积比为25:75。
[0034]
本发明的有益效果在于:
[0035]
(1)本发明通过选择合适的色谱柱,调整流动相的比例、柱温、流速,设置梯度洗脱,利用高效液相色谱法建立稳定可靠的实验方法定性检测倍他米松的含量。
[0036]
(2)该检测方法进行了系统的方法学验证,结果表明专属性、精密度、准确度和耐受性较好,并与中国药典2015版各论中倍他米松质量标准中倍他米松含量测定进行了对比,结果基本一致。
[0037]
(3)与中国药典2015版中倍他米松含量测定方法相比,该测定方法的测定时间大幅度减少从原来的40min,缩短到15min。
附图说明
[0038]
图1为本发明实施例1空白溶液的hplc图
[0039]
图2为本发明实施例1供试品溶液hplc图
[0040]
图3为本发明实施例1杂质混合液的hplc图
[0041]
图4为本发明实施例1、3混合溶液的hplc图
[0042]
图5为本发明实施例2、3倍他米松和地塞米松的hplc图
[0043]
图6为本发明实施例2倍他米松和地塞米松使用bt-170321药典方法的hplc图
[0044]
图7为本发明实施例3混合溶液柱温23℃的hplc图
[0045]
图8为本发明实施例3混合溶液柱温27℃的hplc图
[0046]
图9为本发明实施例3混合溶液流速0.8ml/min的hplc图
[0047]
图10为本发明实施例3混合溶液流速1.0ml/min的hplc图
[0048]
图11为本发明实施例3混合溶液有机相比例18%的hplc图
[0049]
图12为本发明实施例3混合溶液有机相比例22%的hplc图
[0050]
图13为本发明实施例4样品bt-170321的hplc图
[0051]
图14为本发明实施例4样品bt-170321药典方法的hplc图
具体实施方式
[0052]
所举实施例是为了更好地对本发明进行说明,但并不是本发明的内容仅局限于所举实施例。所以熟悉本领域的技术人员根据上述发明内容对实施方案进行非本质的改进和调整,仍属于本发明的保护范围。
[0053]
取倍他米松原成品40mg,精密称定,置100ml量瓶中,加乙腈:甲醇体积比1:1,50ml溶解后,用稀释剂乙腈:水体积比为25:75,稀释至刻度,摇匀,再精密移取5.0ml置50ml量瓶中,加稀释剂乙腈:水体积比为25:75,稀释至刻度,摇匀,作为供试品溶液。另取倍他米松对照品适量,同法配制,作为对照品溶液。照高效液相色谱法(中国药典2015年版四部通则0512)试验,用十八烷基硅烷键合硅胶为填充剂(ods hypersil 100
×
4mm,3μm;或效能相当的色谱柱);以四氢呋喃-异丙醇(体积比88:12):水的体积比为20:80为流动相,检测波长为240nm;流速为每分钟0.9ml;柱温为25℃。
[0054]
样品/杂质名称及结构式见表1:
[0055]
表1样品/杂质名称及结构式
[0056]
[0057][0058]
由于部分杂质在该色谱条件下保留较强,在规定的时间内不能有效洗脱下来,且混合溶液中各已知杂质加入含量较大,故方法专属性和方法耐用性设置为梯度洗脱,以防止未被洗脱下来的杂质干扰检测。样品检测时,供试品溶液浓度较低,样品在符合有关物质标准规定的条件下,各已知杂质不能有效出峰,故不会干扰含量检测。
[0059]
梯度洗脱程序见表2:
[0060]
表2梯度洗脱程序
[0061]
时间/min流速ml/min四氢呋喃/异丙醇(%)水(%)00.92080150.9208015.50.65406023.00.65406026.00.9208032.00.92080
[0062]
实施例1
[0063]
专属性:
[0064]
倍他米松中可能存在的杂质:杂质i、杂质ii、杂质iii、杂质iv、杂质v、杂质vi、杂质vii、杂质viii、杂质ix、杂质x、杂质十一共计11个杂质,我们对上述11个杂质在含量方法验证中进行研究,考察上述杂质是否干扰样品的检测。
[0065]
取空白溶液、供试品溶液、杂质混合溶液和混合溶液分别进样,考察各已知杂质与倍他米松间分离情况。试验结果见表3-7(附图:图1~图4)。
[0066]
表3空白溶液的hplc数据表
[0067][0068]
表4供试品溶液的hplc数据表
[0069][0070]
表5杂质溶液的hplc数据表
[0071][0072]
表6混合溶液的hplc数据表
[0073][0074]
表7专属性试验结果
[0075][0076]
结论:空白稀释剂不干扰样品测定;主峰与相邻杂质分离度为1.77,专属性符合要求。
[0077]
实施例2
[0078]
系统适应性:
[0079]
根据中国药典2015版各论中倍他米松质量标准中倍他米松含量测定规定,取每1ml中含倍他米松与地塞米松各40μg的溶液20μl注入液相色谱仪,倍他米松峰与地塞米松峰的分离度应大于1.9。该发明方法的分离度数据见表8-10(附图:图5~图6):
[0080]
表8倍他米松和地塞米松的hplc数据表
[0081][0082]
表9倍他米松和地塞米松使用ch.p 2015药典方法的hplc数据表
[0083][0084]
表10系统适用性试验结果
[0085]
名称主峰保留时间(min)分离度
倍他米松10.8082.37地塞米松11.9232.37
[0086]
结论:倍他米松和地塞米松间分离度为2.37,大于1.9,符合要求。
[0087]
实施例3
[0088]
色谱条件耐用性:
[0089]
取杂质供试品混合溶液以及中国药典2015版各论中倍他米松质量标准中倍他米松含量测定规定的系统适应性溶液,分别使用正常流动相,预定测试的不同流动相比例、柱温、柱流速,待系统稳定后注入液相色谱仪,记录色谱图,考察主峰与其他杂质间的分离情况,试验结果见表11-17(附图为:图4~图5,图7~图12)。
[0090]
表11混合溶液在柱温23℃的hplc数据表
[0091][0092]
表12混合溶液在柱温27℃的hplc数据表
[0093][0094]
表13混合溶液在流速0.8ml/min的hplc数据表
[0095][0096]
表14混合溶液在流速1.0ml/min的hplc数据表
[0097][0098]
表15混合溶液在有机相比例18%的hplc数据表
[0099][0100][0101]
表16混合溶液在有机相比例22%的hplc数据表
[0102][0103]
表17色谱条件耐用性测试数据
[0104][0105]
结论:从表中的实验数据可知,色谱条件在略有变化的情况下,倍他米松与邻近杂质间分离度均大于1.5,倍他米松与地塞米松间分离度均大于1.9,符合要求。
[0106]
实施例4
[0107]
含量对比实验:
[0108]
精密称取倍他米松40mg,置100ml量瓶中,加[乙腈-甲醇(1:1)]50ml溶解,再用水稀释至刻度,摇匀,精密移取5.0ml置50ml量瓶中,加稀释剂定容,摇匀,即得。按外标法计算倍他米松的含量,同时运用中国药典方法检测含量,对两种方法的结果进行对比。色谱条件及试验结果见表18-21(附图:图13、图14)。
[0109]
表18发明方法与ch.p 2015药典含量方法色谱条件对比表
[0110][0111]
表19样品bet-170321使用该发明方法的hplc数据表
[0112][0113]
表20样品bet-170321使用ch.p 2015药典方法的hplc数据表
[0114][0115]
表21发明方法与ch.p 2015药典含量方法测定结果对比表
[0116][0117]
结论:从表中的实验数据可知,发明方法与药典方法比较,各批次倍他米松的含量基本一致。发明方法运行时间是15min,中国药典方法需要运行约40min(按记录色谱图至主成分峰保留时间的1.5倍计),采用发明方法可大大节省运行时间。
[0118]
最后说明的是,以上实施例仅用以说明本发明的技术方案而非限制,尽管参照较佳实施例对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的宗旨和范围,其均应涵盖在本发明的权利要求范围当中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1