一种胶乳免疫比浊胶乳试剂及制备方法与流程
1.本发明属于体外诊断技术领域,具体涉及一种提高胶乳免疫比浊法抗原或抗体过剩和线性范围的方法。
背景技术:
2.体外诊断领域,胶乳免疫比浊试剂盒中通常将抗体偶联在活化胶乳微球的表面,在缓冲溶液中与被测抗原反应,形成抗原抗体胶乳微球复合物,带来吸光度信号值变化。使用确定浓度的标准品绘制信号值与浓度的标准曲线,测定未知浓度样品时,由全自动分析仪器根据样品所得信号值与标准曲线比较,计算出被测物浓度。
3.抗原过剩和线性范围是免疫比浊试剂盒最重要的性能指标之一。抗原过剩是免疫比浊试剂实现定量检测的前提和范围,即在抗原过剩范围内才可以定量报告结果,是线性范围的前提。线性范围指被测物含量的测定结果与被测物含量(通常为稀释估算值)成直线比例关系的能力。抗原抗体反应时,当抗体量过剩时,称为前带,当抗原量过剩时,称为后带。超过线性范围上限的样本需要进行稀释复测,复测结果乘以稀释倍数得到该样本结果。
4.线性范围上限越高,需要稀释复检的样本少,减少了医院测试成本和人力需求。
5.诊断项目中,有不少项目需要宽线性范围。如重要的炎症标志物c反应蛋白(crp),线性范围上限一般要达到320mg/l、肾病标志物微量白蛋白(malb),线性范围上限一般要达到400mg/l、免疫系统指标血液免疫球蛋白g(igg),线性范围上限一般要达30g/l-60g/l、肿瘤标志物甲胎蛋白(afp),线性范围上限一般要求达到250ng/ml-1000ng/ml。
6.本领域技术人员在胶乳免疫比浊中常规提高抗原过剩以及线性范围的方式,为增加抗体使用量。
7.增加抗体使用量在一定范围内可以提高线性和抗原过剩范围,但在其他条件不变情况下,该方案即增加了试剂成本,又只能在较小幅度使用。同时由于增加抗体量带来的微球表面抗体密度提高,会导致试剂灵敏度提升。在检测系统检测范围有限的情况下,灵敏度和线性范围互相制约,当灵敏度高到一定程度后,就算降低增敏剂用量至零,仍然会因为仪器吸光度检测范围有限,仪器无法区分高浓度样本的信号差异,限制了线性范围和抗原过剩范围。
8.鉴于此,特提出本发明。
技术实现要素:
9.本发明的目的是解决上述问题,提供一种提高胶乳免疫比浊法线性范围的试剂以及制备试剂的方法。
10.本发明中所述“游离的抗体”指的是相对于偶联有胶乳的抗体而言,抗体没有偶联胶乳称为游离的抗体。
11.本发明中所述“封闭抗体的氨基或者羧基”指的是通过化学修饰将抗体上的氨基或者羧基进行反应封闭,本领域常用的修饰剂有乙酸、amcc、sulfo-nhs acetate等。
12.本发明中所述的“胶乳活化”指的是通过化学修饰在胶乳表面形成游离基团,使得活化后的胶乳可以跟抗原或抗体偶联。本领域常用的活化剂有edc、cdi、硼氢化氰、四六磺酸钠等。
13.为解决上述技术问题,本发明提供一种胶乳试剂,所述胶乳试剂中总抗体包括偶联有胶乳的抗体和游离的抗体。
14.本发明的一些实施例中,胶乳试剂中总抗体包括偶联有胶乳的抗体和游离的抗体,其中游离的抗体占总抗体的质量百分比为10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%。
15.本发明的一些实施例中,抗体偶联到胶乳上是通过氨基偶联,在另一些实施例中也可以通过羧基偶联。
16.本发明的一些实施例中,偶联在胶乳上的抗体可以是多克隆抗体也可以是单克隆抗体也可以是抗体片段,例如fab。
17.本发明的一些实施例中,制备本发明的胶乳试剂的方法包括以下步骤:
18.a.胶乳活化:活化胶乳表面的氨基或者羧基;
19.b.抗体与活化后的胶乳偶联;
20.c.去除未偶联胶乳;
21.d.加入游离的抗体。
22.本发明的另一些实施例中,制备本发明的胶乳试剂的方法包括以下步骤:
23.a.胶乳活化:活化胶乳表面的氨基或者羧基;
24.b.封闭抗体的氨基或者羧基;
25.c.将封闭和未封闭的抗体按比例混合成偶联混合液;
26.d.偶联混合液与活化后的胶乳混匀进行偶联反应;
27.e.去除未偶联胶乳。
28.本发明的一些实施例中提供一种具体的c反应蛋白胶乳免疫比浊胶乳试剂,其特征在于,所述胶乳试剂中总抗体包括有偶联胶乳的c反应蛋白抗体和游离的c反应蛋白抗体。其中游离的c反应蛋白抗体占总抗体的质量百分比为10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%。
29.发明的一些实施例中提供一种具体的afp胶乳免疫比浊胶乳试剂,其特征在于,所述胶乳试剂中总抗体包括有偶联胶乳的afp抗体和游离的afp抗体。其中游离的afp抗体占总抗体的质量百分比为10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%。
30.本发明的有益效果是:本发明所提供的胶乳免疫比浊胶乳试剂及制备方法,从胶乳试剂入手,通过相对简单的可放大工艺,直接对胶乳试剂进行改良,不涉及抗体亲和力改进,不增加原料成本,适用范围广,有效减少了宽线性要求项目开发的难度。而且该技术可以结合以往其他技术使用,提高胶乳免疫比浊试剂性能,降低试剂成本。
31.而且,该试剂和方法适用范围广,不受项目不同限制,可应用羧基化胶乳微球中也可以应用在氨基化胶乳微球中。并且可以应用于多个需要线性范围宽的项目,如尿液微量白蛋白(malb),尿液igg(uigg),尿液α1酸性糖蛋白(uorm),尿液转铁蛋白(utrf),血液甲胎蛋白(afp),血液癌胚抗原(cea),血液免疫球蛋白g/a/m(igg/a/m);血液c反应蛋白(crp),血清淀粉样蛋白a(saa)等项目。
具体实施方式
32.下面结合实施例,进一步阐述本发明:
33.实施例1封闭氨基的crp抗体制备:
34.1)sulfo-nhs acetate配制:称取固体0.0135g加入135ul纯化水溶解,浓度0.1mg/ul即100mg/ml。
35.2)crp抗体用稀释液稀释至2mg/ml(10mmpb+150mm naclph7.2)。
36.3)按照摩尔比(抗体:sulfo-nhs acetate=1:50)比例混合,抗体和试剂的量具体如下crp单抗2mg/ml*5ml+sulfo-nhs acetate 8.6ul。
37.4)室温反应1小时,通过透析或脱盐除去未反应的试剂。
38.实施例2制备胶乳试剂1
39.1)390ul交联液(50mm hepes,ph6.1),加入100ul胶乳(jsr),在摇床上震荡混匀,为胶乳液;
40.2)胶乳液中加入13ul的edac溶液,37摄氏度震荡活化1小时;
41.3)加入50ulcrp抗体(2mg/ml)(封闭氨基的crp抗体占10%)到胶乳液中,37摄氏度震荡交联4小时;
42.4)加入50ul的tw-20溶液,37摄氏度震荡封闭1小时;
43.5)将交联液体加入到离心管中,离心后,小心用移液枪弃上清;
44.6)加入2ml清洗液(50mm甘氨酸+0.1%nan3,ph8.0),旋涡震荡,再离心一次,小心弃上清;
45.7)加入5ml胶乳悬浮液(50mm甘氨酸+0.1%bsa+10%蔗糖+0.1%nan3,ph8.0),超声分散处理。
46.实施例3制备胶乳试剂2-15。
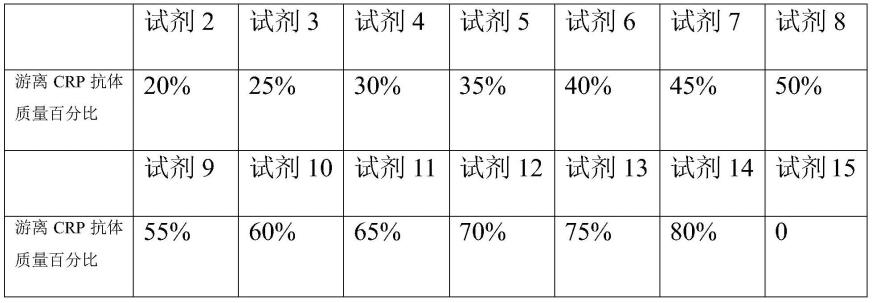
47.以实施例相同的实验方法,制备含有不同浓度的游离crp抗体胶乳试剂,具体含量如表1。
48.表1:不同浓度的游离crp抗体胶乳试剂
[0049][0050]
实施例4上机测试
[0051]
仪器:日立全自动生化仪7060
[0052]
检测流程:吸取样本盘上的样本2ul,同时吸取r1 267ul,加入比色杯中,机械搅拌,37℃下孵育5分钟;在比色杯中加入r2 40ul,机械搅拌;仪器记录下从加入样本开始算起的5分30秒和7分钟的吸光度值,差值就是样本的反应吸光度,吸光度和样本浓度在特定条件下成正比关系。
[0053]
加样比s:r1:r2=2:267:40
[0054]
波长:0/800
[0055]
读点:18-22
[0056]
r1:tris缓冲液
[0057]
r2:标记有crp抗体的胶乳试剂(试剂1-15)
[0058]
采用本发明的实施例能够有效提高crp检测的前带,结果如下:
[0059]
表2:ccp项目中胶乳试剂1-15在300mg/l线性前带检测结果
[0060][0061][0062]
分析表2数据,使用本发明制备胶乳试剂相对有现有技术制备的乳胶试剂可以明显提高crp检测的抗原过剩,其中最优方案已经达到超过2000mg/ml的范围。
[0063]
实施例5制备胶乳试剂16
[0064]
1)390ul交联液(50mm hepes,ph6.1),加入100ul胶乳(jsr),在摇床上震荡混匀,为胶乳液;
[0065]
2)胶乳液中加入13ul的edac溶液,37摄氏度震荡活化1小时;
[0066]
3)加入50ulcrp抗体(2mg/ml)到胶乳液中,37摄氏度震荡交联4小时;
[0067]
4)加入50ul的tw-20溶液,37摄氏度震荡封闭1小时;
[0068]
5)将交联液体加入到离心管中,离心后,小心用移液枪弃上清;
[0069]
6)加入2ml清洗液(50mm甘氨酸+0.1%nan3,ph8.0),旋涡震荡,再离心一次,小心弃上清;
[0070]
7)加入4985ul胶乳悬浮液(50mm甘氨酸+0.1%bsa+10%蔗糖+0.1%nan3,ph8.0)和15ul crp抗体(2mg/ml),超声分散处理。
[0071]
实施例六按实施例5的方式制备含游离crp抗体不同占比的乳胶试剂17-19,具体组分如下:
[0072]
表3:不同胶乳试剂中游离crp抗体不同占比:
[0073][0074]
实施例7上机测试
[0075]
仪器:日立全自动生化仪7060
[0076]
检测流程:吸取样本盘上的样本2ul,同时吸取r1 267ul,加入比色杯中,机械搅拌,37℃下孵育5分钟;在比色杯中加入r2 40ul,机械搅拌;仪器记录下从加入样本开始算起的5分30秒和7分钟的吸光度值,差值就是样本的反应吸光度,吸光度和样本浓度在特定条件下成正比关系。
[0077]
加样比s:r1:r2=2:267:40
[0078]
波长:0/800
[0079]
读点:18-22
[0080]
r1:tris缓冲液
[0081]
r2:标记有crp抗体的胶乳试剂(试剂16-19)
[0082]
采用本发明的实施例能够有效提高crp检测的前带,结果如下:
[0083]
表4:ccp项目中胶乳试剂16-19在300mg/l线性前带检测结果
[0084]
浓度mg/ml150300400500600700800100012001400160018002000试剂16156.7334.2346.1349.4352.6361.4368.2372.2375.3369.8343.6321.7289.8试剂17153.4331.6337.6342.6348.4351.7355.5362.8367.9374.8369.8365.6357.1试剂18151.7323.1331.5333.9337.2345.8351.2360.1363.9357.4346.9331.5284.6试剂19157.6338.4334.6318.2285.1263.4244.7209.3174.6107.485.273.451.8
[0085]
通过表4的数据可以看到,使用本发明实施例5和6的制备胶乳试剂相对有现有技术制备的乳胶试剂可以明显提高crp检测的抗原过剩,其中最优方案已经超过2000mg/ml的抗原过剩。
[0086]
实施例8
[0087]
本实施例的一种提高胶乳免疫比浊法抗原过剩和线性范围的方法,应用于甲胎蛋白检测试剂盒(胶乳免疫比浊法),简写afp。试剂中的胶乳试剂含有游离的afp抗体,能够提高afp检测线性范围。
[0088]
一、胶乳试剂制备
[0089]
1)390ul交联液(50mm hepes,ph6.1),加入100ul胶乳(jsr),在摇床上震荡混匀,为胶乳液;
[0090]
2)胶乳液中加入13ul的edac溶液,37摄氏度震荡活化1小时;
[0091]
3)加入50ulafp抗体(5mg/ml)到胶乳液中,37摄氏度震荡交联4小时;
[0092]
4)加入50ul的tw-20溶液,37摄氏度震荡封闭1小时;
[0093]
5)将交联液体加入到离心管中,离心后,小心用移液枪弃上清;
[0094]
6)加入2ml清洗液(50mm甘氨酸+0.1%nan3,ph8.0),旋涡震荡,再离心一次,小心弃上清;
[0095]
7)加入4985ul胶乳悬浮液(50mm甘氨酸+0.1%bsa+10%蔗糖+0.1%nan3,ph8.0)和15ul afp抗体(5mg/ml),超声分散处理。
[0096]
参照上述的方法制备不同游离afp抗体量的胶乳试剂20-23,具体占比如下:
[0097]
表5:不同胶乳试剂中游离afp抗体不同占比:
[0098][0099]
二上机检测
[0100]
上机参数使用denkaseikenafp试剂参数(hitachi7180),20ul样本,200ul试剂1,100ul试剂2,18-34读点,570/800nm双波长,多点函数spline定标。测定均使用相同试剂1和定标品,试剂2替换成上述试剂20-试剂23。
[0101]
表6:afp抗原过剩测试结果:
[0102][0103]
通过表:6的数据可以看到,使用本发明制备的胶乳试剂20-胶乳25试剂可以改善现有技术中afp抗原过剩的情况。通过本发明的制备方法制备的胶乳试剂获得了超过250000ng/ml的抗原过剩范围。
[0104]
本领域的普通技术人员将会意识到,这里所述的实施例是为了帮助读者理解本发明的原理,应被理解为本发明的保护范围并不局限于这样的特别陈述和实施例。本领域的普通技术人员可以根据本发明公开的这些技术启示做出各种不脱离本发明实质的其它各种具体变形和组合,这些变形和组合仍然在本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1