用于检测液态样品的浓度的检测方法和测试条与流程
本公开大体涉及化学检测技术领域,具体涉及一种用于检测液态样品的浓度的检测方法和测试条。
背景技术:
在临床或科研等实践中,往往需要对多种物质进行浓度检测,例如,c反应蛋白(c-reactiveprotein,crp)和降钙素原(procalcitonin,pct)是常见的抗原,通过对crp和pct的检测,能够为炎症感染提供良好的指标。具体而言,c反应蛋白是机体受到微生物入侵或组织损伤等炎症性刺激时肝细胞合成的急性相蛋白。pct是降钙素的前肽,为一种无激素活性的糖蛋白,作为一个新的炎症指标,广泛应用于感染性疾病的诊断和鉴别诊断,pct是细菌感染所致重症全身性炎症反应的良好指标,在全身性细菌感染和脓毒症辅助鉴别诊断、预后判断、疗效观察等方面有很高的临床价值。
然而,由于不同物质自身的含量或检测需求存在巨大差距,在很多情况下往往无法使用一种测试条进行联合检测。例如,正常检测要求下crp的线性范围是0.5-100mg/l,但crp表面具有较多相同的抗原决定簇,因此检测时需要进行百倍稀释才能解决检测范围窄的局限,若样品不进行稀释,使用常规方式制作的测试条时会发现检测范围较窄,并且在超过一定范围时会产生hook效应(钩状效应),钩状效应是指由于抗原抗体比例不合适而导致假阴性的现象。而pct线性范围是0.1-100ng/ml,对试条的检测灵敏度(0.1ng/ml)要求比较高,所需样本量越多,灵敏度才能越高。因此,由于两种待检物的指标的检测点具有矛盾性,因此联合检测方式在设计和开发上难以操作。
技术实现要素:
本公开是有鉴于上述现有技术的状况而提出的,其目的在于提供一种能够针对具有不同的含量或检测需求的待测物进行联合检测的用于检测液态样品的浓度的检测方法和测试条。
为此,本公开的第一方面提供了一种用于检测液态样品的浓度的检测方法,所述液态样品包括具有第一浓度的第一待测物和具有比所述第一浓度低的第二浓度的第二待测物,所述第一待测物和所述第二待测物不同,所述检测方法包括:准备测试条,所述测试条包括被配置为接收液态样品的样品垫、具有标记物的标记垫、包括沿着层析方向依次设置的具有中和物的中和带和具有检测物的检测带的反应垫、以及被配置为吸收液体的吸收垫,所述层析方向为从所述样品垫朝向所述吸收垫的方向,并且沿着所述层析方向,所述样品垫部分覆盖所述标记垫,所述标记垫部分覆盖所述反应垫,所述反应垫被所述吸收垫部分覆盖,所述中和物固定于所述中和带,所述检测物固定于所述检测带;将液态样品添加至所述样品垫;使液态样品经过所述标记垫,使所述标记物与液态样品中的所述第一待测物结合并形成带有第一标记的第一结合物,使所述标记物与液态样品中的所述第二待测物结合并形成带有第二标记的第二结合物;使液态样品经过所述反应垫,使所述中和物与液态样品中的所述第一结合物中的一部分结合以降低所述第一结合物的浓度,所述中和物不与所述第二结合物结合,并且使液态样品中的所述第一结合物中的剩余部分与所述检测物结合形成第一产物,使液态样品中的所述第二结合物与所述检测物结合形成第二产物;使剩余的液态样品被所述吸收垫吸收;并且通过检测所述检测带中的所述第一产物的含量以得到所述第一待测物的含量,通过检测所述检测带中的所述第二产物的含量以得到所述第二待测物的含量。在本公开中,利用中和带将第一待测物的一部分进行中和,降低第一待测物进入检测带时的浓度,使得有较大浓度差距的第一待测物和第二待测物到达检测带时的浓度差距减小,同时,中和物是固定在反应垫上的,中和产生的复合物会留在中和带,不会到达检测带,不干扰检测带的检测功能,从而能够使用一个测试条对两种含量差距大的物质进行联合检测。
另外,在本公开所涉及的用于检测液态样品的浓度的检测方法,可选地,所述反应垫还包括沿着所述层析方向设置于所述检测带之后的质控带,并且所述标记垫还包括带有第三标记的质控物,所述质控带包括能够与所述质控物结合的质控结合物,所述质控结合物固定于所述质控带;在液态样品经过所述标记垫和所述反应垫时,所述标记垫的质控物跟随液态样品进入所述反应垫,并且使液态样品经过所述质控带以使液态样品中的质控物与所述质控结合物结合,其中,所述质控物不与所述第一待测物、所述第二待测物、所述第一结合物、所述第二结合物、所述中和物或所述检测物结合。由此,能够通过质控带对测试条进行质控,避免检测结果的假阴性。
另外,在本公开所涉及的用于检测液态样品的浓度的检测方法,可选地,所述第一待测物为人体血液中的c反应蛋白,所述第二待测物为人体血液中的降钙素原;所述第一结合物为荧光标记c反应蛋白抗原-抗体复合物,所述第二结合物为荧光标记降钙素原抗原-抗体复合物;所述中和物为能够与荧光标记c反应蛋白抗原-抗体复合物结合的c反应蛋白抗体。在这种情况下,c反应蛋白和降钙素原作为临床常用的检测对象,通过使用荧光标记对crp抗体和pct抗体进行标记,从而能够使用一个测试条对c反应蛋白和降钙素原这两种含量差距大的物质进行联合检测。
另外,在本公开所涉及的用于检测液态样品的浓度的检测方法,可选地,在所述测试条中,所述c反应蛋白抗体的含量为2.4~7.2μg。由此,使中和物的浓度保持在合适范围,既不会中和过少c反应蛋白导致钩状效应,也不会中和过多c反应蛋白导致无法检测,从而能够实现对crp和pct的联合检测。
本公开第二方面提供了一种用于检测液态样品的浓度的测试条,所述液态样品包括具有第一浓度的第一待测物和具有比所述第一浓度低的第二浓度的第二待测物,且所述第一待测物和所述第二待测物不同,所述测试条包括依次设置在衬垫上的样品垫、标记垫、反应垫和吸收垫;所述样品垫被配置为接收液态样品;所述标记垫具有标记物,所述标记物能够与所述第一待测物结合并形成带有第一标记的第一结合物,所述标记物能够与所述第二待测物结合并形成带有第二标记的第二结合物;从所述样品垫至所述吸收垫的方向为层析方向,沿着所述层析方向,所述样品垫部分覆盖所述标记垫,所述标记垫部分覆盖所述反应垫,所述反应垫被所述吸收垫部分覆盖;所述反应垫包括沿着所述层析方向依次设置的中和带和检测带,所述中和带具有用于与所述第一结合物中的一部分结合以降低所述第一结合物的浓度的中和物,所述中和物不与所述第二结合物结合,并且所述中和物固定于所述中和带,所述检测带具有能够与所述第一结合物中的剩余部分以及所述第二结合物结合以进行检测的检测物,并且所述检测物固定于所述检测带;所述吸收垫由吸液材料制成,所述吸收垫被配置为吸收进入所述吸收垫的液体。在本公开中,利用中和带将第一待测物的一部分进行中和,降低第一待测物进入检测带时的浓度,使得有较大浓度差距的第一待测物和第二待测物到达检测带时的浓度差距减小,同时,中和物是固定在反应垫上的,中和产生的复合物会留在中和带,不会到达检测带,不干扰检测带的检测功能,从而能够使用一个测试条对两种含量差距大的物质进行联合检测。
另外,在本公开所涉及的用于检测液态样品的浓度的测试条,可选地,所述反应垫还包括沿着所述层析方向设置于所述检测带之后的质控带,并且所述标记垫还包括带有第三标记的质控物,所述质控带具有能够与所述质控物结合的质控结合物,所述质控结合物固定于所述质控带,并且所述质控物不与所述第一待测物、所述第二待测物、所述第一结合物、所述第二结合物、所述中和物或所述检测物结合。由此,通过质控带对测试条进行质控,从而能够避免假阴性。
另外,在本公开所涉及的用于检测液态样品的浓度的测试条,可选地,所述第一待测物为人体血液中的c反应蛋白,所述第二待测物为人体血液中的降钙素原。由此,能够使用一个测试条对c反应蛋白和降钙素原这两种含量差距大的物质进行联合检测。
另外,在本公开所涉及的用于检测液态样品的浓度的测试条,可选地,所述第一结合物为荧光标记c反应蛋白抗原-抗体复合物,所述第二结合物为荧光标记降钙素原抗原-抗体复合物。由此,能够通过荧光信号来判定抗原含量。
另外,在本公开所涉及的用于检测液态样品的浓度的测试条,可选地,所述中和物为能够与所述荧光标记c反应蛋白抗原-抗体复合物结合的c反应蛋白抗体,在所述测试条中,所述c反应蛋白抗体的含量为2.4~7.2μg。由此,能够使中和物的浓度保持在合适范围,既不会中和过少c反应蛋白导致钩状效应,也不会中和过多c反应蛋白导致无法检测,从而能够实现对crp和pct的联合检测。
另外,在本公开所涉及的用于检测液态样品的浓度的测试条,可选地,所述中和带与所述检测带之间的距离为5~10mm,所述检测带与所述质控带之间的距离为3~5mm。
根据本公开,提供一种能够对具有不同的含量或检测需求的待测物进行联合检测的检测液态样品的浓度的检测方法和测试条。
附图说明
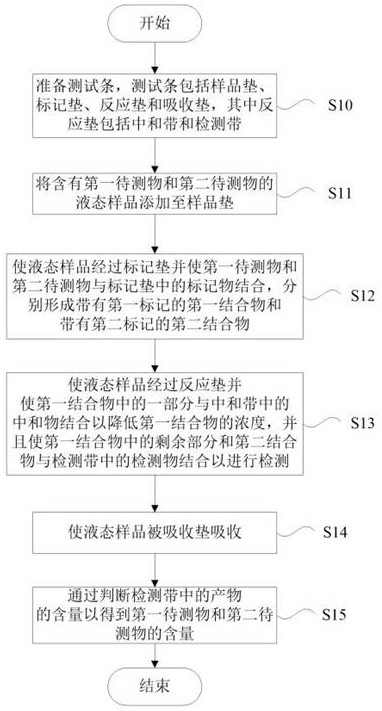
图1是示出了本公开的实施方式所涉及的用于检测液态样品的浓度的检测方法的流程示意图。
图2是示出了本公开的实施方式所涉及的用于检测液态样品的浓度的测试条的结构示意图。
图3是示出了本公开的实施方式所涉及的用于检测液态样品的浓度的测试条的制备流程示意图。
图4是示出了本公开的实施方式所涉及的用于检测液态样品的浓度的测试条用于检测crp的测试结果线性回归图。
图5是示出了本公开的实施方式所涉及的用于检测液态样品的浓度的测试条用于检测pct的测试结果线性回归图。
具体实施方式
以下,参考附图,详细地说明本公开的优选实施方式。在下面的说明中,对于相同的部件赋予相同的符号,省略重复的说明。另外,附图只是示意性的图,部件相互之间的尺寸的比例或者部件的形状等可以与实际的不同。
需要说明的是,本公开中的术语“包括”和“具有”以及它们的任何变形,例如所包括或所具有的一系列步骤或单元的过程、方法、系统、产品或设备不必限于清楚地列出的那些步骤或单元,而是可以包括或具有没有清楚地列出的或对于这些过程、方法、产品或设备固有的其它步骤或单元。
另外,在本公开的下面描述中涉及的小标题等并不是为了限制本公开的内容或范围,其仅仅是作为阅读的提示作用。这样的小标题既不能理解为用于分割文章的内容,也不应将小标题下的内容仅仅限制在小标题的范围内。
以下,参考图1和图2,详细地描述本公开的实施方式所涉及的用于检测液态样品的浓度的方法,图1是示出了本公开的实施方式所涉及的用于检测液态样品的浓度的检测方法的流程示意图。图2是示出了本公开的实施方式所涉及的用于检测液态样品的浓度的测试条的结构示意图。
在本实施方式中,如图1和图2所示,用于检测液态样品的浓度的方法可以包括准备测试条2,测试条2包括样品垫21、标记垫22、反应垫23和吸收垫24,其中反应垫23包括中和带231和检测带232(步骤s10);将含有第一待测物和第二待测物的液态样品1添加至样品垫21(步骤s11);使液态样品1经过标记垫22并使第一待测物和第二待测物与标记垫22中的标记物结合,分别形成带有第一标记的第一结合物和带有第二标记的第二结合物(步骤s12);并且使液态样品1经过反应垫23并使第一结合物中的一部分与中和带231中的中和物结合以降低第一结合物的浓度,并且使第一结合物中的剩余部分和第二结合物与检测带232中的检测物结合以进行检测(步骤s13);使液态样品1被吸收垫24吸收(步骤s14);并且通过判断检测带232中的产物的含量以得到第一待测物和第二待测物的含量(步骤s15)。
在一些示例中,在步骤s10中,液态样品1可以包括具有第一浓度的第一待测物和具有比第一浓度低的第二浓度的第二待测物,且第一待测物和第二待测物不同。
在一些示例中,在步骤s10中,样品垫21可以被配置为接收含有第一待测物和第二待测物的液态样品1。
在一些示例中,在步骤s10中,标记垫22可以包括标记物。
在一些示例中,在步骤s10中,中和带231和检测带232可以沿着层析方向s依次设置于反应垫23。在一些示例中,中和带231可以包括中和物。在一些示例中,中和物可以固定于中和带231。在一些示例中,检测带232可以包括检测物。在一些示例中,检测物可以固定于检测带232。
在一些示例中,在步骤s10中,吸收垫24被配置为吸收液体。
在一些示例中,在步骤s10中,层析方向s可以为从样品垫21至吸收垫24的方向,并且沿着层析方向s,样品垫21可以部分覆盖标记垫22,标记垫22可以部分覆盖反应垫23,反应垫23可以被吸收垫24部分覆盖。
在本实施方式中,如图1所示,用于检测液态样品的浓度的检测方法可以包括将含有第一待测物和第二待测物的液态样品1添加至样品垫21(步骤s11)。
在一些示例中,在步骤s11中,第一待测物可以为人体血液中的c反应蛋白,第二待测物可以为人体血液中的降钙素原。
在本实施方式中,如图1所示,用于检测液态样品的浓度的方法可以包括使液态样品1经过标记垫22并使第一待测物和第二待测物与标记垫22中的标记物结合,分别形成带有第一标记的第一结合物和带有第二标记的第二结合物(步骤s12)。
在一些示例中,在步骤s12中,第一待测物可以全部与标记物结合,使第一待测物全部带有第一标记。在一些示例中,第二待测物可以全部与标记物结合,使第二待测物全部带有第二标记。
在一些示例中,在步骤s12中,标记物还可以包括带有第三标记的质控物。在一些示例中,质控物不与第一待测物、第二待测物、第一结合物、第二结合物结合。
在一些示例中,在步骤s12中,第一标记、第二标记和第三标记可以相同。
在一些示例中,在步骤s12中,第一结合物可以为荧光标记c反应蛋白抗原-抗体复合物,第二结合物可以为荧光标记降钙素原抗原-抗体复合物。
在本实施方式中,如图1所示,用于检测液态样品的浓度的方法可以包括使液态样品1经过反应垫23并使第一结合物中的一部分与中和带231中的中和物结合以降低第一结合物的浓度,并且使第一结合物中的剩余部分和第二结合物与检测带232中的检测物结合以进行检测(步骤s13)。
在一些示例中,在步骤s13中,中和物可以固定于中和带231。另外,中和物不和第二待测物结合。
在一些示例中,中和物可以为能够与荧光标记c反应蛋白抗原-抗体复合物结合的c反应蛋白抗体。
在一些示例中,在测试条2中,c反应蛋白抗体的含量可以为2.4~7.2μg。
在一些示例中,检测物可以固定于检测带232。在一些示例中,可以使第一结合物中的剩余部分和第二结合物与检测带232中的检测物全部结合。在一些示例中,中和物和检测物不与质控物结合。
在一些示例中,检测带232可以包括第一检测带2321和第二检测带2322。在一些示例中,第一检测带2321可以包括第一检测物。在一些示例中,第二检测带2322可以包括第二检测物。
在一些示例中,可以使液态样品1中的第一结合物中的剩余部分与第一检测物结合形成第一产物,使液态样品1中的所述第二结合物与第二检测物结合形成第二产物。
在一些示例中,在步骤s13中,反应垫23还可以包括质控带233。在一些示例中,质控带233可以沿着层析方向s设置于检测带232之后。在一些示例中,质控带233可以包括质控结合物,质控结合物可以固定于质控带233。在一些示例中,质控物可以与质控结合物进行结合。
在一些示例中,在步骤s13中,在液态样品1经过标记垫22和反应垫23时,标记垫22的质控物跟随液态样品1进入反应垫23,并且使液态样品1经过质控带233以使液态样品1中的质控物与质控结合物结合,其中,质控物不与第一待测物、第二待测物、第一结合物、第二结合物、中和物或检测物结合。
在本实施方式中,如图1所示,用于检测液态样品的浓度的方法可以包括使液态样品1被吸收垫24吸收(步骤s14)。
在一些示例中,在步骤s14中,吸收垫24可以由吸水性良好的材料制成。在这种情况下,能够吸收进入吸收垫24的液体。
在本实施方式中,如图1所示,用于检测液态样品的浓度的方法可以包括通过判断检测带232中的产物的含量以得到第一待测物和第二待测物的含量(步骤s15)。
在一些示例中,在步骤s15中,通过检测检测带232中的第一产物的含量以得到第一待测物的含量,通过检测检测带232中的第二产物的含量以得到所第二待测物的含量。
在一些示例中,在步骤s15中,还可以通过检测质控带233中的产物的含量判断得到的第一待测物和第二待测物的含量是否可信。在一些示例中,质控带233中产物含量为零,则得到的第一待测物和第二待测物的检测结果为不可信。
以下,再参考图2,详细地描述本公开的实施方式所涉及的用于检测液态样品的浓度的测试条,图2是示出了本公开的实施方式所涉及的用于检测液态样品的浓度的测试条的结构示意图。
在本实施方式中,如图2所示,用于检测液态样品的浓度的测试条2的检测对象可以为液态样品1,用于检测液态样品的浓度的测试条2可以包括样品垫21、标记垫22、反应垫23、吸收垫24和衬垫25,其中反应垫23包括中和带231、检测带232、质控带233,检测带232包括第一检测带2321和第二检测带2322。
在一些示例中,从样品垫21至吸收垫24的方向为层析方向s,沿着层析方向s,样品垫21部分覆盖标记垫22,标记垫22部分覆盖反应垫23,反应垫23被吸收垫24部分覆盖。
在一些示例中,样品垫21、标记垫22、反应垫23和吸收垫24均设置在衬垫25上。
在一些示例中,液态样品1可以包括待测物包括具有第一浓度的第一待测物和具有比第一浓度低的第二浓度的第二待测物。在一些示例中,液态样品1可以为人血液样本,例如可以为全血、血浆或血清。
在一些示例中,第一待测物可以为人体血液中的c反应蛋白(crp)。
在一些示例中,第二待测物可以为人体血液中的降钙素原(pct)。
在一些示例中,全血的样本量可以为75~150μl,优选为100μl;血浆或者血清的样本量可以为60~100μl,优选为70μl。由此,使测试条2能够承载更多加样量,并且更准确地进行检测。
在一些示例中,样品垫21可以具有全血过滤功能,可以为市场上已有的滤血膜如全血滤血膜gf2和全血滤血膜mf1,也可以为抗红细胞抗体(rbc抗体)处理后的玻璃纤维膜。
在一些示例中,标记垫22可以为聚酯纤维或玻璃纤维。在一些示例中,标记垫22包被有标记物。在一些示例中,标记物可以为荧光标记crp抗体、荧光标记pct抗体和荧光标记鸡igy的混合物。
在一些示例中,荧光标记crp抗体可以与液态样品1中的crp特异性结合形成荧光标记crp抗原-抗体复合物。
在一些示例中,荧光标记pct抗体可以与液态样品1中的pct特异性结合形成荧光标记pct抗原-抗体复合物。
在一些示例中,荧光标记鸡igy不与液态样品1中的crp、pct结合。在一些示例中,荧光标记鸡igy不与荧光标记crp抗原-抗体复合物和荧光标记pct抗原-抗体复合物结合。
在一些示例中,反应垫23可以为硝酸纤维素膜(nc膜)。在一些示例中,硝酸纤维素膜的尺寸为80×4mm。
在一些示例中,中和带231可以包被有中和物(未图示)。由此,将中和物固定至中和带231上。在一些示例中,中和物(未图示)可以为能够与荧光标记crp抗原-抗体复合物相结合的crp抗体。在一些示例中,crp抗体的含量可以为2.4~7.2μg。
在一些示例中,检测带232可以包被有检测物(未图示)。由此,将检测物固定至检测带232上。
在一些示例中,检测物可以包括第一检测物和第二检测物。
在一些示例中,检测带232可以包括第一检测带2321和第二检测带2322。
在一些示例中,第一检测带2321可以为crp检测带,第一检测物可以为能够与荧光标记crp抗原-抗体复合物相结合的crp检测抗体。
在一些示例中,crp抗体和crp检测抗体可以相同。
在一些示例中,第二检测带2322可以为pct检测带,第二检测物可以为能够与荧光标记pct抗原-抗体复合物相结合的pct检测抗体。
在一些示例中,第一检测带2321和第二检测带2322包被的抗体种类可以互换,也即,第一检测带2321可以为pct检测带,pct检测带包被有能够与荧光标记pct抗原-抗体复合物相结合的pct检测抗体;第二检测带2322可以为crp检测带,crp检测带包被有能够与荧光标记crp抗原-抗体复合物相结合的crp检测抗体;crp抗体和crp检测抗体可以相同。
在一些示例中,反应垫23包括可以质控带233,质控带233包被有质控结合物(未图示)。由此,将质控结合物固定至质控带233上。
在一些示例中,质控结合物(未图示)可以为能够与荧光标记鸡igy结合的羊抗鸡igy。在一些示例中,质控结合物不与中和物、检测物结合。
在一些示例中,中和带231与第一检测带2321之间的距离可以为5~10mm。在一些示例中,第一检测带2321和第二检测带2322之间的距离可以为3~5mm。在一些示例中,第二检测带2322和质控带233之间的距离可以为3~5mm。
在一些示例中,吸收垫24可以由吸水性良好的材料制成,在这种情况下,能够吸收进入吸收垫24的液体。在一些示例中,吸收垫24可以为吸水纸。
在一些示例中,衬垫25可以由支撑性良好的材料制成。例如,衬垫25可以为pvc(聚氯乙烯)板。
以下,再参考图3,详细地描述本公开的实施方式所涉及的用于检测液态样品的浓度的测试条的制备流程,图3是示出了本公开的实施方式所涉及的用于检测液态样品的浓度的测试条的制备流程图。
在本实施方式中,如图3所示,用于检测液态样品的浓度的测试条的制备流程可以包括提供样品垫21、标记垫22、反应垫23、吸收垫24和衬垫25(步骤s20);使标记垫22包被标记物(步骤s21);使反应垫23包被中和物、检测物和质控物(步骤s22);并且将样品垫21、标记垫22、反应垫23、吸收垫24、衬垫25组装形成测试条2(步骤s23)。
在一些示例中,在步骤s20中,样品垫21可以具有全血过滤功能,可以为市场上已有的滤血膜如全血滤血膜gf2和全血滤血膜mf1,也可以为抗红细胞抗体处理过(rbc抗体)的玻璃纤维膜。
在一些示例中,在步骤s20中,标记垫22可以为聚酯纤维或玻璃纤维,标记垫包可以被有标记物。
在一些示例中,在步骤s20中,反应垫23可以为硝酸纤维素膜(nc膜)。在一些示例中,硝酸纤维素膜的尺寸为80×4mm。
在一些示例中,在步骤s20中,吸收垫24可以由吸水性良好的材料制成,例如可以为吸水纸。
在一些示例中,在步骤s20中,衬垫25可以由支撑性良好的材料制成,例如可以为pvc(聚氯乙烯)板。
在本实施方式中,如图3所示,用于检测液态样品的浓度的测试条的制备流程可以包括使标记垫22包被标记物(步骤s21)。
在一些示例中,在步骤s21中,标记物可以为荧光标记crp抗体、荧光标记pct抗体和荧光标记鸡igy的混合物。
在一些示例中,在步骤s21中,荧光标记crp抗体可以与人血液样本中的crp特异性结合形成荧光标记crp抗原-抗体复合物,
在一些示例中,在步骤s21中,荧光标记pct抗体可以与人血液样本中的pct特异性结合形成荧光标记pct抗原-抗体复合物。
在一些示例中,在步骤s21中,荧光标记鸡igy不与人血液样本中的crp、pct结合。在一些示例中,荧光标记鸡igy不与荧光标记crp抗原-抗体复合物、荧光标记pct抗原-抗体复合物结合。
在一些示例中,在步骤s21中,荧光标记可以通过使用荧光物质进行标记。
在一些示例中,在步骤s21中,荧光物质可以包括荧光染料、荧光微球、量子点。
在一些示例中,在步骤s21中,可以将crp抗体、pct抗体和鸡igy分别用荧光物质进行标记,获得浓度均为0.5~2mg/ml的荧光标记抗体溶液。
在一些示例中,在步骤s21中,可以用荧光抗体稀释液将不同荧光抗体进行稀释,其中crp抗体稀释比例为10%~25%,pct抗体稀释比例为10%~25%,鸡igy稀释比例为5%~10%。
在一些示例中,在步骤s21中,荧光抗体稀释液成分可以包括:0.01~0.05mol/l的pbs;1%~5%海藻糖;0.1%~2%bsa;0.5%~2%t-20;0.1%~1%酪蛋白;0.1~1%pvp;0.05~0.1%nan3。
在一些示例中,在步骤s21中,荧光抗体稀释液成分可以为:0.02mol/l的pbs,1%海藻糖,1%t-20,0.2%酪蛋白,0.5%pvp,0.05%nan3。
在一些示例中,在步骤s21中,可以将稀释后的荧光标记crp抗体、pct抗体和鸡igy按1:1:1的体积比进行混合均匀。
在一些示例中,在步骤s21中,可以将5μl的混匀的荧光标记crp抗体、pct抗体和鸡igy均匀地涂抹或喷洒在标记垫22上。
在一些示例中,在步骤s21中,可以将包被了荧光标记crp抗体、pct抗体和鸡igy的标记垫22进行干燥。
在一些示例中,在步骤s21中,干燥环境的温度可以为25~45℃,湿度可以为0%~25%,干燥时间可以为4~12h。
在本实施方式中,如图3所示,用于检测液态样品的浓度的测试条的制备流程可以包括使反应垫23包被中和物、检测物和质控物(步骤s22)。
在一些示例中,在步骤s22中,反应垫23沿着层析方向s依次具有中和带231、检测带232和质控带233。
在一些示例中,在步骤s22中,中和物可以为crp抗体,通过在反应垫23上包被crp抗体形成中和带231,crp抗体可以与荧光标记crp抗原-抗体复合物进行结合。
在一些示例中,在步骤s22中,可以包括用包被稀释液对crp抗体进行稀释,获得浓度为2~6mg/ml的crp抗体溶液。例如,crp抗体溶液的浓度可以为2mg/ml、3mg/ml、4mg/ml、5mg/ml、6mg/ml。
在一些示例中,在步骤s22中,包被稀释液成分可以为0.01~0.1mol/l的pbs;3%~5%甲醇、0.1%~0.5%t-20。
在一些示例中,在步骤s22中,可以将稀释后的crp抗体溶液包被至反应垫23上,划线速度为2~5μl/cm。在一些示例中,划线速度为3μl/cm。
在一些示例中,在步骤s22中,检测带232可以包括第一检测带2321和第二检测带2322,检测物可以包括第一检测物和第二检测物。
在一些示例中,在步骤s22中,第一检测带2321可以为crp检测带,第一检测物可以为能够与荧光标记crp抗原-抗体复合物相结合的crp检测抗体。
在一些示例中,在步骤s22中,第二检测带2322可以为pct检测带,第二检测物可以为能够与荧光标记pct抗原-抗体复合物相结合的pct检测抗体。
在一些示例中,在步骤s22中,在反应垫23上分别包被crp检测抗体和pct检测抗体形成crp检测带和pct检测带,crp检测抗体可以与荧光标记crp抗原-抗体复合物进行结合,pct检测抗体可以与荧光标pct抗原-抗体复合物进行结合。
在一些示例中,在步骤s22中,可以包括用包被稀释液对crp检测抗体进行稀释,获得浓度为0.5~5mg/ml的crp检测抗体溶液。
在一些示例中,在步骤s22中,可以包括用包被稀释液对crp检测抗体进行稀释,获得浓度为2mg/ml的crp检测抗体溶液。
在一些示例中,在步骤s22中,包被稀释液成分可以为0.01~0.1mol/l的pbs;3%~5%甲醇、0.1%~0.5%t-20。
在一些示例中,在步骤s22中,可以包括将稀释后的crp检测抗体溶液包被至反应垫23上,划线速度为0.6~1.5μl/cm。在一些示例中,划线速度为1μl/cm。
在一些示例中,在步骤s22中,可以包括用包被稀释液对pct检测抗体进行稀释,获得浓度为0.5~5mg/ml的pct检测抗体溶液。
在一些示例中,在步骤s22中,可以包括用包被稀释液对pct检测抗体进行稀释,获得浓度为2mg/ml的pct检测抗体溶液。
在一些示例中,在步骤s22中,包被稀释液成分可以为0.01~0.1mol/l的pbs;3%~5%甲醇、0.1%~0.5%t-20。
在一些示例中,在步骤s22中,可以包括将稀释后的pct检测抗体溶液包被至反应垫23上,划线速度为0.6~1.5μl/cm。在一些示例中,划线速度为1μl/cm。
在一些示例中,在步骤s22中,质控物可以为羊抗鸡igy。
在一些示例中,在步骤s22中,质控物不与中和物、检测物结合。
在一些示例中,在步骤s22中,可以通过在反应垫23上包被羊抗鸡igy形成质控带233,羊抗鸡igy可以与荧光标记鸡igy进行结合。
在一些示例中,在步骤s22中,可以包括用包被稀释液对羊抗鸡igy进行稀释,获得浓度为0.3~3mg/ml的羊抗鸡igy溶液。
在一些示例中,在步骤s22中,可以包括用包被稀释液对羊抗鸡igy进行稀释,获得浓度为1mg/ml的羊抗鸡igy溶液。
在一些示例中,在步骤s22中,包被稀释液成分可以为0.01~0.1mol/l的pbs;3%~5%甲醇、0.1%~0.5%t-20。
在一些示例中,在步骤s22中,可以包括将稀释后的羊抗鸡igy溶液包被至反应垫23上,划线速度为0.6~1.5μl/cm。在一些示例中,划线速度为1μl/cm。
在一些示例中,在步骤s22中,可以将包被了crp抗体、crp检测抗体、pct检测抗体和羊抗鸡igy的反应垫23进行干燥。在一些示例中,干燥环境的温度可以为25~45℃,湿度可以为0%~25%,干燥时间可以为4~12h。
在一些示例中,在步骤s22中,反应垫23沿着层析方向s依次具有中和带231、crp检测带、pct检测带和质控带233,其中crp检测带和pct检测带的位置也可以互换。
在一些示例中,在步骤s22中,中和带231与crp检测带之间的距离可以为5~10mm。
在一些示例中,在步骤s22中,crp检测带和pct检测带之间的距离可以为3~5mm。
在一些示例中,在步骤s22中,pct检测带和质控带233之间的距离可以为3~5mm。
在本实施方式中,如图3所示,用于检测液态样品的浓度的测试条的制备流程可以包括将样品垫21、标记垫22、反应垫23、吸收垫24、衬垫25组装形成测试条2(步骤s23)。
在一些示例中,在步骤s23中,沿着层析方向s,样品垫21部分覆盖标记垫22,标记垫22部分覆盖反应垫23,反应垫23被吸收垫24部分覆盖,样品垫21、标记垫22、反应垫23和吸收垫24均固定于衬垫25上。
【实施例】
为了进一步说明本公开,以下结合实施例与对比例对本公开提供用于检测液态样品的浓度的测试条进行详细描述,并结合对比例对本公开实现的有益效果进行充分说明。
首先,根据表1分别准备各实施例(实施例1至实施例5)及对比例的抗体溶液,然后,按照表1所示浓度的荧光标记鸡crp抗体、荧光标记pct抗体和荧光标记鸡igy包被至标记垫22,标记垫22由玻璃纤维材料制成;反应垫23沿着层析方向s依次具有中和带231、crp检测带(第一检测带2321)、pct检测带(第一检测带2322)和质控带233,中和带231和crp检测带距离为6mm,crp检测带、pct检测带和质控带233之间距离均为5mm,将下列浓度的crp抗体包被至中和带231、将crp检测抗体包被至crp检测带、将pct检测抗体包被至pct检测带、将羊抗鸡igy包被至质控带233,反应垫23的组成材料为硝酸纤维素膜(nc膜),硝酸纤维素膜的尺寸为80×4mm,其中包被crp抗体时的划线速度为3μl/cm,包被crp检测抗体时的划线速度为1μl/cm,包被pct检测抗体时的划线速度为1μl/cm,包被羊抗鸡igy时的划线速度为1μl/cm。然后将包被好抗体的标记垫22和反应垫23与样品垫21、吸收垫24和衬垫25进行组装,由此,得到实施例(实施例1至实施例5)及对比例的用于检测液态样品的浓度的测试条2。
其中,各实施例中crp抗体的浓度为2mg/ml至6mg/ml,也即,通过单位换算可得,在测试条2中,crp抗体的含量为(2~6mg/ml)×(3μl/cm)×(4mm)=(2.4~7.2μg)。
表1实施例与对比例各组分浓度
结果测试
对根据表1得到的实施例(实施例1至实施例5)及对比例的用于检测液态样品的浓度的测试条,用不同浓度的crp溶液与pct溶液进行加标测试,将不同浓度的crp与pct溶液加至各实施例和对比例得到的测试条2的样品垫21上,加样量均为70μl,然后使用荧光检测设备对各实施例和对比例中检测带232中产物的荧光含量进行测定,得到crp和pct的测试结果浓度值。其中crp溶液的加标浓度值是由生化分析仪测定得出,pct溶液的加标浓度值是由电化学分析仪测定得出。
测试结果见表2和表3,其中,表2的第一列为crp的加标浓度(单位为mg/l),第2-6列为crp的测试结果浓度(单位为mg/l),表3的第一列为pct的加标浓度(单位为ng/ml),第2-6列为pct的测试结果浓度(单位为ng/ml)。
并根据表2进行线性模拟得到线性回归图(图4),图4是示出了本公开的实施方式所涉及的用于检测液态样品的浓度的测试条用于检测crp的测试结果线性回归图。图4中横坐标为crp加标浓度值,纵坐标为crp测试结果浓度值。
并根据表3进行线性模拟得到线性回归图(图5),图5是示出了本公开的实施方式所涉及的用于检测液态样品的浓度的测试条用于检测pct的测试结果线性回归图。图5中横坐标为pct加标浓度值,纵坐标为pct测试结果浓度值。
表2crp检测结果
表3pct检测结果
从表2和图4可知,相比对比例的测试条,实施例1-5的测试条,对于crp的检测均可以实现0.5-100mg/l的检测范围,其中实施例3-5的测试条对于crp的检测可以实现0.5-200mg/l的检测范围,各实施例(实施例1-5)的线性相关性良好,其中实施例4的线性相关性最好,换言之,实施例4的测试条检测准确度最高;而对比例对crp的检测范围为0-30mg/l,其线性相关性也差,不能满足检测需求。具体地,实施例1的线性回归方程为y=0.506x+7.270,r²=0.851;实施例2的线性回归方程为y=0.567x+6.57,r²=0.907;实施例3的线性回归方程为y=0.867x+2.480,r²=0.986;实施例4的线性回归方程为y=1.010x-0.481,r²=0.999;实施例5的线性回归方程为y=1.054x-1.162,r²=0.998;对比例的线性回归方程为y=0.038x+8.393,r²=0.064。
从表3和图5可知,实施例1-5的测试条对于pct的检测均可以实现0.1-100ng/ml的检测范围,最低检测限为0.1ng/ml,且线性相关性良好。具体地,实施例1的线性回归方程为y=0.821x+0.989,r²=0.986;实施例2的线性回归方程为y=0.873x+0.413,r²=0.994;实施例3的线性回归方程为y=0.916x+0.922,r²=0.994;实施例4的线性回归方程为y=0.966x+0.348,r²=0.994;实施例5的线性回归方程为y=0.977x+0.210,r²=0.999;对比例的线性回归方程为y=0.783x+0.782,r²=0.996。
综上,本发明的实施例通过添加适量的crp抗体至中和带231,使得用于检测液态样品的浓度的测试条实现对crp于pct的同时检测或联合检测,且检测范围和检测灵敏度均能够满足临床要求(检测范围crp:0.5-100mg/l,pct:0.1-100ng/ml;灵敏度pct:0.1ng/ml)。而对比例未添加crp抗体至中和带231,则无法实现对crp的检测需求,也即对比例的测试条无法实现对crp于pct的同时检测或联合检测。
虽然以上结合附图和示例对本公开进行了具体说明,但是可以理解,上述说明不以任何形式限制本公开。本领域技术人员在不偏离本公开的实质精神和范围的情况下可以根据需要对本公开进行变形和变化,这些变形和变化均落入本公开的范围内。
- 还没有人留言评论。精彩留言会获得点赞!