一种基于近红外传感器融合的药物结晶过程质量非线性表征方法
1.本发明属于检测分析和药物质量控制技术领域,具体涉及一种基于近红外光谱数据融合的药物结晶过程质量非线性表征方法
背景技术:
2.公开该背景技术部分的信息仅仅旨在增加对本发明的总体背景的理解,而不必然被视为承认或以任何形式暗示该信息构成已经成为本领域一般技术人员所公知的现有技术。
3.近红外光谱技术(near infrared spectroscopy,nirs)是近几年发展起来的一种快速检测技术,属于分子振动光谱。近红外(near infrared,nir)谱区是指介于可见区(visible region,vis)和中红外(mid infrared spectroscopy,mir)区之间的电磁波,其波长范围为780~2526nm,分为短波近红外(700~1100nm)和长波近红外(1100~2500nm)。由于其较易获取图谱,且图谱稳定,但同时也存在与光谱重叠严重的缺陷,因此需要通过化学计量学方法的协助,以便于从近红外光谱多组分吸收的重叠和交叉中找出有用的吸收波长,完成分析过程。
4.结晶作为一种重要的药物纯化手段,应用于原料药的分离、纯化过程,尤其适用于具有目标特性原料的生产。利用nir技术对结晶过程进行检测,有助于增强对于产品质量形成过程的理解,加强对结晶工艺的分析、设计和优化,从而确保原料和最终产品的质量达到设计指标。有研究人员认为在某些结晶体系中,固体的存在易使探针结垢,导致光谱失真,对结晶的模型预测产生较大偏差,所以其在应用于结晶过程时要注意创造理想的条件。但另有研究者认为这种特点其实也代表近红外中同时包含了固液两相的丰富信息,而不再是一种不利的缺点。
5.对于过程分析来说,以实验室台式机为代表的第一代在线分析仪器具有准确度高、稳定性强的优势,但是也存在光谱采集速度慢、安装环境要求高、性价比较低等限制。微型化、低成本的nir传感器开始进入研究人员的视野。微型近红外光谱传感器具有技术成熟稳定、集成度高、体积小质量轻、性价比高、适应性强、可选择性好等优点,但同时存在波长范围短的缺点。
技术实现要素:
6.针对上述现有技术中存在的问题,本发明提供了一种近红外传感器融合的药物结晶过程质量非线性表征方法,开发基于微型传感器融合的新一代在线分析方法,有效解决波长范围的限制,降低nir过程分析的成本,实现药物结晶过程中关键质量的快速分析,并提升模型的预测能力,具有显著的社会、经济效益。本发明是通过如下技术方案实现的:
7.本发明的第一个方面,提供一种近红外传感器融合方法,所述方法包括,近红外光经过待测物质再通过光纤分路器分别到达并联的两个或两个以上近红外传感器,检测信号
通过上位机进行读取,完成融合光谱的采集,所述近红外传感器型号不同。
8.本发明的第二个方面,提供一种近红外传感器融合的药物结晶过程质量非线性表征方法,其特征在于,所述方法包括:基于近红外传感器融合方法的多光谱采集平台的搭建及光谱的采集,对近红外光谱进行处理并构建卷积神经网络(convolutional neural networks,cnn)非线性融合模型。
9.本发明的第三个方面,构建了莱鲍迪苷a(rebaudioside a,ra)结晶过程中上清液含量表征的方法,通过利用两个可检测波长范围不同的近红外传感器融合采集光谱以及原始光谱融合数据的卷积神经网络建立非线性莱鲍迪苷a含量模型。
10.本发明具有以下优点和积极效果:
11.(1)本发明通过近红外传感器融合,利用融合光谱测量平台,可以采集融合光谱,可以有效解决波长范围的限制,降低nir过程分析的成本,具有显著的社会、经济效益。
12.(2)本发明通过对于融合光谱的处理,建立基于cnn的非线性表征技术,可以准确的预测结晶过程药物的质量变化。
13.(3)本技术发明基于近红外光谱技术实现对ra结晶过程中上清液ra含量的快速表征,基于cnn的非线性融合模型可以有效的提升模型的预测能力,实现ra结晶过程中关键质量的快速分析,从而为其质量控制奠定基础。
14.(4)本发明方法测量准确、快速,并且对样品不产生损害,无污染,缩短监测时间,节省人力财力物力;对于实现产品质量的在线监测与质量管控具有重要意义,因此具有良好的实际应用之价值。
附图说明
15.构成本发明的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。
16.图1为多光谱采集平台;
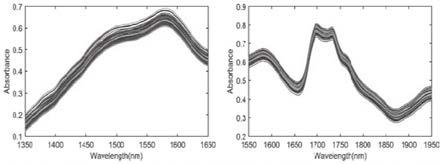
17.图2为两个微型传感器采集到的光谱(左传感器1,右传感器2);
18.图3为异常样品的剔除;
19.图4为样品集的划分;
20.图5为设计的cnn模型网络结构;
21.图6为cnn模型迭代训练过程损失函数的变化;
22.图7为原始光谱串联融合cnn模型建模结果;
23.图8为外积融合cnn模型不同卷积核大小的建模结果;
24.图9pca融合cnn模型建模结果。
具体实施方式
25.应该指出,以下详细说明都是例示性的,旨在对本发明提供进一步的说明。除非另有指明,本文使用的所有技术和科学术语具有与本发明所属技术领域的普通技术人员通常理解的相同含义。
26.需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本发明的示例性实施方式。如在这里所使用的,除非上下文另外明确指出,否则单数形式
也意图包括复数形式,此外,还应当理解的是,当在本说明书中使用术语“包含”和/或“包括”时,其指明存在特征、步骤、操作、器件、组件和/或它们的组合。应理解,本发明的保护范围不局限于下述特定的具体实施方案;还应当理解,本发明实施例中使用的术语是为了描述特定的具体实施方案,而不是为了限制本发明的保护范围。
27.结合具体实例对本发明作进一步的说明,以下实例仅是为了解释本发明,并不对其内容进行限定。如果实施例中未注明的实验具体条件,通常按照常规条件,或按照试剂公司所推荐的条件;下述实施例中所用的试剂、耗材等,如无特殊说明,均可从商业途径得到。
28.如前所述,目前针对药物结晶纯化过程的表征方法虽然众多,但是普遍存在检测方法繁琐、检测速度较慢、检测成本高昂等问题。
29.有鉴于此,本发明的一个典型具体实施方式中,提供一种近红外传感器融合方法,所述方法包括,近红外光经过待测物质再通过光纤分路器分别到达并联的两个或两个以上近红外传感器,检测信号通过上位机进行读取,完成融合光谱的采集,所述近红外传感器型号不同;
30.本发明的一个典型具体实施方式中,所述近红外传感器为微型近红外光传感器,优选地,近红外传感器所述不同的近红外光传感器可检测波长范围不同;
31.本方法支持不同型号的nirone sensor并联,同时检测待测物质,其优点为可以随意组合不同型号nirone sensor,不同型号的传感器覆盖不同的波长,蕴含不同的光谱特征信息,基于本专利搭建的光谱检测系统,可以根据目标物质的特征波长选择不同的传感器组合,通过对不同波段微型传感器的融合改善模型性能,可以代替台式光谱仪全波长的检测,省时省力,降低光谱采集成本,提高经济效益。
32.本发明的一个典型具体实施方式中,优选地,近红外光谱采集模式为透射模式。
33.本发明的一个典型具体实施方式中,优选地,所述方法中采用温控附件控温,温度的影响对于液体样品的nir光谱影响比较大,采用的温控附件将温度控制在
±
0.01℃,从而进一步提升光谱的准确性。
34.本发明的一个典型具体实施方式中,提供一种近红外传感器融合的药物结晶过程质量非线性表征方法,所述方法包括:基于近红外传感器融合方法的多光谱采集平台的搭建及光谱的采集,对近红外光谱进行处理并构建卷积神经网络非线性融合模型,其中多光谱采集平台的搭建包括近红外传感器融合。
35.本发明的一个典型具体实施方式中,提供一种莱鲍迪苷a结晶过程中上清液中药物含量的快速表征方法,其特征在于,通过利用两个可检测波长范围不同的近红外传感器融合采集光谱以及原始光谱融合数据的卷积神经网络建立非线性莱鲍迪苷a含量模型;
36.基于cnn的非线性融合模型可以有效的提升模型的预测能力,实现ra结晶过程中关键质量的快速分析,从而为其质量控制奠定基础。
37.本发明的一个典型具体实施方式中,提供一种莱鲍迪苷a结晶过程中上清液中药物含量的快速表征方法的具体步骤,包括:
38.(1)基于近红外传感器融合方法的多光谱采集平台的搭建:搭建基于透射模式的多光谱采集平台。光源通过光纤进入具有准直功能的温控样品池,比色皿中放入待测物质后,近红外光经过待测物质再通过光纤分路器分别到达近红外光谱仪传感器1和传感器2,检测信号通过上位机进行读取,从而完成光谱的采集;
39.(2)样品准备:在实验室模拟药物结晶纯化过程,根据结晶过程含量变化趋势间隔时间取样,得到结晶过程样品;
40.(3)光谱采集:将样品装于内径为1mm的比色皿中,利用温控附件将温度控温。设置采集参数后采集光谱数据;
41.(4)异常光谱并集剔除与样本集划分:利用pca对原始光谱进行分析,通过样本集的聚散程度筛选异常点的存在。为了保证单传感器和两传感器融合模型所用样本的一致性,剔除两传感器光谱异常样本的并集,对剩余样本进行样本集划分和模型建立与验证;
42.(5)cnn网络结构设计:设置cnn网络结构,进行模型训练;
43.(6)原始光谱融合cnn模型建立:模型配置好后将光谱数据与一级数据导入神经网络进行训练。优化卷积核大小、卷积核个数及全连接神经元个数,建立原始光谱融合cnn模型;
44.(7)外积融合cnn模型建立:同理,优化卷积核大小、卷积核个数及全连接神经元个数,建立外积融合cnn模型;
45.(8)主成分融合cnn模型建立:对传感器1和传感器2分别进行主成分分析,确定融合的主成分数,建立主成分融合cnn模型;
46.(9)模型比较确定最佳融合模型:以rmsep、r
p2
、rpd为模型评价参数,好的模型应该具有较低的rmsep、较高的r
p2
和rpd值。
47.实施例基于近红外光谱数据融合的ra结晶过程质量非线性表征
48.(1)基于近红外传感器融合方法的多光谱采集平台的搭建:基于本专利搭建的透射模式的多光谱采集平台,本实例中选择的传感器的波长范围为:1350nm
‑
1650nm和1550nm
‑
1950nm,此两个波段不仅包含ra的光谱特征信息,同时包含了水分子的光谱特征信息,两种信息交汇,更易提升模型的预测能力。
49.(2)样品准备:在实验室模拟甜菊糖ra80的结晶纯化过程,根据结晶过程含量变化趋势间隔时间取样,用0.22μm的微孔滤膜过滤,备用。共模拟5批结晶过程,得到119个样品。
50.(3)光谱采集:将样品装于内径为1mm的比色皿中,利用温控附件将温度控制在30℃。采用微型传感器1和2结合光谱采集软件nirone_v1.6.2进行光谱采集,采集方式为透射。采用默认采集参数:波长平均100,扫描平均为1,分辨率为1nm,扫描间隔为5s。以空气为背景,每批次采集一次背景。采集过程中每个样品采集3次光谱,取其平均光谱为最终的原始光谱,光谱采集共分两天完成。光谱采集结果如图2所示。
51.(4)异常光谱并集剔除与样本集划分:利用pca对原始光谱进行分析,通过样本集的聚散程度筛选异常点的存在。传感器1和传感器2采集的样品光谱的pca得分散点图如图3所示,从图中可以看出对于传感器1光谱,样本1、2、10、40、94位于95%置信限外,对于传感器2光谱,样本11、12、13、22、40、94、116位于95%置信限外。为了保证单传感器和两传感器融合模型所用样本的一致性,剔除两传感器光谱异常样本的并集,以最终剩余的109个样本划分校正集验证集(80:29)进行模型建立与验证。
52.(5)cnn网络结构设计:设置cnn网络结构,选定leakyrelu激活函数和adam优化器。网络结构示意图和迭代训练的结果如图5所示,在设置的优化器和失活率下,随着迭代的进行,损失函数稳定下降,且在迭代500次后即基本平稳,为节省建模时间,提高工作效率,设置迭代次数为500。
53.(6)原始光谱融合cnn模型建立:模型配置好后将光谱数据与一级数据导入神经网络进行训练。经多次实验确定卷积核个数128,全连接神经元个数64,再对卷积核大小进行优化,确定卷积核大小为15,建立原始光谱融合cnn模型。模型的rmsec、rmsep、r
c2
、r
p2
、rpd分别为2.520、2.895、0.958、0.935、3.919。
54.表1为原始光谱串联融合cnn模型不同卷积核大小的建模结果;
[0055][0056]
(7)外积融合cnn模型建立:同理,在卷积核个数128,全连接神经元个数64基础上对卷积核大小进行优化,确定卷积核大小为30,建立外积融合cnn模型。模型的rmsec、rmsep、r
c2
、r
p2
、rpd分别为3.858、3.382、0.902、0.911、3.355。
[0057]
表2为外积融合cnn模型不同卷积核大小的建模结果;
[0058][0059]
(8)主成分融合cnn模型建立:对传感器1和传感器2分别进行主成分分析,经多次实验确定各提取前5个主成分进行融合(解释变量分别为99.88%和99.67%)。同理,在卷积核个数128,全连接神经元个数64基础上对卷积核大小进行优化,确定卷积核大小为5,建立主成分融合cnn模型。模型的rmsec、rmsep、r
c2
、r
p2
、rpd分别为3.187、3.029、0.933、0.929、3.745。
[0060]
表3为pca融合(5+5)cnn模型参数寻优;
[0061][0062]
(9)模型比较确定最佳融合模型:以rmsep、r
p2
、rpd为模型评价参数,好的模型应该具有较低的rmsep、较高的r
p2
和rpd值。原始光谱融合cnn模型rmsep最低,r
p2
和rpd值最高,rpd值达3.919,能够实现对ra结晶过程的准确表征。
[0063]
综上,本发明中通过对ra结晶过程进行近红外光谱采集,并对两传感器数据进行异常样本的并集剔除,运用cnn特征提取结合数据融合验证了近红外传感器融合实现药物结晶过程质量非线性表征的准确性。通过对各融合模型建模结果的比较,确定原始光谱融合所建的cnn模型是实现ra结晶过程非线性表征的最佳方法。
[0064]
最后应该说明的是,以上所述仅为本发明的优选实施例而已,并不用于限制本发明,尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述实施例所记载的技术方案进行修改,或者对其中部分进行等同替换。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。上述虽然结合附图对本发明的具体实施方式进行了描述,但并非对本发明保护范围的限制,所属领域技术人员应该明白,在本发明的技术方案的基础上,本领域技术人员不需要付出创造性劳动即可做出的各种修改或变形仍在本发明的保护范围以内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1