一种生物标志物CRP的Simoa试剂盒及其使用方法
一种生物标志物crp的simoa试剂盒及其使用方法
技术领域
1.本发明涉及免疫检测技术领域,特别是指一种生物标志物crp的simoa试剂盒及其使用方法。
背景技术:
2.急性期反应蛋白(c
‑
reactive protein,crp)是在肝脏由白介素6(il
‑
6)诱导合成的,生理状态下crp含量甚微,但在肿瘤形成和浸润过程中,il
‑
6表达活跃,大量分泌,在il
‑
6这种炎症因子的刺激下,会诱导合成大量的crp,正常血清中crp含量为0
‑
5μg/ml,肺癌患者的crp血清水平远高于健康人,随着化疗或者其他治疗后病情改善,crp水平又会快速下降,因此可以作为一种有效的生物标志物进行临床诊断和指导治疗。
3.目前临床上使用的crp检测方法主要是免疫扩散、乳胶凝集法和免疫比浊法以及免疫层析,免疫扩散、乳胶凝集及免疫比浊法和免疫层析只能定性,不能定量,只能作为诊断的辅助手段。酶联免疫法灵敏度低,重复性差,定量准确性差,操作时间长,自动化程度低。
4.单分子阵列(single molecule array,simoa)技术又称为数字elisa,是基于磁珠的蛋白质超灵敏检测方法。在传统双抗体夹心elisa中,酶
‑
底物反应的荧光产物扩散至约50
‑
100μl的大体积,需要依赖数百万酶标记的免疫复合物在背景之上产生可测量的荧光信号。在数字elisa中,酶
‑
底物反应的荧光产物被限制在46飞升(fl)大小的微孔中,其被称为单分子阵列(simoa)。使用该方法,可以检测单个酶分子的存在。在simoa免疫测定中,将抗体包被的捕获珠过量加入含有低浓度靶蛋白分子的样品中。基于泊松分布原理,一个或零个目标蛋白质分子将与每个磁珠结合。结合多于一个蛋白质分子的磁珠可以忽略不计。然后将磁珠与生物素化的检测抗体和链霉亲和素
‑
β
‑
半乳糖苷酶一起孵育,形成酶标记的免疫复合物。接着,将磁珠载入到46fl的微孔阵列上,其中每个孔仅能够容纳一个磁珠。用荧光底物填充微孔并用全氟油密封。含有单一免疫复合物的珠子将导致许多底物分子经酶催化产生大量荧光产物。由于荧光产物被限制在约46fl的极小体积,结合荧光显微成像技术即可实现单个微孔的荧光成像,从而实现单个蛋白分子的检测。以这种方式,simoa可以使用数字读数模式定量蛋白质浓度,并实现超过4个数量级的检测范围。
5.因此,基于simoa技术开发一种高灵敏度、自动化程度高、快速、准确性好且适合推广的crp检测方法,对快速检测生物标志物crp具有重大的意义。
技术实现要素:
6.一种生物标志物crp的simoa试剂盒,所述simoa试剂盒包括捕获抗体包被的磁珠、crp标准品、生物素化的检测抗体、sbg溶液、荧光底物溶液和样本稀释液。
7.本发明的技术方案是这样实现的:
8.所述捕获抗体包被的磁珠的制备方法为:
9.(1)将捕获抗体通过超滤管进行换液处理;
10.(2)将2.7μm磁珠用edc进行活化;
11.(3)于4℃条件下,将步骤(1)处理的捕获抗体与步骤(2)活化的磁珠混合孵育2
‑
3h;
12.(4)经步骤(3)孵育的产物用pbst溶液洗两次后,用封闭液于37℃封闭,最后用磁珠稀释液洗两次,即获得捕获抗体包被的磁珠,于磁珠稀释液中储存。
13.所述步骤(1)中捕获抗体为单克隆抗体l30601;超滤使用的缓冲液是为50
‑
60mmol/ml吗啉乙磺酸缓冲液,ph=6.2
‑
6.4。
14.所述步骤(3)中捕获抗体的反应浓度为0.1
‑
0.2mg/ml;活化的磁珠的反应浓度为0.5
‑
2.1
×
109/ml。
15.所述步骤(4)中pbst溶液为10
‑
12mmol/l pbs+1
‑
1.5%tween 20,ph=7.4
‑
7.9;封闭液为10
‑
16mmol/l pbs+1
‑
1.2%bsa,ph=7.4
‑
8.2;磁珠稀释液为50
‑
60mmol/l tris
‑
hcl+10
‑
13mmol/l edta+0.1
‑
0.3%tween20+1
‑
1.9%bsa,ph=7.4
‑
9.0。
16.所述生物素化的检测抗体的制备方法为:将检测抗体用pbs溶液通过超滤管进行换液处理,于室温下加入nhs
‑
biotin或其衍生物,反应30
‑
45min,超滤纯化后获得生物素化的检测抗体,其中检测抗体为单克隆抗体l30602。
17.所述检测抗体与nhs
‑
biotin或其衍生物的反应物质的量比为1:30
‑
1:50,pbs溶液为10
‑
30mmol/l磷酸盐缓冲液,ph=7.4
‑
9.0。
18.所述sbg溶液浓度为50
‑
400pmol/l,sbg缓冲液为10
‑
13mmol/l pbs+0.5%bsa+1
‑
2mmol/l mgcl2,ph=7.4
‑
8;荧光底物为试卤灵
‑
β
‑
半乳糖苷,荧光底物溶液的浓度为100
‑
120μmol/l。
19.所述生物标志物crp的simoa试剂盒在制备诊断试剂中的使用方法。
20.所述生物标志物crp的simoa试剂盒在检测人体液中crp含量中的使用方法。
21.本发明具有以下有益效果:
22.本发明提供的基于simoa单分子阵列技术平台和双抗体夹心法以检测人体液中crp含量的simoa试剂盒,以单克隆抗体l30601为捕获抗体,以单克隆抗体l30602为检测抗体,可以定量的检测人体液中crp含量;
23.提供了完整的上机检测试剂,仅需处理样本或者仪器自动稀释,操作简便,降低人工误差,重复性高,提高临床诊断的准确度;
24.一次上机检测可同时最多288个样本同时并行检测,检测时间相比同类产品缩短两倍,相当于每2min就检测一个样本。节约大量时间;
25.最低检测限为0.06pg/ml,能够精准检测低水平crp含量;
26.需要样品量低,1μl样品就可以进行检测;
27.检测范围为0.1
‑
1000pg/ml,检测范围比较宽,应用范围广;
28.由附图1可知本技术的最低检测限可达0.06pg/ml。
附图说明
29.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以
根据这些附图获得其他的附图。
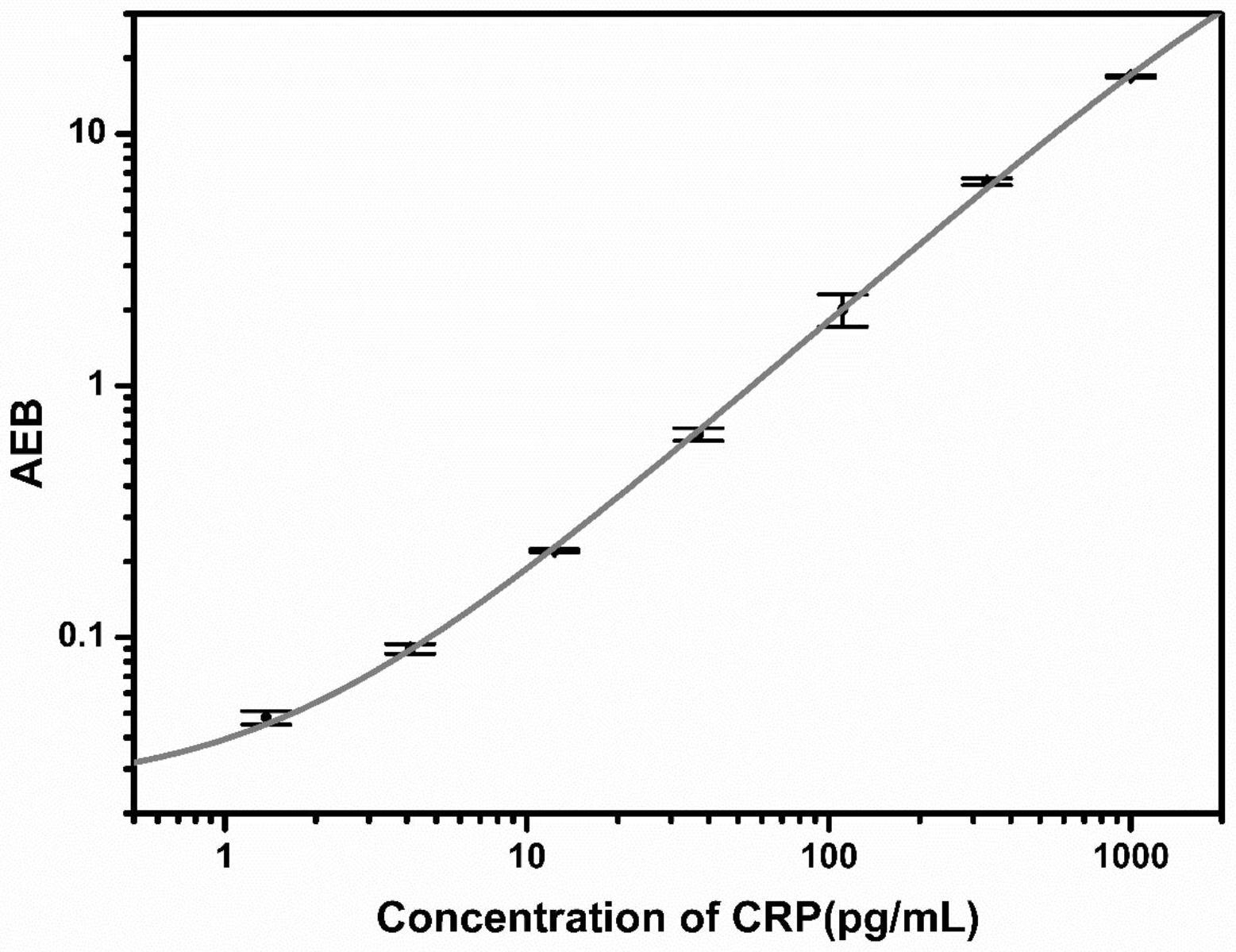
30.图1为本发明crp simoa试剂盒标准曲线图。
具体实施方式
31.下面将结合本发明实施例,对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有付出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
32.实施例
33.本发明提供的用于检测人体液中crp含量的simoa试剂盒,包含捕获抗体包被的2.7μm磁珠、crp标准品、生物素化的检测抗体、sbg溶液、荧光底物溶液和样本稀释液,以及试验方法电子文件。
34.在本发明中,磁珠、捕获抗体、标准品、检测抗体、生物素化试剂、sbg和荧光底物的原始材料通过购买获得;其中捕获抗体为单克隆抗体l30601,检测抗体为单克隆抗体l30602。
35.在本发明的捕获抗体包被磁珠制备过程为:首先,储存的抗体通过超滤管进行换液处理,所使用的缓冲液是mes,为50
‑
60mmol/ml吗啉乙磺酸缓冲液,ph=6.2
‑
6.4。
36.然后,磁珠用edc进行活化,4℃环境下,捕获抗体和活化的磁珠孵育2h。接着,用pbst洗两次,再用封闭液37℃封闭,最后用磁珠稀释液洗两次,储存在磁珠稀释液中,即获得捕获抗体包被的磁珠。其中捕获抗体的反应浓度为0.1
‑
0.2mg/ml;活化的磁珠的反应浓度为0.5
‑
2.1
×
109/ml。
37.所述pbst配方:10
‑
12mmol/l pbs+1
‑
1.5%tween 20,ph=7.4
‑
7.9;封闭液配方:10
‑
16mmol/l pbs+1
‑
1.2%bsa,ph=7.4
‑
8.2。磁珠稀释液为50
‑
60mmol/l tris
‑
hcl+10
‑
13mmol/ledta+0.1
‑
0.3%tween20+1
‑
1.9%bsa,ph=7.4
‑
9.0。
38.在本发明的生物素化检测抗体制备过程为:首先,原始储存的检测抗体用pbs通过超滤管进行换液处理。然后,室温下加入nhs
‑
biotin或其衍生物,反应30min。最后,生物素化后的检测抗体用超滤管进行纯化,即获得生物素化的检测抗体。pbs配方:10
‑
30mmol/l磷酸盐缓冲液(pbs),ph=7.4
‑
9.0。其中检测抗体与nhs
‑
biotin或其衍生物的反应物质的量比为1:30
‑
1:50。
39.酶和底物溶液的配制:所述sbg溶液浓度为50
‑
400pmol/l,sbg缓冲液为:10
‑
13mmol/lpbs+0.5%bsa+1
‑
2mmol/l mgcl2,ph=7.4
‑
8.0;
40.上述最终浓度均是工作浓度,用于最终的成像。
41.所述底物为:试卤灵
‑
β
‑
半乳糖苷(rgp)
42.标准品溶液的配制:100ng/ml crp标准品通过样本稀释液被配制成1ml。其余标准品可以根据需要自行配制。
43.crp simoa试剂盒的使用方法:
44.首先,将试验方法电子文档导入quanterix生产的hd
‑
1/hd
‑
x simoa分析仪上,该试验方法电子文档包含了试验运行的方式。该试验方法电子文档上的方法,可以根据需求进行更改,以适合试剂盒的试剂用途。
45.此试验方法电子文档包括:磁珠、样本及检测抗体的反应时间(35min),磁珠用量(25μl),检测抗体的用量(20μl),标准品和样品的用量(100μl),sbg的用量(100μl)及反应时间(5min)。本发明默认反应时间设置为(35min
‑
5min),默认方法是simoa 2.0两步法。标准品浓度可以被自定义设置,默认设置为(1000,333,111,37.0,12.3,4.12,1.37,0pg/ml)。
46.然后,浓度为2
×
107/ml的磁珠,浓度为1
‑
2μg/ml的检测抗体,浓度为50
‑
400pmol/l的sbg,浓度为100
‑
120μmol/l的荧光底物rgp和加有标准品和样本的96孔板装载到分析仪指定位置,同时扫描标签和设置位置参数。
47.最后,运行试验。待实验验结束,导出试验结果,仪器自动拟合曲线和计算样本结果,见图1。
48.拟合方程为:四参数logistic曲线拟合方程:y=(a
‑
d)/[1+(x/c)
^
b]+d。
[0049]
本技术的simoa试剂盒在检测人体液中crp含量中的使用方法也属于本发明的保护范围。
[0050]
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1