一种新型冠状病毒高亲和力中和抗体检测试剂盒及其制备方法与应用与流程
1.本发明涉及一种新型冠状病毒(sars
‑
cov
‑
2)中和抗体的检测,尤其涉及一种新型冠状病毒高亲和力中和抗体检测试剂盒及其制备方法与应用,属于临床检验技术领域。
背景技术:
2.接种新冠病毒疫苗是防控疫情最经济、最有效的手段,也是全球各国预防控制新冠肺炎感染和传播采取的最主要的措施之一。我国自2020年12月15日启动大规模人群接种工作,灭活疫苗、腺病毒载体疫苗、重组亚单位疫苗等不同技术路线疫苗先后在国内紧急使用或附条件批准上市,截至2021年7月28日,31个省(自治区、直辖市)和新疆生产建设兵团累计报告接种新冠病毒疫苗160124.9万剂次。为全面维护人民群众生命健康安全发挥了重要作用。
3.中和抗体是由病毒入侵机体后产生的一类能与病毒结合并使之丧失感染力的抗体,是具有保护作用的抗体,与传统的临床上检测的igm、igg、iga抗体在功能上有着较大的不同,是疫苗研发和临床评价过程中重要的指标之一,中和抗体检测的实验室金标准是感染抑制试验,主要包括蚀斑减少中和试验和微量中和试验。这两种方法均使用定量的活病毒与不同稀释度的等量血清混合后,接种预先准备好的单层细胞,通过不同的指标评价细胞的病变程度评价中和抗体效价。采用体外培养的活病毒进行的中和试验反映的是人体血液样本中能够阻断病毒感染的总中和抗体的效价。这两种实验均需使用活的新冠病毒需要在生物安全三级实验室内完成,但该类方法操作技术难度大,耗时较长,生物安全的要求高,不适合普通接种疫苗人群高通量筛查。
4.中国医科院病原微生物研究所在nature communication上发表研究论文,利用假病毒系统证明了sars
‑
cov
‑2‑
s蛋白在病毒入侵细胞时表现出的特征,并对其与sars
‑
cov产生的免疫交叉反应进行了阐述。该研究使用慢病毒sars
‑
cov
‑2‑
s假病毒系统,确定了huh7、vero81、llcmk2、calu3等细胞对于该系统易感,文中还详细论述了病毒与受体ace2结合进入细胞的途径。新型冠状病毒s蛋白是病毒毒力的关键因子,识别新冠病毒的s(刺突)蛋白上的rbd区(受体结合域)的中和抗体,就可以阻断新冠病毒和人细胞上的ace2受体结合,使得新冠病毒无法感染人细胞,是决定病毒毒力、组织嗜性和宿主范围的关键部分,也是中和抗体和疫苗设计的主要靶标。
5.通常伴随着疫苗的研究和上市,国内外研究机构和生产企业致力于采用体外诊断试剂进行中和抗体检测的研究,用于评价疫苗的有效性,主要通过建立的体外诊断试剂与体外培养活病毒的中和试验进行对比研究,从而建立一个有效的cut
‑
off值,确立体外诊断试剂检测中和抗体的性能,并通过确定适合的判断界值,建立与病毒保护力之间的相关性,确定最低保护水平。例如已经较为成熟的流感疫苗、ev71疫苗、狂犬病疫苗、脊髓灰质炎疫苗等,均已建立了who认可的标准化的中和抗体试验,有相应的who标准品和推荐使用的标准毒株,并设定了明确的判断界值。针对新冠病毒疫苗,最直接的检测方法为新冠中和抗体
的检测,一般是基于单抗原表位或多抗原表位采用竞争抑制原理的酶联免疫法进行中和抗体检测,但是检测速度较慢。
6.有鉴于此,急需提供一种新型冠状病毒高亲和力中和抗体检测试剂盒及其制备方法。
技术实现要素:
7.针对现有技术不足,本发明提供了一种新型冠状病毒高亲和力中和抗体检测试剂盒及其制备方法与应用。
8.术语说明:
9.bsa:牛血清白蛋白。
10.本发明的技术方案如下:
11.一种新型冠状病毒高亲和力中和抗体检测试剂盒,包括高敏结合蛋白、重组rbd蛋白酶结合物和样品稀释液;
12.所述高敏结合蛋白制备方法为利用灭活的新型冠状病毒感染者血清经过装有重组rbd中和抗体偶联的琼脂糖微球层析柱过滤,高敏结合蛋白会结合到琼脂糖微球上,经过洗杂、洗脱得到纯化的高敏结合蛋白;
13.所述重组rbd蛋白酶结合物是辣根过氧化物酶标记的重组rbd蛋白;该酶标rbd酶结合物工作效价为1:9000;所述重组rbd蛋白是利用cho细胞表达的新型冠状病毒sars
‑
cov
‑
2rbd三聚体的重组蛋白;
14.所述样品稀释液的配方是:除菌的1000ml纯水中,含nacl 8g、nah2po4·
2h2o 0.2g、na2hpo4·
12h2o 2.9g、ctab 1g、bsa 5g、tritonx
‑
100 0.1ml、proclin300 1ml,ph 7.4。
15.根据本发明优选的,所述新型冠状病毒高亲和力中和抗体检测试剂盒还包括:微孔板、作为阳性对照的rbd中和抗体标准品溶液、作为阴性对照的正常人新冠病毒sars
‑
cov
‑
2抗体阴性血清、酶结合物稀释液、20
×
浓缩洗涤液、显示液a、显示液b和终止液。
16.进一步优选的,所述微孔板为96或48孔的聚苯乙烯微孔板,且其各孔包被有浓度为5
‑
10μg/ml的高敏结合蛋白。
17.进一步优选的,所述rbd中和抗体标准品溶液为:样品稀释液稀释的浓度为1μg/ml的rbd中和抗体溶液;所述的rbd中和抗体是用来自于测定的新冠康复患者中和抗体可变区序列并与人源化fc融合,通过cho细胞重组表达形成得到。
18.进一步优选的,所述酶结合物稀释液的配方是:除菌的1000ml纯水中,含nacl 8g、nah2po4·
2h2o 0.2g、na2hpo4·
12h2o 2.9g、bsa 5g、proclin300 1ml。
19.进一步优选的,所述20
×
浓缩洗涤液的配方是:除菌的50ml双蒸水中,含nacl 8.0g、nah2po4·
2h2o 0.2g、na2hpo4·
12h
2 o 2.9g、吐温20 0.5ml;
20.进一步优选的,所述显示液a是浓度为0.3mg/ml的四甲基联苯胺(tmb)溶液;所述显示液b是浓度为0.74mg/ml的过氧化脲溶液;使用时将显示液a与显示液b按体积比1﹕1混合;
21.进一步优选的,所述终止液是浓度为2mol/l的硫酸溶液。
22.本发明中的新型冠状病毒高亲和力中和抗体检测试剂盒还包括盒体、封板膜、密
封袋和说明书。
23.一种上述新型冠状病毒高亲和力中和抗体检测试剂盒的制备方法,包括如下步骤:
24.1)酶标板的制备:
25.1.1)配制包被液:即配制碳酸盐缓冲溶液,并调整ph值为9.6,包被液的配方是:
26.na2co31.59gnahco32.94g纯化水定容至1000ml
27.配制完成后过滤除菌,4℃保存;
28.1.2)配制洗涤液,洗涤液的配方是:
29.nacl8.0gnah2po4·
2h2o0.2gna2hpo4·
12h2o2.9g吐温200.5ml纯化水定容至1000ml
30.配制完成后过滤除菌,4℃保存;
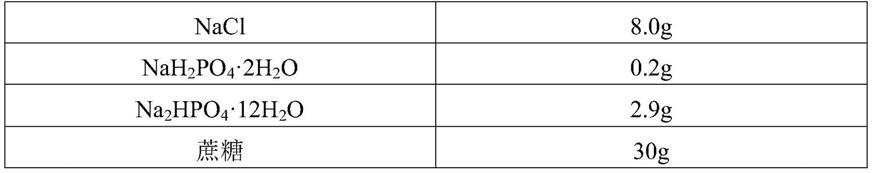
31.1.3)配制封闭液,封闭液的配方是:
[0032][0033][0034]
配制完成后过滤除菌,4℃保存;
[0035]
1.4)用包被液将高敏结合蛋白稀释至工作浓度5
‑
10μg/ml,混匀,并静置15分钟;
[0036]
1.5)取标记好的微孔板,用8孔道排枪点板,使高敏结合蛋白液达到150μl/孔,盖上盖板膜;
[0037]
1.6)置于2℃
‑
8℃冰箱,包被4
‑
6小时,然后,每孔加入5μl 0.1%sds水溶液,过夜包被12
‑
16小时;
[0038]
1.7)取出过夜包被的微孔板,室温平衡30min,甩掉高敏结合蛋白液,吸水纸拍干,每孔每次加300μl洗涤液,洗涤2次,吸水纸拍干;
[0039]
1.8)每孔加入250μl封闭液,2℃
‑
8℃过夜封闭16小时;
[0040]
1.9)取出过夜封闭的微孔板,室温平衡30min,甩掉封闭液,吸水纸拍干;放在硅胶干燥器中干燥,在室温条件下,湿度30%以下保持5小时;
[0041]
1.10)以铝箔袋真空包装包被板,做好标记,2
‑
8℃保存,备用。
[0042]
2)试剂盒溶液的配制:
[0043]
2.1)酶结合物稀释液的配制,酶结合物稀释液的配方是:
[0044]
nacl8.0gnah2po4·
2h2o0.2gna2hpo4·
12h2o2.9gbsa5gproclin3001ml纯化水定容至1000ml
[0045]
配制完成后过滤除菌,4℃保存;
[0046]
2.2)20
×
浓缩洗涤液的配制,20
×
浓缩洗涤液的配方是:
[0047]
nacl8.0gnah2po4·
2h2o0.2gna2hpo4·
12h2o2.9g吐温200.5ml双蒸水定容至50ml
[0048]
配制完成后过滤除菌,4℃保存;
[0049]
2.3)样品稀释液的配制,样品稀释液的配方是:
[0050][0051][0052]
配制完成后过滤除菌,4℃保存;
[0053]
2.4)显示液a、显示液b的配制是以二甲基亚砜(dmso)为溶剂配制浓度为0.3mg/ml的四甲基联苯胺(tmb)溶液,命名为a液,以ph5.5、0.2mol/l磷酸氢二钠与0.1mol/l柠檬酸缓冲液为溶剂配制浓度为0.74mg/ml的过氧化脲溶液,命名为b液,使用时将a液与b液按体积比1﹕1混合;
[0054]
2.5)终止液是浓度为2mol/l的硫酸溶液。
[0055]
上述新型冠状病毒高亲和中和抗体检测试剂盒在检测新型冠状病毒中和抗体中的应用。
[0056]
上述新型冠状病毒高亲和中和抗体检测试剂盒的使用方法,包括步骤如下:
[0057]
(1)于微孔板内每孔先加入25ul样品稀释液,再将待测样品、阳性对照和阴性对照各取25ul分别加入到微孔板含有样品稀释液的孔中,37℃温浴30分钟;
[0058]
(2)反应结束后,用洗涤液洗板5次,每次应浸泡20~40s,每孔加液量不少于350μl,洗涤完之后拍干;
[0059]
(3)每孔再加入100ul重组rbd蛋白酶结合物,混匀后用不干胶封片封盖反应板,37℃温浴20分钟;
[0060]
(4)反应结束后,用洗涤液洗板5次,每次应浸泡20~40s,每孔加液量不少于350μl,洗涤完之后拍干;
[0061]
(5)先加入显色液a 50μl,再加入显色液b 50μl,37℃避光温浴10分钟;
[0062]
(6)加入终止液50μl,终止反应,用酶标仪检测各孔在450nm和630nm双波长的吸光值;
[0063]
(7)根据cut off判断结果;od值≥0.130:阳性,od值<0.130:阴性。
[0064]
本发明所述新型冠状病毒高亲和中和抗体检测试剂盒的应用及该指标在接种新冠疫苗人群和新冠感染后康复人群的中和抗体评价中的应用。
[0065]
本发明提供的新型冠状病毒高亲和中和抗体检测试剂盒具有高通量、灵敏度高、特异性好、重复性好等特点,可在生物安全二级实验室或普通实验室开展的快速中和抗体检测方法,有利于疫病流行病学调查、免疫抗体监测以及疫苗免疫效力评价。
[0066]
本发明所述新型冠状病毒高亲和中和抗体检测试剂盒的检测原理为:用高敏结合蛋白包被聚苯乙烯微孔板,加入样本稀释液、样本,样本中的中和抗体与高敏结合蛋白结合形成复合物,经过洗涤,与辣根过氧化物酶标记rbd蛋白(hrp
‑
rbd)制备酶结合物,如果样本中含有新型冠状病毒中和抗体,则形成“高敏结合蛋白
‑
中和抗体
‑
rbd”复合物,如果样本中不含有新型冠状病毒中和抗体,则不显色,最后加入酶底物显色,在酶标仪上,于450nm,630nm处读取od值。od值与样本中rbd中和抗体的效价成正比。
[0067]
本发明的有益效果是:
[0068]
1、现有技术中酶联免疫试剂盒多采用rbd蛋白作为结合蛋白,辣根过氧化物酶ace2作为酶结合物无法与中和抗体结合,通过辣根过氧化物酶ace2与中和抗体进行竞争,来达到检测中和抗体的目的,但是其操作复杂,操作时长,结果易受加样时间影响。本发明采用从新型冠状病毒感染人群的血清提取的高敏结合蛋白与rbd中和抗体具有极高的亲和力,将高敏结合蛋白作为捕捉蛋白,高敏结合蛋白来源于新型冠状病毒在人体内组装的,能够与新冠中和抗体结合的蛋白质,是新型冠状病毒s1蛋白、ntd蛋白和其他人体内的结合蛋白的混合物,利用重组rbd三聚体蛋白标记的hrp作为检测蛋白如果样本中含有新型冠状病毒中和抗体,则形成“高敏结合蛋白
‑
中和抗体
‑
rbd”复合物,如果样本中不含有新型冠状病毒中和抗体,则不显色,最后加入酶底物显色,并通过检测od值确定样本是否含有新型冠状病毒中和抗体。以结合的方式检测中和蛋白,相较于竞争方式检测中和蛋白,操作时间更短,检测速度更快,不易受加样时间影响,结果更加准确。
[0069]
2、本发明中的高敏结合蛋白与rbd三聚体蛋白均具有天然蛋白结构,可以最真实、最有效实现新冠中和抗体免疫反应,利用夹心法原理,具有稳定性高、灵敏度高、选择性强的优点。
附图说明
[0070]
图1为本发明所述新型冠状病毒高亲和中和抗体检测试剂盒线性分析曲线。
[0071]
图中:横坐标为中和抗体浓度(μg/ml),纵坐标为od值
具体实施方式
[0072]
下面结合具体附图和实施例对本发明内容进行详细说明。如下所述例子仅是本发明的较佳实施方式而已,应该说明的是,下述说明仅仅是为了解释本发明,并非对本发明作任何形式上的限制,凡是依据本发明的技术实质对实施方式所做的任何简单修改,等同变化与修饰,均属于本发明技术方案的范围内。
[0073]
下述实施例中,所使用的材料、试剂等,如无特殊说明,均从商业途径得到。
[0074]
实施例1
[0075]
一种新型冠状病毒高亲和力中和抗体检测试剂盒,包括:盒体,设在盒体内的微孔板、作为阳性对照的rbd中和抗体标准品溶液、作为阴性对照的正常人新冠病毒sars
‑
cov
‑
2抗体阴性血清、酶结合物稀释液、样品稀释液、重组rbd蛋白酶结合物、高敏结合蛋白、20
×
浓缩洗涤液、显示液a、显示液b、终止液及封板膜、密封袋和说明书;
[0076]
其中,
[0077]
所述微孔板为96或48孔的聚苯乙烯微孔板,且其各孔包被有浓度为5μg/ml的高敏结合蛋白;
[0078]
所述高敏结合蛋白制备方法为利用灭活的新型冠状病毒感染者血清经过装有重组rbd中和抗体偶联的琼脂糖微球层析柱过滤,高敏结合蛋白会结合到琼脂糖微球上,经过洗杂、洗脱得到纯化的高敏结合蛋白;
[0079]
所述重组rbd蛋白酶结合物是辣根过氧化物酶标记的重组rbd蛋白;该酶标rbd酶结合物工作效价为1:9000;所述rbd蛋白是利用cho细胞表达的新型冠状病毒sars
‑
cov
‑
2rbd三聚体的重组蛋白;
[0080]
所述rbd中和抗体标准品溶液为:样品稀释液稀释的浓度为1μg/ml的rbd中和抗体溶液;所述的rbd中和抗体是用来自于测定的新冠康复患者中和抗体可变区序列并与人源化fc融合,通过cho细胞重组表达形成得到;
[0081]
所述酶结合物稀释液的配方是:除菌的1000ml纯水中,含nacl 8g、nah2po4·
2h2o 0.2g、na2hpo4·
12h2o 2.9g、bsa 5g、proclin300 1ml;
[0082]
所述样品稀释液的配方是:除菌的1000ml纯水中,含nacl 8g、nah2po4·
2h2o 0.2g、na2hpo4·
12h2o 2.9g、ctab 1g、bsa 5g、tritonx
‑
100 0.1ml、proclin300 1ml,ph 7.4;
[0083]
所述20
×
浓缩洗涤液的配方是:除菌的50ml双蒸水中,含nacl 8.0g、nah2po4·
2h2o 0.2g、na2hpo4·
12h
2 o 2.9g、吐温20 0.5ml;
[0084]
所述显示液a是浓度为0.3mg/ml的四甲基联苯胺(tmb)溶液;所述显示液b是浓度为0.74mg/ml的过氧化脲溶液;使用时将显示液a与显示液b按体积比1﹕1混合;
[0085]
所述终止液是浓度为2mol/l的硫酸溶液。
[0086]
上述试剂盒每盒中包括高敏结合蛋白包被微孔板1块、重组rbd蛋白酶结合物的试剂、标准品1瓶、样品稀释液、酶结合物稀释液、显示液a、显示液b、终止液、洗涤液(20
×
浓缩)各一瓶,说明书一份,不干胶封片2张。
[0087]
实施例2
[0088]
实施例1中的试剂盒的制备方法,包括如下步骤:
[0089]
1)酶标板的制备:
[0090]
1.1)配制包被液:即配制碳酸盐缓冲溶液,并调整ph值为9.6,包被液的配方是:
[0091][0092][0093]
配制完成后过滤除菌,4℃保存;
[0094]
1.2)配制洗涤液,洗涤液的配方是:
[0095]
nacl8.0gnah2po4·
2h2o0.2gna2hpo4·
12h2o2.9g吐温200.5ml纯化水定容至1000ml
[0096]
配制完成后过滤除菌,4℃保存;
[0097]
1.3)配制封闭液,封闭液的配方是:
[0098]
nacl8.0gnah2po4·
2h2o0.2gna2hpo4·
12h2o2.9g蔗糖30gbsa10g酪蛋白钠盐10gctab1g纯化水定容至1000ml
[0099]
配制完成后过滤除菌,4℃保存;
[0100]
1.4)用包被液将高敏结合蛋白稀释至工作浓度5
‑
10μg/ml,混匀,并静置15分钟;
[0101]
1.5)取标记好的微孔板,用8孔道排枪点板,使高敏结合蛋白液达到150μl/孔,盖上盖板膜;
[0102]
1.6)置于2℃
‑
8℃冰箱,包被4
‑
6小时,然后,每孔加入5μl 0.1%sds水溶液,过夜包被12
‑
16小时;
[0103]
1.7)取出过夜包被的微孔板,室温平衡30min,甩掉高敏结合蛋白液,吸水纸拍干,每孔每次加300μl洗涤液,洗涤2次,吸水纸拍干;
[0104]
1.8)每孔加入250μl封闭液,2℃
‑
8℃过夜封闭16小时;
[0105]
1.9)取出过夜封闭的微孔板,室温平衡30min,甩掉封闭液,吸水纸拍干;放在硅胶干燥器中干燥,在室温条件下,湿度30%以下保持5小时;
[0106]
1.10)以铝箔袋真空包装包被板,做好标记,2
‑
8℃保存,备用。
[0107]
2)试剂盒溶液的配制:
[0108]
2.1)酶结合物稀释液的配制,酶结合物稀释液的配方是:
[0109]
[0110][0111]
配制完成后过滤除菌,4℃保存;
[0112]
2.2)20
×
浓缩洗涤液的配制,20
×
浓缩洗涤液的配方是:
[0113]
nacl8.0gnah2po4·
2h2o0.2gna2hpo4·
12h2o2.9g吐温200.5ml双蒸水定容至50ml
[0114]
配制完成后过滤除菌,4℃保存;
[0115]
2.3)样品稀释液的配制,样品稀释液的配方是:
[0116]
nacl8.0gnah2po4·
2h2o0.2gna2hpo4·
12h2o2.9g表面活性剂s93g酪蛋白钠盐5gproclin3001ml纯化水定容至1000ml
[0117]
配制完成后过滤除菌,4℃保存;
[0118]
2.4)显示液a、显示液b的配制是以二甲基亚砜(dmso)为溶剂配制浓度为0.3mg/ml的四甲基联苯胺(tmb)溶液,命名为a液,以ph5.5、0.2mol/l磷酸氢二钠与0.1mol/l柠檬酸缓冲液为溶剂配制浓度为0.74mg/ml的过氧化脲溶液,命名为b液,使用时将a液与b液按体积比1﹕1混合;
[0119]
2.5)终止液是浓度为2mol/l的硫酸溶液。
[0120]
其中,
[0121]
所述高敏结合蛋白制备方法为利用灭活的新型冠状病毒感染者血清经过装有重组rbd中和抗体偶联的琼脂糖微球层析柱过滤,高敏结合蛋白会结合到琼脂糖微球上,经过洗杂、洗脱得到纯化的高敏结合蛋白得到,并通过bca法进行定量。
[0122]
高敏结合蛋白的包被量采用棋盘法依照灵敏度,检测范围为指标进行选择。
[0123]
所述rbd蛋白制备方法为利用cho细胞表达的新型冠状病毒sars
‑
cov
‑
2rbd三聚体重组蛋白。
[0124]
所述重组rbd中和抗体制备方法为用来自于测定的新冠康复患者中和抗体可变区序列并与人源化fc融合,通过cho细胞重组表达形成的。
[0125]
所述rbd酶结合物的制备方法为:利用过碘酸钠法标记的重组rbd三聚体蛋白与辣
根过氧化物酶(hrp)的结合物。制备方法不限于此方法,其余蛋白标记方法亦可。
[0126]
hrp标记的新冠刺突蛋白rbd使用量的优化:采用棋盘法依照灵敏度,检测范围为指标进行选择。优选的使用效价浓度为1:9000。
[0127]
实施例3
[0128]
实施例1所述新型冠状病毒高亲和中和抗体检测试剂盒在检测中和抗体中的应用,包括步骤如下:
[0129]
(1)于微孔板内每孔先加入25ul样品稀释液,再将待测样品、阳性对照和阴性对照各取25ul分别加入到微孔板含有样品稀释液的孔中,37℃温浴30分钟;
[0130]
(2)反应结束后,用洗涤液洗板5次,每次应浸泡20~40s,每孔加液量不少于350μl,洗涤完之后拍干;
[0131]
(3)每孔再加入100ul重组rbd蛋白酶结合物,混匀后用不干胶封片封盖反应板,37℃温浴20分钟;
[0132]
(4)反应结束后,用洗涤液洗板5次,每次应浸泡20~40s,每孔加液量不少于350μl,洗涤完之后拍干;
[0133]
(5)先加入显色液a 50μl,再加入显色液b 50μl,37℃避光温浴10分钟;
[0134]
(6)加入终止液50μl,终止反应,用酶标仪检测各孔在450nm和630nm双波长的吸光值;
[0135]
(7)根据cut off判断结果;od值≥0.130:阳性,od值<0.130:阴性。
[0136]
实施例4
[0137]
实施例1所述新型冠状病毒高亲和中和抗体检测试剂盒的线性、准确性、回收率、精密度的检测
[0138]
1)试剂盒的线性
[0139]
(1)定标品配制:用样品稀释液分别将rbd中和抗体稀释至0.025μg/ml、0.050μg/ml、0.075μg/ml、0.100μg/ml、0.250μg/ml、0.500μg/ml、1μg/ml。
[0140]
(2)定标品测试:将配制好的定标品通过实施例2所述方法检测,得到od值;
[0141]
(3)标准曲线的建立:根据校准品的制备浓度和od值采用合适的拟合方式生成该批试剂的校准曲线。见表1和图1。
[0142]
表1试剂盒线性
[0143]
浓度0μg/ml0.025μg/ml0.050μg/ml0.075μg/ml0.100μg/ml0.250μg/ml0.500μg/ml1μg/mlod值0.020.0950.2150.4120.4411.0892.3573.673
[0144]
2)精密性试验:
[0145]
分别以0.075μg/ml、0.5μg/ml的rbd中和抗体标准品平行测试10次,结果统计见表2。
[0146]
表2:精密性试验结果
[0147]
板孔号12345678910均值sdcv0.075μg/ml0.4120.4340.4230.4270.4360.4150.4230.420.4110.4170.42180.008602.04%0.5μg/ml2.3652.3782.4122.3212.4422.4682.3092.3542.3912.3772.38170.049602.08%
[0148]
cv均<15%,精密性良好。
[0149]
对比例1
[0150]
应用ace2竞争机制的试剂盒检测中和抗体,检测方法如下:
[0151]
(1)于微孔板内每孔先加入25ul样品稀释液,再将待测样品、阳性对照和阴性对照各取25ul分别加入到微孔板含有样品稀释液的孔中,最后每孔再加入100ul重组ace2蛋白酶结合物,混匀后用不干胶封片封盖反应板,37℃温浴30分钟;
[0152]
(2)反应结束后,用洗涤液洗板5次,每次应浸泡20s~40s,每孔加液量不少于350μl,洗涤完之后拍干;
[0153]
(3)先加入显色液a 50μl,再加入显色液b 50μl,37℃避光温浴15分钟;
[0154]
(4)加入终止液50μl,终止反应,用酶标仪检测各孔在450nm和630nm双波长的吸光值;
[0155]
(5)根据吸光值计算抑制率,并判断结果;
[0156]
结果判定标准:
[0157]
s/co≥20%:阳性,s/co<20%:阴性。
[0158]
试验例1
[0159]
本发明的新型冠状病毒高亲和中和抗体检测试剂盒和应用ace2竞争机制的试剂盒在注射疫苗临床样本筛查中的应用
[0160]
使用355例完成临床注射新冠疫苗免疫样本与650例未注射新冠疫苗样本,与微量细胞中和实验比对,计算本发明试剂盒测定结果与微量细胞中和实验结果符合或差异程度的统计学指标,结果如表3。
[0161]
表3本发明试剂盒与微量细胞中和试验对比
[0162][0163][0164]
灵敏度计算:340/340
×
100%=100%。
[0165]
特异性计算:652/665
×
100%=98.01%
[0166]
总符合率:(340+652)/1005
×
100%=98.71%
[0167]
以上试验说明,本发明提供的检测新型冠状病毒中和抗体的试剂盒及其检测方法,与中和抗体检测金标准有很好的一致性,可以用于接种新型冠状病毒疫苗后中和抗体产生评估,其灵敏度、特异性均较好,利于临床准确评估疫苗效果。并且现有技术中酶联免疫试剂盒多采用rbd蛋白作为结合蛋白,辣根过氧化物酶ace2作为酶结合物,通过辣根过氧化物酶ace2与中和抗体进行竞争,来达到检测中和抗体的目的,但是其操作复杂,操作时长,结果易受加样时间影响。本发明采用从新型冠状病毒感染人群的血清提取的高敏结合
蛋白与rbd中和抗体具有极高的亲和力,将高敏结合蛋白作为捕捉蛋白,利用重组rbd三聚体蛋白标记的hrp作为检测蛋白如果样本中含有新型冠状病毒中和抗体,则形成“高敏结合蛋白
‑
中和抗体
‑
rbd”复合物,如果样本中不含有新型冠状病毒中和抗体,则不显色,最后加入酶底物显色。以结合的方式检测中和蛋白,相较于竞争方式检测中和蛋白,操作时间更短,检测速度更快,使用对比例1所述的试剂盒每检测90例需要75min,而本发明试剂盒每检测90例用时为60min,每检测90例就能节省15min的检测时间,不易受加样时间影响,结果更加准确。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1