苍耳子中药配方颗粒的近红外定量检测模型的构建方法及其定量检测方法与流程
1.本发明涉及中药配方颗粒分析技术领域,特别涉及苍耳子中药配方颗粒的近红外定量检测模型的构建方法及其定量检测方法,具体是涉及苍耳子中药配方颗粒的近红外定量检测模型的构建方法、苍耳子中药配方颗粒中羧基苍术苷或绿原酸的定量检测方法。
背景技术:
2.据《中华人民共和国药典》(2020年版)记载,苍耳子为菊科植物苍耳xanthium sibiricum patr.的干燥成熟带总苞的果实。苍耳子具有散风寒,通鼻窍,祛风湿的功效。苍耳子属于有毒品种,2015年版中国药典采用高效液相色谱法测定苍耳子毒性成分羧基苍术苷含量,现行版中国药典采用高效液相色谱法测定绿原酸含量。苍耳子中药配方颗粒是由苍耳子饮片经水提、浓缩、干燥、制粒而成的颗粒。因此,对苍耳子中药配方颗粒的羧基苍术苷和绿原酸进行含量测定,有利于对药品安全性和有效性的控制。传统的高效液相色谱法技术至少存在:制样过程繁复、样品被破坏、分析时间长、化学试剂污染等缺点。
技术实现要素:
3.基于此,本发明采用近红外光谱技术(near infrared spectroscopy),同时结合计算机技术和化学计量学技术,实现苍耳子中药配方颗粒中羧基苍术苷、绿原酸含量的快速测定。
4.本发明的技术方案如下:
5.一种苍耳子中药配方颗粒的近红外定量检测模型的构建方法,包括以下步骤:
6.获取苍耳子中药配方颗粒中羧基苍术苷或绿原酸的含量,并采集所述苍耳子中药配方颗粒的近红外光谱,分为校正光谱集和检验光谱集;
7.在近红外光谱范围,对所述校正光谱集的近红外光谱进行预处理,采用偏最小二乘法,将预处理后的近红外光谱的数据与苍耳子中药配方颗粒中羧基苍术苷或绿原酸的含量进行关联,构建羧基苍术苷的预选近红外定量检测模型或绿原酸的预选近红外定量检测模型,所述近红外光谱范围选自12000.0cm-1
~4000.0cm-1
中的一段或多段范围;所述预处理的方法选自多元散射校正、一阶导数、二阶导数和矢量归一化中一种或多种组合;
8.将所述检验光谱集的近红外光谱导入所述羧基苍术苷的预选近红外定量检测模型或绿原酸的预选近红外定量检测模型,进行检验集检验,以相关系数为指标,选择预处理的方法,以及选择近红外光谱范围,确定苍耳子中药配方颗粒中羧基苍术苷的近红外定量检测模型或苍耳子中药配方颗粒中绿原酸的近红外定量检测模型。
9.在其中一个实施例中,所述校正光谱集中的近红外光谱数与检验光谱集中的近红外光谱数的比值为(1.5~2.5):1。
10.在其中一个实施例中,以相关系数大于0.9为指标,选择预处理的方法,以及选择近红外光谱范围,确定苍耳子中药配方颗粒中羧基苍术苷的近红外定量检测模型或苍耳子
中药配方颗粒中绿原酸的近红外定量检测模型。
11.在其中一个实施例中,预处理的方法选自多元散射校正、一阶导数和矢量归一化中的一种或多种组合;近红外光谱范围选自5452.2cm-1
~4244.2cm-1
、6105.2cm-1
~4244.2cm-1
、9402.6cm-1
~8447.7cm-1
和6105.2cm-1
~4244.2cm-1
中的一个或多个,构建苍耳子中药配方颗粒中羧基苍术苷的近红外定量检测模型。
12.可选地,预处理的方法为多元散射校正;近红外光谱范围为5452.2cm-1
~4244.2cm-1
,构建苍耳子中药配方颗粒中羧基苍术苷的近红外定量检测模型。
13.优选地,预处理的方法为一阶导数和矢量归一化的组合;近红外光谱范围为6105.2cm-1
~4244.2cm-1
,构建苍耳子中药配方颗粒中羧基苍术苷的近红外定量检测模型。
14.更优选地,预处理的方法为一阶导数和多元散射校正的组合;近红外光谱范围为9402.6cm-1
~8447.7cm-1
和6105.2cm-1
~4244.2cm-1
,构建苍耳子中药配方颗粒中羧基苍术苷的近红外定量检测模型。
15.在其中一个实施例中,预处理的方法选自二阶导数、一阶导数或矢量归一化;近红外光谱范围选自6105.2cm-1
~4595.2cm-1
、7500.9cm-1
~5444.0cm-1
、6472.5cm-1
~5444.0cm-1
和4603.4cm-1
~4423.8cm-1
中的一个或多个,构建苍耳子中药配方颗粒中绿原酸的近红外定量检测模型。
16.可选地,预处理的方法为二阶导数;近红外光谱范围为6105.2cm-1
~4595.2cm-1
,构建苍耳子中药配方颗粒中绿原酸的近红外定量检测模型。
17.优选地,预处理的方法为一阶导数;近红外光谱范围为7500.9cm-1
~5444.0cm-1
和4603.4cm-1
~4423.8cm-1
,构建苍耳子中药配方颗粒中绿原酸的近红外定量检测模型。
18.更优选地,预处理的方法为矢量归一化;近红外光谱范围为6472.5cm-1
~5444.0cm-1
和4603.4cm-1
~4423.8cm-1
,构建苍耳子中药配方颗粒中绿原酸的近红外定量检测模型。
19.在其中一个实施例中,还包括采用苍耳子中药配方颗粒中羧基苍术苷或绿原酸的含量真值对所述苍耳子中药配方颗粒中羧基苍术苷的近红外定量检测模型或苍耳子中药配方颗粒中绿原酸的近红外定量检测模型进行评价的步骤。
20.在其中一个实施例中,所述采集苍耳子中药配方颗粒的近红外光谱之前,还包括对所述苍耳子中药配方颗粒进行粉碎和过筛的步骤。
21.可以理解地,所述苍耳子中药配方颗粒的基原均为菊科植物苍耳xanthium sibiricum patr.的干燥成熟带总苞的果实。
22.可以理解地,采集近红外光谱的测量仪器可为但不限于傅立叶变换近红外光谱仪;所用计算机软件可为但不限于tango软件、opus软件;光谱测量模式可为但不限于漫反射模式;测量参数可为但不限于光谱扫描范围、扫描次数、分辨率和样品测量次数。
23.可以理解地,近红外光谱范围的选择方式可为但不限于软件自动选择、人工选择、软件自动选择与人工选择相结合。
24.一种苍耳子中药配方颗粒中羧基苍术苷或绿原酸的定量检测方法,包括以下步骤:
25.获取上述苍耳子中药配方颗粒中羧基苍术苷的近红外定量检测模型或苍耳子中药配方颗粒中绿原酸的近红外定量检测模型;
26.采集待测样品的近红外光谱,将所述待测样品的近红外光谱的数据导入所述苍耳子中药配方颗粒中羧基苍术苷的近红外定量检测模型或苍耳子中药配方颗粒中绿原酸的近红外定量检测模型,获得羧基苍术苷的含量或绿原酸的含量。
27.可以理解地,采集待测样品的近红外光谱的方法与上述苍耳子中药配方颗粒的近红外光谱的方法相同。
28.在一个实施例中,采集待测样品的近红外光谱之前,还包括对所述待测样品进行粉碎和过筛的步骤。
29.与现有方案相比,本发明具有以下有益效果:
30.本发明采用近红外光谱技术,同时结合计算机技术和化学计量学技术,对苍耳子中药配方颗粒中羧基苍术苷、绿原酸含量进行快速测定。为用药安全性和有效性提供了保障。与传统的方法相比,制样过程简单、不破坏样品,无化学试剂污染,结果准确。
附图说明
31.图1为苍耳子中药配方颗粒的近红外光谱图;
32.图2为苍耳子中药配方颗粒中羧基苍术苷的近红外定量检测模型3的羧基苍术苷含量预测值与真值的相关图;
33.图3为苍耳子中药配方颗粒中绿原酸的近红外定量检测模型6的绿原酸含量预测值与真值的相关图。
具体实施方式
34.以下结合具体实施例对本发明作进一步详细的说明。本发明可以以许多不同的形式来实现,并不限于本文所描述的实施方式。相反地,提供这些实施方式的目的是使对本发明公开内容理解更加透彻全面。
35.除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。
36.术语
37.除非另外说明或存在矛盾之处,本文中使用的术语或短语具有以下含义:
38.本发明中,所使用的术语“和/或”、“或/和”、“及/或”的可选范围包括两个或两个以上相关所列项目中任一个项目,也包括相关所列项目的任意的和所有的组合,所述任意的和所有的组合包括任意的两个相关所列项目、任意的更多个相关所列项目、或者全部相关所列项目的组合。
39.本发明中,“一种或几种”指所列项目的任一种、任两种或任两种以上。其中,“几种”指任两种或任两种以上。
40.本发明中,所使用的“其组合”、“其任意组合”、“其任意组合方式”等中包括所列项目中任两个或任两个以上项目的所有合适的组合方式。
41.本发明中,“可选地”、“可选的”、“可选”,指可有可无,也即指选自“有”或“无”两种并列方案中的任一种。如果一个技术方案中出现多处“可选”,如无特别说明,且无矛盾之处或相互制约关系,则每项“可选”各自独立。
42.本发明中,“优选”仅为描述效果更好的实施方式或实施例,应当理解,并不构成对本发明保护范围的限制。
43.本发明中,以开放式描述的技术特征中,包括所列举特征组成的封闭式技术方案,也包括包含所列举特征的开放式技术方案。
44.本发明中,涉及到数值区间,如无特别说明,则包括数值区间的两个端点。
45.本发明中,涉及到百分比含量,如无特别说明,对于固液混合和固相-固相混合均指质量百分比,对于液相-液相混合指体积百分比。
46.本发明中,涉及到百分比浓度,如无特别说明,均指终浓度。所述终浓度,指添加成分在添加该成分后的体系中的占比。
47.实施例1:苍耳子中药配方颗粒中羧基苍术苷的近红外定量检测模型的构建
48.1仪器与材料
49.1.1仪器tango-r傅立叶变换近红外光谱仪(德国bruker公司),配置积分球漫反射检测器,控制软件为tango 7.5,分析处理软件为opus 7.5。万分之一电子天平(梅特勒-托利多仪器有限公司)。
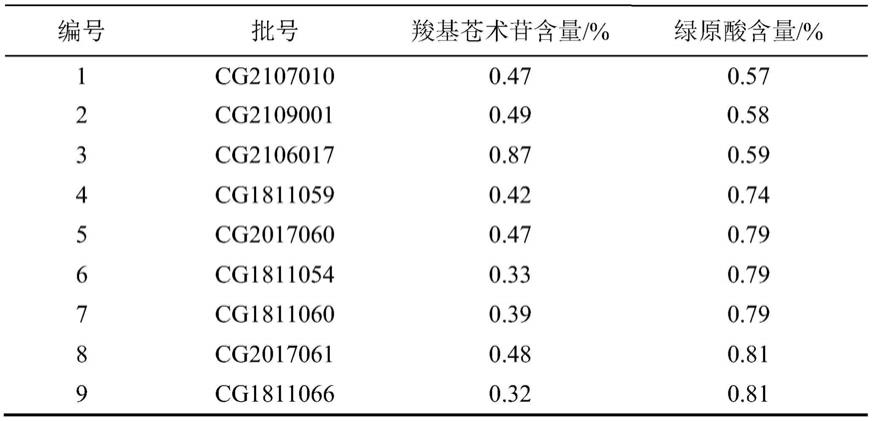
50.1.2材料苍耳子中药配方颗粒由广东一方制药有限公司提供,各批次苍耳子中药配方颗粒中的羧基苍术苷、绿原酸含量数据由广东省中药配方颗粒企业重点实验室提供。见表1。
51.表1苍耳子中药配方颗粒批号和含量
[0052][0053]
2方法与结果
[0054]
2.1近红外光谱的采集
[0055]
取各批次苍耳子中药配方颗粒,粉粹,过50目筛,得样品粉末。取样品粉末约5.0g,装入具塞玻璃样品瓶中,用积分球漫反射采集近红外光谱。采集条件:以仪器内置背景为参比,设置扫描范围为12000cm-1
~4000cm-1
,分辨率为16cm-1
,扫描次数为32次,取平均光谱。每批苍耳子中药配方颗粒样品取2个平行样,每个平行样再平行测量2次,共得4张近红外光谱,苍耳子中药配方颗粒的近红外光谱见图1。
[0056]
2.2校正光谱集与检验光谱集样品光谱的选择
[0057]
随机选取苍耳子的校正光谱集与检验光谱集样品批数,并使其比例接近2:1,见表
2。
[0058]
表2苍耳子的校正光谱集和检验光谱集样品
[0059][0060]
2.3羧基苍术苷的近红外定量检测模型的构建与评价
[0061]
2.3.1光谱预处理方法的选择
[0062]
从多元散射校正(multiple scattering correction)、一阶导数(first derivative)和矢量归一化(vector normalization)及其组合中选择预处理的方法。
[0063]
2.3.2建模光谱范围的选择
[0064]
选择近红外光谱范围12000.0cm-1
~4000.0cm-1
中的一段或多段范围。
[0065]
2.3.3模型的构建与评价
[0066]
采用多元散射校正对校正光谱集的近红外光谱进行预处理,在近红外光谱范围5452.2cm-1
~4244.2cm-1
,采用偏最小二乘法(partial least squares regression),将预处理后的近红外光谱的数据与苍耳子中药配方颗粒中羧基苍术苷的含量进行关联,构建羧基苍术苷的预选近红外光谱定量检测模型1。
[0067]
采用一阶导数和矢量归一化对校正光谱集的近红外光谱进行预处理,在近红外光谱范围6105.2cm-1
~4244.2cm-1
,采用偏最小二乘法,将预处理后的近红外光谱的数据与苍耳子中药配方颗粒中羧基苍术苷的含量进行关联,构建羧基苍术苷的预选近红外光谱定量检测模型2。
[0068]
采用一阶导数和多元散射校正对校正光谱集的近红外光谱进行预处理,在近红外光谱范围9402.6cm-1
~8447.7cm-1
和6105.2cm-1
~4244.2cm-1
,采用偏最小二乘法,将预处理后的近红外光谱的数据与苍耳子中药配方颗粒中羧基苍术苷的含量进行关联,构建羧基苍术苷的预选近红外光谱定量检测模型3。
[0069]
将检验光谱集的近红外光谱分别导入羧基苍术苷的预选近红外光谱定量检测模型1、羧基苍术苷的预选近红外光谱定量检测模型2和羧基苍术苷的预选近红外光谱定量检测模型3,采用近红外opus 7.5分析软件进行检验集检验,得到各模型参数。结果如表3所示。
[0070]
表3羧基苍术苷定量检测模型及其性能
[0071][0072]
相关系数越趋近于1,代表所构建的模型的性能越好。由表3可知,羧基苍术苷的预选近红外光谱定量检测模型1的相关系数为0.9724,大于0.9,可确定羧基苍术苷的预选近红外光谱定量检测模型1为苍耳子中药配方颗粒中羧基苍术苷的近红外定量检测模型1。
[0073]
优选的,羧基苍术苷的预选近红外光谱定量检测模型2的相关系数为0.9830,大于0.9,且更趋近于1,可确定羧基苍术苷的预选近红外光谱定量检测模型2为苍耳子中药配方颗粒中羧基苍术苷的近红外定量检测模型2。
[0074]
更优选的,羧基苍术苷的预选近红外光谱定量检测模型3的相关系数为0.9956,大于0.9,且更趋近于1。表明该模型的定量检测性能较好,可确定羧基苍术苷的预选近红外光谱定量检测模型3为苍耳子中药配方颗粒中羧基苍术苷的近红外定量检测模型3。该模型的预测值与真值的相关图见图2。
[0075]
2.4方法学验证
[0076]
2.4.1精密度考察
[0077]
取苍耳子中药配方颗粒供试品(g1811059),按“2.1”项下的方法采集和处理待分析样品的近红外光谱,用所构建的苍耳子中药配方颗粒中羧基苍术苷的近红外定量检测模型3测定羧基苍术苷含量,重复扫描、测定6次,结果见表4。rsd值为0.98%,表明该模型的精密度良好。
[0078]
表4精密度考察结果
[0079][0080]
2.4.2重复性考察
[0081]
分别取6份苍耳子中药配方颗粒供试品(g1811060),按“2.1”项下的方法采集和处理待分析样品的近红外光谱,用所构建的苍耳子中药配方颗粒中羧基苍术苷的近红外定量检测模型3测定羧基苍术苷含量,结果见表5。rsd值为1.31%,表明该模型的重复性良好。
[0082]
表5重复性考察结果
[0083][0084]
2.4.3稳定性考察
[0085]
取苍耳子中药配方颗粒供试品(g2017060),分别于取样后0、2、4、6、8、10h,按“2.1”项下的方法采集和处理待分析样品的近红外光谱,用所构建的苍耳子中药配方颗粒中羧基苍术苷的近红外定量检测模型3测定羧基苍术苷含量,结果见表6。rsd值为0.87%,表明该模型的稳定性良好。
[0086]
表6稳定性考察结果
[0087][0088]
实施例2:待测苍耳子中药配方颗粒样品的羧基苍术苷含量快速测定
[0089]
取待测苍耳子中药配方颗粒样品,参照实施例1中项2.1下的方法,采集其近红外光谱,导入上述苍耳子中药配方颗粒中羧基苍术苷的近红外定量检测模型3中,模型出示该待测苍耳子中药配方颗粒中羧基苍术苷含量为:0.35%。
[0090]
实施例3:苍耳子中药配方颗粒中绿原酸定量检测模型的构建
[0091]
1仪器与材料
[0092]
与实施例1相同
[0093]
2方法与结果
[0094]
2.1近红外光谱的采集
[0095]
与实施例1相同
[0096]
2.2校正光谱集与检验光谱集样品光谱的选择
[0097]
与实施例1相同
[0098]
2.3绿原酸的近红外定量检测模型的构建与评价
[0099]
2.3.1光谱预处理方法的选择
[0100]
从二阶导数(second derivative)、一阶导数(first derivative)和矢量归一化(vector normalization)及其组合中选择预处理的方法。
[0101]
2.3.2建模光谱范围的选择
[0102]
选择近红外光谱范围12000.0cm-1
~4000.0cm-1
中的一段或多段范围。
[0103]
2.3.3模型的构建与评价
[0104]
采用二阶导数对校正光谱集的近红外光谱进行预处理,在近红外光谱范围
6105.2cm-1
~4595.2cm-1
,采用偏最小二乘法(partial least squares regression),将预处理后的近红外光谱的数据与苍耳子中药配方颗粒中绿原酸的含量进行关联,构建绿原酸的预选近红外光谱定量检测模型4。
[0105]
采用一阶导数对校正光谱集的近红外光谱进行预处理,在近红外光谱范围7500.9cm-1
~5444.0cm-1
和4603.4cm-1
~4423.8cm-1
,采用偏最小二乘法,将预处理后的近红外光谱的数据与苍耳子中药配方颗粒中绿原酸的含量进行关联,构建绿原酸的预选近红外光谱定量检测模型5。
[0106]
采用矢量归一化对校正光谱集的近红外光谱进行预处理,在近红外光谱范围6472.5cm-1
~5444.0cm-1
和4603.4cm-1
~4423.8cm-1
,采用偏最小二乘法,将预处理后的近红外光谱的数据与苍耳子中药配方颗粒中绿原酸的含量进行关联,构建绿原酸的预选近红外光谱定量检测模型6。
[0107]
将检验光谱集的近红外光谱分别导入绿原酸的预选近红外光谱定量检测模型4、绿原酸的预选近红外光谱定量检测模型5和绿原酸的预选近红外光谱定量检测模型6,采用近红外opus7.5分析软件进行检验集检验,得到各模型参数。结果如表7所示。
[0108]
表7苍耳子定量检测模型及其性能
[0109][0110][0111]
相关系数越趋近于1,代表所构建的模型的性能越好。由表7可知,绿原酸的预选近红外光谱定量检测模型4的相关系数为0.9734,大于0.9,可确定绿原酸的预选近红外光谱定量检测模型4为苍耳子中药配方颗粒中绿原酸的近红外定量检测模型4。
[0112]
优选的,绿原酸的预选近红外光谱定量检测模型5的相关系数为0.9882,大于0.9,且更趋近于1,可确定绿原酸的预选近红外光谱定量检测模型5为苍耳子中药配方颗粒中绿原酸的近红外定量检测模型5。
[0113]
更优选的,绿原酸的预选近红外光谱定量检测模型6的相关系数为0.9958,大于0.9,且更趋近于1。表明该模型的定量检测性能较好,可确定绿原酸的预选近红外光谱定量检测模型6为苍耳子中药配方颗粒中绿原酸的近红外定量检测模型6。该模型的预测值与真值的相关图见图3。
[0114]
2.4方法学验证
[0115]
2.4.1精密度考察
[0116]
取苍耳子中药配方颗粒供试品(g1811059),按“2.1”项下的方法采集和处理待分析样品的近红外光谱,用所构建的苍耳子中药配方颗粒中绿原酸的近红外定量检测模型6
测定绿原酸含量,重复扫描、测定6次,结果见表8。rsd值为0.55%,表明该模型的精密度良好。
[0117]
表8精密度考察结果
[0118][0119]
2.4.2重复性考察
[0120]
分别取6份苍耳子中药配方颗粒供试品(g1811060),按“2.1”项下的方法采集和处理待分析样品的近红外光谱,用所构建的苍耳子中药配方颗粒中绿原酸的近红外定量检测模型6测定绿原酸含量,结果见表9。rsd值为2.24%,表明该模型的重复性良好。
[0121]
表9重复性考察结果
[0122][0123]
2.4.3稳定性考察
[0124]
取苍耳子中药配方颗粒供试品(g2017060),分别于取样后0、2、4、6、8、10h,按“2.1”项下的方法采集和处理待分析样品的近红外光谱,用所构建的苍耳子中药配方颗粒中绿原酸的近红外定量检测模型6测定绿原酸含量,结果见表10。rsd值为0.66%,表明该模型的稳定性良好。
[0125]
表10稳定性考察结果
[0126][0127]
实施例4:苍耳子中药配方颗粒样品的绿原酸含量快速测定
[0128]
取待测苍耳子中药配方颗粒样品,参照实施例3中项2.1下的方法,采集其近红外光谱,导入上述苍耳子中药配方颗粒中绿原酸的近红外定量检测模型6中,模型出示该待测苍耳子中药配方颗粒中绿原酸含量为:0.61%。
[0129]
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存
在矛盾,都应当认为是本说明书记载的范围。
[0130]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1